Изобретение относится к области медицины, а именно к медицинским макропористым гидрогелевым полимерным материалам и изделиям на их основе, в частности имплантатам, подложкам для клеточной инженерии, матрицам с контролируемым выделением лекарственных средств, дренажным средствам и т.п. Изделия из данного материала могут быть применены в офтальмологии, микрохирургии, пластической хирургии, общей, торакальной, сердечно-сосудистой и челюстно-лицевой хирургии, гинекологии, стоматологии, отоларингологии и других областях практической медицины.
УРОВЕНЬ ТЕХНИКИ
Полимерные гидрогели различного химического строения нашли широкое применение в различных областях медицины, биотехнологии и смежных областях [например, Biomaterials Science. / Eds. By B.D.Ratner e.a., Acad. Press, 2004; Shtilman M.I. Polymeric Biomaterials. Part. l. Polymer implants. VSP: Utrecht-Boston, 2003. - 293 pp.; Штильман М.И. Полимеры медико-биологического назначения. Москва: Академкнига, 2006. - 309 с.; Искаков P.M. и др. Полимерные биоматериалы. - ИХН: Алматы, 2006. - 273 с.; Сулейменов И.Э. и др. Полимерные гидрогели в фармацевтике: физико-химические аспекты. ИХН: Алматы - Санкт-Петербург, 2004. - 210 с.].
Новой группой полимерных гидрогелей являются макропористые полимерные гидрогели (т.е. гидрогели, содержащие поры размером десятки и сотни микрон).
Согласно данному изобретению предлагаются пористые полимерные гидрогели на основе сшитого поливинилового спирта. Поливиниловый спирт является известным материалом медицинского назначения, находящим применение в качестве носителя лекарственных препаратов и компонента кровезаменителей (препарат «Полидез»), порошкообразных систем (материал «Гелевин»), волоконных материалов (материал «Ивалон»).
Использование его в виде изделий на основе пористых гелей расширяет возможности медицинского использования этого полимера.
Известен способ получения пористого гидрогеля поливинилового спирта является образование трехмерной полимерной системы, образованной межмолекулярными водородными связями, формируемой в присутствии гетерофазы замороженного растворителя (вода, формамид) [Лозинский В.И. «Способ получения геля поливинилового спирта», RU 2070901, С1]. Однако системы, полученные криогенным структурированием растворов полимера путем проведения циклов «замораживание-размораживание», неустойчивы и разрушаются, образуя раствор полимера при нагревании. Это требует фиксирования пористой структуры до или после размораживания с использованием сшивающих агентов, обладающих высокой токсичностью, которые требуется тщательно удалять из готового геля, или радиационным облучением. Все это требует дополнительной очистки продуктов, существенно ограничивает сферы их применения, а также усложняет технологию получения.
Ближайшим аналогом данного изобретения является пористый сорбционный перевязочный материал на основе поливинилового спирта, сшивающего агента, минеральной кислоты, хлорида натрия, пенообразующего агента RU 2151615. Количественное соотношение ПВС и сшивающего агента составляет на 100 частей ПВС 150-170 частей сшивающего агента.
Недостатком указанного материала является недостаточная термическая стабильность продукта, относительно небольшие количество пор и их суммарный объем. Существенно, что продукт необходимо тщательно очищать от сшиваемого агента.
Задачей данного изобретения является создание макропористого биосовместимого медицинского материала, имеющего повышенную термостабильность, развитую пористость, высокую дренирующую способность.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Предлагаемое техническое решение, позволяющее устранить указанные выше недостатки, заключается в том, что макропористый полимерный материал на основе сшитого поливинилового спирта получают путем проведения полимеризации в водных замороженных растворах заранее приготовленных и очищенных водорастворимых ненасыщенных производных поливинилового спирта общей формулы
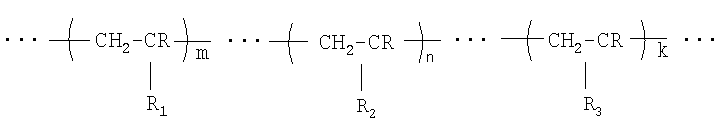
где R-Н,
R1-OH,
R2 - ненасыщенная группа,
R3-O-CO-R4,
R4-СН3 или остаток другой кислоты, из поливинилового эфира которой был получен поливиниловый спирт,
m = 80-99 мол.%,
n = 0,5-15 мол.%,
k = 0-12 мол.%.
Вводимый в боковую цепь ненасыщенный радикал R2 содержит одну или две ненасыщенные связи и обеспечивает образование пространственной структуры в условиях радикальной полимеризации и сополимеризации. Радикал R2 может содержать остаток ненасыщенной кислоты, например акриловой, метакриловой, сорбиновой, кротоновой, коричной:
СН2=СН-СО-O-,
СН2-С(СНз)-СО-О-,
СН3-СН=СН-СН=СН-СО-O-,
СН3-СН=СН-СО-O-,
С6Н5-СН=СН-СО-O-,
СН2-С(СН3)-СО-O-СН2-СН(ОН)-СН2-O-,
СН2=СН-СО-O-СН2-СН(ОН)-СН2-O-,
CH2=CH-CH2-O-CH2-CH(OH)-CH2-O-
или алкеновую группу, например
СН2=СН-O-,
СН2=СН-СН2-O-,
СН2=СН-O-СН2-СН2-O-.
Ненасыщенная группа может быть также введена в виде бокового ацетального заместителя.
Формирование гелей протекает при одноразовом замораживании водных растворов водорастворимых ненасыщенных производных карбоцепных полимеров. Процесс проводят в интервале температур от -5 до -30°С, причем замораживание может проводится как «простым» охлаждением, так и методом «температурной закалки» - быстрым охлаждением (например, жидким азотом) с последующим увеличением температуры до температуры протекания реакции. При использовании вместо воды других сред температурный диапазон полимеризации определяется типом растворителя.
Условия синтеза обеспечивают наличие в полученных гелевых системах пор размером десятки и сотни микрон. Общая пористость, средний размер пор и их распределение по размерам могут регулироваться условиями проведения процесса (изменением концентрации замораживаемого раствора, температурой синтеза, методом заморозки, количеством инициатора), что является ноу-хау изобретения.
Степень сшивания ПВС влияет на физические и функциональные свойства материала. Количество групп с кратными связями, содержащихся в боковой цепи полимера, составляет достаточное количество для достижения желаемых свойств, таких как твердость получаемого геля (от мягкого до твердого). Однако их количество может быть различно в зависимости от назначения материала. Так, например, для увеличения прочности материала количество таких групп в составе полимера может быть велико, в то время как для повышения пластичности материала может быть использован полимер с меньшей степенью замещения.
Существенным преимуществом предлагаемого технического решения, по сравнению с методом сополимеризации низкомолекулярных мономеров, является отсутствие остаточного количества последних в качестве примесей в составе конечного продукта, а также возможность регулирования размера полимерных фрагментов, образующихся при биодеградации полимерного гидрогеля (что имеет весьма существенное значение для сфер применения, связанных с медициной).
По сравнению с методом формирования гидрогеля за счет образования физических межмолекулярных связей, данный метод позволяет увеличить термостабильность синтезируемых полимерных систем и также исключает необходимость дополнительной фиксации структуры получаемых полимерных гидрогелей.
Полимеризацию ненасыщенного производного можно проводить в присутствии инициаторов радикальной полимеризации или под действием радиационного облучения.
Реакционная система и получаемые продукты в данном случае не содержат остатков низкомолекулярных мономеров.
Получаемые в этом случае гелевые системы после размораживания сохраняют пористую структуру, в том числе до температуры кипения при нагревании в водной среде, не требуя дополнительного закрепления структуры, не содержат остаточных мономеров, что упрощает технологию их очистки и расширяет возможности их использования. Помимо этого, данный метод позволяет легко вводить методом «включения в гель» в состав синтезируемых полимерных систем различные биологические лиганды, с последующим их выделением из объема полимерного геля. Предлагаемый гидрогелевый материал, в силу того, что концентрация растворов полимера при изготовлении составляет, как правило, не более 10%, характеризуются более развитой пористостью, большим средним диаметром пор. Образование достаточно прочного пористого гидрогеля на основе поливинилового спирта за счет межмолекулярных водородных связей при этих концентрациях зачастую невозможно.
Сбалансированность качественного и количественного состава указанных структурных компонентов полимера позволяет получить материал, обладающий высокой биосовместимостью и способностью обеспечивать прорастание фибрилл соединительной ткани в поры материала.
В зависимости от назначения изделия материал может обеспечит комплексное действие - гемостатический эффект, подавление патогенной микрофлоры, противовоспалительное, противоотечное, обезболиващее действие, тем самым стимулируя воздействие на репаративные процессы в зоне раны.
Материал имеет меньшую себестоимость за счет отсутствия дополнительных сшивающих и других компонентов, а также за счет упрощения способа его изготовления.
Сущность изобретения может быть проиллюстрирована следующими примерами:
ПРИМЕРЫ
Пример 1
Навеску модифицированного полимера на основе поливинилового спирта, состава
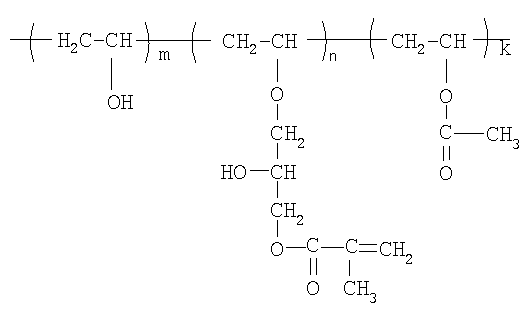
(m = 94,4 мол.%; n = 4,3 мол.%, k = 1,3 мол.%,. Mw = 25000) массой 1 г растворяли при нагревании в 25 мл дистиллированной воды, охлаждали до комнатной температуры, добавляли 0,06 г персульфата калия в 1,5 мл дистиллированной воды, смесь вакууммировали для удаления растворенного воздуха и охлаждали до температуры 5°С, добавляли 30 мкл N,N,N',N'-тетраметилэтилендиамина. Смесь заливали в предварительно охлажденную разъемную стеклянную форму, замораживали и выдерживали в течение 6 часов при температуре - 15°С. По окончании реакции форму размораживали, размыкали, образовавшийся макропористый гидрогель промывали в 200 мл горячей дистиллированной воды, после чего лиофильно сушили. Выход продукта 92%. Общая пористость 64%, средний размер пор 25,4 мкм.
Пример 2
Навеску модифицированного полимера на основе поливинилового спирта, состава
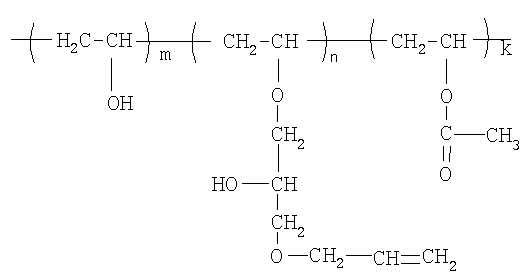
(m = 88 мол.%; n = 10,2 мол.%, k = 1,8 мол.%,. Mw = 77000) массой 1 г растворяли при нагревании в 7,5 мл дистиллированной воды, охлаждали до комнатной температуры, добавляли 0,06 г перекиси водорода в 1 мл дистиллированной воды, смесь вакууммировали для удаления растворенного воздуха и охлаждали до температуры 5°С, добавляли 0,06 мг аскорбиновой кислоты в 0,5 мл дистиллированной воды. Смесь заливали в предварительно охлажденную разъемную стеклянную форму, замораживали в жидком азоте и выдерживали в течение 12 часов при температуре -15°С. По окончании реакции форму размораживали, размыкали, образовавшийся макропористый гидрогель промывали в 200 мл горячей дистиллированной воды, затем трижды промывали этиловым спиртом порциями по 100 мл, после чего сушили в вакууме до постоянной массы. Выход продукта 72%. Общая пористость 54%, средний размер пор 16,3 мкм.
Пример 3
Навеску модифицированного полимера на основе поливинилового спирта, состава
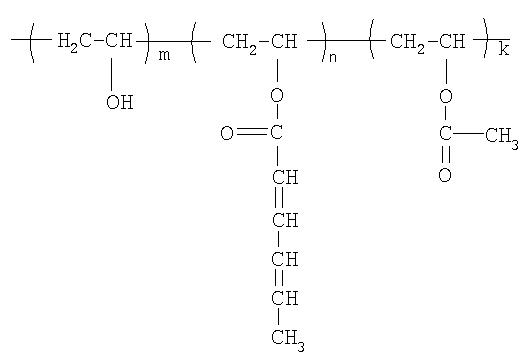
(m = 90,6 мол.%; n = 8,2 мол.%, k = 1,2 мол.%,. Mw = 44000) массой 1 г растворяли при нагревании в 11 мл дистиллированной воды, охлаждали до комнатной температуры, добавляли 0,06 г перекиси водорода в 1 мл дистиллированной воды, смесь охлаждали до температуры 5°С, добавляли 30 мкл. N,N,N',N'-тетраметилэтилендиамина. Смесь заливали в предварительно охлажденную разъемную стеклянную форму, замораживали в жидком азоте и выдерживали в течение 8 часов при температуре - 10°С. По окончании реакции форму размораживали, размыкали, образовавшийся макропористый гидрогель промывали в 200 мл горячей дистиллированной воды, после чего сушили лиофильно. Выход продукта 85%. Общая пористость 74%, средний размер пор 36,1 мкм.
Толщина изделий из данного материала в значительной степени зависит от желаемого использования и может широко варьироваться.
Материал, отвечающий настоящему изобретению, может при необходимости дополнительно содержать мази на водной основе, лекарственные вещества, которые вводятся во время изготовления материала или наносятся непосредственно на готовый материал.
Установлено направленное регулирование фармакодинамических свойств данного материала за счет изменения условий проведения процесса (температуры, концентрации полимера, степени его замещения, метода охлаждения) введения антимикробных веществ, содержащих функциональные группы основного характера. Так, материал может быть модифицирован различными ферментами роста, антисептическими препаратами, например, гентамицином, линкомицином, хлоргексидином и др., а также пропитан растворами глюкозы (20-40%), аскорбиновой кислоты (5%). Также материал может дополнительно содержать местный анальгетик, например, лидокаин.
При изучении деформационно-прочностных характеристик было выявлено, что прочность материала-аналога при увлажнении падает в 5-10 раз, вследствие этого в ряде случаев материал теряет структурную прочность. Максимальное разрывное удлинение, отражающее эластичность материала по данному изобретению, при увлажнении увеличивается в 2,5 раза. Степень адгезии к раневой поверхности (или атравматичность) по отношению к марле медицинской составила 55-60%, что свидетельствует о возможности фиксирования данного материала без применения клеевого слоя и снятии без значительной травматизации подлежащих тканей.
Таким образом, получен атравматичный, сорбционный, пластичный и прочный материал, ингибирующая активность которого сохраняется после двух суток контакта с модельной жидкой средой.
Материал применяют в хирургии, а именно при закрытии чистых колотых, резаных, ушибленных ран, что позволило уменьшить количество гнойных осложнений в полтора раза. Закрытие послеоперационных ран при первичной обработке, гнойных ран после оперативного вмешательства, закрытие швов при брюшнополостных операциях также уменьшило количество гнойных осложнений на 40%. При лечении травматических повреждений отмечено ускорение процессов заживления, быстрое уменьшение отека и гиперемии.
Данный материал применим также при паренхиматозных кровотечениях. В месте с тем возможно сочетание данного материала с гемостатическими средствами, например лиофилизированного феракрила. Местное применение данного материала в сочетании с лиофилизированным феракрилом при анатомических резекциях селезенки собак приводят к остановке кровотечения на 8-10 сек после аппликации. При гистологическом исследовании в плоскости среза селезенки видны тромбированные сосуды, нити фибрина и полиморфноядерные лейкоциты. На границе со здоровой тканью имеется пролиферация фибробластов, зачатки гранулированной ткани.
Материал химически стоек и биологически инертен, стерилизуется в автоклаве. Материал быстро (десятки секунд) впитывает воду в значительных количествах (не мене 8 г на 1 г сухого материала), поверхность гладкая и высокоэластичная.
Сравнительные результаты изучения воздействия материала на раневой процесс отражают следующие данные: использование материала для лечения гнойных ран, иммобилизованного ферментами (трипсин, террилитин, лизоцим, коллагеназа-С, протеаза-С и др.), приводит к значительному сокращению сроков очищения ран от гнойно-некротических масс и уменьшает бактериальную обсемененность их по отношению к группе не леченых экспериментальных животных на 43,3% - 52,5% в случае применения нативной формы материала, а при иммобилизации ферментов - на 48,3% - 64,6%;
заживление - соответственно на 16,7-24,7% и 32,2% - 33,3%.
Введение дополнительно в материал, модифицированный ферментами, хлоргексидина биглюконата (1,0%) приводит к значительному уменьшению сроков очищения и заживления гнойных ран.
Также на основании данного материала может быть изготовлен имплантат или же материал может быть использован для замещения дефектов мягких тканей или заполнения послеоперационных полостей. Макропоры материала достаточно быстро прорастают фибрилами.
Материал можно использовать в качестве дренажного устройства в виде покрытия, полоски, свернутого в рулон или трубки. После образования сочной грануляции дренажное устройство легко отделяется.
На основе материала могут выпускаться изделия медицинского назначения, например, такие как пластины - аппликаторы, салфетки, тупферы, турунды различной формы, в частности для осушения операционного поля или раневой и ожоговой поверхностей.
Раневое покрытие из данного материала удобно и безопасно, им можно пользоваться для перевязки на дому, закрывать бытовые травмы (ожоги, порезы, ссадины и т.д.). Благодаря успокаивающему действию покрытия особенно удобны для лечения небольших травм у детей. Аллергических осложнений при использовании материала в качестве медицинского материала широкого применения не наблюдалось. При чем перевязки при чистых ранах можно не производить, т.к. материал биоразлагаем.
Предлагаемый материал рекомендован для широкого его использования в различных областях хирургии, при трансдермальном введении лекарственных средств, при лечении ран и ожогов различной этиологии, а также при оказании первой помощи в бытовых условиях.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГИДРОГЕЛЕВЫЙ МАТЕРИАЛ НА ОСНОВЕ СШИВАЕМОГО ПОЛИВИНИЛОВОГО СПИРТА | 2013 |
|
RU2543895C2 |
| ИММЕРСИОННАЯ СРЕДА ДЛЯ ПРОВЕДЕНИЯ ОБЪЕМНОЙ ЭХОГРАФИИ ОРБИТЫ ПРИ АНОФТАЛЬМЕ И СУБАТРОФИИ ГЛАЗА И СПОСОБ ПРОВЕДЕНИЯ ОБЪЕМНОЙ ЭХОГРАФИИ ОРБИТЫ ПРИ АНОФТАЛЬМЕ И СУБАТРОФИИ ГЛАЗА | 2011 |
|
RU2470589C1 |
| СПОСОБ ПОЛУЧЕНИЯ СИСТЕМЫ ДОСТАВКИ ВОДОНЕРАСТВОРИМЫХ И ПЛОХОРАСТВОРИМЫХ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ И ЛЕКАРСТВЕННАЯ ФОРМА НА ЕЕ ОСНОВЕ | 2006 |
|
RU2325151C2 |
| СПОСОБ ПОЛУЧЕНИЯ МАКРОПОРИСТЫХ ФОРМОУСТОЙЧИВЫХ ПОЛИМЕРНЫХ ГИДРОГЕЛЕЙ С ИСПОЛЬЗОВАНИЕМ МИКРОВОЛНОВОГО ИЗЛУЧЕНИЯ (ВАРИАНТЫ) | 2019 |
|
RU2715198C1 |
| Способ получения гидрогеля из поливинилового спирта | 1988 |
|
SU1680720A1 |
| ПОЛИМЕРНЫЙ МАТЕРИАЛ ДЛЯ РЕГУЛИРОВАНИЯ РОСТА И РАЗВИТИЯ РАСТЕНИЙ | 2012 |
|
RU2515886C1 |
| СЛОЖНЫЙ (МЕТ)АКРИЛОВЫЙ ЭФИР ПОЛИАЛКОКСИЛИРОВАННОГО ТРИМЕТИЛОЛПРОПАНА (ВАРИАНТЫ) И ЕГО ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ АБСОРБИРУЮЩИХ ВОДОСОДЕРЖАЩИЕ ЖИДКОСТИ ПОЛИМЕРОВ | 2003 |
|
RU2320677C2 |
| Способ получения макропористой пленки для регенеративной медицины на основе L-цистеина, нитрата серебра и поливинилового спирта | 2020 |
|
RU2746882C1 |
| Способ получения сополимеров с влагоудерживающей и загущающей способностью | 1987 |
|
SU1481236A1 |
| КОМПОЗИЦИЯ ДЛЯ ИММОБИЛИЗАЦИИ БИОЛОГИЧЕСКИХ МАКРОМОЛЕКУЛ В ГИДРОГЕЛЯХ, СПОСОБ ПРИГОТОВЛЕНИЯ КОМПОЗИЦИИ, БИОЧИП, СПОСОБ ПРОВЕДЕНИЯ ПЦР НА БИОЧИПЕ | 2001 |
|
RU2206575C2 |
Изобретение относится к области медицины, а именно к медицинским макропористым сшитым полимерным материалам и изделиям на их основе, в частности имплантатам, подложкам для клеточной инженерии, матрицам с контролируемым выделением лекарственных средств, дренажным средствам, и т.п. Изделия из данного материала могут быть применены в офтальмологии, микрохирургии, пластической хирургии, общей, торакальной, сердечно-сосудистой и челюстно-лицевой хирургии, гинекологии, стоматологии, отоларингологии и других областях практической медицины. Макропористый сшитый полимерный материал получен путем проведения полимеризации в водных замороженных растворах водорастворимых ненасыщенных производных поливинилового спирта. Вводимый в боковую цепь ненасыщенный радикал содержит одну или две ненасыщенные группы и обеспечивает образование пространственной структуры в условиях радикальной полимеризации и сополимеризации. Радикал может содержать остаток ненасыщенной кислоты, например, акриловой, метакриловой, сорбиновой, кротоновой, коричной, или алкеновую группу, ненасыщенная группа может быть также введена в виде бокового ацетального заместителя. Материал имеет повышенную термостабильность, развитую пористость высокую дренирующую способность. 11 з.п. ф-лы.
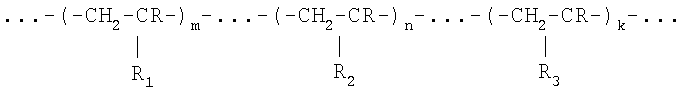
где R - H,
R1 - OH,
R2 - 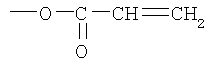
или 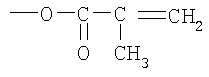
или 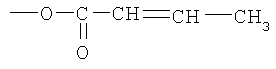
или 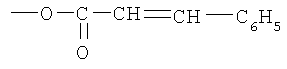
или 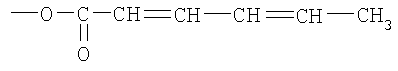
или 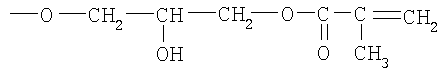
или 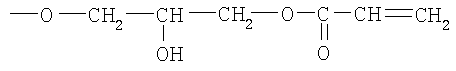
или 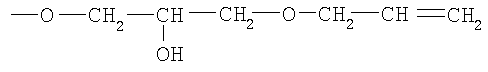
R3 - O-CO-R4,
R4 - СН3 или остаток другой кислоты, из поливинилового эфира которой был получен поливиниловый спирт,
m = 80-99 мол.%,
n = 0,5-15 мол.%,
k = 0-12 мол.%.
| БЕЗВОРСОВЫЙ ПОРИСТЫЙ СОРБЦИОННЫЙ МАТЕРИАЛ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ И ПЕРЕВЯЗОЧНЫЕ ИЗДЕЛИЯ ИЗ НЕГО | 1999 |
|
RU2151615C1 |
| ЛИСТ ЦЕЛЛЮЛОЗЫ, СПОСОБ ЕГО ПОЛУЧЕНИЯ, СПОСОБ ПРОИЗВОДСТВА УПЛОТНЕННОГО ПОЛОТНА, СПОСОБ МОДИФИЦИРОВАНИЯ СВОЙСТВ И ИЗДЕЛИЕ | 2004 |
|
RU2266926C1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2008-07-10—Публикация
2006-07-19—Подача