Изобретение относится к области медицины и касается противовирусных профилактических и лечебных средств и способов их получения.
Существующие противовирусные препараты, как правило, активны только в отношении определенных вирусов. А так как в настоящее время обнаружены уже более тысячи разновидностей вирусов, причем около половины из них представляют опасность для человека, то создание новых противовирусных препаратов просто необходимо. Механизм действия современных противовирусных препаратов заключается в блокировании одного из этапов воспроизводства вирусов в клетках вирусоносителя (человека), которые включают этап прикрепления вируса к клетке и проникновение внутрь ее, встраивание нуклеиновой кислоты вируса в геном клетки хозяина, синтез собственной ДНК и РНК, синтез и сборку собственных белков вируса. Большинство имеющихся противовирусных препаратов представляют собою аналоги нуклеозидов. Они эффективны, однако после их применения у ряда больных наблюдаются рецидивы, возможен феномен рикошета, приводящий к обострению болезни. Кроме того, для ряда противовирусных препаратов характерно развитие устойчивости вирусов к ним. Все перечисленные факторы являются свидетельством того, что только создание новых противовирусных препаратов может обеспечить прогресс в лечении вирусных заболеваний.
Имеется множество публикаций, описывающих производные 6-галоген-5-гидроксииндол-3-карбоксилатов.
В WO 05/87729 описываются производные 5-гидроксииндол-3-карбоксилатов общей формулы М:
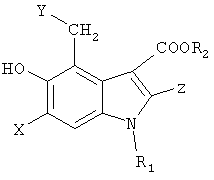 ,
,
где Х - галоген,
Y означает группу NR3R4, в которой R3 и R4 могут быть водородом, С1-10алкилом,
С3-7циклоалкилом, С2-10алкенилом или С2-10алкинилом или R3 и R4 вместе с N образуют 5-10-членный гетероцикл, который может содержать дополнительно в качестве гетероатома N, O или S,
R1 может означать С1-5алкил, С3-7циклоалкил,
R2 может означать С1-5алкил,
Z-CH2-S-R5, CH2-S(O)m-R5, m=1, 2; CH2-S(O)m,-(CH2)(n или p)-(O)q-Ar, где n, р означают 0-5, q=0, или n, р и q=0 или n, p=1-4, q=0-1. У казанные соединения могут быть использованы в качестве медикаментов против вируса гепатита В (anti-HBV) и вируса иммунодефицита человека (anti-HIV). Описываются также способы получения соединений.
В WO 04/0600873 описываются соединения общей формулы N:
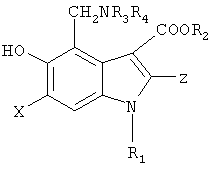
где Х - галоген, Z-СН2-S-R5, CH2NR6R7, R1 может означать С1-10алкил, С3-7циклоалкил, R2 может означать С1-4алкил, R5 может означать С1-4алкил, R3 и R3 могут быть водородом, алкилом и т.д., или R3 и R3 вместе с N образуют цикл. Соединения обладают высоким ингибирующим действием при вирусе гриппа и острого респираторного заболевания и могут быть использованы как противогриппозные агенты для лечения и профилактики при вирусе острого респираторного заболевания. Описывается также фармацевтическая композиция и способ получения соединений.
В CN 1482118 описываются соединения общей формулы N, где Z-Н, -CH2-S-R5, -CH2-NR6R7, С1-10алкил, С2-10алкенил или С2-10алкинил, которые могут быть использованы как противогриппозные агенты и для лечения и профилактики при вирусе острого респираторного заболевания. Описывается также фармацевтическая композиция и способ получения соединений.
В JP 63-188665 описываются 6-галоген-5-гидроксииндол-3-карбоксилаты формулы Р:
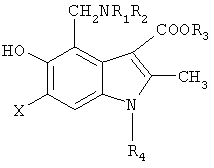
где R1 и R2 - водород, алкил, аралкил или R1 и R2 вместе с атомом азота образуют гетерциклическую группу, R3-алкил, аралкил, R4-Н, алкил, циклоалкил, арил или аралкил, Х-галоген, и их кислотно-аддитивные соли. В частности, раскрываются метил-1-циклогексил-4-пиперидинометил-6-бром-5-гидроксииндол-3-карбоксилат и метил-1-бензил-4-пиперидинометил-6-бром-5-гидроксииндол-3-карбоксилат. Соединения формулы Р могут быть использованы для лечения циркулирующих заболеваний, таких как заболевания крови, а также обладают антикоагуляционным эффектом, свойствами ингибитора 5-липогеназы и т.д.
В Chinese Chemical Letters (English), 2004, 15(9), 1039-1041 описывается синтез и противовирусная активность в отношении вируса гриппа производных этил-6-бром-5-гидроксииндол-3-карбоксилатов, в частности, этилового эфира 6-бром-1-циклопропил-4-диметиламинометил-5-гидрокси-2-[(фенилтио)метил]-1Н-индол-3-карбоновой кислоты. В Journal Indian Chemical Society, 1994, 71(4), 175-8 описывается синтез и антимикробная активность производных 5-гидроксииндолов, в частности, этилового эфира 6-бром-5-гидрокси-2-метил-1-(фенилметил)-4-(1-пирролидинилметил)-1Н-индол-3-карбоновой кислоты и этилового эфира 6-бром-5-гидрокси-2-метил-1-(фенилметил)-4-(1-пиперидинилметил)-1Н-индол-3-карбоновой кислоты.
В WO 90/08135, RU 2033156 опубл. в 1995 г.; RU 2033I57 опубл. в 1995 г. описывается моногидрат гидрохлорида этилового эфира-6-бром-5-гидрокси-4-диметиламинометил-1-метил-2-фенилтиометилиндол-3-карбоновой кислоты (Арбидол), обладающий противотивирусным, интерферониндуцирующим и иммуномодулирующим действием, а также способ его получения и фармацевтическая композиция.
Указанное соединение является наиболее близким по структуре и по активности к соединениям настоящего изобретения.
Однако арбидол проявляет недостаточную эффективность к некоторым штаммам вирусов.
Задача, решаемая изобретением, - новые соединения с расширенным спектром противовирусного действия, способ их получения, фармацевтическая композиция и применение соединений. Ни в одном из известных документов не раскрываются указанные ниже конкретные соединения общей формулы I или применение соединений общей формулы I для лечения или профилактики вируса гриппа А и В.
Согласно изобретению предлагаются производные 4-аминометил-5-гидрокси-6-бром-3-алкоксикарбонилиндола общей формулы I:
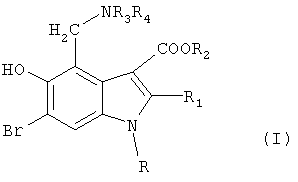
R - циклогексил, циклогептил,
R1-C1-С3-алкил, -CH2-X-фенил,
X-NH, O, S,
R2-С1-С5-алкил,
R3, R4 имеют одинаковое значение и выбираются из C1-С3алкила, преимущественно, СН3, или
R3 и R4 вместе с атомом азота образуют - 5-10-членный гетероцикл, который содержит 1-2-гетероатома,выбираемых из N, О, S,
или их фармацевтически приемлемые соли,
за исключением
6-бром-5-гидрокси-4-диметиламинометил-2-фенилтиометил-1-циклогексил-3-этоксикарбонилиндола,
6-бром-5-гидрокси-4-диметиламинометил-2-метил-1-циклогексил-3-этоксикарбонилиндола и
6-бром-5-гидрокси-4-диметиламинометил-2-(1-пиперидинометил)-1-циклогексил-3-этоксикарбонилиндола,
6-бром-5-гидрокси-4-диметиламинометил-2-(1-пирролидинометил)-1-циклогексил-3-этоксикарбонилиндола.
Соли могут быть приготовлены обычными методами, например обработкой соединения формулы I соответствующей кислотой.
К солям относятся, например, гидрохлориды, мезилаты, оксалаты и др.
Способ получения соединений формулы I, где R1 означает C1-С3-алкил включает следующие стадии:
а) взаимодействие соответствующего алкил-β-аминокротоната с п-бензохиноном, с получением алкил-2-алкил-5-гидроксииндол-3-карбоксилата формулы II
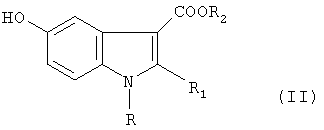
где R, R2, имеют значения, указанные в п.1, R1-C1-С3-алкил
б) соответствующий алкил-2-алкил-5-гидроксииндол-3-карбоксилат формулы II:
подвергают бромированию бромирующим агентом в кислой среде с получением соответствующего алкил-2-алкил-6-бром-5-гидроксииндол-3-карбоксилата формулы
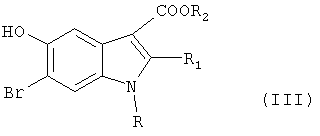
где R1, R2, R имеют вышеуказанные значения,
в) полученное на стадии б) соединение формулы III подвергают аминометилированию соответствующим аминометилирующим агентом для получения соответствующего вышеуказанного соединения изобретения общей формулы 1, где R1 означает С1-С3-алкил
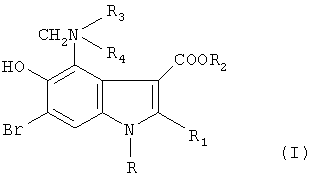
Способ получения соединений формулы I, где R1 означает -СН2-Х-фенил, в которой Х выбирается из NH, O или S, включает стадии:
а) взаимодействие соответствующего алкил-β-аминокротоната с п-бензохиноном, с получением алкил-2-метил-5-гидроксииндол-3-карбоксилата формулы II
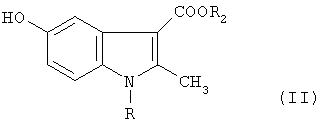
где R, R2, имеют значения, указанные в п.1,
б) бромирование соответствующего алкил-2-метил-5-гидроксииндол-3-карбоксилата формулы II, с получением соответствующего 6-бромпроизводного формулы III:
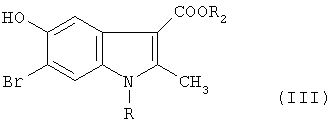
где R, R2 имеют значения, указанные выше.
в) полученное на стадии а) соединение формулы III обрабатывают уксусным ангидридом и получают производные 5-ацетоксииндола формулы IV:
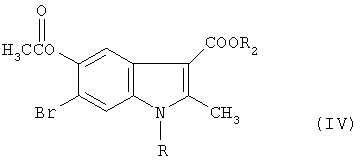
где R, R2 имеют значения, указанные выше
г) в полученном соединении формулы IV бромируют СН3-группу и получают бромметильное соединение формулы V:
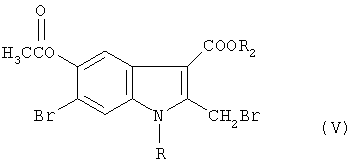
где R, R2 имеют значения, указанные выше,
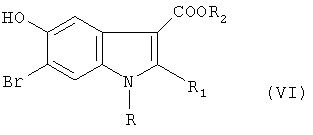
д) соединение формулы V подвергают взаимодействию с соединением, выбираемым из соответствующего тиофенола, фенола, первичного или вторичного амина в среде органического растворителя и после удаления в кислой среде защитной ацетоксигруппы получают соединение формулы VI:
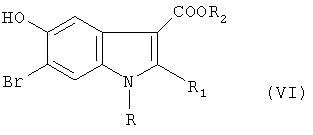
где R, R2 имеют значения, указанные выше, а
R1 означает -CH2; -Х-фенил, в которой Х выбирается из NH, O или S.
е) полученное на стадии г) соединение VI аминометилируют соответствующим аминометилирующим агентом и получают соединение общей I, где R1 означает -СН2-X-фенил.
Соединение общей I, получаемое по любому из вышеуказанных способов, выделяют или, при необходимости, переводят в соответствующую фармацевтически приемлемую соль.
Предлагаемые противовирусные соединения оказались эффективными в отношении различных штаммов вируса гриппа. При этом имеются различия в эффективности предлагаемых препаратов и ближайшего аналога (Арбидола) по отношению к различным штаммам. Заявляемые соединения оказались эффективными и в отношении других вирусов и при этом не являются аналогами нуклеозидов, что позволяет надеяться на то, что они пополнят список препаратов с иным более «мягким», не затрагивающим обменные процессы в клетках механизмом действия. Таким образом, достигается технический результат.
Более подробно изобретение описывается ниже.
Приведенные ниже примеры показывают возможность осуществления предлагаемого изобретения.
6-Бром-5-гидрокси-4-диметиламинометил-2-метил-1-циклогексил-n-пропоксикарбонилиндол соответствующий формуле В:
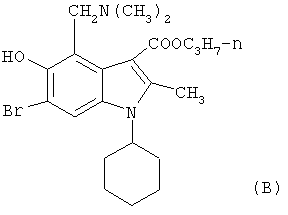
Способ синтеза этого нового, не описанного в литературе соединения приводится ниже. 3-гидрокси-2-метил-1-циклогексил-3-n-пропоксикарбонилиндол бромируют в положение 6 бромом в уксусной кислоте или N-бромсукцинимидом в хлороформе.
Полученный 6-бром-5-гидрокси-2-метил-1-циклогексил-3-n-пропоксикарбонилиндол подвергают аминометилироваиию бис (диметиламино) метаном в среде органического растворителя, например в диоксане.
СХЕМА СИНТЕЗА соединения В.
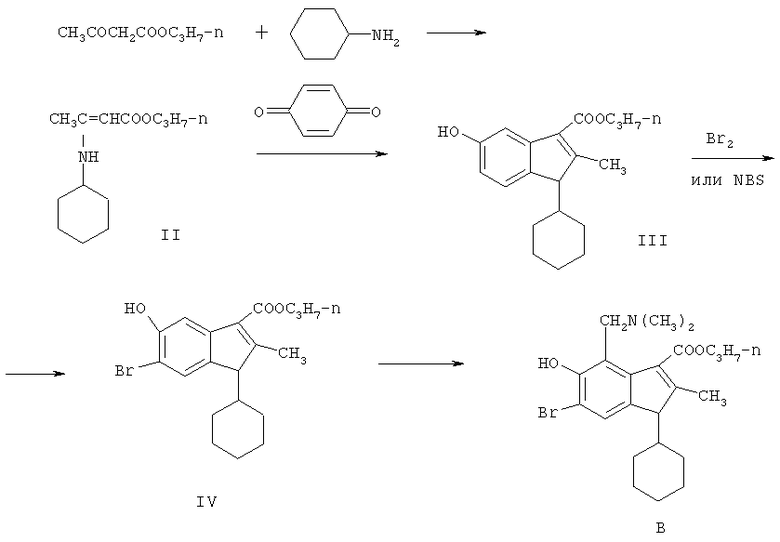
Пример 1. н-Пропиловый эфир β-циклогексиламинокротоновой кислоты (II).
К 14,47 г (0,1 моль) n-пропилацетоуксусного эфира в 20 мл толуола добавляют 11,9 г (0,12 моль) циклогексиламина и 1 каплю концентрированной соляной кислоты. Затем отгоняют выделившуюся воду с насадкой Дина-Старка. Толуол и избыток циклогексиламина отгоняют в вакууме, остаток используют без перегонки. Выход 87%.
Пример 2. 5-Гидрокси-2-метил-1-циклогексил-3-n-пропоксикарбонилиндол (III).
К раствору 2,24 г (0,01 моль) II в 10 мл ледяной уксусной кислоты при помешивании добавляют 1,08 г (0,01 моль) 1,4-бензохинона. Реакционную смесь оставляют на сутки при комнатной температуре. Образовавшийся осадок отфильтровывают, промывают холодной уксусной кислотой, водой и спиртом. Выход (III) 0,64 г (20%), т.пл. 225°С (из диоксана).
Пример 3. 6-Бром-5-гидрокси-2-метил-1-циклогексил-3-пропоксикарбонилиндол (IV)
А) К суспензии 3,15 г (0,01 моль) III в 20 мл уксусной кислоты при перемешивании и комнатной прикапывают раствор 1,6 г (0,01 моль) брома в 2 мл уксусной кислоты в течение 30 минут. Помешивают 2 часа при комнатной температуре, добавляют воду, осадок отфильтровывают, промывают водой. Выход 2,7 г (68,4%). т.пл. 215°С уксусной кислоты).
Б) К суспензии 6,3 г (0,02 моль) III в 100 мл хлороформа при помешивании добавляют 3,6 г N-бромсукцинимида и оставляют при комнатной температуре на ночь.
Осадок IV отфильтровывают. Хлороформ упаривают в вакууме, добавляют спирт и воду. Образовавшиеся осадки объединяют и промывают спиртом. Выход 4,92 (62,5%). Т.пл. 215°С (из диоксана). Идентичность подтверждена также хроматографически в системе бензол-спирт 10:2 на пластинках Silufol UV 254.
Пример 4. 6-Бром-5-гидрокси-4-диметиламинометил-2-метил-1-циклогексил-3-n-пропоксикарбонилиндол (В).
Смесь 0,79 г (0,002 моль) IV, 0.45 мл бис(диметиламино)метана в 10 мл диоксана кипятят 3 часа. После упаривания диоксана добавляют спирт и воду, декатируют спиртоводный слой, снова добавляют спирт, осадок отфильтровывают. Выход В 0,52 г (57,5%) т.пл. 135°С (из спирта).
Строение полученных соединений подтверждено данными элементного анализа, спектрами ПМР, индивидуальность - хроматографически в системе бензол - спирт 10:2 и бензол-спирт-триэтиламин 10:2:0,1 на пластинках Silufol UV 254.
6-Бром-5-гидрокси-4-диметиламинометил-2-фенилтиометил-1-циклогексил-3-n-пропоксикарбонилиндол имеет структуру соответствующую формуле С:
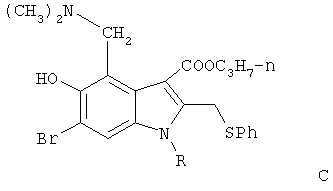
Соединение С получают согласно ниже указанной схеме синтеза.
Синтез ведут бромированием 5-гидрокси-2-метил-1-циклогексил-3-n-пропоксикарбонилиндола в 6-е положение бромом в уксусной кислоте или N-бромсукцинимидом (NBS) в хлороформе. Полученный 6-бром-5-гидрокси-2-метил-1-циклогексил-3-n-пропоксикарбонилиндол после обработки уксусным ангидридом бромируют в боковую цепь N-бромсукцинимидом, преимущественно в среде CCl4, в присутствии катализатора - инициатора радикального процесса (перекиси бензоила) при освещении. Затем полученный продукт обрабатывают тиофенолятом калия в среде органического растворителя и далее гидролизуют раствором минеральной кислоты в органическом растворителе. Полученное соединение подвергают аминометилированию аминометилирующим агентом, таким как бис- (диметиламино)метан, в органическом растворителе. Возможно также использование диметиламина и формальдегида в качестве аминометилирующего агента.
СХЕМА СИНТЕЗА:
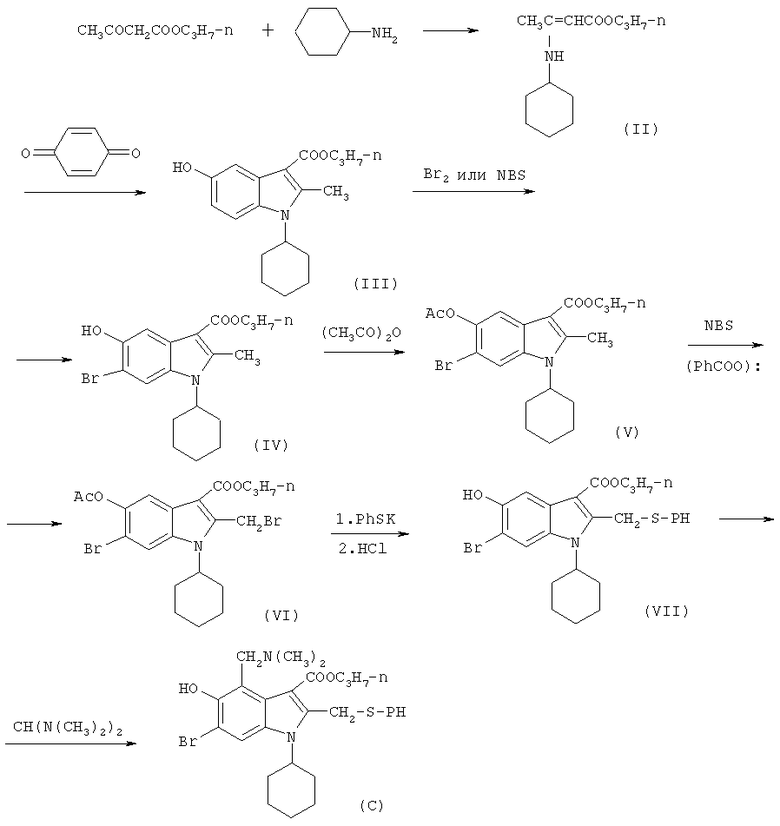
Пример 5. 5-Ацетокси-6-бром-2 метил-1-циклогексил-3-n-пропоксикарбонилиндол (V).
Смесь 2,36 г (0,006 моль) IV 0,61 мл уксусного ангидрида и 0,7 мл пиридина кипятят 3 часа. Реакционную смесь охлаждают, добавляют воду, осадок отфильтровывают, промывают водой. Выход 2,15 г (82%), т.пл. 165°С (из спирта).
Пример 6. 5-Ацетокси -6-бром-2-бромметил-1-циклогексил-3-n-пропоксикарбонилиндол (VI).
Смесь 1,96 г (0,0045 моль) V, 0.8 г (0,0045 моль) N-бромсукцинимида, 0,04 г перекиси бензоила в 10 мл четыреххлористого углерода кипятят 4 часа при освещении лампой 300 Вт. От горячего раствора отфильтровывают сукцинимид, промывают его горячим CCl4. После упаривания растворителя выделяют VI. Выход 2,3 г (88,8%), т.пл. 130°С (из гептана).
Пример 7. 6-Бром-5-гидрокси-2-фенилтиометил-1-циклогексил-3-n-пропоксикарбонилиндол (VII).
К раствору 0,2 г (0,0035 моль) едкого калия в 6 мл спирта при перемешивании добавляют 0,39 г (0,0035 моль) тиофенола, затем раствор 1,76 г (0,0035 моль) VI в 10 мл бензола. Через 4 часа отфильтровывают осадок бромистого калия. Маточник упаривают в вакууме. К остатку добавляют 10 мл спирта, 4 мл концентрированной соляной кислоты и кипятят 1 час. После охлаждения и разбавления водой осадок отфильтровывают, промывают водой. Выход VII 0,93 г (52,9%) VII, т.пл. 180°С (из спирта).
Пример 8. 6-Бром-5-гидрокси-4-диметиламинометил-2-фенилтиометил-1-циклогексил-3-n-пропоксикарбонилиндол (С).
Смесь 0,75 г (0,0015 моль) VII, 0,25 мл бис(диметиламино) метана в 5 мл диоксана кипятят 4 часа. После упаривания диоксана добавляют воду, экстрагируют хлороформом. Хлороформенный раствор промывают водой, сушат б/в Na2SO4, упаривают в вакууме хлороформ, к остатку добавляют гексан. Осадок отфильтровывают. Выход 0,62 г (74%), т.пл. 145 (из спирта).
Аналогично способу получения соединений В и С могут быть получены другие соединения данного изобретения с использованием соответствующих исходных соединений.
6-Бром-5-гидрокси-4-морфолинометил-2-фенилтиометил-1-циклогексил-3-n-ропоксикарбонилиндол, Тпл. 153°С.
6-Бром-5-гидрокси-4-пирролидинометил-2-фенилтиометил-1-циклогексил-3-n-пропоксикарбонилиндол, Тпл. 148°С.
6-Бром-5-гидрокси-4-диметиламинометил-2-фениламинометил-1-циклогексил-3-n-пропоксикарбонилиндол, Тпл. 175°С.
6-Бром-5-гидрокси-4-диметиламинометил-2-феноксиметил-1 -циклогексил-3-n-пропоксикарбонилиндол, Тпл. 135°C.
Изучение действия соединений на вирусы гриппа А и В было проведено в культуре клеток MDCK. Выполнялось исследование по следующей схеме: на монослой 96-луночной панели вносили вещество (предварительно растворяли в ДМСО, затем питательной среде) в различных концентрациях (12,5; 10,0; 7,5; 5,0 мкг/мл), инкубировали 2-3 часа при 37,0°С, а затем вносили разведения вируса (10-I. 10-2, 10-3, 10-4). Панели инкубировали 24 часа при 37,0°С, а затем реакцию заканчивали постановкой имуноферментного анализа, последовательно нанося мышиные моноклональные антитела к вирусам гриппа А или В, конъюгат (козьи антитела к моноклоальным мышиным антителам, меченные пероксидазой хрена), субстрат (орто-фенилендиамин). Учет результатов проводили при сравнении показателей оптической плотности в контрольных, (вирус) и опытных лунках (вирус + заявленное соединение). В таблицах 1, 2 и 3 приведены результаты подавления репродукции (%) вирусов гриппа А и В в присутствии соединений В и С. Необходимо подчеркнуть, что в исследование были включены вирусы гриппа, имевшие эпидемическую активность в сезонах 2003-2004 и 2001-2005 гг., а также эталонный штамм вируса гриппа А/Калифорния/7/04 (H3N2). Степень чувствительности вирусов определялась их штаммовой принадлежностью.
Сравнительная эффективность действия соединения В и арбидола на вирус гриппа А
Сравнительная эффективность действия соединение С и арбидола на вирус гриппа А
Полученные результаты свидетельствуют о вирусспецифической ативности заявленных соединений, которая сравнима с активностью препаратов «Арбидол» и «Ремантадин».
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ 5-ГИДРОКСИ-4-АМИНОМЕТИЛ-1-ЦИКЛОГЕКСИЛ (ИЛИ ЦИКЛОГЕПТИЛ)-3-АЛКОКСИКАРБОНИЛИНДОЛОВ, ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ОБЛАДАЮЩИЕ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2008 |
|
RU2386616C2 |
| ПРОИЗВОДНЫЕ ИНДОЛ-3-КАРБОНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЕ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2552422C2 |
| ПРОИЗВОДНЫЕ 5-ЗАМЕЩЕННЫХ ИНДОЛ-3-КАРБОНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЕ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2007 |
|
RU2387642C2 |
| ПОЛУЧЕНИЕ ВОДОРАСТВОРИМОГО СОЕДИНЕНИЯ ДИГИДРОХЛОРИДА 6-БРОМ-1-МЕТИЛ-5-МЕТОКСИ-2-(1-ПИПЕРИДИНОМЕТИЛ)-3-(2-ДИЭТИЛАМИНОЭТОКСИ) КАРБОНИЛИНДОЛА | 2024 |
|
RU2835077C1 |
| ПРОИЗВОДНОЕ ИНДОЛ-3-КАРБОНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩЕЕ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ SARS-COV-2 | 2022 |
|
RU2820633C1 |
| КЛАТРАТНЫЙ КОМПЛЕКС β-ЦИКЛОДЕКСТРИНА С ПРОИЗВОДНЫМ 5-ГИДРОКСИ-4-АМИНОМЕТИЛ-1-ЦИКЛОГЕКСИЛ(ИЛИ ЦИКЛОГЕПТИЛ)-3-АЛКОКСИКАРБОНИЛИНДОЛА, СПОСОБ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2011 |
|
RU2464042C1 |
| ЗАМЕЩЕННЫЕ ЭФИРЫ 1Н-ИНДОЛ-3-КАРБОНОВОЙ КИСЛОТЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2006 |
|
RU2323210C9 |
| АКТИВНЫЕ СУБСТАНЦИИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2007 |
|
RU2338531C1 |
| ЗАМЕЩЕННЫЕ ЭФИРЫ 1,2,3,7-ТЕТРАГИДРОПИРРОЛО[3,2-f][1,3]БЕНЗОКСАЗИН-5-КАРБОНОВЫХ КИСЛОТ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И ПРИМЕНЕНИЯ | 2006 |
|
RU2323221C9 |
| ЗАМЕЩЕННЫЕ ЭФИРЫ 5-ГИДРОКСИ-1Н-ИНДОЛ-3-КАРБОНОВОЙ КИСЛОТЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2007 |
|
RU2344817C1 |
Изобретение относится к новым производным 4-аминометил-5-гидрокси-6-бром-3-алкоксикарбонилиндола общей формулы I:
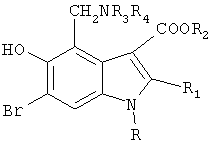
где: R означает циклогексил, циклогептил;
R1 означает C1-С3-алкил, -СН2-Х-фенил;
Х означает NH, О, S;
R2 означает С1-С5-алкил, R3, R4 имеют одинаковое значение и выбираются из C1-С3алкила, преимущественно, СН3, или
R3 и R4 вместе с атомом азота образуют - 5-10-членный гетероцикл, который
содержит 1-2-гетероатома, выбираемых из N, О, S,
или их фармацевтически приемлемые соли,
за исключением
6-бром-5-гидрокси-4-диметиламинометил-2-фенилтиометил-1-циклогексил-3-этоксикарбонилиндола,
6-бром-5-гидрокси-4-диметиламинометил-2-метил-1-циклогексил-3-этоксикарбонилиндола,
6-бром-5-гидрокси-4-диметиламинометил-2-(1-пиперидинометил)-1-циклогексил-3-этоксикарбонилиндола,
6-бром-5-гидрокси-4-диметиламинометил-2-(1-пирролидинометил)-1-циклогексил-3-этоксикарбонилиндола, и
метил-1-циклогексил-4-пиперидинометил-6-бром-5-гидрокси-2-метил-индол-3-карбоксилата.
Соединения проявляют противовирусную активность и могут быть использованы для лечения гриппа типа А. Описаны способы получения соединений I. 4 н. и 1 з.п. ф-лы, 2 табл.
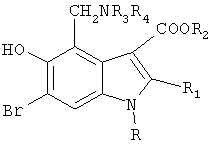
где R - циклогексил, циклогептил,
R1 - C1-С3-алкил, -СН2-Х-фенил,
X - NH, О, S,
R2 - С1-С5-алкил,
R3, R4 имеют одинаковое значение и выбираются из C1-С3алкила,
преимущественно СН3, или
R3 и R4 вместе с атомом азота образуют 5-10-членный гетероцикл, который содержит 1-2-гетероатома, выбираемых из N, О, S,
или их фармацевтически приемлемые соли,
за исключением
6-бром-5-гидрокси-4-диметиламинометил-2-фенилтиометил-1-циклогексил-3-этоксикарбонилиндола,
6-бром-5-гидрокси-4-диметиламинометил-2-метил-1-циклогексил-3-этоксикарбонилиндола,
6-бром-5-гидрокси-4-диметиламинометил-2-(1-пиперидинометил)-1-циклогексил-3-этоксикарбонилиндола,
6-бром-5-гидрокси-4-диметиламинометил-2-(1-пирролидинометил)-1-циклогексил-3-этоксикарбонилиндола и
метил-1-циклогексил-4-пиперидинометил-6-бром-5-гидрокси-2-метил-индол-3-карбоксилата.
а) взаимодействие соответствующего алкил-β-аминокротоната с п-бензохиноном с получением алкил-2-алкил-5-гидроксииндол-3-карбоксилата формулы II
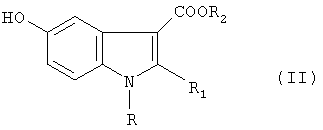
где R, R2, имеют значения, указанные в п.1, R1 - C1-С3-алкил
б) соответствующий алкил-2-алкил-5-гидроксииндол-3-карбоксилат формулы II
подвергают бромированию бромирующим агентом в кислой среде с получением соответствующего алкил-2-алкил-6-бром-5-гидроксииндол-3-карбоксилата формулы III
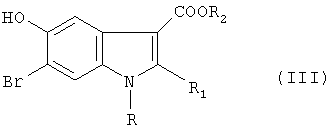
где R1, R2, R имеют вышеуказанные значения,
в) полученное на стадии б) соединение формулы III подвергают аминометилированию соответствующим аминометилирующим агентом для получения соответствующего вышеуказанного соединения общей формулы I, где R1 означает С1-С3-алкил, которое выделяют или переводят в соответствующие фармацевтически приемлемые соли.
а) взаимодействие соответствующего алкил-β-аминокротоната с п-бензохиноном с получением алкил-2-метил-5-гидроксииндол-3-карбоксилата формулы II
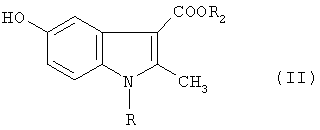
где R, R2, имеют значения, указанные в п.1,
б) бромирование соответствующего алкил-2-метил-5-гидроксииндол-3-карбоксилата формулы II в кислой среде с образованием 6-бромпроизводного формулы III
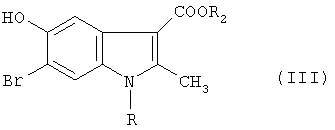
где R, R2 имеют значения, указанные выше.
в) полученное на стадии а) соединение формулы III обрабатывают уксусным ангидридом и получают производные 5-ацетоксииндола формулы IV
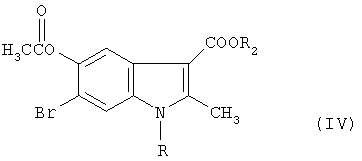
где R, R2 имеют значения, указанные выше
г) в полученном соединении формулы IV бромируют СН3-группу и получают бромметильное соединение формулы V
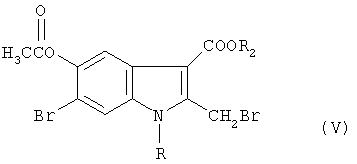
где R, R2 имеют значения, указанные выше,
д) соединение формулы V подвергают взаимодействию с соответствующим тифенолом, или фенолом, или NH2 фенилом в среде органического растворителя и после удаления в кислой среде защитной ацетоксигруппы получают соединение формулы VI
где R, R2 имеют значения, указанные выше, а
R1 означает -СН2-Х-фенил, в которой Х выбирается из NH, O или S.
е) полученное на стадии д) соединение VI аминометилируют соответствующим аминометилирующим агентом и получают соединение общей формулы I, указанное выше.
которое выделяют или переводят в соответствующие фармацевтически приемлемые соли.
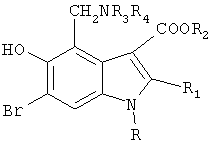
где R - циклогексил, циклогептил,
R1 - C1-С3-алкил, -СН2-Х-фенил,
X - NH, O, S,
R2 - С1-С5-алкил,
R3, R4 имеют одинаковое значение и выбираются из С1-С3алкила, преимущественно СН3 или
R3 и R4 вместе с атомом азота образуют 5-10-членный гетероцикл, который
содержит 1-2-гетероатома, выбираемых из N, О, S,
или их фармацевтически приемлемых солей для приготовления лекарственных средств для лечения гриппа типа А.
| J | |||
| of the Indian Chemical Society, 71 (4), 175-178, 1994 | |||
| Хлоргидрат 1-метил-2-фенилтиометил-3-карбэтокси-4-диметиламинометил-5-окси-6-броминдола, обладающий противовирусным действием, и способ его получения | 1974 |
|
SU1685933A1 |
Авторы
Даты
2008-07-27—Публикация
2006-04-18—Подача