Группа изобретений относится к медицине и может быть использована для лечения бактериальных инфекций, вызванных грамположительными бактериями. Способы по изобретению включают введение далбаванцина для лечения бактериальных инфекций, в частности грамположительных бактериальных инфекций кожи и мягких тканей. Схемы дозировки включают введение далбаванцина один раз в неделю, что обеспечивает его содержание на терапевтическом уровне в плазме на протяжении, по меньшей мере, 1 недели. Фармацевтические композиции по изобретению включают единичную дозу далбаванцина в количестве, достаточном для обеспечения терапевтически эффективного уровня далбаванцина в плазме. Данная группа изобретений обеспечивает длительное терапевтическое действие против грамположительной бактериальной инфекции. 8 н. и 78 з.п. ф-лы, 13 ил., 17 табл.
1. Способ лечения бактериальной инфекции, включающей грамположительные бактерии, у нуждающегося в этом человека, включающий:
введение начальной и последующих терапевтически эффективных доз далбаванцина в фармацевтически приемлемом носителе пациенту,
причем каждая доза отделена 5-10 днями, и при этом начальная доза составляет от приблизительно 500 мг до приблизительно 5000 мг, причем начальная доза содержит, по меньшей мере, приблизительно в 2 раза больше далбаванцина, чем содержится в последующей дозе.
2. Способ по п.1, который включает введение единственной последующей дозы.3. Способ по п.2, в котором последующая доза вводится приблизительно через 1 нед после начальной дозы без какой-либо промежуточной дозы далбаванцина.4. Способ по п.1, который включает введение множественных последующих доз.5. Способ по п.4, в котором указанные последующие дозы вводятся с интервалом приблизительно в 1 нед без какой-либо промежуточной дозы далбаванцина.6. Способ по п.1, в котором бактериальная инфекция представляет собой инфекцию кожи и мягких тканей.7. Способ по п.1, в котором начальная доза составляет приблизительно 1500 мг.8. Способ по п.1, в котором начальная доза составляет приблизительно 1000 мг.9. Способ по п.1, в котором начальная доза составляет приблизительно 800 мг.10. Способ по п.1, в котором начальная доза составляет приблизительно 500 мг.11. Способ по п.1, в котором каждая последующая доза составляет от приблизительно 400 мг до приблизительно 1000 мг.12. Способ по п.1, в котором каждая последующая доза составляет приблизительно 500 мг.13. Способ по п.1, в котором каждая последующая доза составляет приблизительно 400 мг.14. Способ по п.1, в котором каждая последующая доза составляет приблизительно 250 мг.15. Способ по п.1, в котором каждая последующая доза составляет приблизительно 200 мг.16. Способ по п.1, в котором начальная доза составляет приблизительно 1000 мг и каждая последующая доза составляет приблизительно 250 мг.17. Способ лечения бактериальной инфекции, включающей грамположительные бактерии, у нуждающегося в этом человека, включающий:введение начальной и последующих терапевтически эффективных доз далбаванцина в фармацевтически приемлемом носителе пациенту,
причем каждая доза отделена одной неделей, и при этом начальная доза составляет приблизительно 1000 мг, и каждая последующая доза составляет приблизительно 500 мг.
18. Способ по п.17, который включает введение единственной последующей дозы.19. Способ по п.17, в котором последующая доза вводится через приблизительно 1 неделю после начальной дозы без какой-либо промежуточной дозы далбаванцина.20. Способ по п.17, который включает введение множественных последующих доз.21. Способ по п.20, в котором последующие дозы вводятся с интервалом в приблизительно 1 нед без какой-либо промежуточной дозы далбаванцина.22. Способ по п.17, в котором бактериальная инфекция представляет собой инфекцию кожи и мягких тканей.23. Способ лечения бактериальной инфекции, включающей грамположительные бактерии, у нуждающегося в этом человека, включающий:введение начальной и последующих терапевтически эффективных доз далбаванцина в фармацевтически приемлемом носителе пациенту,
причем каждая доза отделена 5-10 днями, и при этом начальная доза составляет от приблизительно 500 мг до приблизительно 5000 мг, и каждая последующая доза составляет от приблизительно 250 мг до приблизительно 2500 мг.
24. Способ по п.23, который включает введение единственной последующей дозы.25. Способ по п.24, в котором последующая доза вводится через приблизительно 1 нед после начальной дозы без какой-либо промежуточной дозы далбаванцина.26. Способ по п.23, который включает введение множественных последующих доз.27. Способ по п.26, в котором последующие дозы вводятся с интервалом в приблизительно 1 нед без какой-либо промежуточной дозы далбаванцина.28. Способ по п.23, в котором бактериальная инфекция представляет собой инфекцию кожи и мягких тканей.29. Способ по п.28, в котором бактериальная инфекция представляет собой осложненную инфекцию кожи и мягких тканей.30. Способ по п.28, в котором бактериальная инфекция представляет собой неосложненную инфекцию кожи и мягких тканей.31. Способ по п.23, в котором начальная доза составляет приблизительно 1500 мг.32. Способ по п.23, в котором начальная доза составляет приблизительно 1000 мг.33. Способ по п.23, в котором начальная доза составляет приблизительно 800 мг.34. Способ по п.23, в котором начальная доза составляет приблизительно 500 мг.35. Способ по п.23, в котором каждая последующая доза составляет от приблизительно 400 мг до приблизительно 1000 мг.36. Способ по п.23, в котором каждая последующая доза составляет приблизительно 500 мг.37. Способ по п.23, в котором каждая последующая доза составляет приблизительно 400 мг.38. Способ по п.23, в котором каждая последующая доза составляет приблизительно 250 мг.39. Способ по п.23, в котором каждая последующая доза составляет приблизительно 200 мг.40. Способ по п.23, в котором начальная доза составляет приблизительно 1000 мг и каждая последующая доза составляет приблизительно 250 мг.41. Способ лечения бактериальной инфекции, включающей грамположительные бактерии, у нуждающегося в этом человека, включающий:введение начальной и последующих терапевтически эффективных доз далбаванцина в фармацевтически приемлемом носителе пациенту,
причем каждая доза отделена 5-10 днями, и при этом начальная доза составляет от приблизительно 200 мг до приблизительно 1500 мг, и каждая последующая доза составляет от приблизительно 200 мг до приблизительно 1500 мг.
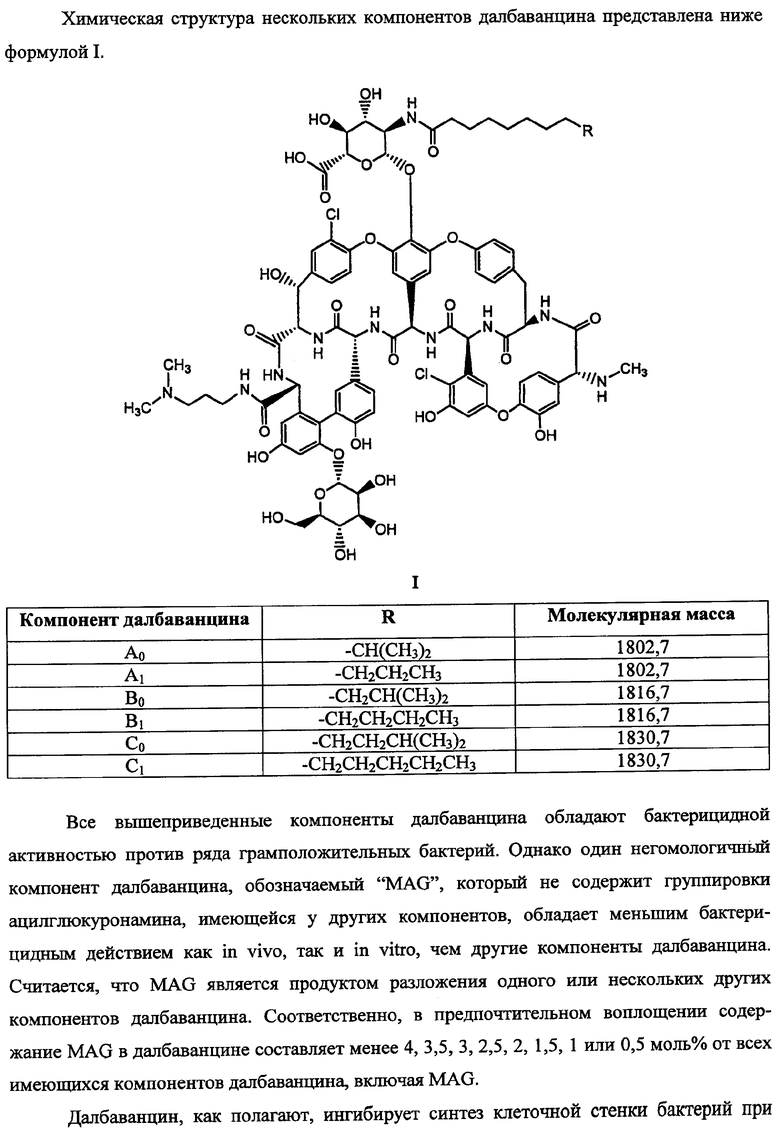
42. Способ по п.41, который включает введение единственной последующей дозы.43. Способ по п.42, в котором последующая доза вводится через приблизительно 1 нед после начальной дозы без какой-либо промежуточной дозы далбаванцина.44. Способ по п.41, который включает введение множественных последующих доз.45. Способ по п.44, в котором указанные последующие дозы вводятся с интервалом в приблизительно 1 нед без какой-либо промежуточной дозы далбаванцина.46. Способ по п.41, в котором бактериальная инфекция представляет собой инфекцию кожи и мягких тканей.47. Способ по п.46, в котором бактериальная инфекция представляет собой осложненную инфекцию кожи и мягких тканей.48. Способ по п.46, в котором бактериальная инфекция представляет собой неосложненную инфекцию кожи и мягких тканей.49. Способ по п.41, в котором начальная доза составляет приблизительно 1500 мг.50. Способ по п.41, в котором начальная доза составляет приблизительно 1000 мг.51. Способ по п.41, в котором начальная доза составляет приблизительно 800 мг.52. Способ по п.41, в котором начальная доза составляет приблизительно 500 мг.53. Способ по п.41, в котором каждая последующая доза составляет от приблизительно 400 мг до приблизительно 1000 мг.54. Способ по п.41, в котором каждая последующая доза составляет приблизительно 500 мг.55. Способ по п.41, в котором каждая последующая доза составляет приблизительно 400 мг.56. Способ по п.41, в котором каждая последующая доза составляет приблизительно 250 мг.57. Способ по п.41, в котором каждая последующая доза составляет приблизительно 200 мг.58. Способ по п.41, в котором начальная доза составляет приблизительно 1000 мг, и каждая последующая доза составляет приблизительно 250 мг.59. Фармацевтическая композиция, включающая:фактор В0 и MAG далбаванцина,
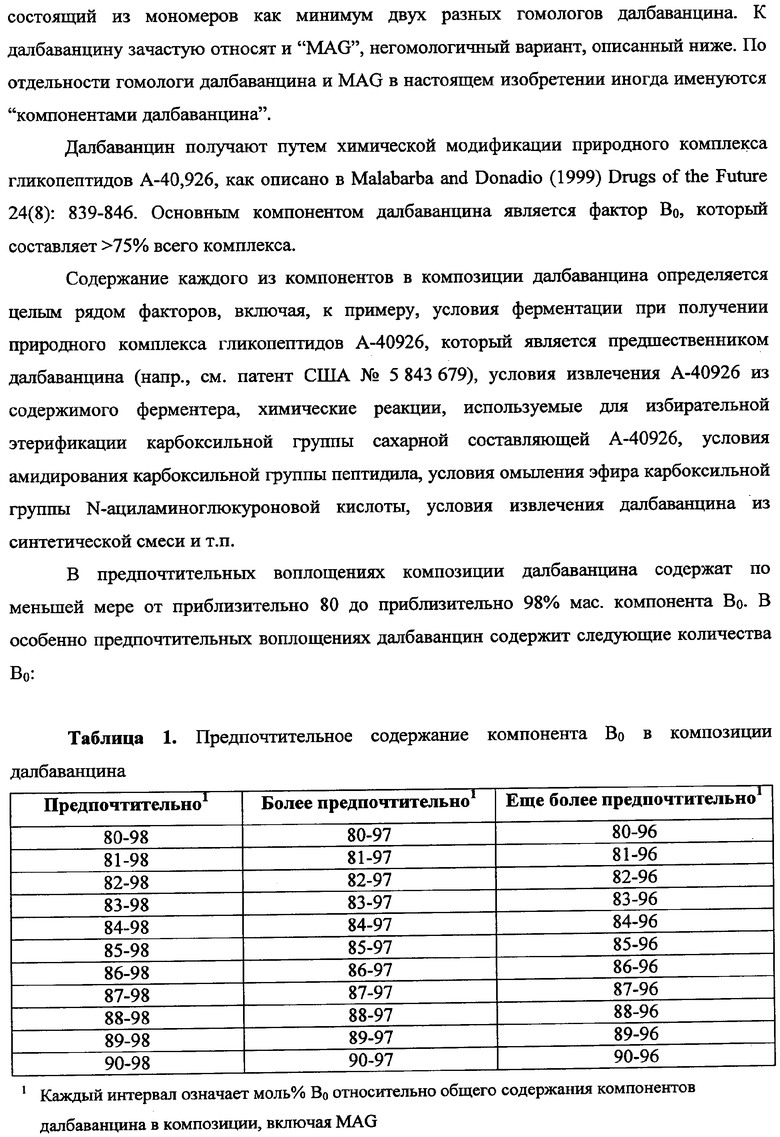
причем содержание фактора В0 составляет не менее приблизительно 75 мол.% от всех наличных компонентов далбаванцина,
причем содержание MAG не превышает 4 мол.% от всех наличных компонентов далбаванцина.
60. Фармацевтическая композиция по п.59, дополнительно включающая стабилизирующее вещество.61. Фармацевтическая композиция по п.60, в которой стабилизирующее вещество представляет собой маннит.62. Фармацевтическая композиция по п.60, в которой стабилизирующее вещество представляет собой смесь маннита и лактозы.63. Фармацевтическая композиция по п.60, в которой содержание фактора В0 составляет по меньшей мере приблизительно 80 мол.% от всех наличных компонентов далбаванцина.64. Фармацевтическая композиция по п.60, в которой содержание MAG не превышает 3,5 мол.% от всех наличных компонентов далбаванцина.65. Фармацевтическая композиция по п.60, в которой содержание MAG не превышает 3 мол.% от всех наличных компонентов далбаванцина.66. Фармацевтическая композиция по п.60, в которой содержание MAG не превышает 2 мол.% от всех наличных компонентов далбаванцина.67. Фармацевтическая композиция по п.60, в которой содержание MAG не превышает 1 мол.% от всех наличных компонентов далбаванцина.68. Фармацевтическая композиция по п.60, в которой содержание MAG не превышает 0,5 моль% от всех наличных компонентов далбаванцина.69. Фармацевтическая композиция по п.60, дополнительно содержащая по меньшей мере один дополнительный фактор далбаванцина, выбранный из группы, состоящей из факторов далбаванцина А0, A1, B1, C0 и С1.70. Фармацевтическая композиция, включающая:далбаванцин и
стабилизатор, причем стабилизатор включает маннит и лактозу, в которой весовое соотношение манит:лактоза:далбаванцин составляет 1:1:4.
71. Фармацевтическая композиция по п.70, которая имеет значение рН приблизительно от 3 до 5.72. Фармацевтическая композиция по п.70, которая имеет значение рН приблизительно 4,5.73. Фармацевтическая композиция, включающая:далбаванцин и
стабилизатор, причем стабилизатор включает маннит при рН приблизительно 3-5.
74. Фармацевтическая композиция по п.73, в которой рН составляет приблизительно 3,5.75. Фармацевтическая композиция по п.73, в которой весовое соотношение маннит: далбаванцин составляет 1:2.76. Способ лечения бактериальной инфекции, включающей грамположительные бактерии, у нуждающегося в этом пациента, включающий стадии:получение терапевтически эффективной дозы стерильного, устойчивого порошка далбаванцина и стабилизатора при рН приблизительно 3-5,
где указанный порошок далбаванцина находится в форме композиции лишенной остаточных частиц, который растворяют в количестве воды, достаточном для растворения, и
введение терапевтически эффективной дозы нуждающемуся в этом пациенту.
77. Способ по п.76, дополнительно включающий введение единственной последующей терапевтически эффективной дозы.78. Способ по п.77, в котором единственная последующая терапевтически эффективная доза вводится приблизительно через 5-10 дней после начальной дозы без какой-либо промежуточной дозы далбаванцина.79. Способ по п.76, дополнительно включающий введение множественных последующих терапевтически эффективных доз.80. Способ по п.79, в котором последующие терапевтически эффективные дозы вводятся с интервалом приблизительно в 5-10 дней без каких-либо промежуточных доз далбаванцина.81. Способ по п.76, в котором стабилизатор включает сахар.82. Способ по п.81, в котором сахар выбран из группы, состоящей из маннита, лактозы, сахарозы, сорбита, глицерина, целлюлозы, трегалозы, мальтозы, декстрозы и их комбинаций.83. Способ по п.81, в котором стабилизатор представляет собой маннит.84. Способ по п.83, в котором весовое соотношение маннит:далбаванцин составляет 1:2.85. Способ по п.81, в котором стабилизатор представляет собой смесь маннита и лактозы.86. Способ по п.85, в котором весовое соотношение маннит:лактоза:далбаванцин составляет 1:1:4.