ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способу лечения бактериальных инфекций. Более конкретно настоящее изобретение относится к способу лечения инфекционных поражений стопы при диабете посредством парентерального, внутривенного и перорального введения известных фармацевтически пригодных оксазолидиноновых противобактериальных средств.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Инфекции стоп и их последствия находятся среди наиболее частых и тяжелых осложнений сахарного диабета (Benjamin A. Lipsky "Osteomyelitis of the Foot in Diabetic Patients" Clinical Infectious Diseases 25: 1318-1326 (1997)). Инфекция стоп представляет собой осложнение диабета, наиболее часто приводящее к госпитализации (Carl Norden et al. Infections in Bones and Joints: Part Three, p.181 (1994)). Это главный участвующий в развитии диабета фактор, представляющий собой основную причину ампутаций нижних конечностей в Соединенных Штатах. Риск ампутации нижних конечностей у пациентов с диабетом выше в 5-15 раз, а половину проводимых каждый год в Соединенных Штатах не связанных с травмами ампутаций проводят у пациентов с диабетом. Остеомиелит костей стоп у пациентов с диабетом в значительной степени представляет собой последствие непрерывного инфицирования из вышележащей мягкой ткани. В большинстве сообщений обнаружено, что приблизительно у трети пациентов с инфекционными поражениями стопы при диабете обнаруживают признаки остеомиелита. Инфекционное поражение стопы при диабете (DFI) представляет собой инфекционное поражение стопы пациентов с диабетом, получивших незначительную травму стопы при наличии периферической нейропатии и/или сосудистого заболевания, вызывающее формирование язвы (Avery's Drug Treatment, 4th ed. (1997), p.742). Инфекционные поражения стопы при диабете могут являться полимикробными, включая в себя и аэробные, и анаэробные грамположительные и грамотрицательные организмы. Аэробные грамположительные бактерии или кокки (GPC) очевидно являются наиболее частыми причинами данных инфекций, включая в себя в качестве неограничивающих примеров Staphylococcus aureus, streptococci группы B или Enterococci (Lipsky et al., "Outpatient management of uncomplicated lower-extremity infections in diabetic patients", Arch. Intern Med. 150: 790-797 (1990)). Часто они представляют собой единственные патогенные микроорганизмы. Важными видами рода staphylococci являются Staphylococcus aureus, Staphylococcus epidermidis и Staphylococcus hemolyticus.
Факультативно аэробные грамотрицательные бациллы также представляют собой большую часть патогенных микроорганизмов при инфекционных поражениях стопы при диабете, а часто - единственные патогенные микроорганизмы. Аэробные грамотрицательные бактерии и анаэробные микроорганизмы, как правило, выделяют как часть смешанных инфекций, особенно у пациентов, недавно получавших антибиотикотерапию. Важно, чтобы применяемый при инфекционных поражениях стопы при диабете антибиотик являлся эффективным против аэробных грамположительных бактерий. Также полезно, чтобы лечение действовало на аэробные грамотрицательные бациллы, энтерококки и анаэробы, хотя инфекции, вызываемые исключительно данными организмами, являются более редкими. Кроме того, когда данным инфекциям сопутствует бактериемия, ее, как правило, вызывают стафилококки или, иногда, виды Bacteroides. В настоящее время для начального практического лечения сложной инфекции рекомендуют множество режимов, но ни одно средство или сочетание не продемонстрировали превосходства. Такие инфекционные поражения очень трудно лечить известными антибиотиками, вследствие их локализации и поскольку часто происходят случаи неудачного лечения, что требует дополнительных курсов лечения. Конкретная проблема представляет собой возрастающее применение противобактериальных средств и последующую устойчивость данных организмов, например устойчивые к метициллину Staphylococcus aureus (MRSA), устойчивые к ванкомицину Enterococci (VRE), Staphylococcus aureus со сниженной чувствительностью к гликопептиду (GISA) и устойчивые к ванкомицину Staphylococcus aureus (VISA) (Tenbouris et al., "Methicillin-resistant Staphylococcus aureus: an increasing problem in a diabetic foot clinic", Diabetic Med. 16: 767-771 (1999)).
Предлагаемые для лечения диабетической стопы лекарственные средства включают в себя флуклоксациллин, цефалексин, метронидазол, амоксициллин и клавулановую кислоту, клиндамицин, ципрофлоксацин, фусидовую кислоту и рифампицин (Avery's Drug Treatment, 4th ed. (1997), p.742). Большинство из данных антибиотиков, предлагаемых для лечения диабетической стопы, необходимо принимать перорально (п/о) или внутривенно (в/в) (Merck Manual p.1103-1120; Avery's Drug Treatment, 4th ed. (1997), p.1461-1469), а противобактериальные средства, как правило, вводят перорально или парентерально вследствие низкой проницаемости антибиотиков. Однако в дополнение к отмеченным выше проблемам из-за вводимых перорально антибиотиков иногда возникают неблагоприятные побочные эффекты, в том числе тошнота. Кроме того, вследствие метаболизма реципиента, которому планируют ввести лекарственное средство, оральные и внутривенные дозы должны являться более высокими, чем терапевтически эффективное количество для получения системных уровней в системе кровообращения млекопитающего, подлежащего лечению. Подобным образом, для того чтобы они являлись эффективными против несистемных инфекций, таких как инфекционные поражения стопы при диабете, перорально или парентерально вводимые антибиотики необходимо транспортировать в очаг инфекции. При инфекционных поражениях стопы при диабете кровообращение является недостаточным, так что нет возможности лечить инфекции системно, и бактериальные инфекции могут приводить к необходимости ампутации стопы. Вследствие этого противобактериальные средства для несистемных инфекций иногда применяют местно на поверхности кожи или непосредственно рядом с открытой раной, хотя инфекционные поражения стопы при диабете не являются "местными инфекциями". "Местные инфекции" известны в данной области как инфекционные поражения поверхностей, такие как простая рана.
В следующих публикациях, полностью включенных сюда в качестве ссылки, раскрыты различные оксазолидиноновые антибиотики и способы получения оксазолидиноновых антибиотиков, которые, как хорошо известно специалистам в данной области, обладают высокой активностью против грамположительных организмов: патенты США №№6313307; 6239152; 6166056; 6069160; 6051716; 6043266; 5968962; 5952324; 5827857; 5792765; 5698574; 5688792; 5684023; 5652238; 5627181; 5565571; 5547950; 5529998; 5523403; 5254577; 5247090; 5231188; 5225565; 5182403; 5164510; 5043443; 4705799 и PCT Application и публикации PCT/US93/04850, WO94/01110; PCT/US94/08904, WO95/07271; PCT/US95/02972, WO95/25106; PCT/US95/10992, WO96/13502; PCT/US96/05202, WO96/35691; PCT/US96/12766; PCT/US96/13726; PCT/US96/14135; PCT/US96/17120; PCT/US96/19149; PCT/US97/01970; PCT/US95/12751, WO96/15130, PCT/US96/00718, WO96/23788, WO98/54161, WO99/29688, WO97/30995, WO97/09328, WO95/07271, WO00/21960, WO01/40236, WO99/64417 и WO01/81350. В данных публикациях раскрыты различные оксазолидиноновые антибиотики, эффективные против ряда патогенных микроорганизмов человека и животных, которые можно вводить перорально, парентерально или местно для лечения системных бактериальных заболеваний у млекопитающих. Линезолид, (S)-N-[[3-[3-фтор-4-(4-морфолинил)фенил]-2-оксо-5-оксазолидинил]метил]ацетамид, (ZYVOX®, Pharmacia-Upjohn) представляет собой пример оксазолидинонового противомикробного средства, активного почти против всех аэробных грамположительных бактерий, включающих в себя streptococci, MRSA и VRE, а также некоторых грамотрицательных бактерий, например Pasteurella multocida, и анаэробных бактерий. Линезолид одобрен для продажи в Соединенных Штатах, поступает в виде препарата для внутривенного введения и обладает высокой биологической доступностью при пероральном приеме (Stevens et al., "Randomized Comparison of Linezolid (PNU-100766) Versus Oxocillindicloxacillin for Treatment of Complicated Skin and Soft tissue Infections", Antimicrob. Agents Chemother. 44: 3408-3414 (2000); Stevens et al., "Linezolid Versus Vancomycin for the Treatment of Methicillin-Resistant Staphylococcus aureus (MRSA) Infections", Clin. Infec. Dis. 34: 1481-1490 (2000) и Zurenko et al., "In Vitro Activities of U-100592 and U-100766, Novel Oxazolidinone Antibacterial Agents", Antimicrob. Agents Chemother. 40: 839-845 (1996)).
Существует необходимость в системных фармацевтических композициях и способах для лечения инфекционных поражений стопы при диабете, которые обеспечили бы присутствие противобактериальных средств в очаге инфекционного поражения стопы при диабете на терапевтически эффективных уровнях. Ввиду важности аэробных грамположительных кокков в инфекционных поражениях стопы при диабете и возрастания случаев устойчивости данных организмов к применяемым в настоящее время антибиотикам, также существует необходимость в фармацевтических композициях и способах для лечения инфекционных поражений стопы при диабете, вызванных устойчивыми штаммами инфекционных агентов.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Один аспект настоящего изобретения относится к способу лечения инфекционных поражений стопы при диабете нуждающихся в таком лечении млекопитающих, который предусматривает парентеральное, внутривенное или пероральное введение фармацевтического препарата, содержащего фармацевтически эффективное количество оксазолидинона, воздействующего на болезнетворные микроорганизмы. Способ может включать в себя введение эффективных против бактерий количеств оксазолидинона в сочетании с другими противобактериальными средствами.
Другой аспект настоящего изобретения относится к применению композиции, содержащей фармацевтически эффективное количество оксазолидинона, для производства лекарственного средства для профилактики и лечения инфекционного поражения стопы при диабете.
Данный и другие аспекты, преимущества и возможности изобретения станут понятны из следующего ниже подробного описания.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг.1 представляет собой диаграмму, отображающую общие степени клинического выздоровления в двух группах пациентов с диабетической стопой, которых лечили пероральным и/или внутривенным введением линезолида, ампициллина/сульбактама или амоксициллина/клавуланата.
Фиг.2 представляет собой диаграмму, отображающую исход заболевания по диагнозу типа первичного инфекционного поражения у пациентов с диабетической стопой, которых лечили пероральным и/или внутривенным введением линезолида, ампициллина/сульбактама или амоксициллина/клавуланата.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к пероральному, парентеральному или внутривенному введению фармацевтически эффективных количеств оксазолидинона, пригодных для лечения инфекционных поражений стопы при диабете. Пероральное, парентеральное или внутривенное действие оксазолидинона, например линезолида, обеспечивает неожиданно эффективное действие при лечении несистемного инфекционного заболевания, такого как инфекционное поражение стопы при диабете.
Следующие ниже определения даны исключительно для пояснения и не предназначены для ограничения области заявки. В Dorland's Illustrated Medical Dictionary (29th edition, 2000, p.1273) "пероральный" определено как "имеющий отношение к ротовой полости, принимаемый через ротовую полость, применяемый в ротовой полости, в качестве перорального лекарственного средства". Следовательно, пероральное введение представляет собой введение в ротовую полость или через ротовую полость. В Dorland's Illustrated Medical Dictionary (29th edition, 2000, p.1324) "парентеральный" определено как "не через пищеварительный тракт, но предпочтительнее посредством инъекции каким-либо другим путем, например подкожным, внутримышечным, интраорбитальным, внутрисуставным, интраспинальным, надчревным или внутривенным". Следовательно, парентеральные введения могут включать в себя инъекции для создания системного действия или инъекции непосредственно в пораженные области, примеры которых представляют собой подкожный, внутривенный, внутримышечный, интрадермальный, интратекальный, внутриглазной, внутрижелудочковый, интраорбитальный, внутрисуставной, интраспинальный, надчревный способы и способ общего вливания.
Кроме того, Dorland's Illustrated Medical Dictionary (29th edition, 2000, p.913) определяет внутривенный как "в вену или вены". Следовательно, внутривенное введение представляет собой введение в вену. Термин «мягкие ткани» описывает внескелетную соединительную ткань, составляющую более чем 50 процентов массы тела и включающую мышцы, сухожилия, жировую ткань, фасции и синовиальные оболочки (Oxford Textbook of Surgery, Morris, Peter J. and Malt, Ronald A., eds, (1994), p.1495). Фасцию определяют как лист или тяж волокнистой ткани, залегающий под кожей или формирующий оболочку для мышц или различных органов организма (Dorland's Illustrated Medical Dictionary 29th edition, 2000, p.652-654). Существует много типов фасций. Целлюлит представляет собой инфекционное поражение некоторого типа фасции. Целлюлит представляет собой диффузное воспаление мягкой или соединительной ткани вследствие инфекции, при котором жидкие водные экссудаты распространяются через места расслоения внутритканевых и тканевых пространств, что может вести к изъязвлению и абсцессу (Dorland's Illustrated Medical Dictionary 29th edition, 2000, p.317). “Подкожный” означает "под кожу" (Dorland's Illustrated Medical Dictionary 29th edition, 2000, p.1718). Синовиальная жидкость представляет собой обладающую сходством с белком яйца прозрачную щелочную густую жидкость, секретируемую синовиальной оболочкой и содержащуюся в полостях суставов, синовиальных сумках и сухожильных влагалищах (Dorland's Illustrated Medical Dictionary 29th edition, 2000, p.1773). Синовиальная сумка представляет собой мешок или подобные мешку полости, заполненные густой жидкостью и расположенные в тех местах тканей, где тем или иным образом может происходить трение (Dorland's Illustrated Medical Dictionary 29th edition, 2000, p.254). Абсцесс представляет собой локализованное скопление гноя в полости, сформированной при разрушении тканей (Dorland's Illustrated Medical Dictionary 29th edition, 2000, p.5-6). Острый абсцесс представляет собой абсцесс, который протекает сравнительно быстро, создавая некоторую лихорадку и болезненное локальное воспаление (Dorland's Illustrated Medical Dictionary 29th edition, 2000, p.6). Абсцесс находится под поверхностью кожи.
Способ лечения инфекционного поражения стопы при диабете у нуждающихся в таком лечении млекопитающих предусматривает парентеральное, внутривенное или пероральное введение количества оксазолидинона, эффективного парентерально, внутривенно или перорально соответственно. Как применяют здесь, термины "количество, эффективное парентерально", "количество, эффективное внутривенно" и "количество, эффективное перорально" относятся к количеству, эффективному для профилактики развития или ослабления существующих симптомов инфекционного поражения стопы при диабете, вызванного бактериями.
Пригодные млекопитающие, находящиеся в объеме настоящего изобретения, включают в себя людей, комнатных животных, таких как собаки и кошки, или коммерчески важный домашний скот, такой как лошади, крупный рогатый скот и свиньи. Предпочтительно, чтобы животное представляло собой человека, собаку или кошку, более предпочтительно - человека.
Оксазолидиноны, пригодные для данного изобретения, как правило, представляют собой средства против грамположительных бактерий. Термины "антибиотик против грамположительных бактерий" или "средство против грамположительных бактерий" относятся к противобактериальному средству, эффективному против грамположительных бактериальных организмов. Термины "антибиотик против грамотрицательных бактерий" или "средство против грамотрицательных бактерий" относятся к противобактериальному средству, эффективному против грамотрицательных бактериальных организмов.
Определенные оксазолидиноновые соединения и способы производства оксазолидиноновых соединений, пригодные для настоящего изобретения описаны в патентах США №№6313307; 6239152; 6166056; 6069160; 6051716; 6043266; 5968962; 5952324; 5827857; 5792765; 5698574; 5688792; 5684023; 5652238; 5627181; 5565571; 5547950; 5529998; 5523403; 5254577; 5247090; 5231188; 5225565; 5182403; 5164510; 5043443; 4705799 и PCT Application и публикациях PCT/US93/04850, WO94/01110; PCT/US94/08904, WO95/07271; PCT/US95/02972, WO95/25106; PCT/US95/10992, WO96/13502; PCT/US96/05202, WO96/35691; PCT/US96/12766; PCT/US96/13726; PCT/US96/14135; PCT/US96/17120; PCT/US96/19149; PCT/US97/01970; PCT/US95/12751, WO96/15130, PCT/US96/00718, WO96/23788, WO98/54161, WO99/29688, WO97/30995, WO97/09328, WO95/07271, WO00/21960, WO01/40236, WO99/64417 и WO01/81350, полные описания которых полностью включены сюда в качестве ссылки. Пригодные соединения обладают формулой I:
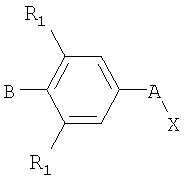
или ее фармацевтически приемлемой солью, где
A представляет собой структуру i, ii, iii или iv
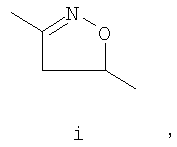
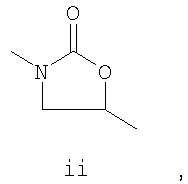
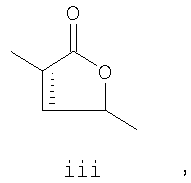
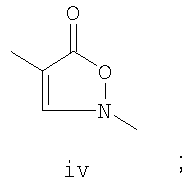
B выбирают из циклоалкила, замещенного циклоалкила, циклоалкенила, замещенного циклоалкенила, арила, замещенного арила, гетероцикла и замещенного гетероцикла, или
B и один из R1 одновременно, с фенильными атомами углерода, с которыми связаны B и один из R1, формируют гетероцикл, где гетероцикл не обязательно представляет собой замещенный гетероцикл;
X представляет собой группу, выбираемую из -CH2-NH-C(O)-R2, -CH2-R2 и -CH2-Y-R2;
Y представляет собой O, S или -NH-;
R1 независимо выбран из H, алкила, алкокси, амино, NO2, CN, галогена, замещенного алкила, замещенного алкокси и замещенного амино; и
R2 независимо выбран из H, -OH, амино, алкила, замещенного алкила, алкокси, замещенного алкокси, алкенила, замещенного алкенила, циклоалкила, замещенного циклоалкила, циклоалкенила, замещенного циклоалкенила, гетероцикла, замещенного гетероцикла, арила и замещенного арила.
Если не описано иначе применяют следующие определения.
Содержание углерода различных содержащих углеводороды групп обозначают посредством префикса, указывающего минимальное и максимальное число углеродных атомов в группе, т.е. префикс Ci-Cj определяет число присутствующих углеродных атомов от целого числа "i" до целого числа "j" включительно. Таким образом, C1-C4-алкил относится к алкильной группе с углеродными атомами от 1 до 4 включительно, например метилу, этилу, пропилу, изопропилу, бутилу и трет-бутилу. C1-C8-алкил представляет собой метил, этил, пропил, бутил, пентил, гексил, гептил, октил и их изомерные формы.
Термин "галоген" относится к галогеновому атому, выбранному из Cl, Br, I и F.
Термин "алкил" относится и к группам с неразветвленной цепью и к группам с разветвленной цепью. Если конкретно не указано иного алкильные группы включают в себя от 1 до 6 углеродных атомов.
Термин "алкенил" относится и к группам с неразветвленной цепью и к группам с разветвленной цепью, содержащим, по меньшей мере, одну -C=C-. Если конкретно не указано иного, алкенильные группы включают в себя от 1 до 6 углеродных атомов.
Термин "алкинил" относится и к группам с неразветвленной цепью и к группам с разветвленной цепью, содержащим, по меньшей мере, одну -C≡C-. Если конкретно не указано иного, алкинильные группы включают в себя от 1 до 6 углеродных атомов.
Термин "алкокси" относится к группам -O-алкил.
Термин "циклоалкил" относится к циклической алкильной группе. Если конкретно не указано иного, циклоалкильные группы, как правило, включают в себя от 3 до 9 углеродных атомов.
Термин "циклоалкенил" относится к циклической алкенильной группе. Если конкретно не указано иного, циклоалкенильные группы, как правило, включают в себя от 3 до 9 углеродных атомов и, по меньшей мере, одну группу -C=C- в циклическом кольце.
Термин "амино" относится к -NH2.
Термин "арил" относится к фенилу, фенилу и нафтилу.
Термин "гетероцикл" относится к моно- или бициклическим системам колец, содержащим, по меньшей мере, один гетероатом, выбранный из O, S и N. Каждое моноциклическое кольцо может являться ароматическим, насыщенным или частично ненасыщенным. Бициклическая система колец может включать в себя содержащее, по меньшей мере, один гетероатом моноциклическое кольцо, конденсированное с циклоалкильной или арильной группой. Бициклическая система колец также может включать в себя содержащее, по меньшей мере, один гетероатом моноциклическое кольцо, конденсированное с другим гетероциклом, моноциклической системой колец.
Примеры "гетероциклов" включают в себя в качестве неограничивающих примеров пиридин, тиофен, фуран, пиразолин, пиримидин, 2-пиридил, 3-пиридил, 4-пиридил, 2-пиримидинил, 4-пиримидинил, 5-пиримидинил, 3-пиридазинил, 4-пиридазинил, 3-пиразинил, 4-оксо-2-имидазолил, 2-имидазолил, 4-имидазолил, 3-изоксазолил, 4-изоксазолил, 5-изоксазолил, 3-пиразолил, 4-пиразолил, 5-пиразолил, 2-оксазолил, 4-оксазолил, 4-оксо-2-оксазолил, 5-оксазолил, 1,2,3-оксатиазол, 1,2,3-оксадиазол, 1,2,4-оксадиазол, 1,2,5-оксадиазол, 1,3,4-оксадиазол, 2-тиазолил, 4-тиазолил, 5-тиазолил, 3-изотиазол, 4-изотиазол, 5-изотиазол, 2-фуранил, 3-фуранил, 2-тиенил, 3-тиенил, 2-пирролил, 3-пирролил, 3-изопирролил, 4-изопирролил, 5-изопирролил, 1,2,3-оксатиазол-1-оксид, 1,2,4-оксадиазол-3-ил, 1,2,4-оксадиазол-5-ил, 5-оксо-1,2,4-оксадиазол-3-ил, 1,2,4-тиадиазол-3-ил, 1,2,4-тиадиазол-5-ил, 3-оксо-1,2,4-тиадиазол-5-ил, 1,3,4-тиадиазол-5-ил, 2-оксо-1,3,4-тиадиазол-5-ил, 1,2,4-триазол-3-ил, 1,2,4-триазол-5-ил, 1,2,3,4-тетразол-5-ил, 5-оксазолил, 3-изотиазолил, 4-изотиазолил, 5-изотиазолил, 1,3,4-оксадиазол, 4-оксо-2-тиазолинил, 5-метил-1,3,4-тиадиазол-2-ил, тиазолдион, 1,2,3,4-тиатриазол, 1,2,4-дитиазолон, фталимид, хинолинил, морфолинил, бензоксазолил, диазинил, триазинил, хинолинил, хиноксалинил, нафтилпиридинил, азетидинил, пирролидинил, гидантоинил, оксатиоланил, диоксоланил, имидазолидинил, пиперазинил, тиопиранил, оксазолидинил, тиофенил, тиоморфолино и азабицикло[2.2.1]гептил.
Термин "замещенный алкил" относится к алкильной группе, включающей в себя 1-4 заместителя, выбранных из галогена, гетероцикла, циклоалкила, циклоалкенила, арила, -OQ10, -SQ10, -S(O)2Q10, -S(O)Q10, -OS(O)2Q10, -C(=NQ10)Q10, -SC(O)Q10,
-NQ10Q10, -C(O)Q10, -C(S)Q10, -C(O)OQ10, -OC(O)Q10, -C(O)NQ10Q10, -C(O)C(Q16)2OC(O)Q10, -CN, =O, =S, -NQ10C(O)Q10, -NQ10C(O)NQ10Q10, -S(O)2NQ10Q10, -NQ10S(O)2Q10, -NQ10S(O)Q10, -NQ10SQ10, -NO2 и -SNQ10Q10. Каждый из гетероцикла, циклоалкила, циклоалкенила и арила являются необязательно замещенными 1-4 заместителями, независимо выбранными из галогена и Q15.
Термин "замещенный арил" относится к арильной группе, несущей 1-3 заместителя, выбранных из -OQ10, -SQ10, -S(O)2Q10, -S(O)Q10, -OS(O)2Q10, -C(=NQ10)Q10, -SC(O)Q10, -NQ10Q10, -C(O)Q10, -C(S)Q10, -C(O)OQ10, -OC(O)Q10, -C(O)NQ10Q10, -C(O)C(Q16)2OC(O)Q10, -CN, =O, =S, -NQ10C(O)Q10, -NQ10C(O)NQ10Q10, -S(O)2NQ10Q10, -NQ10S(O)2Q10, -NQ10S(O)Q10, -NQ10SQ10, -NO2, -SNQ10Q10, алкила, замещенного алкила, гетероцикла, галогена, циклоалкила, циклоалкенила и арила. Гетероцикл, циклоалкил, циклоалкенил и арил являются необязательно замещенными 1-3 заместителями, независимо выбранными из галогена и Q15.
Термин "замещенный гетероцикл" относится к группе гетероцикла, включающей в себя 1-4 заместителя, выбранных из -OQ10, -SQ10, -S(O)2Q10, -S(O)Q10, -OS(O)2Q10, -C(=NQ10)Q10, -SC(O)Q10, -NQ10Q10, -C(O)Q10, -C(S)Q10, -C(O)OQ10, -OC(O)Q10, -C(O)NQ10Q10, -C(O)C(Q16)2OC(O)Q10, -CN, =O, =S, -NQ10C(O)Q10, -NQ10C(O)NQ10Q10, -S(O)2NQ10Q10, -NQ10S(O)2Q10, -NQ10S(O)Q10, -NQ10SQ10, -NO2, -SNQ10Q10, алкила, замещенного алкила, гетероцикла, галогена, циклоалкила, циклоалкенила и арила. Гетероцикл, циклоалкил, циклоалкенил и арил являются необязательно замещенными 1-3 заместителями, независимо выбранными из галогена и Q15.
Термин "замещенный алкенил" относится к алкенильной группе, включающей в себя 1-3 заместителя, выбранных из -OQ10, -SQ10, -S(O)2Q10, -S(O)Q10, -OS(O)2Q10, -C(=NQ10)Q10, -SC(O)Q10, -NQ10Q10, -C(O)Q10, -C(S)Q10, -C(O)OQ10, -OC(O)Q10, -C(O)NQ10Q10, -C(O)C(Q16)2OC(O)Q10, -CN, =O, =S, -NQ10C(O)Q10, -NQ10C(O)NQ10Q10, -S(O)2NQ10Q10, -NQ10S(O)2Q10, -NQ10S(O)Q10, -NQ10SQ10, -NO2, -SNQ10Q10, алкила, замещенного алкила, гетероцикла, галогена, циклоалкила, циклоалкенила и арила. Гетероцикл, циклоалкил, циклоалкенил и арил являются необязательно замещенными 1-3 заместителями, независимо выбранными из галогена и Q15.
Термин "замещенный алкокси" относится к алкоксигруппе, включающей в себя 1-3 заместителя -OQ10, -SQ10, -S(O)2Q10, -S(O)Q10, -OS(O)2Q10, -C(=NQ10)Q10, -SC(O)Q10, -NQ10Q10, -C(O)Q10, -C(S)Q10, -C(O)OQ10, -OC(O)Q10, -C(O)NQ10Q10, - C(O)C(Q16)2OC(O)Q10, -CN, =O, =S, -NQ10C(O)Q10, -NQ10C(O)NQ10Q10, -S(O)2NQ10Q10, -NQ10S(O)2Q10, -NQ10S(O)Q10, -NQ10SQ10, -NO2, -SNQ10Q10, алкил, замещенный алкил, гетероцикл, галоген, циклоалкил, циклоалкенил и арил. Гетероцикл, циклоалкил, циклоалкенил и арил являются необязательно замещенными 1-3 заместителями, независимо выбранными из галогена и Q15.
Термин "замещенный циклоалкенил" относится к циклоалкенильной группе, включающей в себя 1-3 заместителя -OQ10, -SQ10, -S(O)2Q10, -S(O)Q10, -OS(O)2Q10, -C(=NQ10)Q10, -SC(O)Q10, -NQ10Q10, -C(O)Q10, -C(S)Q10, -C(O)OQ10, -OC(O)Q10, -C(O)NQ10Q10, -C(O)C(Q16)2OC(O)Q10, -CN, =O, =S, -NQ10C(O)Q10, -NQ10C(O)NQ10Q10, -S(O)2NQ10Q10, -NQ10S(O)2Q10, -NQ10S(O)Q10, -NQ10SQ10, -NO2, -SNQ10Q10, алкил, замещенный алкил, гетероцикл, галоген, циклоалкил, циклоалкенил и арил. Гетероцикл, циклоалкил, циклоалкенил и арил являются необязательно замещенными 1-3 заместителями, независимо выбранными из галогена и Q15.
Термин "замещенный амино" относится к аминогруппе, в которой один или два водорода аминной группы замещены группой, выбранной из -OQ10, -SQ10, -S(O)2Q10, -S(O)Q10, -OS(O)2Q10, -C(=NQ10)Q10, -SC(O)Q10, -NQ10Q10, -C(O)Q10, -C(S)Q10, -C(O)OQ10, -OC(O)Q10, -C(O)NQ10Q10, - C(O)C(Q16)2OC(O)Q10, -CN, =O, =S, -NQ10C(O)Q10, -NQ10C(O)NQ10Q10, -S(O)2NQ10Q10, -NQ10S(O)2Q10, -NQ10S(O)Q10, -NQ10SQ10, -NO2, -SNQ10Q10, алкила, замещенного алкила, гетероцикла, галогена, циклоалкила, циклоалкенила и арила. Гетероцикл, циклоалкил, циклоалкенил и арил являются необязательно замещенными 1-3 заместителями, независимо выбранными из галогена и Q15.
Каждый Q10 независимо выбран из -H, алкила, циклоалкила, гетероцикла, циклоалкенила и арила. Гетероцикл, циклоалкил, циклоалкенил и арил являются необязательно замещенными 1-3 заместителями, выбранными из галогена и Q13.
Каждый Q11 независимо выбран из -H, галогена, алкила, арила, циклоалкила и гетероцикла. Алкил, арил, циклоалкил и гетероцикл являются необязательно замещенными 1-3 заместителями, независимо выбранными из галогена, -NO2, -CN, =S, =О и Q14.
Каждый Q13 независимо выбран из Q11, -OQ11, -SQ11, -S(O)2Q11, -S(O)Q11,
-OS(O)2Q11, -C(=NQ11)Q11, -SC(O)Q11, -NQ11Q11, -C(O)Q11, -C(S)Q11, -C(O)OQ11, -OC(O)Q11, -C(O)NQ11Q11, -C(O)C(Q16)2OC(O)Q10, -CN, =O, =S, -NQ11C(O)Q11, -NQ11C(O)NQ11Q11, -S(O)2NQ11Q11, -NQ11S(O)2Q11, -NQ11S(O)Q11, -NQ11SQ11, -NO2 и -SNQ11Q11.
Каждый Q14 представляет собой -H или заместитель, выбранный из алкила, циклоалкила, циклоалкенила, фенила или нафтила, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из -F, -Cl, -Br, -I, -OQ16, -SQ16, -S(O)2Q16, -S(O)Q16, -OS(O)2Q16, -NQ16Q16, -C(O)Q16, -C(S)Q16, -C(O)OQ16, -NO2, -C(O)NQ16Q16, -CN, - NQ16C(O)Q16, -NQ16C(O)NQ16Q16, -S(O)2NQ16Q16 и -NQ16S(O)2Q16. Алкил, циклоалкил и циклоалкенил дополнительно являются необязательно замещенными =O или =S.
Каждый Q15 представляет собой алкил, циклоалкил, циклоалкенил, гетероцикл, фенил или нафтил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из -F, -Cl, -Br, -I, -OQ16, -SQ16, -S(O)2Q16, -S(O)Q16, -OS(O)2Q16, -C(=NQ16)Q16, - SC(O)Q16, -NQ16Q16, -C(O)Q16, -C(S)Q16, -C(O)OQ16, -OC(O)Q16, -C(O)NQ16Q16, -C(O)C(Q16)2OC(O)Q16, -CN, -NQ16C(O)Q16, -NQ16C(O)NQ16Q16, -S(O)2NQ16Q16, -NQ16S(O)2Q16, -NQ16S(O)Q16, -NQ16SQ16, -NO2 и -SNQ16Q16. Алкил, циклоалкил и циклоалкенил дополнительно являются необязательно замещенными =O или =S.
Каждый Q16 независимо выбран из -H, алкила и циклоалкила. Алкил и циклоалкил необязательно включают в себя 1-3 атома галогена.
В определенных осуществлениях оксазолидинон может обладать формулами II или III:
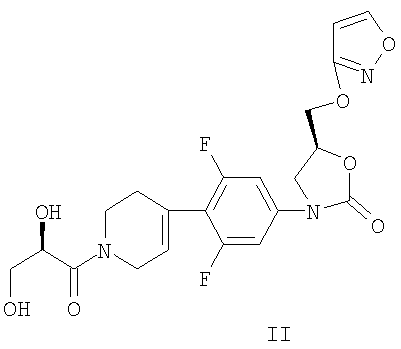
или
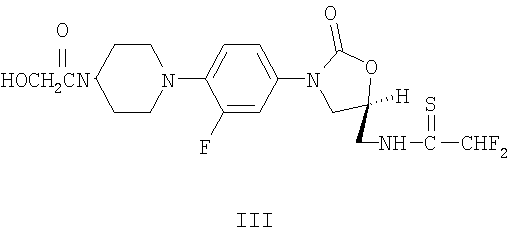
Пригодные для данного изобретения оксазолидиноны, как правило, представляют собой средства против грамположительных бактерий. Определенные соединения оксазолидинона, пригодные для настоящего изобретения, описаны в патенте США №5688792, полное описание которого включено сюда в качестве ссылки. Другие пригодные оксазолидиноновые соединения обладают следующей ниже формулой IV:
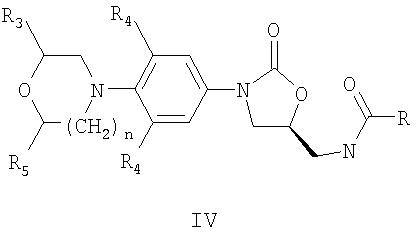
или ее фармацевтически пригодной солью, где
n представляет собой 0, 1 или 2;
R выбран из группы, состоящей из:
водорода;
C1-C8-алкила, необязательно замещенного одним или несколькими заместителями, выбранными из группы, состоящей из F, Cl, гидрокси, C1-C8-алкокси, C1-C8-ацилокси, или -CH2-фенила;
циклоалкила C3-C6;
амино;
C1-C8-алкиламино;
C1-C8-диалкиламино; или
C1-C8-алкокси;
R3 в каждом случае независимо выбран из группы, состоящей из H, CH3, CN, CO2H, CO2R и (CH2)mR6, где m представляет собой 1 или 2;
R4 в каждом случае независимо выбран из группы, состоящей из H, F и Cl;
R5 представляет собой H или CH3;
R6 выбран из группы, состоящей из H, OH, OR, OCOR, NH2, NHCOR и N(R7)2 и
R7 в каждом случае независимо выбран из группы, состоящей из H, p-толуолсульфонила и C1-C4-алкила, необязательно замещенного одним или несколькими заместителями, выбранными из группы, состоящей из Cl, F, OH, C1-C8-алкокси, амино, C1-C8-алкиламино и C1-C8-диалкиламино.
Дополнительно пригодные оксазолидиноновые соединения обладают следующей ниже формулой V:
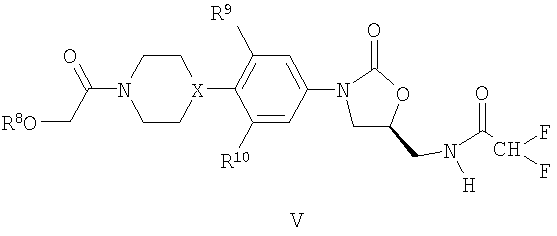
или ее фармацевтически приемлемой солью, где
X представляет собой N или CH;
R9 и R10 независимо представляют собой H или F и
R8 представляет собой H, бензил или -C(=O)C1-4-алкил.
Соединения формулы V можно получить, как изображено на схемах I и II, где X, R8, R9 и R10 представляют собой то, что описано ранее или в формуле изобретения. На схеме I, R11 представляет собой водород, -C(=O)CH2OR8 или подходящие группы защиты аминогруппы, такие как трет-бутоксикарбонил (Boc) и бензилоксикарбонил (Cbz). Исходное вещество, амины (VI), можно получить по способу, описанному в патенте США №6342523. Там, где R11 в амине VI представляет собой -C(=O)CH2OR8 или подходящие группы защиты аминогруппы, им позволяют взаимодействовать со сложным эфиром дифторэтантио-О-кислоты VIII, где R12 представляет собой C1-C4-алкил, необязательно замещенный одной или двумя фенильными группами. Подходящие для данной реакции растворители включают в себя метанол, хлороформ, метиленхлорид или их смеси при температурах приблизительно от 10°C до приблизительно 30°C. Для содействия данному взаимодействию можно применять основание в виде третичного амина, такое как триэтиламин, особенно если применяют соль амина VI. Защитную группу Boc можно удалить кислотным катализатором, таким как трифторуксусная кислота в метиленхлориде или 4N хлористый водород в диоксане, при температурах приблизительно от 0°C до приблизительно 25°C. Удаление группы Cbz можно производить приблизительно в 20% бромистом водороде в уксусной кислоте при температурах приблизительно от 0°C до приблизительно 30°C. Остальные стадии, приводящие от полученных в результате соединений, где R11 представляет собой водород, к соединениям V, показаны на схеме II.
Альтернативный способ получения соединений формулы V приведен на схеме II. Конденсация соединения структуры IX, где R13 представляет собой защитную группу, такую как Boc или Cbz, с дифторуксусной кислотой дает дифторацетамид X. Реагенты и условия для данной конденсации включают в себя применение 1-(3-диметиламинопропил)-3-этилкарбодиимидгидрохлорида (EDC) с 4-(диметиламино)пиридином (DMAP) в пиридине при температуре приблизительно от 0°C до приблизительно 25°C или EDC с 1-гидроксибензтриазолгидратом (HOBT) и триэтиламином в DMF при температуре приблизительно от 0°C до приблизительно 25°C. Защитные группы R13 затем можно удалить для получения соединений XI, которые можно преобразовать в тиоамид XII реагентом Lawesson. Прохождение реакции XI с реагентом Lawesson облегчают посредством применения 1,3-диметил-3,4,5,6-тетрагидро-2(1H)-пиримидона (DMPU) и ее можно проводить в растворителях, таких как THF или диоксан, при температурах приблизительно от 20°C до приблизительно 100°C. Конденсация аминов XII с активированными производными карбоновых кислот затем даст соединения формулы V. Например, для получения соединений V, где R8 представляет собой ацетил, можно применять реакцию XII с ацетоксиацетилхлоридом и триэтиламином в метиленхлориде при температуре приблизительно от 0°C до приблизительно 25°C. Для данной реакции также можно применять конденсирующие средства, такие как EDC с соответствующими кислотами, как описано выше. Соединения, где R8 представляет собой ацетил, водным карбонатом калия в метаноле можно гидролизовать до соответствующих соединений, где R8 представляет собой водород.
Схема I
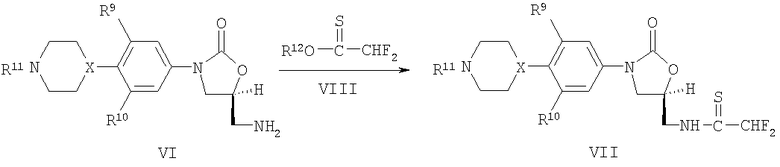
Схема II
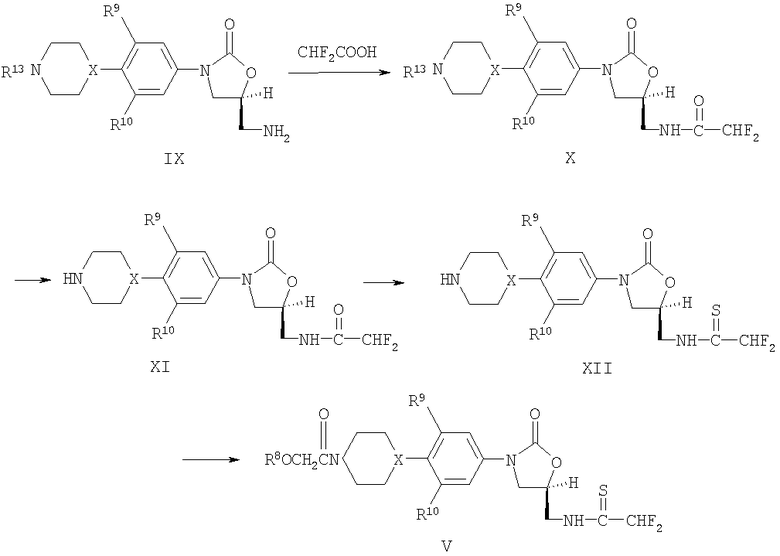
Как применяют здесь, термин "фармацевтически приемлемые соли" относится к органическим и неорганическим кислотно-аддитивным солям исходного соединения. Примеры фармацевтически приемлемых солей представляют собой органические кислотно-основные соли, образуемые с кислотами, формирующими физиологически приемлемый анион, например тозилат, метансульфонат, ацетат, цитрат, малонат, тартрат, сукцинат, бензоат, аскорбат, кетоглутарат и глицерофосфат. Также можно образовать подходящие неорганические соли, включающие в себя гидрохлорид, гидробромид, гидроиодид, сульфат, фосфат, ацетат, пропионат, лактат, мезилат, малеат, малат, сукцинат, тартрат, цитрат, 2-гидроксиэтилсульфат, фумарат, нитрат, бикарбонат, карбонат и т.п.
Фармацевтически приемлемые соли можно получить с применением стандартных способов, хорошо известных в данной области, например, подвергая взаимодействию достаточно основное соединение, такое как амин, с подходящей кислотой, с образованием физиологически приемлемого аниона. Также можно получить соли карбоновых кислот и щелочного металла (например, натрия, калия или лития) или щелочноземельного металла (например, кальция).
Одно пригодное оксазолидиноновое соединение со структурой
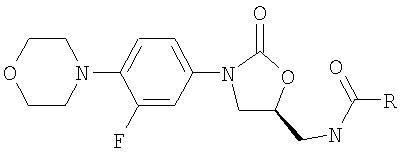
по IUPAC называется (S)-N-[[3-[3-фтор-4-(4-морфолинил)фенил]2-оксо-5-оксазолидинил]метил]ацетамид. Соединение общеизвестно как линезолид и показало особенно эффективное противобактериальное действие.
Соединение линезолид можно получить любым пригодным способом, включающим в себя, например, общие способы, описанные в патенте США №5688792, полное описание которого включено сюда в качестве ссылки. В кратком изложении, гетероарильный заместитель, например оксазиновую или тиазиновую группу, подвергают взаимодействию с функционализированным нитробензолом в присутствии подходящего основания, предпочтительно в органическом растворителе, таком как ацетонитрил, тетрагидрофуран или этилацетат. Нитрогруппу восстанавливают или гидрогенизацией, или применяя подходящее восстанавливающее средство, например водный гидросульфит натрия, для получения анилинового соединения. Анилиновое соединение преобразуют в его бензил- или метилуретановое производное, депротонируют литиевым реагентом с получением соответствующего литиевого промежуточного соединения и обрабатывают (-)-(R)-глицидилбутиратом с получением грубого оксазолидинонового соединения. Пригодный способ получения соединения линезолид более подробно описан в примере 5 патента США 5688792. Линезолид может существовать, по меньшей мере, в двух кристаллических формах, как описано в U.S. Serial No. 09/886641.
Другое пригодное соединение со структурой
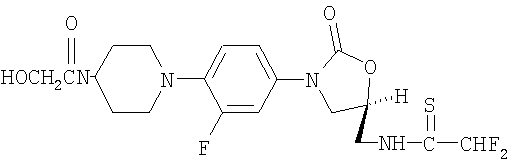
по IUPAC называется 2,2-дифтор-N-({(5S)-3-[3-фтор-4-(4-гликолоилпиперазин-1-ил)фенил]-2-оксо-1,3-оксазолидин-5-ил}метил)этантиоамид.
По изобретению предполагают, что оксазолидиноновое соединение с подобной структурой или физико-химическими свойствами, как любое описанное выше оксазолидиноновое соединение, воздействует на инфекционные поражения стопы при диабете. Для идентификации такого оксазолидинонового соединения тестируемым соединением можно заменить линезолид или любое соединение общей структуры оксазолидинона в способе по изобретению и анализировать на наличие активности по отношению к воздействию на инфекционные поражения стопы при диабете любым пригодным способом.
Способы данного изобретения особенно эффективны против устойчивых штаммов бактериального болезнетворного микроорганизма, включающих в себя, например, устойчивые штаммы Staphylococcus aureus. Более конкретно способы и композиции по данному изобретению могут являться пригодными для лечения заболеваний, вызываемых MRSA, VRE, GISA или VISA. Оксазолидиноны по настоящему изобретению также воздействуют на грамотрицательные инфекции, вызываемые анаэробными микроорганизмами, такими как Bacteroides fragilis. Оксазолидинон можно объединять с другими антибиотиками для лечения инфекционных поражений, вызываемых широким спектром грамотрицательных и/или грамположительных микроорганизмов. Данные инфекционные поражения включают в себя ассоциированные с кожей инфекционные поражения мягких тканей (включающие в себя инфекционные поражения подкожных тканей, абсцессы или миозит), где грамположительные бактерии присутствуют в эпидермисе, дерме, жировом слое и/или мышечных слоях, подлежащих эпидермису. Подобным образом, у пациентов с генерализованным целлюлитом или с более глубоко расположенной инфекцией терапия антибиотиками становится необходимой. На стопах могут находиться язвы, не имеющие отношения к бактериальному инфекционному поражению, возникающему под поверхностью кожи стопы в мягкой ткани.
Специалисту в данной области очевидно, что субъект нуждается в лечении инфекционного поражения стопы при диабете, когда у субъекта присутствуют признаки и симптомы, которые могут включать в себя: гнойные или негнойные отделяемое или выделения, эритему, пульсацию, жар или локализованную гипертермию, боль или болезненность при пальпации, воспаленную, покрасневшую, опухшую, уплотненную или болезненную область на стопе под поврежденной или неповрежденной кожей, и что может являться связанным с лихорадкой. Инфекционные поражения мягких тканей лечат посредством введения необходимого оксазолидинона перорально, парентерально или внутривенно посредством применения соответствующей фармацевтической формы дозирования.
Фармацевтические композиции и препараты по настоящему изобретению могут включать в себя фармацевтически приемлемые носители для содействия введению активных средств. Как применяют здесь, термин "фармацевтически приемлемый" относится к таким характеристикам и/или веществам, которые приемлемы для пациента с фармацевтической/фармакологической точки зрения и для изготавливающего фармацевта с физической/химической точки зрения относительно состава, разработки рецептуры, стабильности, приема пациентом и биологической доступности.
Фармацевтические композиции, содержащие оксазолидиноновые антибиотики по настоящему изобретению, или отдельно, или в сочетании с другими антибиотиками, можно изготавливать хорошо известными в данной области способами, т.е. посредством обычного смешивания, растворения, гранулирования, получения драже, растирания в порошок, эмульгирования, инкапсулирования, захвата, процессов лиофилизации или сушки распылением.
Можно применять любой традиционный фармацевтический препарат. Фармацевтическая композиция для применения по настоящему изобретению, как правило, содержит и эффективную дозу активного вещества и один или несколько физиологически приемлемых носителей, включающих в себя наполнители и вспомогательные вещества, облегчающие переработку активных соединений в препараты, которые можно применять фармацевтически. Надлежащий состав зависит от выбранного пути введения.
Для перорального введения соединения можно составлять посредством объединения активных соединений с фармацевтически приемлемыми носителями, хорошо известными в данной области. Такие носители дают возможность составлять соединения по изобретению в виде таблеток, пилюль, лепешек, порошков, драже, капсул, жидкостей, растворов, эмульсий, гелей, сиропов, взвесей, суспензий, других пригодных средств для доставки активного средства и т.п для перорального приема пациентом. Носитель может представлять собой, по меньшей мере, одно вещество, которое также может служить в качестве разбавителя, вкусовой добавки, солюбилизатора, смазки, суспендирующего средства, связывающего вещества, средства для дезинтеграции таблетки и инкапсулирующего средства. Такие носители или наполнители включают в себя в качестве неограничивающих примеров карбонат магния, стеарат магния, тальк, сахар, лактозу, сахарозу, пектин, декстрин, маннит, сорбит, крахмалы, желатин, целлюлозные вещества, низкоплавкий воск, масло или порошок какао, полимеры, такие как полиэтиленгликоли, коллоидный силикагель, повидон и другие фармацевтически приемлемые вещества.
Предоставлены внутренние части драже с подходящими покрытиями. Для данной цели можно применять концентрированные растворы сахаров, которые необязательно могут содержать гуммиарабик, тальк, поливинилпирролидон, гель карбопол, полиэтиленгликоль и/или диоксид титана, растворы глазури и подходящие органические растворители или смеси растворителей. К покрытиям таблеток или драже можно добавить красители или пигменты для идентификации или для характеристики различных сочетаний доз активных соединений.
Фармацевтические композиции, которые можно применять перорально, включают в себя плотно набитые капсулы, сделанные из желатина, а также мягкие закрытые капсулы, сделанные из желатина и пластификатора, такого как глицерин или сорбит. Плотно набитые капсулы могут содержать активные ингредиенты в смеси с наполнителем, таким как лактоза, связывающим веществом, таким как крахмал, и/или смазочным средством, таким как тальк или стеарат магния, и, необязательно, стабилизаторами. В мягких капсулах активные соединения могут являться растворенными или суспендированными в подходящих жидкостях, таких как жирные масла, жидкий парафин, жидкие полиэтиленгликоли, кремофор, capmul, моно-, ди- или триглицериды со средними или длинными цепями. Также к данным препаратам можно добавлять стабилизаторы.
Композиции жидких форм включают в себя растворы, суспензии и эмульсии. Например, можно предоставить растворы соединений по данному изобретению, растворенные в воде или системах вода-пропиленгликоль и вода-полиэтиленгликоль, необязательно содержащие подходящие традиционные красители, вкусовые добавки, стабилизаторы и загустители.
Также можно составлять соединения для парентерального введения, например, инъекцией, болюсным вливанием или непрерывным вливанием. Препараты для парентерального введения можно предоставлять в стандартной лекарственной форме, например в ампулах или в контейнерах для нескольких доз, с добавлением консерванта. Композиции могут принимать такие формы, как суспензии, растворы или эмульсии в масляных или водных носителях, и могут содержать вещества для составления, такие как суспендирующие, стабилизирующие и/или диспергирующие средства.
Для инъекции соединения по изобретению можно составлять в водном растворе, предпочтительно в физиологически совместимых буферах или физиологическом растворе. Пригодные буферные средства включают в себя трехзамещенный ортофосфат натрия, бикарбонат натрия, цитрат натрия, N-метилглукамин, L(+)-лизин и L(+)-аргинин.
Соединения и композиции также можно вводить внутривенно или внутрибрюшинно вливанием или инъекцией. Растворы активного соединения или их соли можно приготовить в воде, необязательно смешанными с нетоксичным поверхностно-активным средством. Дисперсии можно готовить в глицерине, жидких полиэтиленгликолях, триацетине и их смесях и в маслах. В обычных условиях хранения и применения данные препараты содержат консерванты для предотвращения роста микроорганизмов.
Фармацевтические формы дозирования, пригодные для инъекции или вливания, могут включать в себя стерильные водные растворы или дисперсии, или стерильные порошки, содержащие активный ингредиент, пригодный для приготовляемых для немедленного приема препаратов растворов для инъекций или вливаний или дисперсий, необязательно инкапсулированных в липосомы. Во всех случаях основная форма дозирования должна являться стерильной, жидкой и стабильной при условиях изготовления и хранения. Жидкий носитель может представлять собой растворитель или жидкую дисперсионную среду, содержащую, например, воду, этанол, полиол (например, глицерин, пропиленгликоль, жидкие полиэтиленгликоли и т.п.), растительные масла, нетоксические сложные эфиры глицерина и их пригодные смеси. Надлежащую текучесть можно поддерживать, например, посредством формирования липосом, поддержанием необходимого размера частицы в случае дисперсий или применением поверхностно-активных средств. Предотвращение действия микроорганизмов можно осуществлять при помощи различных противобактериальных или противогрибковых средств, например парааминобензойной кислотой, хлорбутанолом, фенолом, сорбиновой кислотой, тимеросалом и т.п. Во многих случаях предпочтительно включать в композицию средства для создания изотоничности, например сахара, буферы или хлорид натрия. Продолжительного всасывания инъецируемых композиций можно добиться применением в композициях средств с замедленным всасыванием, например моностеарата алюминия и желатина.
Стерильные инъецируемые растворы можно изготовить введением активного соединения в необходимый объем соответствующего растворителя с различными другими ингредиентами, перечисленными выше, по требованию, с последующей стерилизацией фильтрацией. В случае стерильных порошков для приготовления стерильных инъецируемых растворов предпочтительными способами приготовления являются способы вакуумной сушки и лиофилизации, производящие порошок активного ингредиента и любого дополнительного необходимого ингредиента, находящегося в заблаговременно стерилизованных фильтрацией растворах.
Другие парентеральные способы введения также включают в себя водные растворы водорастворимой формы, в качестве неограничивающего примера, такой как соль активного соединения. Дополнительно можно изготовить суспензии активных соединений в липофильном носителе. Пригодные липофильные носители включают в себя жирные масла, такие как кунжутное масло, синтетические сложные эфиры жирных кислот, такие как этилолеат и триглицериды, или такие материалы, как липосомы. Водные суспензии для инъекций могут содержать вещества, увеличивающие вязкость суспензии, такие как карбоксиметилцеллюлозу натрия, сорбит или декстран. Необязательно суспензия также может содержать подходящие стабилизаторы и/или средства, увеличивающие растворимость соединений, принимая во внимание получение высококонцентрированных растворов.
Альтернативно активный ингредиент может находиться в форме порошка для восстановления перед применением пригодным носителем, например стерильной, апирогенной водой.
Дополнительно соединения можно доставлять с применением системы с замедленным высвобождением. Созданы различные вещества для замедленного высвобождения, и они хорошо известны специалистам в данной области. Капсулы с замедленным высвобождением, в зависимости от их химической природы, могут высвобождать соединения в течение периода от 24 часов до нескольких дней. В зависимости от химической природы и биологической стабильности терапевтического средства можно применять дополнительные способы для стабилизации белков.
Водный раствор для парентерального или внутривенного ("в/в") введения можно поместить в пригодный контейнер, такой как пакет, бутылка, флакон, контейнер для парентерального введения большого объема, контейнер для парентерального введения малого объема, шприц, предварительно наполненный шприц или кассета. Как применяют здесь, термин "бутылка" относится к более крупной бутылке, как правило, с достаточным объемом, т.е. объем содержащейся в неиспользованном продукте жидкости составляет, по меньшей мере, 20 мл. Как применяют здесь, термин "флакон" относится к меньшим контейнерам в форме бутылки, как правило, с объемом наполнения менее чем 20 мл, например в единицах по 1 мл, 2 мл, 5 мл и т.п. Предпочтительно, чтобы контейнер представлял собой пакет, бутылку, флакон или предварительно наполненный шприц. Для парентерального введения более предпочтительный контейнер представляет собой контейнер для парентерального введения или шприц. Для в/в введения более предпочтительный контейнер представляет собой пакет или бутылку, а наиболее предпочтительный контейнер представляет собой пакет. Когда его применяют таким образом, предпочтительно, чтобы пакет обладал достаточной способностью для удержания от 25 мл до 2000 мл в/в раствора. Для каждого пакета предпочтительно, чтобы объемы раствора составляли 100 мл, 200 мл или 300 мл. Однако также допустимы большие и/или меньшие объемы.
Вводимый внутривенно раствор вводят пациенту в виде стерильной жидкости. Хотя существует ряд способов стерилизации в/в раствора, предпочтительно, чтобы в/в раствор стерилизовали предельно влажным жаром или стерилизацией паром. Когда применяют термин "стерилизация предельно влажным жаром", он относится к стерилизации паром и включает ее в себя.
Для стерилизации раствора с применением стерилизации предельно влажным жаром раствор помещают в контейнер, пригодный для транспортировки раствора и в качестве резервуара для хранения раствора в течение введения раствора. Соответственно, контейнер выбирают таким образом, чтобы избежать взаимодействия с фармацевтически активным ингредиентом, например оксазолидиноновым соединением, в течение стерилизации, транспортировки или введения.
В частности, содержащий, по меньшей мере, 50% полиолефина контейнер предоставляет значительное преимущество при хранении растворов линезолида. Одна желательная выгода контейнеров с полиолефином состоит в том, что разрушение линезолида в течение и после стерилизации предельно влажным жаром сведено к минимуму. Особенно выгодно, когда основной материал контактной поверхности "контейнер-раствор" представляет собой полиолефин. Остальную часть контейнера можно изготовить из полиолефина и других материалов. Предпочтительно, чтобы контактную поверхность "контейнер-раствор" изготавливали из полиолефина в количестве приблизительно от 50% до приблизительно 100%. Более предпочтительно, чтобы контактная поверхность "контейнер-раствор" содержала приблизительно от 70% до приблизительно 90% полиолефина. Даже более предпочтительно, чтобы контактная поверхность "контейнер-раствор" содержала приблизительно от 75% до приблизительно 85% полиолефина.
Полиолефины включают в себя, например, полиэтилены, полипропилены, полибутены, полиизопрены и полипентены и их сополимеры и смеси. Предпочтительно, чтобы полиолефин представлял собой полиэтилен или полипропилен. Предпочтительный полиолефин представляет собой полипропилен или смесь полипропилена и полиэтилена.
Как правило, противобактериальный оксазолидинон можно вводить от 1 до 4 раз ежесуточно в зависимости от места инфекции, тяжести заболевания и размера и возраста пациента. У пациентов-детей взрослую дозу соответствующим образом уменьшают для ребенка, основываясь на размере ребенка. Оксазолидиноны очень быстро выводятся из организма детей младшего возраста, особенно у тех детей, возраст которых менее или приблизительно равен пяти годам. Таким образом, пациенту в возрасте приблизительно пяти лет или менее может являться необходимым введение соответствующим образом установленной дозы три раза в сутки. Также пациентам, не отвечающим должным образом на однократное суточное дозирование, может являться необходимым введение четыре раза в сутки. В общих чертах, предпочтительно суточное введение, до 24 часов после того, как температура тела вернется к нормальной и/или исчезнет покраснение, опухание и/или воспаление.
Количества активных средств для введения можно легко определить имеющимися в распоряжении у специалиста в области предоставления терапевтического лечения способами. Чтобы ввести читателя в осуществление изобретения, пациенту, как правило, вводят количество оксазолидинона приблизительно от 200 мг до приблизительно 900 мг, как правило, от одного до четырех раз в сутки. Предпочтительно количество оксазолидинона составляет от приблизительно 500 мг до приблизительно 700 мг каждые 12 часов. Курс лечения для взрослого пациента может продолжаться приблизительно от семи суток до приблизительно 60 суток. Следует принимать другие санитарно-гигиенические меры предосторожности, как известно специалистам в данной области.
Ответ пациента на лечение можно проконтролировать стандартными клиническими, радиологическими, микробиологическими и другими лабораторными исследованиями. В частности, можно провести анализы бактерицидности сыворотки для получения ингибитора или бактерицидный титр для помощи в определении конкретной дозы для пациента. Как правило, лечение продолжается приблизительно от 7 суток до приблизительно 28 суток. Для детей младшего возраста, особенно тех, чей возраст составляет пять и менее лет, предпочтительная доза составляет приблизительно 10 мг/кг дважды в сутки.
"Лечение инфекционных поражений стопы при диабете" у нуждающихся в таком лечении млекопитающих означает, что млекопитающее страдает инфекционным поражением стопы при диабете, вызывающим у него проблему, включающую в себя лихорадку, боль, абсцесс или воспаление ткани или раны. Лечение инфекционных поражений означает введение млекопитающему оксазолидинона, так что млекопитающее получает достаточную концентрацию оксазолидинона в пораженной области или для уничтожения присутствующих микроорганизмов, или остановки их роста и/или уменьшения их скорости размножения (увеличение) до того момента, когда природный механизм защиты организма сможет сократить количество нежелательных микроорганизмов или устранить их до уровня, не вызывающего клинических проблем. "Лечение" также включает в себя профилактику инфекции или профилактику перерастания незначительной инфекции в большую инфекцию. Даже несмотря на то, что пациент может не наблюдать таких симптомов, микробные агенты могут все еще присутствовать, но являться менее метаболически активными или в ослабленной стадии. Лечение млекопитающего с инфекционным поражением стопы при диабете для профилактики будущих эпизодов включено в объем "лечения" как применяют в настоящем изобретении.
По способу настоящего изобретения оксазолидиноны можно применять или отдельно или в сочетании с любым другим. Кроме того, их можно применять в сочетании с другими противобактериальными средствами или антибиотическими соединениями, вводимыми посредством перорального, внутривенного, парентерального или местного введения. Термин "другой антибиотик" или "второй антибиотик" относится к противобактериальным средствам, отличным от соединения по настоящему изобретению. Он включает в себя в качестве неограничивающих примеров аминогликозид, цефалоспорин, макролид, пенем, хинолоны, сульфаты, тетрациклин и другие антибиотики, такие как амикацин, гентамицин, спектиномицин, тобрамицин, имипенем, меропенем, цефадроксил, цефазолин, цефалексин, цефаклор, цефотетан, цефокситин, цефпрозил, цефуроксим, лоракарбеф, цефдинир, цефиксим, цефоперазон, цефотаксим, цефподоксим, цефтазидим, цефтибутен, цефтозоксим, цефтриаксон, цефепим, азитромицин, кларитромицин, диритромицин, пенициллин G, клоксациллин, диклоксациллин, нафциллин, оксациллин, амоксициллин, ампициллин, мезлоциллин, пиперациллин, налидиксовая кислота, ципрофлоксацин, эноксацин, ломефлоксацин, норфлоксацин, офлоксацин, левофлоксацин, спарфлоксацин, алатрофлоксацин, гатифлоксацин, моксифлоксацин, триметоприм, сульфизоксазол, сульфаметоксазол, доксициклин, миноциклин, тетрациклин, азтреонам, хлорамфеникол, клиндамицин, квинупристин, фосфомицин, метронидазол, нитрофурантоин, рифампин, триметоприм и ванкомицин. Все из них известны. Их можно получить или коммерчески, или изготовить по ссылке цитированной в PHYSICIANS'DESK REFERENCE, the 53rd Edition (1999) и the U.S.F.D.A.'s Orange book.
Предпочтительно, чтобы данные другие антибиотики вводили для доставки 1-10 мг/кг/сут для взрослого. Кроме того, оксазолидинон для лечения инфекционных поражений стопы при диабете можно применять со средствами, не являющимися антибиотиками. Одним возможным преимуществом данного аспекта изобретения являются относительно меньшие количества активных средств, которые можно применять для получения высокого уровня противобактериальной активности. Изобретение позволяет достигать высоких уровней противобактериального эффекта с применением относительно небольших количеств активного средства по сравнению с отдельными противобактериальными компонентами, применяемые в изобретении. Данное преимущество может являться особенно полезным у пациентов, также страдающих нейтропенией, таких как пациенты, страдающие лейкозом или лимфомой.
Кроме того, совместное применение оксазолидинонового соединения, особенно линезолида, с другими противобактериальными средствами, такими как цефалоспорин, аминогликозид или пенем, обеспечивает новый широкий спектр противобактериальной активности. Способы демонстрируют противобактериальную активность против широкого спектра грамположительных и грамотрицательных инфекционных агентов, включающих в себя грамположительных аэробов и анаэробов. Более того, изобретение позволяет более быстрое и полное устранение трудноизлечимых грамположительных болезнетворных микроорганизмов, особенно в труднодоступных областях организма, где местные условия не благоприятны в отношении устранения микроорганизма одним противобактериальным средством. Данные сочетания можно вводить в соответствии со способом по изобретению. Способ предусматривает лечение инфекционного поражения стопы при диабете посредством введения, отдельно или совместно, активных средств оксазолидинона, цефалоспорина, аминогликозида или пенема. Активные средства можно смешивать для обеспечения смеси с терапевтической активностью, но этого не требуется. Альтернативно активные средства можно вводить отдельно или два из трех активных средств можно объединять и вводить отдельно от третьего активного средства.
Точная дозировка и частота введения зависят от конкретного применяемого оксазолидинона, тяжести состояния, подлежащего лечению, возраста, массы и общего физического состояния конкретного пациента и другого лекарственного лечения, которое может проходить конкретный пациент, как хорошо известно специалистам в данной области, и их можно более точно определить измеряя уровень в крови или концентрацию оксазолидинона в крови пациента и/или ответ пациента на конкретное осуществляемое лечение. Если лечение проводят в сочетании с пероральным, парентеральным или внутривенным введением других лекарственных средств, также можно измерять уровень в крови или концентрацию других лекарственных средств(а) в крови пациента.
Без дальнейшего уточнения, полагают, что специалист в данной области с применением предшествующего описания может осуществить изобретение в его полном объеме. Следующие ниже подробные примеры описывают то, как изготовить различные соединения и/или выполнить различные способы осуществлений изобретения, и их в любом случае следует истолковывать только как иллюстрацию, а не ограничения предшествующего раскрытия. Специалисты в данной области смогут различить соответствующие изменения от способов и в отношении реагентов и в отношении условий и процедур реакций.
ПРИМЕРЫ
ПРИМЕР 1. (S)-N-[[3-[3-фтор-4-(4-морфолинил)фенил]-2-оксо-5-оксазолидинил]метил]ацетамид.
(S)-N-[[3-[3-фтор-4-(4-морфолинил)фенил]-2-оксо-5-оксазолидинил]метил]ацетамид (линезолид) известен. См. патент США 5688792 (пример 5).
ПРИМЕР 2. ЛЕЧЕНИЕ ЧЕЛОВЕКА С ИНФЕКЦИОННЫМ ПОРАЖЕНИЕМ СТОПЫ ПРИ ДИАБЕТЕ ПОСРЕДСТВОМ ПЕРОРАЛЬНОГО И/ИЛИ ВНУТРИВЕННОГО ВВЕДЕНИЯ ОКСАЗОЛИДИНОНА
Мужчин и женщин, по меньшей мере, в возрасте 18 лет, больных сахарным диабетом в истории болезни и инфекционным поражением стопы при диабете, лечили пероральным (п/о) и/или внутривенным (в/в) препаратом линезолида в открытом, контролируемом компаратором исследовании. Всего 371 пациента случайным образом распределяли в соотношении 2:1 между линезолидом (248 пациентов) и аминопенициллинами (123 пациента). Поддающаяся клинической оценке группа составляла 317 пациентов, большинство из которых являлись белыми мужчинами, со средним возрастом 63 года. Пациентов с критической ишемией конечностей исключали, но пациенты с остеомиелитом могли являться включенными в исследование. Госпитализированные пациенты и амбулаторные пациенты получали что-либо из следующего: 1) препарат 600 мг линезолида, вводимый (в/в или п/о) два раза в сутки; 2) препарат 1,53 г ампициллина-сульбактама, вводимый (в/в) четыре раза в сутки; или 3) препарат 500-875 мг ампициллина-клавулоната, вводимый (п/о) от трех до четырех раз в сутки. Лечение продолжали 7-28 суток со средней длительностью лечения, приведенной ниже в таблице 1. Пациентов могли переводить на п/о лечение по усмотрению исследователя.
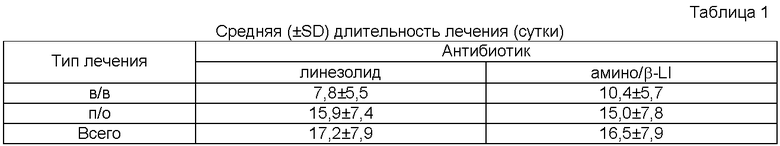
Наиболее общие основные патогенные микроорганизмы представляли собой S. aureus (158 изолятов, 31 из которых представляли собой устойчивые к метициллину S. aureus (MRSA), отрицательные на наличие коагулазы стафилококки (65), enterococci (60) и Streptococcus agalactiae (52)). Для охвата устойчивых к метициллину S. aureus в режиме с аминопенициллином пациентам с выделенными из изучаемой раны MRSA, которых лечили амино/β-LI, в/в добавляли ванкомицин (1 г каждые 12 ч или на общий курс дозирования). Для охвата возможно устойчивых грамотрицательных палочек в каждом режиме допускали в/в азтреонам (1-2 г, в/в, каждые 8-12 ч) в обеих группах лечения для подозреваемых/обнаруженных грамотрицательных патогенных микроорганизмов. Это приведено ниже в таблице 2.

241 пациент получал линезолид, 120 пациентов получали амино/β-LI и 10 пациентов не получали лекарственного средства и не поддавались оценке.
Эффективность и безопасность 7-28 суток лечения линезолидом сравнивали с лечением аминопенициллиновыми средствами, обычно применяемыми при инфекционных поражениях стопы при диабете (DFI), ампициллином/сульбактамом (в/в) и/или амоксициллином/клавуланатом (п/о). Инфекционные поражения определяли по клиническим признакам и симптомам и классифицировали как целлюлиты, инфекционные поражения глубокой мягкой ткани, инфицированную язву, септический артрит, паронихию, абсцесс или остеомиелит. Пациентов в двух группах сравнивали на основании их демографических характеристик, клинических заключений и результатов лабораторных тестов. Наиболее общими типами инфекционных поражений (иногда совместных) являлись: язвы (78%); целлюлит (45%); инфекционные поражения глубокой мягкой ткани (15%); паронихия (6%). Большинство пациентов в обеих группах лечили как амбулаторных пациентов (66%) только с применением перорального лечения (73%) и одним средством (87%). Клинические характеристики инфицированных участков в основном являлись сходными в группах лечения; наиболее общими являлись болезненность (97%), уплотнение (95%), местная гипертермия (92%), негнойный дренаж (82%) и эритема (47%).
Общая оценка двух групп в конце лечения и после него (через 15-21 сутки) приведена в таблицах ниже. По мере необходимости допускали санацию раневой полости и другие хирургические процедуры (исключая полную резекцию/ампутацию) и раны разгружали (избегали механического напряжения пораженной зоны). В двух группах лечения не наблюдали значимых отличий в неблагоприятных явлениях.
Сравнивали степени клинического выздоровления для пациентов, проходивших лечение линезолидом и амино/β-LI в группах "с намерением лечить" (ITT) и поддающейся клинической оценке (CE) (см. фиг.1).
При инфицированных язвах клинически излечили значимо больше пациентов, проходивших лечение линезолидом, чем пациентов, проходивших лечение амино/β-LI (81,4% в сравнении с 67,9%; 95% доверительный интервал (CI): 4,53, 25,7) (см. фиг.2).
У пациентов без остеомиелита, у пациентов, проходивших лечение линезолидом, обнаружили значимо более высокую степень клинического выздоровления, чем у пациентов, получавших амино/β-LI (86% в сравнении с 71%; 95% CI: 4,5, 25,7). У пациентов с остеомиелитом (n=60) сравнивали степени клинического выздоровления (61,0% в сравнении с 69,0% соответственно, см. фиг.2). Значимых различий в клиническом исходе на основании патогенного микроорганизма между группами лечения не наблюдали, за исключением значимо более высокой степени клинического выздоровления, наблюдаемого для линезолида для S. agalactiae (см. таблицу 3).
Клинический исход на основании патогенного микроорганизма (группа MITT)
MITT = модифицированная группа "с намерением лечить" (пациенты "с намерением лечить" на основании идентифицированного патогенного организма); амино/β-LI аминопенициллины/ингибиторы β-лактамазы; n/N=количество пациентов, отвечающих на лечение /количество пациентов, проходящих лечение; CI = доверительный интервал; MSSA = чувствительные к метициллину Staphylococcus aureus; MRSA = устойчивые к метициллину Staphylococcus aureus.
Как суммировано ниже в таблице 4, сравнивали степени микробиологического успеха (поддающиеся микробиологической оценке (ME) пациенты включали в себя пациентов CE, с подтвержденным основным грамположительным патогенным микроорганизмом, чувствительным к исследуемому лекарственному средству) между данными двумя типами лечения: 72,2% у пациентов, проходивших лечение линезолидом в сравнении с 63,0% пациентов, проходивших лечение амино/β-LI (95% CI: -5,5, 23,8). Ни один из выделенных патогенных микроорганизмов не проявлял устойчивости к линезолиду исходно или развил устойчивость в течение испытания. Устойчивость к ампициллину/сульбактаму обнаружили в 1 изоляте S. aureus. Устойчивость к амоксициллину/клавуланату обнаружили в 7 изолятах S. aureus и 4 изолятах S. epidermidis.
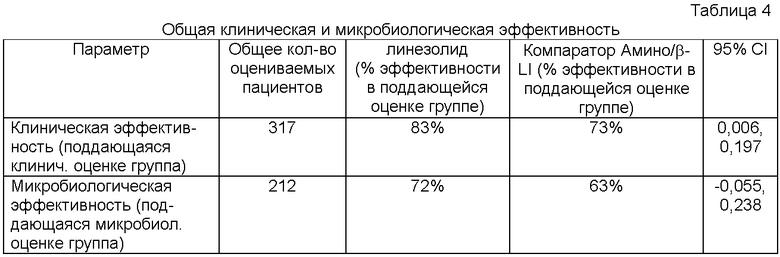
Из данного большого, рандомизированного испытания по лечению DFI, линезолид (как правило, назначаемый отдельно, п/орально, амбулаторным пациентам) в целом являлся, по меньшей мере, таким же эффективным, как амино/β-LI в отношении клинических и микробиологических исходов при лечении DFI и являлся клинически превосходящим при лечении инфицированных язв и случаев с отсутствием остеомиелита. Следовательно, линезолид представляет собой дополнительное в/в или п/о средство против потенциально устойчивых грамположительных организмов и выступает в качестве альтернативы терапии амино/β-LI при лечении DFI.
ПРИМЕР 3. ЧЕЛОВЕКА С ИНФЕКЦИОННЫМ ПОРАЖЕНИЕМ СТОПЫ ПРИ ДИАБЕТЕ ЛЕЧАТ ПАРЕНТЕРАЛЬНЫМ ВВЕДЕНИЕМ ОКСАЗОЛИДИНОНА
Женщину в возрасте 64 лет массой 70 кг с диабетом и инфицированными изъязвлениями стоп, что также известно как диабетическая стопа, в истории болезни, лечат парентеральным препаратом 600 мг (S)-N-[[3-[3-фтор-4-[4-(морфолинил)фенил]-2-оксо-5-оксазолидинил]метил]ацетамида. Препарат вводят два раза в сутки в течение 7-28 суток. Пациента оценивают посредством клинических обследований и рентгеновским излучением на предмет наличия остеомиелита, включая сюда тест "зонд к костной ткани" и биопсию кости, если у пациента открытая рана. После курса лечения оксазолидиноном разрушение ткани в изъязвленной области заметно приостанавливалось и начиналось восстановление ткани, как оценивали по отсутствию "выделения" серозной жидкости и уменьшению опухания.
Таким образом, пероральное, парентеральное или внутривенное введение линезолида предоставляет многообещающую активность при лечении инфекционных поражений стопы при диабете. Способ может являться пригодным для лечения инфекционных поражений стопы при диабете, включающих в себя инфекционные поражения, вызываемые резистентными штаммами с уменьшенной чувствительностью к другим антибиотикам.
Предыдущее подробное описание приведено только для ясности понимания, и не следует подразумевать из него ненужные ограничения, так как для специалистов в данной области могут являться очевидными модификации в пределах области изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| МЕДИЦИНСКИЕ УСТРОЙСТВА, УСТОЙЧИВЫЕ К ИНФИЦИРОВАНИЮ | 2003 |
|
RU2314831C2 |
| СОЕДИНЕНИЯ ИМИДАЗО[1,2-а] ПИРИДИНА, ИХ СИНТЕЗ И СПОСОБЫ ПРИМЕНЕНИЯ | 2010 |
|
RU2608611C2 |
| 5,5-ГЕТЕРОАРОМАТИЧЕСКИЕ ПРОТИВОИНФЕКЦИОННЫЕ СОЕДИНЕНИЯ | 2013 |
|
RU2696278C2 |
| ОКСАЗОЛИДИНОНОВЫЕ ПРОИЗВОДНЫЕ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2006 |
|
RU2417223C2 |
| НОВЫЕ ПРОТИВОМИКРОБНЫЕ СРЕДСТВА | 2009 |
|
RU2522582C2 |
| ЛЕЧЕНИЕ ОЖИРЕНИЯ | 2019 |
|
RU2822679C2 |
| ЛЕЧЕНИЕ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ | 2019 |
|
RU2815647C2 |
| ОКСАЗОЛИДИНОНОВЫЕ СОЕДИНЕНИЯ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ В КАЧЕСТВЕ ПРОТИВОБАКТЕРИАЛЬНЫХ СРЕДСТВ | 2016 |
|
RU2794494C2 |
| ГЕТЕРОЦИКЛИЧЕСКОЕ ПРОИЗВОДНОЕ, ОБЛАДАЮЩЕЕ АКТИВИРУЮЩЕЙ AMPK АКТИВНОСТЬЮ | 2015 |
|
RU2700703C2 |
| ПРИМЕНЕНИЕ АГОНИСТОВ ФОРМИЛПЕПТИДНОГО РЕЦЕПТОРА 2 ДЛЯ ЛЕЧЕНИЯ ДЕРМАТОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2014 |
|
RU2696487C2 |
Настоящая группа изобретений относится к медицине, в частности к эндокринологии, и касается лечения инфекционных поражений стопы при диабете. Для этого вводят оксазолидиноновый антибиотик линезолид в эффективном количестве. Способ обеспечивает лечение инфекции, вызванной устойчивыми к антибиотикам штаммами микроорганизмов. Этот результат обусловлен способностью линезолида проникать в пораженные диабетом ткани и накапливаться в них в эффективных количествах. 3 н. и 27 з.п. ф-лы, 4 табл., 2 ил.
1. Способ лечения инфекционного поражения стопы при диабете у млекопитающего, включающий парентеральное, внутривенное или пероральное введение млекопитающему фармацевтически эффективного количества отдельно (S)-N-[[3-[3-фтор-4-(4-морфолинил)фенил]-2-оксо-5-оксазолидинил] метил]ацетамида.
2. Способ лечения инфекционного поражения стопы при диабете по п.1, где (S)-N-[[3-[3-фтор-4-(4-морфолинил)фенил]-2-оксо-5-оксазолидинил] метил] ацетамид или его фармацевтически приемлемая соль находятся в форме фармацевтического препарата.
3. Способ лечения инфекционного поражения стопы при диабете по п.1, где млекопитающее выбрано из группы, состоящей из человека, домашнего скота и комнатного животного.
4. Способ лечения инфекционного поражения стопы при диабете по п.3, где млекопитающее представляет собой человека.
5. Способ лечения инфекционного поражения стопы при диабете по п.2, где фармацевтический препарат содержит простые или покрытые таблетки, капсулы, лепешки, порошки, растворы, суспензии, эмульсии, сиропы или их сочетания.
6. Способ лечения инфекционного поражения стопы при диабете по п.2, где фармацевтический препарат содержит фармацевтически эффективное количество (S)-N-[[3-[3-фтор-4-(4-морфолинил)фенил]-2-оксо-5-оксазолидинил]метил]ацетамида или его фармацевтически приемлемой соли от приблизительно 200 мг до приблизительно 900 мг.
7. Способ лечения инфекционного поражения стопы при диабете по п.6, где фармацевтический препарат содержит фармацевтически эффективное количество (S)-N-[[3-[3-фтор-4-(4-морфолинил)фенил]-2-оксо-5-оксазолидинил]метил]ацетамида или его фармацевтически приемлемой соли от приблизительно 500 мг до приблизительно 700 мг.
8. Способ лечения инфекционного поражения стопы при диабете по п.7, где фармацевтический препарат содержит фармацевтически эффективное количество (S)-N-[[3-[3-фтор-4-(4-морфолинил)фенил]-2-оксо-5-оксазолидинил] метил] ацетамида или его фармацевтически приемлемой соли приблизительно 600 мг.
9. Способ лечения инфекционного поражения стопы при диабете по п.1, где указанный способ проводят от 1 до 60 суток.
10. Способ лечения инфекционного поражения стопы при диабете по п.1, где фармацевтический препарат вводят от 2 до 4 раз в сутки.
11. Способ лечения инфекционного поражения стопы при диабете по п.1, где инфекционное поражение стопы при диабете проявляется посредством гнойных или негнойных отделяемого или выделений, эритемы, пульсации, жара или локализованной гиперемии, боли или болезненности при пальпации, воспаленной, покрасневшей, опухшей, уплотненной или болезненной области на стопе под поврежденной или неповрежденной кожей и что может являться связанным с лихорадкой.
12. Способ лечения инфекционного поражения стопы при диабете по п.1, где инфекционное поражение вызывают staphylococci, streptococci, enterococci или их сочетания.
13. Способ лечения инфекционного поражения стопы при диабете по п.12, где инфекционное поражение вызывают staphylococci.
14. Способ лечения инфекционного поражения стопы при диабете по п.1, где инфекционное поражение вызывает устойчивый штамм бактерий, выбранных из группы, состоящей из устойчивых к метициллину Staphylococcus aureus (MRSA), устойчивых к ванкомицину Enterococci (VRE), Staphylococcus aureus со сниженной чувствительностью к гликопептиду (GISA) и устойчивых к ванкомицину Staphylococcus aureus (VISA) и их сочетания.
15. Способ лечения инфекционного поражения стопы при диабете у млекопитающего, включающий в себя парентеральное введение млекопитающему фармацевтически эффективного количества (S)-N-[[3-[3-фтор-4-(4-морфолинил)фенил]-2-оксо-5-оксазолидинил]метил]ацетамида или его фармацевтически приемлемой соли.
16. Способ лечения инфекционного поражения стопы при диабете по п.15, где парентеральное введение представляет собой внутривенное введение.
17. Способ лечения инфекционного поражения стопы при диабете по п.15, где (S)-N-[[3-[3-фтор-4-(4-морфолинил)фенил]-2-оксо-5-оксазолидинил]метил]ацетамид или его фармацевтически приемлемая соль находятся в форме фармацевтического препарата.
18. Способ лечения инфекционного поражения стопы при диабете по п.15, где млекопитающее выбрано из группы, состоящей из человека, домашнего скота и комнатного животного.
19. Способ лечения инфекционного поражения стопы при диабете по п.18, где животное представляет собой человека.
20. Способ лечения инфекционного поражения стопы при диабете по п.17, где фармацевтический препарат содержит растворы, суспензии, эмульсии, сиропы или их сочетания.
21. Способ лечения инфекционного поражения стопы при диабете по п.15, где фармацевтический препарат содержит фармацевтически эффективное количество (S)-N-[[3-[3-фтор-4-(4-морфолинил)фенил]-2-оксо-5-оксазолидинил]метил]ацетамида или его фармацевтически приемлемой соли от приблизительно 200 мг до приблизительно 900 мг.
22. Способ лечения инфекционного поражения стопы при диабете по п.21, где фармацевтический препарат содержит фармацевтически эффективное количество (S)-N-[[3-[3-фтор-4-(4-морфолинил)фенил]-2-оксо-5-оксазолидинил]метил]ацетамида или его фармацевтически приемлемой соли от приблизительно 500 мг до приблизительно 700 мг.
23. Способ лечения инфекционного поражения стопы при диабете по п.22, где фармацевтический препарат содержит фармацевтически эффективное количество (S)-N-[[3-[3-фтор-4-(4-морфолинил)фенил]-2-оксо-5-оксазолидинил]метил]ацетамида или его фармацевтически приемлемой соли приблизительно 600 мг.
24. Способ лечения инфекционного поражения стопы при диабете по п.15, где указанный способ проводят от 1 до 60 суток.
25. Способ лечения инфекционного поражения стопы при диабете по п.15, где фармацевтический препарат вводят от 2 до 4 раз в сутки.
26. Способ лечения инфекционного поражения стопы при диабете по п.15, где инфекционное поражение стопы при диабете проявляется посредством гнойных или негнойных отделяемого или выделений, эритемы, пульсации, жара или локализованной гиперемии, боли или болезненности при пальпации, воспаленной, покрасневшей, опухшей, уплотненной или болезненной области на стопе под поврежденной или неповрежденной кожей и что может являться связанным с лихорадкой.
27. Способ лечения инфекционного поражения стопы при диабете по п.15, где инфекционное поражение вызывают staphylococci, streptococci, enterococci или их сочетания.
28. Способ лечения инфекционного поражения стопы при диабете по п.27, где инфекционное поражение вызывают staphylococci.
29. Способ лечения инфекционного поражения стопы при диабете по п.15, где инфекционное поражение вызывает устойчивый штамм бактерий, выбранных из группы, состоящей из устойчивых к метициллину Staphylococcus aureus (MRSA), устойчивых к ванкомицину Enterococci (VRE), Staphylococcus aureus со сниженной чувствительностью к гликопептиду (GISA) и устойчивых к ванкомицину Staphylococcus aureus (VISA) и их сочетания.
30. Способ лечения инфекционного поражения стопы при диабете у человека, предусматривающий парентеральное, внутривенное или пероральное введение человеку фармацевтически эффективного количества отдельно (S)-N-[[3-[3-фтор-4-(4-морфолинил)фенил]-2-оксо-5-оксазолидинил] метил] ацетамида.
| СПОСОБ ПОЛУЧЕНИЯ НАФТАЛИНА | 0 |
|
SU202095A1 |
| ПРОИЗВОДНОЕ ОКСАЗОЛИДИНОНА ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ, СПОСОБ ЛЕЧЕНИЯ МИКРОБНЫХ ИНФЕКЦИЙ У ТЕПЛОКРОВНЫХ ЖИВОТНЫХ | 1993 |
|
RU2105003C1 |
| US 5688792, 18.11.1997 | |||
| RICHARD TL | |||
| Et al | |||
| "The diabetic foot" | |||
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
| WAGNER А et al | |||
| "Highly resistant pathogens, especially methicillin-resistant Staph, aureus, in diabetic patients with foot infections" | |||
| DMW Deutsche Medizinische Wochenschrift, 2001, vol.126, no 48, р.1353-1356. | |||
Авторы
Даты
2009-05-10—Публикация
2003-03-21—Подача