Изобретение относится к электрохимическому восстановлению оксидов металлов.
Настоящее изобретение относится, в частности, к непрерывному и полунепрерывному электрохимическому восстановлению оксидов металлов в виде порошка и/или гранул для получения металла с низкой концентрацией кислорода, - обычно не более 0,2% по массе.
Настоящее изобретение было сделано во время выполнения текущего исследовательского проекта по электрохимическому восстановлению оксидов металлов, проводившегося заявителем. Этот исследовательский проект был направлен на восстановление оксида титана (TiO2).
Во время выполнения данного исследовательского проекта заявитель провел экспериментальную работу по восстановлению оксида титана с использованием электролизеров, которые включают в себя ванну расплавленного электролита на основе CaCl2, выполненный из графита анод и ряд катодов.
Электролит на основе CaCl2 представлял собой коммерчески доступный источник CaCl2, а именно - дигидрат хлорида кальция, который разлагался при нагревании и давал очень небольшое количество СаО.
Заявитель эксплуатировал эти электролизеры при потенциалах выше потенциала разложения СаО и ниже потенциала разложения CaCl2.
Заявитель обнаружил, что при этих потенциалах электролизеры могут электрохимически восстанавливать оксид титана до титана с низкими концентрациями кислорода, т.е. концентрациями менее 0,2 мас.%.
У заявителя нет ясного понимания механизма работы электролизера на данном этапе.
Тем не менее, хотя и не желая быть связанным комментариями, приведенными в следующих параграфах, заявитель предлагает следующие комментарии с целью наметить в общих чертах возможный механизм работы электролизера.
Выполненная заявителем экспериментальная работа выявила доказательства присутствия металлического Са, растворенного в электролите. Заявитель полагает, что металлический Са являлся результатом электроосаждения катионов Са++ в виде металлического Са на катодах.
Как отмечалось выше, экспериментальная работа выполнялась с использованием электролита на основе CaCl2 при потенциале электролизера ниже потенциала разложения CaCl2. Заявитель полагает, что начальное осаждение металлического Са на катоде электролизера происходило из-за присутствия катионов Са++ и анионов О--, образовавшихся из СаО в электролите. Потенциал разложения СаО меньше потенциала разложения CaCl2.
В случае данного механизма работы электролизера функционирование электролизера зависит от разложения СаО, причем катионы Са++ мигрируют к катоду электролизера и осаждаются в виде металлического Са, а анионы О-- мигрируют к анодам и образуют СО и/или СО2 (в ситуации, когда анод является графитовым анодом), высвобождая при этом электроны, которые способствуют электрохимическому осаждению металлического Са на катоде.
Заявитель полагает, что металлический Са, который осаждался на катоде, принимал участие в химическом восстановлении оксида титана, приводя к высвобождению анионов О-- из оксида титана.
Заявитель также полагает, что анионы О--, будучи извлеченными из оксида титана, мигрировали к аноду и реагировали с углеродом анода, при этом образовывался СО и/или СО2 и освобождались электроны, которые способствовали электрохимическому осаждению металлического Са на катоде.
Заявитель эксплуатировал электролизеры на периодической основе с оксидом титана в виде гранул (таблеток) и более крупных твердых блоков на ранней стадии работы и с порошками оксида титана - на более поздней стадии работы.
Заявитель также эксплуатировал электролизеры на периодической основе с другими оксидами металлов.
И хотя исследовательская работа показала, что в таких электролизерах возможно электрохимически восстановить оксид титана (и другие оксиды металлов) до металлов с низкими концентрациями кислорода, заявитель обнаружил, что есть значительные практические трудности при коммерческой эксплуатации таких электролизеров на периодической основе.
Тем не менее, в ходе рассмотрения результатов этой исследовательской работы и возможной коммерциализации данной технологии заявитель обнаружил, что коммерческое производство может быть достигнуто при работе электролизера на непрерывной или полунепрерывной основе с порошками и/или гранулами оксидов металлов, транспортируемыми через электролизер контролируемым образом и выгружаемыми из электролизера в восстановленном виде.
Таким образом, согласно настоящему изобретению предложен способ электрохимического восстановления оксида металла, такого как оксид титана, в твердом состоянии в электролизере, который включает в себя ванну расплавленного электролита, катод и анод, причем этот способ включает в себя этапы: приложения потенциала электролизера между анодом и катодом, который способен электрохимически восстанавливать оксид металла, подаваемый в ванну расплавленного электролита; непрерывной или полунепрерывной подачи оксида металла в виде порошка и/или гранул в ванну расплавленного электролита; транспортировки порошка и/или гранул вдоль некоторого пути внутри ванны расплавленного электролита и восстановления оксида металла по мере движения порошка и/или гранул оксида металла вдоль этого пути; и непрерывного или полунепрерывного удаления восстановленного материала из ванны расплавленного электролита.
Термин «в виде порошка и/или гранул» используется здесь для обозначения частиц с размером частиц 3,5 мм или менее. Верхний предел диапазона размера данных частиц покрывает частицы, которые обычно описывают как гранулы. Остальная часть данного диапазона размера частиц покрывает частицы, которые обычно описывают как порошок.
Предпочтительный размер частиц составляет 2,5 мм или менее.
Термин «полунепрерывный» используется здесь для обозначения того, что данный способ включает в себя: (а) периоды, во время которых порошок и/или гранулы оксида металла подают в электролизер, и периоды, во время которых отсутствует такая подача порошка и/или гранул оксида металла в электролизер; и (b) периоды, во время которых восстановленный материал удаляют из электролизера, и периоды, во время которых отсутствует такое удаление восстановленного материала из электролизера.
Общая цель использования терминов «непрерывно» и «полунепрерывно» заключается в том, чтобы описать работу электролизера, отличную от работы на периодической основе.
В данном контексте термин «периодический» понимают здесь как охватывающий ситуации, в которых оксид металла непрерывно подают в электролизер, и восстановленный материал накапливается в электролизере до конца цикла работы электролизера, например так, как описано в Международной заявке WO 01/62996 на имя Министерства обороны Великобритании.
Предпочтительный способ включает в себя транспортировку порошка и/или гранул вдоль пути внутри ванны расплавленного электролита в непосредственном контакте с катодом на протяжении, по меньшей мере, значительной части, обычно - по меньшей мере 50 процентов, этого пути.
Более предпочтительный способ включает в себя транспортировку порошка и/или гранул вдоль пути внутри ванны расплавленного электролита в непосредственном контакте с катодом на протяжении, по меньшей мере, 90 процентов этого пути.
Несмотря на вышеописанное предпочтение, настоящее изобретение распространяется и на транспортировку порошка и/или гранул вдоль пути внутри ванны расплавленного электролита в условиях, когда нет непосредственного контакта на протяжении значительной части этого пути.
Имеется большое число возможных вариантов пути движения порошка и/или гранул оксида металла внутри ванны расплавленного электролита и средств достижения требуемого движения.
В качестве примера порошки и/или гранулы оксида металла могут подаваться в расплавленную ванну, обычно - сверху по отношению к поверхности ванны на одной стороне ванны, и транспортироваться вверх внутри ванны вдоль наклоненного вверх пути к разгрузочному выходу, обычно - на другой стороне ванны.
Наклонное, направленное вверх движение может быть достигнуто посредством шнека или другого подходящего средства транспортировки. В зависимости от обстоятельств шнек может быть катодом, или же катод может быть отделен от шнека.
В качестве дополнительного примера порошки и/или гранулы оксида металла могут подаваться в расплавленную ванну, обычно - сверху по отношению к поверхности ванны, и транспортироваться вниз через ванну к разгрузочному выходу на нижнем конце ванны.
Движение вниз может быть достигнуто посредством шнека или другого подходящего средства транспортировки. В зависимости от обстоятельств шнек может быть катодом, или же катод может быть отделен от шнека.
В ряде ситуаций могут иметь место проблемы, связанные с уплотнением нижнего конца расплавленной ванны, что может сделать разгрузку через нижний конец заметно менее предпочтительным вариантом, чем другие варианты.
В качестве дополнительного примера порошки и/или гранулы оксида металла могут подаваться в расплавленную ванну, обычно - сверху по отношению поверхности ванны, и транспортироваться по непрерывному, предпочтительно - круговому, пути через ванну к разгрузочному выходу из ванны.
Предпочтительно, порошок и/или гранулы оксида металла подают на катод электролизера и транспортируют на таком катоде в виде горизонтально расположенной пластины для поддерживания оксидов металла, которая поддерживается с возможностью вращения вокруг вертикальной оси.
Предпочтительно, при использовании оксиды металлов в виде порошка и/или гранул непрерывно или полунепрерывно подают на верхнюю поверхность пластины в выбранном месте на пути движения пластины вокруг оси и образуют слой на этой пластине и перемещают вместе с пластиной по пути, и электрохимически восстанавливают по мере движения пластины по пути, и непрерывно или полунепрерывно выгружают из электролизера в другом выбранном месте на этом пути.
Такая конструкция с вращающейся пластиной позволяет минимизировать длину пути электрического тока катода и, таким образом, минимизировать сопротивление катода и, тем самым, максимизировать протекающий через катод ток. Заявитель установил, что работа электролизера при большом токе является важной задачей.
Таким образом, данный способ, предпочтительно включает в себя этапы: приложения потенциала электролизера между анодом и катодом, который способен электрохимически восстанавливать оксид металла, подаваемый в ванну расплавленного электролита; непрерывной или полунепрерывной подачи оксида металла в виде порошка и/или гранул на верхнюю поверхность катодной пластины и образования слоя порошка и/или гранул; движения катодной пластины вокруг вертикальной оси и, тем самым, транспортировки порошка и/или гранул оксида металла вдоль некоторого пути вокруг оси внутри ванны расплавленного электролита, и электрохимического восстановления оксида металла; и непрерывной или полунепрерывной выгрузки восстановленного материала из ванны расплавленного электролита.
В некоторых ситуациях предпочтительно, чтобы способ включал в себя поддержание слоя с глубиной, которая составляет не более чем удвоенный средний диаметр частиц порошка и/или гранул в этом слое.
В других ситуациях предпочтительно, чтобы способ включал в себя поддержание слоя с глубиной, которая более чем в 2 раза превышает средний диаметр частиц порошка и/или гранул в этом слое.
В данных ситуациях способ предпочтительно включает в себя перемешивание слоя, по мере того как катодная пластина движется и транспортирует порошок и/или гранулы вдоль пути.
При перемешивании слоя решаются две основные задачи. Одна задача заключается в том, чтобы обеспечить наличие по существу равномерного контакта между порошком и/или гранулами и расплавленным электролитом и по существу равномерного электрического контакта между порошком и/или гранулами и катодной пластиной. Перемешивание слоя позволяет избежать нежелательной ситуации, при которой: (а) частицы наверху слоя имеют сравнительно большее время для взаимодействия с расплавленным электролитом, чем частицы на дне слоя, и (b) частицы на дне слоя имеют сравнительно больший электрический контакт с катодной пластиной, чем частицы наверху слоя.
Слой может перемешиваться любым подходящим средством.
Подходящее средство включает в себя гребенку («грабли») с зубцами, которые простираются вниз в слой, выборочное нагревание секций ванны и использование выделяемых в ванне газов.
Предпочтительно, зубцы являются электропроводящими и образуют часть пути катодного тока.
Предпочтительно, способ позволяет электрохимически восстанавливать оксид металла до восстановленного материала в виде металла с концентрацией кислорода, которая составляет не более 0,2% по массе.
Более предпочтительно, концентрация кислорода составляет не более 0,1% по массе.
Способ может быть одно- или многостадийным способом с использованием одного или более чем одного электролизера.
В случае многостадийного способа с использованием более чем одного электролизера способ предпочтительно включает в себя постепенное прохождение восстановленных и частично восстановленных оксидов металла из первого электролизера через один или более чем один расположенный ниже по ходу (ниже по потоку) электролизер и непрерывное восстановление оксидов металла в данных электролизерах.
Другой возможный вариант многостадийного способа включает в себя рециркуляцию восстановленных и частично восстановленных оксидов металла через один и тот же электролизер.
Способ предпочтительно включает в себя промывку металла, который удаляется из электролизера, для отделения электролита, который выносится из электролизера с восстановленным материалом.
Способ предпочтительно включает в себя извлечение электролита, который вымывается из восстановленного материала, и рециркуляцию этого электролита в электролизер.
Альтернативно или дополнительно способ включает в себя подачу добавочного электролита в электролизер (т.е. подпитку электролизера свежим электролитом).
Анод и катод могут быть любых подходящих типов.
В качестве примера анод может быть выполнен из графита. В этом случае графит может образовывать, по меньшей мере, часть стенки электролизера или быть выполнен в виде одного или более блоков, простирающихся в электролизер. Альтернативно анод может представлять собой анод из расплавленного металла в непосредственном или опосредованном контакте с электролитом.
Предпочтительно, способ включает в себя поддержание температуры электролизера ниже температур испарения и/или разложения электролита.
Предпочтительно, способ включает в себя приложение потенциала электролизера выше потенциала разложения по меньшей мере одного компонента электролита.
В ситуации, когда оксид металла представляет собой оксид титана, предпочтительно, чтобы электролит был электролитом на основе CaCl2, который в качестве одного из компонентов включает в себя СаО.
В такой ситуации предпочтительно, чтобы способ включал в себя поддержание потенциала электролизера выше потенциала разложения СаО.
Согласно настоящему изобретению также предложен электролизер (электрохимическая ячейка) для электрохимического восстановления оксида металла в твердом состоянии, который включает в себя: (а) ванну расплавленного электролита, (b) катод, (с) анод, (d) средство для приложения потенциала между анодом и катодом, (е) средство для подачи оксида металла в виде порошка и/или гранул в ванну расплавленного электролита, (f) средство для транспортировки оксида металла в виде порошка и/или гранул вдоль некоторого пути внутри ванны расплавленного электролита таким образом, что оксид металла может быть электрохимически восстановлен в этой ванне, и (g) средство для удаления восстановленного материала из ванны расплавленного электролита.
Предпочтительно, катод выполнен в виде горизонтально расположенной пластины для поддерживания оксидов металлов, которая погружена в ванну электролита и поддерживается с возможностью вращения вокруг вертикальной оси.
Предпочтительно, средство для транспортировки оксида металла вдоль пути внутри ванны включает в себя средство для приведения катодной пластины в движение вокруг вертикальной оси.
Предпочтительно, средство для подачи оксида металла в ванну приспособлено для подачи порошка и/или гранул оксида металла на верхнюю поверхность пластины при вращении пластины вокруг вертикальной оси с образованием движущегося слоя порошка и/или гранул на верхней поверхности.
Предпочтительно, катодная пластина является круглой пластиной.
Предпочтительно, катод включает в себя вертикальный вал, соединенный с катодной пластиной, простирающийся вверх от катодной пластины и совпадающий с вертикальной осью.
При такой конструкции средство для приведения катодной пластины в движение вокруг вертикальной оси предпочтительно поддерживает вал с возможностью вращения вокруг вертикальной оси.
Предпочтительно, поддерживающий (несущий) вал изготовлен из электропроводящего материала и образует часть электрической цепи, которая включает в себя катод, анод и средство для приложения потенциала между анодом и катодом.
Предпочтительно, электролизер дополнительно включает в себя мембрану, которая разделяет катод и анод и является проницаемой для анионов кислорода и непроницаемой для растворенного металла в электролите, а необязательно - является непроницаемой для любого одного или более из следующих типов частиц: (i) иных анионов электролита, чем анионы кислорода, (ii) катионов металла анода и (iii) любых других ионов и атомов.
Предпочтительно, когда мембрана выполнена из твердого электролита.
Твердый электролит может представлять собой стабилизированный оксидом иттрия оксид циркония.
Предпочтительно, анод простирается вниз в ванну электролита и расположен на заданном расстоянии над катодной пластиной.
В ситуации, когда анод представляет собой расходуемый анод, например, выполненный из графита, электролизер предпочтительно включает в себя средство для поддерживания и перемещения анода вниз в ванну электролита по мере расходования анода.
Предпочтительно, это средство поддерживания/перемещения выполнено с возможностью сохранения в ходе работы предварительно заданного расстояния между анодом и катодом.
Предпочтительно, анод включает в себя множество анодных блоков, которые простираются радиально от вертикальной оси катодной пластины.
Предпочтительно, расстояние между соседними анодными блоками достаточно для того, чтобы позволить выделяющимся на аноде газам выходить из ванны электролита для минимизации накопления выделившихся газов вокруг анодных блоков.
Предпочтительно, электролизер включает в себя средство для обработки газов, выходящих из электролизера.
Средство для обработки газов может включать в себя средство для удаления любого одного или более из диоксида углерода, HCl, хлора и фосгена из выходящих газов.
Средство для обработки газов может также включать в себя средство для сжигания монооксида углерода в этих газах.
В ситуации, когда оксид металла представляет собой оксид титана, предпочтительно, чтобы электролит был электролитом на основе CaCl2, который в качестве одного из компонентов включает в себя СаО.
Настоящее изобретение описывается далее в виде примеров со ссылками на сопровождающие чертежи, среди которых:
Фиг.1 представляет собой вертикальное сечение электролизера согласно одному варианту осуществления настоящего изобретения;
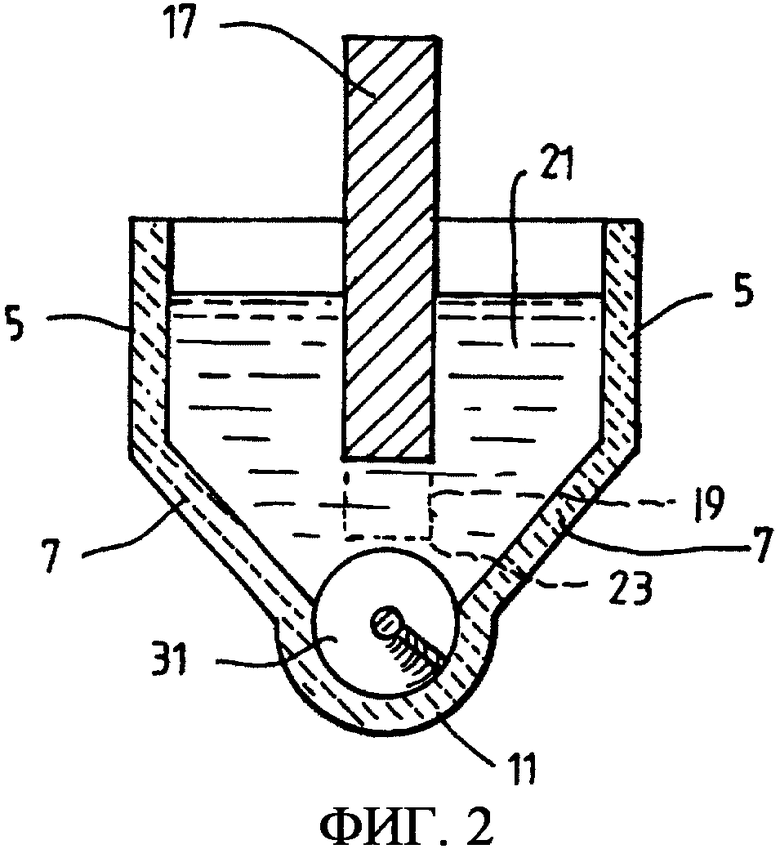
Фиг.2 представляет собой сечение вдоль линии 2-2 на фиг.1;
Фиг.3 представляет собой вертикальное сечение электролизера согласно другому варианту осуществления настоящего изобретения;
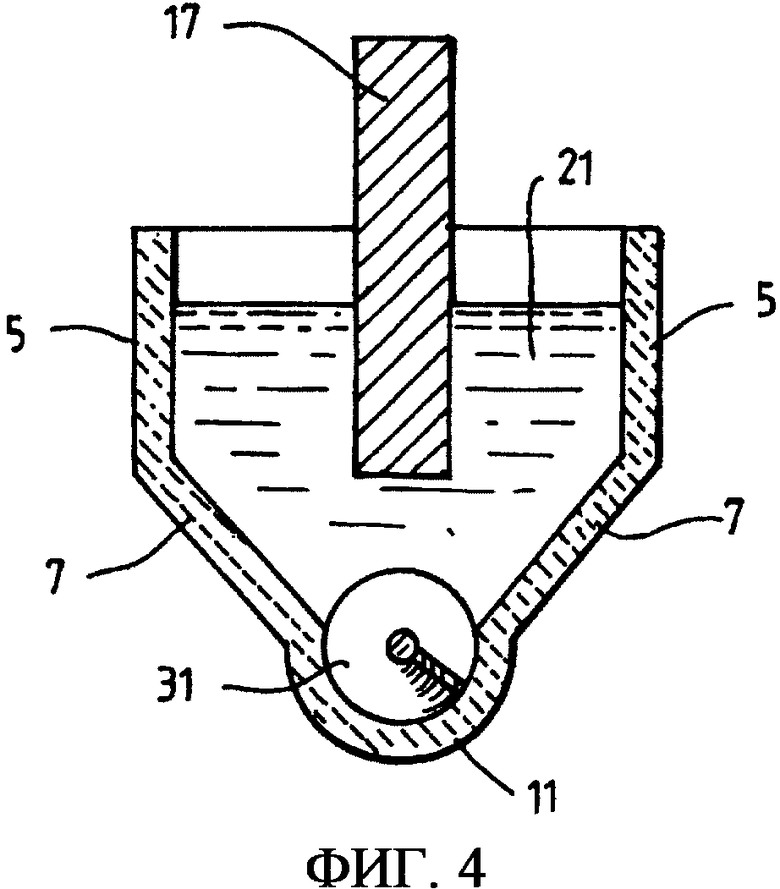
Фиг.4 представляет собой сечение вдоль линии 4-4 на фиг.3;
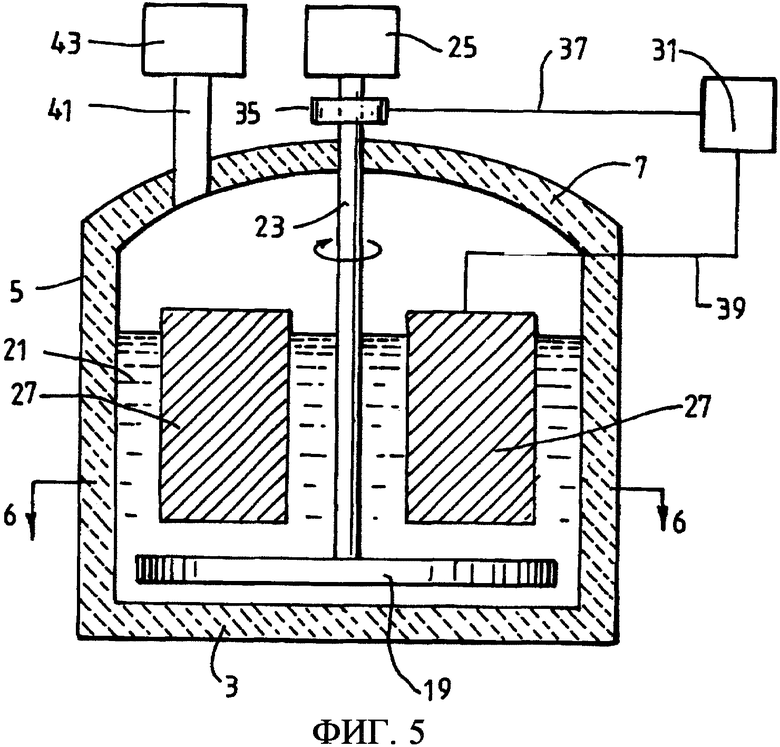
Фиг.5 представляет собой вертикальное сечение электролизера согласно еще одному варианту осуществления настоящего изобретения;
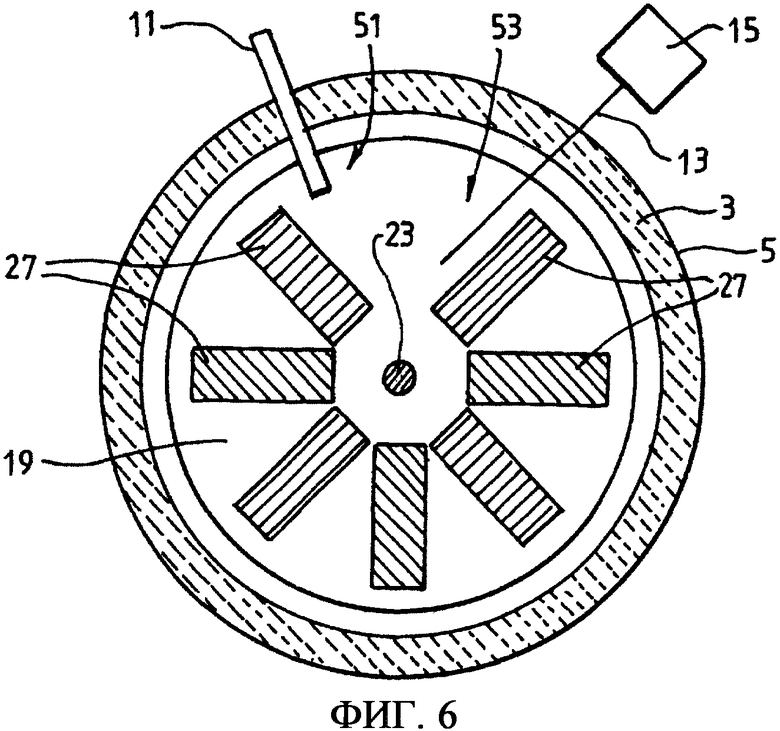
Фиг.6 представляет собой сечение вдоль линии 6-6 на фиг.3.
Последующее описание варианта выполнения электролизера, показанного на фиг.1 и 2, дано в контексте электрохимического восстановления порошка и/или гранул оксида титана с размером менее 3,5 мм до металлического титана с концентрацией кислорода, которая составляет не более 0,2% по массе.
Электролизер, показанный на фиг.1 и 2, является обычно удлиненным (вытянутым). Этот электролизер включает в себя верхние вертикальные секции 5 боковых стенок и нижние, сходящиеся вниз и внутрь, секции 7 боковых стенок. Электролизер также включает в себя полукруглую секцию 11 основания. Секция 11 основания наклонена вверх от конца 13 подачи порошка оксида металла к концу 15 выгрузки металла. Секция 11 основания выполнена имеющей такую форму, чтобы принимать шнек 31, который предназначен для транспортировки порошка металла во время работы вдоль наклоненного вверх пути от конца 13 подачи до конца 15 выгрузки.
Электролизер дополнительно включает в себя ванну 21 расплавленного электролита.
Электролизер дополнительно включает в себя анод 17, расположенный на конце 13 подачи электролизера.
Электролизер дополнительно включает в себя катод в виде вытянутого, простирающегося в электролизер блока 19 и шнек 31. Блок 19 проходит по длине электролизера и имеет наклоненную вверх нижнюю стенку 23, которая находится на постоянном расстоянии над шнеком 31 и электрически соединена любыми средствами (не показаны) со шнеком 31.
Электролизер дополнительно включает в себя источник 27 питания для приложения потенциала между анодом и катодом.
Электролит может быть любым подходящим электролитом. Подходящие электролиты включают в себя коммерчески доступный CaCl2, а именно - дигидрат хлорида кальция, и коммерчески доступный безводный CaCl2, которые дают очень малые количества СаО в ванне.
Анод 17 и катодный блок 19 могут быть выполнены из любого подходящего материала.
При использовании электролизер помещают в подходящую печь для поддержания электролита в расплавленном состоянии.
Атмосфера вокруг электролизера, предпочтительно, представляет собой инертный газ, такой как аргон, который не реагирует с расплавленным электролитом.
После того как электролизер достигнет своей рабочей температуры, на электролизер подают предварительно выбранное напряжение, затем в электролизер на непрерывной или полунепрерывной основе подают порошок и/или гранулы оксида металла и приводят в действие шнек 31. В ситуациях, когда электролитом является коммерчески доступный CaCl2, предпочтительно, чтобы электролизер работал при потенциале, который выше потенциала разложения СаО и ниже потенциала разложения CaCl2. Порошок и/или гранулы оксида металла движутся вниз к основанию электролизера и транспортируются вдоль восходящего наклонного основания шнеком 31 и восстанавливаются до металла, как описано выше, по мере того как порошок и/или гранулы движутся вдоль наклонного пути. Металлический порошок и/или гранулы и электролит, который удерживается захваченным в порах металлического порошка и/или гранул, удаляют из электролизера непрерывно или полунепрерывно на конце 15 выгрузки. Выгруженный материал охлаждают до температуры, которая ниже, чем температура затвердевания электролита, вследствие чего электролит блокирует прямое воздействие атмосферы на металл и тем самым ограничивает окисление этого металла. Выгруженный материал далее промывают, чтобы отделить захваченный электролит от металлического порошка. Металлический порошок после этого обрабатывают, как требуется для получения конечных продуктов.
Описанный выше электролизер способен восстанавливать порошок и/или гранулы оксида металла до низких концентраций кислорода, обычно - не более 0,2 мас.%, за относительно короткие периоды времени, по сравнению с временами обработки, требуемыми для больших гранул или больших блоков из оксидов металла.
Последующее описание варианта выполнения электролизера, показанного на фиг.3 и 4, дано в контексте электрохимического восстановления порошка и/или гранул оксида титана с размером менее 3,5 мм до металлического титана, имеющего концентрацию кислорода, которая составляет не более 0,2% по массе.
Электролизер, показанный на фиг. 3 и 4, очень похож по конструкции на электролизер, показанный на фиг.1 и 2, и основные принципы работы электролизера аналогичны описанному выше в отношении электролизера, показанного на фиг.1 и 2.
Главные различия между этими электролизерами состоят в том, что: (а) электролизер, показанный на фиг.3 и 4, не имеет катодного блока 19 того электролизера, который показан на фиг.1 и 2, - катод содержит только шнек 31 - и (b) электролизер, показанный на фиг.3 и 4, включает в себя множество анодов 17, расположенных через некоторые интервалы вдоль длины электролизера, а не единственный анод 17, расположенный только на конце подачи, как в показанном на фиг.1 и 2 электролизере.
Последующее описание варианта выполнения электролизера, показанного на фиг.5 и 6, дано в контексте электрохимического восстановления гранул оксида титана с размером 1-3 мм до металлического титана, имеющего концентрацию кислорода, которая составляет не более 0,2% по массе.
Электролизер, показанный на фиг.5 и 6, имеет стенку 3 основания, круглую боковую стенку 5 и изогнутую верхнюю стенку 7. Стенки 3, 5, 7 выполнены из подходящих изолирующих материалов с тем, чтобы минимизировать потери тепла из электролизера.
Электролизер дополнительно включает в себя ванну 21 расплавленного электролита в виде коммерчески доступного CaCl2, который разлагается при нагревании и образует очень малое количество СаО в этой ванне.
Электролизер дополнительно включает в себя катод в виде круглой пластины 19, которая расположена горизонтально и погружена в ванну 21 электролита, и вертикальный вал 23, соединенный с центром катодной пластины и проходящий вверх от центра катодной пластины.
Электролизер дополнительно включает в себя средство 25 для поддерживания узла из катодной пластины 19 и вала 23 в электролизере, как показано на этих чертежах, и для вращения этого узла вокруг вертикальной оси вала 23 и пластины 19.
Катодная пластина 19 образует горизонтальную несущую поверхность для гранул оксида титана. Электролизер включает в себя вибрационный питатель 11 или другое подходящее загрузочное устройство для непрерывной или полунепрерывной подачи гранул на пластину в одном месте (положении) 51 и узел из скребка 13 и приемника 15 для непрерывной или полунепрерывной выгрузки гранул с пластины в другом месте (положении) 53. Рабочие условия электролизера выбирают и регулируют так, чтобы гранулы оксида титана на катодной пластине 19 электрохимически восстанавливались до титана по мере того, как пластина вращается между положениями 51, 53 подачи и разгрузки.
Электролизер дополнительно включает в себя анод в виде набора радиально вытянутых графитовых блоков 27, которые простираются вниз в электролизер в ванну 21 электролита и располагаются на заранее заданном расстоянии над верхней поверхностью катодной пластины 19. Это расстояние выбирают как можно более малым с учетом физических ограничений в электролизере и рабочих ограничений в способе. Анодные блоки 27 изображены на чертежах в виде прямоугольных блоков. Вместе с тем анодные блоки 27 не ограничены по форме и могут быть выполнены имеющими любую подходящую форму.
При использовании электролизера анодные блоки 27 постепенно расходуются за счет реакции между углеродом в анодных блоках 27 и анионами О--, образовавшимися на катодной пластине 19, причем эта реакция протекает, преимущественно, на нижних кромках анодных блоков 27. Предпочтительно, чтобы расстояние между верхней поверхностью катодной пластины 19 и нижними кромками анодных блоков 27 поддерживалось по существу постоянным для того, чтобы минимизировать изменения, которые могут быть необходимы для других рабочих параметров способа. Поэтому электролизер дополнительно включает в себя средство (не показано) для постепенного опускания анодных блоков в ванну 21 электролита с тем, чтобы поддерживать расстояние между верхней поверхностью катодной пластины 19 и нижними кромками анодных блоков 27 по существу постоянным.
Электролизер дополнительно включает в себя источник 31 электропитания для приложения потенциала между анодными блоками 27 и катодной пластиной 19 и электрическую цепь, которая электрически взаимно соединяет источник 31 электропитания, анодные блоки 27 и катодную пластину 19.
Предпочтительно, электролизер работает при потенциале, который выше потенциала разложения CaO и ниже потенциала разложения CaCl2. В зависимости от обстоятельств этот потенциал может достигать 4-5 В. В соответствии с описанным выше механизмом работа выше потенциала разложения СаО способствует осаждению металлического Са на катодной пластине 19 благодаря присутствию катионов Са++ и миграции анионов О-- к анодным блокам вследствие приложенного поля и взаимодействию анионов О-- с углеродом анодных блоков с образованием монооксида углерода и диоксида углерода и высвобождением электронов. В дополнение к этому в соответствии с вышеописанным механизмом осаждение металлического Са приводит к химическому восстановлению оксида титана по описанному выше механизму и генерирует анионы О--, которые мигрируют к анодным блокам вследствие приложенного поля и дополнительно высвобождают электроны. Работа электролизера ниже потенциала разложения CaCl2 минимизирует выделение газообразного хлора и на основании этого является преимуществом.
Вертикальный вал 23, который соединен с катодной пластиной 19, предназначен быть частью электрической цепи. Вертикальный вал 23 изготовлен из электропроводящего материала и электрически соединен с источником 31 электропитания через узел 35 из медной муфты и, контактных щеток и электрической шины 37.
Каждый анодный блок 27 соединен с источником 31 электропитания через серию электрических шин 39 (только одна из которых показана на фиг.1).
Как указано выше, работающий электролизер генерирует диоксид углерода и, потенциально, газообразный хлор на аноде, и при этом является очень важным удалять данные газы из электролизера. Пространства между анодными блоками 27 облегчают выход выделившихся газов из ванны электролита. Электролизер дополнительно включает в себя канал 41 сброса газа в крыше 7 электролизера и блок 43 обработки газов, который обрабатывает отходящие газы перед выбросом обработанных газов в атмосферу. Обработка газов включает в себя очистку газа в скруббере для удаления диоксида углерода и любых хлорсодержащих газов, и при этом она может также включать в себя сжигание монооксида углерода, с тем чтобы получить тепло для данного способа.
Гранулы титана и электролит, который остался в порах этих гранул титана, непрерывно или полунепрерывно удаляют из электролизера в месте 53 выгрузки. Выгруженный материал охлаждают до температуры, которая ниже температуры затвердевания электролита, вследствие чего электролит блокирует прямое воздействие атмосферы на металл и тем самым ограничивает окисление этого металла. Выгруженный материал далее промывают с тем, чтобы отделить захваченный электролит от металлического порошка. Металлический порошок после этого обрабатывают, как требуется для получения конечных продуктов.
Вышеописанные электролизеры и способы являются эффективными, и такая эффективность означает непрерывное или полунепрерывное электрохимическое восстановление оксидов металла в виде порошка и/или гранул с получением металла, имеющего низкую концентрацию кислорода.
В описанные выше варианты осуществления настоящего изобретения может быть внесено множество модификаций, не выходящих за рамки сущности и объема настоящего изобретения.
Конкретно, показанные на чертежах электролизеры являются только тремя примерами из большого количества возможных конфигураций электролизеров, которые находятся в рамках объема настоящего изобретения.
Кроме того, хотя электролизер согласно варианту выполнения, показанному на фиг.5 и 6, включает в себя анод в виде множества анодных блоков 27, настоящее изобретение не ограничено этим и распространяется на другие конструкции. Одна такая конструкция имеет анод в виде единичного анодного блока, который по существу покрывает катодную пластину 19 и является пористым, что облегчает удаление выделившихся газов из электролизера.
Кроме того, хотя является предпочтительным, чтобы описанные выше электролизеры работали при потенциалах вплоть до потенциала разложения CaCl2, настоящее изобретение распространяется на работу при более высоких потенциалах.
Кроме того, хотя варианты осуществления описаны в контексте электрохимического восстановления оксида титана, настоящее изобретение таким образом не ограничено и распространяется на электрохимическое восстановление других подходящих оксидов металлов.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭЛЕКТРОХИМИЧЕСКОЕ ВОССТАНОВЛЕНИЕ ОКСИДОВ МЕТАЛЛОВ | 2004 |
|
RU2347015C2 |
| МИНИМИЗАЦИЯ ПЕРЕНОСА УГЛЕРОДА В ЭЛЕКТРОЛИЗЕРЕ | 2003 |
|
RU2302482C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКОВ ТУГОПЛАВКИХ МЕТАЛЛОВ | 2009 |
|
RU2397279C1 |
| ПОЛУЧЕНИЕ ТИТАНА | 2005 |
|
RU2370575C2 |
| СПОСОБ ПРОИЗВОДСТВА ХИМИЧЕСКИ АКТИВНЫХ МЕТАЛЛОВ И ВОССТАНОВЛЕНИЯ ШЛАКОВ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2008 |
|
RU2401875C2 |
| Способ получения сплава титан-железо и устройство для его осуществления | 2019 |
|
RU2734610C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА ТУГОПЛАВКОГО МЕТАЛЛА | 2009 |
|
RU2401888C1 |
| ВОССТАНОВЛЕНИЕ ОКСИДОВ МЕТАЛЛОВ В ЭЛЕКТРОЛИЗЕРЕ | 2002 |
|
RU2298050C2 |
| ЭЛЕКТРОЛИЗЕР ДЛЯ ЭЛЕКТРОХИМИЧЕСКОГО ПОЛУЧЕНИЯ АЛЮМИНИЯ, РАБОТАЮЩИЙ С АНОДАМИ НА ОСНОВЕ МЕТАЛЛА | 2002 |
|
RU2283372C2 |
| СПОСОБ ВОЛКОВА ДЛЯ ПРОИЗВОДСТВА ХИМИЧЕСКИ АКТИВНЫХ МЕТАЛЛОВ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2008 |
|
RU2401874C2 |

Группа изобретений относится к способу и устройству электрохимического восстановления оксидов металлов. Способ электрохимического восстановления оксида металла, такого как оксид титана, в твердом состоянии осуществляют в электролизере, содержащем ванну расплавленного электролита, катод и анод. Способ включает следующие этапы: а) приложение потенциала электролизера между анодом и катодом, способного электрохимически восстанавливать оксид металла, подаваемый в ванну расплавленного электролита; b) непрерывную или полунепрерывную подачу оксида металла в виде порошка и/или гранул в ванну расплавленного электролита; с) транспортировку порошка и/или гранул вдоль некоторого пути внутри ванны расплавленного электролита и восстановление оксида металла по мере движения порошка и/или гранул вдоль этого пути; и d) непрерывное и/или полунепрерывное удаление металла из ванны расплавленного электролита. Техническим результатом является повышение эффективности непрерывного или полунепрерывного электрохимического восстановления оксидов металлов в виде порошка и/или гранул с получением металла, имеющего низкую концентрацию кислорода. 2 н. и 30 з.п. ф-лы, 6 ил.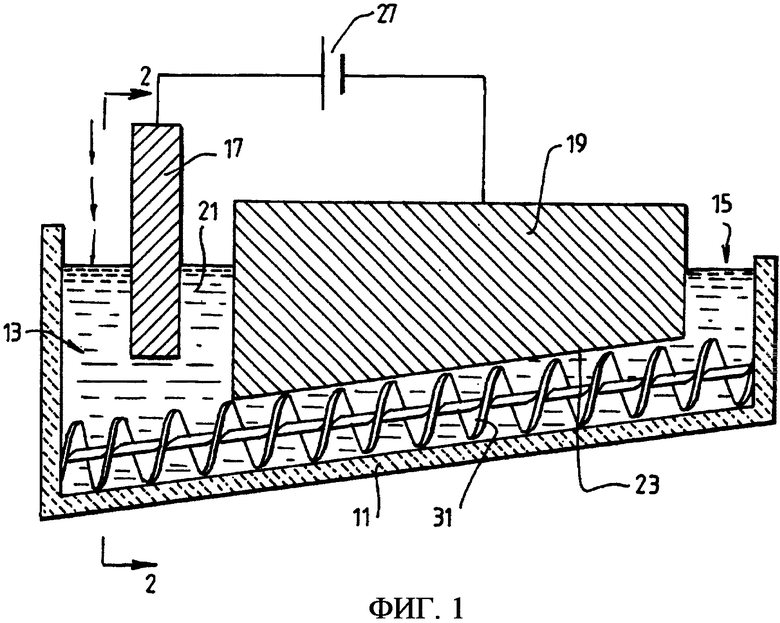
Приоритет по пунктам:
| WO 9964638 A1, 16.12.1999 | |||
| Способ получения металлов | 1981 |
|
SU1416060A3 |
| СПОСОБ ПОЛУЧЕНИЯ ТУГОПЛАВКИХ МЕТАЛЛОВ ИЗ РУДНЫХ КОНЦЕНТРАТОВ | 1994 |
|
RU2103391C1 |
| US 4487677 A, 11.12.1984 | |||
| JP 57116791 A, 20.07.1982 | |||
| WO 9849357 A1, 05.11.1998 | |||
| JP 62086188 A, 20.04.1987. | |||
Авторы
Даты
2008-09-20—Публикация
2003-12-12—Подача