Изобретение относится к области медицины, в частности исследованию крови, и может быть использовано для выявления дисплазминогенемии (ДП).
Известно, что ДП - это вариант тромбофилии и эта патология является причиной рецидивирующих тромбозов, тромбоэмболии, инфарктов и других тромботических нарушений. Сущность патогенеза тромботических нарушений при ДП заключается в недостаточной способности плазмина (активированной формы плазминогена) разрушать фибрин. Выявление ДП в крови определяет тактику лечения тромботического нарушения, поэтому быстрая и точная диагностика ДП является актуальной задачей.
В настоящее время базовым способом диагностики ДП является способ, заключающийся в применении полимеразной цепной реакции [Murata М., Оое A., Izumi Т. Ala601-Thr type dysplasminogenaemia genetically diagnosed in patients with retinochoroidal vascular disorders. // Br. J. Haematol. 1997 Nov; 99(2), P.301-303].
Однако известный способ трудоемок, требует оснащения лаборатории специальным дорогостоящим оборудованием для ПЦР-анализа и не может быть использован в повседневной диагностической практике.
Кроме того, известный способ не дает какой-либо информации о степени функциональной неполноценности плазминогена.
Авторами разработан новый способ диагностики ДП, который отличается от существующего простотой выполнения, сокращает время исследования, дает количественное выражение результатов исследования и может выполняться практически в любой клинической лаборатории, поскольку для его осуществления необходим лишь фотометр.
Техническим результатом заявляемого изобретения является упрощение способа диагностики и повышение его эффективности за счет количественного определения функциональной неполноценности плазминогена.
Технический результат достигается тем, что для осуществления диагностики используют два раствора стрептокиназы, вычисляют отношение индексов поглощения и при значении отношения больше 1,32 диагностируют ДП.
Способ осуществляют следующим образом:
Реактивы и оборудование
1. Лимоннокислый натрий, трехзамещенный, 3,8% раствор.
2. Буфер Трис-HCl, (РН=7,4), 10 мл, концентрированный (20:1), производитель ООО фирма «Технология-Стандарт», Россия.
3. Хромогенный субстрат For-Ala-Phe-Lys-pNA.HBr (6 мг), реагент из диагностического набора реагентов Хромо-Тех-Плазминоген), производитель ООО фирма «Технология-Стандарт», Россия.
4. Стрептокиназа (высокая активность, 125000 МЕ/мл), компонент диагностического набора "ХромоТех-Плазминоген", производитель ООО фирма «Технология-Стандарт», Россия.
5. Стрептокиназа (низкая активность, 1000 МЕ/мл), производитель ООО фирма «Технология-Стандарт», Россия.
6. Референтная нормальная плазма (РНП) для контрольных исследований, лиофильно высушенная смесь нормальной плазмы от 30-40 доноров), производитель "Технология-Стандарт", Россия.
7. 30% раствор уксусной кислоты.
8. Пробирки полистероловые на 15 мл, градуированные, производитель Sardstedt, Швейцария.
9. Центрифуга ОПН-8.
10. Фотометр RA-50 (Bayer Diagnostics) или аналогичный. Длина волны - 405 нм, ширина оптического пути кюветы 1 см.
Разведение реагентов
1. 3,8% раствор лимоннокислого натрия. Получают растворением 3,8 г тринатрия-цитрата в 100 мл дистиллированной воды.
2. Буфер Трис-HCl. Содержимое флакона с концентрированным буфером переносят в мерный цилиндр и доводят объем дистиллированной водой до 200 мл. В результате получают рабочий раствор буфера (рН 7,4).
3. Стрептокиназа (рабочий раствор №1). Во флакон с высокой активностью стрептокиназы (125000 МЕ/мл) добавляют 5 мл рабочего раствора буфера и при легком покачивании растворяют реагент в течение 2 мин.
4. Стрептокиназа (рабочий раствор №2). Во флакон с низкой активностью стрептокиназы (5000 МЕ/мл) добавляют 5 мл рабочего раствора буфера и при легком покачивании растворяют реагент в течение 2 мин.
5. Хромогенный субстрат. Во флакон с лиофильно высушенным субстратом добавляют 6,0 мл дистиллированной воды и при легком покачивании растворяют реагент в течение 5 мин.
6. РНП-плазма. Для подготовки РНП-плазмы во флакон вносят 1,0 мл дистиллированной воды и растворяют содержимое при комнатной температуре (+18...+25°С) и легком покачивании в течение 3 мин.
7. 30% раствор уксусной кислоты. Получают растворением 30 мл ледяной уксусной кислоты в 100 мл дистиллированной воды.
Подготовка образцов бедной тромбоцитами плазмы (БТП)
Кровь получают из локтевой вены иглой в пробирку, содержащую 3,8% раствор лимоннокислого натрия (соотношение крови и лимоннокислого натрия 9:1). Кровь центрифугируют 5 мин при 1000 об/мин (200 g). Полученную богатую тромбоцитами плазму повторно центрифугируют в течение 20 мин при 3500 об/мин (1200 g). Полученную таким способом БТП используют для проведения исследования.
Ход определения
Для осуществления процедуры диагностики применяют последовательность манипуляций (Таблица 1). В таблице 1 представлена схема добавления реагентов для получения четырех проб и определения в них поглощения (длина волны 405 нм; ширина оптического пути 10 мм).
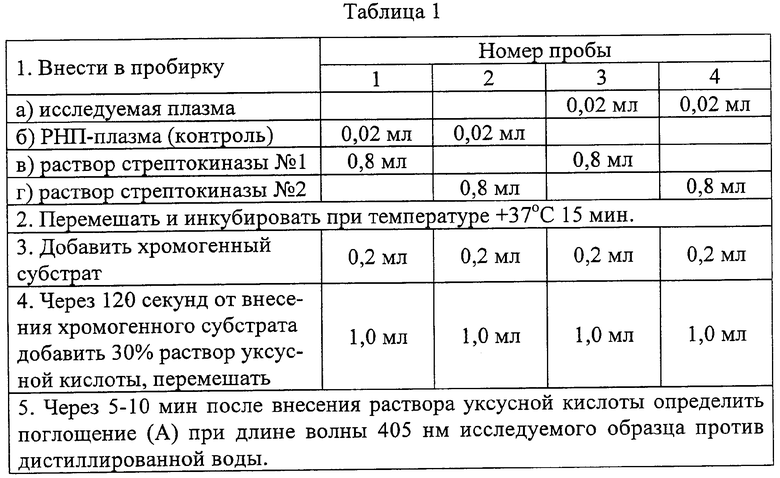
Оценка полученных результатов
После определения поглощения в четырех пробах вычисляют показатели отношения для контрольного образца O(K) и для больного O(Б) по следующим формулам:
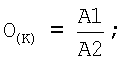
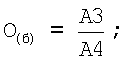
где:
А1 - поглощение, в пробе №1;
А2 - поглощение, в пробе №2;
A3 - поглощение, в пробе №3;
А4 - поглощение, в пробе №4;
О(К) - отношение поглощения для контрольного образца;
О(Б) - отношение поглощения для исследуемого образца.
Затем вычисляют нормализованное отношение (НО) по следующей формуле:
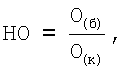
где НО - нормализованное отношение, которое количественно оценивает функциональную неполноценность плазминогена.
При обследовании здоровых людей установлено, что показатель НО равен 1,02; SD=0,15; m=0,03; n=28, а пределы нормальных колебаний (Х±2SD) составили 0,72-1,32. Следовательно, НО у здоровых людей всегда меньше 1,32, а в тех случаях, когда НО равняется или больше этого значения, диагностируют дисплазминогенемию.
Воспроизводимость предлагаемого способа
Для оценки воспроизводимости способа диагностики ДП использовали коэффициент вариации CV(%). Как и все методы с использованием хромогенных субстратов, этот метод показал высокую воспроизводимость. Коэффициент вариации этого теста при исследовании в разные дни не превышал 5%.
Апробация предлагаемого способа
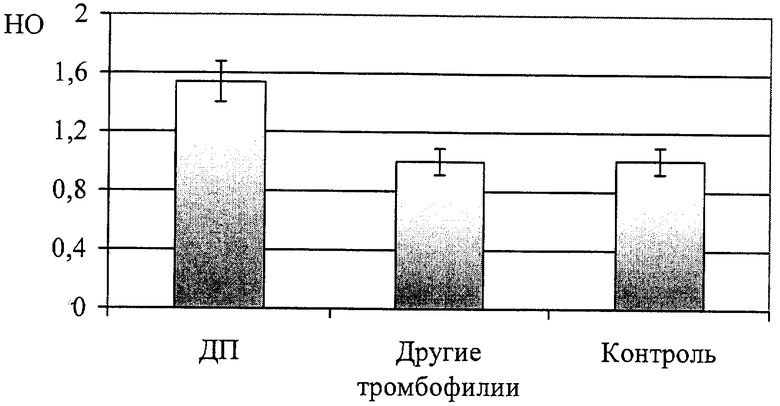
Апробацию заявляемого способа диагностики провели на 189 больных с рецидивирующими артериальными и венозными тромбозами различной локализации. Для выявления причины развития тромбозов применяли современные диагностические процедуры (определяли резистентность фактора Va к активированному протеину С, дефицит протеина С, дефицит протеина S, полиглобулию, высокую концентрацию факторов VIII и IX и другие маркеры тромбофилического состояния). Контрольные исследования были выполнены на группе здоровых людей 28 человек (см. чертеж).
Выявили 5 больных с ДП. У этих больных не было выявлено каких-либо других причин развития тромбозов, кроме ДП. Из чертежа видно, что показатель НО был выше у больных с ДП в сравнении с аналогичным показателем, полученным при исследовании больных с другими причинами тромбозов.
Дополнительно изучали частоту тромботических осложнений у больных с ДП и показатель НО. При проведении корреляционного анализа установлено, что эти два показателя связаны положительной корреляционной зависимостью (RSperman=0,71; P=0,0231).
Диагностика ДП у больных, получающих гепарин
Известно, что основными клиническими проявлениями любой тромбофилии являются тромботические нарушения, и поэтому этим больным часто применяют гепарин. Терапевтическая концентрация гепарина в плазме крови составляет обычно 0,05-0,40 МЕ/мл. Большинство способов, которые выявляют разные виды тромбофилий, дают искаженные результаты при наличии гепарина в крови, но заявляемый способ позволяет осуществлять диагностику ДП больным, которым применяют гепарин. Такая возможность имеется благодаря тому, что в тесте, основанном на применении хромогенных субстратов, используют два раствора стрептокиназы, которые имеют разную тропность к плазминогену, но не связываются с гепарином.
Специфичность способа
Заявляемый способ отличается высокой специфичностью к ДП. Другие причины, вызывающие тромботические нарушения, не оказывают влияния на показания заявляемого способа, так как при диагностике использованы лишь различные концентрации стрептокиназы, обладающие различной способностью связываться с плазминогеном из исследуемого образца БТП.
Пример практического использования предлагаемого способа.
Больной Ш., 47 лет, поступил в отделение сосудистой хирургии 21.10.2003 г. с жалобами на боли в правой нижней конечности, появляющиеся при ходьбе на небольшие расстояния, парастезии, зябкость нижних конечностей. Состоит на "Д" учете по поводу системного атеросклероза в течение десяти лет. За время заболевания дважды отмечает тромботические осложнения: инфаркт миокарда в августе 1997 года и тромбоз левой бедренной артерии в сентябре 1999 года. Состоит на диспансерном учете у кардиолога с диагнозом ишемическая болезнь сердца и у сосудистого хирурга с облитерирующим атеросклерозом сосудов нижних конечностей. Постоянно принимает адреноблокаторы, нитраты. Последнее ухудшение с начала октября 2003 года проявляется вышеперечисленными жалобами.
Проведено исследование крови:
Hb - 145 г/л; СОЭ 7 мм/ч; лейкоциты - 5,4×109/л; лейкоцитарная формула: Б - 1%, Э - 1%, П - 1%, С - 57%, Л - 32%, М - 8%.
Биохимический анализ крови: креатинин 74 мкмоль/л; мочевина 5,9 ммоль/л; общий билирубин 13 мкмоль/л, прямой 4 мкмоль/л, непрямой 9 мкмоль/л; глюкоза 4,6 ммоль/л; ЦРБ +; общий белок - 82,9 г/л, альбумины - 50,0%, α1 - 5,0%, α2 - 11,0%, β - 14,0%, γ - 20,0%.
Общий анализ мочи без особенностей. На ЭКГ блокада правой ножки пучка Гиса, постинфарктный кардиосклероз.
Выполнено исследование системы гемостаза для выявления причины тромботических нарушений (Таблица 2).
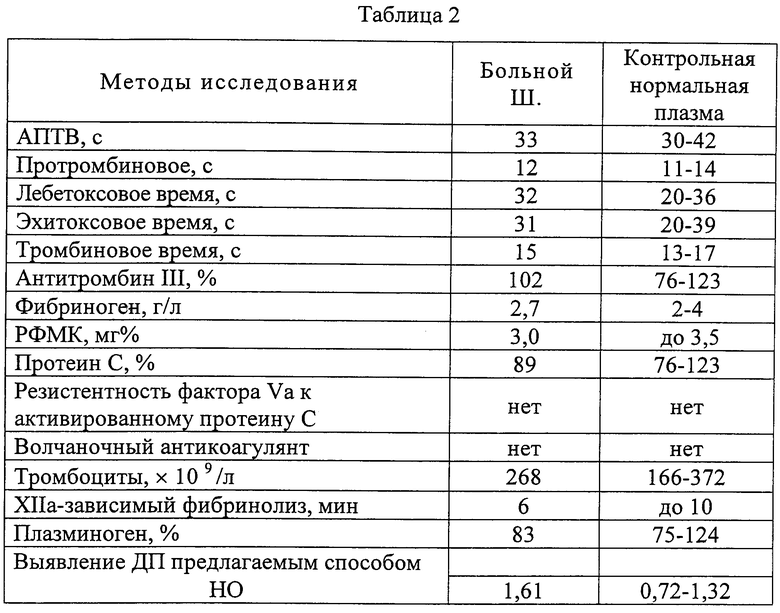
Как видно из представленной таблицы, выявлена лишь выраженная ДП, а другие показатели системы гемостаза в пределах нормы. На основании клинических и лабораторных данных сформулирован следующий диагноз: тромбофилия, обусловленная дисплазминогенемией. Ишемическая болезнь сердца. Постинфарктный кардиосклероз (1997, 1999). Системный атеросклероз с преимущественным поражением сосудов сердца и нижних конечностей.
В представленном клиническом примере иллюстрируется практическое применение заявляемого способа. Как видно из представленного клинического примера, ДП была связана с ранним развитием атеросклероза.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗА ОСЛОЖНЕНИЙ БЕРЕМЕННОСТИ У ПАЦИЕНТОК С ТРОМБОФИЛИЕЙ | 2010 |
|
RU2429478C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПЛАЗМИНОГЕНА | 2000 |
|
RU2189590C2 |
| Способ прогнозирования развития тромботических осложнений после панкреатодуоденальной резекции при раке головки поджелудочной железы | 2015 |
|
RU2618402C1 |
| СПОСОБ ОПТИМИЗАЦИИ В КОРОТКИЕ СРОКИ ИНГИБИТОРА АКТИВАТОРА ПЛАЗМИНОГЕНА В КРОВИ ПРИ АРТЕРИАЛЬНОЙ ГИПЕРТОНИИ С НАРУШЕНИЕМ ТОЛЕРАНТНОСТИ К ГЛЮКОЗЕ | 2009 |
|
RU2406491C1 |
| СПОСОБ ОПТИМИЗАЦИИ СОДЕРЖАНИЯ В ПЛАЗМЕ ИНГИБИТОРА АКТИВАТОРА ПЛАЗМИНОГЕНА У НОВОРОЖДЕННЫХ ПОРОСЯТ С АНЕМИЕЙ | 2009 |
|
RU2399374C1 |
| СПОСОБ НОРМАЛИЗАЦИИ УРОВНЯ ИНГИБИТОРА АКТИВАТОРА ПЛАЗМИНОГЕНА У НОВОРОЖДЕННЫХ ПОРОСЯТ С АНЕМИЕЙ | 2007 |
|
RU2350319C1 |
| СПОСОБ ДИАГНОСТИКИ ТРОМБОФИЛИИ, ОБУСЛОВЛЕННОЙ РЕЗИСТЕНТНОСТЬЮ ФАКТОРА V К АКТИВИРОВАННОМУ ПРОТЕИНУ С | 2001 |
|
RU2205411C2 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ HBV- И HCV-ИНФЕКЦИИ У ПАЦИЕНТОВ С ЦИРРОЗОМ ПЕЧЕНИ | 2010 |
|
RU2444997C1 |
| СПОСОБ ДИАГНОСТИКИ ТРОМБОФИЛИИ, ОБУСЛОВЛЕННОЙ ВЫСОКОЙ АКТИВНОСТЬЮ КОАГУЛЯЦИОННОГО ФАКТОРА VIII | 2002 |
|
RU2227918C1 |
| СПОСОБ НОРМАЛИЗАЦИИ УРОВНЯ ИНГИБИТОРА АКТИВАТОРА ПЛАЗМИНОГЕНА ПРИ АНЕМИИ У НОВОРОЖДЕННЫХ ТЕЛЯТ И ПОРОСЯТ | 2009 |
|
RU2403024C1 |
Изобретение относится к области медицины, в частности исследованию крови, и может быть использовано для выявления дисплазминогенемии. Способ диагностики дисплазминогенемии, заключающийся в том, что в первую и вторую пробирки добавляют образцы контрольной плазмы, в третью и четвертую пробирки добавляют исследуемую плазму; в первую и третью пробирки добавляют раствор с активностью стерптокиназы 125000 МЕ/мл, во вторую и четвертую пробирки добавляют раствор с активностью стрептокиназы 5000 МЕ/мл; полученные смеси инкубируют в течение 15 мин, добавляют хромогенный субстрат, определяют поглощение всех полученных смесей после двухминутной инкубации, после чего вычисляют нормализованное отношение и при значении нормализованного отношения больше 1,32 диагностируют дисплазминогенемию. Заявленное изобретение обеспечивает упрощение способа диагностики и повышение его эффективности за счет количественного определения функциональной неполноценности плазминогена. 2 табл., 1 ил.
Способ диагностики дисплазминогенемии, заключающийся в том, что в первую и вторую пробирки добавляют образцы контрольной плазмы, в третью и четвертую пробирки добавляют исследуемую плазму; в первую и третью пробирки добавляют раствор с активностью стрептокиназы 125000 МЕ/мл, во вторую и четвертую пробирки добавляют раствор с активностью стрептокиназы 5000 МЕ/мл; полученные смеси инкубируют в течение 15 мин, добавляют хромогенный субстрат, определяют поглощение всех полученных смесей после двухминутной инкубации, после чего вычисляют нормализованное отношение и при значении нормализованного отношения больше 1,32 диагностируют дисплазминогенемию.
| Momot A.P | |||
| et al | |||
| A method for determining plazminogen with a Russian chromogenic substrate and its diagnostic significance | |||
| Klin | |||
| Lab | |||
| Diagn | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| ЗАО «АстраФармСервис», 1999 с.485 | |||
| Moser M | |||
| et al | |||
| Recombinant plasminogen activators: a comparative review of the clinical | |||
Авторы
Даты
2008-10-20—Публикация
2006-11-29—Подача