Изобретение относится к химии и медицине и касается получения фармацевтически приемлемого оксалата N,N-диметил-2-N,N-диметиламинометилпиридил-карбамата, обладающего антихолинэстеразными и антиамнестическими свойствами.
Ранее дигидрохлорид этой структуры под названием аминостигмин описан как соединение, обладающее антихолинэстеразной активностью /1/, а также как лекарственный препарат, используемый в инъекционной лекарственной форме в качестве антидота при отравлении холиноблокирующими веществами /2/, но не использовался для лечения различных деменций. Существенным недостатком аминостигмина является гигроскопичность, что в значительной степени затрудняет его стандартизацию и усложняет производство лекарственных форм.
Целью настоящего изобретения является создание фармацевтически приемлемого потенциального лекарственного средства ряда 3-оксипиридина, обладающего антихолинэстеразной активностью и способностью улучшать когнитивные функции.
Следует подчеркнуть, что для решения поставленной задачи была синтезирована большая группа солей основания N,N-диметил-2-N,N-диметиламинометилпиридил-3-карбамата с различными органическими и неорганическими кислотами и лишь оксалат N,N-диметил-2-N,N-диметиламинометилпиридил-3-карбамата(I) не проявил гигроскопических свойств.
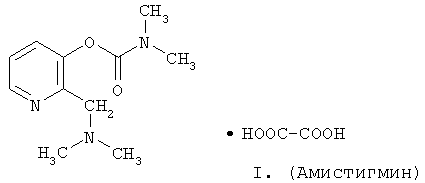
Соединение I получают взаимодействием основания N,N-диметил-2-N,N-диметиламинометилпиридил-3-карбамата /3/ со щавелевой кислотой в среде органического растворителя, например ацетона. Строение I подтверждено данными элементного анализа, ПМР- и масс-спектров.
Пример. Получение оксалата N,N-диметил-2-N,N-диметиламинометилпиридил-3-карбамата (I, амистигмин).
К раствору 1,89 г (0,02 моля) щавелевой кислоты в 1 5 мл ацетона при 20°С постепенно прибавляют раствор 4,47 г (0,02 моля) N,N-диметил-2-N,N-диметиламинометилпиридил-3-карбамата в 15 мл ацетона. Смесь перемешивают 30 мин, осадок отфильтровывают, промывают 5 мл ацетона и сушат, получают 5,23 г (83,55%), ТПЛ 155-157°С (из изо-С3Н7ОН). Найдено, %: С 49,7; Н 6,40; N 13,42. С13Н19N3О6. Вычислено, %: С 49,83; Н 6,11; N 13,42.
Изучение фармакологической активности амистигмина проводили в сравнении с его аналогом по действию ривастигмином (экселоном), который применяется в качестве средства, улучшающего когнитивные функции у больных с различными деменциями, в частности, при болезни Альцгеймера /4/. В нашей стране ривастигмин (экселон) используется ограниченно из-за высокой стоимости.
В условиях in vitro с использованием коммерческих препаратов ацетилхолин-эстеразы эритроцитов человека и бутирилхолинэстеразы сыворотки лошадей амистигмин по антихолинэстеразной активности, определяемой по величинам констант ингибирования (KJ), существенно (на 2 порядка в отношении ацетилхолинэстеразы и на 1 порядок - бутирилхолинэстеразы) превосходит ривастигмин (табл.1). При этом, если амистигмин эффективно ингибирует оба фермента, то ривастигмин (экселон) ингибирует бутирилхолинэстеразу на 1 порядок сильнее, чем ацетилхолинэстеразу.
В условиях ex vivo (на выделенных препаратах ацетилхолинэстеразы головного мозга и крови крыс, время инкубации 10 мин) амистигмин по антихолинэстеразной активности, определяемой по величинам k1 и IC50, также существенно (на 3 порядка) превосходит ривастигмин (экселон) (табл.2 и 3).
В опытах на крысах изучали влияние однократного перорального введения амистигмина и ривастигмина (экселона) в эквитоксических дозах на нарушения обучения и памяти, вызываемые скополамином, с использованием метода условной реакции пассивного избегания /5/. Установлено, что под влиянием скополамина число животных, сохранивших навык условной реакции пассивного избегания, снижается (табл.4). Амистигмин вызывает мало зависимое от дозы ослабление амнестического эффекта скополамина. В целом аналогичные результаты получены и при изучении ривастигмина (экселона). При этом не установлено существенных различий в антиамнестическом действии исследуемых препаратов.
В опытах на крысах изучали влияние однократного перорального введения амистигмина и ривастигмина (экселона) в эквитоксических дозах на нарушения памяти и обучения, вызываемые электрошоком, с использованием метода условной реакции пассивного избегания /5/. Установлено, что на этой модели амнезии (в отличие от приведенных выше данных, полученных на скополаминовой модели) как амистигмин, так и ривастигмин (экселон) оказывали слабое (статистически недостоверное) антиамнестическое действие (табл.5).
В опытах на мышах изучали влияние однократного перорального введения амистигмина и ривастигмина (экселона) в эквитоксических дозах на нарушения памяти и обучения, вызываемые электрошоком, с использованием метода условной реакции пассивного избегания /5/. Установлено, что у интактных животных амистигмин вызывает зависимое от дозы достоверное улучшение обучаемости (отмечается существенное увеличение латентного периода захода животных в темный отсек камеры). В целом, сходный эффект отмечается и под влиянием ривастигмина (экселона) в эквитоксических дозах (средняя колонка табл.6). У мышей, получавших после обучения электрошок (без введения исследуемых препаратов) отмечается существенное ухудшение условно-рефлекторной деятельности, что проявляется 3-кратным уменьшением латентного периода захода в темный отсек камеры. Введение амистигмина, равно как и ривастигмина (экселона), сразу после обучения (до электрошока) приводит к зависимому от дозы существенному ослаблению амнестического эффекта электрошока (латентный период увеличивается более чем в 2 раза) (правая колонка табл.6).
В опытах на крысах изучали влияние многократного (5 дней) перорального введения амистигмина и ривастигмина (экселона) в эквитоксических дозах на нарушения памяти и обучения, при многократном (5 дней) введении скополамина с использованием метода условной реакции активного избегания /6/. Установлено, что введение скополамина за 30-60 мин до сеанса обучения существенно нарушает процесс запоминания информации (табл.7). Амистигмин, начиная со 2 дня обучения, в отличие от ривастигмина, существенно уменьшает нарушение обучения, вызываемые скополамином (табл.8).
Таким образом, заявляемое соединение (амистигмин) по антихолинэстеразной активности и по способности улучшать когнитивные функции превосходит используемый в клинической практике для лечения деменций препарат ривастигмин (экселон), в связи с чем оно представляет интерес в качестве потенциального антиамнестического средства.
Список литературы
1. Прозоровский В.Б., Павлова Л.В., Панова П.А. и др. - Хим.-фарм. журнал, 1991, № 1, 87-88.
2. Машковский М.Д. Лекарственные средства. Москва, Новая Волна. 2005, с.202.
3. John A., Aeschlimann, Arthur Stempel, Pat. US 2,512,732, June 27, 1950; Chem. Abstr., v.44, № 19-20, p.8961-8962 (1950).
4. Гаврилова С.И. Фармакотерапия болезни Альцгеймера. Москва, Пульс, 2003, с.115.
5. Андреева Н.И., Ленина В.В., Калинкина М.А. и др. - Хим.-фарм. журнал, 2005, № 1, с.6-9.
6. Буреш Я., Бурешова О., Хьюстон Д.П. Методики и основные эксперименты по изучению мозга и поведения. Москва, Высшая школа, 1991, 399 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНИРОВАННЫЕ ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ, СОСТОЯЩИЕ ИЗ СОЛЕЙ 2-ЭТИЛ-3-(N, N-ДИМЕТИЛКАРБАМОИЛОКСИ)-6-МЕТИЛПИРИДИНА С ОРГАНИЧЕСКИМИ И НЕОРГАНИЧЕСКИМИ КИСЛОТАМИ И ЯНТАРНОЙ КИСЛОТЫ, ОБЛАДАЮЩИЕ АНТИГИПОКСИЧЕСКОЙ, АНТИАМНЕСТИЧЕСКОЙ И ПРОТИВОСУДОРОЖНОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2440115C2 |
| СПОСОБ ЛЕЧЕНИЯ НАРУШЕНИЙ МНЕСТИЧЕСКИХ ФУНКЦИЙ | 2004 |
|
RU2268726C2 |
| 13-[(2S)2-АМИНО-4-КАРБОКСИБУТАНОИЛ]-1,4,7,10- ТЕТРАОКСА-13-АЗАЦИКЛОПЕНТАДЕКАН ГИДРОХЛОРИД, ОБЛАДАЮЩИЙ АНТИАМНЕСТИЧЕСКИМ И АНТИГИПОКСИЧЕСКИМ ДЕЙСТВИЕМ | 1987 |
|
RU1512079C |
| НЕЙРОТРОПНОЕ СРЕДСТВО И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2007 |
|
RU2359962C1 |
| ВЕЩЕСТВО, ПРОЯВЛЯЮЩЕЕ НООТРОПНУЮ АКТИВНОСТЬ | 1990 |
|
RU2050851C1 |
| @ -Никотиноиламинокислоты, обладающие противогипоксической и антиамнестической активностью | 1984 |
|
SU1368314A1 |
| КОМБИНИРОВАННОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ ВИНПОЦЕТИНА И ЯНТАРНОЙ КИСЛОТЫ, ОБЛАДАЮЩЕЕ АНТИГИПОКСИЧЕСКОЙ, АНТИАМНЕСТИЧЕСКОЙ И ПРОТИВОСУДОРОЖНОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2372913C2 |
| СПОСОБ КОРРЕКЦИИ ИНТЕЛЛЕКТУАЛЬНО-МНЕСТИЧЕСКИХ ФУНКЦИЙ У ДЕТЕЙ С ЗАДЕРЖКОЙ ПСИХИЧЕСКОГО РАЗВИТИЯ | 1991 |
|
RU2020938C1 |
| НЕЙРОПРОТЕКТОРНОЕ СРЕДСТВО | 2004 |
|
RU2268715C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИАМНЕСТИЧЕСКИМ И ПРОТИВОГИПОКСИЧЕСКИМ ДЕЙСТВИЕМ | 1991 |
|
RU2099055C1 |
Изобретение относится к области органической химии и касается получения приемлемого для фармацетических целей оксалата N,N-диметил-2-N,N-диметиламинометилпиридил-3-карбамата, обладающего антихолинэстеразной и антиамнестической активностью, который в отличие от других солей этой структуры не является гигроскопическим соединением. Технический результат: полученное соединение обладает более высокой антихолинэстеразной активностью чем ривастигмин (экселон), что дает основание рассматривать его как потенциальное лекарственное средство для лечения различных деменций. 8 табл.
Оксалат N, N-диметил-2-N, N-диметиламинометилпиридил-3-карбамата, отличающийся от других солей, например дигидрохлорида, отсутствием гигроскопичности, обладающий антихолинэстеразной активностью и улучшающий когнитивные функции.
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОГО ВЕЩЕСТВА НА ОСНОВЕ СОЛИ N,N-ДИМЕТИЛ-(2-N`,N`-ДИМЕТИЛАМИНОМЕТИЛПИРИДИЛ-3)КАРБАМАТА И СТИРОЛВИНИЛБЕНЗОЛЬНОГО СУЛЬФОКАТИОНИТА, ОБЛАДАЮЩЕГО СВОЙСТВОМ ИНГИБИРОВАТЬ ХОЛИНЭСТЕРАЗЫ | 1990 |
|
RU1767843C |
| ОКСАЛАТ N,N-ДИМЕТИЛ-[2-(N'-МЕТИЛ-N'-ОКТИЛАМИНОМЕТИЛ)-ПИРИДИЛ-3]-КАРБАМАТА, ОБЛАДАЮЩИЙ АНТИХОЛИНЭСТЕРАЗНОЙ АКТИВНОСТЬЮ | 1989 |
|
SU1626620A1 |
| ОКСАЛАТ N-МЕТИЛ-N-ПРОПАРГИЛ-(2-N',N'-ДИМЕТИЛАМИНОМЕТИЛПИРИДИЛ-3)-КАРБАМАТА, ОБЛАДАЮЩИЙ АНТИХОЛИНЭСТЕРАЗНОЙ И МИОТИЧЕСКОЙ АКТИВНОСТЬЮ | 1989 |
|
SU1637248A1 |
| GB 1269476, 06.04.1972. | |||
Авторы
Даты
2008-11-27—Публикация
2007-07-09—Подача