Настоящее изобретение относится к применению производных формулы (I):
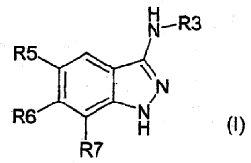
или их фармацевтически приемлемых солей в качестве ингибитора киназ.
Объектами изобретения является применение производных аминоиндазолов формулы (I) и их фармацевтически приемлемых солей для получения фармацевтических композиций, предназначенных для профилактики и лечения заболеваний, которые могут явиться результатом аномальной активности киназ, таких как, например, киназы, участвующие в механизме нейродегенеративных заболеваний, болезни Альцгеймера, Паркинсона, лобно-височной деменции, кортико-базальной дегенерации, болезни Пика, сосудисто-мозговых нарушений, травм головного и спинного мозга и периферический невропатий, ожирения, нарушений обмена веществ, диабета типа II, эссенциальной гипертонии, атеросклеротических сердечно-сосудистых заболеваний, синдрома поликистозных яичников, синдрома Х, иммунодефицита и рака; а также фармацевтические композиции, содержащие новые производные аминоиндазолов и их фармацевтически приемлемые соли и новые производные аминоиндазолов и их фармацевтически приемлемые соли.
В заявке на патент WO 02/074388 описаны производные аминоиндазолов типа (а) активаторов калиевых каналов
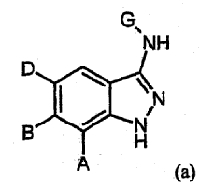
в которой G обозначает 
Z обозначает NX0, S, O,
E обозначает N, CX1,
Y обозначает галоген, X2, OX2,
X0, X1, X2 обозначают галоген, алкил или замещенный алкил,
A, B, D обозначают водород, галоген, замещенный или незамещенный алкил, C(O)pR13, C(O)NR13R14, S02NR13, R14, S(O)pR15, OR15, NR13R14,
p обозначает целое число от 0 до 2,
R13, R14 обозначают водород, замещенный или незамещенный алкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероарил, замещенный или незамещенный гетероцикл, замещенный или незамещенный гетероалкил, замещенный или незамещенный гетероарил-гетероалкил, замещенный или незамещенный арил-гетероалкил,
R15 обозначает замещенный или незамещенный алкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероарил, замещенный или незамещенный гетероцикл, замещенный или незамещенный гетероалкил, замещенный или незамещенный гетероарилгетероалкил, замещенный или незамещенный арилгетероалкил.
Настоящее изобретение относится к производным формулы (I), в которой:
R3 обозначает (С1-С6)алкил, арил, арил(С1-С6)алкил, гетероарил, гетероарил(С1-С6)алкил, арил или гетероарил, конденсированный с (С1-С10)циклоалкилом, гетероцикл, гетероциклоалкил, циклоалкил, адамантил, полициклоалкилы, алкенил, алкинил, CONR1R2, CSNR1R2, CSNR1R2, COOR1, SO2R1, C(=NH)R1, C(=NH)NR1; эти радикалы могут быть в случае необходимости замещены одним или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR1, COOH, C(O)OR1, -O-С(O)R1, NR1R2, NHC(O)R1, C(O)NR1R2, SR1, S(O)R1, SO2R1, NHSO2R1, SO2NR1R2, C(S)NR1R2, NHC(S)R1, -O-SO2R1, -SO2-O-R1, арила, гетероарила, гетероцикла, формила, трифторметила, трифторметилсульфанила, трифторметокси, (С1-С6)алкила;
R5, R6, R7 независимо один от другого выбраны из следующих радикалов: галоген, CN, NO2, NH2, OH, COOH, C(O)OR8, -О-C(O)R8, NR8R9, NHC(O)R8, C(O)NR8R9, NHC(S)R8, C(S)NR8R9, SR8, S(O)R8, SO2R8, NHSO2R8, SO2NR8R9, -O-SO2R8, -SO2-O-R8, трифторметил, трифторметокси, (С1-С6)алкил, (С1-С6)алкокси, арил, арил(С1-С6)алкил, гетероарил, гетероарил(С1-С6)алкил, гетероцикл, циклоалкил, алкенил, алкинил, адамантил, полициклоалкилы; эти радикалы могут быть в случае необходимости замещены одним или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR10, COOH, C(O)OR10, -O-С(O)R10, NR10R11, NHC(O)R10, C(O)NR10R11, NHC(S)R10, C(S)NR10R11, SR10, S(O)R10, SO2R10, NHSO2R10, SO2NR10R11, -O-SO2R10, -SO2-O-R10, арила, гетероарила, формила, трифторметила, трифторметокси, (С1-С6)алкила;
R1, R2, R8, R9, R10, R11 независимо один от другого обозначают водород, (С1-С6)алкил, арил, алкенил, алкинил, гетероарил, которые сами могут быть замещены одним или несколькими заместителями, выбранными из галогена, (С1-С6) алкила, (С1-С6)алкокси, CN, NO2, NH2, OH, COOH, COOалкила, CONH2, формила, трифторметила, трифторметокси;
R1 и R2 или R8 и R9 или R10 и R11 могут образовывать 5 или 6-членный цикл, включающий или не включающий гетероатом, такой как О, S, N;
и когда R3 обозначает азотсодержащий 6-членный гетероарил или тиазолил, или имидазолил, или оксазолил, тогда по меньшей мере один из радикалов R5, R6 обозначает арил, который может быть замещен 1 или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR10, COOH, C(O)OR10, -O-С(O)R10, NR10R11, NHC(O)R10, C(O)NR10R11, NHC(S)R10, C(S)NR10R11, SR10, S(O)R10, SO2R10, NHSO2R10, SO2NR10R11, -O-SO2R10, -SO2-O-R10, арила, гетероарила, формила, трифторметила, трифторметокси, (С1-С6)алкила; их рацематам, энантиомерам, диастереоизомерам и их смесям, таутомерам и фармацевтически приемлемым солям.
В частности, настоящее изобретение относится к производным формулы (I), в которой:
R3 обозначает (С1-С6)алкил, арил, арил(С1-С6)алкил, гетероарил, гетероарил(С1-С6)алкил, арил или гетероарил, конденсированный с (С1-С10)циклоалкилом, гетероцикл, гетероциклоалкил, циклоалкил, адамантил, полициклоалкилы, алкенил, алкинил, CONR1R2, CSNR1R2, CSNR1R2, COOR1, SO2R1, C(=NH)R1, C(=NH)NR1; эти радикалы могут быть в случае необходимости замещены одним или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR1, COOH, C(O)OR1, -O-C(O)R1, NR1R2, NHC(O)R1, C(O)NR1R2, SR1, S(O)R1, SO2R1, NHSO2R1, SO2NR1R2, C(S)NR1R2, NHC(S)R1, -O-SO2R1, -SO2-O-R1, арила, гетероарила, гетероцикла, формила, трифторметила, трифторметилсульфанила, трифторметокси, (С1-С6)алкила;
R5, R6, независимо один от другого выбраны из следующих радикалов: галоген, CN, NO2, NH2, OH, COOH, C(O)OR8, -О-C(O)R8, NR8R9, NHC(O)R8, C(O)NR8R9, NHC(S)R8, C(S)NR8R9, SR8, S(O)R8, SO2R8, NHSO2R8, SO2NR8R9, -O-SO2R8, -SO2-O-R8, трифторметил, трифторметокси, (С1-С6)алкил, (С1-С6)алкокси, арил, арил(С1-С6)алкил, гетероарил, гетероарил(С1-С6)алкил, гетероцикл, циклоалкил, алкенил, алкинил, адамантил, полициклоалкилы; эти радикалы могут быть в случае необходимости замещены одним или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR10, COOH, C(O)OR10, -O-С(O)R10, NR10R11, NHC(O)R10, C(O)NR10R11, NHC(S)R10, C(S)NR10R11, SR10, S(O)R10, SO2R10, NHSO2R10, SO2NR10R11, -O-SO2R10, -SO2-O-R10, арила, гетероарила, формила, трифторметила, трифторметокси, (С1-С6)алкила;
R7 обозначает галоген, метил, циклопропил, CN, OH, метокси, трифторметил, этиленил, ацетиленил, трифторметокси, NO2, NH2, NMe2;
R1, R2, R8, R9, R10, R11 независимо один от другого обозначают водород, (С1-С6)алкил, арил, алкенил, алкинил, гетероарил, которые сами могут быть замещены одним или несколькими заместителями, выбранными из галогена, (С1-С6) алкила, (С1-С6)алкокси, CN, NO2, NH2, OH, COOH, COOалкила, CONH2, формила, трифторметила, трифторметокси;
R1 и R2 или R8 и R9 или R10 и R11 могут образовывать 5 или 6-членный цикл, содержащий или не содержащий гетероатом, такой как O, S, N;
и когда R3 обозначает азотсодержащий 6-членный гетероарил или тиазолил, или имидазолил, или оксазолил, тогда по меньшей мере один из радикалов R5, R6 обозначает арил, который может быть замещен 1 или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR10, COOH, C(O)OR10, -O-С(O)R10, NR10R11, NHC(O)R10, C(O)NR10R11, NHC(S)R10, C(S)NR10R11, SR10, S(O)R10, SO2R10, NHSO2R10, SO2NR10R11, -O-SO2R10, -SO2-O-R10, арила, гетероарила, формила, трифторметила, трифторметокси, (С1-С6)алкила;
их рацематам, энантиомерам, диастереоизомерам и их смесям, таутомерам и фармацевтически приемлемым солям. Предпочтительно, настоящее изобретение относится к производным формулы (I), в которой:
R3 обозначает (С1-С6)алкил, арил, арил(С1-С6)алкил, гетероарил, гетероарил(С1-С6)алкил, арил или гетероарил, конденсированный с (С1-С10)циклоалкилом, гетероцикл, гетероциклоалкил, циклоалкил, адамантил, полициклоалкилы, алкенил, алкинил, CONR1R2, CSNR1R2, COOR1, SO2R1, C(=NH)NR1; эти радикалы могут быть в случае необходимости замещены одним или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR1, COOH, C(O)OR1, -O-C(O)R1, NR1R2, NHC(O)R1, C(O)NR1R2, SR1, S(O)R1, SO2R1, NHSO2R1, SO2NR1R2, C(S)NR1R2, NHC(S)R1, -O-SO2R1, -SO2-O-R1, арила, гетероарила, формила, оксо-группы, трифторметила, трифторметилсульфанила, трифторметокси, (С1-С6)алкила;
R5 обозначает арил;
R6, R7 независимо один от другого обозначают галоген, метил, циклопропил, CN, OH, метокси, трифторметил, этиленил, ацетиленил, трифторметокси, NO2, NH2, NMe2;
R1, R2 независимо один от другого обозначают водород, (С1-С6)алкил, арил, алкенил, алкинил, гетероарил, которые сами могут быть замещены одним или несколькими заместителями, выбранными из галогена, (С1-С6)алкила, (С1-С6)алкокси, CN, NO2, NH2, OH, COOH, COOалкил, CONH2, формила, оксо-группы, трифторметила, трифторметокси;
R1 и R2 могут образовывать 5 или 6-членный цикл, содержащий или не содержащий гетероатом, такой как O, S, N;
их рацематам, энантиомерам, диастереоизомерам и их смесям, таутомерам и фармацевтически приемлемым солям.
Предпочтительно, настоящее изобретение относится к производным формулы (I), в которой:
R3 обозначает (С1-С6)алкил, арил, арил(С1-С6)алкил, гетероарил, гетероарил(С1-С6)алкил, арил или гетероарил, конденсированные с (С1-С10)циклоалкилом, гетероцикл, гетероциклоалкил, циклоалкил, адамантил, полициклоалкилы, алкенил, алкинил, CONR1R2, CSNR1R2, COOR1, SO2R1, C(=NH)NR1; эти радикалы могут быть в случае необходимости замещены одним или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR1, COOH, C(O)OR1, -O-C(O)R1, NR1R2, NHC(O)R1, C(O)NR1R2, SR1, S(O)R1, SO2R1, NHSO2R1, SO2NR1R2, C(S)NR1R2, NHC(S)R1, -O-SO2R1, -SO2-O-R1, арила, гетероарила, формила, оксо-группы, трифторметила, трифторметилсульфанила, трифторметокси, (С1-С6)алкила;
R5 обозначает арил;
R6 обозначает галоген, метил, циклопропил, CN, OH, метокси, трифторметил, этиленил, ацетиленил, трифторметокси, NO2, NH2, NMe2;
R7 обозначает галоген;
R1, R2 независимо один от другого обозначают водород, (С1-С6)алкил, арил, алкенил, алкинил, гетероарил, которые сами могут быть замещены одним или несколькими заместителями, выбранными из галогена, (С1-С6)алкила, (С1-С6)алкокси, CN, NO2, NH2, OH, COOH, COOалкила, CONH2, формила, оксо-группы, трифторметила, трифторметокси;
R1 и R2 могут образовывать 5 или 6-членный цикл, содержащий или не содержащий гетероатом, такой как O, S, N;
их рацематам, энантиомерам, диастереоизомерам и их смесям, таутомерам и фармацевтически приемлемым солям.
В вышеприведенных и последующих определениях, (С1-С6)алкилы содержат от 1 до 6 атомов углерода в прямой или разветвленной цепи; алкенилы содержат от 2 до 6 атомов углерода и от 1 до 3 сопряженных или несопряженных двойных связей в прямой или разветвленной цепи; алкинилы содержат от 2 до 6 атомов углерода и от 1 до 3 сопряженных или несопряженных тройных связей в прямой или разветвленной цепи; арилы выбирают из фенила, нафтила или инденила; гетероарилы содержат от 3 до 10 звеньев, которые могут включать один или несколько гетероатомов, выбранных из кислорода, серы и азота, в частности, тиазолил, тиенил, пирролил, пиридинил, фурил, имидазолил, оксазолил, пиразинил, тетразолил, оксадиазолил, тиадиазолил, изоксадиазолил, изотиадиазолил, изотиазолил, изоксазолил, тиазолил, пиразолил, индолил; галоген представляет собой хлор, йод, фтор, бром; полициклоалкилы выбирают из адамантила, хинуклидинила, борнанила, норборнанила, борненила, норборненила; гетероарилы, конденсированные с (С1-С10)циклоалкилом, выбирают из инданила, изохроманила, хроманила, 1,2,3,4-тетрагидроизохинолила, 1,2,3,4-тетрагидрохинолила; гетероциклы содержат от 1 до 2 гетероатомов, выбранных из кислорода, серы, азота и представляют собой, в частности, пиперидинил, морфолинил, пирролидинил, имидазолидинил, пирразолидинил, изотиазолидинил, тиазолидинил, изоксазолидинил, оксазолидинил, пиперазинил, азетидинил, 2-пиперидон, 3-пиперидон, 4-пиперидон, 2-пирролидон, 3-пирролидон.
Соединения формулы (I) содержат один или несколько асимметрических атомов углерода и могут, таким образом, быть в форме изомеров, рацематов, энантиомеров и диастереоизомеров; эти формы, а также их смеси, также составляют часть изобретения.
Из соединений формулы (I), пригодных для использования согласно изобретению, можно назвать следующие соединения:
N-(бицикло[2,2,1]гепт-5-ен-2-илметил)-6-хлор-7-фтор-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-(3,3-диметилбутил)-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-(3-фенилпропил)-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-(циклопропилметил)-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-(циклопентилметил)-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-[3-(метилтио)пропил]-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-(фенилэтил)-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-(циклогексилметил)-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-пропил-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-(2,2,3,3,4,4,4-гептафторбутил)-5-фенил-1H-индазол-3-амин, гидрат
6-хлор-7-фтор-N-(4,4,4-трифторбутил)-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-[(4-метоксифенил)метил]-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-(фенилметил)-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-[(4-цианофенил)метил]-5-фенил-1H-индазол-3-амин
N-[(4-хлорфенил)метил]-6-хлор-7-фтор-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-[(3-метоксифенил)метил]-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-[[4-(трифторметокси)фенил]метил]-5-фенил-1H-индазол-3-амин
N-[4-[[[6-хлор-7-фтор-5-фенил-1H-индазол-3-ил]амино]метил]фенил]ацетамид
6-хлор-7-фтор-N-[(3,5-дихлорфенил)метил]-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-5-фенил-N-[[4-(трифторметил)фенил]метил]-1H-индазол-3-амин
6-хлор-7-фтор-N-[(4-фторфенил)метил]-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-[3-(4-метилфенокси)фенилметил]-5-фенил-1H-индазол-3-амин
N-(2,2,3,3,4,4,4-гептафторбутил]-6-хлор-7-фтор-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-5-фенил-N-[[3,5-бис(трифторметил)фенил]метил]-1H-индазол-3-амин
6-хлор-7-фтор-5-фенил-N-[[3-(трифторметил)фенил]метил]-1H-индазол-3-амин
6-хлор-7-фтор-N-[(6-метокси-2-нафталинил)метил]-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-[(пентафторфенил)метил]-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-[[4-(метилтио)фенил]метил]-5-фенил-1H-индазол-3-амин
N-[(4-хлор-3-фторфенил)метил]-6-хлор-7-фтор-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-5-фенил-N-(3,3,3-трифторпропил)-1H-индазол-3-амин
6-хлор-7-фтор-5-фенил-N-(3-тиенилметил)-1H-индазол-3-амин
N-(бицикло[2,2,1]гепт-5-ен-2-илметил)-6-хлор-7-фтор-5-фенил-1H-индазол-3-амин
N-([1,1'-бифенил]-4-илметил)-6-хлор-7-фтор-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-[[4-(диметиламино)фенил]метил]-5-фенил-1H-индазол-3-амин
N-([2,2'-битиофен]-5-илметил)-6-хлор-7-фтор-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-5-фенил-N-[[1-(фенилметил)-1H-имидазол-2-ил]метил]-1H-индазол-3-амин
6-хлор-7-фтор-N-[[1-метил-1H-имидазол-2-ил]метил]-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-[(1-метил-1H-индол-3-ил)метил]-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-[(5-метил-2-фуранил)метил]-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-5-фенил-N-(1H-пиррол-2-илметил)-1H-индазол-3-амин
6-хлор-7-фтор-5-фенил-N-(1H-имидазол-2-ил)метил]-1H-индазол-3-амин
6-хлор-7-фтор-5-фенил-N-(1H-имидазол-4-ил)метил]-1H-индазол-3-амин
6-хлор-7-фтор-5-фенил-N-(1H-пиразол-3-илметил)-1H-индазол-3-амин
6-хлор-7-фтор-N-[[2-метил-1H-имидазол-4-ил]метил]-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-[(3,5-диметил-1-фенил-1H-пиразол-4-ил)метил]-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-5-фенил-N-[[2-фенил-1H-имидазол-4-ил]метил]-1H-индазол-3-амин
6-хлор-7-фтор-N-[[5-(4-хлорфенил)-2-фуранил]метил]-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-5-фенил-N-[(1-метил-1H-пиррол-2-ил)метил]-1H-индазол-3-амин
4-[5-[[[6-хлор-7-фтор-5-фенил-1H-индазол-3-ил]амино]метил]-2-фуранил]бензолсульфонамид
6-хлор-7-фтор-5-фенил-N-(3-тиенилметил)-1H-индазол-3-амин
6-хлор-7-фтор-5-фенил-N-[[2-фенил-1H-имидазол-4-ил]метил]-1H-индазол-3-амин
этил-2-[[[6-хлор-7-фтор-5-фенил-1H-индазол-3-ил]амино]метил]-5-(метилтио)-1H-имидазол-4-карбоксилат
6-хлор-7-фтор-5-фенил-N-[[5-[4-(трифторметил)фенил]-2-фуранил]метил]-1H-индазол-3-амин
6-хлор-7-фтор-5-фенил-N-[2-(1-пиперидинил)этил]-1H-индазол-3-амин
6-хлор-7-фтор-N-[2-(4-морфолинил)этил]-5-фенил-1H-индазол-3-амин
N-(6-хлор-7-фтор-5-фенил-1H-индазол-3-ил)-N'-(3,5-дихлорфенил)мочевина
N-(6-хлор-7-фтор-5-фенил-1H-индазол-3-ил)-N'-(2-пропенил)мочевина
N-(6-хлор-7-фтор-5-фенил-1H-индазол-3-ил)-N'-(фенилметил)мочевина
N-(6-хлор-7-фтор-5-фенил-1H-индазол-3-ил)-N'-4-(феноксифенил)мочевина
N-(6-хлор-7-фтор-5-фенил-1H-индазол-3-ил)-N'-[(4-метоксифенил)метил]мочевина
N-(6-хлор-7-фтор-5-фенил-1H-индазол-3-ил)-N'-[4-(трифторметил)фенил]мочевина
N-(6-хлор-7-фтор-5-фенил-1H-индазол-3-ил)-N'-(4-метоксифенил)мочевина
N-(6-хлор-7-фтор-5-фенил-1H-индазол-3-ил)-N'-циклогексилмочевина
N-(6-хлор-7-фтор-5-фенил-1H-индазол-3-ил)-N'-пропилмочевина
N-(6-хлор-7-фтор-5-фенил-1H-индазол-3-ил)-N'-(4-хлорфенил)мочевина
N-(6-хлор-7-фтор-5-фенил-1H-индазол-3-ил)-N'-(4-фторфенил)мочевина
N-[6-хлор-7-фтор-5-фенил-1H-индазол-3-ил]-N'-трицикло[3,3,1,13,7]дец-1-илмочевина
N-(6-хлор-7-фтор-5-фенил-1H-индазол-3-ил)-N'-(4-метилфенил)мочевина
N-(6-хлор-7-фтор-5-фенил-1H-индазол-3-ил)мочевина
N-(6-хлор-7-метил-5-фенил-1H-индазол-3-ил)мочевина
N-(6-хлор-7-циано-5-фенил-1H-индазол-3-ил)мочевина
N-(6-хлор-7-циклопропил-5-фенил-1H-индазол-3-ил)мочевина
N-(6-хлор-7-гидрокси-5-фенил-1H-индазол-3-ил)мочевина
N-(6-хлор-7-метокси-5-фенил-1H-индазол-3-ил)мочевина
N-(6-хлор-7-трифторметил-5-фенил-1H-индазол-3-ил)мочевина
N-(6-хлор-7-трифторметокси-5-фенил-1H-индазол-3-ил)мочевина
N-(6-хлор-7-нитро-5-фенил-1H-индазол-3-ил)мочевина
N-(6-хлор-7-амино-5-фенил-1H-индазол-3-ил)мочевина
N-(6-хлор-7-диметиламино-5-фенил-1H-индазол-3-ил)мочевина
N-(6-хлор-7-этинил-5-фенил-1H-индазол-3-ил)мочевина
N-[6-хлор-7-фтор-5-фенил-1H-индазол-3-ил]-4-метилбензолсульфонамид
N-[6-хлор-7-фтор-5-фенил-1H-индазол-3-ил]метансульфонамид
N-[6-хлор-7-фтор-5-фенил-1H-индазол-3-ил]-2-пропансульфонамид
N-[6-хлор-7-фтор-5-фенил-1H-индазол-3-ил]-2,2,2-трифторэтансульфонамид
N-[6-хлор-7-фтор-5-фенил-1H-индазол-3-ил]-2-тиофенсульфонамид
N-[6-хлор-7-фтор-5-фенил-1H-индазол-3-ил]бензолсульфонамид
N-[6-хлор-7-фтор-5-фенил-1H-индазол-3-ил]-4-(трифторметил)бензолсульфонамид
N-[6-хлор-7-фтор-5-фенил-1H-индазол-3-ил]-5-(3-изоксазолил)-2-тиофенсульфонамид
N-[6-хлор-7-фтор-5-фенил-1H-индазол-3-ил]-4-фторбензолсульфонамид
N-[6-хлор-7-фтор-5-фенил-1H-индазол-3-ил]-4-метоксибензолсульфонамид
N-[6-хлор-7-фтор-5-фенил-1H-индазол-3-ил]бензолметансульфонамид
N-[6-хлор-7-фтор-5-фенил-1H-индазол-3-ил]-1-метил-1H-имидазол-4-сульфонамид
N-[6-хлор-7-фтор-5-фенил-1H-индазол-3-ил]-4-(1,1-диметилэтил)бензолсульфонамид
N-[4-[[(6-хлор-7-фтор-5-фенил-1H-индазол-3-ил)амино]сульфонил]фенил]ацетамид
N-[6-хлор-7-фтор-5-фенил-1H-индазол-3-ил]-4-метилбензолметансульфонамид
6-хлор-7-фтор-N-(пентафторфенил)-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-(3,4-дифторфенил)-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-5-фенил-N-(2,3,5,6-тетрафторфенил)-1H-индазол-3-амин
6-хлор-7-фтор-5-фенил-N-(2,4,6-трифторфенил)-1H-индазол-3-амин
6-хлор-7-фтор-N-(4-фторфенил)-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-[3-(трифторметил)фенил]-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-[4-(трифторметил)фенил]-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-[3-фтор-5-(трифторметил)фенил]-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-(4-нитрофенил)-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-(3-нитрофенил)-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-(3-метоксифенил)-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-(4-метоксифенил)-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N,5-дифенил-1H-индазол-3-амин
6-хлор-7-фтор-N-(1-пиридинил)-5-фенил-1H-индазол-3-амин
6-хлор-7-фтор-N-(2-пиридинил)-5-фенил-1H-индазол-3-амин
N-бутил-6-хлор-7-фтор-5-фенил-1H-индазол-3-амин
N-(6-хлор-7-фтор-5-фенил-1H-индазол-3-ил)-N'-фенилмочевина
N-(6-хлор-7-фтор-5-фенил-1H-индазол-3-ил)-3-метоксибензолсульфонамид
их изомеры, смеси, рацематы, энантиомеры, диастереоизомеры, таутомеры, а также их фармацевтически приемлемые соли,
и, в частности, следующие соединения:
(6,7-дифтор-5-фенил-1H-индазол-3-ил)амид пиперидин-1-карбоновой кислоты
(6,7-дифтор-5-фенил-1H-индазол-3-ил)амид пирролидин-1-карбоновой кислоты
1-(6,7-дифтор-5-фенил-1H-индазол-3-ил)-3-[3-(4-метилпиперазин-1-ил)пропил]мочевина
N-(6,7-дифтор-5-фенил-1H-индазол-3-ил)-N'-фенилмочевина
их таутомеры, а также их фармацевтически приемлемые соли.
Изобретение также относится к фармацевтическим композициям, содержащим в качестве действующего начала производное формулы (I), в которой:
R3 обозначает (С1-С6)алкил, арил, арил(С1-С6)алкил, гетероарил, гетероарил(С1-С6)алкил, арил или гетероарил, конденсированный с (С1-С10)циклоалкилом, гетероцикл, гетероциклоалкил, циклоалкил, адамантил, полициклоалкилы, алкенил, алкинил, CONR1R2, CSNR1R2, CSNR1R2, COOR1, SO2R1, C(=NH)R1, C(=NH)NR1; эти радикалы могут быть в случае необходимости замещены одним или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR1, COOH, C(O)OR1, -О-C(O)R1, NR1R2, NHC(O)R1, C(O)NR1R2, SR1, S(O)R1, SO2R1, NHSO2R1, SO2NR1R2, C(S)NR1R2, NHC(S)R1, -O-SO2R1, -SO2-O-R1, арила, гетероарила, гетероцикла, формила, трифторметила, трифторметилсульфанила, трифторметокси, (С1-С6)алкила;
R5, R6, R7 независимо один от другого выбраны из следующих радикалов: галоген, CN, NO2, NH2, OH, COOH, C(O)OR8, -О-C(O)R8, NR8R9, NHC(O)R8, C(O)NR8R9, NHC(S)R8, C(S)NR8R9, SR8, S(O)R8, SO2R8, NHSO2R8, SO2NR8R9, -O-SO2R8, -SO2-O-R8, трифторметил, трифторметокси, (С1-С6)алкил, (С1-С6)алкокси, арил, арил(С1-С6)алкил, гетероарил, гетероарил(С1-С6)алкил, гетероцикл, циклоалкил, алкенил, алкинил, адамантил, полициклоалкилы; эти радикалы могут быть в случае необходимости замещены одним или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR10, COOH, C(O)OR10, -O-C(O)R10, NR10R11, NHC(O)R10, C(O)NR10R11, NHC(S)R10, C(S)NR10R11, SR10, S(O)R10, SO2R10, NHSO2R10, SO2NR10R11, -О-SO2R10, -SO2-О-R10, арила, гетероарила, формила, трифторметила, трифторметокси, (С1-С6)алкила;
R1, R2, R8, R9, R10, R11 независимо один от другого обозначают водород, (С1-С6)алкил, арил, алкенил, алкинил, гетероарил, которые сами могут быть замещены одним или несколькими заместителями, выбранными из галогена, (С1-С6) алкила, (С1-С6)алкокси, CN, NO2, NH2, OH, COOH, COOалкила, CONH2, формила, трифторметила, трифторметокси;
R1 и R2 или R8 и R9 или R10 и R11 могут образовывать 5 или 6-членный цикл, включающий или не включающий гетероатом, такой как О, S, N;
и когда R3 обозначает азотсодержащий 6-членный гетероарил или тиазолил, или имидазолил, или оксазолил, тогда по меньшей мере один из радикалов R5, R6 обозначает арил, который может быть замещен 1 или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR10, COOH, C(O)OR10, -O-С(O)R10, NR10R11, NHC(O)R10, C(O)NR10R11, NHC(S)R10, C(S)NR10R11, SR10, S(O)R10, SO2R10, NHSO2R10, SO2NR10R11, -O-SO2R10, -SO2-O-R10, арила, гетероарила, формила, трифторметила, трифторметокси, (С1-С6)алкила; их рацематы, энантиомеры, диастереоизомеры и их смеси, таутомеры и фармацевтически приемлемые соли.
В частности, настоящее изобретение относится к фармацевтическим композициям, содержащим в качестве действующего начала производное формулы (I), в которой:
R3 обозначает (С1-С6)алкил, арил, арил(С1-С6)алкил, гетероарил, гетероарил(С1-С6)алкил, арил или гетероарил, конденсированный с (С1-С10)циклоалкилом, гетероцикл, гетероциклоалкил, циклоалкил, адамантил, полициклоалкилы, алкенил, алкинил, CONR1R2, CSNR1R2, CSNR1R2, COOR1, SO2R1, C(=NH)R1, C(=NH)NR1; эти радикалы могут быть в случае необходимости замещены одним или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR1, COOH, C(O)OR1, -O-C(O)R1, NR1R2, NHC(O)R1, C(O)NR1R2, SR1, S(O)R1, SO2R1, NHSO2R1, SO2NR1R2, C(S)NR1R2, NHC(S)R1, -O-SO2R1, -SO2-O-R1, арила, гетероарила, гетероцикла, формила, трифторметила, трифторметилсульфанила, трифторметокси, (С1-С6)алкила;
R5, R6, независимо один от другого выбраны из следующих радикалов: галоген, CN, NO2, NH2, OH, COOH, C(O)OR8, -О-C(O)R8, NR8R9, NHC(O)R8, C(O)NR8R9, NHC(S)R8, C(S)NR8R9, SR8, S(O)R8, SO2R8, NHSO2R8, SO2NR8R9, -O-SO2R8, -SO2-O-R8, трифторметил, трифторметокси, (С1-С6)алкил, (С1-С6)алкокси, арил, арил(С1-С6)алкил, гетероарил, гетероарил(С1-С6)алкил, гетероцикл, циклоалкил, алкенил, алкинил, адамантил, полициклоалкилы; эти радикалы могут быть в случае необходимости замещены одним или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR10, COOH, C(O)OR10, -O-С(O)R10, NR10R11, NHC(O)R10, C(O)NR10R11, NHC(S)R10, C(S)NR10R11, SR10, S(O)R10, SO2R10, NHSO2R10, SO2NR10R11, -O-SO2R10, -SO2-O-R10, арила, гетероарила, формила, трифторметила, трифторметокси, (С1-С6)алкила;
R7 обозначает галоген, метил, циклопропил, CN, OH, метокси, трифторметил, этиленил, ацетиленил, трифторметокси, NO2, NH2, NMe2;
R1, R2, R8, R9, R10, R11 независимо один от другого обозначают водород, (С1-С6)алкил, арил, алкенил, алкинил, гетероарил, которые сами могут быть замещены одним или несколькими заместителями, выбранными из галогена, (С1-С6) алкила, (С1-С6)алкокси, CN, NO2, NH2, OH, COOH, COOалкила, CONH2, формила, трифторметила, трифторметокси;
R1 и R2 или R8 и R9 или R10 и R11 могут образовывать 5 или 6-членный цикл, содержащий или не содержащий гетероатом, такой как O, S, N;
и когда R3 обозначает азотсодержащий 6-членный гетероарил или тиазолил, или имидазолил, или оксазолил, тогда по меньшей мере один из радикалов R5, R6 обозначает арил, который может быть замещен 1 или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR10, COOH, C(O)OR10, -O-С(O)R10, NR10R11, NHC(O)R10, C(O)NR10R11, NHC(S)R10, C(S)NR10R11, SR10, S(O)R10, SO2R10, NHSO2R10, SO2NR10R11, -O-SO2R10, -SO2-O-R10, арила, гетероарила, формила, трифторметила, трифторметокси, (С1-С6)алкила;
их рацематы, энантиомеры, диастереоизомеры и их смеси, таутомеры и фармацевтически приемлемые соли.
Предпочтительно, настоящее изобретение относится к фармацевтическим композициям, содержащим в качестве действующего начала производное формулы (I), в которой:
R3 обозначает (С1-С6)алкил, арил, арил(С1-С6)алкил, гетероарил, гетероарил(С1-С6)алкил, арил или гетероарил, конденсированный с (С1-С10)циклоалкилом, гетероцикл, гетероциклоалкил, циклоалкил, адамантил, полициклоалкилы, алкенил, алкинил, CONR1R2, CSNR1R2, COOR1, SO2R1, C(=NH)NR1; эти радикалы могут быть в случае необходимости замещены одним или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR1, COOH, C(O)OR1, -O-C(O)R1, NR1R2, NHC(O)R1, C(O)NR1R2, SR1, S(O)R1, SO2R1, NHSO2R1, SO2NR1R2, C(S)NR1R2, NHC(S)R1, -O-SO2R1, -SO2-O-R1, арила, гетероарила, формила, оксо-группы, трифторметила, трифторметилсульфанила, трифторметокси, (С1-С6)алкила;
R5 обозначает арил;
R6, R7 независимо один от другого обозначают галоген, метил, циклопропил, CN, OH, метокси, трифторметил, этиленил, ацетиленил, трифторметокси, NO2, NH2, NMe2
R1, R2 независимо один от другого обозначают водород, (С1-С6)алкил, арил, алкенил, алкинил, гетероарил, которые сами могут быть замещены одним или несколькими заместителями, выбранными из галогена, (С1-С6)алкила, (С1-С6)алкокси, CN, NO2, NH2, OH, COOH, COOалкила, CONH2, формила, оксо-группы, трифторметила, трифторметокси;
R1 и R2 могут образовывать 5 или 6-членный цикл, содержащий или не содержащий гетероатом, такой как O, S, N;
их рацематы, энантиомеры, диастереоизомеры и их смеси, таутомеры и фармацевтически приемлемые соли.
Настоящее изобретение также относится к применению в качестве лекарственного средства производных аминоиндазолов формулы (I), в которой:
R3 обозначает (С1-С6)алкил, арил, арил(С1-С6)алкил, гетероарил, гетероарил(С1-С6)алкил, арил или гетероарил, конденсированный с (С1-С10)циклоалкилом, гетероцикл, гетероциклоалкил, циклоалкил, адамантил, полициклоалкилы, алкенил, алкинил, CONR1R2, CSNR1R2, CSNR1R2, COOR1, SO2R1, C(=NH)R1, C(=NH)NR1; эти радикалы могут быть в случае необходимости замещены одним или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR1, COOH, C(O)OR1, -O-С(O)R1, NR1R2, NHC(O)R1, C(O)NR1R2, SR1, S(O)R1, SO2R1, NHSO2R1, SO2NR1R2, C(S)NR1R2, NHC(S)R1, -O-SO2R1, -SO2-O-R1, арила, гетероарила, гетероцикла, формила, трифторметила, трифторметилсульфанила, трифторметокси, (С1-С6)алкила;
R5, R6, R7 независимо один от другого выбраны из следующих радикалов: галоген, CN, NO2, NH2, OH, COOH, C(O)OR8, -О-C(O)R8, NR8R9, NHC(O)R8, C(O)NR8R9, NHC(S)R8, C(S)NR8R9, SR8, S(O)R8, SO2R8, NHSO2R8, SO2NR8R9, -O-SO2R8, -SO2-O-R8, трифторметил, трифторметокси, (С1-С6)алкил, (С1-С6)алкокси, арил, арил(С1-С6)алкил, гетероарил, гетероарил(С1-С6)алкил, гетероцикл, циклоалкил, алкенил, алкинил, адамантил, полициклоалкилы; эти радикалы могут быть в случае необходимости замещены одним или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR10, COOH, C(O)OR10, -O-С(O)R10, NR10R11, NHC(O)R10, C(O)NR10R11, NHC(S)R10, C(S)NR10R11, SR10, S(O)R10, SO2R10, NHSO2R10, SO2NR10R11, -O-SO2R10, -SO2-O-R10, арила, гетероарила, формила, трифторметила, трифторметокси, (С1-С6)алкила;
R1, R2, R8, R9, R10, R11 независимо один от другого обозначают водород, (С1-С6)алкил, арил, алкенил, алкинил, гетероарил, которые сами могут быть замещены одним или несколькими заместителями, выбранными из галогена, (С1-С6) алкила, (С1-С6)алкокси, CN, NO2, NH2, OH, COOH, COOалкила, CONH2, формила, трифторметила, трифторметокси;
R1 и R2 или R8 и R9 или R10 и R11 могут образовывать 5 или 6-членный цикл, включающий или не включающий гетероатом, такой как О, S, N;
и когда R3 обозначает азотсодержащий 6-членный гетероарил или тиазолил, или имидазолил, или оксазолил, тогда по меньшей мере один из радикалов R5, R6 обозначает арил, который может быть замещен 1 или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR10, COOH, C(O)OR10, -O-С(O)R10, NR10R11, NHC(O)R10, C(O)NR10R11, NHC(S)R10, C(S)NR10R11, SR10, S(O)R10, SO2R10, NHSO2R10, SO2NR10R11, -O-SO2R10, -SO2-O-R10, арила, гетероарила, формила, трифторметила, трифторметокси, (С1-С6)алкила;
их рацематов, энантиомеров, диастереоизомеров и их смесей, таутомеров и фармацевтически приемлемых солей.
В частности, настоящее изобретение относится к применению в качестве лекарственного средства производных аминоиндазолов формулы (I), в которой:
R3 обозначает (С1-С6)алкил, арил, арил(С1-С6)алкил, гетероарил, гетероарил(С1-С6)алкил, арил или гетероарил, конденсированный с (С1-С10)циклоалкилом, гетероцикл, гетероциклоалкил, циклоалкил, адамантил, полициклоалкилы, алкенил, алкинил, CONR1R2, CSNR1R2, CSNR1R2, COOR1, SO2R1, C(=NH)R1, C(=NH)NR1; эти радикалы могут быть в случае необходимости замещены одним или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR1, COOH, C(O)OR1, -O-C(O)R1, NR1R2, NHC(O)R1, C(O)NR1R2, SR1, S(O)R1, SO2R1, NHSO2R1,SO2NR1R2, C(S)NR1R2, NHC(S)R1, -O-SO2R1, -SO2-O-R1, арила, гетероарила, гетероцикла, формила, трифторметила, трифторметилсульфанила, трифторметокси, (С1-С6)алкила;
R5, R6, независимо один от другого выбраны из следующих радикалов: галоген, CN, NO2, NH2, OH, COOH, C(O)OR8, -О-C(O)R8, NR8R9, NHC(O)R8, C(O)NR8R9, NHC(S)R8, C(S)NR8R9, SR8, S(O)R8, SO2R8, NHSO2R8, SO2NR8R9, -O-SO2R8, -SO2-O-R8, трифторметил, трифторметокси, (С1-С6)алкил, (С1-С6)алкокси, арил, арил(С1-С6)алкил, гетероарил, гетероарил(С1-С6)алкил, гетероцикл, циклоалкил, алкенил, алкинил, адамантил, полициклоалкилы; эти радикалы могут быть в случае необходимости замещены одним или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR10, COOH, C(O)OR10, -O-С(O)R10, NR10R11, NHC(O)R10, C(O)NR10R11, NHC(S)R10, C(S)NR10R11, SR10, S(O)R10, SO2R10, NHSO2R10, SO2NR10R11, -O-SO2R10, -SO2-O-R10, арила, гетероарила, формила, трифторметила, трифторметокси, (С1-С6)алкила;
R7 обозначает галоген, метил, циклопропил, CN, OH, метокси, трифторметил, этиленил, ацетиленил, трифторметокси, NO2, NH2, NMe2;
R1, R2, R8, R9, R10, R11 независимо один от другого обозначают водород, (С1-С6)алкил, арил, алкенил, алкинил, гетероарил, которые сами могут быть замещены одним или несколькими заместителями, выбранными из галогена, (С1-С6) алкила, (С1-С6)алкокси, CN, NO2, NH2, OH, COOH, COOалкила, CONH2, формила, трифторметила, трифторметокси;
R1 и R2 или R8 и R9 или R10 и R11 могут образовывать 5 или 6-членный цикл, содержащий или не содержащий гетероатом, такой как O, S, N;
и когда R3 обозначает азотсодержащий 6-членный гетероарил или тиазолил, или имидазолил, или оксазолил, тогда по меньшей мере один из радикалов R5, R6 обозначает арил, который может быть замещен 1 или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR10, COOH, C(O)OR10, -O-С(O)R10, NR10R11, NHC(O)R10, C(O)NR10R11, NHC(S)R10, C(S)NR10R11, SR10, S(O)R10, SO2R10, NHSO2R10, SO2NR10R11, -O-SO2R10, -SO2-O-R10, арила, гетероарила, формила, трифторметила, трифторметокси, (С1-С6)алкила;
их рацематов, энантиомеров, диастереоизомеров и их смесей, таутомеров и фармацевтически приемлемых солей.
Предпочтительно, настоящее изобретение относится к применению в качестве лекарственного средства производных аминоиндазолов формулы (I), в которой:
R3 обозначает (С1-С6)алкил, арил, арил(С1-С6)алкил, гетероарил, гетероарил(С1-С6)алкил, арил или гетероарил, конденсированный с (С1-С10)циклоалкилом, гетероцикл, гетероциклоалкил, циклоалкил, адамантил, полициклоалкилы, алкенил, алкинил, CONR1R2, CSNR1R2, COOR1, SO2R1, C(=NH)NR1; эти радикалы могут быть в случае необходимости замещены одним или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR1, COOH, C(O)OR1, -O-C(O)R1, NR1R2, NHC(O)R1, C(O)NR1R2, SR1, S(O)R1, SO2R1, NHSO2R1, SO2NR1R2, C(S)NR1R2, NHC(S)R1, -O-SO2R1, -SO2-O-R1, арила, гетероарила, формила, оксо-группы, трифторметила, трифторметилсульфанила, трифторметокси, (С1-С6)алкила;
R5 обозначает арил;
R6, R7 независимо один от другого обозначают галоген, метил, циклопропил, CN, OH, метокси, трифторметил, этиленил, ацетиленил, трифторметокси, NO2, NH2, NMe2;
R1, R2 независимо один от другого обозначают водород, (С1-С6)алкил, арил, алкенил, алкинил, гетероарил, которые сами могут быть замещены одним или несколькими заместителями, выбранными из галогена, (С1-С6)алкила, (С1-С6)алкокси, CN, NO2, NH2, OH, COOH, COOалкил, CONH2, формила, оксо-группы, трифторметила, трифторметокси;
R1 и R2 могут образовывать 5 или 6-членный цикл, содержащий или не содержащий гетероатом, такой как O, S, N;
их рацематов, энантиомеров, диастереоизомеров и их смесей, таутомеров и фармацевтически приемлемых солей.
Производные формулы (I) могут быть получены из соответствующих 3-амино-производных (V), в которых азот в положении 1 в случае необходимости защищен группой Pr. Pr обозначает триметилсилилэтоксиметил, тозил, мезил, бензил или группы, известные в качестве защитных групп для групп NH-ароматических гетероциклов, как указано в T. W. GREENE, Protective groups in organic Synthesis, J. Wiley-Interscience Publication (1999)
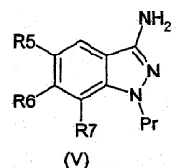
3-амино-1H-индазолы формулы (II) могут быть получены реакцией 2-фторбензонитрила с гидразином, гидратом или хлоргидратом при кипячении с обратным холодильником в течение 2-18 часов в спирте типа этанола или н-бутанола согласно (R. F. KALTENBACH, Bioorg. Med. Chem. Lett., 9, (15), 2259-62, (1999)):
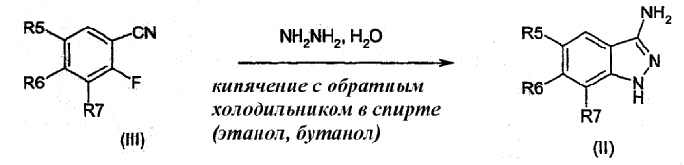
В случае соединений, в которых R5, R6 независимо один от другого выбраны из следующих радикалов: галоген, CN, NO2, NH2, OH, COOH, C(O)OR8, -О-C(O)R8, NR8R9, NHC(O)R8, C(O)NR8R9, NHC(S)R8, C(S)NR8R9, SR8, S(O)R8, SO2R8, NHSO2R8, SO2NR8R9, -O-SO2R8, -SO2-O-R8, трифторметил, трифторметокси, (С1-С6)алкил, (С1-С6)алкокси, арил, арил(С1-С6)алкил, гетероарил, гетероарил(С1-С6)алкил, циклоалкил, алкенил, алкинил, адамантил; причем эти радикалы могут быть в случае необходимости замещены одним или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR10, COOH, C(O)OR10, -O-C(O)R10, NR10R11, NHC(O)R10, C(O)NR10R11, NHC(S)R10, C(S)NR10R11, SR10, S(O)R10, SO2R10, NHSO2R10, SO2NR10R11, -O-SO2R10, -SO2-O-R10, арила, гетероарила, формила, оксо-группы, трифторметила, трифторметокси, (С1-С6)алкила; могут быть получены реакциями, в которых используют химию палладия: Suzuki, (A. SUZUKI, Pure Appl. Chem. 63, 419-22, (1991), Stille (J. STILLE, Angew. Chem. Int. Ed. 25, 508-24, (1986), Heck, (R. F. HECK, Org. React., 27, 345-90, (1982), Sonogashira, (K. SONOGASHIRA, Synthesis 777, (1977), Buchwald (S. L. BUCHWALD, Acc. Chem. Re., 31, 805, (1998) исходя из соответствующих галогенированных производных.
Для этого необходимо защитить реакционноспособные функциональные группы. Так, группы ОН, SH, СООН, NH2 должны быть защищены перед проведением взаимодействия. Защитные группы вводят всеми известными специалисту методами и, в частности, такими, которые описаны T. W. GREENE, Protective groups in Organic Synthesis, J. Wiley-Interscience Publication (1999). Предпочтительно, азот в положении 1 защищают такими группами, как трет.-бутоксикарбонил или кремнийсодержащими производными. Предпочтительно, выбирают силилсодержащую группу: трет.-бутилдиметилсилил, триизопропилсилил, которые могут быть удалены фтор-анионами или уксусной кислотой, в частности, триметилсилилэтоксиметильную группу, которая может быть расщеплена тетрабутиламмонийфторидом при кипячении с обратным холодильником в таких растворителях, как тетрагидрофуран, диоксан (J. P. WHITTEN, J. Org. Chem., 51, 1891, (1986); B. H. LIPSHUTZ, Tetrahedron Lett., 4095, (1986)) или 2 н. соляной кислотой в метаноле или этаноле при кипячении с обратным холодильником.
Производные, защищенные в положении 1 триметилсилилэтоксиметилом, получают, осуществляя реакцию между исходными соединениями и триметилсилилэтоксиметилхлоридом в присутствии гидрида натрия в растворителе, таком как диметилформамид при комнатной температуре (J. P. WHITTEN, J. Org. Chem., 51, 1891, (1986); M. P. EDWARDS, Tetrahedron, 42, 3723, (1986)).
Точно так же, азотсодержащую группу 1-NH индазола защищают такими группами, как тозил, карбамат, бензил или силилсодержащими производными. Например, в случае, когда осуществляют взаимодействие через палладий с галогенированным производным в положении 6, следует защитить азот в положении 1, как показано ниже (X=Cl, Br, I):
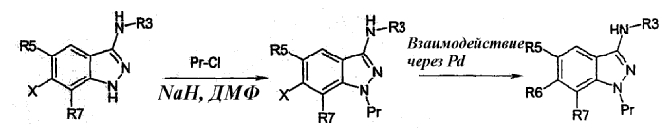
Снятие защиты осуществляют согласно известным специалисту методам, описанным T. W. GREENE, Protective groups in Organic Synthesis, J. Wiley-Interscience Publication (1999). Например, если защитной группой в положении 1 является триметилсилилэтоксиметил, снятие защиты может быть осуществлено с помощью тетрабутиламмонийфторида, как показано ниже:

Если одна из групп R5, R6, участвующих во взаимодействии с использованием химии палладия, сама содержит реакционноспособную функциональную группу, такую как гидроксильная, амино-, тиольная, кислотная группы или, в общем случае, содержит гетероатом, последний также необходимо защитить перед проведением взаимодействия через палладий. Так, например, фенольную группу вводят в защищенной (например, О-бензильной) форме исходя из хлорсодержащего производного, при этом азот в положении 1 защищают, как подробно объяснено ранее:
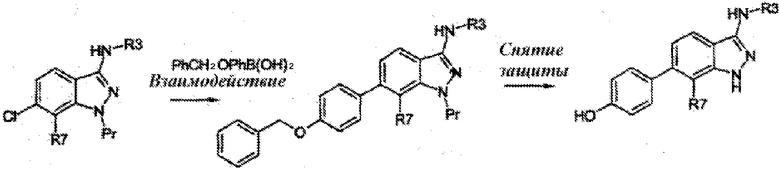
Бензильную группу затем удаляют, например, путем обработки триметилсилилиодидом при кипячении с обратным холодильником в ацетонитриле. Защиту также можно осуществить с помощью триметилсислилэтоксиметильной группы, которая может быть расщеплена тетрабутиламмонийфторидом при кипячении с обратным холодильником в растворителях, таких как тетрагидрофуран, диоксан (J. P. WHITTEN, J. Org. Chem., 51, 1891, (1986); B. H. LIPSHUTZ, Tetrahedron Lett., 4095, (1986)), или 2н. соляной кислотой в метаноле или этаноле при кипячении с обратным холодильником.
Когда R5 и R6 независимо один от другого обозначают арил и галоген, арильную группу вводят исходя из взаимодействия через палладий по бромированному положению, при этом азот в положении 1 и 3 защищают подходящим образом. Предпочтительно, Pr обозначает триметилсилилэтоксиметил, а Pr' обозначает н-бутилкарбокси-группу, которая образует с азотом н-бутиламид. Стадию снятия защиты с амида осуществляют в присутствии этаноламина при кипячении с обратным холодильником в течение недели в ДМФ. Это расщепление может также быть осуществлено с помощью хлорида олова в этаноле (R J Griffin, J. Chem. Soc. Perkin I 1992, 1811-1819) или метилата натрия в метаноле (Y.Furukawa, Chem. Pharm. Bull. 1968, 16, 1076) или любого другого алкоголята в соответствующем спирте.
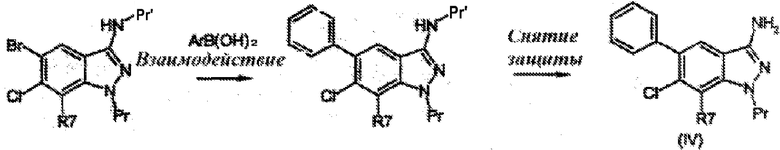
Когда R5 и R6 независимо один от другого обозначают арил и галоген, арильную группу вводят взаимодействием через палладий по бромированному положению, при этом азот в положении 1 и 3 защищают подходящим образом. Предпочтительно, Pr обозначает триметилсилилэтоксиметил, а Pr' обозначает н-бутилкарбокси-группу, которая образует с азотом н-бутиламид. Электрофильное замещение осуществляют, например, с помощью тетрафторбората нитрония (NO2BF4). Взаимодействие в положении 5 осуществляют исходя из химии палладия (сочетание по Suzuki, Heck, Sonogashira). Положение 7 функционализируют в зависимости от заместителей, используемых для восстановлений, галогенирований, для введения брома, взаимодействия с помощью химии палладия (сочетание по Suzuki, Heck, Sonogashira), для введения арильных, гетероарильных, алкильных, алкенильных, алкинильных, ацетиленовых функциональных групп. Стадию снятия защиты с амида осуществляют в присутствии этаноламина при кипячении с обратным холодильником в течение недели в ДМФ. Это расщепление может также быть осуществлено с помощью хлорида олова в этаноле (R J Griffin, J. Chem. Soc. Perkin I 1992, 1811-1819) или метилата натрия в метаноле (Y.Furukawa, Chem. Pharm. Bull. 1968, 16, 1076) или любого другого алкоголята в соответствующем спирте. Снятие защиты в положении 3 позволяет получить группу NH2, которая может реагировать с группами, необходимыми для введения требуемых заместителей в положение 3, как описано на следующих страницах.
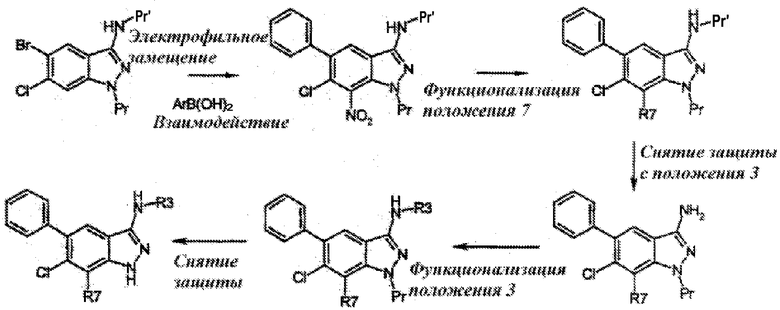
Соединения формулы II являются отправной точкой для получения большого разнообразия продуктов, получаемых реакцией первичной аминогруппы 3-аминоиндазола во всех обычных реакциях этой группы, таких как: алкилирование, ацилирование, реакции с карбонилсодержащими производными с последующим восстановлением, сульфонирование, превращение в мочевины или карбаматы, арилирование (реакции Castro или Buchwald) и т.д.
Аминовосстановление производных общей формулы (I), где R3 обозначает H, когда Pr обозначает триметилсилилэтоксиметил может быть осуществлено с помощью производных бора, таких как триацетоксиборгидрид натрия в дихлорметане в присутствии альдегида типа R1CHO, в условиях, описанных в Organic Reactions vol 59 1-714 (E. Baxter, A. Reitz) или с помощью других восстановителей, обычно используемых для восстановления иминов, с получением продуктов, в которых R3 обозначает (С1-С6)алкил, арил(С1-С6)алкил, гетероарил(С1-С6)алкил, гетероциклоалкил, циклоалкил, полициклоалкилы, причем эти радикалы могут быть в случае необходимости замещены одним или несколькими заместителями, выбранными из галогена, CN, NO2, NH2, OH, OR1, COOH, C(O)OR1, -О-C(O)R1, NR1R2, NHC(O)R1, C(O)NR1R2, SR1, S(O)R1, SO2R1, NHSO2R1, SO2NR1R2, C(S)NR1R2, NHC(S)R1, -О-SO2R1,
-SO2-O-R1, арила, гетероарила, формила, оксо-группы, трифторметила, трифтормитилсульфанила, трифторметокси, (С1-С6)алкила.
Реакции конденсации с производными общей формулы (I), где R3 обозначает H, на изоцианатах типа OCNR1 могут быть, в частности, осуществлены в тетрагидрофуране согласно примерам, описанным в Comprehensive Organic functionnal Group Transformations vol 6 (Katritzky, Meth-Cohn, Rees 1995), с получением продуктов, в которых R3 обозначает CONR1R2, CSNR1R2; R1, R2 независимо один от другого обозначают водород, (С1-С6)алкил, арил, алкенил, алкинил, гетероарил, которые сами могут быть 1 или несколькими заместителями, выбранными из галогена, (С1-С6)алкила, (С1-С6)алкокси, CN, NO2, NH2, OH, COOH, COOалкила, CONH2, формила, оксо-группы, трифторметила, трифторметокси.
Сульфонирование производных общей формулы (I), где R3 обозначает H, может быть осуществлено исходя из сульфонилхлорида типа R1SO2C1, в присутствии основания (в частности, третичных аминов, таких как триэтиламин, или ароматических оснований, таких как пиридин) в обычном растворителе, таком как, например, дихлорметан, с получением продуктов, в которых R3 обозначает SO2R1, а R1 обозначает водород, (С1-С6)алкил, арил, алкенил, алкинил, гетероарил, которые сами могут быть замещены одним или несколькими заместителями, выбранными из галогена, (С1-С6)алкила, (С1-С6)алкокси, CN, NO2, NH2, OH, COOH, COOалкила, CONH2, формила, оксо-группы, трифторметила, трифторметокси.
Соединения формулы (I) выделяют, и их можно очистить обычными известными способами, например, кристаллизацией, хроматографией или экстракцией.
Соединения формулы (I) могут быть в случае необходимости превращены в соли присоединения с неорганической или органической кислотой воздействием такой кислоты в органическом растворителе, таком как спирт, кетон, простой эфир или хлорированный растворитель. Эти соли также составляют часть изобретения.
В качестве примеров фармацевтически приемлемых солей можно назвать следующие соли: бензолсульфонат, гидробромид, гидрохлорид, цитрат, этансульфонат, фумарат, глюконат, йодат, малеат, изетионат, метансульфонат, метилен-бис-b-оксинафтоат, нитрат, оксалат, памоат, фосфат, салицилат, сукцинат, сульфат, тартрат, теофиллинацетат и п-толуолсульфонат.
Соединения формулы (I) являются ингибиторами киназы и в этом качестве пригодны для профилактики и лечения нейродегенеративных заболеваний, болезни Альцгеймера, Паркинсона, лобно-височной деменции, кортико-базальной дегенерации, болезни Пика, сосудисто-мозговых нарушений, травм головного и спинного мозга и периферический невропатий, ожирения, эссенциальной гипертонии, атеросклеротических сердечно-сосудистых заболеваний, синдрома поликистозных яичников, синдрома Х, иммунодефицита и рака.
Их активность устанавливали путем измерения ингибирования фосфорилирования белка tau в срезах коры головного мозга взрослой крысы.
Срезы коры толщиной 300 мкм получали от самцов крыс OFA (Iffa-Credo) в возрасте 8-10 недель, умерщвленных путем обезглавливания. Их инкубируют в 5 мл среды DMEM, содержащей пируват и глюкозу 4,5 г/л при 37°C в течение 40 мин. Затем срезы промывают 2 раза средой, распределяют в микропробирки (50 мкл в 500 мкл среды, включающей или не включающей тестируемое соединение) и инкубируют при 37°C при взбалтывании. Через два часа эксперимент останавливают центрифугированием. Срезы лизируют, разрушают ультразвуком и центрифугируют при 18300g в течение 15 мин при 4°C. Концентрацию белков в супернатанте определяют с помощью теста для количественного определения (ВСА Protein Assay, Pierce), основанного на способе Lowry.
Образцы, предварительно денатурированные 10 мин при 70°C, разделяют на вертикальном геле 4-12% Bis-Tris в присутствии буфера MOPS-SDS и электрохимически переносят на нитроцеллюлозную мембрану. Иммуномечение осуществляют с использованием моноклонального антитела AD2, которое специфически распознает фосфорилированные эпитопы Ser396/404 белка tau. Иммунореактивные белки становятся видимыми при добавлении второго антитела, направленного к IgG мыши и копулированного с пероксидазой, и хемолюминесцентного субстрата. Полученные ауторадиограммы количественно расшифровывают с помощью программы "GeneTools", Syngene (GeneGnome, Ozyme) для определения CI50.
Соединения формулы (I) обладают очень ценной активностью, в частности, некоторые соединения имеют CI50 менее 100 мкМ.
Следующие примеры иллюстрируют изобретение, не ограничивая его объема.
Условия анализа продуктов по LC/MS осуществляли на аппаратуре Waters Alliance 2695 в части LC и Waters-Micromass Platform II в части, касающейся массы.
Получение промежуточных продуктов:
6,7-дифтор-1H-индазол-3-амин:
к 0,46 см3 2,3,4-трифторбензонитрила в 10 см3 абсолютного этанола, добавляют 0,32 см3 моногидрата гидразина. Среду нагревают при 75°C в течение 17 часов, затем добавляют 10 см3 этилацетата, 5 см3 тетрагидрофурана и 5 см3 дистиллированной воды. Органическую фазу декантируют и промывают 10 см3 дистиллированной воды, затем 10 см3 насыщенного водного раствора хлорида натрия. Органическую фазу декантируют, высушивают над сульфатом магния, фильтруют и концентрируют досуха при пониженном давлении (2 кПа; 50°C). Полученный остаток очищают хроматографией под давлением аргона 50 кПа, на колонке с силикагелем (гранулометрия 40-60 мкм; диаметр 1,5 см), используя в качестве элюента смесь циклогексан-этилацетат (50/50 об.). Фракции, содержащие целевой продукт, объединяют, затем упаривают при пониженном давлении (2 кПа; 40°C); после высушивания (90 Па; 40°C) получают 100 мг 6,7-дифтор-1H-индазол-3-амина в виде твердого белого вещества с температурой плавления 183°C.
Спректр ЯМР 1H (300 МГц, (CD3)2SO d6, δ ppm): 5,57 (массив: 2H); 6,93 (м: 1H); 7,52 (ддд, J=8,5-4,5 и 1 Гц: 1H); 12,01 (массив: 1H).
N-(6,7-дифтор-1H-индазол-3-ил)бутанамид:
К 1 г 6,7-дифтор-1H-индазол-3-амина, описанного перед этим, в 15 см3 пиридина, после охлаждения до 3°C добавляют 0,61 см3 бутирилхлорида, затем оставляют при комнатной температуре в течение 76 часов. Реакционную среду концентрируют при пониженном давлении (2 кПа; 40°C) и остаток помещают в 25 см3 этилацетата и 25 см3 воды. Органическую фазу промывают 25 см3 дистиллированной воды, затем 25 см3 насыщенного водного раствора хлорида натрия. После высушивания над сульфатом магния, фильтрования и концентрирования при пониженном давлении (2 кПа; 40°C), полученный остаток очищают хроматографией под давлением аргона 50 кПа, на колонке с силикагелем (гранулометрия 40-60 мкм; диаметр 3 см), используя в качестве элюента смесь дихлорметанметанол (98/2 об.). Фракции, содержащие целевой продукт, объединяют затем упаривают при пониженном давлении (2 кПа; 40°С); после высушивания (90 Па; 40°С), получают 596 мг N-(6,7-дифтор-1Н-индазол-3-ил)бутанамида в виде твердого белого вещества с температурой плавления 191°С. Спектр ЯМР 1Н (300 МГц, (CD3)2SO d6, δ ppm): 0,97 (т, J=7,5 Гц: 3Н); 1,67 (м: 2Н); 2,40 (т, J=7 Гц: 2Н); 7,10 (м: 1Н); 7,63 (уш.дд, J=9 и 4,5 Гц: 1Н); 10,47 (уш.массив: 1Н); 13,35 (уш.массив: 1Н).
N-[6,7-дифтор-1-[[2-(триметилсилил)этокси]метил]-1Н-индазол-3-ил]бутанамид.
К 1,65 г 60% гидрида натрия в масле, в 50 см3 диметилформамида добавляют по каплям раствор 1,1 г N-(6,7-дифтор-1Н-индазол-3-ил)бутанамида, полученного в предыдущем примере, и 7,28 мл триметилсилилэтоксиметила в 180 см3 диметилформамида в течение 3 часов. Реакционную среду концентрируют досуха при пониженном давлении и помещают в 250 см3 этилацетата и 200 см3 воды; органическую фазу декантируют, промывают 150 см3 воды, высушивают над сульфатом магния, фильтруют и концентрируют досуха при пониженном давлении (2 кПа; 50°С). Сырой продукт очищают хроматографией под давлением аргона 50 кПа, на колонке с силикагелем (гранулометрия 40-60 мкм; диаметр 6 см), используя в качестве элюента смесь циклогексан-этилацетат (80/20 об.). Фракции, содержащие целевой продукт, объединяют и упаривают при пониженном давлении (2 кПа; 50°С), получая 7,3 г N-[6,7-дифтор-1-[[2-(триметилсилил)этокси]метил]-1Н-индазол-3-ил]бутанамида в форме желтого масла. Спектр ЯМР 1H (300 МГц, (CD3)2SO d6, δ ppm): -0,09 (с: 9H); 0,82 (т, J=8 Гц: 2H); 0,96 (т, J=7,5 Гц: 3H); 1,67 (м: 2H); 2,41 (т, J=7 Гц: 2H); 3,56 (т, J=8 Гц: 2H); 5,66 (с: 2H); 7,22 (ддд, J=11-9 и 7 Гц: 1H); 7,69 (уш.дд, J=9 и 4,5 Гц: 1H); 10,60 (массив: 1H). Масс-спектр: M=369.
N-[5-бром-6,7-дифтор-1-[[2-(триметилсилил)этокси]метил]-1H-индазол-3-ил]бутанамид
К 1 г N-[6,7-дифтор-1-[[2-(триметилсилил)этокси]метил]-1H-индазол-3-ил]бутанамида, описанного перед этим, в 30 см3 хлороформа, добавляют 0,87 см3 пиридина, затем добавляют 0,56 см3 брома и кипятят с обратным холодильником в течение ночи. Добавляют к реакционной среде 50 см3 дихлорметана и 50 см3 10% водного раствора тиосульфата натрия. После 10 мин перемешивания, нерастворимую часть удаляют фильтрованием через пористое стекло, а органическую фазу промывают 50 см3 воды и 50 см3 насыщенного раствора хлорида натрия. Органическую фазу декантируют, высушивают над сульфатом магния, фильтруют и концентрируют досуха при пониженном давлении (2 кПа; 45°C). Сырой продукт (1,1 г) очищают хроматографией под давлением аргона 50 кПа, на колонке с силикагелем (гранулометрия 40-60 мкм; диаметр 3 см), используя в качестве элюента смесь циклогексан-этилацетат (90/10 об.). Фракции, содержащие целевой продукт, объединяют и упаривают при пониженном давлении (2 кПа; 50°C). После высушивания (90 Па; 45°C), получают 230 мг N-[5-бром-6,7-дифтор-1-[[2-(триметилсилил)этокси]метил]-1H-индазол-3-ил]бутанамида в виде бесцветного масла. Спектр ЯМР 1H (300 МГц, (CD3)2SO d6, δ ppm): -0, 08 (с: 9H); 0,82 (т, J=8 Гц: 2H); 0,96 (т, J=7,5 Гц: 3H); 1,67 (м: 2H); 2,42 (т, J=7 Гц: 2H); 3,55 (т, J=8 Гц: 2H); 5,66 (с: 2H); 8,08 (дд, J=6 и 2 Гц: 1H); 10,72 (массив: 1H). Масс-спектр: M=447.
N-[6,7-дифтор-5-фенил-1-[[2-(триметилсилил)этокси]метил]-1H-индазол-3-ил]бутанамид
К 1,15 г N-[5-бром-6,7-дифтор-1-[[2-(триметилсилил)этокси]метил]-1H-индазол-3-ил]бутанамида, полученного в предыдущем примере, в 150 см3 диоксана, добавляют 469 мг фенилбороновой кислоты, 760 мг карбоната натрия в 30 см3 воды и 379 мг тетракис-трифенилфосфинпалладия и кипятят с обратным холодильником в течение 4 часов. Реакционную среду разбавляют 100 см3 этилацетата и 75 см3 воды и фильтруют через пористое стекло с целитом. Органическую фазу декантируют, промывают 75 см3 воды и 75 см3 насыщенного раствора хлорида натрия, высушивают над сульфатом магния, фильтруют и концентрируют досуха при пониженном давлении (2 кПа; 50°C), получая 2 г сырого продукта в виде черного масла. Сырой продукт очищают хроматографией под давлением аргона 50 кПа, на колонке с силикагелем (гранулометрия 40-60 мкм; диаметр 3,5 см), используя в качестве элюента смесь циклогексан-этилацетат (85/15 об.). Фракции, содержащие целевой продукт, объединяют, упаривают при пониженном давлении (2 кПа; 50°C) и высушивают (90 Па, 45°C); получая 1,1 г N-[6,7-дифтор-5-фенил-1-[[2-(триметилсилил)этокси]метил]-1H-индазол-3-ил]бутанамида в виде желтого масла. Спектр ЯМР 1H (300 МГц, (CD3)2SO d6, δ ppm): -0,05 (с: 9H); 0,84 (т, J=8 Гц: 2H); 0,95 (т, J=7,5 Гц: 3H); 1,66 (м: 2H); 2,43 (т, J=7 Гц: 2H); 3,59 (т, J=8 Гц: 2H); 5,69 (с: 2H); 7,40-7,65 (м: 5H); 7,82 (уш.д, J=7 Гц: 1H); 10,64 (массив: 1H). Масс-спектр: M=445.
N-[6,7-дифтор-5-фенил-1-[[2-(триметилсилил)этокси]метил]-1H-индазол-3-амин
К 1,6 г N-[6,7-дифтор-5-фенил-1-[[2-(триметилсилил)этокси]метил]-1H-индазол-3-ил]бутанамида, описанного перед этим, в 50 см3 диметилформамида добавляют 1,1 см3 этаноламина, затем 1,50 г карбоната калия и кипятят с обратным холодильником в течение недели. Реакционную среду концентрируют досуха при пониженном давлении и помещают в 150 см3 этилацетата и 75 см3 воды. Органическую фазу декантируют и промывают последовательно дважды 75 см3 воды и 50 см3 рассола. Органическую фазу высушивают над сульфатом магния, фильтруют, затем концентрируют досуха при пониженном давлении (2 кПа; 50°C). Полученное сырое масло очищают хроматографией под давлением аргона 50 кПа, на колонке с силикагелем (гранулометрия 40-60 мкм; диаметр 4 см), используя в качестве элюента смесь циклогексан-этилацетат (80/20 об.). Фракции, содержащие целевой продукт, объединяют и упаривают при пониженном давлении (2 кПа; 50°C). После высушивания (90 Па; 45°C), получают 0,32 г 6,7-дифтор-5-фенил-1-[[2-(триметилсилил)этокси]метил]-1H-индазол-3-амина.
6,7-дифтор-5-фенил-1H-индазол-3-амин:
К 661 мг 6,7-дифтор-5-фенил-1-[[2-(триметилсилил)этокси]метил]-1H-индазол-3-амина в 15 мл метанола добавляют 1,1 мл 2 н. HCl. Реакционную среду помещают в микроволновую печь на 3 мин при 140°C. После гидролиза с насыщенным раствором KH2PO4 и экстракции метиленхлоридом среду упаривают и хроматографируют на силикагеле (метиленхлорид/этилацетат), получая 314 мг 6,7-дифтор-5-фенил-1H-индазол-3-амина.
Пример 1: (6,7-дифтор-5-фенил-1H-индазол-3-ил)амид пиперидин-1-карбоновой кислоты
Стадия 1
К 387,8 мг соединения (6,7-дифтор-5-фенил-1-[[2-(триметилсилил)этокси]метил]-1H-индазол-3-амина в 8 мл метиленхлорида, последовательно добавляют 131 мкл пиридина и 154 мкл этилхлороформиата. После 75 мин реакцию завершают. После гидролиза, экстракции и упаривания получают 840 мг сырого этилового эфира (6,7-дифтор-5-фенил-1H-индазол-3-ил)карбаминовой кислоты.
Стадия 2
К 161 мг сырого этилового эфира (6,7-дифтор-5-фенил-1H-индазол-3-ил)карбаминовой кислоты в 2,5 мл трифтортолуола добавляют 184 мг пиперидина и проводят реакцию в микроволновой печи 20 мин при 200°C. После очистки препаративной LC/MS (ацетонитрил/буфер pH 9) получают 80 мг (6,7-дифтор-5-фенил-1-[[2-(триметилсилил)этокси]метил]-1H-индазол-3-ил)амида пиперидин-1-карбоновой кислоты.
Стадия 3
80 мг (6,7-дифтор-5-фенил-1-[[2-(триметилсилил)этокси]метил]-1H-индазол-3-ил)амида пиперидин-1-карбоновой кислоты в 2,5 мл метанола обрабатывают 0,82 мл 2 н. HCl в течение 1 ч при кипячении с обратным холодильником. После упаривания и очистки препаративной LC/MS (ацетонитрил/буфер pH 9) получают 11 мг (6,7-дифтор-5-фенил-1H-индазол-3-ил)амида пиперидин-1-карбоновой кислоты.
Масс-спектр: время удержания 3,99; 357=[M+H]+.
Спектр ЯМР 1H (300 МГц, (ДМСО-d6, δ ppm): 1,50 (м, 4H); 1,58 (м, 2H); 3,45 (м, 4H); 7,42 (м, 1H); 7,51 (м, 5H); 9,16 (с, 1H); 13,20 (с1, 1H)
Пример 2: (6,7-дифтор-5-фенил-1H-индазол-3-ил)амид пирролидин-1-карбоновой кислоты
Стадия 1
К 161 мг этилового эфира (6,7-дифтор-5-фенил-1H-индазол-3-ил)карбаминовой кислоты в 2,5 мл трифтортолуола добавляют 154 мг пирролидина и проводят реакцию в микроволновой печи 20 мин при 200°C. Очищают на колонке с силикагелем и получают 75 мг (6,7-дифтор-5-фенил-1-[[2-(триметилсилил)этокси]метил]-1H-индазол-3-ил)амида пирролидин-1-карбоновой кислоты.
Стадия 2
75 мг (6,7-дифтор-5-фенил-1-[[2-(триметилсилил)этокси]метил]-1H-индазол-3-ил)амида пирролидин-1-карбоновой кислоты в 3 мл метанола обрабатывают 0,82 мл 2 н. HCl 1 ч при кипячении с обратным холодильником. После упаривания и очистки препаративной LC/MS (ацетонитрил/буфер pH 9) получают 36 мг (6,7-дифтор-5-фенил-1H-индазол-3-ил)амида пирролидин-1-карбоновой кислоты.
Масс-спектр: время удержания 3,72 мин; 343=[M+H]+.
Спектр ЯМР 1H (300 МГц, (ДМСО-d6, δ ppm): 1,86 (м, 4H); 3,40 (м, 4H); 7,42 (м, 1H); 7,45-7,54 (м, 4H); 7,63 (д1, J=7 Гц, 1H); 8,84 (с, 1H); 13,20 (с1, 1H).
Пример 3: осуществляют согласно примеру 2 исходя из 3-(4-метилпиперазин-1-ил)пропиламина; получают 1-(6,7-Дифтор-5-фенил-1H-индазол-3-ил)-3-[3-(4-метилпиперазин-1-ил)пропил]мочевину.
Спектр ЯМР 1H (300 МГц, (ДМСО-d6, δ ppm): 1,92 (м, 2H); 2,82 (с, 3H); 3,01-3,75 (м, частично замаскированные, 12H); 7,43 (м, 1H); 7,47-7,56 (м, 4H); 7,71 (т, J=7 Гц, 1H); 8,05 (дд, J=1,5-7 Гц, 1H); 9,61 (с, 1H).
Масс-спектр: время удержания 2,57 мин; 429=[M+H]+.
Фармацевтические композиции по изобретению состоят из соединения формулы (I) или соли такого соединения, в чистом виде или в форме композиции, в которой оно комбинировано с любым другим фармацевтически совместимым продуктом, который может быть инертным или физиологически активным. Лекарственные средства согласно изобретению могут быть использованы перорально, парентерально, ректально или топически.
В качестве твердых композиций для перорального введения могут быть использованы таблетки, пилюли, порошки (желатиновые капсулы, облатки) или гранулы. В этих композициях действующее начало по изобретению смешано в токе аргона с одним или несколькими инертными разбавителями, такими как крахмал, целлюлоза, сахароза, лактоза или двуокись кремния. Эти композиции могут также содержать вещества, отличные от разбавителей, например, один или несколько лубрификаторов, таких как стеарат магния или тальк, краситель, агент для формирования оболочки (драже) или лак.
В качестве жидких композиций для перорального введения можно использовать фармацевтически приемлемые растворы, суспензии, эмульсии, сиропы и эликсиры, содержащие инертные разбавители, такие как вода, этанол, глицерин, растительные масла или парафиновое масло. Эти композиции могут содержать вещества, отличные от разбавителей, например, смачивающие продукты, подсластители, загустители, ароматизаторы или стабилизаторы.
Стерильные композиции для парентерального введения могут, предпочтительно, представлять собой водные или неводные растворы, суспензии или эмульсии. В качестве растворителя или носителя можно использовать воду, пропиленгликоль, полиэтиленгликоль, растительные масла, в частности. Оливковое масло, пригодные для инъекций сложные органические эфиры, например этилолеат, или другие подходящие органические растворители. Эти композиции могут также содержать адъюванты, в частности, смачивающие, изотонизирующие, эмульгирующие, диспергирующие и стабилизирующие агенты.
Стерилизацию можно осуществлять несколькими способами, например, асептической фильтрацией, введением в композицию стерилизующих агентов, облучением или нагреванием. Они также могут быть получены в форме твердых стерильных композиций, которые могут быть растворены в момент использования в стерильной воде или в любой другой стерильной среде для инъекций.
Композиции для ректального введения представляют собой суппозитории или ректальные капсулы, содержащие кроме действующего начала эксципиенты, такие как масло какао, полусинтетические глицериды или полиэтиленгликоли.
Композиции для топического нанесения могут представлять собой, например, кремы, лосьоны, примочки для глаз, жидкости для полоскания полости рта, капли для носа или аэрозоли.
Объектом изобретения являются соединения аминоиндазолов формулы (I) и их фармацевтически приемлемые соли, а также их применение для получения фармацевтичеких композиций, предназначенных для профилактики и лечения заболеваний, которые могут явиться результатом аномальной активности киназ, таких как, например, киназы, участвующие в механизме нейродегенеративных заболеваний, болезни Альцгеймера, Паркинсона, лобно-височной деменции, кортико-базальной дегенерации, болезни Пика, сосудисто-мозговых нарушений, травм головного и спинного мозга и периферический невропатий, ожирения, нарушений обмена веществ, диабета типа II, эссенциальной гипертонии, атеросклеротических сердечно-сосудистых заболеваний, синдрома поликистозных яичников, синдрома Х, иммунодефицита и рака.
В качестве аномальной активности киназ можно назвать, например PI3K, AkT, GSK3бета, CDK.
В терапии человека соединения по изобретению особенно полезны для лечения и/или профилактики нейродегенеративных заболеваний, болезни Альцгеймера, Паркинсона, лобно-височной деменции, кортико-базальной дегенерации, болезни Пика, сосудисто-мозговых нарушений, травм головного и спинного мозга и периферический невропатий, ожирения, нарушений обмена веществ, диабета типа II, эссенциальной гипертонии, атеросклеротических сердечно-сосудистых заболеваний, синдрома поликистозных яичников, синдрома Х, иммунодефицита и рака.
Дозы зависят от искомого эффекта, продолжительности лечения и используемого пути введения; они обычно составляют от 5 мг до 1000 мг в сутки при пероральном введении для взрослого человека при разовой дозе от 1 мг до 250 мг в расчете на действующее вещество.
В общем случае врач определяет подходящую дозу в зависимости от возраста, массы тела и всех прочих факторов, связанных с пациентом.
Следующие примеры иллюстрируют композиции по изобретению.
ПРИМЕР A
Получают обычными методами желатиновые капсулы, содержащие 50 мг действующего продукта, имеющие следующий состав:
- Соединение формулы (I) 50 мг
- Целлюлоза 18 мг
- Лактоза 55 мг
- Коллоидная двуокись кремния 1 мг
- Карбоксиметилкрахмал натрия 10 мг
- Тальк 10 мг
- Стеарат магния 1 мг.
ПРИМЕР B
Получают обычными методами таблетки, содержащие 50 мг действующего продукта, имеющие следующий состав:
- Соединение формулы (I) 50 мг
- Лактоза 104 мг
- Целлюлоза 40 мг
- Поливидон 10 мг
- Карбоксиметилкрахмал натрия 22 мг
- Тальк 10 мг
- Стеарат магния 2 мг
- Коллоидная двуокись кремния 2 мг
- Смесь гидроксиметилцеллюлозы, глицерина, оксида титана (72-3,5-24,5) qsp 1 таблетки, покрытой пленкой с конечной массой 245 мг.
ПРИМЕР C
Получают раствор для инъекций, содержащий 10 мг действующего продукта, имеющий следующий состав:
- Соединение формулы (I) 10 мг
- Бензойная кислота 80 мг
- Бензиловый спирт 0,06 мл
- Бензоат натрия 80 мг
- Этанол 95% 0,4 мл
- Гидроксид натрия 24 мг
- Пропиленгликоль 1,6 мл
- Вода qsp 4 мл.
Настоящее изобретение также относится к способу профилактики и лечения заболеваний, в механизме которых участвует фосфорилирование белка Tau, путем введения соединения формулы (I) и его фармацевтически приемлемых солей.
Настоящее изобретение относится к соединениям формулы (I) и их применению для лечения заболеваний, которые могут явиться результатом аномальной активности киназ. Соединения формулы (I) могут быть эффективны в отношении заболеваний, при которых наблюдается фосфорилирование белка Tau.
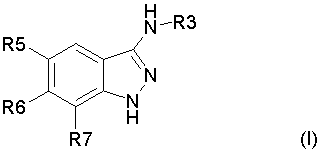
R3 обозначает CONR1R2, где R1 и R2 могут быть замещены гетероциклом;
R5, R6, R7 независимо один от другого выбраны из галогена и фенила;
R1, R2 независимо один от другого обозначают водород, (С1-С6)алкил или вместе с азотом группы CONR1R2 могут образовывать гетероцикл. Технический результат - получение новых биологически активных соединений. 4 н.п. и 2 з.п. ф-лы.
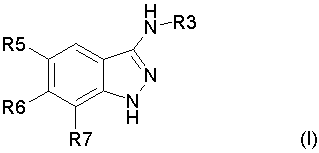
R3 обозначает CONR1R2, где R1 и R2 могут быть замещены гетероциклом, представляющим собой 5-6 членный цикл, содержащий от 1 до 2 гетероатомов, выбранных из кислорода, серы и азота;
R5, R6, R7 независимо один от другого выбраны из галогена и фенила;
R1, R2, независимо один от другого обозначают водород, (С1-С6)алкил или вместе с азотом группы CONR1R2 могут образовывать 5 или 6-членный цикл, содержащий от 1 до 2 гетероатомов, выбранных из О, S, N;
их смеси и фармацевтически приемлемые соли.
(6,7-дифтор-5-фенил-1Н-индазол-3-ил)амида пиперидин-1-карбоновой кислоты,
(6,7-дифтор-5-фенил-1Н-индазол-3-ил)амида пирролидин-1-карбоновой кислоты,
1-(6,7-дифтор-5-фенил-1Н-индазол-3-ил)-3-[3-(4-метилпиперазин-1-ил)пропил]мочевины
и их фармацевтически приемлемых солей.
6,7-дифтор-1Н-индазол-3-амина,
N-(6,7-дифтор-1Н-индазол-3-ил)бутанамида,
N-[6,7-дифтор-1-[[2-(триметилсилил)этокси]метил]-1Н-индазол-3-ил]бутанамида,
N-[5-бром-6,7-дифтор-1-[[2-(триметилсилил)этокси]метил]-1Н-индазол-3-ил]бутанамида,
N-[6,7-дифтор-5-фенил-1-[[2-(триметилсилил)этокси]метил]-1Н-индазол-3-ил]бутанамида,
6,7-дифтор-5-фенил-1-[[2-(триметилсилил)этокси]метил]-1Н-индазол-3-аминаи
6,7-дифтор-5-фенил-1Н-индазол-3-амина.
| КАРУСЕЛЬ "НЕОПОЗНАННЫЙ ЛЕТАЮЩИЙ ОБЪЕКТ (НЛО)" | 1991 |
|
RU2022601C1 |
| WO 03028720 A (PHARMACIA ITALIA SPA) 10.04.2003 | |||
| Способ получения производных 3-аминоиндазолкарбоновой кислоты | 1975 |
|
SU604487A3 |
Авторы
Даты
2008-11-27—Публикация
2003-09-03—Подача