ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к соединению, способному усиливать метаболизм алкоголя (этанола) и тем самым предупреждать неблагоприятные последствия от употребления алкоголя. Более точно, настоящее изобретение направлено на применение D-глицериновой кислоты или ее соли, или сложного эфира для изготовления фармацевтической композиции для усиления метаболизма алкоголя. Изобретение также направлено на способ усиления метаболизма алкоголя у субъекта, включающий введение эффективного количества одного или более соединений, выбранных из группы, состоящей из D-глицериновой кислоты и ее солей и сложных эфиров, субъекту, нуждающемуся в этом. Раскрыта фармацевтическая композиция для перорального или парентерального введения, содержащая указанные соединения.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Известно, что 5% этилового спирта, т.е. этанола (в дальнейшем также именуемый "алкоголь"), С2Н5ОН, проглоченного человеком, выделяется в неизменном виде, тогда как оставшиеся 95% распадаются до ацетальдегида (в дальнейшем АсА), СН3СНО, в клетках алкоголь-метаболизирующих тканей, в основном печени. Эта реакция (Реакция 1) протекает в цитоплазме гепатоцитов и катализируется местным ферментом алкогольдегидрогеназой (alcohol dehydrogenase, ADH). В реакции используется одна молекула кофермента никотинамид-адениндинуклеотида (nicotinamide-adeninedinucleotide, NAD) на каждую молекулу этанола:
(1)
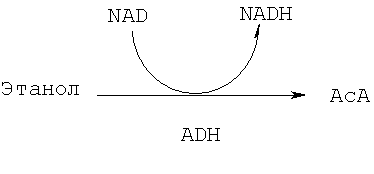
Во время реакции NAD и ADH образуют фермент-коферментный (ADH-NAD) комплекс с одновременным восстановлением NAD до NADH. NADH затем отщепляется, и ADH готова повторить реакцию путем связывания новой молекулы NAD. Клетка имеет ограниченную способность к окислению NADH обратно до NAD, что определяет максимальную скорость этой реакции. Нормальная печень метаболизирует этанол (алкоголь) со скоростью примерно 8 г/ч. Эта скорость не зависит от концентрации этанола в крови. Существует избыток фермента ADH для этой реакции.
Молекулы АсА, образующиеся из этанола, перемещаются в цитоплазматические органеллы, известные как митохондрии, где они окисляются до уксусной кислоты (СН3СООН) в реакции (Реакция 2), катализируемой ферментом альдегиддегидрогеназой (ALDH):
(2)
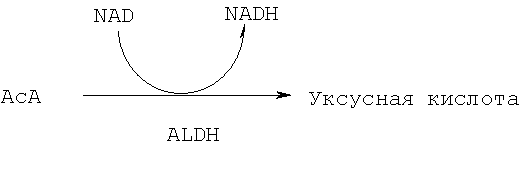
В этой реакции также одна молекула кофермента NAD восстанавливается до NADH. Как последний, так и NADH, предварительно накопленный в цитоплазме, снова окисляются до NAD в митохондриальной дыхательной цепи при максимальной активности этой системы. Максимальная активность митохондриальной дыхательной цепи зависит от общего уровня метаболизма в организме.
Вышеописанный процесс метаболизма этанола проиллюстрирован на Фиг.1.
Метаболически безвредная уксусная кислота, получаемая из этанола через АсА, окисляется до углекислого газа и воды в основном во внепеченочных тканях.
Способность клеток окислять NADH обратно до NAD превышается во время деградации этанола согласно Реакциям 1 и 2. В результате этого клетки накапливают избыток NADH по сравнению с NAD. Это изменение в равновесии клеточного окисления-восстановления, которое всегда имеет место в связи с метаболизмом этанола, является причиной ингибирования NAD-опосредованной ферментативной реакции, типичной для нормального метаболизма гепатоцита. Наиболее важной из этих ингибирующих систем является цикл лимонной кислоты. Положительное соотношение NADH/NAD, приводящее к ингибированию цикла лимонной кислоты, считают наиболее важной причиной развития алкогольного ожирения печени.
В нормальной печени 99% этанола, доставляемого кровотоком, метаболизируется до уксусной кислоты. Оставшийся 1% высвобождается в виде АсА в кровоток. Поэтому активность алкоголь-метаболизирующих тканей не вполне достаточна для окисления всего АсА, образующегося в Реакции 1, до уксусной кислоты согласно Реакции 2. Это очевидно, например, из факта, что венозная кровь, вытекающая из печени в процессе метаболизма этанола, несет 15 мкМ концентрацию АсА (Eriksson and Fukunaga, 1992).
Острая токсичность АсА (LD100=0,75 г/кг, мыши) в несколько раз выше по сравнению с токсичностью этанола (LD70=6,5 г/кг, мыши).
Как объяснено выше, во время употребления алкоголя примерно 1% АсА обычно "ускользает" от Реакции 2 в печени и поступает в кровоток со скоростью примерно 1 мг/мин (60 мг/ч). Если употребление алкоголя достаточно для поддержания концентрации алкоголя в крови в течение 24 часов (достаточно 200 г этанола, т.е. количества, содержащегося в 1/2 литра перегнанного спирта), то количество АсА, высвобожденного в кровоток, составляет в среднем 1,5 г. В качестве однократной дозы этого количества АсА было бы достаточно, чтобы убить 100 мышей, каждую массой 20 г.
Еще большие количества АсА, чем те, которые упомянуты выше, высвобождаются в кровоток в случае пониженной активности ALDH. Уменьшение в пределах 10% активности печеночной ALDH в три раза увеличивает количество АсА, попадающего в кровоток.
ALDH может ингибироваться некоторыми лекарствами, такими как дисульфирам (Antabuse®). У человека, которого лечат дисульфирамом, прием внутрь нескольких грамм алкоголя будет вызывать очень неприятные симптомы, длящиеся до нескольких часов. Эти симптомы включают головную боль и гиперемию. Одышка и тошнота также являются обычными, как тахикардия и гипотензия. Эти симптомы являются следствием накопления АсА в организме.
После интенсивного употребления алкоголя наступает похмельный синдром, хорошо известное следствие алкогольного опьянения. Человек, опасающийся похмельного синдрома, может попытаться продолжить употребление алкоголя. Тот факт, что попытки создать адекватное фармакологическое средство для лечения похмельного синдрома до сих пор были безуспешными, также может способствовать такому поведению. Похмельный синдром пытались смягчить витаминами и микроэлементами (см., например US 4496548). Основная часть симптомов похмельного синдрома может быть следствием токсических эффектов АсА.
Биохимическое и медицинское исследование предполагает основную роль АсА в развитии алкогольной зависимости. Эти выводы основаны на изменениях, которые АсА индуцирует в структурах мозговых нейротрансмиттеров. Было также обнаружено, что АсА ингибирует ферменты, вовлеченные в белковый синтез, и изменяет иммунологические свойства тканей. Благодаря таким механизмам АсА фактически может играть более существенную роль, чем этанол, в этиологии многих заболеваний, связанных с употреблением алкоголя, таких как поражение головного мозга и цирроз печени, а также в самом по себе патологическом влечении к алкоголю.
Как объяснено выше, понятно, что увеличение соотношения NADH/NAD, которое подавляет нормальный метаболизм в алкоголь-метаболизирующих тканях, и высвобождение и накопление АсА в системном кровообращении и, следовательно, в организме в целом, являются основными механизмами в развитии проблем со здоровьем, связанных с употреблением алкоголя.
В свете упомянутых фактов были использованы АсА-связывающие соединения для снижения количества АсА, высвобождающегося в системное кровообращение, и для уменьшения последствий такого высвобождения. Эти соединения включают в себя серосодержащие аминокислоты цистеин и метионин. Пероральное введение метионина экспериментальным субъектам во время употребления алкоголя давало 20%-ное снижение концентрации АсА в крови (Tabakoff et al., 1989). Однако следует принимать во внимание, что метионин-связанный АсА может позже расщепляться, тем самым уничтожая достигаемое небольшое преимущество. Кроме того, метионин и другие похожие вещества не влияют ни на скорость метаболизма этанола, ни на соотношение NADH/NAD.
Помимо упомянутых способов предполагается, что вредное для здоровья воздействие алкоголя может уменьшаться агентами, которые модифицируют скорость метаболизма этанола: И количество АсА, высвобождающегося из печени, и соотношение NADH/NAD могут быть уменьшены с помощью 4-метилпиразола (4-МР). Он представляет собой ингибитор ADH, который уменьшает скорость Реакции 1 (см. стр.1). В результате этого продуцирование АсА уменьшается, а при меньшем количестве субстрата Реакция 2 становится более эффективной, что делает возможным большее превращение АсА в уксусную кислоту. Вследствие пониженной общей активности этих реакций не наблюдается внутриклеточного накопления NADH. 4-МР полезен в особых обстоятельствах, требующих замедления метаболизма этанола, например в регуляции отравления метанолом. 4-МР не подходит для решения упомянутой проблемы накопления АсА. Из-за его замедляющего эффекта на элиминацию (удаление) алкоголя его невозможно использовать в связи с обычным употреблением алкоголя (риск алкогольного отравления).
Ускоряющий эффект фруктозы на скорость элиминации алкоголя известен давно (Crownover et al., 1986). Скорость элиминации может быть увеличена вплоть до 20%, но это требует больших доз (1-5 г/кг), которые следует принимать вместе с алкоголем. Были проведены испытания по предотвращению симптомов похмельного синдрома с помощью фруктозы без ощутимого преимущества. Было установлено, что ускорение метаболизма этанола с помощью фруктозы осуществляется специфически согласно Реакции 1. Этот способ увеличения скорости метаболизма этанола приводит к образованию соответствующего количества АсА, которое клетка неспособна метаболизировать до уксусной кислоты. Это отражается в виде соответствующего повышения концентрации АсА в крови, вытекающей из печени (Eriksson and Fukunaga, 1992).
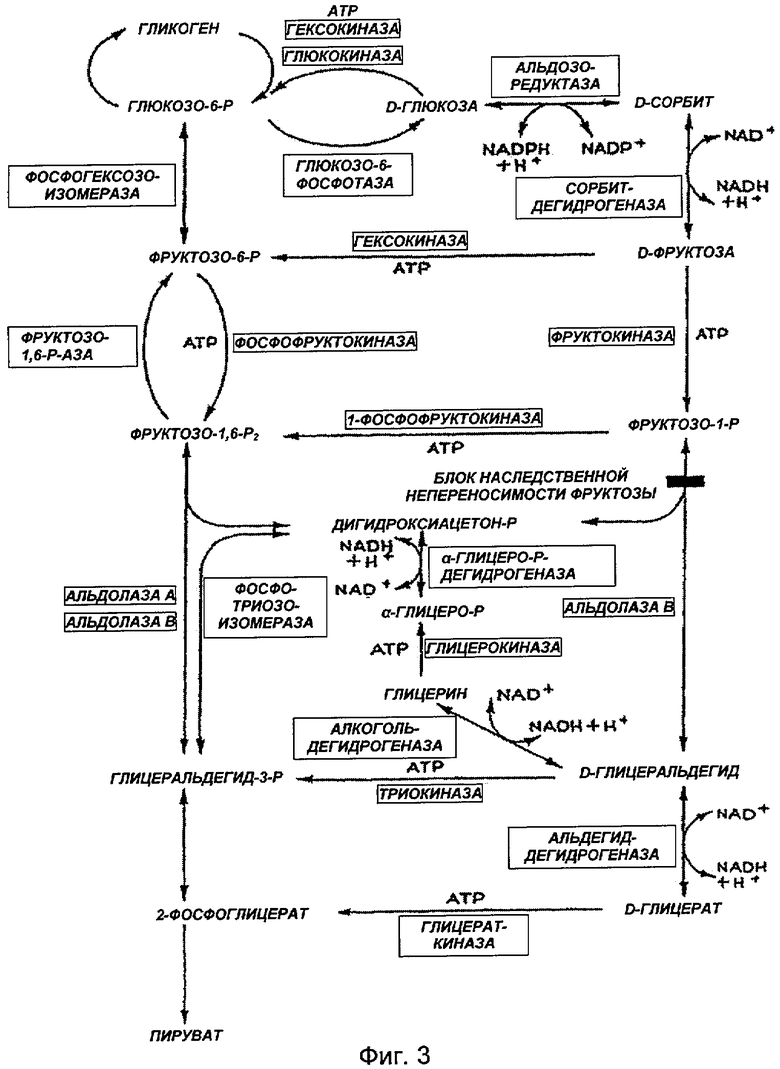
Также известно, что D-глицеральдегид (в дальнейшем D-GA; смотри Фиг.3, "Метаболизм фруктозы" (Harper et al., 1977)) - метаболит фруктозы - оказывает ускоряющий эффект на метаболизм этанола (Thieden et al., 1972). Эффект D-GA на метаболизм АсА аналогичен эффекту фруктозы в том, что ускоряющий эффект на метаболизм этанола осуществляется через Реакцию 1, а не через Реакцию 2. Поэтому аналогично фруктозе D-GA имеет тенденцию вызывать накопление АсА.
В патенте US 4450153 предложен раствор, с помощью которого концентрацию этанола в крови можно быстро уменьшить с использованием фермента алкогольоксидазы, выделенного из некоторых видов дрожжей. Указанный фермент расщепляет этанол до АсА во внеклеточном пространстве. Это приводит к образованию больших количеств АсА, попадающих в кровоток, и, следовательно, к риску АсА отравления.
Настоящее изобретение позволяет по существу преодолеть недостатки, описанные выше.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В настоящем изобретении предложено применение D-глицериновой кислоты или ее соли, или сложного эфира для изготовления фармацевтической композиции для усиления метаболизма алкоголя.
Кроме того, в изобретении предложен способ усиления метаболизма алкоголя у субъекта, включающий введение эффективного количества D-глицериновой кислоты или ее соли, или сложного эфира субъекту, нуждающемуся в этом.
В изобретении дополнительно предложена фармацевтическая композиция для перорального или парентерального введения для усиления метаболизма алкоголя, содержащая одно или более соединений, выбранных из группы, состоящей из D-глицериновой кислоты и ее солей и сложных эфиров.
Некоторые из предпочтительных форм осуществления изобретения описаны в независимых пунктах формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фиг.1 иллюстрирует метаболизм алкоголя.
Фиг.2 иллюстрирует метаболизм алкоголя в присутствии D-глицериновой кислоты (D-GLAC).
Фиг.3 иллюстрирует метаболизм фруктозы.
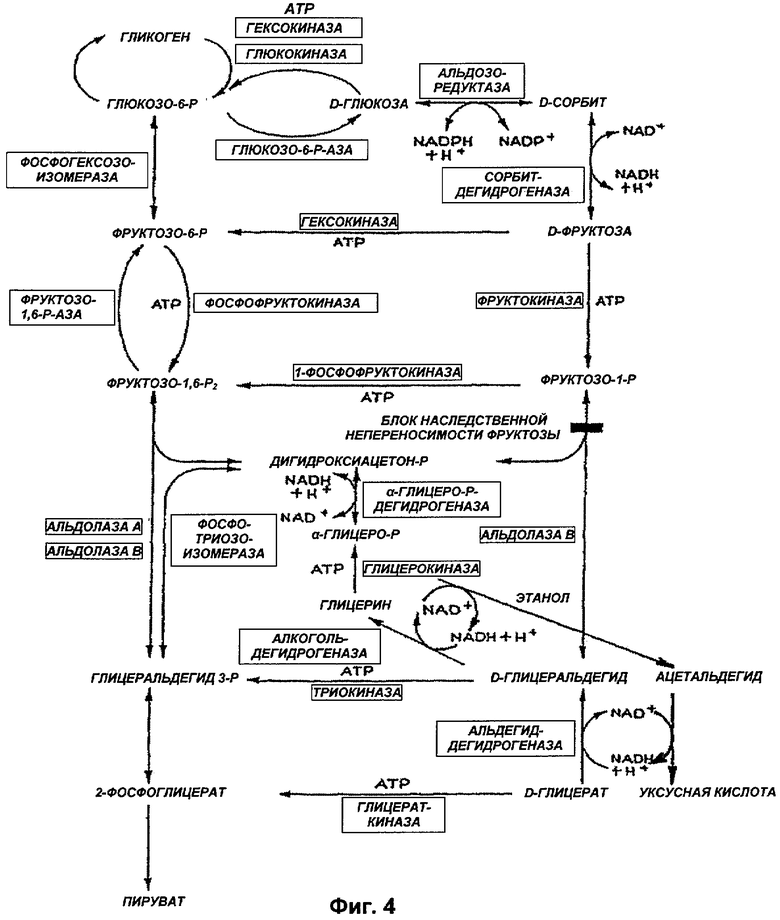
Фиг. 4 иллюстрирует принцип настоящего изобретения.
СВЕДЕНИЯ, ПОДТВЕРЖДАЮЩИЕ ВОЗМОЖНОСТЬ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Действие и сущность изобретения описаны ниже.
Согласно изобретению, D-глицериновую кислоту (в дальнейшем D-GLAC), т.е. правовращающий оптический изомер глицериновой кислоты, используют для усиления метаболизма алкоголя в организме. Общеизвестно в физиологии и биохимии, что организм способен физиологически утилизировать только один изомер органического соединения, которое содержит асимметричные атомы углерода и, следовательно, существует в виде как D-, так и L-изомеров. Другой изомер является физиологически инертным. Вследствие этого физиологически активный изомер соединения и его физиологически инертный двойник имеют различные метаболические пути. Это верно и для глицериновой кислоты. Метаболический путь и, следовательно, физиологические характеристики L-глицериновой кислоты, т.е. изомера глицериновой кислоты, который вращает плоскость поляризованного света влево, совершенно отличаются от таковых для D-GLAC - объекта настоящего изобретения (см., например, Bonham et al., 1977). Поэтому D-GLAC и L-глицериновая кислота также различаются по их фармакологическим свойствам.
"Глицериновая кислота" упоминается как компонент фармацевтических композиций, описанных, например, в документах патент US 4380549, европейский патент ЕР 775486 и международная публикация WO 96/11572. Терапевтическое показание для каждой из этих композиций, описанных в указанных документах, отличается от такового в настоящем изобретении. Кроме того, указанные документы не упоминают или не обеспечивают основу для заключения о том, какие из оптических изомеров глицериновой кислоты - D-GLAC или L-глицериновая кислота - представляют собой активную субстанцию в конкретном изобретении. Это утверждение является справедливым в силу того, что, как указано выше, каждый из двух оптических изомеров глицериновой кислоты имеет свои собственные фармакологические свойства. Европейский патент ЕР 508324 раскрывает композиции для местного применения, содержащие 2-гидроксикарбоновые кислоты, включая глицериновую кислоту, для облегчения симптомов старения кожи. Lesova с соавт. (2001) раскрывают смесь сложных эфиров глицериновой кислоты, продуцируемую Penicillium funiculosum. Смесь вела себя как неконкурентный ингибитор трипсина. Известно, что Penicillia продуцирует D-GLAC из DL-формы. Однако ни одна из приведенных ссылок не показывает или не предполагает эффекта усиления метаболизма алкоголя в результате введения D-GLAC и, следовательно, ее перорального или парентерального применения.
D-GLAC представляет собой сиропоподобное соединение со слабокислотными свойствами, которое легко растворяется в воде и спирте и может быть получено путем окисления глицерина. D-GLAC может быть высвобождено из ее имеющейся в продаже кальциевой соли путем простой обработки разбавленной соляной кислотой. Будучи органической кислотой D-GLAC также способна образовывать сложные эфиры. D-GLAC может быть высвобождена из ее сложных эфиров, например, с помощью эстеразных ферментов. В организме человека эти ферменты присутствуют в стенке тонкой кишки, где они расщепляют этерифицированные питательные вещества до формы, которая может всасываться из желудочно-кишечного тракта.
D-GLAC производится в процессе нормального метаболизма сахара в организме человека. Запас энергии, который организм способен утилизировать, составляет 17 кДж/г. Для цели, связанной с настоящим изобретением, D-GLAC можно предпочтительно вводить перорально в форме кислоты или ее фармацевтически, или физиологически приемлемой соли, или сложного эфира. Возможные лекарственные формы включают сироп, порошок, таблетки, капсулы и т.п. Ее можно вводить также в алкогольных или других напитках, или в пищевом продукте, или в качестве компонента одного из них.
На Фиг.3 показано, что D-GLAC образуется из D-GA в реакции, катализируемой ALDH, а D-GA в свою очередь образуется из глицерина в реакции, катализируемой ADH. Обе реакции протекают в алкоголь-метаболизирующих тканях, в частности в печени.
Структурные формулы глицерина (a), D-GA (b) и D-GLAC (с) представлены ниже:
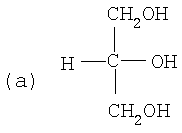
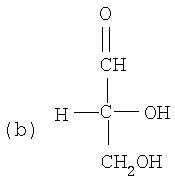
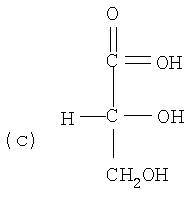
Глицерин метаболизируется до D-GA в реакции, катализируемой ADH, следующим образом (Реакция З):
(3)
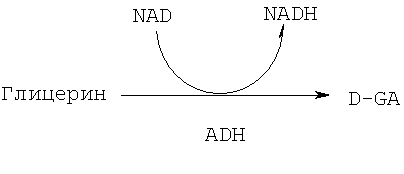
В этой реакции используется эквимолярное количество NAD, которое восстанавливается до NADH.
D-GA метаболизируется до D-GLAC в реакции, катализируемой ALDH, следующим образом (Реакция 4):
(4)
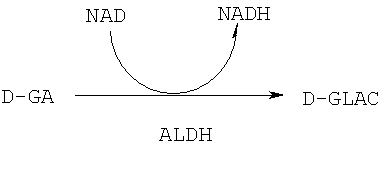
В этой реакции также используется кофермент NAD, который превращается в NADH.
На Фиг.3 показано, что и Реакция 3, и Реакция 4 представляют собой равновесные реакции, другими словами, они могут протекать также в противоположном направлении.
При осуществлении изобретения путем введения D-GLAC людям или другим млекопитающим это соединение транспортируется кровотоком в алкоголь-метаболизирующие ткани. Поскольку D-GLAC не имеет других метаболических путей, и его вводят в количествах, значительно превышающих физиологические количества, оно будет подвергаться превращению в D-GA в Реакции 5, которая представляет собой обратную реакцию для Реакции 4:
(5)
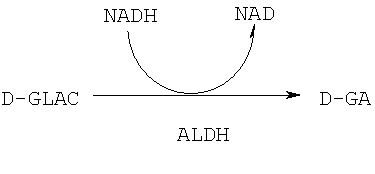
В этой реакции используется кофермент NADH, который окисляется до NAD.
Поскольку количество вводимой D-GLAC значительно превышает физиологическое количество, то количество необходимого NADH также превышает физиологические потребности.
Ситуация, когда существует достаточный запас NADH, возникает, когда рассматриваемая клетка метаболизирует помимо D-GLAC также этанол согласно Реакции 2. Вместе эти реакции могут быть описаны следующим образом (Реакция 6):
(6)
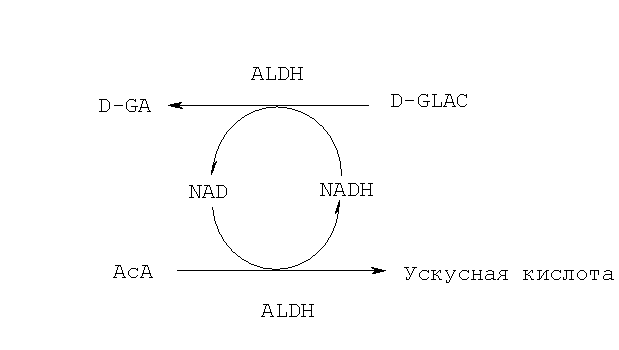
Два субстрата АсА и D-GLAC не конкурируют за общий фермент ALDH, поскольку АсА способен использовать этот фермент только тогда, когда последний образует комплекс с NAD, a D-GLAC способна использовать этот фермент только в виде комплекса ALDH-NADH. Когда Реакция 2 протекает в отсутствие D-GLAC, то некоторое количество фермента будет присутствовать в виде комплекса ALDH-NADH, который не может быть использован для окисления АсА до уксусной кислоты. При введении D-GLAC в качестве второго субстрата NADH, связанный с ферментом, будет немедленно окисляться до NAD вместе с превращением D-GLAC в D-GA. NAD, образующийся таким образом, доступен для использования в Реакции 2. Таким образом, ферментативная активность ALDH в отношении АсА будет увеличиваться, и выход Реакции 2 будет улучшаться по молярному количеству, соответствующему употреблению D-GLAC.
Это обнаруживает преимущество подхода, используемого в настоящем изобретении.
Несмотря на ускорение Реакции 2 никакого избытка NADH не возникает, поскольку NADH одновременно используется для превращения D-GLAC в D-GA (Реакция 5).
D-GA, образующийся таким образом, затем метаболизируется либо до D-глицеральдегид-3-фосфата в реакции, катализируемой ферментом триокиназой, либо до глицерина в реакции, катализируемой ADH (ср. Фиг.3). Первый путь является однонаправленным и требует энергии одной молекулы аденозинтрифосфата.
Второй метаболический альтернативный путь, приводящий к образованию глицерина, использует NADH в качестве кофермента согласно Реакции 7:
(7)
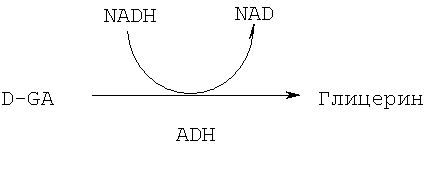
D-GA направляется на этот метаболический путь (который представляет собой обратную реакцию Реакции 3) путем окисления этанола до АсА согласно Реакции 1, которая дает избыток NADH. Общая реакция может быть описана следующим образом (Реакция 8):
(8)
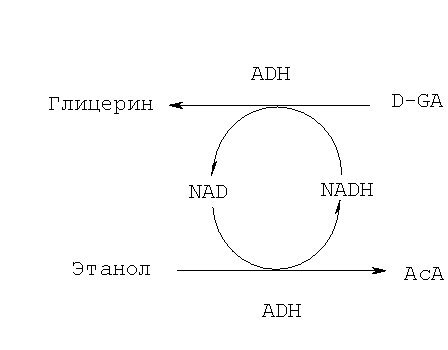
Как показано на Фиг.3, глицерин затем метаболизируется до α-глицерофосфата в АТР-опосредованной реакции и затем через различные промежуточные стадии до глюкозы.
Реакция 8 показывает, что превращение этанола в АсА ускоряется в таком же молярном соотношении, в каком образуется глицерин - снова без продуцирования какого-либо избытка NADH. Таким образом, эта ситуация похожа на Реакцию 6, где D-GLAC ускоряет превращение АсА в уксусную кислоту, хотя и с количественным различием: количество D-GA, т.е. субстрата, который поступает в Реакцию 8 и ускоряет превращение этанола в АсА, меньше, чем количество D-GLAC, соответствующего субстрата для Реакции 6. Это происходит благодаря некоторому количеству образующегося D-GA, направляемого на второй путь. В качестве итога: активность Реакции 1 увеличивается, но активность Реакции 2 увеличивается еще больше.
Когда скорость элиминации алкоголя из организма увеличивается благодаря введению D-GLAC согласно настоящему изобретению, то ускорение окисления этанола осуществляется параллельно, благодаря усилению окисления АсА до уксусной кислоты. Последнее соединение является метаболически безвредным и затем распадается на углекислый газ и воду. Поэтому в соответствии с изобретением метаболизм алкоголя усиливается до известной степени, что делает возможным "более полное" сгорание этанола в организме, то есть сгорание этанола с меньшими неблагоприятными для здоровья последствиями, чем это может быть при других обстоятельствах.
Один лишь факт, что скорость элиминации алкоголя, введенного в организм, увеличивается, является важным преимуществом, предоставляемым настоящим изобретением.
Принцип изобретения проиллюстрирован на Фиг.4 и схематически показан на Фиг.2.
В соответствии с изобретением, D-GLAC предпочтительно вводят перорально в ее кислотной и/или солевой, и/или сложноэфирной форме. Общеизвестно, что соли слабых кислот, таких как D-GLAC, превращаются в кислотную форму в кислом окружении, преобладающем в желудке, и, кроме того, что сложноэфирные связи сложных эфиров этих соединений разрушаются в результате воздействия эстераз, присутствующих в стенке кишечника, высвобождая при этом исходное соединение, в нашем случае D-GLAC. Кислотная форма D-GLAC напоминает сироп по консистенции и таким образом подходит для перорального введения в виде сиропа, раствора или в капсулах. Кроме этих лекарственных форм соли и сложные эфиры D-GLAC подходят для перорального приема в форме порошков или таблеток. При необходимости в этих препаратах могут быть использованы общепринятые фармацевтические или физиологические наполнители. Подходящая доза D-GLAC в кислотной, солевой или сложноэфирной форме в связи с приемом алкоголя составляет от 1 до 2 г в час с помощью любого из упомянутых способов введения до тех пор, пока алкоголь присутствует в кровотоке. Фармацевтически приемлемые кислотные и солевые формы D-GLAC подходят также для парентерального введения. Такое введение обычно предпочтительно в случаях тяжелого алкогольного опьянения. В этих случаях предпочтительным является раствор Рингера или 5%-ный раствор глюкозы, содержащий D-GLAC в кислотной форме, нейтрализующейся в растворе солью D-GLAC. При этом подходящее общее количество D-GLAC и ее соли может составлять 30 г/л, что дает от 3 до 15 г D-GLAC в час при скорости введения 100-500 мл/ч.
Настоящее изобретение проиллюстрировано следующими не ограничивающими примерами.
ОПИСАНИЕ ПРИМЕРОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Пример 1
Образование уксусной кислоты из АсА, опосредованное NAD, образующимся при восстановлении D-GLAC, как описано в Реакции 6 выше, было продемонстрировано впервые.
320 мг (3 ммоль) D-GLAC, высвобожденного из коммерчески полученной гемикальциевой соли (Sigma-Aldrich) серной кислотой, добавляли в 2 мл воды к 30 мл 0,25 мМ калий-дигидрофосфатного буферного раствора (рН 6,865). Непосредственно перед этим 13,2 мг (0,3 ммоль) АсА, 2 мг (5 единиц) лиофилизированной ALDH и 210 мг (3 ммоль) NADH было добавлено к буферу на льду. Раствор перемешивали в течение 6 часов. Его кислотность затем увеличивали до рН 3 путем добавления 1 М раствора фосфорной кислоты (Н3PO4) по одной капле за раз. Затем этот раствор подвергали непрерывной эфирной экстракции в течение 6 часов, после чего его концентрировали до 5 мл и анализировали с помощью газовой хроматографии.
Использовали газовый хроматограф Micromat, снабженный колонкой и пламенно-ионизационным детектором. Колонка имела размеры 30 см × 0,32 см в.д. PE-Wax(N 931-6413), заполненная полиэтиленгликолем (ПЭГ) (Perkin Elmer). Гелий использовали в качестве газа-носителя. Температуру инжектора устанавливали при 200°С, а температуру детектора при 240°С.
Печь была запрограммирована таким образом, что колонка работала при 40°С в течение первых 15 минут после введения образца, и температуру колонки затем увеличивали на 15°С в минуту до конечной температуры 230°С, которую затем поддерживали в течение последних 10 минут.
Анализ хроматограмм показал, что образовывалась уксусная кислота, причем время ее удерживания составляло 783 с. Этот результат проверяли, используя в качестве контроля коммерческий препарат уксусной кислоты (Baker Analyzed Reagent).
Пример 2
Эффект D-GLAC на метаболизм этанола исследовали на 80 взрослых самцах крыс весом 210-440 г (не предрасположенные к употреблению алкоголя крысы линии ANA, Alcohol Research Unit, National Public Health Institute, Helsinki). 40 животных голодали в течение 12 часов до эксперимента, и 40 животных кормили как обычно.
В этом эксперименте каждая крыса получала внутрибрюшинно опьяняющую разовую дозу этанола (1,2 г/кг, 10% мас./об.) в физиологическом растворе.
Помимо этанола половина крыс (20 голодных и 20 неголодных крыс) получала гемикальциевую соль D-GLAC (Sigma-Aldrich), растворенную в указанной дозе этанола (0,5 г/кг, 5% мас./об.).
Образцы крови отбирали из подкожной вены хвоста каждой крысы до, через 1 час и через 2 часа после введения этанола и D-GLAC. Образцы крови затем анализировали с помощью газовой хроматографии в свободном пространстве над продуктом (headspace gas chromatography).
Результаты представлены в Таблице 1.
3сравнение между глицерат + и глицерат -;
4сравнение между натощак + и натощак-; *Р<0,05; ***Р<0,001
Среди голодных и неголодных крыс группа, которая получала D-GLAC, имела в среднем на 20% меньшую концентрацию этанола в крови, чем соответствующая контрольная группа, которая не получала D-GLAC, но получала такое же количество этанола, что и соответствующая D-GLAC группа.
Можно сделать вывод, что D-GLAC существенно усиливала метаболизм этанола.
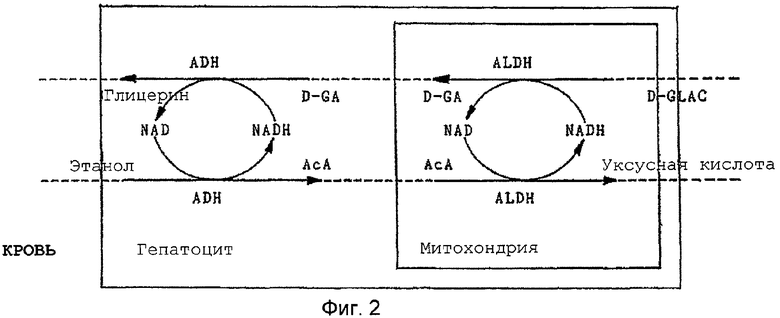
Предложены применение D-глицериновой кислоты и/или ее соли и сложного эфира для изготовления фармацевтического препарата для усиления метаболизма алкоголя и соответствующий способ усиления метаболизма алкоголя. D-глицериновая кислота усиливает метаболизм алкоголя и тем самым предотвращает неблагоприятные последствия от употребления алкоголя. D-глицериновую кислоту вводят одновременно с алкоголем, чтобы ускорить элиминацию алкоголя из организма. D-глицериновая кислота превращается в D-глицеральдегид и затем в глицерин в реакциях, катализируемых NADH-альдегиддегидрогеназным и NADH-алкогольдегидрогеназным комплексами, которые продуцируются в избытке во время окисления этанола в клетках алкоголь-метаболизирующих тканей. В этих реакциях NADH-комплексы становятся NAD-альдегиддегидрогеназным и NAD-алкогольдегидрогеназным комплексами. Эти комплексы в свою очередь ускоряют окисление этанола, которое происходит параллельно благодаря усилению окисления ацетальдегида до метаболически безвредной уксусной кислоты. 2 н. и 4 з.п. ф-лы, 4 ил., 1 табл.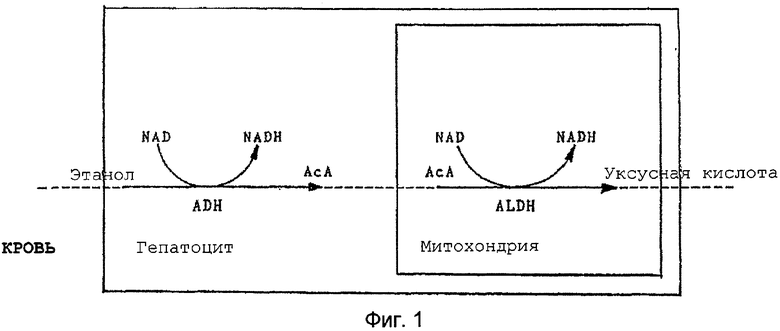
| US 4450153 А 22.05,1984 | |||
| СПОСОБ КОРРЕКЦИИ МЕТАБОЛИЧЕСКОЙ ЗАВИСИМОСТИ ОТ АЛКОГОЛЯ И СРЕДСТВО Л.Е.ПАНИНА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1991 |
|
RU2072239C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ПРОТИВОАЛКОГОЛЬНОГО, СТИМУЛИРУЮЩЕГО ЭНЕРГЕТИЧЕСКИЙ ОБМЕН, КИСЛОТООБРАЗУЮЩУЮ И СЕКРЕТОРНУЮ ФУНКЦИЮ СЛИЗИСТОЙ ЖЕЛУДКА, РАДИОПРОТЕКТОРНОГО И ПРОТИВОХОЛЕРНОГО ДЕЙСТВИЯ, СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ АЛКОГОЛЬНОГО ОПЬЯНЕНИЯ И АЛКОГОЛЬНОГО АБСТИНЕНТНОГО СИНДРОМА, СПОСОБ СТИМУЛЯЦИИ ЭНЕРГЕТИЧЕСКОГО ОБМЕНА, СПОСОБ СТИМУЛЯЦИИ И ДИАГНОСТИКИ КИСЛОТООБРАЗУЮЩЕЙ И СЕКРЕТОРНОЙ ФУНКЦИИ СЛИЗИСТОЙ ЖЕЛУДКА И СПОСОБ ЗАЩИТЫ ОТ РАДИАЦИОННОГО ПОРАЖЕНИЯ ТЕПЛОКРОВНЫХ ЖИВОТНЫХ | 1993 |
|
RU2039556C1 |
| Керамическая масса для изготовлениялитейных стержней | 1973 |
|
SU508324A1 |
| Сигнализатор объемного электрического сопротивления материалов | 1978 |
|
SU721728A1 |
| МИХАЙЛОВ И.Б | |||
| Настольная книга по клинической фармакологии | |||
| - СПб.: Фолиант, 2001, с.326-327 | |||
| реферат Entrez PubMed: Lesova К | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2009-01-20—Публикация
2003-10-13—Подача