Изобретение относится к медицине, в частности к способам диагностики и наборам для диагностики инфекционных заболеваний, а именно иерсиниоза.
Проблема диагностики иерсиниоза, острой кишечной инфекции, вызываемой патогенной для человека Yersinia enterocolitica, в настоящее время остается актуальной для практического здравоохранения. Широкое распространение и выраженное разнообразие клинических вариантов иерсиниоза определяют трудности распознавания данного заболевания и значительную частоту диагностических ошибок. Иерсиниоз имеет сходную клиническую картину с острым гепатитом, ревматизмом, аппендицитом, болезнью Крона, острым гастроэнтероколитом, нодозной эритемой и т.д. [1-3]. Кроме того, доказана этиологическая роль иерсиний в развитии вторично-очаговых форм заболеваний (иммунопатологий), связанных с поражением сердечно-сосудистой и нервной систем, опорно-двигательного аппарата, а также желудочно-кишечного тракта и мочевыводящих путей [4, 5]. В последние годы зафиксирован неуклонный подъем заболеваемости иерсиниозными инфекциями населения на всей территории Российской Федерации. Наиболее частой причиной возникновения кишечного иерсиниоза у людей являются Y. enterocolitica серотипов 0:3 и 0:9. Однако отмечается рост заболевания, вызванного Y. enterocolitica серотипов 0:5, 0:6, 0:7, 0:8 и др. [3]. Кроме того, установлено, что у так называемого «здорового» человека обнаруживаются маркеры иерсиний, вызывающие длительное маломанифестное заболевание, или бессимптомное носительство, которые могут привести к серьезным осложнениям [3].
Установление природы иерсиниозной инфекции возможно только в результате проведения комплексной клинико-лабораторной диагностики с применением специфических методов анализа.
Лабораторная диагностика иерсиниоза осуществляется с помощью бактериологических и серологических методов [6-15]. В диагностике инфекционных заболеваний бактериологическое подтверждение играет неоспоримую роль [6]. Однако, учитывая неоднозначность результатов, трудоемкость и длительность бактериологического анализа, особое значение в диагностике иерсиниоза приобретают ускоренные методы выявления Y. enterocolitica, среди которых серологическая идентификация заболевания играет доминирующую роль.
Серологических методов диагностики иерсиниоза описано достаточно много [7-15]. Существующие методы серодиагностики иерсиниоза основаны на определении бактериального антигена (первая группа методов) в различных биологических жидкостях (кровь, слюна, моча, копрофильтрат) и на определении антител в сыворотке крови пациента к антигенам возбудителя (вторая группа методов).
К первой группе серологических методов диагностики иерсиниоза относятся реакция коагглютинации (РКоА) [7] и полимеразная цепная реакция (ПЦР) [8]. Использование РКоА эффективно в ранние сроки заболевания (до 90% положительных результатов на 1-й неделе заболевания), но малоэффективно при обследовании пациентов на 2-4-й неделях болезни, в течение которых процент обращений в лечебные учреждения остается достаточно высоким. ПЦР, являясь высокотехнологичным методом диагностики иерсиниоза, не нашла широкого практического использования в виду ее высокой стоимости и низкой технической оснащенности клинических лабораторий.
Из второй группы серологических методов, основанных на определении антител в сыворотке крови больных, первой стала применяться реакция агглютинации (РА) с O-диагностикумами (взвесь бактерий, убитых кипячением или автоклавированием) и с ОН-диагностикумами (взвесь живых или обработанных формалином бактерий) [9]. Недостатком метода является типоспецифичность реакции: для постановки РА необходимы эталонные штаммы Y. enterocolitica наиболее распространенных серовариантов (0:3, 0:9, 0:4.3, 0:5.27 и др.), что значительно снижает диагностические возможности данного метода. Кроме того, эти диагностикумы дают положительные реакции с гетерологичными сыворотками против энтеробактерий и бруцеллезной сывороткой. К недостаткам метода относится ретроспективность результатов диагностики, поскольку антитела в диагностических титрах выявляются, как правило, на 2-4-й неделях заболевания. Описан усовершенствованный вариант РА, латексный диагностикум, основанный на использовании полистирольных микросфер, окрашенных различными красителями, соответствующими определенной специфичности иммобилизованных на них O-антигенов Y. enterocolitica различных серотипов [10]. Данный метод характеризуется также низкой специфичностью и результативностью в ранние сроки заболевания (1-ая неделя), что снижает возможности серологической диагностики. Кроме того, способ трудоемок в исполнении и требует значительных затрат времени и средств как на получение О-антигенов Y. enterocolitica разных серовариантов, так и последующей их иммобилизации на поверхности полистирольных микросфер.
Широкое распространение получила реакция непрямой гемагглютинации (РНГА), которая используется практически во всех клинических лабораториях. Метод основан на определении титра антител в сыворотках крови больных с использованием в качестве антигена липополисахарида (ЛПС) из Y. enterocolitica 0:3 и 0:9 серологических вариантов [11]. Недостатком РНГА является низкая специфичность, поскольку реакция типоспецифическая, что не позволяет диагностировать заболевание, вызванное другими серовариантами Y. enterocolitica. Кроме того, титры антител достигают диагностически значимых величин в более поздние сроки заболевания, т.е. на 15-20 сутки, что снижает эффективность диагностики иерсиниоза в ранние сроки заболевания.
В последние годы для серодиагностики иерсиниоза широко применяется иммуноферментный анализ (ИФА) с использованием антигенов различной природы.
Известен способ диагностики иерсиниоза, основанный на использовании в ИФА типоспецифического антигена - липополисахарида (ЛПС) из Y. enterocolitica 0:3 серотипа [12]. Недостатком этого способа является низкая специфичность и чувствительность при верификации иерсиниоза, обусловленного другими серотипами (0:5, 0:6, 0:7, 0:8, 0:9) Y. enterocolitica.
Разработан способ диагностики иерсиниозов (иерсиниоза и псевдотуберкулеза), в котором используется протеиновый антиген, свободно секретируемый в культуральную среду патогенными иерсиниями, с последующим выявлением антител в сыворотках крови больных с помощью ИФА [13]. Способ не позволяет достоверно диагностировать иерсиниоз, вызванный Y. enterocolitica серотипа 0:9 в виду общей антигенной детерминанты ЛПС (4,6-дезокси-4-формамидо-L-D-маннопиранозила), присущей данному серотипу Y. enterocolitica и некоторым видам бруцелл.
Богаутдиновым и соавторами предложен способ иммуноферментной диагностики иерсиниоза, основанный на использовании инактивированного корпускулярного антигена из Y. enterocolitica 0:3 сероварианта [14]. Данный способ следующие этапы:
1) посадка антигена на полистироловый планшет, в качестве антигена используется инактивированный корпускулярный антиген из Y. enterocolitica 0:3 сероварианта;
2) отмывка планшеты;
3) нанесение исследуемой сыворотки, рабочее разведение сыворотки 1:400;
4) отмывка планшеты;
5) нанесение конъюгата;
6) отмывка планшеты;
7) нанесение субстратной смеси;
8) регистрация результатов реакции.
Набор для осуществления известного способа диагностики иерсиниоза с использованием инактивированного корпускулярного антигена из Y. enterocolitica 0:3 сероварианта представляет собой набор реагентов для выявления антител к антигену Y. enterocolitica методом ИФА. В состав набора входят следующие реагенты:
планшет с иммобилизованным антигеном - ЛПС из Y. enterocolitica 0:3 серотипа;
раствор для отмывки планшета и для разведения сыворотки крови;
инактивирующий реагент (0,5% раствор твина-20);
конъюгат (вторые общевидовые антитела);
субстратиндикаторный раствор;
образцы положительного и отрицательного контролей.
К недостаткам известного способа и набора можно отнести ограничение сферы
применения - область ветеринарии. Использование данного способа в медицинской практике для диагностики иерсиниоза у людей требует дополнительных исследований. Кроме того, невысокое значение диагностического титра (1:400) в ИФА не исключает перекрестных реакций с другими возбудителями острых кишечных инфекций, и способ не позволяет выявлять иерсиниоз, обусловленный возбудителем, не относящихся к 0:3, 0:9, 0:6, 0:5, 0:8 серовариантам. В связи с этим данный способ характеризуется невысокой специфичностью и чувствительностью.
Общим недостатком известных методов диагностики иерсиниоза является использование типоспецифических антигенов Y. enterocolitica, что существенно снижает их диагностическую ценность.
Задача изобретения - совершенствование диагностики иерсиниоза, а именно разработка высокоэффективного способа ранней и дифференциальной диагностики иерсиниоза и разработка набора для его осуществления.
В результате решения поставленной задачи разработан способ дифференциальной диагностики иерсиниоза, включающий определение специфических антител к Yersinia enterocolitica в сыворотке крови больного методом твердофазного иммуноферментного анализа, в котором согласно изобретению в качестве антигена используют видоспецифический белок-порин наружной мембраны Yersinia enterocolitica, за диагностический титр принимают разведение сыворотки 1:800-1:1600, и результат считают положительным при величине, соответствующей отношению значения оптической плотности раствора ферментативной реакции со специфической сывороткой к значению оптической плотности раствора реакции с нормальной сывороткой, больше или равной 2,1.
Порообразующие белки наружной мембраны (НМ) грамотрицательных бактерий являются иммунологическими маркерами, характерными для вида или рода микроорганизмов, и относятся к высокоиммуногенным компонентам бактериальной клетки, и определение антител к ним используется для диагностики инфекционных заболеваний [15].
Авторы заявляемого способа установили, что порин НМ Y. enterocolitica, является видоспецифическим антигеном возбудителя иерсиниоза, антитела к которому обнаруживаются независимо от серологического варианта возбудителя как в антисыворотках лабораторных животных, иммунизированных лизатом клеток Y. enterocolitica, так и в сыворотках крови больных иерсиниозом. Эти результаты явились предпосылкой для использования порина НМ Y. enterocolitica в качестве видоспецифического антигена для серодиагностики иерсиниоза с помощью ИФА.
Порин выделяли стандартным методом в модификации авторов заявляемого способа [16].
ИФА на основе порина из Y. enterocolitica осуществляется по стандартной методике выявления специфических антител в сыворотке крови человека (непрямой, неконкурентный анализ антител) [17].
Анализ состоит из следующих этапов:
1) посадка антигена на твердый носитель (96 луночный полистироловый планшет) (концентрация антигена 5,0-2,5 мкг/мл в карбонат-бикарбонатном буфере с рН 9,0);
2) отмывка планшета 3-5 раз по 5 мин от несвязавшихся компонентов буфером "В", состоящим из фосфатно-солевого буфера с рН 7,4 (буфер "А")+0,05% твин-20 (или твин-80);
3) инактивация планшета (предотвращение неспецифического связывания антигена с антителами) буфером "С", состоящим из фосфатно-солевого буфера с рН 7,4 (буфер "А")+0,1% твин-20;
4) нанесение исследуемой сыворотки (серия разведений 1:800-1:1600 готовится с использованием буфера "В");
5) отмывка планшета;
6) нанесение конъюгата (вторые общевидовые антитела, меченные пероксидазой хрена):
рабочее разведение готовится с использованием буфера "С";
7) отмывка планшета;
8) нанесение субстратиндикаторного раствора: 0.04% о-фенилендиамин в цитратно-фосфатном буфере (рН 5,0)+10 мкл 33% Н2O2 (в расчете на 10 мл буфера);
9) нанесение стоп-реагента: 0,5М раствор серной кислоты (раствор готовится при разбавлении 1 мл концентрированной серной кислоты 15 мл дистиллированной воды);
10) регистрация результатов реакции.
Для исследования диагностических качеств и специфичности ИФА тест-системы на основе порина нами было обследовано 657 сывороток крови больных с характерными клиническими признаками иерсиниоза (57 из них - с бактериологически подтвержденным диагнозом), из них 357 - дети в возрасте от 1 года до 14 лет, и 200 сывороток крови взрослых пациентов. Кроме того, учитывая полиморфизм иерсиниозной инфекции, были проанализированы 256 сывороток крови больных с острыми кишечными инфекциями, не обусловленных Y. enterocolitica (псевдотуберкулез - 134, сальмонеллез - 54, острые вирусные гепатиты (А и В) - 68). Верификация указанных заболеваний проводилась с учетом клинико-эпидемиологических, бактериологических и/или специфических серологических исследований. Контрольную группу составили 86 практически здоровых человек, сопоставимых по возрасту и полу с обследуемыми больными.
Диагностический титр в ИФА определяли, сравнивая статистически достоверные значения [18], равные отношению средних значений оптической плотности раствора реакции с сыворотками крови больных иерсиниозом и здоровых людей (Fon/Fзд) при различных разведениях, где Fon=Fс+Fф
Fc - значение оптической плотности раствора специфической реакции антиген/антитело (антитела - сыворотка крови больного с подтвержденным диагнозом, или положительный контроль),
Fзд - значение оптической плотности раствора реакции с сыворотками крови здорового донора, или отрицательный контроль,
Fф - значение оптической плотности раствора неспецифической фоновой реакции.
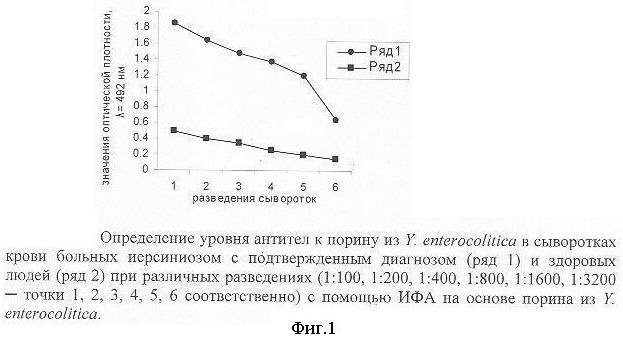
Для исследуемых сывороток (с бактериологически подтвержденным диагнозом) в разведениях 1:100, 1:200, 1:400, 1:800, 1:1600 1:3200 эти величины оказались соответственно равны 3,6; 4,0; 4,2; 5,5; 5,0; 4,1 (фиг.1). За диагностический титр приняли разведение сыворотки, для которого соотношение Fon/Fзд оказалось наибольшим. Таким образом, в ИФА на основе порина из Y. enterocolitica за диагностический титр принято разведение 1: 800-1:1600. Анализ сывороток крови больных иерсиниозом с помощью данной тест-системы на основе порина показал, что уровень специфических антител зарегистрирован в пределах 0,64-2,0 единиц оптической плотности раствора ферментативной реакции, что достоверно отличалось от контрольных значений (0,1-0,3 единиц оптической плотности раствора ферментативной реакции) (фиг.2). При апробации тест-системы на основе порина из Y. enterocolitica в сывороках крови у 12% здоровых доноров обнаружен повышенный уровень антител к Y. enterocolitica. Такой результат совпадает с литературными данными о том, что в местах с постоянной циркуляцией возбудителей иерсиниозов у здоровых людей в крови определяется повышенный уровень антител к этим возбудителям [3].
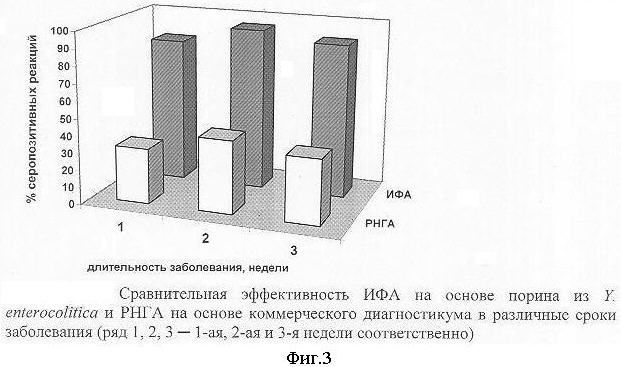
Для определения эффективности ИФА тест-системы на основе порина использовали параллельную постановку РНГА с коммерческим типоспецифическим иерсиниозным диагностикумом. При сравнительном анализе статистически достоверных результатов серологического обследования больных иерсиниозом (с бактериологически подтвержденным диагнозом) с помощью ИФА на основе порина и РНГА установлено, что на 1-й неделе заболевания ИФА выявляет специфические антитела в 85,2% случаев (среднее значение оптической плотности раствора ферментативной реакции составило 1,64 относительных единиц), а при постановке РНГА у этих же больных диагностические уровни антител были выявлены в 32,3% случаев (титр 1:100-1:200) (фиг.3). На 2-й неделе заболевания в сыворотках крови больных с помощью ИФА на основе порина антитела к Y. enterocolitica в диагностическом титре были выявлены в 95,0% случаев, (среднее значение оптической плотности раствора ферментативной реакции было равно 1,94 относительных единиц), а РНГА - в 42,7% случаев (титр 1:100-1:400). На 3 и 4-й неделях заболевания положительных реакций в ИФА на основе порина установлено в 90,7% случаев (среднее значение оптической плотности раствора ферментативной реакции составило 1,78 относительных единиц), в РНГА - 37,7% (титры антител 1:100-1:800) (фиг.3). Полученные данные свидетельствуют о том, что ИФА на основе порина из Y. enterocolitica является высокоэффективным методом и выявляет как в ранние, так и в более поздние сроки заболевания в сыворотках крови больных иерсиниозом специфические антитела к Y. enterocolitica в 2 раза эффективнее, чем РНГА, традиционно используемая клиническими лабораториями.
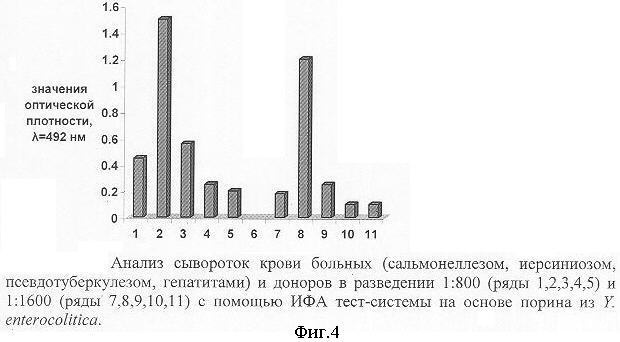
Для подтверждения специфичности и чувствительности ИФА на основе порина из Y. enterocolitica исследовали сыворотки крови больных острыми кишечными инфекциями, не обусловленных Y. enterocolitica. В результате обнаружено, что сыворотки крови больных псевдотуберкулезом и сальмонеллезом в диагностическом титре (1:800) взаимодействуют с порином. Однако значения оптической плотности раствора ферментативной реакции этих сывороток в 2-3 раза меньше значения оптической плотности раствора при взаимодействии порина с сыворотками крови больных иерсиниозом. При разведении этих сывороток 1:1600 антитела к порину из Y. enterocolitica были определены на уровне отрицательного контроля. При анализе сывороток крови больных гепатитами антител к порину из Y. enterocolitica не обнаружено ни в одном из случаев (фиг.4). Это свидетельствует о том, что предлагаемая тест-система позволяет эффективно и достоверно осуществлять дифференциальную диагностику иерсиниоза от других острых кишечных заболеваний. Следовательно, ИФА на основе порина из Y. enterocolitica является чувствительным методом диагностики иерсиниоза, обладает высокой специфичностью и не дает перекрестных реакций с антителами к возбудителям заболеваний, сходных по клинике с иерсиниозом.
Таким образом, ИФА тест-система на основе видоспецифического белка-порина НМ Y. enterocolitica обеспечивает выявление специфических антител к Y. enterocolitica в сыворотках крови больных иерсиниозом в разведениях 1:800 и 1:1600 и, по сравнению с существующими способами диагностики иерсиниоза, является более чувствительным и более специфичным способом диагностики иерсиниоза за счет определения всех серовариантов У enterocolitica, вызывающих иерсиниоз. Заявляемый способ отличается более высокой эффективностью диагностики иерсиниоза, поскольку позволяет диагностировать заболевание, как на ранних (на 1-й неделе заболевания - в 85,2% случаев), так и в более поздние сроки инфекционного процесса (на 2-й и 3-4 неделях - в 95% и 90,7% случаев соответственно).
Определение специфических антител к порину из У enterocolitica у здоровых лиц с помощью ИФА является ранним способом дифференциальной и этиологической диагностики иерсиниозного заболевания или бактерионосительства, что необходимо для своевременного назначения лечения и профилактики неблагоприятных исходов.
Изобретение иллюстрируется следующими чертежами:
На фиг.1 представлены результаты определения среднего значения уровня специфических антител к порину из Y. enterocolitica в сыворотках крови больных иерсиниозом с подтвержденным диагнозом (ряд 1) и здоровых людей (ряд 2) при различных разведениях (1:100, 1:200, 1:400, 1:800, 1:1600, 1:3200 - точки 1, 2, 3, 4, 5, 6 соответственно) с помощью ИФА тест-системы на основе порина из Y enterocolitica.
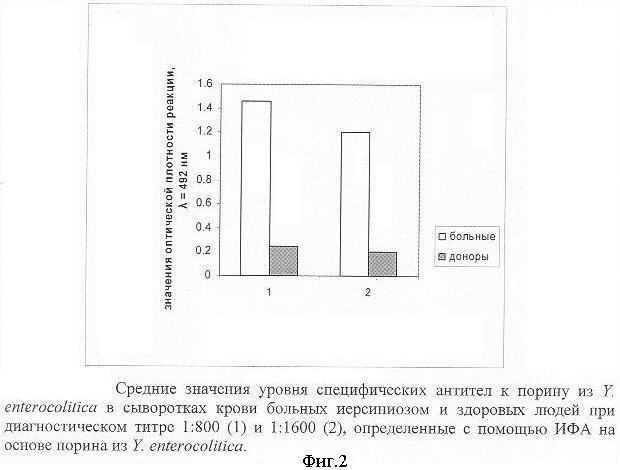
На фиг.2 представлены средние значения уровня специфических антител к порину из Y. enterocolitica в сыворотках крови больных иерсиниозом (1) и здоровых людей (2) при диагностическом титре (1:800 -1:1600) с помощью ИФА тест-системы на основе порина из Y. enterocolitica.
На фиг.3 представлена сравнительная эффективность ИФА на основе порина из Y. enterocolitica и РНГА на основе коммерческого иерсиниозного диагностикума в различные сроки заболевания (1, 2, 3 - 1-ая, 2-ая и 3-я недели соответственно)
На фиг.4 представлен анализ сывороток крови больных острыми кишечными инфекциями (сальмонеллез, иерсиниоз, псевдотуберкулез, гепатит) и доноров в разведении 1:800 (ряды 1, 2, 3, 4, 5) и 1:1600 (ряды 7, 8, 9, 10, 11) с помощью ИФА тест-системы на основе порина из Y. enteracolitica.
Заявляемый способ иллюстрируется следующим примером:
В лунки планшета (96 луночный полистироловый планшет фирмы «Dynatech», Швейцария или «Costar», США) вносят по 100 мкл раствора антигена (концентрация 5 мкг/мл в карбонат-бикарбонатном буфере с рН 9.0) и сенсибилизируют планшет при 37°С в течение 2 часов. Затем содержимое лунок удаляют сильным встряхиванием, и планшет промывают 3 раза буфером "В", состоящим из 0,02М фосфатно-солевого буфера рН 7,4 (буфер "А")+0,05% твин-20. Буфер "А" содержит 5,68 г Na2HPO4+6,24 г NaH2PO4+11,2 г NaCl+2 л Н2О. На каждой стадии промывки планшета необходимо тщательно удалять остатки влаги из лунок постукиванием перевернутого планшета о фильтровальную бумагу. Затем в каждую лунку планшета вносят по 300 мкл буфера "С", состоящего из фосфатно-солевого буфера рН 7,4 (буфер "А")+0,1% твин-20, и планшет инактивируют в течение 16-18 часов при 4°С. Затем вносят по 100 мкл исследуемой сыворотки крови, положительного и отрицательного контролей, по два повтора для каждого разведения. Разведения (1:800 и 1:1600) исследуемых образцов сывороток крови больного, положительного и отрицательного контролей готовятся с использованием буфера "В" (буфер "А"+0,05% твин-20, см. пункт 2). Далее планшеты инкубируют 2 ч при 37°С, затем отмывают 3-5 раз по 5 мин от не связавшихся компонентов буфером "В", тщательно удаляя остатки влаги из лунок. Затем в каждую лунку планшета вносят по 100 мкл конъюгата (меченные ферментом вторые общевидовые антитела) в рабочем разведении (1:1000) в буфере "С" (буфер "А"+0,1% твин-20) и инкубируют 1,5 ч при 37°С, далее планшеты отмывают, как описано выше. Затем в лунки планшета вносят по 70 мкл субстратиндикаторного раствора, содержащего 0,04% ортофенилендиамина в цитратно-фосфатном буфере (рН-5,0) и 10 мкл 33% Н2O2 (в расчете на 10 мл используемого буфера). Цитратно-фосфатный буфер готовят при смешивании 49,3 мл 0,2М двузамещенного фосфорнокислого натрия (1,42 г на 50 мл Н2О) и 50,7 мл 0,1М лимоннокислого натрия (2,1 г на 100 мл Н2О). Планшеты выдерживают 15-20 мин в темноте (для развития цветной реакции) при комнатной температуре, затем для остановки реакции добавляют в каждую лунку по 30 мкл 0,5М раствора H2SO4 (стоп-реагент). Результаты реакции учитывают с помощью спектрофотометра, измеряя оптическую плотность раствора в лунках планшета при длине волны равной 492 нм. При постановке ИФА на каждом планшете одновременно измеряют оптическую плотность раствора в лунках, содержащих следующие контроли:
- контроль положительный (контроль специфического связывания) - 100 мкл сыворотки крови больного иерсиниозом с бактериологически подтвержденным диагнозом + 100 мкл конъюгата + 70 мкл субстратиндикаторного раствора + 30 мкл H2SO4;
- контроль отрицательный - 100 мкл сыворотки крови здорового донора + 100 мкл конъюгата + 70 мкл субстратиндикаторного раствора + 30 мкл H2SO4;
- контроль неспецифического связывания - 100 мкл буферного раствора + 100 мкл конъюгата + 70 мкл субстратиндикаторного раствора + 30 мкл H2SO4.
Результат считают положительным, если величина, соответствующая отношению значения оптической плотности раствора в лунках со специфической сывороткой к значению оптической плотности раствора в лунках с нормальной сывороткой, больше или равна 2,1.
В настоящее время промышленный выпуск иммуноферментных диагностикумов (ИФА тест-систем) на иерсиниоз в нашей стране не осуществляется. Методы дифференциальной диагностики иерсиниоза, предлагаемые разными авторами [12-14], не оснащены необходимыми наборами реагентов для проведения иммунодиагностики иерсиниоза.
Предлагаемый диагностический набор на иерсиниоз для проведения заявляемого способа, а именно иммуноферментной диагностики с использованием видоспецифического антигена - порина НМ Y. enterocolitica, предназначен для выявления специфических антител к Y. enterocolitica в сыворотке крови человека и может быть использован в клинических и эпидемиологических исследованиях, а также службой крови.
Набор содержит все необходимые для проведения ИФА реагенты, кроме дистиллированной воды.
В состав набора входят:
1) планшет полистироловый 96-луночный (фирма «Dynatech», Швейцария или «Costar», США) с иммобилизованным антигеном - порином НМ Y. enterocolitica в герметично закрытом пакете - 1 шт.;
2) фосфатно-солевой буфер (концентрированный раствор буфера для инактивации и отмывки планшета, для разведения сывороток и конъюгата) - 2 флакона.
3) конъюгат (фракция общевидовых антител против суммарной фракции иммуноглобулинов человека, меченных пероксидазой хрена) - 1 флакон;
4) субстрат (орто-фенилендиамин, 4 мг) - 1 флакон;
5) цитратно - фосфатный буфер - 1 флакон;
6) отрицательный и положительный контроли (лиофильно высушенные образцы сывороток крови больного иерсиниозом с подтвержденным диагнозом и здорового донора) - 2 флакона;
7) инактивирующий реагент (твин-20 или твин-80) - 1 флакон;
8) перекись водорода (Н2О2, концентрированный раствор) - 1 флакон;
9) стоп-реагент (раствор 0,5 М серной кислоты) - 1 флакон;
Набор рассчитан на 96 определений, включая контроли.
В заявляемом диагностическом наборе в качестве инактивирующего реагента используют твин-20 или твин-80 вместо традиционно используемых дорогостоящих нормальной сыворотки крови или альбумина, что удешевляет стоимость предлагаемого набора.
Приготовление реагентов для проведения анализа:
1. Буфер "А": содержимое 1 флакона с концентратом фосфатно-солевого буфера (рН 7,4) (смесь солей: 0,02М натрия фосфорнокислого двузамещенного 12-водного, 0,02М натрия фосфорнокислого однозамещенного 2-водного и 0,1М натрия хлористого) необходимо растворить в 1 л дистиллированной воды (буфер "А").
2. Буфер "В" для отмывки планшета и разведения исследуемых сывороток крови больных, положительного и отрицательного контролей: к 1 л буфера "А" добавить 0,5 мл твин-20 (или твин-80) и получают буфер "В".
3. Буфер "С" для инактивации планшета и разведения конъюгата: к 200 мл буфера "А" добавить 0,2 мл твин-20 (или твин-80) и получают буфер "С".
4. Разведение сывороток: исследуемые сыворотки крови, контрольные, положительную и отрицательную сыворотки разводят буфером "В" до рабочего разведения.
5. Субстратная смесь готовится непосредственно перед употреблением. Содержимое флакона с субстратом (4 мг орто-фенилендиамина) растворить в 10 мл цитратно-фосфатного буфера (готового к употреблению) и добавить 10 мкл 33% H2O2.
6. Стоп-реагент (раствор 0,5 М серной кислоты) готов к использованию.
Для достоверности результатов анализа исследуемые и контрольные образцы сыворотки крови рекомендуются ставить в дубликатах, используя для каждого образца две лунки.
Проведение иммуноферментного анализа с помощью предлагаемого диагностического набора иллюстрируется следующим примером:
Предварительно готовый планшет (после сенсибилизации антигена - порина НМ Y. enterocolitica и отмывки планшета) для проведения следующих стадий анализа требуется проинактивировать.
1. Инактивация планшета (предотвращение неспецифического связывания антигена с антителами): вносят во все лунки по 300 мкл буфера "С" и инкубируют в течение ночи (16-18 ч) при 6-8°С. Буфер "С", состоящий из фосфатно-солевого буфера с рН 7,4 (буфер "А")+0,1% твин - 20 или твин-80, готовят путем растворения содержимого 1-го флакона (смесь солей - 0,02М натрия фосфорнокислого двузамещенного 12 - водного; 0,02М натрия фосфорнокислого однозамещенного 2-водного и 0,1М натрия хлористого) в 1 л дистиллированной воды (получают буфер "А"). Затем к 200 мл буфера "А" добавляют 0,2 мл твин-20 или твин-80 и получают буфер "С" для инактивации планшета и для разведения конъюгата. Раствор не хранят.
2. Отмывка планшета: после инактивации удаляют содержимое лунок декантированием и промывают их 3-5 раз по 5 мин от не связавшихся компонентов буфером "В". Для приготовления буфера "В" к 1 л буфера "А" добавляют 0,5 мл твин-20 или твин-80 и получают раствор для отмывания планшета и разведения сывороток. При каждой промывке во все лунки добавляют по 300 мкл промывочного буфера "В". При каждом декантировании тщательно удаляют остатки жидкости из лунок постукиванием планшета в перевернутом положении по фильтровальной бумаге.
3. Наносят в двух параллелях по 100 мкл исследуемой сыворотки, положительного и отрицательного контролей: сыворотки наносят в разведениях 1:800-1:1600 в буфере "В";
4. Инкубирование планшета при 37°С в течение 2 часов.
5. По окончании инкубации содержимое лунок удаляют и планшет промывают тщательно 3 раза буфером "В";
6. Вносят во все лунки по 100 мкл раствора конъюгата в рабочем разведении: рабочее разведение (1:1000) готовят при растворении содержимого флакона (сухого препарата) в буфере "С".
7. Инкубирование планшета при 37°С в течение 1,5 часа.
8. По окончании инкубации из лунок удаляют содержимое и планшет промывают.
9. Нанесение субстратной смеси. Субстратиндикаторный раствор готовят непосредственно перед употреблением: к 10 мл 0,05 М цитратно-фосфатного буфера (рН 5.0), содержащего 0,04% орто-фенилендиамин, добавляют 10 мкл 33% H2O2. Для приготовления 0.05 М раствора цитратно-фосфатного буфера содержимое флакона (смесь солей) растворяют в 10 мл дистиллированной воды. Перед нанесением субстратиндикаторного раствора планшет ополаскивают дистиллированной водой и высушивают.
10. Во все лунки планшета вносят по 70 мкл субстратной смеси и инкубируют в темноте в течение 15-20 мин при комнатной температуре.
11. Во все лунки планшета в той последовательности, как и субстратную смесь, добавляют по 30 мкл стоп-реагента для остановки ферментативной реакции.
12. Регистрация результатов реакции: измеряют оптическую плотность раствора ферментативной реакции в лунках при длине волны, равной 492 нм.
Результат считают положительным, если величина, соответствующая отношению значения оптической плотности раствора в лунках со специфической сывороткой к значению оптической плотности раствора в лунках с нормальной сывороткой больше или равна 2,1.
Литература
1. Кононова Д.Г., Шарапова Т.А. Кишечный иерсиниоз и его значение в патологии человека. Информационное письмо. Владивосток. 1980. С.1-15.
2. Попова О.В., Шепелева Г.К., Шестокова И.В., Андреев И.В., Попова Т.И., Ющук Н.Д. Клинико-иммунологическая характеристика иерсиниозной инфекции. // Инфекц. болезни. 2006. Т. 4. №3. С.51-55.
3. Ценева Г.Я. Иерсинии и иерсиниозы. СПб. Санкт-Петербург. 2006. 168 с.
4. Акбаров С.В., Султанов Х.К., Маткаримов Б.Д., Балтабаева М.А. Клинические варианты иерсиниозного реактивного артрита у детей. // Педиатрия. 1993. №.6. С.54-56.
5. Каманцев В.Н., Скрипченко Н.В., Тихомирова О.В., Бехтерева М.К. Поражения периферической нервной системы при иерсиниозной инфекции у детей. // Российский мед. журн. 2003. №2. С.27-29.
6. Ющук Н.Д., Кареткина Г.Н. Иерсиниозы. // Росс. журн. гастроэнтерол., гепатол., колопроктол. 1997. №5. С.58-60.
7. Климанова Е.М., Белая О.Ф., Лаврова К.В. и др. Использование реакции коагглютинации в диагностике иерсиниозов у детей. // Педиатрия. 1993. №.4. С.48-49.
8. Малышева Е.Б., Московкина Е.Д., Волнова О.М., Оскерко Е.Ф., Шелалуева М.В. Значение метода ПЦР в диагностике иерсиниоза: новые технологии в оценке эффективности лечения и прогноза. // Генодиагностика в современной медицине. Тез. Докл. 3-й Всеросс.научн. - практ.конф. Москва. 2000. С.169.
9. Koroliuk A.M., Golovacheva S.N., Dulatova M.V. The choice of rational methods for determining antibodies to Yersinia enterocolitica. The agglutination reaction. // Zh. Mikrobiol. Epidemiol. Immunobiol. 1988. №9. P.45-47.
10. Александер С.К., Лукин Ю.В., Фидлер Л.М. Приготовление Ig G диагностикума на основе окрашенных полиакролеиновых латексов для применения в реакции латексной агглютинации. // ЖМЭИ. 1990. №6. С.84-88.
11. Королюк A.M., Головачева С.Н, Дулатова М.В. Серологическая диагностика кишечного иерсиниоза. Конструирование стабильного эритроцитарного препарата для реакции непрямой гемагглютинации. // ЖМЭИ. 1990. №3. С.30-34.
12. Granfors K., Ogasawara М., Hill J.L., Lahesmaa-Rantala R., Toivanen A., Yu DTY.
Analisis of IgA antiboddies to lipopolisaccharide in Yersiniatriggered reactive artritis. // J. Infect. Dis. 1989. V.159. P.1142-1147.
13. Малов И.В., Рубцов И.В., Ющенко Г.В., Леоненко В.В. Способ иммуноферментной диагностики иерсиниозов. //Патент SU 1767435 А1 от 1992. 10.07.
14. Богаутдинов З.Ф., Вылегжанина Е.С., Кузьмина В.Б., Астахова Т.С., Ниязов У.Э., Шумилов К.В. Способ диагностики иерсиниозов. // Патент RU 2152037 С1 от 2000.06.27.
15. Дельвиг А.А., Семенов Б.Ф. Механизмы формирования иммунного ответа к пориновым белкам наружной мембраны менингококков серогруппы В. // Журн. микробиол., эпидемиол. и иммунологии. 1997. №6. С.92-96.
16. Вострикова О.П., Ким Н.Ю., Лихацкая Г.Н., Гузев К.В., Вакорина Т.И., Хоменко В.А., Новикова О.Д., Соловьева Т.Ф. Структура и функция порообразующих белков бактерий рода YERSINIA. II Биоорган, химия. 2006. Т.32. №4. С.371-383.
17. Егоров A.M., Осипов А.П., Дзантиев Б.Б, Гаврилова Е.М. Теория и практика иммуноферментного анализа. М.: Высшая школа, 1991. 228 с.
18. Ашмарин И.П.. Воробьев А.А. Статистические методы в микробиологических исследованиях. - М., 1962. С.30-66.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ПСЕВДОТУБЕРКУЛЕЗА И КИШЕЧНОГО ИЕРСИНИОЗА И ДИАГНОСТИЧЕСКИЙ НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2007 |
|
RU2339952C1 |
| СПОСОБ ДИАГНОСТИКИ ПСЕВДОТУБЕРКУЛЕЗА | 1998 |
|
RU2153172C1 |
| СПОСОБ ДИАГНОСТИКИ ПСЕВДОТУБЕРКУЛЕЗА | 2009 |
|
RU2429480C1 |
| СПОСОБ ДИАГНОСТИКИ БРУЦЕЛЛЕЗА | 1999 |
|
RU2152035C1 |
| СПОСОБ ДИАГНОСТИКИ ИЕРСИНИОЗОВ | 1999 |
|
RU2152037C1 |
| БЕЗЫНСТРУМЕНТАЛЬНЫЙ СПОСОБ ДИАГНОСТИКИ ПСЕВДОТУБЕРКУЛЕЗА | 2011 |
|
RU2464573C1 |
| Способ иммуноферментной диагностики иерсиниозов | 1990 |
|
SU1767435A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПСЕВДОТУБЕРКУЛЕЗНОГО АНТИГЕННОГО ПОЛИМЕРНОГО ДИАГНОСТИКУМА | 2010 |
|
RU2430376C1 |
| ШТАММ F26 ПОСТОЯННОЙ ГИБРИДОМНОЙ ЛИНИИ КЛЕТОК МЫШИ MUS. MUSCULUS - ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ К ОЛИГОПОЛИСАХАРИДНОМУ (ОПС) АНТИГЕНУ B. ABORTUS | 2014 |
|
RU2560260C1 |
| СПОСОБ ПРИЖИЗНЕННОЙ ДИАГНОСТИКИ ТРИХИНЕЛЛЕЗА ПЛОТОЯДНЫХ И ВСЕЯДНЫХ ЖИВОТНЫХ | 2006 |
|
RU2339038C2 |
Изобретение относится к медицине, а именно к способам диагностики инфекционных заболеваний, и касается иммуноферментной (ИФА) диагностики кишечного иерсиниоза, вызванного различными серовариантами Yersinia enter ocolitica, и наборам для диагностики иерсиниоза. Сущность способа: в качестве антигена используется видоспецифический порообразующий белок (порин) наружной мембраны У. enterocolitica который обеспечивает определение специфических антител к порину из Y. enterocolitica в сыворотке крови человека независимо от серологического варианта возбудителя. В качестве реагента для предотвращения неспецифического связывания используется 0,1%-ный раствор твина-20 или твина-80. Диагностическим титром является разведение сыворотки крови больного 1:800-1:1600. Способ диагностики и предлагаемый набор для его осуществления повышают эффективность диагностики кишечного иерсиниоза, так как позволяют определять в сыворотке крови человека специфические антитела к Y. enterocolitica всех серовариантов как в ранние (на 1-й неделе заболевания), так и в более поздние сроки заболевания (на 2-й и 3-4-й неделях). 2 н.п. ф-лы, 4 ил.
| СПОСОБ ДИАГНОСТИКИ ИЕРСИНИОЗОВ | 1999 |
|
RU2152037C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ИЕРСИНИОЗА | 1992 |
|
RU2087913C1 |
| СПОСОБ ДИАГНОСТИКИ ИЕРСИНИОЗА | 1990 |
|
RU2008684C1 |
| ПОРТНЯГИНА О.Ю | |||
| и др | |||
| Бактериальные порины как перспективные антигены для диагностики и вакцинопрофилактики инфекционных заболеваний, Вестник ДВО РАН, 2004, №3, с.35-44 | |||
| НОВИКОВА О.Д | |||
| и др | |||
| Использование порина из внешней мембраны Yersinia pseudotuberculosis для серодиагностики псевдотуберкулеза, Бюлл.эксп.биол | |||
| мед., 2005, №8, с.199-202. | |||
Авторы
Даты
2009-01-27—Публикация
2007-05-29—Подача