Изобретение относится к химии гетероциклических соединений, а именно к замещенным O-[ω-(азол-1-ил)алкил]-N-фенилтиокарбаматам общей формулы I:
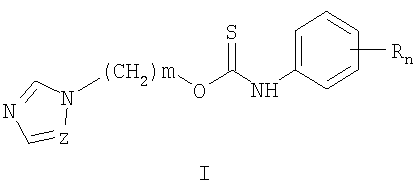
где Z означает атом азота или СН-группу; n означает целое число от 1 до 5; m означает целое число от 1 до 3; R одинаковые или разные означают атом водорода, галогена, алкильную группу с числом атомов углерода от 1 до 4, алкоксигруппу с числом атомов углерода от 1 до 4, алкоксикарбонильную группу числом атомов углерода от 1 до 4, алкилсульфанильную группу с числом атомов углерода от 1 до 4, перфторалкильную группу с числом атомов углерода от 1 до 4; обладающим фунгицидной активностью. Соединения общей формулы I могут найти применение в качестве сельскохозяйственных, промышленных, медицинских или ветеринарных фунгицидов.
Изобретение относится также к способам получения соединений общей формулы I, к использованию этих соединений в композициях с другими активными и вспомогательными соединениями для борьбы с грибковыми болезнями сельскохозяйственных культур, животных и человека.
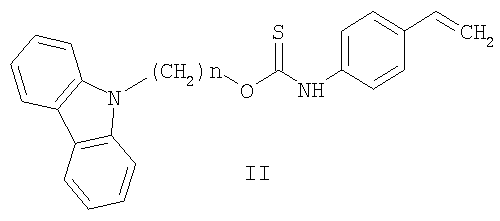
Известен ряд тиокарбаматов общей формулы II. [Барба Н.А., Драгалина Г.А., Панасюк Л.М. Синтез некоторых светочуствительных мономеров, содержащих остатки карбазола и антрацена. // Химические и физико-химические методы исследования соединений: Вопросы химии и химической технологии. Меж. вуз. сб. - Кишинев: Штиинца. - 1980. - С.53-56], которые являются мономерами для получения полимерных материалов, стабильных к термоокислительной деструкции, к свето- и озоностарению.
Известен также O-(2-оксобензоксазол-3-илметил)фенилтиокарбамат III. [Zinner H., Pinkert H. [2-Oxo-benzoxazolyl-(3)-methyl] - ester von Carbonsäuren und Thiocarbonsäuren. // J. prakt. Chemie. - 1975. - В.317, H.3. - S.379-86.], который получают взаимодействием (2-оксобензоксазол-3-ил)метанола с фенилизотиоцианатом в пиридине в течение 24 часов при 20°С.

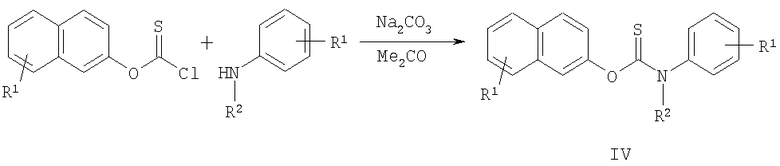
Наиболее близким к заявленным O-[ω-(азол-1-ил)алкил]фенилтиокарбаматам по структуре и по способу получения являются нафтилсодержащие антимикробные препараты общей формулы IV, где R1 одинаковые или разные означают атом водорода, галогена; низшую алкильную группу, алкоксигруппу, гидроксигруппу, карбонильную группу, перфторалкильную группу с числом атомов углерода от 1 до 4, нитрогруппу; R2 означает атом водорода, алкильную группу с числом атомов углерода от 1 до 12 [патент США №3334126; МКИ С07С 155/08, заявл. 18.02.1966, опубл. 01.08.1967; Noguchi Т., Hashimoto Y., Miyazaki K., Kaji A. Relationship between Chemical Structure and Selective Antimicrobial Activities of Aryl thiocarbamates. // Yakugaku Zasshi. - 1968. - Vol.88. - No.3. - P.335-343], которые обладают антимикотической активностью. Соединения общей формулы IV получают реакцией N-алкиланилинов с 2-нафтилхлоротиоформиатами в ацетоне, метилэтилкетоне или этаноле в течение 0.25-2 ч в присутствии гидроксидов или карбонатов щелочных металлов.
Известны способы получения (азол-1-ил)метанолов взаимодействием имидазола или 1,2,4-триазола с формалином [патент Германии №2618756 МКИ C07D 233/64, заявл. - 28.04.1976, опубл. - 03.11.1977; P.W. Alley. The imidazole-formaldehyde reaction. Formation of 1-imidazolemethanol. // J. Org. Chem. - 1975. - Vol.40, №12. - P.] или параформом [Европейский патент 60222 МКИ C07D 249/08, заявл. 10.03.81, опубл. 15.09.82].
Известны способы получения 2-(азол-1-ил)этанолов взаимодействием имидазола или 1,2,4-триазола с этиленкарбонатом [Banfi A., Sala A., Soresinetti A. Synthesis of New Imidazole Derivatives as Potential Inhibitors of Thromboxane Synthetase. // J. Heterocyclic. Chem. - 1990. - Vol.27, №2. - P.215-219.] или этиленхлоргидрином в присутствии гидроксида натрия в условиях межфазного катализа [Асратян Г.В., Аттарян О.С., Погосян А.С., Элиазян Г.А., Дарбинян Э.Г., Мацоян С.Г. Алкилирование азолов β-функционально замещенными галогеналкилами в условиях межфазного катализа. // Журн. прикл. хим. - 1986. - №6. - С.1296-1300].
Задача, решаемая данным изобретением, состоит в увеличении эффективности борьбы с вредоносными грибами и расширении ассортимента фунгицидных препаратов.
Поставленная задача решается получением соединений общей формулы I, обладающих фунгицидной активностью, а также увеличением эффективности фунгицидных средств за счет применения замещенных O-[ω-(азол-1-ил)алкил]-N-фенилтиокарбаматов I и расширением ассортимента фунгицидных препаратов.
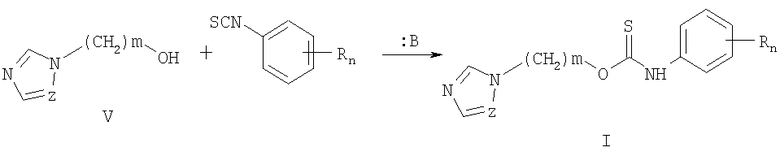
Согласно настоящему изобретению замещенные O-[ω-(азол-1-ил)алкил]-фенилтиокарбаматы общей формулы I получают взаимодействием ω-(азол-1-ил)-1-алканолов V, где Z означает атом азота или СН-группу, m означает целое число от 1 до 3, с замещенными фенилизотиоцианатами VI, где R одинаковые или разные означают атом водорода, галогена, алкильную группу с числом атомов углерода от 1 до 4, алкоксигруппу с числом атомов углерода от 1 до 4, алкоксикарбонильную группу числом атомов углерода от 1 до 4, алкилсульфанильную группу с числом атомов углерода от 1 до 4, перфторалкильную группу с числом атомов углерода от 1 до 4, в полярных апротонных растворителях, например абсолютном ацетонитриле, тетрагидрофуране, диоксане и др. в условиях катализа основаниями, например триэтиламином, диазобицикло[5.4.0]ундец-7-еном (ДБУ), гидроксидом тетрабутиламмония и др. в количестве от 0,1 до 20% мольн., при температуре от 20 до 80°С.
Техническим результатом изобретения являются новые соединения - замещенные O-[ω-(азол-1-ил)алкил]-N-фенилтиокарбаматы общей формулы I и способ их получения. В указанном патенте [патент США №3334126] тиокарбаматы предлагается получать ацилированием в присутствии оснований замещенных N-алкиланилинов O-нафтилтиокарбамоилхлоридами, предварительно полученными взаимодействием нафтолов с тиофосгеном. Мы предлагаем получать новые соединения - замещенные O-[ω-(азол-1-ил)алкил]-N-фенилтиокарбаматы общей формулы I, более простым и эффективным малоотходным способом: взаимодействием азолилалканолов с фенилтиокарбаматами, в присутствии каталитических количеств оснований.
Успешное применение пестицидов для борьбы с различными вредными организмами в большой степени зависит от препаративной формы препарата и условий, при которых действующее вещество контактирует с вредителями и возбудителями заболеваний растений. В зависимости от физико-химических свойств препарата, его назначения и способа применения выбирается наиболее эффективная и экономичная препаративная форма (композиция), это могут быть, например, дусты, гранулы, микрокапсулированные препараты, смачивающиеся порошки, концентраты эмульсий, мази, вододиспергируемые гранулы, суспензионные концентраты. Препаративные формы помимо действующего вещества могут включать в свой состав вспомогательные вещества: наполнители, растворители, поверхностно-активные вещества, умягчители воды, синергические добавки и др. Известен препарат цинеб, который применяют в виде 70 и 80%-ного смачивающегося порошка для борьбы с болезнями яблони, сливы, картофеля, томатов, огурцов, капусты в период вегетации, а также как протравитель семян. [Пестициды и регуляторы роста растений: Справ, изд. / Н.Н.Мельников, К.В.Новожилов, С.Р.Белан. - М.: Химия, 1995, с.24, с.316.]
Техническим результатом изобретения также является разработка фунгицидных композиций, состоящих из замещеных O-[ω-(азол-1-ил)алкил]-фенилтиокарбаматы общей формулы I в концентрации 0,1-99% и вспомогательных веществ, которые успешно могут быть применены для борьбы с вредоносными грибковыми болезнями сельскохозяйственных культур, животных или человека. По результатам фунгицидных испытаний in vitro замещенные O-[ω-(азол-1-ил)алкил]-N-фенилтиокарбаматы, например соединения 2, 11, 16 и 17, превосходят используемый в качестве эталонного известный фунгицид - триадимефон (3,3-диметил-1 -(1,2,4-триазол-1-ил)-1-(4-хлорфенокси)-2-бутанон) по отношению ко всем испытанным видам грибов-патогенов. Упомянутые в патенте-прототипе соединения, в том числе наиболее известный препарат толнафтат (O-(2-нафтил)-метил-(3-метилфенил)тиокарбамат) предлагают применять, например, в качестве антимикотика для борьбы с грибными болезнями человека, в частности Trichophyton mentagrophytes, в то время как он неэффективен при борьбе с болезнями сельскохозяйственных культур [Noguchi Т., Hashimoto Y., Miyazaki К., Kaji A. // Yakugaku Zasshi. - 1968. - Vol.88. - No.3. - P.335-343]. Широко применяемый триазольный фунгицид триадимефон фунгитоксичен по отношению к грибам-патогенам различных таксономических классов, в то же время заявляемые нами замещеные O-[ω-(азол-1-ил)алкил]-фенилтиокарбаматы общей формулы I превосходят его по отношению к большинству испытанных грибов-фитопатогенов.
Изобретение может быть проиллюстрировано следующими примерами:
Пример 1. O-(1,2,4-Триазол-1-илметил)-N-фенилтиокарбамат (1)
К раствору 0,99 г (0,01 моль) (1,2,4-триазол-1-ил)метанола в 10 мл абсолютного ацетонитрила добавляют 1,35 г (0,01 моль) фенилизотиоцианата и 0.1 мл (0.7 ммоль, 0.072 г) триэтиламина. Реакционную массу кипятят в течение 2 часов при температуре 80°С, растворитель удаляют в вакууме водоструйного насоса, остаток кристаллизуют из диэтилового эфира. Кристаллы отфильтровывают, промывают 2 мл холодного ацетонитрила, 2 мл диэтилового эфира и получают 0,57 г (24%) O-(1,2,4-триазол-1-илметил)-N-фенилтиокарбамата (1) с т.пл. 124-125°С.
Пример 2. Этил 4-(1,2,4-триазол-1-илметокситиокарбониламино)бензоат (9)
К 0,99 г (0,01 моль) (1,2,4-триазол-1-ил)метанола в 10 мл абсолютного тетрагидрофурана добавляют 2,07 г (0,01 моль) этил 4-изотиоцианатобензоата и 0.1 мл (0.7 ммоль, 0.072 г) триэтиламина. Реакционную массу кипятят в течение 4 часов при температуре 67°С, растворитель удаляют в вакууме водоструйного насоса, остаток перекристаллизовывают из метанола и получают 1,93 г (63%) этил 4-(1,2,4-триазол-1-илметокситиокарбонил-амино)бензоата (9) с т.пл. 85-86°С. Аналогично получают другие замещенные O-(1,2,4-триазол-1-илметил)-N-фенилтиокарбаматы. (Таблица 1).
Пример 3. O-(Имидазол-1-илметил)-N-фенилтиокарбамат (10)
К 0,98 г (0,01 моль) (имидазол-1-ил)метанола в 10 мл абсолютного ацетонитрила добавляют 1,35 г (0,01 моль) фенилизотиоцианата и 0.05 мл (0.4 ммоль, 0.036 г) триэтиламина. Реакционную массу кипятят в течение 2 часов при температуре 80°С, растворитель удаляют в вакууме водоструйного насоса, остаток кристаллизуют из диэтилового эфира. Кристаллы отфильтровывают, промывают 2 мл холодного ацетонитрила, 2 мл диэтилового эфира и получают 0,81 г (35%) O-(имидазол-1-илметил)-N-фенилтиокарбамата (10) с т.пл. 142-143°С.
Пример 4. Этил 4-(имидазол-1-илметокситиокарбониламино)бензоат (17)
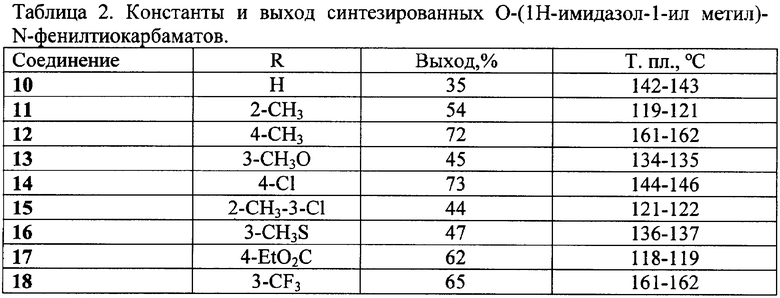
К 0,98 г (0,01 моль) (имидазол-1-ил)метанола в 10 мл абсолютного ацетонитрила добавляют 2,07 г (0,01 моль) 4-изотиоцианатобензоата и 0.1 мл (0.7 ммоль, 0.072 г) триэтиламина. Реакционную массу кипятят в течение 3 часов при температуре 80°С, растворитель удаляют в вакууме водоструйного насоса, остаток перекристаллизовывают из изопропанола и получают 1,89 г (62%) этил 4-(имидазол-1-илметокситиокарбонил-амино)бензоата (17) с т.пл. 118-119°С.Аналогично получают другие замещенные O-(имидазол-1-илметил)фенилтио-карбаматы. (Таблица 2).
Пример 5. O-[2-(Имидазол-1-ил) этил]-N-фенилтиокарбамат(19)
К 1,12 г (0,01 моль) 2-(имидазол-1-ил)этанола в 10 мл абсолютного ацетонитрила добавляют 1,35 г (0,01 моль) фенилизотиоцианата и 0.1 мл (0.7 ммоль, 0.072 г) триэтиламина. Реакционную массу перемешивают в течение 24 часов при комнатной температуре, растворитель упаривают наполовину в вакууме водоструйного насоса, добавляют 20 мл диэтилового эфира, охлаждают до 0°С, кристаллы отфильтровывают и промывают 2 мл диэтилового эфира. Получают 1,11 г (45%) O-[2-(имидазол-1-ил)этил]-фенилтиокарбамата (19)с т.пл. 154-155°С.
Пример 6. Этил 4-[2-(имидазол-1-ил)этокситиокарбониламино]бензоат (26)
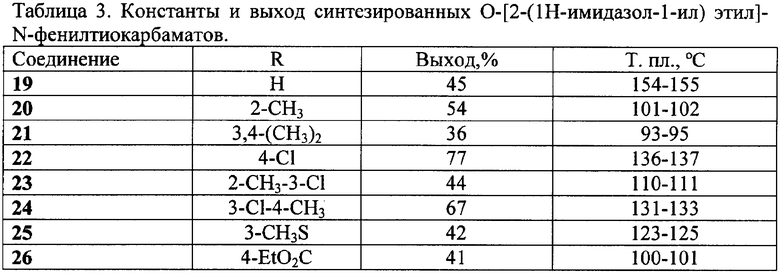
К 1,12 г (0,01 моль) 2-(имидазол-1-ил)этанола в 10 мл абсолютного ацетонитрила добавляют 2,07 г (0,01 моль) 4-изотиоцианатобензоата и 0.05 мл (0.3 ммоль, 0.046 г) диазобицикло[5.4.0]ундец-7-ена (ДБУ). Реакционную массу кипятят в течение 6 часов при температуре 80°С, растворитель удаляют в вакууме водоструйного насоса, остаток перекристаллизовывают из изопропанола и получают 1,31 г (41%) этил 4-[2-(имидазол-1-ил)этокситиокарбониламино]бензоата (26) с т.пл. 100-101°С.Аналогично получают другие замещенные O-[2-(1H-имидазол-1-ил)этил]-N-фенилтиокарбаматы. (Таблица 3).
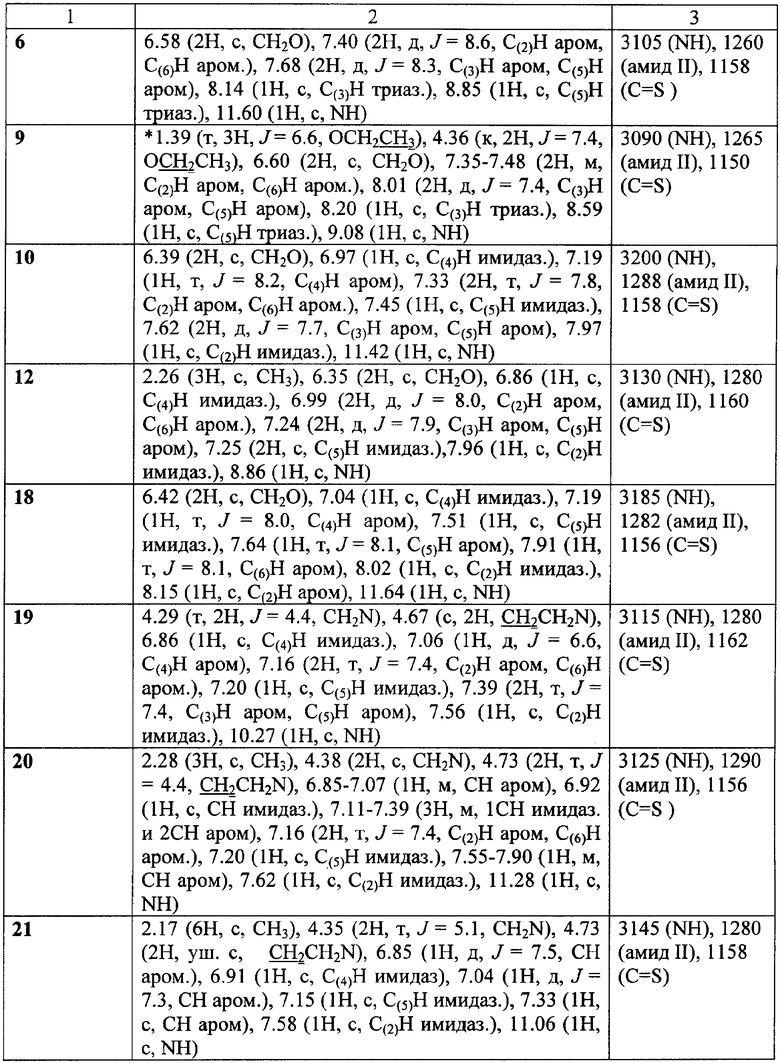
Данные о выходе и температуре плавления полученных продуктов приведены в таблицах 1,2,3 спектральные характеристики - в таблице 4.
1Н ЯМР-спектры записаны на приборе «Bruker AC-200» (рабочая частота 200 МГц), сдвиги измерены относительно тетраметилсилана, в качестве растворителя использовали d6-DMSO. ИК-спектры регистрировали с призмами NaCl в тонкой пленке в вазелиновом масле на приборе «Specord M80».



Пример 7. Композиция концентрата эмульсии
Действующее вещество (замещений O-[ω-(азол-1-ил)алкил]-N-фенилтио-карбамат) 80 г. Алкилбензолсульфокислоты кальциевая соль (АБСК) 20 г. Оксиэтилированный октилфенол (ОП-7) 80 г. Циклогексанон 290 г. Ксилол 150 г. Нефтяной сольвент 280 г.
Пример 8. Испытания на фунгицидную активность соединений проводили в экспериментах in vitro. [Методические рекомендации по определению фунгицидной активности новых соединений. Черкассы: НИИТЭХИМ. 1984. 34 с.]. Действие препаратов на радиальный рост мицелия определяли растворением композиции соединения в ацетоне и внесением аликвоты в картофелесахарозный агар при 50°С до концентрации 30 мг/л по действующему веществу. Конечная концентрация ацетона в контрольных растворах с действующими веществами составили 1%. В чашки Петри, содержащие 15 мл агаровой среды, наносили иглой культуры грибов на агаровую поверхность. Образцы выдерживали в инкубаторе при 25°С и измеряли радиальный рост через 3 суток. Процент ингибирования рассчитывали по Эбботу по отношению к необработанному контролю. В качестве эталона использовали коммерческий фунгицид триадимефон в той же концентрации. Результаты испытаний представлены в таблице 5.
* в концентрации 15 мг/л; ** в концентрации 5 мг/л; *** триадимефон
Применение соединений общей формулы I как в индивидуальном виде, так и в композициях с другими активными и вспомогательными соединениями, позволяет более эффективно бороться с грибковыми заболеваниями сельскохозяйственных культур в сравнении, например, с таким широко используемым фунгицидом, как триадимефон.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ О-[ω-(АЗОЛ-1-ИЛ)АЛКИЛ]-N-ФЕНИЛКАРБАМАТЫ В КАЧЕСТВЕ СРЕДСТВ С АНТИАГРЕГАЦИОННОЙ АКТИВНОСТЬЮ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2009 |
|
RU2488583C2 |
| Замещенные 4-(азол-1-илметил)-1-фенил-5,5-диалкилспиро-[2.5]октан-4-олы, способ их получения (варианты), фунгицидная и рострегуляторная композиции на их основе | 2016 |
|
RU2648240C1 |
| ЗАМЕЩЕННЫЕ N-[ω-АЗОЛ-1-ИЛ)АЛКИЛ]БЕНЗОЛСУЛЬФАМИДЫ В КАЧЕСТВЕ СРЕДСТВ С АНТИАГРЕГАЦИОННОЙ АКТИВНОСТЬЮ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2006 |
|
RU2339625C2 |
| Замещенные 4-(азол-1-илметил)-1,6-бисфенилдиспиро[2.1.2.3]декан-4-олы, способ их получения и фунгицидная композиция на их основе | 2019 |
|
RU2730490C1 |
| ЗАМЕЩЕННЫЕ ОМЕГА-АЗОЛИЛАЛКАНАНИЛИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТИАГРЕГАНТОВ | 2006 |
|
RU2322440C1 |
| N-Замещенные 3-алкилсульфанил-5-(1,2,4-триазол-1-илметил)-1,2,4-триазолы, способ их получения, фунгицидные и рострегуляторные композиции на их основе | 2017 |
|
RU2668212C1 |
| 2-Алкилтио-5-(1Н-1,2,4,-триазол-1-илметил)-1,3,4-тиадиазолы, способ их получения и фунгицидные композиции на их основе | 2020 |
|
RU2757808C1 |
| N-(5-(1,2,4-Триазол-1-илметил)-1,2,4-триазол-3-ил)-метанимины и способ их получения | 2023 |
|
RU2827565C1 |
| Способ получения 3-азолилпропанолов | 2022 |
|
RU2786670C1 |
| ЗАМЕЩЕННЫЕ 2-(1,2,4-ТРИАЗОЛ-1-ИЛМЕТИЛ)-6-БЕНЗИЛИДЕН-1,4-ДИОКСАСПИРО[4.5]ДЕКАНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФУНГИЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2006 |
|
RU2326878C1 |
Описываются замещенные O-[ω-(азол-1-ил)алкил]-N-фенилтиокарбаматы формулы I:

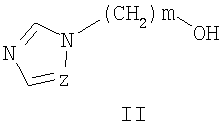
где Z=CH, N, R=H, Alk, AlkO, Hal и др., m=1, 2, 3, n=0-5, которые получают ацилированием ω-(азол-1-ил)алканолов формулы II замещенными фенилизотиоцианатами в полярных апротонных растворителях в присутствии третичных аминов. Изобретение позволяет за счет применения фунгицидной композиции, содержащей замещенные O-[ω-(азол-1-ил)алкил]-фенилтиокарбаматы I, например O-(имидазол-1-илметил)-N-(2-метил-фенил)тиокарбамат при испытаниях in vitro существенно эффективнее подавлять развитие грибов-фитопатогенов, чем с помощью такого эталона, как триадимефон. 3 н. и 1 з.п. ф-лы, 5 табл.
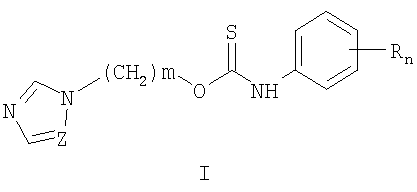
где Z означает атом азота или СН-группу, n означает целое число от 1 до 5, m означает целое число атомов от 1 до 3, R одинаковые или разные означают атом водорода, галогена, алкильную группу с числом атомов углерода от 1 до 4, алкоксигруппу с числом атомов углерода от 1 до 4, алкоксикарбонильную группу числом атомов углерода от 1 до 4, алкилсульфанильную группу с числом атомов углерода от 1 до 4, перфторалкильную группу с числом атомов углерода от 1 до 4.
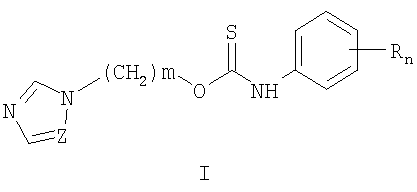
где Z означает атом азота или СН-группу, n означает целое число от 1 до 5, m означает целое число атомов от 1 до 3, R одинаковые или разные означают атом водорода, галогена, алкильную группу с числом атомов углерода от 1 до 4, алкоксигруппу с числом атомов углерода от 1 до 4, алкоксикарбонильную группу числом атомов углерода от 1 до 4, алкилсульфанильную группу с числом атомов углерода от 1 до 4, перфторалкильную группу с числом атомов углерода от 1 до 4, заключающийся в том, что ω-(азол-1-ил)-1-алканолы II, где Z и m имеют те же значения, что и в формуле I, вводят во взаимодействие с замещенными фенилизотиоцианатами III, где R и n имеют те же значения, что и в формуле I
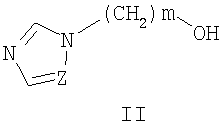
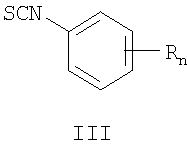
в полярных апротонных растворителях в присутствии оснований при температуре от 20 до 80°С.
| US 3334126, 01.08.1967 | |||
| ПИРАЗОЛЬНЫЕ КАРБОКСАНИЛИДЫ И СРЕДСТВА ДЛЯ БОРЬБЫ С БАКТЕРИЯМИ И ГРИБАМИ НА ИХ ОСНОВЕ | 1999 |
|
RU2240314C2 |
| RU 94030811 A1, 20.04.1996 | |||
| Staab Heinz A | |||
| et al | |||
| Synthesis of isothiocyanates | |||
| Justus Liebigs Annalen der Chemie, 1962, 657, 104-7. | |||
Авторы
Даты
2009-02-20—Публикация
2007-08-07—Подача