Изобретение относится к химии гетероциклических соединений, а именно к замещенным O-[ω-(азол-1-ил)алкил]-N-фенилкарбаматам общей формулы I:
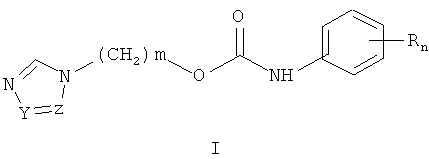
где Z и Y означают атом азота или CH-группу, или одновременно являются цепью C-CH=CH-CH=CH-C составляющую вместе аннелированное кольцо; m означает целое число от 1 до 3; R одинаковые или разные означают атом водорода, галогена, алкильную группу с числом атомов углерода от 1 до 4, алкоксигруппу с числом атомов углерода от 1 до 4, перфторалкильную группу с числом атомов углерода от 1 до 4, нитрогруппу, алкоксикарбонильную группу, сульфамоилгруппу, n означает целое число атомов от 0 до 2;
к их солям с фармацевтически подходящими кислотами, обладающим антиагрегационной активностью.
Соединения общей формулы I могут найти применение в качестве медицинских, ветеринарных и фитотерапевтических препаратов, в первую очередь лекарственных препаратов с антиагрегационной активностью.
Изобретение относится также к способам получения соединений общей формулы I и использованию этих соединений в качестве антиагрегантов в фармацевтических композициях.
Известны бис(азол-1-илэтил)карбаматы производные 2-фенил-4-хиназолона обладающие противораковой активностью общей формулы II, где Z означает атом азота или CH-группу [Патент Германии №2050092; МКИ C07D 51/48. Заявл. - 11.10.1971].
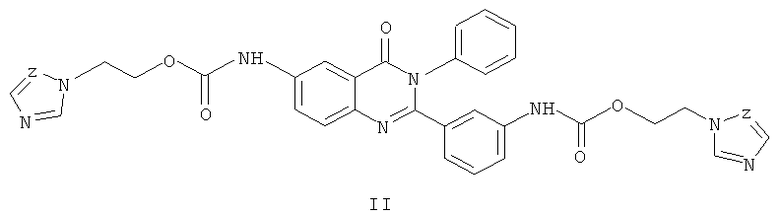
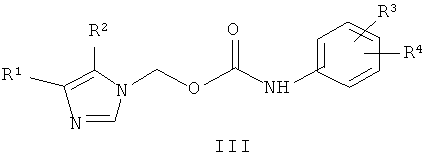
Наиболее близкими к заявленным замещенным O-[ω-(азол-1-ил)алкил]-N-фенилкарбаматам по структуре и по способу получения являются O-(азол-1-илметил)-N-арилкарбаматы общей формулы III, где R1 и R2 каждый означают атом водорода или вместе -CH=CH-CH=CH-группу, которая может содержать низшую алкильную, галогеналкильную, алкоксильную группу с числом атомов углерода от 1 до 4, атом галогена, нитро группу; R3 и R4 каждый независимо один от другого означают атом водорода, низшую алкильную, галогеналкильную, алкоксильную галогеналкоксильную группу с числом атомов углерода от 1 до 4, атом галогена, нитро группу или вместе означают -CH=CH-CH=CH-группу, [патент США №3915984, МКИ C07D 235/06. - Заявл. - 07.12.1973], применяемые как гиполипидемические средства. Соединения общей формулы III получают взаимодействием азолилметанолов с арилизоцианатами или N-арилкарбамоилхлоридами в инертном растворителе.
Первое место среди причин летального исхода занимают заболевания сердечнососудистой системы. Назначение антитромбоцитарных препаратов (антиагрегантов) предупреждает развитие тяжелых сосудистых осложнений, снижает риск тяжелых сосудистых исходов: инфаркта миокарда, инсультов. Данная группа препаратов является важной составной частью лечения и профилактики стенокардии, атеросклероза периферических артерий и проявлений атеротромбоза.
Антиагреганты ингибируют агрегацию тромбоцитов, уменьшают их способность к склеиванию и прилипанию (адгезии) к эндотелию кровеносных сосудов. Антиагреганты способны не только предупреждать агрегацию, но и вызывать дезагрегацию уже агрегированных кровяных пластинок. Применяют их для предупреждения образования послеоперационных тромбов, при тромбофлебитах, тромбозах сосудов сетчатки, нарушениях мозгового кровообращения, а также для предупреждения тромбоэмболических осложнений при ишемической болезни сердца, в том числе и при инфаркте миокарда. [Харкевич Д.А. Фармакология. - М.: ГЭОТАР Медицина, 2000. - 664 с.]
Важное место среди антиагрегантов занимают производные азолов, в первую очередь имидазола, являющимися ингибиторами тромбоксансинтетазы. [Демина О.В., Ходонов А.А., Швец В.И., Варфоломеев С.Д. Агрегация тромбоцитов человека: молекулярно-кинетические механизмы и пути регуляции. // Биолог. мембраны. - 2002. - Т.19, №2. - С.115-152.]
После стимуляции клетки, арахидоновая кислота высвобождается из мембранных фосфолипидов и превращается в результате последовательности ферментных реакций (каскад арахидоновой кислоты) во множество различных производных метаболитов по двум основным путям - липоксигеназному и циклооксигеназному. Продуктами циклооксигеназного пути являются широко распространенные простагландины, из устойчивого простациклина PGH2, образуется как простациклин (PGI2), образующийся в эндотелии сосудов, так и тромбоксан (TxA2), который синтезируется в тромбоцитах. При ряде заболеваний наблюдается дисбаланс между этими двумя эйкозаноидами, перепроизводство тромбоксана A2, выявлено при многих паталогических состояниях. Ингибиторы тромбоксансинтетазы, например, дазоксибен, блокируют биосинтез тромбоксана, при этом наблюдается конверсия тромбоцитарных эндоперекисей (PGH2) в простациклин PGI2, что способствует повышению атромбогенных свойств сосудистой стенки, ингибированию адгезии тромбоцитов, их агрегации и коагуляции, а также может сопровождаться понижением давления. [Garsia-Szabo R.R., Peterson M.B., Watkins W.D. et al. Thromboxane generation after thrombin. Protective effect of thromboxane synthetase inhibition on lang fluid balance. // Circ. Res. - 1983. - Vol.53, N2. - P.214-222.]
Многие антиагреганты - ингибиторы тромбоксансинтетазы применяют в качестве вазодилаторов, антигипертензивных препаратов, антиангинальных средств, церебровазодилаторов, коронарных вазодилаторов, средств лечения бронхиальной астмы и ринита.
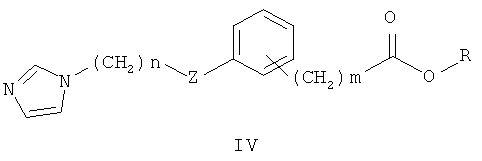
Наиболее близкими к заявленным замещенным O-[ω-(азол-1-ил)алкил]-N-фенилкарбаматам по применению в качестве антиагрегантов, в том числе в составе фармацевтической композиции, являются феноксиалкилимидазолы общей формулы IV, где R означает водород или алкил; с числом метиленовых групп n от 1 до 9; m от 0 до 8; Z означает атом О, S или NH группа [патент США №4632934. - Заявл. - 21.08.1979], которые ингибируют тромбоксансинтетазу и за счет этого находят применение как антигипертензивные противовоспалительные, противотромбоэлические средства. [Cross P.E., Dickinson R.P., Parry M.J., Randall M.J. Selective tromboxane synthetase Inhibitors. I. 1-[(Aryloxy)alkyl]-1H-imidazoles. // J. Med. Chem. - 1985. - Vol.28. - P.1427-32.]
Известны способы получения (азол-1-ил)метанолов, взаимодействием имидазола или 1,2,4-триазола с формалином [патент Германии №2618756, МКИ C07D 233/64, заявл. - 28.04.1976, опубл. - 03.11.1977; Alley P.W. The imidazole-formaldehyde reaction. Formation of 1-imidazolemethanol. // J. Org. Chem. - 1975. - Vol.40, №12. - P.375-376.] или параформом [Европейский патент №60222, МКИ C07D 249/08, заявл. 10.03.81, опубл. 15.09.82].
Известны способы получения 2-(азол-1-ил)этанолов, взаимодействием имидазола или 1,2,4-триазола с этиленкарбонатом [Banfi A., Sala A., Soresinetti A. Synthesis of New Imidazole Derivatives as Potential Inhibitors of Thromboxane Synthetase. // J. Heterocyclic. Chem. - 1990. - Vol.27, №2. - P.215-219.] или этиленхлоргидрином в присутствии гидроксида натрия в условиях межфазного катализа [Асратян Г.В., Аттарян О.С., Погосян А.С., Элиазян Г.А., Дарбинян Э.Г., Мацоян С.Г. Алкилирование азолов β-функционально замещенными галогеналкилами в условиях межфазного катализа. // Журн. прикл. хим. - 1986. - №6. - С.1296-1300].
Техническая задача, данного изобретения состоит в увеличении эффективности антиагрегационных лекарственных средств и расширении ассортимента гематотропных препаратов.
Поставленная задача решается получением соединений общей формулы I, обладающих антиагрегационной активностью, а также в увеличении эффективности антиагрегационных средств за счет применения замещенных O-[ω-(азол-1-ил)алкил]-фенилкарбаматов I и расширении ассортимента гематотропных препаратов.
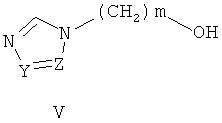
Согласно настоящему изобретению, замещенные O-[ω-(азол-1-ил)алкил]-фенилкарбаматы общей формулы I, получают взаимодействием ω-(азол-1-ил)-1-алканолов V,
где Z и Y означают CH-группу, или одновременно являются цепью C-CH=CH-CH=CH-C составляющую вместе аннелированное кольцо, m означает 1, с замещенными фенилизоцианатами VI, где R одинаковые или разные означают алкоксикарбонильную группу, сульфамоилгруппу, n означает целое число групп от 0 до 1, а также взаимодействием ω-(азол-1-ил)-1-алканолов V, где Y означают CH-группу, Z означает атом азота, m означает целое число от 1 до 3, Z и Y означают CH-группу, или одновременно являются цепью C-CH=CH-CH=CH-C составляющую вместе аннелированное кольцо, m означает целое число от 2 до 3, с замещенными фенилизоцианатами VI, где R одинаковые или разные означают атом водорода, галогена, алкильную группу с числом атомов углерода от 1 до 4, алкоксигруппу с числом атомов углерода от 1 до 4, перфторалкильную группу с числом атомов углерода от 1 до 4, нитрогруппу, алкоксикарбонильную группу, сульфамоилгруппу, n означает целое число групп от 0 до 2, в полярных апротонных растворителях, например, абсолютном ацетонитриле, тетрагидрофуране, диоксане, γ-бутиролактоне и др. при температуре от 20 до 100°C.
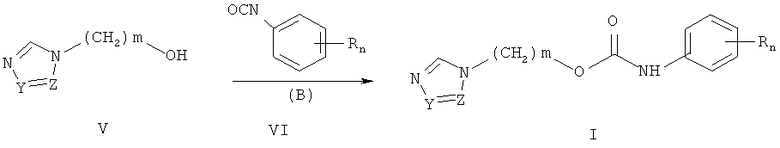
По второму способу соединения общей формулы I получают взаимодействием ω-(азол-1-ил)-1-алканолов V, где Z и Y означают атом азота или CH-группу, или одновременно являются цепью C-CH=CH-CH=CH-C составляющую вместе аннелированное кольцо; m означает целое число от 1 до 3, с замещенными фенилизоцианатами VI, где R одинаковые или разные означают атом водорода, галогена, алкильную группу с числом атомов углерода от 1 до 4, алкоксигруппу с числом атомов углерода от 1 до 4, перфторалкильную группу с числом атомов углерода от 1 до 4, нитрогруппу, алкоксикарбонильную группу, сульфамоилгруппу, n означает целое число атомов от 0 до 2; в полярных апротонных растворителях, например, абсолютном ацетонитриле, тетрагидрофуране, диоксане, γ-бутиролактоне и др. при температуре от 20 до 100°C. в присутствии органических оснований в качестве катализаторов, например, триэтиламина, пиридина, 1,8-диазабицикло[5,4.0]ундец-7-ена (ДБУ), 1,4-диазабицикло[2.2.2]октана, гидроксида тетрабутиламмония и др. в количестве от 0,1 до 20% мольн.
Использование основного катализатора позволяет сократить время взаимодействия и увеличить выход целевых замещенных O-[ω-(азол-1-ил)алкил]-N-фенилкарбаматов общей формулы I.
В приведенной схеме R, n, m, Z и Y имеют те же значения, что и в формуле I; В означает основание, например, триэтиламин, ДБУ и т.п.
Техническим результатом изобретения являются новые вещества - замещенные O-[ω-(азол-1-ил)алкил]-N-фенилкарбаматы общей формулы I и способ их получения. В указанном патенте [патент США №3915984, МКИ C07D 235/06. - Заявл. - 07.12.1973.] имидазол-1-илметил- и бензимидазол-1-илметил-N-арилкарбаматы предлагают получать без выделения индивидуальных промежуточных азолилметанолов, что ухудшает качество целевых O-(азол-1-илметил)-N-арилкарбаматов и снижает их выход. Мы предлагаем проводить ацилирование индивидуальных азолилалканолов арилизоцианатами в эквимолярных соотношениях, что позволяет получить более чистые замещенные O-[ω-(азол-1-ил)алкил]-N-фенилкарбаматы общей формулы I.
Лекарственные средства, используемые при лечении заболеваний, могут быть включены в состав различных лекарственных форм: таблеток, порошков, гранул, капсул, эмульсий, мазей, инъекционных форм. При изготовлении фармацевтической композиции, помимо активного вещества в состав включают вспомогательные вещества. В состав лекарственной формы например, в форме таблеток, в качестве вспомогательных веществ могут быть включены глюкоза, лактоза, крахмал, твердые растительные масла, каолин, тальк, стеарат магния и др. При создании инъекционной фармацевтической композиции, лекарственное вещество растворяют или суспендируют в воде, изотоническом растворе, этаноле, пропиленгликоле и т.п. Лекарственный препарат может содержать буферные вещества, красители, подсластители и другие фармацевтически подходящие добавки.
Техническим результатом изобретения также является разработка антиагрегационных фармацевтических композиций, состоящих из замещенных O-[ω-(азол-1-ил)алкил]-N-фенилкарбаматов общей формулы I в концентрации 0,1-99% и вспомогательных веществ, которые успешно могут быть применены для лечения и профилактики стенокардии, атеросклероза периферических артерий и проявлений атеротромбоза, для предупреждения развития тяжелых сосудистых осложнений, инфаркта миокарда, инсультов. Замещенные O-[ω-(азол-1-ил)алкил]-N-фенилкарбаматы формулы I являющиеся антиагрегантами, превосходят по активности известный антиагрегационный препарат дазоксибен (гидрохлорид 4-[2-(имидазол-1-ил)этокси]бензойной кислоты) [J. Med. Chem. - 1985. - Vol.28. - P.1427-32], что позволяет при их включении в состав фармацевтических композиций увеличить эффективность антиагрегационных лекарственных средств и расширить ассортимент гематотропных препаратов. Эффект замещенных O-[ω-(азол-1-ил)алкил]-N-фенилкарбаматов формулы I в экспериментах in vitro проявлялся в диапазоне фармакологически приемлемых концентраций 10-3-10-6 М, при этом оптическая плотность плазмы снижалась до 16%. Исследуемые соединения, например, карбамат 63 превосходили эталон дазоксибен, при агрегации вызываемой АДФ.
Изобретение может быть проиллюстрировано следующими примерами:
Пример 1. (1H-Имидазол-1-ил)метанол (1).
Смесь 13.6 г (0.2 моль) имидазола, 6,0 г (0.2 моль) параформа и 0.2 мл триэтиламина при перемешивании нагревают до 90°C в течение 2 часов, охлаждают и перекристаллизовывают из ацетона. Получают 18.0 г (92%) (1H-имидазол-1-ил)метанола (1) с т.пл. 60-62°C.
Аналогично получены (1H-1,2,4-триазол-1-ил)метанол (2) и (1H-бензимидазол-1-ил)метанол (3) (Таблица 1 и 2).
Пример 2. 2-(1H-Имидазол-1-ил)этанол (4).
К смеси 10,2 г (0,15 моль) 1H-имидазола, 6,0 г (0,15 моль) гидроксида натрия, 1,13 г (0,005 моль) хлорида триэтилбензиламмония и 50 мл диоксана нагретой до 35°C при интенсивном перемешивании добавляют 10 мл (12.07 г, 0,15 моль) этиленхлоргидрина в течение 2-х часов, выдерживают реакционную массу еще в течение 8 часа при той же температуре, выпавший осадок отфильтровывают и промывают диоксаном. Фильтрат упаривают в вакууме водоструйного насоса, а остаток перегоняют в вакууме масляного насоса. Получают 11.13 г (82%) 2-(1H имидазол-1-ил)этанола (4) с т.кип. 138-141°C/0.5 Торр, nD 18=1.5144, т.пл. 34-35°C.
Пример 3. 2-(1Н-1,2,4-Триазол-1-ил)этанол (5).
В 20 мл толуола растворяют при перемешивании 6.9 г (0.1 моль) 1H-1,2,4 триазола и 10.8 г (0.12 моль) этиленкарбоната, выдерживают при 80°C в течение 3.5 ч. Реакционную массу охлаждают, разделяют слои, нижний слой перегоняют в вакууме масляного насоса. Получают 7.1 г (63%) 2-(1Н 1,2,4-триазол-1-ил)этанола (5) с т.кип. 140-150°C/1 Торр, т.пл. 53-55°C (из эфира).
Пример 4. 2-(1H-Бензимидазол-1-ил)этанол (6).
Через раствор 23.6 г (0.2 моль) 1H-бензимидазола и 0.80 г (0.02 моль) гидроксида натрия в 90 мл этанола, нагретый до температуры 60°C в течение 1.5 ч пропускают ток 10.03 г (0.228 моль) этиленоксида, выдерживают при 70°C в течение 2 ч. Реакционную массу охлаждают, добавляют 1.76 мл (2.08 г, 0.205 моль) 36%-ной соляной кислоты, осадок отфильтровывают, из фильтрата отгоняют растворитель в вакууме водоструйного насоса, остаток перегоняют в вакууме масляного насоса. Получают 29.4 г (90%) 2-(1H-бензимидазол-1-ил)этанола (6) с т.кип. 190-192°C/0.15 Торр, т.пл. 103-104°C (из толуола).
2(1H-Азол-1-ил)этанолы могут быть получены аналогично примерам 2-4 способами (Таблицы 1 и 2).
ЯМР 1Н-спектры записаны на приборе «Broker AC-200» и «Broker Avance II 300» (рабочая частота 200 и 300 МГц), сдвиги измерены относительно тетраметилсилана, в качестве растворителя использовали d6-ДМСО. ИК-спектры регистрировали с призмами NaCl и KBr в тонкой пленке в вазелиновом масле на спектрометре «Specord M80».
ние
Пример 5. Этил-2-[(1H-имидазол-1-ил)метоксикарбониламино]бензоат (7).
К раствору 0.98 г (0.01 моль) (1H)имидазол-1-илметанола (1) в 20 мл абсолютного ацетонитрила добавляют 1.91 г (0,01 моль) этил-2-изоцианатобензоата, перемешивают в течение 2 ч, выпавший осадок отфильтровывают и перекристаллизовывают из изопропанола. Получают 1.16 г (40%) этил-2-[(1H-имидазол-1-ил)метоксикарбониламино]бензоата (7) с т.пл. 69-70°C.
Пример 6. O-[1-(1Н-1,2,4-Триазол-1-ил)метил]-N-фенилкарбамат (8).
К раствору 0.99 г (0.01 моль) (1H-1,2,4-триазол-1-ил)метанола (2) в 20 мл абсолютного ацетонитрила добавляют 1.19 г (0,01 моль) фенилизоцианата, перемешивают в течение 6 ч, выпавший осадок отфильтровывают, промывают 5 мл ацетонитрила, растворяют в 10 мл горячего метанола, отфильтровывают, фильтрат упаривают наполовину и охлаждают. Получают 0.58 г (24%) O-[1-(1Н-1,2,4-триазол-1-ил)метил]-N фенилкарбамата (8) с т.пл. 139-140°C.
Пример 7. Этил-4-[(1H-бензимидазол-1-ил)метоксикарбониламино]бензоат (9).
К раствору 1.095 г (7.4 ммоль) (1H)бензимидазол-1-илметанола (3) в 20 мл абсолютного ацетонитрила добавляют 1.414 г (7.4 моль) этил-4-изоцианатобензоата, перемешивают в течение 2 ч, выпавший осадок отфильтровывают. Получают 1.76 г (70%) этил-4-[(1H-бензимидазол-1-ил)метоксикарбониламино]бензоата (9) с т.пл. 192-194°C.
Аналогично примерам 5-7 получены замещенные O-(азол-1-илметил)-N-фенилкарбаматы (Таблица 3 и 4).
ние
Пример 8. O-[2-(1H-Имидазол-1-ил)этил]-N-(4-фторфенил)карбамат (40).
К раствору 1.123 г (0.01 моль) 2-(1H-имидазол-1-ил)этанола (4) в 20 мл абсолютного ацетонитрила добавляют 1.371 г (0,01 моль) 4-фторфенилизоцианата и 0.007 г (0.07 ммоль) триэтиламина, перемешивают в течение 1 ч, выпавший осадок отфильтровывают и промывают ацетонитрилом. Получают 1.28 г (51%) O-[2-(1H-имидазол-1-ил)этил]-N-(4-фторфенил)-карбамата (40). с т.пл. 125-127°C.
Пример 9. O-[2-(1H-1,2,4-Триазол-1-ил)этил]-N-фенилкарбамат (41).
К раствору 2.3 г (0.02 моль) 2-(1Н-1,2,4-триазол-1-ил)этанола (5) в 10 мл γ-бутиролактона добавляют 2.4 г (0.02 моль) фенилизоцианата, нагревают на кипящей водяной бане в течение 0.5 ч, охлаждают, осадок отфильтровывают, перекристаллизовывают из изопропилового спирта. Получают 2.3 г (50%) O-[2-(1Н-1,2,4-триазол-1-ил)этил]-N-фенилкарбамата (41) с т.пл. 140-142°C.
Пример 10. O-[2-(1H-Бензимидазол-1-ил)этил]-N-(3-трифторметилфенил)карбамат (42).
К раствору 1.62 г (10 ммоль) 2-(1H-бензимидазол-1-ил)этанола (6) в 25 мл абсолютного ацетонитрила добавляют 1.346 г (7.2 моль) 3-трифторметилрфенилизоцианата перемешивают в течение 2 ч, выпавший осадок отфильтровывают. Маточник упаривают досуха и перекристаллизовывают из изопропанола. Получают 2.473 г (99%) O-[2-(1H-бензимидазол-1-ил)этил]-N-(3-трифторметилфенил)карбамата(42) с т.пл. 179-181°C.
Аналогично примерам 8-10 получены замещенные O-(азол-1-илэтил)-N-фенилкарбаматы (Таблица 5 и 6).
Пример 11. Гидрохлорид этил-4-[2-(1H-имидазол-1-ил)этоксикарбониламино]бензоата (60). К раствору 0.454 г (1.5 ммоль) этил-4-[2-(1H-имидазол-1-ил)этоксикарбониламино]бензоата (45) в 5 мл метилового спирта при перемешивании добавляют 1.5 мл (2.25 ммоль) 1,5 М раствора хлороводорода в метаноле. Растворитель отгоняют в вакууме водоструйного насоса досуха. Получают 0.494 г (97%) гидрохлорида этил-4-[2-(1H-имидазол-1-ил)этоксикарбониламино]бензоата (60) с т.пл. 184-185°C.
Аналогично получены гидрохлориды замещенных O-[ω-(азол-1-ил)алкил]-N-фенилкарбаматов: из O-[1-(1Н-имидазол-1-ил)метил]-N-(3-трифторметилфенил)карбамата (20) гидрохлорид O-[1-(1Н-имидазол-1-ил)метил]-N-(3-трифторметилфенил)карбамата (61) с т.пл. 118-119°C; из этил-4-[(1Р-1,2,4-триазол-1-ил)метоксикарбониламино]бензоата (29) гидрохлорид этил 4-[2-(1Н-1,2,4-триазол-1-ил)метоксикарбониламино]бензоата (62) с т.пл. 177-178°C, из O-[2-(1Н-имидазол-1-ил)этил]-N-(3-трифторметилфенил)карбамата (50) гидрохлорид O-[2-(1Н-имидазол-1-ил)этил]-N-(3-трифторметилфенил)карбамата(63) с т.пл. 124-125°C.
Пример 12. Проведение испытаний замещенных O-[ω-(азол-1-ил)алкил]-N-фенилкарбаматов на наличие антиагрегационной активности in vitro.
Методика проведения эксперимента. Богатую тромбоцитами плазму (в среднем 3×108 в 1 см3 тромбоцитов) получали центрифугированием свежеполученной крови здоровых доноров (стабилизатор - 3.8%-ный цитрат натрия, соотношение крови и раствора цитрата 9:1) в течение 10 минут при 1000 об/мин при комнатной температуре. До проведения эксперимента и в конце его, в каждом образце подсчитывали количество тромбоцитов. В том случае, если плазма содержала большее количество кровяных пластинок, то ее разводили до необходимого количества безтромбоцитарной плазмой, полученной центрифугированием цитратной крови в течение 10 минут при 3000 об/мин. В качестве индуктора агрегации использовали АДФ, коллаген (НПО «РЕНАМ», Россия). Агрегацию тромбоцитов изучали методом светорассеяния по методу Вот [Born J.V.R. Aggregation of blood platelets by adenosine diphosphate and its reversal // Nature - 1962. - V.194., N5. - P.927-929. Born J.V.R. Quantitative investigation into the aggregation of blood platelets // J. Physiol. - 1962. - V.162., N4. - P.487-511], на агрегомегре фирмы «CHRONO-LOG» (США).
Условия проведения эксперимента: 37°C, объем богатой тромбоцитами плазмы 450 мкл, объем фармацевтической композиции в виде раствора исследуемого вещества в воде 50 мкл, время прединкубации с препаратом ингибитора 5 минут при перемешивании, объем индуктора агрегации 50 мкл, конечная концентрация для АДФ 1×10-5 М, коллагена - 0,2 мг/мл. (В качестве контроля использовали богатую тромбоцитами плазму в объеме 450 мл.) Количественной характеристикой степени агрегации служило относительное падение оптической плотности на максимуме амплитуды агрегатограммы. В процессе записи наблюдали изменение оптической плотности исследуемой плазмы в диапазоне 100% (богатой тромбоцитами плазмы) до 0% (безтромбоцитарная плазма) (длина волны зондированного светового потока 660 нм). Результат выражали в процентах падения оптической плотности на максимуме амплитуды агретограммы. Были проведены эксперименты сравнения антиагрегационных свойств веществ и эталона, известного препарата дазоксибена.
Пример 14. Композиция для изготовления таблеток
O-[2-(1Н-Имидазол-1-ил)этил]-N-(3-трифторметилфенил)карбамат (50) - 20 мг,
Пшеничный крахмал - 10 мг,
Лактоза - 67 мг,
Стеарат магния - 3 мг.
Часть пшеничного крахмала используют для приготовления гранулированной пасты крахмала, которую вместе с остатками пшеничного крахмала гранулируют, просеивают и смешивают с активным инградиентом и стеаратом магния. Смесь прессуют в таблетки 100 мг каждая.
Подобным же образом изготавливают таблетки, активным инградиентом которых являются другие замещенные O-[ω-(азол-1-ил)алкил]-N-фенилкарбаматы.
Пример 15. Раствор для инъекций:
Гидрохлорид O-[2-(1Н-имидазол-1-ил)этил]-N-(3-трифторметилфенил)карбамата (63) растворяют в воде или физиологическом растворе из расчета 30 мг/мл. Для инъекций используют свежеприготовленный раствор.
Подобным же образом готовят растворы. Активным инградиентом которых являются фармацевтически приемлимые соли других O-[ω-(азол-1-ил)алкил]-N-арилкарбаматов.
Применение O-[ω-(азол-1-ил)алкил]-N-арилкарбаматов формулы I в качестве антиагрегантов в медицине позволяет увеличить эффективность антиагрегационных лекарственных средств и расширить ассортимент гематотропных препаратов. По проявленному эффекту в эксперементах in vitro некоторые исследуемые соединения, например, карбамат 63 превосходили эталон дазоксибен при агрегации вызываемой АДФ. Таким образом указанные соединения могут расширить арсенал лекарственных препаратов применяемых при заболеваниях сердечно-сосудистой системы.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 2-(АЗОЛ-1-ИЛ)ЭТАНАМИНОВ | 2006 |
|
RU2317984C2 |
| ЗАМЕЩЕННЫЕ 1-(ПИРИДИНИЛ-2)-2-АЗОЛИЛЭТАНОЛЫ, ИХ СПОСОБ ПОЛУЧЕНИЯ И ФУНГИЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2004 |
|
RU2301227C2 |
| ПРИМЕНЕНИЕ ЗАМЕЩЕННЫХ 1-(2-ФЕНОКСИЭТИЛ)-1,2,4-ТРИАЗОЛОВ В КАЧЕСТВЕ ФУНГИЦИДНЫХ СРЕДСТВ И ФУНГИЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2005 |
|
RU2329646C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-[2-(МОРФОЛИН-4-ИЛ)ЭТИЛ]-4-ХЛОРБЕНЗАМИДА (ВАРИАНТЫ) | 2014 |
|
RU2570898C2 |
| 1-(ПИРИДИНИЛ-2)-2-АЗОЛИЛ-1-(ФТОРФЕНИЛ)ЭТАНОЛЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФУНГИЦИДОВ | 2004 |
|
RU2267483C2 |
| Способ получения 3-азолилпропанолов | 2022 |
|
RU2786670C1 |
| Замещенные 4-(азол-1-илметил)-1-фенил-5,5-диалкилспиро-[2.5]октан-4-олы, способ их получения (варианты), фунгицидная и рострегуляторная композиции на их основе | 2016 |
|
RU2648240C1 |
| N,N-ДИЗАМЕЩЕННЫЕ НИКОТИНАМИД-(Z)-O-МЕТИЛОКСИМЫ, ОБЛАДАЮЩИЕ ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2010 |
|
RU2442784C1 |
| ЗАМЕЩЕННЫЕ 2-(1,2,4-ТРИАЗОЛ-1-ИЛМЕТИЛ)-6-БЕНЗИЛИДЕН-1,4-ДИОКСАСПИРО[4.5]ДЕКАНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФУНГИЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2006 |
|
RU2326878C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-МЕТИЛ-5-ЗАМЕЩЕННЫХ-1,3,4-ОКСАДИАЗОЛОВ | 2004 |
|
RU2317986C2 |
Описываются новые замещенные O-[ω-(азол-1-ил)алкил]-N-фенилкарбаматы общей формулы I
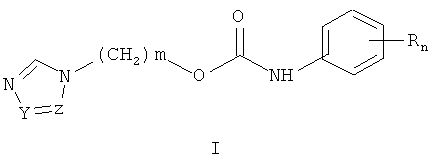
где Z и Y=CH, N или совместно образуют аннелированное кольцо с цепью C-CH-CH-CH=CH-C; или Y=CH, Z означает атом азота, m=1-3; R=Hal, алкил, алкоксикарбонил, сульфамоил, нитро и др., n=0-2, и их фармацевтически приемлемые соли, которые получают ацилированием фенилизоцианатами, соответствующими ω-(азол-1-ил)-1-алканолу в полярных апротонных растворителях при температуре от 20 до 100°C, предпочтительно в присутствии органических оснований в качестве катализаторов. Антиагрегационная активность некоторых замещенных O-[ω-(азол-1-ил)алкил]-N-фенилкарбаматов общей формулы I, например, гидрохлорида O-[2-(1Н-имидазол-1-ил)этил]-N-(3-трифторметилфенил)карбамата выше, чем у эталона дазоксибена. 4 н.п. ф-лы, 7 табл.
1. Замещенные O-[ω-(азол-1-ил)алкил]-N-фенилкарбаматы общей формулы I:
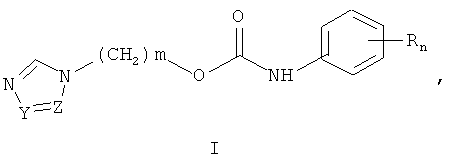
где Z и Y означают CH-группу или совместно образуют аннелированное кольцо с цепью C-CH=CH-CH=CH-C, m означает 1, R означает алкоксикарбонильную группу или сульфамоилгруппу, n означает целое число 0 или 1, или
m означает целое число 2 или 3, тогда R одинаковые или разные и означают атом галогена, алкильную группу, алкоксигруппу перфторалкильную группу, каждая с числом атомов углерода от 1 до 4, нитрогруппу, алкоксикарбонильную группу или сульфамоилгруппу, n означает целое число от 0 до 2, или
Y означают CH-группу, Z означает атом азота, m означает целое число от 1 до 3, тогда R одинаковые или разные и означают атом галогена, алкильную группу, алкоксигруппу, перфторалкильную группу, каждая с числом атомов углерода от 1 до 4, нитрогруппу, алкоксикарбонильную группу или сульфамоилгруппу, n означает целое число от 0 до 2,
или их фармацевтически приемлемые соли.
2. Способ получения замещенных O-[ω-(азол-1-ил)алкил]-N-фенилкарбаматов общей формулы I

где Z и Y означают CH-группу или совместно образуют аннелированное кольцо с цепью C-CH=CH-CH=CH-C, m означает 1, R означает алкоксикарбонильную группу или сульфамоилгруппу, n означает целое число 0 или 1, или
m означает целое число 2 или 3, тогда R одинаковые или разные и означают атом галогена, алкильную группу, алкоксигруппу перфторалкильную группу, каждая с числом атомов углерода от 1 до 4, нитрогруппу, алкоксикарбонильную группу или сульфамоилгруппу, n означает целое число от 0 до 2, или
Y означают СН-группу, Z означает атом азота, m означает целое число от 1 до 3, R одинаковые или разные и означают атом галогена, алкильную группу, алкоксигруппу, перфторалкильную группу, каждая с числом атомов углерода от 1 до 4, нитрогруппу, алкоксикарбонильную группу или сульфамоилгруппу, n означает целое число от 0 до 2, заключающийся в том, что замещенными фенилизоцианатами VI ацилируют ω-(азол-1-ил)-1-алканолы V, где R, Z, Y, m и n имеют те же значения, что и в формуле I, в полярных апротонных растворителях при температуре от 20 до 100°C
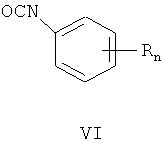
3. Способ получения замещенных O-[ω-(азол-1-ил)алкил]-N-фенилкарбаматов общей формулы I

где Z и Y означают CH-группу или совместно образуют аннелированное кольцо с цепью C-CH=CH-CH=CH-C;
или Y означает CH-группу, Z означает атом азота, m означает целое число от 1 до 3, R одинаковые или разные и означают атом галогена, алкильную группу, алкоксигруппу, перфторалкильную группу, каждая с числом атомов углерода от 1 до 4, нитрогруппу, алкоксикарбонильную группу или сульфамоилгруппу, n означает целое число от 0 до 2, заключающийся в том, что замещенными фенилизоцианатами VI, где R и n имеют указанные выше значения, ацилируют ω-(азол-1-ил)-1-алканолы V, где Z, Y и m имеют указанные выше значения, в полярных апротонных растворителях при температуре от 20 до 100°C в присутствии органических оснований в качестве катализаторов.
4. Фармацевтическая композиция, обладающая антиагрегационным действием, содержащая антиагрегант в концентрации 0,1-99% и вспомогательные вещества, отличающаяся тем, что в качестве антиагреганта используют замещенные O-[ω-(азол-1-ил)алкил]-N-фенилкарбаматы общей формулы I

где Z, Y, m и n имеют указанные в п.3 значения, или их фармацевтически приемлемые соли.
| US 3915984 A, 28.10.1975 | |||
| СИСТЕМА И СПОСОБ КОМПЕНСАЦИИ ВРЕМЕННЫХ ЗАДЕРЖЕК В ОРУЖЕЙНЫХ СИСТЕМАХ | 2013 |
|
RU2618756C1 |
| ПРИМЕНЕНИЕ ЗАМЕЩЕННЫХ 1-(2-ФЕНОКСИЭТИЛ)-1,2,4-ТРИАЗОЛОВ В КАЧЕСТВЕ ФУНГИЦИДНЫХ СРЕДСТВ И ФУНГИЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2005 |
|
RU2329646C2 |
| RU 2007136142 A, 10.04.2009. | |||
Авторы
Даты
2013-07-27—Публикация
2009-03-05—Подача