Изобретение относится к биотехнологии и сельскому хозяйству, а именно к штамму бактерий Fusobacterium necrophorum subspecies necrophorum, депонированном в НИИ ККМ ГНЦ ВБ «Вектор» под номером В-1076 для изготовления диагностических и профилактических препаратов против некробактериоза животных.
Известен ряд штаммов бактерий вида Fusobacterium necrophorum, являющихся возбудителями некробактериоза у сельскохозяйственных животных и людей: Fusobacterium necrophorum subspecies necrophorum штамм FnSI (CAA48747, NCIBI), а также Fusobacterium nucleatum subspecies vincentii штамм АТСС49256 (ZP00143866, NCIBI) и Fusobacterium necrophorum subspecies funduliforme штамм JCM3724.
Наиболее близким техническим решением (прототипом) является штамм АТСС 28256 (ААО 12762, NCIBI) бактерии Fusobacterium necrophorum subspecies necrophorum, используемый для получения диагностических и профилактических препаратов против возбудителей некробактериоза крупного рогатого скота. Однако у данного штамма не определен ряд нуклеотидных последовательностей фрагментов генов: белка оболочки (rpoB), ДНК-гиразы (DNA gyrase В protein gene, TopoisomerasaII), гемагглютинина (ompH).
Технической задачей настоящего изобретения является расширение арсенала штаммов бактерий Fusobacterium necrophorum subspecies necrophorum, которые могут быть использованы для изготовления диагностических и профилактических препаратов против некробактериоза животных. На основе заявляемого штамма возможно дифференцировать выделенные изоляты от других анаэробов, морфологически схожих с Fusobacterium necrophorum, проводить разграничение на подвиды: subspecies necrophorum и subspecies funduliforme, а также проводить подбор производственных культур для изготовления вакцин.
Задача решается новым штаммом бактерий Fusobacterium necrophorum subspecies necrophorum, депонированном в НИИ ККМ ГНЦ ВБ «Вектор» под номером В-1076 для изготовления диагностических и профилактических препаратов против некробактериоза животных.
Штамм, депонированный в НИИ ККМ ГНЦ ВБ «Вектор» под номером В-1076 выделен 02.12.95 года от больной первотелки Высокогорского района Республики Татарстан из хозяйства неблагополучного по некробактериозу. Получен бактериологическим и биологическим исследованием патологического материала методом отбора витальных срезов с последующей их микроскопией, постановкой биопробы на кроликах и изоляцией чистой культуры возбудителя некробактериоза на печеночной питательной среде (среда Китта-Тароцци) в анаэробных условиях. В мазках-отпечатках из патологического материала она имеет форму длинных, иногда переплетающихся, неравномерно окрашенных грамотрицательных нитей, достигающих длины от 10 до 100 мкм, или палочек. Они неподвижны и не образуют спор. Колонии на агарозированной среде росинчатые, серебристые, выпуклые, прозрачные, круглые, диаметром 2-4 мм; на кровяном агаре зона гемолиза 8-10 мм, агглютинирует эритроциты кур в разведении 1:128. Штамм обладает достаточной иммуногенностью, так в реакции непрямой иммунофлуоресценции с гомологичной сывороткой выявляет антиген в разведении 1:5180. Штамм по этим признакам идентифицирован по "Определителю микроорганизмов Берги", как вид Fusobacterium necrophorum и подвид subspecies necrophorum по следующим генам: белка оболочки (RNA polymerase beta subunit (rpoB) в 906 н.п., гемагглютинина (outer membrane protein gene) в 540 н.п., ДНК-гиразы (gyrase В subunit) в 427 н.п., транспозазы (repeated DNA sequence) в 557 н.п.с помощью ПЦР и последующим секвенированием соответствующих фрагментов. Штамм бактерий НИИ ККМ ГНЦ ВБ «Вектор» В-1076 Fusobacterium necrophorum subspecies necrophorum депонирован в НИИ «Коллекция культур микроорганизмов» ФГУП ГНЦ ВБ «Вектор» под номером НИИ ККМ ГНЦ ВБ «Вектор» В-1076 от 8 сентября 2005 года.
Выделенный штамм бактерий некробактериоза вызывает хроническую инфекционную болезнь, характеризующуюся гнойно-некротическим поражением кожи, слизистых оболочек, конечностей и паренхиматозных органов.
Культуральные и морфологические особенности штамма: грамотрицательные нити и разной длины палочки, не спорообразующие, неподвижные, расположенные в виде сплетений, колонии на агарозированной среде росинчатые, серебристые, выпуклые, прозрачные, круглые, диаметром 2-4 мм; на кровяном агаре зона гемолиза 8-10 мм, агглютинирует эритроциты кур в разведении до 1:128. Продуцирует индол и сероводород. Ферментирует с образованием масляной кислоты и незначительного количества газа глюкозу, сахарозу, мальтозу, манит, дульцин, инулин. Слабо ферментирует лактозу. Образовывает термолабильный экзотоксин, вызывающий гибель белых мышей на 1 -2 сутки после их внутрибрюшинного заражения.
Активность (продуктивность) штамма (с указанием условий культивирования), другие производственные показатели: в среде Китта-Тароцци растет при +37°С в течение 24 часов в виде обильного помутнения, в начале в нижних слоях, затем и всей среды. При последующем культивировании выпадает рыхлый осадок, и среда становится прозрачной.
Способ определения активности штамма с указанием метода. При подкожном заражении суточной бульонной культурой белые мыши погибают на 4-5 сутки, кролики - на 8-10 сутки с выраженным гнойно-некротическим поражением тканей на месте введения и обширными поражениями паренхиматозных органов (легкие, сердце, печень). В РНИФ с гемологичной сывороткой титр антигена 1:5180, с гетерологичными 1: 320-1: 640.
Способ, условия и состав сред для длительного хранения штамма: лиофилизация и в нативном виде в среде Китта-Тароцци с добавлением 10% нормальной сыворотки крупного рогатого скота, а также путем замораживания в питательной среде с добавлением глицерина.
Способ, условия и состав сред для размножения: среда Китта-Тароцци с добавлением 10% нормальной сыворотки крупного рогатого скота. Условия и состав среды для ферментации: в условиях термостата в бутылях - стационарно и в реакторах в среде, приготовленной на основе перевара Хоттингера под вазелиновым маслом с добавлением 10% нормальной сыворотки крупного рогатого скота, при температуре 37°С и рН 7,2-7,6.
Генетические особенности штамма: прототроф, в качестве фактора роста использует нормальную сыворотку, устойчив к стрептомицину, мономицину, неомицину.
Изобретение иллюстрируется следующими примерами.
Пример 1. Выделение штамма. Штамм, депонированный в НИИ ККМ ГНЦ ВБ «Вектор» под номером В-1076 Fusobacterium necrophorum subspecies necrophorum был выделен от больной первотелки из хозяйства, неблагополучного по некробактериозу. При гнойно-некротическом процессе в области пальца удаляют омертвевшие ткани. На границе живой и некротизированной тканей копытец делают соскобы. Из соскобов делают мазки и окрашивают по Романовскому-Гимза и Граму. В мазках из патологического материала были видны грамотрицательные нити разной длины или палочки. Такие соскобы подвергают бактериологическому и биологическому исследованию.
При бактериологическом исследовании из патологического материала делают 10% суспензию на стерильном физиологическом растворе или мясопептонном бульоне и высевают на среду Китта-Тароцци с добавлением до 10% нормальной сыворотки крупного рогатого скота. Среду Китта-Тароцци перед посевом регенерируют прогреванием в кипящей водяной бане в течение 20-30 мин, после чего быстро охлаждают до 45-50°С. Выращивают культуру в термостате при температуре +37°С в течение 5 суток при ежедневном просматривании. Через 14-24 часа в среде Китта-Тароцци Fusobacterium necrophorum образует нитевидную муть вначале в нижних слоях среды, а позднее в верхних, газообразование очень слабое. На 5 сутки наступает просветление бульона, при этом на дно пробирки выпадает осадок. При микроскопировании мазков из культуры обнаруживают зернисто окрашенные длинные переплетающиеся нити, имеющие местами колбовидные расширения.
Бактериологическое исследование проводят для получения чистой культуры. С этой целью одновременно с посевом на питательную среду проводят заражение кролика. Для этого заражают исходной 10% суспензией патологического материала или суточной бульонной культурой под кожу средней трети наружной поверхности уха в дозе 0,5-1,0 мл. Наблюдение за зараженным животным ведут в течение 10 суток.
При наличии в патологическом материале или исследуемой культуре Fusobacterium necrophorum у зараженного животного на месте инъекции через 4-7 дней развивается сухой некроз. Из очага некроза делают высевы на среду Китта-Тароцци и мазки, которые окрашивают по Граму. При обнаружении в мазках зернисто окрашенных нитей биопробу считают положительной, а культуру Fusobacterium necrophorum - выделенной.
Таким образом, использование микробиологических и биологических методов позволяет выделить культуру Fusobacterium, возбудителя некробактериоза животных и идентифицировать, как вид Fusobacterium necrophorum.
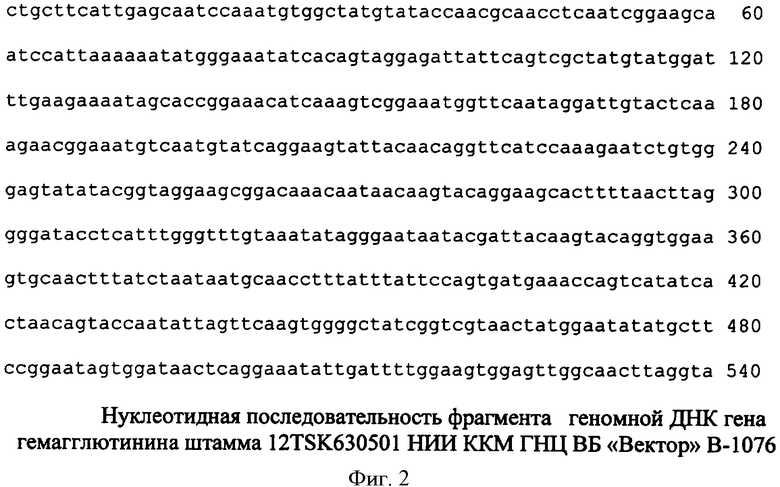
Пример 2. Генотипирование штамма. Проводят полимеразные цепные реакции по синтезу фрагментов ДНК различных генов штамма. В качестве праймеров используют первые и последние 18-20 нуклеотидов ниже приведенных нуклеотидных последовательностей. Затем проводят секвенирование синтезированных фрагментов ДНК соответствующих фрагментов генов: белка оболочки, гемагглютинина, ДНК-гиразы и транспозазы. (рис.1-4) Определение нуклеотидной последовательности фрагментов проводят по двум цепочкам ДНК, используя общепринятую методику Максама-Гилберта. При анализе нуклеотидных последовательностей фрагментов вышеназванных генов с прототипом было установлено, что фрагменты ДНК в 906 н.п.гена rpoB (RNA polymerase beta subunit), в 540 н.п.гена ompH (outer membrane protein gene) штамма НИИ ККМ ГНЦ ВБ «Вектор» В-1076 совпадают с последовательностью Fusobacterium necrophorum subsp.necrophorum шт.АТСС25286 (AF527637).
Ген гемагглютинина отсутствует у Fusobacterium necrophorum subsp.funduliforme и Fusobacterium nucleatum. Нуклеотидная последовательность в 427 н.п. фрагмента гена фермента ДНК-гиразы (gyrase В subunit) штамма НИИ ККМ ГНЦ ВБ «Вектор» В-1076 совпадала с нуклеотидной последовательностью штаммов Fusobacterium necrophorum subsp.necrophorum NCTC10576 (AY372007), Fnl (AY370663) и Fusobacterium necrophorum subsp.funduliforme Fn45 (AY370665). Нуклеотидная последовательность ДНК в 557 н.п. гена транспозона (repeated DNA sequence) штамма НИИ ККМ ГНЦ ВБ «Вектор» В-1076 совпадает с нуклеотидной последовательностью штамма FnS1 Fusobacterium necrophorum subsp.necrophorum (CAA48747, NCIBI), что подтверждает его отношение к семейству Fusobacterium. На основании результатов генотипирования по генам белка оболочки, ДНК-гиразы штамм НИИ ККМ ГНЦ ВБ «Вектор» В-1076 отнесен к виду Fusobacterium necrophorum и по генам гемагглютинина и транспозона к подвиду (subspecies) necrophorum.
Для дополнительного подтверждения принадлежности штамма, депонированного в НИИ ККМ ГНЦ ВБ «Вектор» под номером В-1076 к Fusobacterium necrophorum subsp.necrophorum проводят изучение полиморфизма длин рестрикционных фрагментов (ПДРФ) синтезируемого гена транспозона. С этой целью осуществляют синтез с помощью гнездовых праймеров внутреннего фрагмента в 289 н.п., применяя гнездовые праймеры согласно протоколу, описанному в «Способе выявления Fusobacterium necrophorum в гнездовой ПЦР» №2203951 от 10.05.03. Затем проводят гидролиз эндонуклеазой MspI (C'CGG) ампликона и анализируют с помощью электрофореза в 2% агарозе. Получают генетический профиль, состоящий из двух фрагментов длиной в 170 и 119 н.п. Маркером служит ДНК pUC18, гидролизованная AluI. Получаемый генетический профиль внутреннего фрагмента транспозона подтверждает принадлежность штамма НИИ ККМ ГНЦ ВБ «Вектор» В-1076 к Fusobacterium necrophorum subsp.necrophorum.
Таким образом, проведенное генотипирование позволяет идентифицировать культуру, выделенную с помощью микробиологических и биологических методов, как штамм Fusobacterium necrophorum subspecies necrophorum НИИ ККМ ГНЦ ВБ «Вектор» В-1076.
Пример 3. По результатам генотипирования штамма Fusobacterium necrophorum subspecies necrophorum, депонированного в НИИ ККМ ГНЦ ВБ «Вектор» под номером В-1076 был разработан «Способ выявления Fusobacterium necrophorum в гнездовой ПЦР» №2203951 от 10.05.03, на основе которого была разработана «Тест-система для выявления Fusobacterium necrophorum subsp.necrophorum методом полимеразной цепной реакции (ПЦР) с помощью гнездовых праймеров», прошедшая государственные комиссионные испытания.
Пример 4. Для изготовления диагностической тест-системы, выявляющей оба патогенных подвида Fusobacterium necrophorum, выбираются праймеры в последовательностях общих для этих подвидов - это последовательность ДНК гена гроВ, кодирующего один из белков клеточной мембраны или последовательность ДНК-гиразы. В качестве праймеров используют 18-20 нуклеотидов последовательности ДНК. Один из них прямой в районе 5', а другой обратный - в районе 3' конца, так чтобы между праймерами заключался фрагмент в 300-500 нуклеотидных пар.
Выделение ДНК Fusobacterium necrophorum из биологических образцов. Из фрагмента соскоба с пораженного участка копыт готовят 20% суспензию на 0,9% NaCl. Далее к 50 мкл суспензии добавляют 500 мкл подогретого 10% СТАВ, перемешивают и инкубируют при 80°С в течение 2 часов. Затем добавляют в половинном объеме смеси: фенол/хлороформ/изоамиловый спирт (25:24:1) и центрифугируют 10 минут при 13000 об/мин. Водную фазу переносят в другую пробирку и прибавляют 1/10 объема 3 М ацетата натрия рН 4,8 и 2 объема этанола и выдерживают 40 минут или ночь при -20°С. Преципитат ДНК осаждают скоростным центрифугированием. Осадок ДНК растворяют в 20-30 мкл стерильной бидистиллированной воды или 10 мМ ТЕ-буфере рН 8,0.
Полимеразную цепную реакцию проводили в течение 27 циклов в следующем режиме: предварительный нагрев ДНК при 95°С в течение 3,0 мин - 1 цикл; далее 25 циклов по три сегмента в каждом: денатурация ДНК при 94°С в течение 0,3 мин, гибридизация при 56°С в течение 0,4 мин, элонгация при 72°С в течение 0,5 мин и 1 цикл - досинтез при 72°С в течение 1,2 мин. О положительном результате анализа судят, сопоставляя к размеру в положительном контроле ДНК, которые должны совпадать.
Пример 5. В случае выявления только более патогенного подвида Fusobacterium necrophorum subsp.necrophorum праймеры выбирают, взяв за основу последовательность ДНК гена гемагглютинина. Остальные операции аналогичны описанным в примере 4.
Пример 6. Изготовление вакцинного препарата для профилактики заболевания животных некробактериозом включает следующие этапы:
1. Приготовление матриксной расплодки. 1-2 мл культуры данного штамма вносят в 200 мл флакон, содержащий 80-100 мл среды Китта-Тароцци, и по 0,1 мл в пробирку с этой же средой. Посевы культивируют 18-20 часов при +37°С. Выращенную культуру проверяют на чистоту, сделав мазок и окрасив по Граму.
2. Чистую культуру из флаконов засевают в 10-ти литровую бутыль (или реактор) со средой Китта-Тароцци, заполненную на половину объема. Параллельно вновь проводят посевы в пробирку со средой Китта-Тароцци для контроля чистоты. Культуру в бутыле выращивают при плавном перемешивании с добавлением 40% глюкозы до конечной концентрации 0,2% при +37°С и рН среды 7,6.
3. После окончания выращивания определяют концентрацию микробных тел в культуре по оптическому стандарту мутности и чистоту культуры путем высева в пробирки на среду Китта-Тароцци для контроля чистоты. Выращенную бактериальную массу в бутыле разводят стерильным физиологическим раствором до концентрации 10 млрд микробных тел в 1 мл.
4. К бактериальной массе добавляют при постоянном перемешивании формалин, разведенный физиологическим раствором 1:1 с таким расчетом, чтобы его концентрация в культуре была 0,3% и тимерсал в количестве 0,1 г на литр культуры. Инактивацию культуры проводят в течение 15-16 суток при +37°С. Два раза в сутки культуру перемешивают по 5 минут. Через 12 суток берут пробу бактериальной массы для проверки на чистоту (готовят мазок) и полноту инактивации путем высева на питательную среду Китта-Тароцци. Учет результатов проводят через 8 дней.
5. К инактивированной культуре добавляют стерильный 6% раствор гидроокиси алюминия до 30% к объему и по 0,05 г тимерсала на 1 литр вакцины и перемешивают каждые 1,5-2,0 часа в течение первых 10-12 часов. Затем проверяют рН вакцины и доводят до 7,2-7,4 10% раствором гидроокиси натрия. Отбирают пробу для проверки на стерильность и безвредность.
6. Проверенную на стерильность и безвредность вакцину расфасовывают во флаконы при постоянном перемешивании. Закрывают резиновыми пробками и закатывают металлическими колпачками.
7. Вакцину применяют для вакцинации животных с профилактической целью в пунктах, неблагополучных по некробактериозу крупного рогатого скота. Вакцину животным вводят в мышцы в дозе 2 мл. Иммунитет у привитых животных наступает через 14 дней после прививки и продолжается до 6 месяцев.
Таким образом, из примеров 1-5 по проверке предлагаемого штамма Fusobacterium necrophorum subspecies necrophorum, депонированного в НИИ ККМ ГНЦ ВБ «Вектор» под номером В-1076 видно, что предлагаемое изобретение может быть использовано в сельском хозяйстве для изготовления диагностических и профилактических препаратов против некробактериоза животных.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ НАЛИЧИЯ В ПРОБЕ ПАТОГЕННОГО ПОДВИДА FUSOBACTERIUM NECROPHORUM SUBSPECIES NECROPHORUM С ПОМОЩЬЮ ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ | 2004 |
|
RU2294374C2 |
| СПОСОБ ВЫЯВЛЕНИЯ FUSOBACTERIUM NECROPHORUM В ГНЕЗДОВОЙ ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ | 2001 |
|
RU2203951C1 |
| АССОЦИИРОВАННАЯ ВАКЦИНА "НЕКОВАК" ПРОТИВ НЕКРОБАКТЕРИОЗА КРУПНОГО РОГАТОГО СКОТА | 1996 |
|
RU2098127C1 |
| ШТАММ БАКТЕРИОФАГА Citrobacter freundii CF17, СПОСОБНЫЙ ЛИЗИРОВАТЬ ПАТОГЕННЫЕ ШТАММЫ CITROBACTER FREUNDII | 2014 |
|
RU2565559C1 |
| ДНК-конструкция, кодирующая модифицированный вариант протективного антигена Bacillus anthracis | 2015 |
|
RU2622085C2 |
| АССОЦИИРОВАННАЯ ВАКЦИНА "ОВИКОН" ПРОТИВ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ КОНЕЧНОСТЕЙ ОВЕЦ | 1996 |
|
RU2098128C1 |
| Искусственный ген, кодирующий бицистронную структуру, образованную последовательностями рецептор-связующего домена гликопротеина S коронавируса SARS-CoV-2, P2A-пептида и гликопротеина G VSV, рекомбинантная плазмида pStem-rVSV-Stbl_RBD_SC2, обеспечивающая экспрессию искусственного гена и рекомбинантный штамм вируса везикулярного стоматита rVSV-Stbl_RBD_SC2, используемого для создания вакцины против коронавируса SARS-CoV-2 | 2020 |
|
RU2733831C1 |
| СИНТЕТИЧЕСКИЕ ОЛИГОНУКЛЕОТИДНЫЕ ПРАЙМЕРЫ И СПОСОБ ВЫЯВЛЕНИЯ ДНК ВИРУСА ИНФЕКЦИОННОГО РИНОТРАХЕИТА КРУПНОГО РОГАТОГО СКОТА С ПОМОЩЬЮ СПЕЦИФИЧЕСКИХ ОЛИГОНУКЛЕОТИДНЫХ ПРАЙМЕРОВ В ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ (ПЦР) | 2003 |
|
RU2259398C1 |
| ОЛИГОНУКЛЕОТИДНЫЕ ПРАЙМЕРЫ И СПОСОБ ВЫЯВЛЕНИЯ ДНК Mycobacterium avium МЕТОДОМ ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ | 2013 |
|
RU2554842C2 |
| Способ лечения радиационных поражений организма | 2018 |
|
RU2675598C1 |


Изобретение относится к области микробиологии. Получен штамм бактерий Fusobacterium necrophorum subspecies necrophorum, депонированный в НИИ ККМ ГНЦ ВБ «Вектор» В-1076. Штамм может быть использован для изготовления диагностических и профилактических препаратов против некробактериоза животных. 4 ил.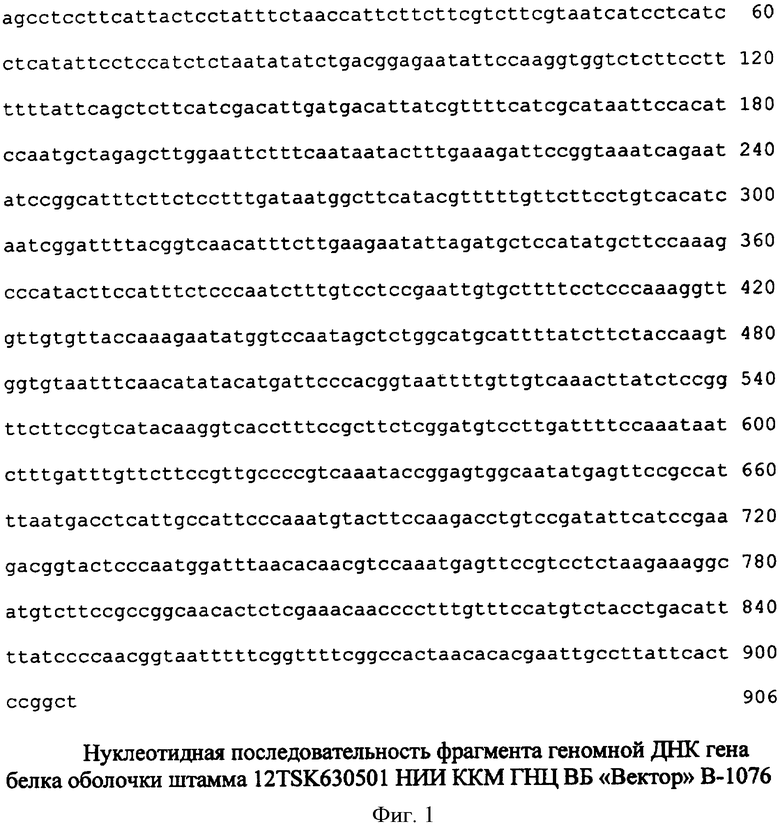
Штамм бактерий Fusobacterium necrophorum subspecies necrophorum, депонированный в НИИ ККМ ГНЦ ВБ «Вектор» под номером В-1076 для изготовления диагностических и профилактических препаратов против некробактериоза животных.
| ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ НЕКРОБАКТЕРИОЗА РОГАТОГО СКОТА | 1991 |
|
SU1816348A3 |
| СПОСОБ ВЫЯВЛЕНИЯ FUSOBACTERIUM NECROPHORUM В ГНЕЗДОВОЙ ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ | 2001 |
|
RU2203951C1 |
Авторы
Даты
2009-02-27—Публикация
2007-01-18—Подача