В отношении данной заявки заявлен приоритет от 22 сентября 2004 года согласно предварительной заявке на патент США № 60/612459 и от 9 мая 2005 года согласно предварительной заявке на патент США № 60/679296, содержание которых во всей их полноте включены в данное описание ссылкой.
Область изобретения
Настоящее изобретение относится к новым полиморфным и аморфной формам фосфатной соли 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она и к способам их получения. Изобретение также относится к фармацевтическим композициям, содержащим по меньшей мере одну полиморфную или аморфную форму, и к терапевтическому или профилактическому применению таких полиморфных и аморфной форм и композиций.
Предшествующий уровень техники
Соединение 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-он, представленное формулой 1
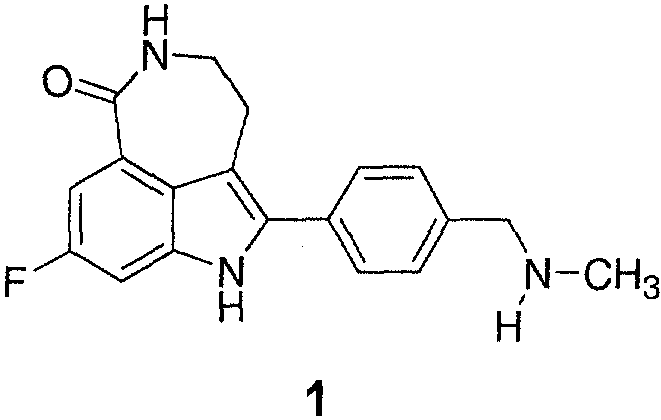
является ингибитором поли(ADP-рибоза)полимеразы (поли(аденозин-5'-дифосфат-рибоза)полимераза, PARP), имеющим молекулу небольшого размера. Соединение формулы 1 и его соли могут быть получены как описано в патенте США № 6495541, заявке РСТ № РСТ/IB 2004/000915, международной публикации № WO 2004/087713 и предварительной заявке на патент США № 60/612457, описания которых во всей их полноте включены в данное описание ссылкой.
До настоящего времени по гомологии последовательностей ДНК в семействе PARP были идентифицированы восемнадцать ферментов и были исследованы биохимические и ферментативные свойства семи: PARP-1 и PARP-2 стимулируются разрывами нитей ДНК, PARP-3 взаимодействует с PARP-1 и центросомой, PARP-4, также известная как VPARP (vault PARP (PARP, ассоциированная с рибонуклеотидпротеиновыми частицами)), является самой большой PARP и ассоциируется с цитоплазматическими рибонуклеотидпротеиновыми частицами, танкираза 1 и 2 (PARP-5a и 5b) ассоциируется с теломерными белками, и функция PARP-7 (TiPARP) в настоящее время не ясна, но она может быть вовлечена в Т-клеточную функцию, и она может осуществлять полиАОР-рибозилирование жетонов (Ате J.C., Splenlehauer С.and de Murcia G. The PARP Superfamily. Bioessays 26 882-893 (2004)). Фармакологические исследования показали, что соединение формулы 1 является ингибитором PARP-1 (Кi=1,4 нМ) и PARP-2 (Кi=0,17 нМ). В силу структурного сходства аминокислотных последовательностей у PARP ферментов соединение формулы 1, связывается также, по всей вероятности, с другими членами этого семейства с высокой аффинностью.
Опосредованная ферментом репарация одно- или двухнитевых разрывов в ДНК представляет собой потенциальный механизм резистентности к радиотерапии или цитотоксическим лекарственным средствам, чей механизм зависит от повреждения ДНК. Поэтому ингибирование ферментов репарации ДНК представляет собой стратегию усиления действия этих агентов. PARP-1, лучше всего охарактеризованный член семейства PARP, является нуклеарным ферментом, который при активации повреждением ДНК опосредует перенос фрагментов ADP-рибозы от NAD+ к целому ряду акцепторных белков. В зависимости от степени повреждения ДНК активация PARP-1 и последующее полиАОР-рибозилирование опосредуют репарацию поврежденной ДНК или индуцируют гибель клеток. При умеренном повреждении ДНК PARP-1 играет значительную роль в процессе репарации ДНК. И, наоборот, в случае большого повреждения ДНК чрезмерная активация PARP-1 обедняет АТР пулы (пытаясь пополнить NAD+), что, в конечном счете, приводит к гибели клеток в результате некроза (Tentori L, Portarena I, Graziani G. Potential applications of poly(ADP-ribose) polymerase (PARP) inhibitors. Pharmacol. Res. 2002, 45, 73-85). Эта активация PARP может также приводить к высвобождению AIF (апоптоз-индуцирующего фактора), запускающего каспаза-независимый апоптотический путь (Hong SJ, Dawson ТМ и Dawson VL. Nuclear and mitochondrial conversations in cell death: PARP-1 and AIF. Trends in PharmacoJogical Sciences 25 259-264 (2004)).
Из-за этой двойственной роли PARP-1 ингибиторы этого фермента, такие как 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-он, представленный формулой 1, могут играть роль хемосенситизирующих агентов (предупреждая репарацию ДНК, например, после противораковой терапии) или средств для лечения различных болезненных и токсических состояний, в которые вовлечены оксидативный или индуцированный оксидом азота стресс и последующая гиперактивация PARP. Такие состояния включают неврологические и нейродегенеративные расстройства (например болезнь Паркинсона, болезнь Альцгеймера) (Love S, Barber R, Wilcock GK. Increased poly(ADP-ribosyl)ation of nuclear proteins in Alzheimer's disease. Brain 1999; 122:247-53; Mandir AS, Przedborski S, Jackson-Lewis V, et al. Poly(ADP-robose) polymerase activation mediates l-methyl-4-phenyl-1,2,3,6-tetrahydropyridine (MPTP)-induced parkinsonism. Proc. Natl. Acad. Sci. USA 1999; 96: 5774-9);
сердечно-сосудистые расстройства (например инфаркт миокарда, ишемия-реперфузионное повреждение) (Pieper AA, Walles Т, Wei G, et al. Myocardial postischemic injury is reduced by poly(ADP-ribose) polymerase-1 gene disruption. J. Mol. Med. 2000; 6: 271-82; Szabo G, Bährle S, Stumpf N, et al. Poly(ADP-ribose) polymerase inhibition reduces reperfusion injury after heart transplantation. Circ. Res. 2002; 90: 100-6; патент США № 6423705); воспалительные заболевания (Szaby С, Dawson V. Role of poly(ADP-ribose) synthetase in inflammation and ischaemia-reperfusion. TIPS 1998; 19: 287-98); диабетическую сосудистую дисфункцию (Soriano FG, Virág L, Szaby C. Diabetic endothelial dysfunction: role of reactive oxygen and nitrogen species production and poly(ADP-ribose) polymerase activation. J. Mol. Med. 2001; 79: 437-48); артрит (Szaby С, Virág L, Cuzzocrea S, et al. Protection against peroxynitrite-induced fibroblast injury and arthritis development by inhibition of poly(ADP-ribose) synthase. Proc. Natl. Acad. Sci. USA 1998; 95: 3867-72); и цисплатин-индуцированную нефротоксичность (Racz I, Tory К, Gallyas F, et al. BGP-15-a novel poly(ADP-ribose) polymerase inhibitor - protects against nephrotoxicity of cisplatin without compromising its antitumor activity. Biochem. Pharmacol. 2002; 63: 1099-111). Кроме того, было показано, что опухолевые клетки с дефицитом BRCA2 в наивысшей степени чувствительны только к ингибиторам PARP-1 (Bryant HE, Schultz N, Thomas HD, Parker KM, Flower D, Lopez E, Kyle S, Meuth M, Curtin NJ and Helleday T. "Specific killing of BRCA2 deficient tumors with inhibitors of poly(ADP-ribose)polymerase", Nature: в печати). Ингибиторы PARP также вовлечены в усиление индуцирования экспрессии гена Reg в β клетках и гена HGF и, соответственно, стимулируют пролиферацию панкреатических β-клеток островков Лангерганса и подавляют апоптоз этих клеток (публикация заявки на патент США № 2004/0091453; международная публикация № WO 02/00665). Кроме того, ингибиторы PARP используют также в косметических препаратах, в частности в лосьонах после загара (международная публикация № WO 01/82877). В настоящее время ингибиторы PARP не продаются.
Рак остается заболеванием с высокой неудовлетворенной медицинской потребностью. Цитотоксическая терапия остается главной опорой системной терапии для большинства видов рака, особенно в последней стадии. Однако для пациентов с далеко зашедшим или метастатическим заболеванием несколько цитотоксических химиотерапевтических агентов или режимов были эффективны и внесли вклад в увеличение общей выживаемости. Кроме того, небольшое терапевтическое окно, связанное с цитотоксическими агентами, дает значительную токсичность в сочетании с приближающейся к оптимальной эффективностью. Таким образом, хемосенситизаторы, которые повышают эффективность цитотоксических лекарственных средств в хорошо переносимых дозах, могли бы удовлетворить насущную потребность для раковых пациентов. В предварительных заявках на патент США №№ 60/612458 и 60/683006 под названием "Терапевтические комбинации, содержащие ингибитор поли(ADP-рибоза)полимеразы", описания которых во всей их полноте включены в данное описание ссылкой, описаны фармацевтические комбинации 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она.
Чтобы подготовить фармацевтические композиции, содержащие 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-он, для введения млекопитающим, необходимо получить это соединение в форме, имеющей физические свойства, подходящие для приготовления надежных препаратов. Соответственно, в данной области существует потребность в улучшенных формах 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, имеющих улучшенные свойства, такие как повышенная растворимость или биодоступность и стабильность в отношении воздействия тепла, влаги и света.
Краткое изложение сущности изобретения
В одном аспекте настоящего изобретения предложено шесть полиморфных форм и одна аморфная форма фосфатной соли 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она.
В одном воплощении настоящего изобретения предложена кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы I.
В еще одном воплощении изобретения предложена кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы II.
В еще одном воплощении изобретения предложена кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы III.
В еще одном изобретения воплощении предложена кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы IV.
В еще одном воплощении изобретения предложена кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы V.
В еще одном воплощении изобретения предложена кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы VI.
В еще одном воплощении изобретения предложена фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-сс)]индол-6-она, которая представляет собой по существу чистую аморфную форму.
В еще одном воплощении изобретения предложена кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы I, имеющая картину дифракции рентгеновских лучей на порошке, содержащую пики при углах дифракции (2θ) 10.9, 19.3, 22.9 и 25.0.
В еще одном воплощении настоящего изобретения предложена кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы II, имеющая картину дифракции рентгеновских лучей на порошке, содержащую пики при углах дифракции (2θ) 11.2, 14.0, 20.1 и 23.1.
В еще одном воплощении настоящего изобретения предложена кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы III, имеющая картину дифракции рентгеновских лучей на порошке, содержащую пики при углах дифракции (2θ) 10.7, 11.0, 19.4 и 25.1.
В еще одном воплощении настоящего изобретения предложена кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы IV, имеющая картину дифракции рентгеновских лучей на порошке, содержащую пики при углах дифракции (2θ) 8.2, 16.5, 23.0 и 24.8.
В еще одном воплощении настоящего изобретения предложена кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы V, имеющая картину дифракции рентгеновских лучей на порошке, содержащую пики при углах дифракции (2θ) 10.8, 14.8, 21.6 и 25.8.
В еще одном воплощении настоящего изобретения предложена кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы VI, имеющая картину дифракции рентгеновских лучей на порошке, содержащую пики при углах дифракции (2θ) 14.8, 20.0, 22.3 и 23.5.
В еще одном воплощении настоящего изобретения предложена кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы I, имеющая картину дифракции рентгеновских лучей на порошке, содержащую пики при углах дифракции (2θ), по существу такие же, как пики, показанные на Фиг.1.
В еще одном воплощении настоящего изобретения предложена кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы II, имеющая картину дифракции рентгеновских лучей на порошке, содержащую пики при углах дифракции (2θ), по существу такие же, как пики, показанные на Фиг.4.
В еще одном воплощении настоящего изобретения предложена кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы III, имеющая картину дифракции рентгеновских лучей на порошке, содержащую пики при углах дифракции (2θ), по существу такие же, как пики, показанные на Фиг.7.
В еще одном воплощении настоящего изобретения предложена кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы IV, имеющая картину дифракции рентгеновских лучей на порошке, содержащую пики при углах дифракции (2θ), по существу такие же, как пики, показанные на Фиг.10.
В еще одном воплощении настоящего изобретения предложена кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы V, имеющая картину дифракции рентгеновских лучей на порошке, содержащую пики при углах дифракции (2θ), по существу такие же, как пики, показанные на Фиг.13.
В еще одном воплощении настоящего изобретения предложена кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы VI, имеющей картину дифракции рентгеновских лучей на порошке, содержащую пики при углах дифракции (29), по существу такие же, как пики, показанные на Фиг.18.
В еще одном воплощении настоящего изобретения предложена аморфная форма фосфатной соли 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая имеет картину дифракции рентгеновских лучей на порошке, демонстрирующую широкий пик при углах дифракции (2θ) в пределах от 4 до 40° без каких-либо характерных острых пиков кристаллической формы. Более конкретно, аморфная форма характеризуется тем, что она имеет картину дифракции рентгеновских лучей на порошке, по существу такую же, как картина, представленная на Фиг.21. Еще более предпочтительно, аморфная форма характеризуется спектром комбинационного рассеяния, содержащим сдвиговые пики (см-1), по существу такие же, как пиеи, показанные на Фиг.23.
В еще одном воплощении настоящего изобретения предложена твердая форма фосфатной соли 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая содержит по меньшей мере две из следующих форм: полиморфные Формы I, II, III, IV, V, VI и аморфная форма.
В еще одном воплощении настоящего изобретения предложена фармацевтическая композиция, содержащая кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы I.
В еще одном воплощении настоящего изобретения предложена фармацевтическая композиция, содержащая кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы II.
В еще одном воплощении настоящего изобретения предложена фармацевтическая композиция, содержащая кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы III.
В еще одном воплощении настоящего изобретения предложена фармацевтическая композиция, содержащая кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы IV.
В еще одном воплощении настоящего изобретения предложена фармацевтическая композиция, содержащая кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы V.
В еще одном воплощении настоящего изобретения предложена фармацевтическая композиция, содержащая кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы VI.
В еще одном воплощении настоящего изобретения предложена фармацевтическая композиция, содержащая фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистую аморфную форму.
В еще одном воплощении настоящего изобретения предложена фармацевтическая композиция, содержащая твердую форму фосфатной соли 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая содержит по меньшей мере две из следующих форм: полиморфные Формы I, II, III, IV, V, VI или аморфная форма.
В еще одном воплощении настоящего изобретения предложен способ лечения опосредованного активностью поли(ADP-рибоза)полимеразы болезненного состояния у млекопитающего, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества фармацевтической композиции, содержащей кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы I.
В еще одном воплощении настоящего изобретения предложен способ лечения опосредованного активностью поли(ADP-рибоза)полимеразы болезненного состояния у млекопитающего, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества фармацевтической композиции, содержащей кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы II.
В еще одном воплощении настоящего изобретения предложен способ лечения опосредованного активностью поли(ADP-рибоза)полимеразы болезненного состояния у млекопитающего, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества фармацевтической композиции, содержащей кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы III.
В еще одном воплощении настоящего изобретения предложен способ лечения опосредованного активностью поли(ADP-рибоза)полимеразы болезненного состояния у млекопитающего, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества фармацевтической композиции, содержащей кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы IV.
В еще одном воплощении настоящего изобретения предложен способ лечения опосредованного активностью поли(ADP-рибоза)полимеразы болезненного состояния у млекопитающего, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества фармацевтической композиции, содержащей кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы V.
В еще одном воплощении настоящего изобретения предложен способ лечения опосредованного активностью поли(ADP-рибоза)полимеразы болезненного состояния у млекопитающего, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества фармацевтической композиции, содержащей кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы VI.
В еще одном воплощении настоящего изобретения предложен способ лечения опосредованного активностью поли(ADP-рибоза)полимеразы болезненного состояния у млекопитающего, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества фармацевтической композиции, содержащей кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой посуществу чистую аморфную форму.
В еще одном воплощении настоящего изобретения предложен способ лечения опосредованного активностью поли(ADP-рибоза)полимеразы болезненного состояния у млекопитающего, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества фармацевтической композиции, содержащей твердую форму фосфатной соли 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая содержит по меньшей мере две из следующих форм: полиморфные Формы I, II, III, IV, V, VI и аморфная форма.
В еще одном воплощении настоящего изобретения предложен способ лечения рака у млекопитающего, включающий введение этому млекопитающему терапевтически эффективного количества фармацевтической композиции, содержащей кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы I.
В еще одном воплощении настоящего изобретения предложен способ лечения рака у млекопитающего, включающий введение этому млекопитающему терапевтически эффективного количества фармацевтической композиции, содержащей кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы II.
В еще одном воплощении настоящего изобретения предложен способ лечения рака у млекопитающего, включающий введение этому млекопитающему терапевтически эффективного количества фармацевтической композиции, содержащей кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы III.
В еще одном воплощении настоящего изобретения предложен способ лечения рака у млекопитающего, включающий введение этому млекопитающему терапевтически эффективного количества фармацевтической композиции, содержащей кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы IV.
В еще одном воплощении настоящего изобретения предложен способ лечения рака у млекопитающего, включающий введение этому млекопитающему терапевтически эффективного количества фармацевтической композиции, содержащей кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы V.
В еще одном воплощении настоящего изобретения предложен способ лечения рака у млекопитающего, включающий введение этому млекопитающему терапевтически эффективного количества фармацевтической композиции, содержащей кристаллическую фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистый полиморф Формы VI.
В еще одном воплощении настоящего изобретения предложена способ лечения рака у млекопитающего, включающий введение этому млекопитающему терапевтически эффективного количества фармацевтической композиции, содержащей фосфатную соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая представляет собой по существу чистую аморфную форму.
В еще одном воплощении настоящего изобретения предложен способ лечения рака у млекопитающего, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества фармацевтической композиции, содержащей твердую форму фосфатной соли 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая содержит по меньшей мере две из следующих форм: полиморфные Формы I, II, III, IV, V, VI или аморфная форма.
В еще одном воплощении настоящего изобретения предложена лекарственная форма, содержащая 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-он, которая представляет собой лиофилизированный порошок для инъекций, причем эта лекарственная форма после разведения стерильной водой для инъекций обеспечивает конечную концентрацию 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она в виде свободного основания от 1,0 до 4,5 мг/мл при рН от 8,0 до 3,0.
В еще одном воплощении настоящего изобретения предложена лекарственная форма, содержащая 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-он, которая представляет собой лиофилизированный порошок для инъекций, причем эта лекарственная форма после разведения стерильной водой для инъекций обеспечивает конечную концентрацию 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она в виде свободного основания от 2 до 3 мг/мл при рН от 5,0 до 6,0.
Определения
Термин "Соединение I" относится к фосфатной соли 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она. Термин "соединение формулы 1" относится к 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-ону, свободному основанию.
Термин "активный агент" или "активный ингредиент" относится к полиморфной форме фосфатной соли 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она (Соединение I) или к твердой форме, которая содержит две или более полиморфные формы или аморфную форму фосфатной соли 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она (Соединение I).
Термин "температура окружающей среды" относится к температурным условиям, обычно встречающихся в лабораторных помещениях. Этот термин охватывает приблизительный температурный диапазон от примерно 20 до примерно 30°С.
Термин "аморфный" относится к некристаллической форме соединения.
Термин "водное основание" относится к любому органическому или неорганическому основанию. Водные основания включают, исключительно в качестве примера, бикарбонаты металлов, такие как бикарбонат натрия, карбонат калия, карбонат цезия и т.п.
Термин "ароматический растворитель" относится к органическому растворителю, имеющему ароматическую группировку, включая, исключительно в качестве примера, бензол, толуол, изомеры ксилола или их смеси и т.п.
Термин "химическая стабильность" относится к типу стабильности, когда конкретное соединение сохраняет свою химическую целостность, и охватывает, но не ограничивается ими, термостойкость, светостойкость и влагостойкость.
Термин "обнаружимое количество" относится к количеству или количеству на единицу объема, которое может быть обнаружено с использованием общепринятых методов, таких как дифракция рентгеновских лучей на порошке, дифференциальная сканирующая калориметрия, ВЭЖХ, инфракрасная Фурье-спектроскопия (ИК-ФС), спектроскопия комбинационного рассеяния и т.п.
Термин "подвергание воздействию влажности" относится к процессу подвергания вещества воздействию водяного пара в установке для увлажнения воздуха, камере влажности или любой установке с возможностью контролирования относительной влажности. Этот термин может характеризовать также процесс воздействия влажности окружающей среды на вещество во время хранения.
Термин "рак" включает, но не ограничивается ими, рак легкого, рак кости, рак поджелудочной железы, рак кожи, рак в области головы или шеи, кожную или внутриглазную меланому, рак матки, рак яичника, рак прямой кишки, рак в анальной области, рак желудка, рак ободочной кишки, рак молочной железы, рак матки, карциному фаллопиевых труб, карциному эндометрия, карциному шейки матки, карциному вагины, карциному вульвы, болезнь Ходжкина, рак пищевода, рак тонкого кишечника, рак эндокринной системы, рак щитовидной железы, рак паращитовидной железы, рак надпочечника, саркому мягкой ткани, рак уретры, рак пениса, рак простаты, хронический или острый лейкоз, лимфоцитарную лимфому, рак мочевого пузыря, рак почки или мочеточника, почечно-клеточную карциному, карциному почечной лоханки, неоплазмы центральной нервной системы (ЦНС), первичную лимфому ЦНС, опухоли позвоночника, глиому ствола мозга, аденому гипофиза или комбинацию одного или более вышеупомянутых видов рака. В еще одном воплощении указанного способа указанный аномальный рост клеток представляет собой доброкачественное пролиферативное заболевание, включая, но не ограничиваясь ими, псориаз, доброкачественную гипертрофию простаты или рестеноз.
Термин "инертный растворитель" относится к любому растворителю или жидкому компоненту суспензии, который химически не взаимодействует с другими компонентами в растворе или суспензии. Инертные растворители включают, исключительно в качестве примера, апротонные растворители, такие как ароматические растворители, этилацетат, ацетон, метил-трет-бутиловый эфир, диоксан, тетрагидрофуран (ТГФ) и т.п. Протонные растворители включают, исключительно в качестве примера, метанол, этанол, изомеры пропанола, изомеры бутанола и т.п.
Термин "опосредованное активностью поли(ADP-рибоза)полимеразы (PARP)" относится к биологическим или молекулярным процессам, которые регулируются, модулируются или ингибируются активностью PARP. Для некоторых применений ингибирование активности PARP, связанной с раком, является предпочтительным. Настоящее изобретение охватывает способы модулирования или ингибирования активности PARP, например у млекопитающих, путем введения полиморфной формы фосфатной соли 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она (Соединение I) или твердой формы, которая содержит две или более полиморфные формы Соединения I. Активность или эффективность полиморфов Соединения I или твердой формы, которая содержит две или более полиморфные формы Соединения I, может быть измерена как описано, например, в патенте США №6495541 и предварительной заявке на патент США № 60/612458, описания которых во всей их полноте включено в данное описание ссылкой.
Термин "минимальное количество" относится к наименьшему количеству растворителя, которое требуется для полного растворения вещества при данной температуре.
Используемый здесь термин "полиморф" относится к разным кристаллическим формам одного и того же соединения и другим молекулярным формам в твердом состоянии, включая псевдополиморфы, такие как гидраты (например, в кристаллической форме присутствует связанная вода) и сольваты (например, связанные растворители, иные чем вода) одного и того же соединения. Разные кристаллические полиморфы имеют разную структуру кристалла, обусловленную разной упаковкой молекул в решетке. Это дает в результате разную симметрию кристалла и/или разные параметры ячейки, что непосредственно влияет на его физические свойства, такие как характеристики дифракции рентгеновских лучей на кристаллах или порошках. Например, другой полиморф будет, как правило, дифрагировать при другом наборе углов и будет давать другие значения интенсивности. Следовательно, дифракция рентгеновских лучей на порошке может быть использована для идентификации разных полиморфов или твердой формы, которая содержит более чем один полиморф, воспроизводимым и достоверным способом (S.Byrn et al, Pharmaceutical Solids: A Strategic Approach to Regulatory Considerations, Pharmaceutical research, Vol.12, No.7, p.945-954, 1995; J.К.Haleblian and W.McCrone, Pharmaceutical Applications of Polymorphism, Journal of Pharmaceutical Sciences, Vol.58, No.8, p.911-929, 1969). Кристаллические полиморфные формы представляют интерес для фармацевтической промышленности и особенно для тех ее секторов, которые занимаются разработкой подходящих лекарственных форм. Если полиморфная форма не сохраняется неизменной во время клинических испытаний или исследований стабильности, точная применяемая или исследуемая лекарственная форма не может быть сравнимой от одной партии к другой. Когда соединение используют в клинических испытаниях или промышленных продуктах, желательно также иметь процессы производства соединения с выбранной полиморфной формой высокой чистоты, поскольку присутствующие примеси могут вызывать нежелательные токсикологические эффекты. Некоторые полиморфные формы могут проявлять повышенную термодинамическую стабильность или более легко могут быть изготовлены с высокой чистотой в больших количествах, и поэтому они больше подходят для включения в состав фармацевтических препаратов. Некоторые полиморфы могут проявлять другие полезные физические свойства, такие как отсутствие гигроскопических тенденций, улучшенная растворимость и повышенная степень растворения благодаря другим энергиям кристаллической решетки.
Термин "интенсивности пиков" относится к относительным интенсивностям сигналов в картине дифракции рентгеновских лучей. Факторами, которые могут влиять на относительные интенсивности пиков, являются толщина образца и предпочтительная ориентация (т.е. кристаллические частицы распределены не случайным образом).
Используемый здесь термин "позиции пиков" относится к позициям отражения рентгеновского луча, которые измерены и наблюдаются в экспериментах по дифракции рентгеновских лучей на порошке. Позиции пиков напрямую связаны с размерами элементарной ячейки. Пики, идентифицированные по их относительными позициями, были получены из дифракционных картин для различных полиморфных Форм I, II, III, IV, V и VI фосфатной соли 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она (Соединение I).
Термин "PEG" относится к полиэтиленгликолю. PEG является коммерчески доступным полимером с разными диапазонами длины цепи и, следовательно, вязкости. PEG 400 растворим в спиртах, ацетоне, бензоле, хлороформе, уксусной кислоте, CCl4 и воде.
Термин "фармацевтически приемлемый носитель, разбавитель или наполнитель" относится к веществу (или веществам), которое может быть включено вместе с конкретным фармацевтическим агентом в состав фармацевтической композиции и может быть твердым или жидким. Примерами твердых носителей являются лактоза, сахароза, тальк, желатин, агар, пектин, аравийская камедь, стеарат магния, стеариновая кислота и тому подобное. Примерами жидких носителей являются сироп, арахисовое масло, оливковое масло, вода и тому подобное. Подобным образом, носитель или разбавитель может содержать обеспечивающее отсроченное или длительное высвобождение вещество, известное в данной области, такое как глицерилмоностеарат или глицерилдистеарат, один или вместе с воском, этилцеллюлозой, гидроксипропилметилцеллюлозой, метилметакрилатом и тому подобным.
Термин "фармацевтическая композиция" относится к смеси одного или более соединений или полиморфов, описанных здесь, или их физиологически/фармацевтически приемлемым солей или сольватов с другими химическим компонентами, такими как физиологически/фармацевтически приемлемые носители и эксципиенты. Назначение фармацевтической композиции - облегчать введение композиции в организм.
Термин "перекристаллизовывать" относится к процессу полного растворения твердого вещества в первом растворителе при нагревании, если это необходимо, и последующего индуцирования осаждения, обычно путем охлаждения раствора или добавления второго растворителя, в котором это твердое вещество плохо растворяется.
Термин "относительная влажность" относится к отношению количества водяного пара в воздухе при данной температуре к максимальному количеству водяного пара, которое может сохраняться при этой температуре и давлении, выраженное в процентах.
Термин "относительная интенсивность" относится к значению интенсивности, полученному из картины дифракции рентгеновских лучей образца. Весь диапазон шкалы по оси ординат задан значением 100. Пик, имеющий интенсивность в пределах от примерно 50% до примерно 100% по этой шкале интенсивности считается очень сильным (vs); пик, имеющий интенсивность в пределах от примерно 50% до примерно 25% считается сильным (s). Дополнительные более слабые пики присутствуют в типичных дифракционных картинах и также являются характеристикой данного полиморфа.
Термин "суспензия" относится к твердому веществу, суспендированному в жидкой среде, обычно в воде или органическом растворителе.
Термин "выделение из" относится к стадии синтеза, на которой целевое вещество отделяют от других нежелательных веществ, включая, но не ограничиваясь ими, любые из следующих стадий: фильтрование, промывка добавочным растворителем или водой, сушка при нагревании и/или в вакууме.
Термин "по существу чистый" со ссылкой на конкретные полиморфные формы фосфатной соли 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она (Соединение I) означает полиморфную форму, которая содержит менее 10%, предпочтительно менее 5%, предпочтительно менее 3%, предпочтительно менее 1% по массе примесей, включая другие полиморфные формы Соединения I. Такая чистота может быть определена, например, дифракцией рентгеновских лучей на порошке.
Термин "эффективное количество" означает такое количество агента, которое в значительной степени ингибирует пролиферацию и/или предупреждает дедифференциацию эукариотической клетки, например клетки млекопитающего, насекомого, растения или гриба, и является эффективным для указанного применения, например для конкретного терапевтического лечения.
Термин "терапевтически эффективное количество" относится к такому количеству соединения или полиморфа, которое, будучи введенным, до некоторой степени ослабляет один или более симптомов расстройства, которое лечат. При ссылке на лечение рака терапевтически эффективное количество относится к такому количеству, которое оказывает по меньшей мере один из следующих эффектов:
1) сокращение размера опухоли;
2) ингибирование (то есть замедление до некоторой степени, предпочтительно прекращение) метастазирования опухоли;
3) ингибирование до некоторой степени (то есть замедление до некоторой степени, предпочтительно прекращение) роста опухоли; и
4) ослабление до некоторой степени (или, предпочтительно, устранение) одного или более симптомов, связанных с раком.
Термин "значение 2 тета", или "2θ", относится к позиции пика на основе экспериментальной настройки эксперимента по дифракции рентгеновских лучей и представляет собой общепринятую единицу по оси абсцисс на дифракционных картинах. Экспериментальная настройка требует, что, если отражение дифрагируется, когда входящий луч образует угол тета (θ) с определенной плоскостью решетки, отраженный луч записывают при угле 2 тета (2θ).
Термины "лечить", "лечение" и "акт лечения" относятся к способу облегчения или аннулирования гиперпролиферативного расстройства и/или сопутствующих ему симптомов. Что касается конкретно рака, то эти термины просто означают, что средняя ожидаемая продолжительность жизни индивидуума, пораженного раком, будет увеличена или что один или более симптомов заболевания будут ослаблены.
Термин "в вакууме" относится к типичным давлениям, достигаемым с помощью лабораторного масляного или немасляного мембранного вакуумного насоса.
Термин "картина дифракции рентгеновских лучей на порошке" относится к экспериментально наблюдаемой дифрактограмме или к параметрам, получаемым из нее. Картины дифракции рентгеновских лучей на порошке характеризуются позициями пиков (ось абсцисс) и интенсивностями пиков (ось ординат).
Краткое описание графических материалов
Фиг.1 представляет собой рентгеновскую порошковую дифрактограмму полиморфной Формы I (гидрат А) фосфатной соли 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она (Соединение I).
Фиг.2 представляет собой ИК-спектр поглощения полиморфной Формы I (гидрат А) Соединения I.
Фиг.3 представляет собой кривую дифференциальной сканирующей калориметрии (ДСК) полиморфной Формы 1 (гидрат А) Соединения I. Типичная кривая отражает эндотерму с началом при 202°С при скорости сканирования 5°С/мин.
Фиг.4 представляет собой рентгеновскую порошковую дифрактограмму полиморфной Формы II (безводная форма) Соединения I.
Фиг.5 представляет собой ИК-спектр поглощения полиморфной Формы II (безводная форма) Соединения I.
Фиг.6 представляет собой кривую дифференциальной сканирующей калориметрии (ДСК) полиморфной Формы II (безводная форма) Соединения I. Типичная кривая отражает эндотерму с началом при 205°С при скорости сканирования 5°С/мин.
Фиг.7 представляет собой рентгеновскую порошковую дифрактограмму полиморфной Формы III (гидрат В) Соединения I.
Фиг.8 представляет собой ИК-спектр поглощения полиморфной Формы III (гидрат В) Соединения I.
Фиг.9 представляет собой кривую дифференциальной сканирующей калориметрии (ДСК) полиморфной Формы III (гидрат В) Соединения I. Типичная кривая отражает эндотерму с началом при 203°С при скорости сканирования 5°С/мин.
Фиг.10 представляет собой рентгеновскую порошковую дифрактограмму полиморфной Формы IV (МеОН сольват) Соединения I.
Фиг.11 представляет собой ИК-спектр поглощения полиморфной Формы IV (МеОН сольват) Соединения I.
Фиг.12 представляет собой кривую дифференциальной сканирующей калориметрии (ДСК) полиморфной Формы IV (МеОН сольват) Соединения I. Типичная кривая отражает эндотерму с началом при 204°С при скорости сканирования 5°С/мин.
Фиг.13 представляет собой рентгеновскую порошковую дифрактограмму полиморфной Формы V (гидрат С) Соединения I.
На Фиг.14 представлено исследование комбинационного рассеяния водной суспензии полиморфной Формы V (гидрат С) Соединения I.
Фиг.15 представляет собой график зависимости растворимости от рН для полиморфной Формы II (безводная форма) Соединения I.
Фиг.16 представляет собой ИК-спектр поглощения полиморфной Формы V (гидрат С) Соединения I.
Фиг.17 представляет собой кривую дифференциальной сканирующей калориметрии (ДСК) полиморфной Формы V (гидрат С) Соединения I.
Фиг.18 представляет собой рентгеновскую порошковую дифрактограмму полиморфной Формы VI Соединения I.
Фиг.19 представляет собой ИК-спектр поглощения полиморфной Формы VI Соединения I.
Фиг.20 представляет собой кривую дифференциальной сканирующей калориметрии (ДСК) полиморфной Формы VI Соединения I.
Фиг.21 представляет собой рентгеновскую порошковую дифрактограмму аморфной формы Соединения I.
Фиг.22 представляет собой ИК-спектр поглощения аморфной формы Соединения I.
Фиг.23 представляет собой спектр комбинационного рассеяния аморфной формы Соединения I.
Фиг.24 представляет собой кривую дифференциальной сканирующей калориметрии (ДСК) аморфной формы Соединения I.
Подробное описание изобретения
Неожиданно было обнаружено, что фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она (Соединение I) может существовать в более чем одной полиморфной кристаллической форме. Эти формы могут быть использованы в составе продукта для лечения болезненного состояния у млекопитающего, опосредованного активностью поли(ADP-рибоза)полимеразы (PARP), включая рак. Каждая форма может иметь одно или более преимуществ над другими в биодоступности, стабильности или технологичности. Были открыты кристаллические полиморфные формы Соединения I, которые оказались более подходящими для массового производства и обращения с ними, чем другие полиморфные формы. Предложена также аморфная форма Соединения I. Описаны способы получения этих полиморфных форм и аморфной формы высокой чистоты. Также предложены способы получения каждой полиморфной и аморфной формы Соединения I, по существу не содержащей другие полиморфные формы Соединения I. Кроме того, согласно изобретению предложены фармацевтические композиции, содержащие Соединение I в разных полиморфных формах и аморфной форме, которые рассмотрены выше, и способы лечения опосредованного активностью поли(ADP-рибоза)полимеразы (PARP) болезненного состояния у млекопитающего введением таких фармацевтических препаратов.
I. Полиморфные формы фосфатной соли 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6H-азепино[5,4,3-cd]индол-6-она (Соединения I)
Согласно настоящему изобретению предложены несколько полиморфных кристаллических форм Соединения I. Каждая кристаллическая форма Соединения I может быть охарактеризована одним или более из следующего: картина дифракции рентгеновских лучей на порошке (т.е. пики дифракции рентгеновских лучей при различных углах дифракции (2θ)); точка начала плавления (и начала дегидратации для гидратированных форм), как иллюстрируется эндотермами термограммы дифференциальной сканирующей калориметрии (ДСК); картина ИК-ФС спектра; картина спектра комбинационного рассеяния; растворимость в воде; светостойкость в соответствии с требованиями Международной конференции по гармонизации (ICH) технических требований к условиям высокой интенсивности света; и физическая и химическая стабильность при хранении. Например, образцы полиморфных Форм I, II, III, IV, V и VI Соединения I, каждый, были охарактеризованы позициями и относительным интенсивностям пиков на их картинах дифракции рентгеновских лучей на порошке. Параметры дифракции рентгеновских лучей на порошке отличаются для каждой из полиморфных Форм I, II, III, IV, V и VI Соединения I. Следовательно, эти полиморфные формы Соединения I можно различать с использованием дифракции рентгеновских лучей на порошке.
Картину дифракции рентгеновских лучей на порошке для каждой полиморфной формы по изобретению получали на рентгеновском дифрактометре Shimadzu XRD-6000
или Bruker Discover D8, оснащенном Cu источником рентгеновского излучения, работающим при 40 кВ и 30 мА или 40 кВ и 40 мА соответственно. В случае рентгеновского дифрактометра Shimadzu XRD-6000 образцы помещали в держатель образца и затем уплотняли и разравнивали предметным стеклом. Во время анализа образцы вращали при 60 об/мин и анализировали, начиная с угла 4 градуса до угла 40 градусов (9-29) при скорости 5 градусов в минуту с шагом 0,04 градуса или при скорости 2 градуса в минуту с шагом 0,02 градуса. Если имелось ограниченное количество вещества, то образцы помещали на кремниевую пластинку (нулевой фон) и анализировали без вращения. Рентгеновские дифракционные пики, охарактеризованные распределениями позиций и интенсивностей пиков, были получены из рентгеновской порошковой дифрактограммы каждой из полиморфных форм Соединения I. В случае Bruker Discover D8 образцы помещали на предметное стекло и разравнивали прижиманием бумаги. Образцы анализировали, начиная с угла 4° до угла 40° (θ-2θ). Специалисту в данной области должно быть ясно, что позиции пиков (2θ) будут показывать некоторую межаппаратурную вариабельность, типично 0,1°. Соответственно, если полиморфные формы описаны характерными пиками рентгеновской дифракции на порошке, то должно быть понятно, что позиции пиков (2θ) охватывают такую вариабельность. Аналогично, если твердые формы по настоящему изобретению описаны как формы, имеющие картину дифракции рентгеновских лучей на порошке, по существу такую же, как картина, представленная на данной фигуре, то термин "по существу такая же" охватывает такую межаппаратурную вариабельность позиций дифракционных пиков. Специалисту в данной области также должно быть понятно, что относительные интенсивности пиков будут показывать межаппаратурную вариабельность, а также вариабельность, обусловленную степенью кристалличности, предпочтительной ориентацией, поверхностью полученного образца и другими факторами, известными специалистам в данной области, и их следует воспринимать только как количественные характеристики.
Различие между разными полиморфными формами Соединения I определяли также с использованием дифференциальной сканирующей калориметрии (ДСК). ДСК измеряет разницу в тепловой энергии между раствором образца и соответствующим эталонным растворителем с увеличением температуры. ДСК-термограммы характеризуются эндотермами (указывающими на поглощение энергии), а также экзотермами (указывающими на выделение энергии), обычно по мере нагревания образца.
ДСК-термограммы были получены с использованием ТА прибора DSC Q1000 и прибора Mettler Toledo ДСК821е при скорости сканирования 5°С/мин в диапазоне температур 25-250°С. Для ДСК-анализа навески образцов помещали в герметичные алюминиевые кюветы, которые запаивали и протыкали в них одно отверстие. В зависимости от нескольких факторов эндотермы, показанные соединениями по изобретению, могут меняться на примерно 0,01-5°С для кристаллического полиморфа, плавящегося выше или ниже эндотерм, изображенных на прилагаемых фигурах. Факторы, ответственные за такое колебание, включают скорость нагревания (т.е. скорость сканирования), при которой проводят ДСК-анализ, способ установления и определения температуры начала ДСК, используемый калибровочный стандарт, калибровку прибора, относительную влажность и химическую чистоту образца. Для любого данного образца наблюдаемые эндотермы могут также отличаться от прибора к прибору, однако, как правило, это будет в указанных здесь пределах при условии, что приборы откалиброваны аналогично.
Спектры комбинационного рассеяния были получены с использованием спектрометра комбинационного рассеяния Raman RXN1 от Kaiser Optical Instruments. Световым источником возбуждения был 785-нметровый диодный лазер со стабилизирующим внешним резонатором. Детектором был прибор с зарядовой связью (ПЗС). Разрешение составляло 4 см-1.
Инфракрасные спектры регистрировали на ИК-ФС спектрофотометре Bruker Vector33. Образец лекарственного вещества измельчали с бромидом калия и прессовали в таблетки. Таблетку сканировали от 4000 см-1 до 400 см-1. Главные пики были замечены между 3400-1 и 500 см-1.
Разные полиморфные формы Соединения I можно также различать по разным стабильностям и разным растворимостям.
В одном воплощении полиморфные формы по настоящему изобретению являются по существу чистыми, что означает, что каждая полиморфная форма Соединения I содержит менее 10%, например менее 5% или, например, менее 3% или даже, например, менее 1% по массе примесей, включая другие полиморфные формы Соединения I.
Твердые формы по настоящему изобретению могут также содержать более чем одну полиморфную форму. Специалисту в данной области очевидно, что кристаллические формы данного соединения могут существовать в по существу чистой форме единственного полиморфа и могут также существовать в кристаллической форме, которая содержит два или более разных полиморфа. Если твердая форма содержит два или более полиморфа, то картина дифракции рентгеновских лучей также будет иметь характеристику пиков каждого из индивидуальных полиморфов по настоящему изобретению. Например, твердая форма, которая содержит два полиморфа, будет иметь картину дифракции рентгеновских лучей на порошке, которая представляет собой свертку двух картин дифракции рентгеновских лучей, которая соответствует по существу чистым полиморфным формам. В одном воплощении, например, твердая форма по настоящему изобретению, содержащая первую и вторую полиморфную форму, содержит по меньшей мере 10% первого полиморфа. В еще одном воплощении твердая форма содержит по меньшей мере 20% первого полиморфа. Другие воплощения содержат по меньшей мере 30%, по меньшей мере 40% или по меньшей мере 50% первого полиморфа. Специалисту в данной области очевидно, что возможны многие такие комбинации нескольких индивидуальных полиморфов в варьирующих количествах.
В следующем ниже обсуждении дифракция рентгеновских лучей и данные по поглощению в инфракраснй области приведены для разных полиморфов. Хотя измеренные углы дифракции указаны до двух знаков после запятой, должно быть ясно, что точность углов дифракции равна ±0,1°, как описано выше.
А. Полиморфная Форма IV (метанольный сольват)
Полиморфная Форма IV Соединения I может быть получена фосфорилированием соединения 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-он, представленного формулой 1 в метаноле.
Полиморфная Форма IV Соединения I физически и химически стабильна при 40°С в условиях относительной влажности 75% в течение по меньшей мере 3 месяцев.
Полиморфная Форма IV Соединения I имеет растворимость в воде 4,5 мг/мл при рН 5,4.
Картина дифракции рентгеновских лучей на порошке Формы IV была измерена, как описано здесь, и она имеет пики при следующих приблизительных углах дифракции (2θ): 8.20, 13.52, 14.88, 16.48, 18.08, 19.14, 20.26, 21.06, 22.08, 23.00, 24.80, 25.54, 26.42, 27.14, 28.36, 29.02, 29.92, 30.58, 32.48, 33.42, 34.8, 35.32, 36.22, 36.78, 37.44, 39.08. На Фиг.10 представлена картина дифракции рентгеновских лучей на порошке для Формы IV.
ИК-спектр поглощения для Формы IV был измерен, как описано здесь, и он имеет полосы в следующих приблизительных позициях (см-1): 536.57, 600.07, 634.53, 657.47, 792.30, 840.23, 859.36, 873.69, 896.83, 951.68, 1021.79, 1092.70, 1135.05, 1215.91, 1259.88, 1320.12, 1352.07, 1366.62, 1418.17, 1449.57, 1468.60, 1508.23, 1578.49, 1613.42, 2366.47, 2741.05, 3020.46, 3316.12. На Фиг.11 представлен ИК-спектр поглощения полиморфной Формы IV.
ДСК-термограмма для Формы IV, представленная на Фиг.12, показывает начало эндотермы при 204,0°С при скорости сканирования 5°С/мин.
Б. Полиморфная Форма I (гидрат А)
Полиморфная Форма I Соединения I представляет собой гидрат. Полиморфная Форма I Соединения I может быть получена путем обработки полиморфной Формы IV (МЕОН сольват) водой.
Полиморфная Форма I Соединения I химически стабильна при 40°С в условиях относительной влажности 75% в течение по меньшей мере 3 месяцев, но она будет превращаться в Форму III (гидрат В) через одну неделю при этих условиях. Форма I физически стабильна в условиях окружающей среды в течение по меньшей мере 3 месяцев.
Полиморфная Форма I Соединения I имеет растворимость в воде 2,8 мг/мл при рН 5,4.
Картина дифракции рентгеновских лучей на порошке Формы 1 была измерена как описано здесь, и она имеет пики при следующих приблизительных углах дифракции (2θ); 10.56, 10.88, 11.14, 11.54, 13.46, 13,90, 14.30, 15.20, 16.34, 17.12, 18.02, 19.30, 20.02, 20.72, 21.22, 21.76, 22.50, 22.94, 23.70, 24.00, 24.32, 25.02, 25.54, 26.22, 26.60, 27.20, 27.76, 29.02, 29.38, 29.74, 31.26, 31.76, 32.12, 33.52, 35.78. На Фиг.1 представлена картина дифракции рентгеновских лучей на порошке для Формы I.
ИК-спектр поглощения Формы I был измерен, как описано здесь, и он имеет полосы в следующих приблизительных позициях (см-1): 520.70, 605.60, 669.72, 705.80, 785.46, 840.18, 870.55, 895.86, 958.01, 1017.72, 1066.76, 1131.33, 1220.68, 1257.70, 1321.43, 1346.32, 1366.48, 1421.79, 1452.75, 1476.19, 1509.10, 1578.58, 1609.21. На Фиг.2 представлен ИК-спектр поглощения полиморфной Форма I.
ДСК-термограмма для Формы I, представленная на Фиг.3, показывает начало эндотермы при 202°С при скорости сканирования 5°С/мин.
В. Полиморфная Форма II (безводная форма)
Полиморфная Форма II Соединения I представляет собой безводную форму. Форма II может быть получена дегидратацией Формы I.
Полиморфная Форма II Соединения 1 физически стабильна в условиях окружающей среды в течение по меньшей мере 3 месяцев. Форма II может превращаться в Форму III (гидрат В) при 40°С в условиях относительной влажности 75% через 1 неделю или при 25°С в условиях относительной влажности 90% в течение ночи.
Полиморфная Форма II Соединения I имеет растворимость в воде 3,0 мг/мл при рН 5,4. Исследование зависимости растворимости Формы II от рН проводили при рН в пределах от 3,0 до 8,0. Буферными системами, использованными в этом исследовании, были 50 мМ фосфат аммония для рН 3,0 и 4,0 и 50 мМ фосфат натрия для рН от 5,0 до 8,0. Результаты по растворимости показаны в Таблице 1 и на Фиг.15. Можно видеть, что растворимость Формы II снижается с увеличением рН с 3,0 до 8,0. Поскольку Форма II представляет собой фосфатную соль, и в исследовании зависимости растворимости от рН были использованы фосфатные буферы, растворимость, определенная в этих буферных системах, ниже, чем растворимость в воде из-за суммарного ионного эффекта.
Зависимость растворимости Формы II от рН
Картину дифракции рентгеновских лучей на порошке Формы II измеряли, как описано здесь, и она имеет пики при следующих приблизительных углах дифракции (2θ): 7.02, 11.22, 12.12, 14.00, 14.44, 15.36, 18.12, 20.12, 20.92, 22.52, 23.12, 25.28, 26.96, 28.00, 30.02, 31.40, 32.04, 33.72, 34.62, 36.66, 37.26, 39.04. На Фиг.4 представлена картина дифракции рентгеновских лучей на порошке для Формы II.
ИК-спектр поглощения Формы II измеряли, как описано здесь, и он имеет полосы в следующих приблизительных позициях (см-1): 514.55, 552.15, 595.96, 662.04, 683.16, 784.79, 842,83, 878.85, 958.55, 1017.68, 1057.72, 1129.87, 1259.81, 1320.16, 1342.76, 1367.10, 1455.18, 1508.93, 1578.68, 1610.29, 2345.53, 2375.37, 2756.52, 3015.19, 3277.71. На Фиг.5 представлен ИК-спектр поглощения полиморфной Формы II.
ДСК-термограмма для Формы II, представленная на Фиг.6, показывает начало эндотермы при 205°С при скорости сканирования 5°С/мин.
Г. Полиморфная Форма III (гидрат В)
Полиморфная Форма III Соединения I представляет собой гидрат. Полиморфная Форма III Соединения I может быть получена гидратированием Формы I или Формы II.
Полиморфная Форма III Соединения I физически и химически стабильна при 40°С в условиях относительной влажности 75% в течение по меньшей мере 3 месяцев.
Полиморфная Форма III Соединения I имеет растворимость в воде 2,7 мг/мл при рН 5,4.
Картина дифракции рентгеновских лучей на порошке Формы III была измерена, как описано здесь, и она имеет пики при следующих приблизительных углах дифракции (2θ): 10.66, 10.96, 11.62, 13.54, 15.28, 16.42, 19.36, 20.80, 21.30, 21.86, 22.56, 23.28, 23.78, 24.06, 24.42, 25.12, 26.30, 26.62, 27.32, 27.84, 28.32, 29.10, 29.50, 29.80, 30.24, 31.84, 32.20, 32.58, 35.86. На Фиг.7 представлена картина дифракции рентгеновских лучей на порошке для Формы III.
ИК-спектр поглощения Формы III был измерен, как описано здесь, и он имеет полосы в следующих приблизительных позициях (см-1): 521.02, 545.63, 599.97, 672.96, 704.78, 786.38, 811.92, 839.21, 870.68, 897.67, 956.56, 1017.24, 1076.05, 1131.23, 1222.77, 1256.88, 1325.51, 1346.28, 1365.33, 1421.86, 1451.44, 1478,91, 1509.39, 1578.35, 1607.08, 2300.20, 2346.17, 2502.23, 2828.24, 3011.62, 3299.59, 3536.14. На Фиг.8 представлен ИК-спектр поглощения полиморфной Формы III.
ДСК-термограмма для Формы III, представленная на Фиг.9, показывает начало эндотермы при 203°С при скорости сканирования 5°С/мин.
Д. Полиморфная Форма V (гидрат С)
Полиморфная Форма V Соединения I была образована в процессе исследований стабильности Формы II при хранении при 40°С в условиях относительной влажности 75% в течение периода времени 6 месяцев. Полиморфная Форма V Соединения 1 физически и химически стабильна при комнатной температуре в течение по меньшей мере 3 месяцев.
Полиморфная Форма V Соединения 1 имеет растворимость в воде 3,0 мг/мл при рН 5,4.
Картина дифракции рентгеновских лучей на порошке Формы V была измерена, как описано здесь, и она имеет пики при следующих приблизительных углах дифракции (2θ): 8.64, 9.05, 10.26, 10.56, 10.84, 13.88, 14.85, 15.24, 16.24, 16.59, 17.07, 18.26, 18.56, 19.26, 19.56, 20.31, 21.16, 21.61, 22.38, 22.96, 23.40, 24.04, 24.34, 24.92, 25.46, 25.78, 26.22, 26.59, 27.10, 27.60, 27.88, 28.24, 29.03, 30.08, 30.44, 31.54, 32.08, 32.52, 36.45, 36.90, 37.14, 37.58, 37.74, 38.30, 39.00. На Фиг.13 представлена картина дифракции рентгеновских лучей на порошке Формы V.
ИК-спектр поглощения Формы V был измерен, как описано здесь, и он имеет полосы в следующих приблизительных позициях (см-1): 955.28, 1019.70, 1045.84, 1067.25, 1092.06, 1104.99, 1133.50, 1260.13, 1320.27, 1366.85, 1418.85, 1450.75, 1470.01, 1579.05, 1613.39, 1632.61, 2761.48, 3024.44, 3278.09, 3312.93. На Фиг.16 представлен ИК-спектр поглощения полиморфной Формы V.
ДСК-термограмма Формы V, представленная на Фиг.17, имеет эндотерму при 199,40°С с двумя пиками десольватации при 57,29°С и 110,73°С соответственно.
Е. Полиморфная Форма VI
Полиморфная Форма VI Соединения I может быть получена приготовлением водной суспензии Формы II и нагреванием ее при 100°С в течение ночи. Как показано на Фиг.14, конверсия началась при 80°С и закончилась после выдерживания при 100°С в течение ночи.
Картина дифракции рентгеновских лучей на порошке Формы VI была измерена, как описано здесь, и она имеет пики при следующих приблизительных углах дифракции (2θ): 8.44, 8.71, 14.78, 15.10, 15.73, 16.06, 16.24, 16.9, 17.2, 19.99, 22.32, 22.60, 22.94, 23.49, 23.84, 24.55, 25.30, 25.48, 27.74, 26.02, 27.47, 27.84, 28.10, 28.40, 34.02, 35.12, 35.54, 35.88. На Фиг.18 представлена рентгеновская порошковая дифрактограмма полиморфной Формы VI.
ИК-спектр поглощения Формы VI был измерен, как описано здесь, и он имеет полосы в следующих приблизительных позициях (см-1): 535.82, 786.11, 841.00, 954.18, 1020.17, 1133.96, 1216.98, 1260.79, 1320.11, 1367.35, 1418.66, 1450.88, 1470.60, 1508.44, 1579.24, 1613.51, 2410.94, 2760.82, 3025.77, 3277.18. На Фиг.19 представлен ИК-спектр поглощения полиморфной Формы VI.
ДСК-термограмма для Формы VI, представленная на Фиг.20, имеет эндотерму при 219,68°С с двумя пиками десольватации при 88,42°С и 112°С соответственно.
Ж. Аморфная форма
Аморфная Форма может быть получена лиофилизацией водного раствора Соединения I.
Картина дифракции рентгеновских лучей на порошке этой аморфной формы характеризуется типичным аморфным пиком в виде широкого горба от 4 до 40° и не имеет каких-либо остроконечных пиков, характерных для кристаллической формы. На Фиг.21 представлена картина дифракции рентгеновских лучей на порошке для аморфной формы.
ИК-спектр поглощения аморфной формы, представленный на Фиг.22, был измерен, как описано здесь, и он имеет пики в следующих приблизительных позициях (см-1): 433, 505, 518, 596, 609, 664, 674, 705, 746, 785, 856, 896, 937, 955, 1020, 1066, 1106, 1132, 1217, 1260, 1319, 1349, 1367, 1419, 1452, 1472, 1508, 1579, 2300, 2349, 2407, 2830, 3031, 3256.
Спектр комбинационного рассеяния для аморфной формы, представленный на Фиг.23, имеет пики сдвигов частот комбинационного рассеяния (см-1) при приблизительно 1068, 1323, 1350, 1371, 1453, 1556, 1581, 1616.
ДСК-термограмма для аморфной формы, представленная на Фиг.24, не имеет изолированных пиков.
II. Фармацевтическая композиция по изобретению
Активные агенты (т.е. полиморфы или твердые формы, содержащие два или более таких полиморфов или аморфную форму, Соединения I, описанные здесь) по изобретению могут быть включены в состав фармацевтических композиций, пригодных для медицинского применения у млекопитающих. Для предоставления пациенту эффективной дозировки Формы I, II, III, IV, V, VI и аморфной формы Соединения I может быть использован любой путь введения.
Например, могут быть использованы пероральные или парентеральные препараты и тому подобное. Лекарственные формы включают капсулы, таблетки, дисперсии, суспензии и тому подобное, например капсулы и/или таблетки с энтеросолюбильной оболочкой, капсулы и/или таблетки, содержащие гранулы Соединения 1 в энтеросолюбильной оболочке. Во всех лекарственных формах полиморфные Формы I, II, III, IV, V, VI и аморфная форма Соединения 1 могут быть смешанными с другими подходящими компонентами. Композиции могут для удобства быть представлены в стандартной лекарственной форме и могут быть приготовлены любыми способами, известными в фармацевтической области. Фармацевтические композиции по изобретению содержат терапевтически эффективное количество активного агента и один или более чем один инертный фармацевтически приемлемый носитель и возможно любые другие терапевтические ингредиенты, стабилизаторы или тому подобное. Носитель(и) должен быть фармацевтически приемлемыми в смысле совместимости с другими ингредиентами препарата и не оказывать недопустимых вредных воздействий на реципиента. В состав композиции могут также входить разбавители, буферы, связующие вещества, разрыхлители, загустители, смазывающие вещества, консерванты (в том числе антиоксиданты), корригенты, агенты, маскирующие вкус, неорганические соли (например хлорид натрия), противомикробные агенты (например бензалкония хлорид), подсластители, антистатики, поверхностно-активные вещества (например полисорбаты, такие как «TWEEN 20» и «TWEEN 80», и неионные поверхностно-активные вещества, такие как F68 и F88, поставляемые на рынок фирмой BASF), сложные эфиры сорбитана, липиды (например фосфолипиды, такие как лецитин и другие фосфатидилхолины, фосфатидилэтаноламины, жирные кислоты и эфиры жирных кислот, стероиды (например холестерин)) и хелатирующие агенты (например EDTA (этилендиаминтетрауксусная кислота), цинк и другие подходящие катионы). Другие фармацевтические эксципиенты и/или добавки, подходящие для использования в композициях по изобретению, перечислены в "Remington: The Science & Practice of Pharmacy", 19 th ed., Williams & Williams, (1995), и в "Physician's Desk Reference", 52 nd ed., Medical Economics, Montvale, NJ (1998), и в "Handbook of Pharmaceutical Excipients", Third Ed., Ed. A.H.Kibbe, Pharmaceutical Press, 2000. Активные агенты по изобретению могут быть включены в состав композиций, включая композиции, подходящие для перорального, ректального, местного, назального, офтальмического или парентерального (включая интраперитонеальное, внутривенное, подкожное или внутримышечное инъецирование) введения.
Количество активного агента в композиции будет варьироваться в зависимости от целого ряда факторов, в том числе от лекарственной формы, состояния, которое лечат, целевой обследуемой группы пациентов и других соображений, и без труда будет определено специалистом в данной области. Терапевтически эффективное количество представляет собой количество, необходимое для модулирования, регуляции или ингибирования фермента PARP. На практике оно будет варьироваться в широких пределах в зависимости от конкретного активного агента, тяжести состояния, которое лечат, обследуемой группы пациентов, стабильности препарата и тому подобного. Композиции будут содержать активный агент в количестве в пределах от примерно 0,001% по массе до примерно 99% по массе, предпочтительно от примерно 0,01% до примерно 5% по массе и более предпочтительно от примерно 0,01% до 2% по массе, и это также будет зависеть от относительных количеств эксципиентов/добавок, входящих в состав композиции.
Фармацевтическую композицию по изобретению вводят в стандартной лекарственной форме, полученной путем объединения терапевтически эффективного количества активного агента в качестве активного ингредиента с одним или более подходящими фармацевтическими носителями общепринятыми способами. Эти способы могут включать смешивание, гранулирование и прессование или растворение ингредиентов, как подходит для целевого препарата.
Используемый(е) фармацевтический(е) носитель(и) может быть либо твердым, либо жидким. Примеры твердых носителей включают сахара (например лактозу, сахарозу, маннит или сорбит), тальк, желатин, агар, пектин, аравийскую камедь, стеарат магния, стеариновую кислоту и тому подобное. Примеры жидких носителей включают сироп, арахисовое масло, оливковое масло, воду и тому подобное. Аналогично, носитель(и) может включать известные в данной области вещества, обеспечивающие отсроченное или длительное высвобождение, такие как глицерилмоностеарат или глицерилдистеарат, один или вместе с воском, этилцеллюлозой, гидроксипропилметилцеллюлозой, метилметакрилатом и тому подобным.
Могут быть использованы различные фармацевтические формы. Так, если используют твердый носитель, то препарат может быть таблетированным, помещенным в твердую капсулу в форме порошка или гранул или может быть в форме троше или пастилки. Количество твердого носителя может варьировать, но обычно оно будет составлять от примерно 25 мг до примерно 1 г. Если используют жидкий носитель, то препарат может быть в форме сиропа, эмульсии, мягкой желатиновой капсулы, стерильного инъекционного раствора или суспензии в ампуле или в пузырьке или в форме жидкой неводной суспензии.
Для получения стабильной водорастворимой дозовой формы Соединение I может быть растворено в водном растворе органической или неорганической кислоты, например 0,3 М растворе янтарной кислоты или лимонной кислоты. Если растворимая солевая форма недоступна, то активный агент может быть растворен в подходящем сорастворителе или комбинации сорастворителей. Примеры подходящих сорастворителей включают, но не ограничиваются ими, спирт, пропиленгликоль, полиэтиленгликоль 300, полисорбат 80, глицерин и тому подобное в концентрации в пределах 0-60% от общего объема. Композиция может быть также в форме раствора Соединения I в подходящем водном носителе, таком как вода или изотонический физиологический раствор или раствор декстрозы.
Понятно, что фактические дозировки активных агентов, используемые в композициях по изобретению, будут варьировать в зависимости от того, какая конкретная кристаллическая форма используется, каков конкретный состав композиции, способ введения в конкретный сайт, конкретный хозяин и заболевание, которое лечат. Используя стандартные тесты для определения дозировки, принимая во внимание экспериментальные данные для агента, специалисты в данной области смогут установить оптимальные дозировки с учетом данной совокупности условий. Для перорального введения обычно применяемая типичная суточная доза составляет от примерно 0,001 до примерно 1000 мг/кг массы тела, более предпочтительно от примерно 0,001 до примерно 50 мг/кг массы тела при курсах лечения, повторяемых с соответствующими интервалами. При введении пролекарств их обычно дозируют при массовых уровнях, которые химически эквивалентны массовым уровням полностью активной формы. При практическом осуществлении изобретения наиболее подходящий путь введения, а также величина терапевтической дозы будут зависеть от природы и тяжести заболевания, которое лечат. Доза и частота введения дозы также могут варьироваться в зависимости от возраста, массы тела и ответной реакции индивидуального пациента. В общем, подходящая пероральная доза может охватывать диапазон доз от 5 мг до 250 мг суммарной суточной дозы, которые вводят одной дозой или равными разделенными дозами. Предпочтительный диапазон дозировки составляет от 10 мг до 80 мг. В общем, подходящая парентеральная доза может охватывать диапазон доз от 5 мг до 200 мг суммарной суточной дозы, которую вводят одной дозой или равными разделенными дозами. Предпочтительный диапазон дозировки составляет от 10 мг до 100 мг.
Композиции по изобретению могут быть изготовлены способами, общеизвестными для приготовления фармацевтических композиций, например с использованием стандартных методик, таких как смешивание, растворение, гранулирование, дражирование, растирание в порошок, эмульгирование, инкапсулирование, включение или лиофилизация. Фармацевтические композиции могут быть приготовлены в виде препарата общепринятым способом с использованием одного или более физиологически приемлемых носителей, которые могут быть выбраны из эксципиентов и вспомогательных веществ, которые облегчают переработку активных соединений в препараты, которые могут быть использованы в фармацевтических целях.
Для перорального введения соединения без труда могут быть приготовлены в виде препаратов путем объединения активных агентов с фармацевтически приемлемыми носителями, известными в данной области. Такие носители делают возможным получение композиций по изобретению в виде таблеток, пилюль, драже, капсул, гелей, сиропов, взвесей, суспензий и тому подобного для перорального проглатывания пациентом, которого лечат. Фармацевтические препараты для перорального применения могут быть получены с использованием твердого эксципиента в смеси с активным агентом, возможно путем измельчения полученной смеси и обработки смеси гранул после добавления подходящих вспомогательных веществ, если требуется, с получением таблеток или ядер драже. Подходящие эксципиенты включают наполнители, такие как сахара, в том числе лактоза, сахароза, маннит или сорбит, и целлюлозные препараты, например маисовый крахмал, пшеничный крахмал, рисовый крахмал, картофельный крахмал, желатин, камедь, метилцеллюлозу, гидроксипропилметилцеллюлозу, натриевую карбоксиметилцеллюлозу или поливинилпирролидон (PVP). Если желательно, могут быть добавлены разрыхлители, такие как поперечно-сшитый поливинилпирролидон, агар или альгиновая кислота или ее соль, например альгинат натрия.
Ядра драже покрывают подходящими оболочками. Для этой цели могут быть использованы концентрированные растворы сахара, которые возможно могут содержать гуммиарабик, поливинилпирролидон, гель карбопол, полиэтиленгликоль и/или диоксид титана, растворы лаков и подходящие органические растворители или смеси растворителей. Для идентификации или различения разных комбинаций активных агентов в покрытия для таблеток или драже могут быть добавлены красители или пигменты.
Фармацевтические препараты, которые можно применять, включают надвижные капсулы, изготовленные из желатина, а также мягкие, запаянные капсулы, изготовленные из желатина и пластификатора, такого как глицерин или сорбит. Надвижные капсулы могут содержать в себе активные ингредиенты в смеси с наполнителями, такими как лактоза, связующими, такими как крахмал, и/или смазывающими веществами, такими как тальк или стеарат магния, и возможно стабилизаторами. В мягких капсулах активные агенты могут быть растворенными или суспендированными в подходящих жидкостях, таких как жирные масла, вазелиновое масло или жидкие полиэтиленгликоли. Дополнительно могут быть добавлены стабилизаторы. Все препараты для перорального введения должны быть в дозировках, подходящих для такого введения. Для буккального введения композиции могут быть выполнены в форме таблеток или пастилок, изготовленных общепринятым способом.
Для введения интраназально или ингаляцией соединения для использования по настоящему изобретению удобно доставлять в форме, обеспечивающей распыление аэрозоля из упаковок под давлением или небулайзера с использованием подходящего пропеллента, например дихлордифторматана, трихлорфторметана, дихлортетрафторэтана, диоксида углерода или другого подходящего газа. В случае аэрозоля под давлением дозировочную единицу можно устанавливать с помощью клапана для доставки отмеренного количества. Капсулы и картриджи из желатина для использования в ингаляторе или инсуффляторе и т.п.могут быть приготовлены в виде препарата, содержащего порошковую смесь соединения и подходящей порошковой основы, такой как лактоза или крахмал.
Активные агенты могут быть включены в состав препарата для парентерального введения инъецированием, например болюсным инъецированием или непрерывной инфузией. Препараты для инъецирования могут быть представлены в стандартной лекарственной форме, например в ампулах или многодозовых контейнерах, с добавлением консерванта. Композиции могут принимать такие формы, как суспензии, растворы или эмульсии в масляных или водных носителях и могут содержать вспомогательные технологические агенты, такие как суспендирующие, стабилизирующие и/или диспергирующие агенты.
Фармацевтические препараты для парентерального введения включают суспензии активных агентов и могут быть приготовлены в виде подходящих масляных инъекционных суспензий. Подходящие липофильные растворители или носители включают жирные масла, такие как кунжутное масло, или синтетические эфиры жирных кислот, такие как этилолеат или триглицериды, или липосомы. Водные инъекционные суспензии могут содержать вещества, которые увеличивают вязкость суспензии, такие как натриевая соль карбоксиметилцеллюлозы, сорбит или декстран. Возможно, суспензия может также содержать подходящие стабилизаторы или агенты, которые повышают растворимость активных агентов для обеспечения получения высококонцентрированных растворов.
Для введения в глаз активный агент доставляют в таком фармацевтически приемлемом офтальмическом носителе, который поддерживает Соединение 1 в контакте с глазной поверхностью в течение периода времени, достаточного для того, чтобы соединение проникло в корнеальную и внутренние области глаза, включая, например, переднюю камеру, заднюю камеру, стекловидное тело, вгутриглазную жидкость, стекловидное тело, роговицу, радужную оболочку/цилиарное тело, хрусталик, сосудистую оболочку/сетчатку и склеру. Фармацевтически приемлемый офтальмический носитель может представлять собой, например, мазь, растительное масло или инкапсулирующий материал. Активный агент по изобретению также можно инъецировать прямо в стекловидное тело и внутриглазную жидкость или через мембрану, покрывающую мышцы и нервы позади глазного яблока.
Альтернативно, активный ингредиент может быть в форме порошка для разведения перед применением подходящим носителем, например стерильной апирогенной водой. Соединения также могут быть включены в состав препаратов ректальных или вагинальных композиций, таких как суппозитории или удерживающие клизмы, например, содержащие общепринятые суппозиторные основы, такие как масло какао или другие глицериды.
В дополнение к препаратам, описанным выше, полиморфные формы могут быть приготовлены также в виде депо-препарата. Такие длительно действующие препараты можно вводить имплантацией (например, подкожно или внутримышечно) или внутримышечной инъекцией. Так, например, полиморфные формы могут быть приготовлены в виде такого препарата с использованием подходящих полимерных или гидрофобных веществ (например в виде эмульсии в приемлемом масле) или ионообменных смол, или в виде труднорастворимых производных, например в виде труднорастворимой соли.
Дополнительно, активные агенты можно доставлять с использованием систем длительного высвобождения, таких как полупроницаемые матрицы из твердых гидрофобных полимеров, содержащих терапевтический агент. Различные материалы, обеспечивающие длительное высвобождение, установлены и известны специалистам в данной области. Капсулы длительного высвобождения могут, в зависимости от их химической природы, высвобождать соединения в течение времени от нескольких недель до 100 суток и более. В зависимости от химической природы и биологической стабильности терапевтического реагента могут быть использованы дополнительные стратегии стабилизации белков.
Фармацевтические композиции также могут содержать подходящие твердо- или геле-фазные носители или эксципиенты. Примеры таких носителей или эксципиентов включают карбонат кальция, фосфат кальция, сахара, крахмалы, производные целлюлозы, желатин и полимеры, такие как полиэтиленгликоли.
III. Способы применения полиморфов по изобретению
Полиморфные формы Соединения 1 по изобретению полезны для опосредования активности поли(ADP-рибоза)полимеразы (PARP). Более конкретно, полиморфные формы полезны в качестве хемосенсибилизаторов, которые повышают эффективность радиотерапии или цитотоксических лекарственных средств, чей механизм зависит от повреждения ДНК. Эти лекарственные средства включают, но не ограничиваются ими, темозоломид (SCHER1NG), иринотекан (PFIZER), топотекан (GLAXO SMITHKLINE), цисплатин (BRISTOL MEYERS SQUIBB; AM PHARM PARTNERS; BEDFORD; GENSIA SICOR PHARMS; PHARMACHEMIE) и доксорубицина гидрохлорид (AM PHARM PARTNERS; BEDFORD; GENSIA; SICOR PHARMS; PHARMACHEMIE; ADRIA; ALZA).
Полиморфные формы Соединения 1 по изобретению полезны также для усиления индуцирования экспрессии гена Reg в (3 клетках и гена HGF и, соответственно, стимулирования пролиферации панкреатических β-клеток островков Лангерганса и подавления апоптоза этих клеток. Кроме того, полиморфные формы Соединения 1 по изобретению полезны для получения косметических средств, например лосьонов после загара.
Терапевтически эффективные количества агентов по изобретению можно вводить, обычно в форме фармацевтической композиции, для лечения заболеваний, опосредованных модулированием или регулированием PARP. Термин "эффективное количество" означает, что количество агента, которое при введении млекопитающему, в том числе человеку, нуждающемуся в таком лечении, достаточного для осуществления лечения заболевания, опосредованного активностью одного или более чем одного фермента PARP. Таким образом, терапевтически эффективным количеством соединения по изобретению является количество, достаточное для модулирования, регулирования или ингибирования активности одного или более чем одного фермента PARP таким образом, что болезненное состояние, которое опосредовано этой активностью, ослабляется или облегчается. Эффективное количество данного соединения будет варьироваться в зависимости от факторов, таких как болезненное состояние и его тяжесть и особенность и состояние (например, масса) млекопитающего, нуждающегося в лечении, но тем не менее может быть рутинно определена специалистом в данной области. Термин "лечение" означает по меньшей мере ослабление болезненного состояния у млекопитающего, включая человека, на которое влияет, по меньшей мере частично, активность одного или более чем одного фермента PARP, и включает предупреждение болезненного состояния, возникшего у млекопитающего, в частности когда обнаружено, что млекопитающее предрасположено иметь это болезненное состояние, но еще не диагностировано, что оно имеет его;
модулирование и/или ингибирование болезненного состояния; и/или облегчение болезненного состояния. Типичное болезненное состояние включает рак.
Активность полиморфных форм Соединения 1 в качестве модуляторов активности PARP может быть измерена любым из способов, доступных специалистам в данной области, включая in vivo и/или in vitro анализы. Примеры подходящих анализов по измерению активности включают анализы, описанные в патенте США № 6495541 и в заявке на предварительный патент США № 60/612458, описания которых во всей их полноте включены в данное описание ссылкой.
Настоящее изобретение также относится к терапевтическим способам лечения болезненного состояния, опосредованного активностью PARP, например рака и целого ряда болезненных и токсических состояний, в которые вовлечены оксидативный или индуцированный оксидом азота стресс и последующая гиперактивация PARP. Такие состояния включают, но не ограничиваются ими, неврологические и нейродегенеративные расстройства (например болезнь Паркинсона, болезнь Альцгеймера), сердечно-сосудистые расстройства (например инфаркт миокарда, ишемия-репефузионное повреждение), диабетическая сосудистая дисфункция, цисплатин-индуцированная нефротоксичность. Терапевтические способы по настоящему изобретению включают введение млекопитающему, нуждающемуся в этом, терапевтически эффективного количества фармацевтической композиции, которая содержит любую из полиморфных форм или фармацевтических композиций, описанных выше.
Настоящее изобретение также относится к комбинированному терапевтическому способу лечения болезненного состояния, опосредованного активностью PARP, включающему введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества фармацевтической композиции, которая содержит любую из полиморфных форм или фармацевтических композиций, описанных выше, в комбинации с терапевтически эффективным количеством одного или более веществ, выбранных из противоопухолевых агентов, агентов против ангиогенеза, ингибиторов сигнальной трансдукции и антипролиферативных агентов. Такие вещества включают вещества, описанные в международных публикациях №№ WO 00/38715, WO 00/38716, WO 00/38717, WO 00/38718, WO 00/38719, WO 00/38730, WO 00/38665, WO 00/37107 и WO 00/38786, описания которых во всей их полноте включены в данное описание ссылкой.
Примеры противоопухолевых агентов включают темозоломид (SCHERING), иринотекан (PFIZER), топотекан (GLAXO SMITHKLINE), цисплатин (BRISTOL MEYERS SQUIBB; AM PHARM PARTNERS; BEDFORD; GENSIA SICOR PHARMS; PHARMACHEMIE) и доксорубицина гидрохлорид (AM PHARM PARTNERS; BEDFORD; GENSIA; SICOR PHARMS; PHARMACHEMIE; ADRIA; ALZA).
Дополнительные примеры противоопухолевых агентов включают митотические ингибиторы, например производные алкалоидов барвинка, такие как винбластин, винорелбин, виндесин и винкристин; colchines allochochine, галихондрин, N-бензоилтриметил-метиловый эфир колхициновой кислоты, доластатин 10, мэйстансин, ризоксин, таксаны, такие как таксол (паклитаксел), доксетаксел (таксотер), 2'-N-[3-(диметиламино)пропил]глутарамат (производное таксола), тиохолкицин, тритилцистеин, тенипозид, метотрексат, азатиоприн, фторурацил, цитозина арабинозид, 2'2'-дифтордезоксицитидин (гемцитабин), адриамицин и митамицин. Алкилирующие агенты, например карбоплатин, оксиплатин, ипроплатин, этиловый эфир N-ацетил-DL-саркозил-L-лейцина (Asaley или Asalex), 1,4-циклогексадиен-1,4-дикарбаминовая кислота, 2,5-бис(1-азирдинил)-3,6-диоксо-, диэтиловый эфир (диазиквон), 1,4-бис(метансульфонилокси)бутан (бисульфан или лейкосульфан), хлорозотоцин, кломезон, цианоморфолинодоксорубицин, циклодизон, диангидроглактитол, флюородопан, гепсульфам, митомицие С, гикантеонемитомицин С, митозоламид, 1-(2-хлорэтил)-4-(3-хлорпропил)-пиперазина дигидрохлорид, пиперазиндион, пипоброман, порфиромицин, спирогидантоиновый аналог иприта, тероксирон, тетраплатин, тиотепа, триэтиленмеламин, урацильный азотистый аналог иприта, бис(3-мезилоксипропил)амина гидрохлорид, митомицин, агенты на основе нитрозомочевины, такие как циклогексил-хлорэтилнитрозомочевина, метилциклогексил-хлорэтилнитрозомочевина, 1-(2-хлорэтил)-3-(2,6-диоксо-3-пиперидил)-1-нитрозо-мочевина, бис(2-хлорэтил)нитрозомочевина, прокарбазин, дакарбазин, соединения, родственные азотистому аналогу иприта, такие как мехлорэтамин, циклофосфамид, ифосфамид, мелфалан, хлорамбуцил, эстрамустина натрия фосфат и строптозоин. ДНК антиметаболиты, например 5-фторурацил, цитозина арабинозид, гидроксимочевина, 2-[(3-гидрокси-2-пиринодинил)метилен]-гидразинкарботиоамид, дезоксифторуридин, 5-гидрокси-2-формилпиридина тиосемикарбазон, альфа-2'-дезокси-6-тиогуанозин, афидиколина глицинат, 5-азадезоксицитидин, бета-тиогуанина дезоксирибозид, циклоцитидин, гуаназол, инозина гликодиальдегид, макбецин II, пиразолимидазол, кладрибин, пентостатин, тиогуанин, меркаптопурин, блеомицин, 2-хлордезоксиаденозин, ингибиторы тимидилатсинтазы, такие как ралтитрексед и пеметрексед-динатрий, клофарабин, флоксуридин и флударабин. ДНК/РНК антиметаболиты, например L-аланозин, 5-азацитидин, ацивицин, аминоптерин и их производные, такие как N-[2-хлор-5-[[(2,4-диамино-5-метил-6-хиназолинил)-метил]амино]бензил]-L-аспарагиновая кислота, N-[4-[[(2,4-диамино-5-этил-6-хиназолинил)метил]амино]бензоил]-L-аспарагиновая кислота, N-[2-хлор-4-[[(2,4-диаминоптеридинил)метил]амино]бензоил]-L-аспарагиновая кислота, растворимый антифол Бейкера, дихлораллил лоусон, бреквинар, фтораф, дигидро-5-азацитидин, метотрексат, N-(фосфоноацетил)-L-аспарагиновой кислоты тетранатриевая соль, пиразофуран, триметрексат, пликамицин, актиномицин D, криптофицин и аналоги, такие как криптофицин-52 или, например, один из предпочтительных антиметаболитов, раскрытых в заявке на Европейский патент № 239362, такой как N-(5-[N-(3,4-дигидро-2-метил-4-оксохиназолин-6-илметил)-N-метиламино]-2-теноил)-L-глутаминовая кислота; ингибиторы факторов роста; ингибиторы клеточного цикла; интеркалирующие антибиотики, например адриамицин и блеомицин; протеины, например интерферон; и антигормоны, например антиэстрогены, такие как Nolvadex™ (тамоксифен) или, например, антиандрогены, такие как Casodex™ (4'-циано-3-(4-фторфенилсульфонил)-2-гидрокси-2-метил-3'-(трифторметил)-пропиоанилид). Такое комбинированное лечение достигается путем одновременного, последовательного или раздельного введения индивидуальных компонентов лечения.
Антиангиогенные агенты включают ингибиторы ММР-2 (матриксной металлопротеиназы 2), ингибиторы ММР-9 (матриксной металлопротеиназы 9) и ингибиторы СОХ-11 (циклооксигеназы II). Примеры полезных ингибиторов СОХ-11 включают CELEBREX™ (алекоксиб), валдекоксиб и рофекоксиб. Примеры полезных ингибиторов матриксных металлопротеиназ раскрыты в WO 96/33172 (дата публикации 24 октября 1996), WO 96/27583 (дата публикации 7 марта 1996), заявке на Европейский патент № 97304971,1 (дата подачи 8 июля 1997), заявке на Европейский патент № 99308617.2 (дата подачи 29 октября 1999), WO 98/07697 (дата публикации 26 февраля 1998), WO 98/03516 (дата публикации 29 января 1998), WO 98/34918 (дата публикации 13 августа 1998), WO 98/34915 (дата публикации 13 августа 1998), WO 98/33768 (дата публикации 6 августа 1998), WO 98/30566 (дата публикации 16 июля 1998), Европейском патенте 606046 (дата публикации 13 июля 1994), Европейском патенте 931788 (дата публикации 28 июля 1999), WO 90/05719 (дата публикации 31 мая 1990), WO 99/52910 (дата публикации 21 октября 1999), WO 99/52889 (дата публикации 21 октября 1999), WO 99/29667 (дата публикации 17 июня 1999), международной заявке № РСТ/IB 98/01113 (дата подачи 21 июля 1998), заявке на Европейский патент № 99302232.1 (дата подачи 25 марта 1999), заявке на патент Великобритании № 9912961.1 (дата подачи 3 июня 1999), предварительной заявке на патент США № 60/148464 (дата подачи 12 августа 1999), патенте США 5863949 (дата выдачи 26 января 1999), патенте США 5861510 (дата выдачи 19 января 1999) и Европейском патенте 780386 (дата публикации 25 июня 1997), которые все во всей их полноте включены в данное описание изобретения ссылкой. Предпочтительными ингибиторами ММР-2 и ММР-9 являются ингибиторы, которые имеют небольшую активность или не имеют активности ингибирования ММР-1. Более предпочтительными являются ингибиторы, которые селективно ингибируют ММР-2 и/или ММР-9 по сравнению с другими матриксными металлопротеиназами (то есть ММР-1, ММР-3, ММР-4, ММР-5, ММР-6, ММР-7, ММР-8, ММР-10, ММР-11, ММР-12 и ММР-13).
Примеры ингибиторов ММР включают AG-3340, RO 32-3555, RS 13-0830 и следующие соединения: 3-[[4-(4-фтор-фенокси)бензолсульфонил]-(1-гидроксикарбамоил-циклопентил)амино]пропионовая кислота, 3-экзо-3-[4-(4-фтор-фенокси)бензолсульфониламино]-8-окса-бицикло[3.2.1]октан-3-карбоновой кислоты гидроксиамид, (2R,3R)-1-[4-(2-хлор-4-фтор-бензилокси)-бензолсульфонил]-3-гидрокси-3-метил-пиперидин-2-карбоновой кислоты гидроксиамид, 4-[4-(4-фтор-фенокси)бензолсульфониламино]тетрагидропиран-4-карбоновой кислоты гидроксиамид, 3-[[4-(4-фтор-фенокси)бензолсульфонил]-(1-гидроксикарбамоил-циклобутил)-амино]-пропионовая кислота, 4-[4-(4-хлор-фенокси)бензосульфониламино]тетрагидропиран-4-карбоновой кислоты гидроксиамид, 3-[4-(4-хлор-фенокси)бензолсульфониламино]тетрагидропиран-3-карбоновой кислоты гидроксиамид, (2R,3R)-1-[4-(4-фтор-2-метил-бензилокси)-бензолсульфонил]-3-гидрокси-3-метил-пиперидин-2-карбоновой кислоты гидроксиамид, 3-[[4-(4-фтор-фенокси)бензосульфонил]-(1-гидроксикарбамоил-1-метил-этил)амино]пропионовая кислота, 3-[[4-(4-фтор-фенокси)-бензолсульфонил]-(4-гидроксикарбамоил-тетрагидропиран-4-ил)амино]пропионовая кислота, 3-экзо-3-[4-(4-хлор-фенокси)-бензолсульфониламино]-8-окса-бицикло[3.2.1]октан-3-карбоновой кислоты гидроксиамид, 3-эндо-3-[4-(4-фтор-фенокси)бензолсульфониламино]-8-окса-бицикло[3.2.1]октан-3-карбоновой кислоты гидроксиамид, 3-[4-(4-фтор-фенокси)бензолсульфониламино]тетрагидрофуран-3-карбоновой кислоты гидроксиамид и фармацевтически приемлемые соли, сольваты и гидраты указанных соединений.
Примеры ингибиторов сигнальной трансдукции включают агенты, которые могут ингибировать EGFR (рецептор эпидермального фактора роста) ответы, такие как антитела к EGFR, антитела к EGF и молекулы, которые являются ингибиторами EGFR; ингибиторы VEGF (васкулярный эндотелиальный фактор роста); и ингибиторы рецептора erbВ2, такие как органические молекулы или антитела, которые связываются с рецептором erbВ2, например HERCEPTIN™ (Genentech, Inc. of South San Francisco, California, USA).
Ингибиторы EGFR раскрыты, например, в WO 95/19970 (дата публикации 27 июля 1995), WO 98/14451 (дата публикации 9 апреля 1998), WO 98/02434 (дата публикации 22 января 1998) и патенте США 5747498 (дата выдачи 5 мая 1998), EGFR-ингибирующие агенты включают, без ограничений, моноклональные антитела С225 и anti-EGFR 22Mab (ImClone Systems Incorporated of New York, New York, USA), соединения ZD-1839 (AstraZeneca), BIBX-1382 (Boehringer Ingelheim), MDX-447 (Medarex Inc. of Annandale, New Jersey, USA) и OLX-103 (Merck & Co. of Whitehouse Station, New Jersey, USA), VRCTC-310 (Ventech Research) и токсин слияния EGF (Seragen Inc. ofHopkinton, Massachusetts).
Комбинировать или вводить совместно с композицией можно также ингибиторы VEGF, например SU-5416 и SU-6668 (Sugen Inc. of South San Francisco, California, USA). Ингибиторы VEGF раскрыты, например, в WO 99/24440 (дата публикации 20 мая 1999), международной заявке PCT/IB 99/00797 (дата подачи 3 мая 1999), WO 95/21613 (дата публикации 17 августа 1995), WO 99/61422 (дата публикации 2 декабря 1999), патенте США 5834504 (дата выдачи 10 ноября 1998), WO 98/50356 (дата публикации 12 ноября 1998), патенте США 5883113 (дата выдачи 16 марта 1999), патенте США 5886020 (дата выдачи 23 марта 1999), патенте США 5792783 (дата выдачи 11 августа 1998), WO 99/10349 (дата публикации 4 марта 1999), WO 97/32856 (дата публикации 12 сентября 1997), WO 97/22596 (дата публикации 26 июня 1997), WO 98/54093 (дата публикации 3 декабря 1998), WO 98/02438 (дата публикации 22 января 1998), WO 99/16755 (дата публикации 8 апреля 1999) и WO 98/02437 (дата публикации 22 января 1998), которые все включены в данное описание изобретения во всей их полноте ссылкой. Другими примерами некоторых конкретных ингибиторов VEGF являются IM862 (Cytran Inc. of Kirkland, Washington, USA), анти-VEGF моноклональные антитела бевацизумаб (Genentech, Inc. of South San Francisco, California) и Angiozyme™, синтетический рибозим от Ribozyme (Boulder, Colorado) и Chiron (Emeryville, California),
В комбинации с композицией можно вводить ингибиторы erbВ2-рецептора, такие как GW-2S2974 (Glaxo Wellcome pie), и моноклональные антитела AR-209 (Aronex Pharmaceuticals Inc. of The Woodlands, Texas, USA) и 2B-1 (Chiron). Такие ингибиторы erbB2 включают ингибиторы, описанные в WO 98/02434 (дата публикации 22 января 1998), WO 99/35146 (дата публикации 15 июля 1999), WO 99/35132 (дата публикации 15 июля 1999), WO 98/02437 (дата публикации 22 января 1998), WO 97/13760 (дата публикации 17 апреля 1997), WO 95/19970 (дата публикации 27 июля 1995), патенте США 5537453 (дата выдачи 24 декабря 1996) и патенте США 5877305 (дата выдачи 2 марта 1999), каждый из которых во всей своей полноте включен в данное описание изобретения ссылкой. Ингибиторы erbВ2-рецептора, полезные в настоящем изобретении, также описаны в предварительной заявке на патент США № 60/117341 (дата подачи 27 января 1999) и в предварительной заявке на патент США № 60/117346, дата подачи 27 января 1999, которые обе во всей своей полноте включены в данное описание изобретения ссылкой.
Другие антипролиферативные агенты, которые можно использовать, включают ингибиторы фермента фарнезил-протеинтрансфераза и ингибиторы рецепторной тирозинкиназы PDGFR, в том числе соединения, раскрытые и заявленные в следующих заявках на патент США: 09/221946 (дата подачи 28 декабря 1998), 09/454058 (дата подачи 2 декабря 1999), 09/501163 (дата подачи 9 февряля 2000), 09/539930 (дата подачи 31 марта 2000), 09/202796 (дата подачи 22 мая 1997), 09/384339 (дата подачи 26 августа 1999) и 09/383755 (дата подачи 26 августа 1999), и соединения, раскрытые и заявленные в следующих предварительных заявках на патент США: 60/168207 (дата подачи 30 ноября 1999), 60/170119 (дата подачи 10 декабря 1999), 60/177718 (дата подачи 21 января 2000), 60/168217 (дата подачи 30 ноября 1999) и 60/200834 (дата подачи 1 мая 2000). Каждая из вышеуказанных заявок и предварительных заявок на патент США во всей своей полноте включена в данное описание изобретения ссылкой.
Композиции по изобретению можно также использовать с другими агентами, полезными в лечении аномального клеточного роста или рака, включая, без ограничений, агенты, способные усиливать противоопухолевые иммунные ответы, такие как антитела к CTLA4 (антиген 4 цитотоксических лимфоцитов) и другие агенты, способные блокировать CTLA4, и антипролиферативные агенты, например другие ингибиторы фарнезил-протеинтрансферазы. Конкретные антитела к CTLA4, которые можно использовать в настоящем изобретении, включают антитела, описанные в предварительной заявке на патент США 60/113647 (дата подачи 23 декабря 1998), который во всей его полноте включен в данное описание изобретения ссылкой.
Описания всех процитированных ссылок во всей их полноте включены в данное описание ссылкой на них.
Примеры
Примеры, которые приведены ниже, дополнительно иллюстрируют получение отдельных полиморфных форм по изобретению, т.е. полиморфных Форм I, II, III, IV, V, VI и аморфной формы Соединения I, но не ограничивают объем изобретения, как он определен в данном описании или заявлен ниже. Если не указано иное, все температуры приведены в градусах Цельсия и все части и проценты являются массовыми.
Пример 1: Получение и определение характеристик полиморфной Формы IV (метанольный сольват) Соединения I
Полиморфную Форму IV Соединения I получали по следующей методике. В круглодонную колбу емкостью 500 мл загружали соединение 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-он, представленное формулой 1 (1,65 г, 5,10 ммоль, 1,0 экв.), и метанол (200 мл). Смесь перемешивали до получения прозрачного раствора (приблизительно 10 минут). Добавляли 0,5 М раствор фосфорной кислоты в метаноле (11,0 мл, 5,87 ммоль, 1,15 экв., получен растворением 0,7 г 85% фосфорной кислоты в 11,0 мл метанола). Полученную смесь перемешивали в течение 30 минут при температуре окружающей среды. Полученные твердые вещества отфильтровывали и сушили при 45°С с получением полиморфной Формы IV фосфатной соли 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она (1,43 г).
Фиг.10 представляет собой рентгеновскую порошковую дифрактограмму полиморфной Формы IV Соединения I. Фиг.11 представляет собой ИК-спектр поглощения полиморфной Формы IV. Были также сняты параметры полиморфной Формы IV Соединения I дифференциальной сканирующей калориметрией (Фиг.12).
Пример 2: Получение и определение характеристик полиморфной Формы I (гидрат А) Соединения I
Полиморфную Форму I Соединения I получали по следующей методике. В круглодонную колбу емкостью 50 мл загружали полиморфную Форму IV (метанольный сольват) Соединения I (1,0 г), смешивали с 10 мл воды и перемешивали в течение 18-24 часов при температуре окружающей среды. Полученные твердые вещества отфильтровывали, сушили при 45°С с получением полиморфной Формы 1 Соединения 1 (0,67 г). Продукт анализировали на отсутствие метанола методом ЯМР.
Фиг.1 представляет собой рентгеновскую порошковую дифрактограмму полиморфной Формы I Соединения I. Фиг.2 представляет собой ИК-спектр поглощения полиморфной Формы I. Были также сняты параметры полиморфной Формы I Соединения I дифференциальной сканирующей калориметрией (Фиг.3).
Пример 3: Получение и определение характеристик полиморфной Формы II (безводная форма) Соединения I Форму II получали:
а) нагреванием Формы I при 60°С в течение ночи;
б) выдерживанием Формы I в вакууме при комнатной температуре в течение ночи; или
в) выдерживанием Формы I при 25°С в условиях относительной влажности 0% в течение 5 часов.
Фиг.4 представляет собой рентгеновскую порошковую дифрактограмму полиморфной Формы II Соединения I. Фиг.5 представляет собой ИК-спектр поглощения полиморфной Формы II. Были также сняты параметры полиморфной Формы II Соединения I дифференциальной сканирующей калориметрией (Фиг.6).
Форму II хранят при 2-8°С с влагопоглотителем.
Пример 4: Получение и определение характеристик полиморфной Формы III (гидрат В) Соединения I
Полиморфную Форму III Соединения I получали:
а) подверганием Формы I воздействию условий относительной влажности 90% при 25°С в течение 5 часов;
б) подверганием Формы I воздействию условий относительной влажности 75% при 40°С в течение 1 недели; или
в) подверганием Формы II воздействию условий относительной влажности 75% при 40°С в течение ночи.
Фиг.7 представляет собой рентгеновскую порошковую дифрактограмму полиморфной Формы III Соединения I. Фиг.8 представляет собой ИК-спектр поглощения полиморфной Формы III. Были также сняты параметры полиморфной Формы III Соединения I дифференциальной сканирующей калориметрией (Фиг.9).
Пример 5: Получение и определение характеристик полиморфной Формы V (гидрат С) Соединения 1
Полиморфная Форма V Соединения 1 образовывалась во время проведения исследований стабильности Формы II при хранении при 40°С в условиях относительной влажности 75% в течение периода времени 6 месяцев. Полиморфная Форма V Соединения 1 физически и химически стабильна при комнатной температуре в течение по меньшей мере 3 месяца.
Полиморфная Форма V Соединения 1 имеет растворимость в воде 3,0 мг/мл при рН 5,4.
На Фиг.13 представлена рентгеновская порошковая дифрактограмма полиморфной Формы V Соединения I. Фиг.16 представляет собой ИК-спектр поглощения полиморфной Формы V. ДСК-термограмма для Формы V имеет эндотерму при 199,40°С с двумя пиками десольватации при 57,29°С и 110,73°С соответственно (Фиг.17).
Пример 6: Получение и определение характеристик полиморфной формы VI Соединения I
Полиморфная Форма VI Соединения I может быть получена взятием водной суспензии Формы II и нагреванием ее при 100°С в течение ночи. Как показано на Фиг.14, конверсия началась при 80°С и закончилась после выдержки при 100°С в течение ночи.
Полиморфная Форма VI имеет характеристики, описанные выше. Фиг.18 представляет собой рентгеновскую порошковую дифракторграмму полиморфной Формы VI Соединения I. Фиг, 19 представляет собой ИК-спектр поглощения полиморфной Формы VI Соединения I. Фиг.20 представляет собой кривую дифференциальной сканирующей калориметрии (ДСК) полиморфной Формы VI Соединения I.
Пример 7: Применение полиморфной Формы II (безводная форма) Соединения I для приготовления фармацевтической композиции
А. Полная композиция
Полиморфную Форму II (безводная форма) Соединения I использовали для приготовления лиофилизированного порошка для инъекций, 12 мг/флакон (в виде свободного основания), предназначенного для клинического применения.
Лекарственный продукт сначала готовили в виде препарата в виде раствора Соединения 1 для лиофилизации. Количественный состав раствора Соединения 1 для лиофилизации представлен в Таблице 2.
Раствор Соединения 1 для лиофилизации, 3 мг/мл (в виде свободного основания)
Количественный состав единицы лиофилизированного порошка Соединения I для инъекций представлен в Таблице 3.
Лиофилизированный порошок для инъекций, 12 мг/флакон (в виде свободного основания)
Б. Допустимый избыток
Клиническая композиция лиофилизированного порошка Соединения I для инъекций, 12 мг/флакон (в виде свободного основания), содержит теоретический избыток 0,45 мг/флакон (в виде свободного основания). Этот избыток компенсирует объем твердого вещества во флаконе при разведении 6 мл стерильной воды для инъекций (SWFI) и обеспчивает доставку 2,02 мг/мл (в виде свободного основания) раствора лекарственного средства.
В. Контейнер
Компоненты упаковочной системы для лиофилизированного порошка Соединения I для инъекций, 12 мг/флакон (в виде свободного основания), перечислены ниже:
Г. Опытные фармацевтические средства и обоснование выбора лекарственной формы
Лиофилизированный порошок для инъекций представляет собой традиционную лекарственную форму для введения. Клинический препарат содержит маннит в качестве наполнителя и регулятор тоничности. Разведение этого лекарственного продукта 6 мл SWFI дает прозрачный, гипотонический раствор, 2,02 мг/мл (в виде свободного основания). Разведенный лекарственный продукт следует разводить приемлемым изотоническим стерильным разбавителем для инфузии.
Клинический лекарственный продукт был первоначально разработан для разведения 4 мл SWFI с получением прозрачного изотонического раствора, 3 мг/мл (в виде свободного основания). Во время оценки стабильности лекарственного продукта в полученном растворе наблюдали и исследовали события помутнения/мутности. Помутнение/мутность приписывали кристаллизации лекарственного средства из полиморфа лекарственного вещества (гидрат В). Растворимость в воде полиморфной Формы III (гидрат В) составляет 2,7 мг/мл при рН 5,4 и, следовательно, очень близка к первоначальной целевой концентрации разведения лекарственного продукта (3 мг/мл). Объем SWFI для разведения изменяли с 4 мл до 6 мл для обеспечения полного растворения лекарственного средства. Полученная конечная концентрация полученного раствора лекарственного продукта составляет 2,02 мг/мл (в виде свободного основания), значительно ниже растворимости в воде полиморфной Формы III (гидрат В).
Д. Клиническая производственная композиция, процесс производства. контроль в процессе производства и процесс в заданном порядке
Процесс производства лиофилизированного порошка Соединения 1 для инъекций, 12 мг/флакон (в виде свободного основания), суммирован ниже. Текущий размер клинической партии составляет 9,3 л на производственный цикл. Производственная композиция такая же, как и клиническая композиция (см. Таблицу 2 и Таблицу 3),
а) Добавить приблизительно 75% общего количества воды для инъекций (WFI) в емкость для компаундирования.
б) Добавить и полностью растворить требуемое количество маннита в WFI при перемешивании.
в) Нагреть раствор WFI/маннит до приблизительно 58°С, добавить требуемое количество лекарственного вещества, представляющего собой Соединение I, и смешивать до полного растворения.
г) Довести раствор до конечного объема по массе водой для инъекций, смешивать в течение 10 минут и охладить раствор до комнатной температуры.
д) Отобрать аликвоты для тестирования для контроля в процессе производства (т.е. внешний вид, рН, плотность и УФ-анализ).
е) Стерильно фильтровать основной объем раствора для лиофилизации через мембранные фильтры 0,45 мкм и 0,22 мкм и заполнить по 4,15 мл (в том числе переполнение 0,15 мл) во флаконы типа I из бутылочного стекла, 10 мл/20 мм, в асептических условиях.
ж) Лиофилизировать заполненные флаконы с не до конца вставленными пробками.
з) В конце цикла лиофилизации заполнить азотом и закупорить флаконы под легким вакуумом при комнатной температуре.
и) Загерметизировать лиофилизированные флаконы алюминиевыми уплотняющими крышками.
к) Поместить флаконы в охлаждаемый резервуар для хранения.
Пример 8: Получение и определение характеристик аморфной формы Соединения I
Аморфная Форма Соединения I была получена растворением полиморфной Формы II (безводная форма) Соединения I в стерильной воде для инъекций в концентрации 4,46 мг/мл. 2 мл этого раствора заполняли в 10 мл чистый флакон типа 1 и лиофилизировали в FTS LyoStar Lyophilizer (S/N LSACC3). Ниже описан цикл лиофилизации.
Продукт замораживали до -50°С и подвергали вакуумной сушке последовательно при -30°С, -20°С и -15°С каждый раз в течение 12 ч до окончания стадии первичной сушки. Поддерживали вакуум 200 мторр (26,66 Па). Продукт затем сушили при 25°С и при вакууме 200 мторр (26,66 Па) в течение 24 ч до окончания стадии вторичной сушки.
Аморфная Форма Соединения I была получена в виде белого/желтоватого лиофилизированного кека. Аморфная Форма Соединения I может быть разведена 2 мл стерильной воды для инъекций с получением прозрачного желтого раствора.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЛИ И ПОЛИМОРФЫ 8-ФТОР-2-{4-[(МЕТИЛАМИНО)МЕТИЛ]ФЕНИЛ}-1,3,4,5-ТЕТРАГИДРО-6Н-АЗЕПИНО[5,4,3-cd]ИНДОЛ-6-ОНА | 2011 |
|
RU2570198C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИНГИБИТОРОВ ПОЛИ(АДФ-РИБОЗА)ПОЛИМЕРАЗ | 2005 |
|
RU2344138C2 |
| ТАБЛЕТКИ, СОДЕРЖАЩИЕ БОЛЬШУЮ ДОЗУ РУКАПАРИБА | 2015 |
|
RU2705156C2 |
| ТЕРАПЕВТИЧЕСКИЕ КОМБИНАЦИИ, СОДЕРЖАЩИЕ ИНГИБИТОР ПОЛИ(АДФ-РИБОЗА)ПОЛИМЕРАЗЫ | 2005 |
|
RU2361592C2 |
| 6-ОКСО-АЗЕПИНОИНДОЛОВЫЕ СОЕДИНЕНИЯ И ИХ ФИЗИОЛОГИЧЕСКИ ПЕРЕНОСИМЫЕ КИСЛОТНЫЕ СОЛИ ПРИСОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2078765C1 |
| ПОЛИМОРФНЫЕ И АМОРФНЫЕ ФОРМЫ {2-ФТОР-5-[3-((Е)-2-ПИРИДИН-2-ИЛВИНИЛ)-1Н-ИНДАЗОЛ-6-ИЛАМИНО]ФЕНИЛ}АМИДА 2,5-ДИМЕТИЛ-2Н-ПИРАЗОЛ-3-КАРБОНОВОЙ КИСЛОТЫ | 2005 |
|
RU2324692C1 |
| ПРОИЗВОДНЫЕ ТЕТРАГИДРОПИРИДО[3,4-b]ИНДОЛА, ПОЛЕЗНЫЕ ПРИ ЛЕЧЕНИИ РАКА | 2014 |
|
RU2664109C2 |
| ТВЕРДЫЕ ФОРМЫ (1,1-ДИОКСО-4-ТИОМОРФОЛИНИЛ)-[6-[[3-(4-ФТОРФЕНИЛ)-5-МЕТИЛ-4-ИЗОКСАЗОЛИЛ]МЕТОКСИ]-3-ПИРИДИНИЛ]-МЕТАНОНА | 2012 |
|
RU2618524C2 |
| НЕГИГРОСКОПИЧЕСКАЯ КРИСТАЛЛИЧЕСКАЯ МАЛЕАТНАЯ СОЛЬ 5-[(Z)-(5-ФТОР-2-ОКСО-1,2-ДИГИДРО-3H-ИНДОЛ-3-ИЛИДЕН)МЕТИЛ]-N-[(2S)-2-ГИДРОКСИ-3-МОРФОЛИН-4-ИЛПРОПИЛ]-2,4-ДИМЕТИЛ-1H-ПИРРОЛ-3-КАРБОКСАМИДА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ РАКА | 2004 |
|
RU2319702C2 |
| ПОЛИМОРФЫ С-MET/HGFR ИНГИБИТОРА | 2006 |
|
RU2387650C2 |
Настоящее изобретение относится к новым полиморфным и аморфной формам фосфатной соли 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она формулы (I) и к фармацевтической композиции на их основе, обладающей активностью в качестве модулятора активности поли(аденозин-5-дифосфат(АВР)-рибоза)полимеразы.
Технический результат - получение новых полиморфных и аморфной форм фосфатной соли соединения формулы (I) и фармацевтической композиции на их основе в целях лечения болезненного состояния млекопитающих, опосредованного активностью поли(ADP-рибоза)полимеразы, включая такое болезненное состояние, как рак. 8 н.п. ф-лы, 3 табл., 24 ил.
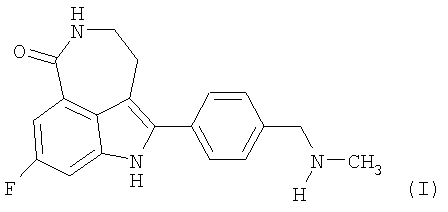
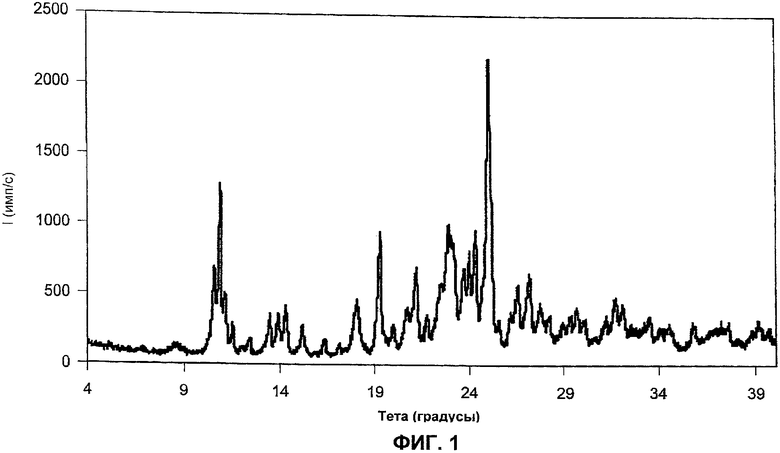
1. Кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, представляющая собой полиморф формы I, имеющая картину дифракции рентгеновских лучей на порошке, содержащую пики при углах дифракции (2θ) 10.9, 19.3, 22.9 и 25.0.
2. Кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, представляющая собой полиморф формы II, имеющая картину дифракции рентгеновских лучей на порошке, содержащую пики при углах дифракции (2θ) 11.2, 14.0, 20.1 и 23.1.
3. Кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, представляющая собой полиморф формы III, имеющая картину дифракции рентгеновских лучей на порошке, содержащую пики при углах дифракции (2θ) 10.7,11.0,19.4 и 25.1.
4. Кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, представляющая собой полиморф формы V, имеющая картину дифракции рентгеновских лучей на порошке, содержащую пики при углах дифракции (2θ) 10.8,14.8, 21.6 и 25.8.
5. Кристаллическая фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, представляющая собой полиморф формы VI, имеющая картину дифракции рентгеновских лучей на порошке, содержащую пики при углах дифракции (2θ) 14.8, 20.0, 22.3 и 23.5.
6. Фосфатная соль 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd|индол-6-она, представляющая собой по существу чистую аморфную форму, имеющая картину дифракции рентгеновских лучей на порошке, демонстрирующую широкий пик при углах дифракции (2θ) в пределах от 4 до 40° без каких-либо характерных острых пиков кристаллической формы.
7. Твердая форма фосфатной соли 8-фтор-2-{4-[(метиламино)метил]фенил}-1,3,4,5-тетрагидро-6Н-азепино[5,4,3-cd]индол-6-она, которая содержит по меньшей мере две из следующих форм: полиморфные форму I, форму II, форму III, форму IV, имеющую картину дифракции рентгеновских лучей на порошке, содержащую пики при углах дифракции (2θ) 8.2, 16.5, 23.0 и 24.8, форму V, форму VI или аморфную форму по любому из пп.1-5 или 6.
8. Фармацевтическая композиция, содержащая соль по любому из пп.1-5 или 6-7, обладающая активностью в качестве модулятора активности поли(аденозин-5'-дифосфат (ADP)-рибоза)полимеразы.
| Шлифовальная головка | 1976 |
|
SU649554A1 |
| Способ получения тетрагидроимидазо-(1,4)-бензодиазепин-12-онов, или их солей присоединения фармацевтически приемлемых кислот, или их стереохимически изомерных форм | 1989 |
|
SU1748647A3 |
| RU 93004873 A, 20.08.1995. | |||
Авторы
Даты
2009-05-20—Публикация
2005-09-12—Подача