Область изобретения
Настоящее изобретение относится к полиморфным и аморфным формам {2-фтор-5-[3-((Е)-2-пиридин-2-илвинил)-1Н-индазол-6-иламино]фенил}амида 2,5-диметил-2Н-пиразол-3-карбоновой кислоты и к терапевтическому или профилактическому использованию таких соединений и фармацевтическим композициям, изготовленных с ними, для лечения рака и других болезненных состояний, связанных с нежелательным ангиогенезом и/или клеточной пролиферацией.
Предпосылки создания изобретения
Патент США № 6531491, который включен сюда в виде ссылки во всей полноте, относится к индазольным соединениям, которые модулируют и/или ингибируют активность некоторых протеинкиназ. Такие соединения пригодны для лечения рака и других заболеваний, связанных с ангиогенезом или клеточной пролиферацией, опосредуемой протеинкиназами. Одним из соединений, описанных в патенте США № 6531491, является {2-фтор-5-[3-((Е)-2-пиридин-2-илвинил)-1Н-индазол-6-иламино]фенил]амид 2,5-диметил-2Н-пиразол-3-карбоновой кислоты, структура которого показана ниже в качестве формулы I:
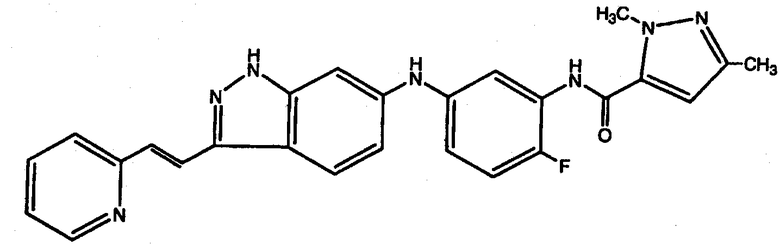
Формула I
Другим названием соединения формулы I является 6-[N-(3-((1,3-диметил-1Н-пиразол-5-ил)карбоксамидо)-4-фторфенил)амино]-3-Е-[2-(пиридин-2-ил)этенил]-1Н-индазол.
Чтобы получить фармацевтические композиции, содержащие соединение формулы I для введения млекопитающим в соответствии с требованиями регистрационных органов здравоохранения международных и США (например, FDA's Good Manufacturing Practices ("GMP")), необходимо получить соединение формулы I в стабильной форме, такой как устойчивая кристаллическая форма, обладающая постоянными физическими свойствами. Кроме того, в данной области технологии существует потребность в получении улучшенных форм соединения формулы I, обладающих улучшенными свойствами, такими как улучшенная растворимость или биодоступность при пероральном приеме.
Краткое изложение изобретения
В одном из аспектов данное изобретение представляет четырнадцать полиморфных форм и одну аморфную форму соединения формулы I. В одном из воплощений данное изобретение представляет, по существу, чистый полиморф соединения, представленного формулой I, где полиморф обозначается как форма I и имеет порошковую рентгенограмму (PXRD), содержащую пики при дифракционных углах (2Θ), равные 5,5 и 28,4. Более конкретно форма полиморфа I имеет PXRD, содержащую пики при углах дифракции (2Θ), равные 5,5; 9,5; 10,7 и 28,4. Еще конкретнее форма полиморфа I имеет PXRD, содержащую пики при углах дифракции (2Θ), по существу, такие, как представлено на фигуре 1А. Еще боле конкретно, форма полиморфа I характеризуется спектром комбинационного рассеяния, по существу, таким же, как показано на фигуре 1С.
В другом воплощении данное изобретение представляет, по существу, чистый полиморф соединения, представленного формулой I, причем данный полиморф обозначается как форма II и имеет PXRD, содержащую пики при углах дифракции (2Θ), равные 12,1 и 16,7. Конкретнее форма II полиморфа имеет PXRD, содержащую пики при углах дифракции (2Θ) 5,5; 9,5; 10,7 и 28,4. Еще конкретнее форма II полиморфа имеет PXRD, содержащую пики при углах дифракции (2Θ), по существу, такую же, как показано на фигуре 2А. И еще конкретнее форма полиморфа II характеризуется спектром комбинационного рассеяния, по существу, таким же, как показано на фигуре 2С.
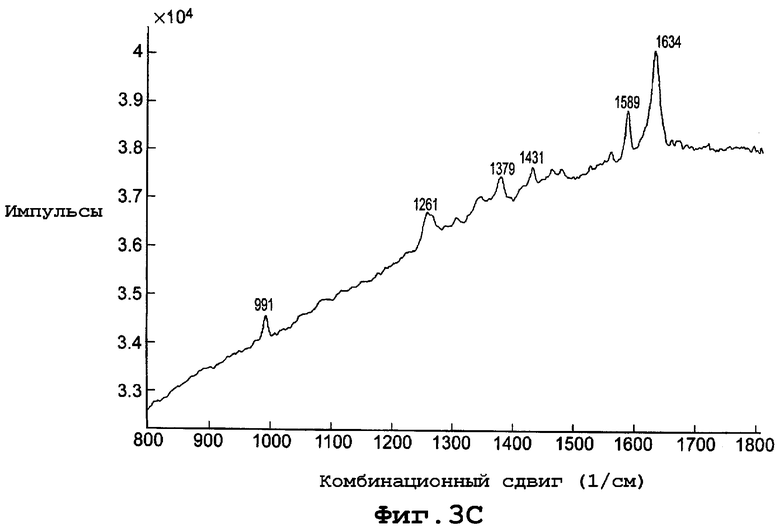
В еще одном воплощении данное изобретение представляет, по существу, чистый полиморф соединения, представленного формулой I, причем полиморф назван формой III и имеет PXRD, содержащую пики при углах дифракции (2Θ), равные 6,4 и 23,4. Конкретнее форма полиморфа III имеет PXRD, содержащую пики при углах дифракции (2Θ), равных 6,4; 23,4; 25,0 и 27,3. Еще конкретнее форма III полиморфа имеет PXRD, содержащую пики при углах дифракции (2Θ), по существу, такую же, как показано на фигуре 3А. И еще конкретнее полиморф формы III характеризуется спектром комбинационного рассеяния, по существу, таким же, как представленно на фигуре 3С.
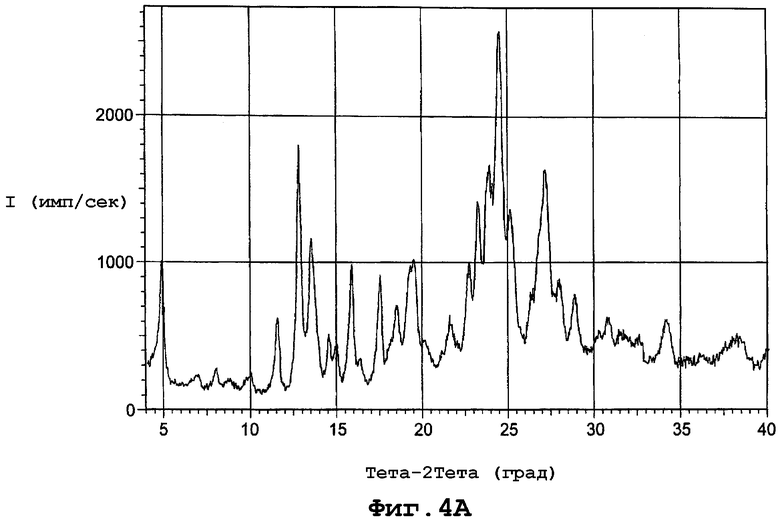
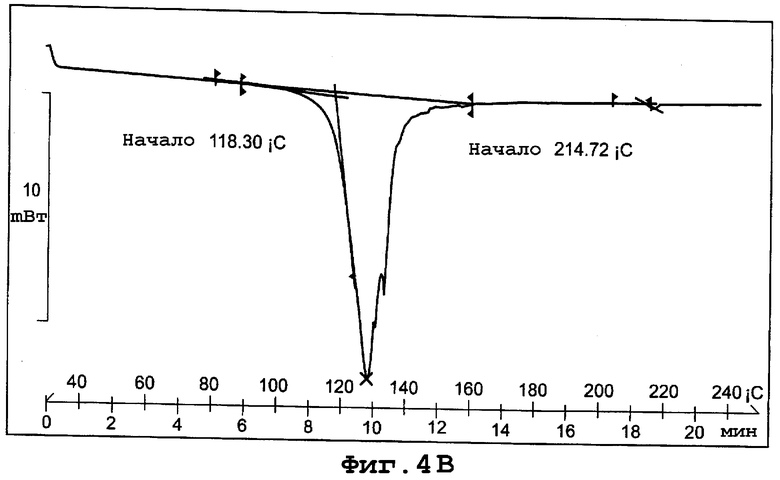
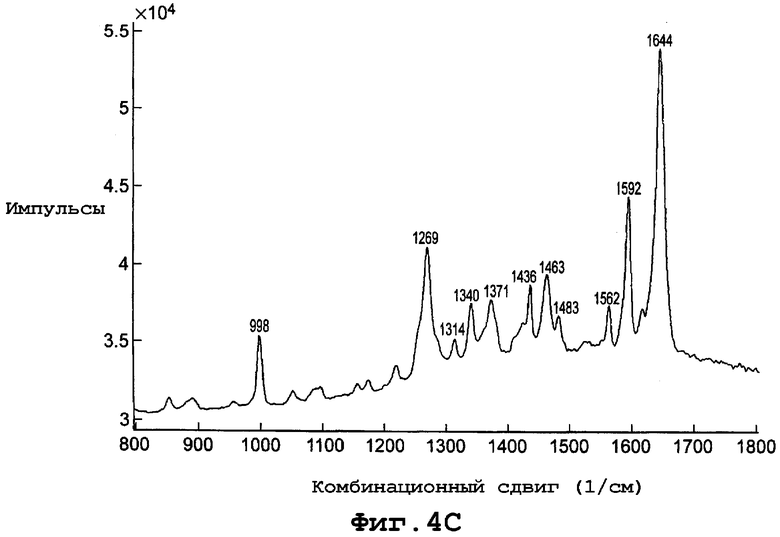
В еще одном воплощении данное изобретение представляет, по существу, чистый полиморф соединения, представленного формулой I, причем полиморф назван формой IV и имеет PXRD, содержащую пики при углах дифракции (2Θ), равные 24,5 и 34,1. Конкретнее форма полиморфа IV имеет PXRD, содержащую пики при углах дифракции (2Θ), равных 12,8; 15,8; 24,5 и 34,1. Еще более конкретно полиморф формы IV имеет PXRD, содержащую пики при углах дифракции (2Θ), по существу, такие, как представлено на фиг. 4А. Еще конкретнее полиморф формы IV характеризуется спектром комбинационного рассеяния, по существу, таким же, как представлено на фигуре 4С. И еще конкретнее полиморф формы IV можно охарактеризовать началом эндотермы плавления кристаллов при примерно 118°С при скорости сканирования 10°С в минуту. И еще конкретнее форма IV полиморфа имеет термограмму DSC, по существу, такую, как представлено на фигуре 4В.
В еще одном воплощении данное изобретение представляет, по существу, чистый полиморф соединения, представленного формулой I, причем данный полиморф обозначен как форма V и имеет PXRD, содержащую пики при углах дифракции (2Θ), равные 8,4 и 26,0. Конкретнее форма полиморфа V имеет PXRD, содержащую пики при углах дифракции (2Θ), равных 8,4; 14,2; 22,2; 26,0. Еще более конкретно полиморф формы V имеет PXRD, содержащую пики при углах дифракции (2Θ), по существу, такие же, как и представленные на фигуре 5А. И еще конкретнее полиморф формы V характеризуется спектром комбинационного рассеяния, по существу, таким же, как представлено на фигуре 5С.
В еще одном воплощении данное изобретение представляет, по существу, чистый полиморф соединения, представленного формулой I, причем данный полиморф обозначен как форма Ia и имеет PXRD, содержащую пики при углах дифракции (2Θ), равные 5,5 и 25,2. Конкретнее форма полиморфа Ia имеет PXRD, содержащую пики при углах дифракции (2Θ), равных 5,5; 10,6; 18,9; 25,2. И еще конкретнее полиморф формы Ia имеет PXRD, содержащую пики при углах дифракции (2Θ), по существу, такие же, как представлено на фигуре 6А.
В еще одном воплощении данное изобретение представляет, по существу, чистый полиморф соединения, представленного формулой I, причем данный полиморф обозначен как форма Ib и имеет PXRD, содержащую пики при углах дифракции (2Θ), равные 10,2 и 13,8. Конкретнее форма полиморфа Ib имеет PXRD, содержащую пики при углах дифракции (2Θ), равных 10,2; 13,8; 20,1; 26,2. Еще конкретнее полиморф формы Ib имеет PXRD, содержащую пики при углах дифракции (2Θ), по существу, такие же, как и представленные на фигуре 7А. И еще конкретнее полиморф формы Ib характеризуется спектром комбинационного рассеяния, по существу, таким же, как и представленный на фигуре 7С.
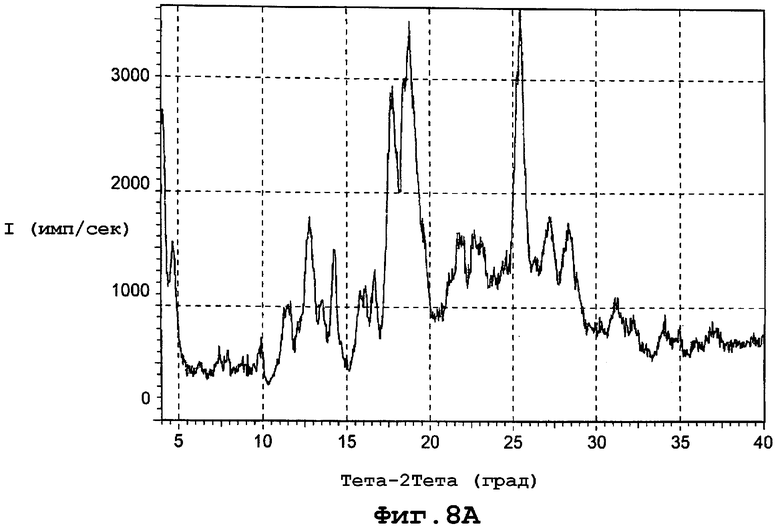
В еще одном воплощении данное изобретение представляет, по существу, чистый полиморф соединения, представленного формулой I, причем данный полиморф обозначен как форма IIa и имеет PXRD, содержащую пики при углах дифракции (2Θ), равные 12,8 и 22,9. Конкретнее форма полиморфа IIa имеет PXRD, содержащую пики при углах дифракции (2Θ), равных 12,8; 16,0; 22,9; 31,2. И еще конкретнее полиморф формы IIa имеет PXRD, содержащую пики при углах дифракции (2Θ), по существу, такие же, как и представленные на фигуре 8А.
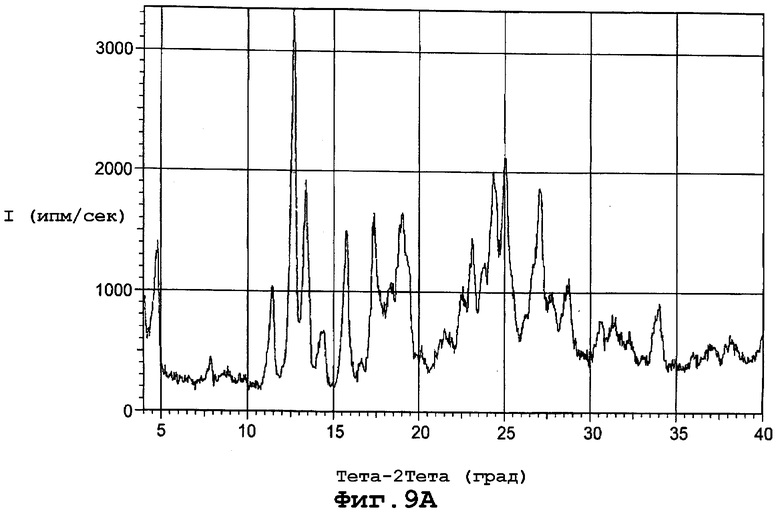
В еще одном воплощении данное изобретение представляет, по существу, чистый полиморф соединения, представленного формулой I, причем данный полиморф обозначен как форма IIb и имеет PXRD, содержащую пики при углах дифракции (2Θ), равные 14,3 и 19,0. Конкретнее форма полиморфа IIb имеет PXRD, содержащую пики при углах дифракции (2Θ), равных 7,9; 14,3; 19,0; 27,0. Еще более конкретно полиморф формы IIb имеет PXRD, содержащую пики при углах дифракции (2Θ), по существу, такие же, как и представленные на фигуре 9А. И еще конкретнее полиморф формы IIb характеризуется спектром комбинационного рассеяния, по существу, таким же, как представленный на фигуре 9С.
В другом воплощении данное изобретение представляет, по существу, чистый полиморф соединения, представленного формулой I, причем данный полиморф обозначен как форма IIIa и имеет PXRD, содержащую пики при углах дифракции (2Θ), равные 24,9 и 36,2. Конкретнее форма полиморфа IIIa имеет PXRD, содержащую пики при углах дифракции (2Θ), равных 14,7; 21,0; 24,9 и 36,2. И еще конкретнее полиморф формы IIIa имеет PXRD, содержащую пики при углах дифракции (2Θ) по существу такие же, как и представленные на фигуре 10А.
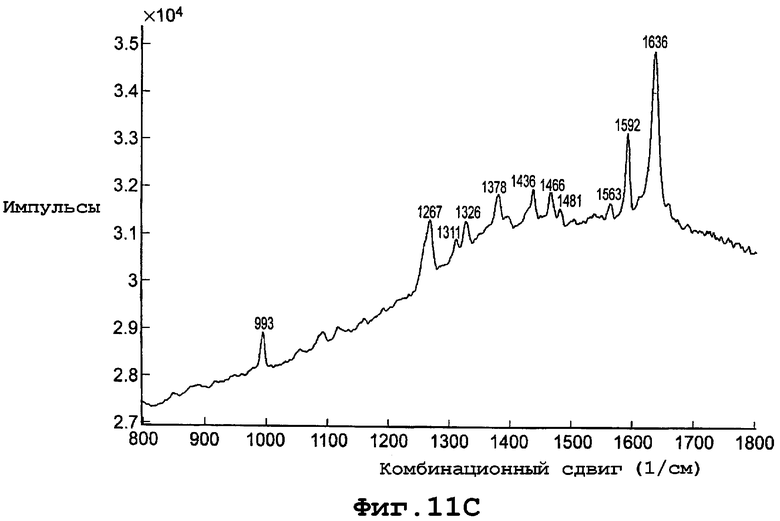
В другом воплощении данное изобретение представляет, по существу, чистый полиморф соединения, представленного формулой I, причем данный полиморф обозначен как форма IIIb и имеет PXRD, содержащую пики при углах дифракции (2Θ), равные 6,8 и 14,5. Конкретнее форма полиморфа IIIb имеет PXRD, содержащую пики при углах дифракции (2Θ), равных 6,8; 14,5; 20,8; 24,8. Еще более конкретно полиморф формы IIIb имеет PXRD, содержащую пики при углах дифракции (2Θ) по существу такие же, как и представленные на фигуре 11А. И еще конкретнее полиморф формы IIIb характеризуется спектром комбинационного рассеяния, по существу таким же, как представленный на фигуре 11С.
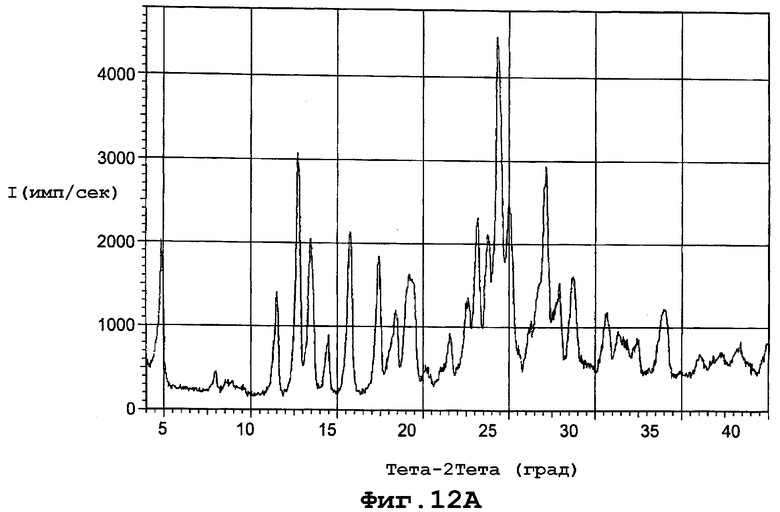
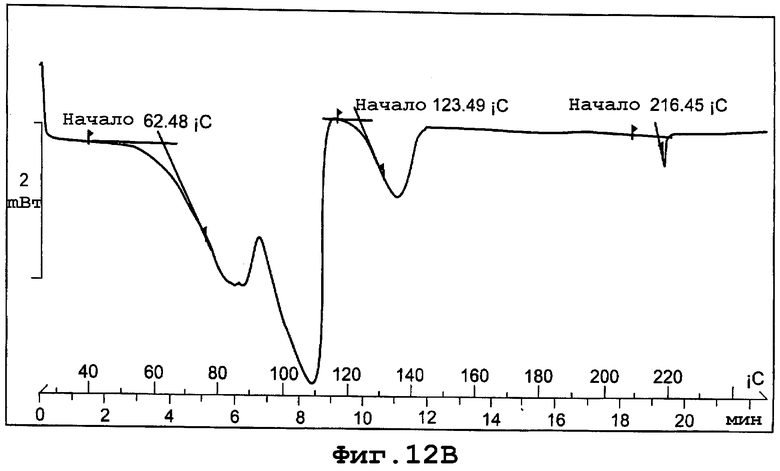
В еще одном воплощении данное изобретение представляет, по существу, чистый полиморф соединения, представленного формулой I, причем полиморф назван формой IVa и имеет PXRD, содержащую пики при углах дифракции (2Θ), равные 13,5 и 32,5. Конкретнее форма полиморфа IVa имеет PXRD, содержащую пики при углах дифракции (2Θ), равных 13,5; 15,8; 27,0 и 32,5. Еще более конкретно полиморф формы IVa имеет PXRD, содержащую пики при углах дифракции (2Θ), по существу, такие же, как и представленные на фиг. 12А. И еще конкретнее полиморф формы IVa имеет начало эндотермы дегидратации при примерно 63°С и начало эндотермы плавления кристаллов при примерно 123°С при скорости сканирования 10°С в минуту. И кроме того, форма IVa полиморфа имеет термограмму DSC, по существу, такую же, как и представленную на фигуре 12В.
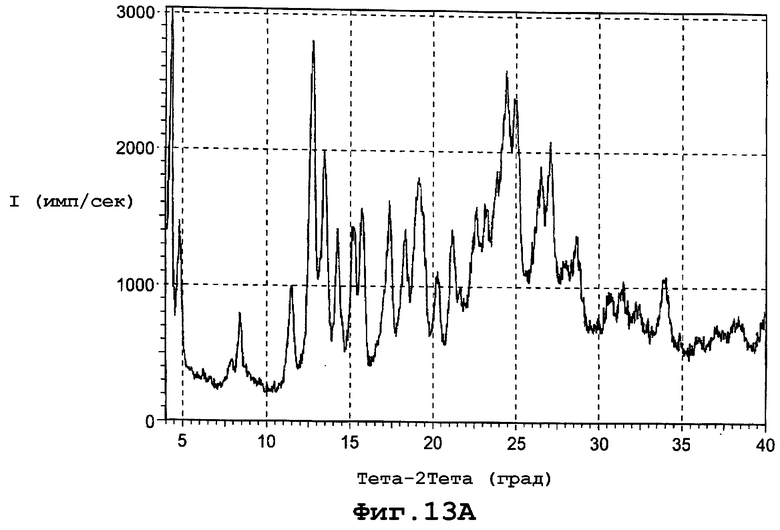
В еще одном воплощении данное изобретение представляет, по существу, чистый полиморф соединения, представленного формулой I, причем данный полиморф обозначен как форма Va и имеет PXRD, содержащую пики при углах дифракции (2Θ), равные 19,2 и 33,9. Конкретнее форма полиморфа Va имеет PXRD, содержащую пики при углах дифракции (2Θ), равных 11,5; 19,2; 24,4; 33,9. Еще более конкретно полиморф формы Va имеет PXRD, содержащую пики при углах дифракции (2Θ), по существу, такие же, как и представленные на фигуре 13А. И еще конкретнее полиморф формы Va характеризуется спектром комбинационного рассеяния, по существу таким же, как и представленный на фигуре 13С.
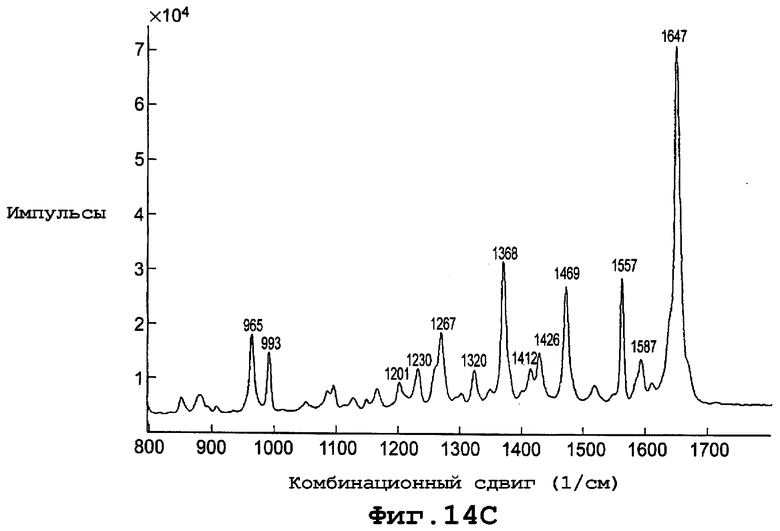
В другом воплощении данное изобретение представляет, по существу, чистый полиморф соединения, представленного формулой I, причем данный полиморф обозначен как форма VI и имеет PXRD, содержащую пики при углах дифракции (2Θ), равные 7,7 и 26,8. Конкретнее форма полиморфа VI имеет PXRD, содержащую пики при углах дифракции (2Θ), равных 7,7; 12,9; 18,5; 26,8. Еще конкретнее полиморф формы VI имеет PXRD, содержащую пики при углах дифракции (2Θ) по существу, такие же, как и представленные на фигуре 14А. И еще конкретнее, полиморф формы VI характеризуется спектром комбинационного рассеяния, по существу таким же, как представленный на фигуре 14С.
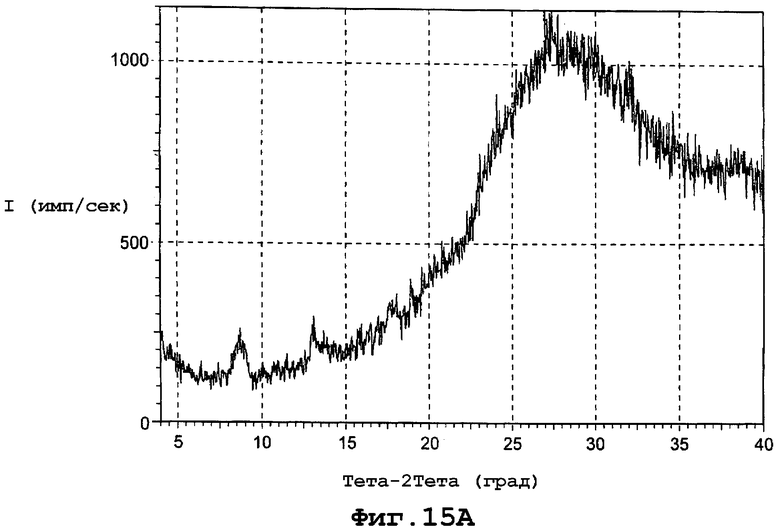
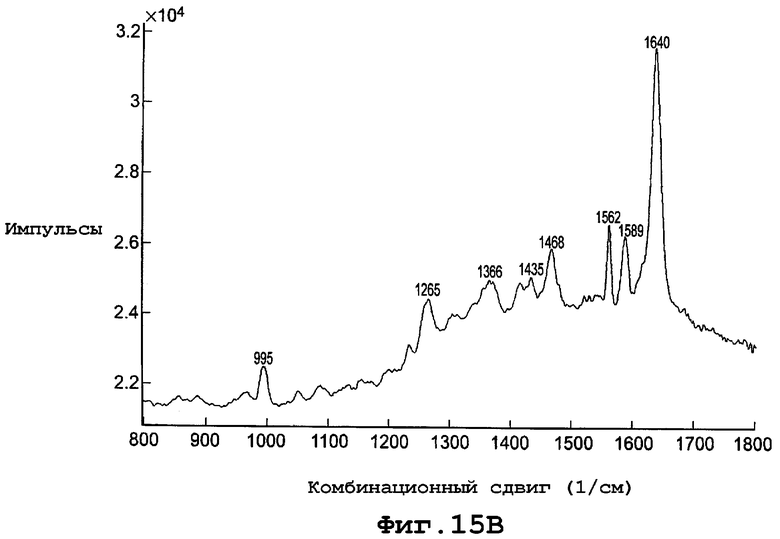
В другом воплощении данное изобретение представляет, по существу, чистый полиморф соединения, представленного формулой I, причем данный полиморф имеет PXRD, представляющую широкий пик при углах дифракции (2Θ) в интервале 4 - 40°С без каких-либо острых пиков, характерных для кристаллической формы. Конкретнее аморфная форма характеризуется тем, что имеет PXRD, по существу, такую же, как и представленное на фигуре 15А. И еще конкретнее аморфная форма характеризуется спектром комбинационного рассеяния, включающим сдвиги пиков (см-1), по существу, такие же, как представленные на фигуре 15В.
В еще одном воплощении данное изобретение представляет твердую форму соединения, представляемого формулой I, причем данная твердая форма является смесью, состоящей из, по меньшей мере, двух из следующих твердых форм: полиморф форм I, II, III, IV, V, Ia, Ib, IIa, IIb, IIIa, IIIb, IVa, Va, VI и аморфной формы.
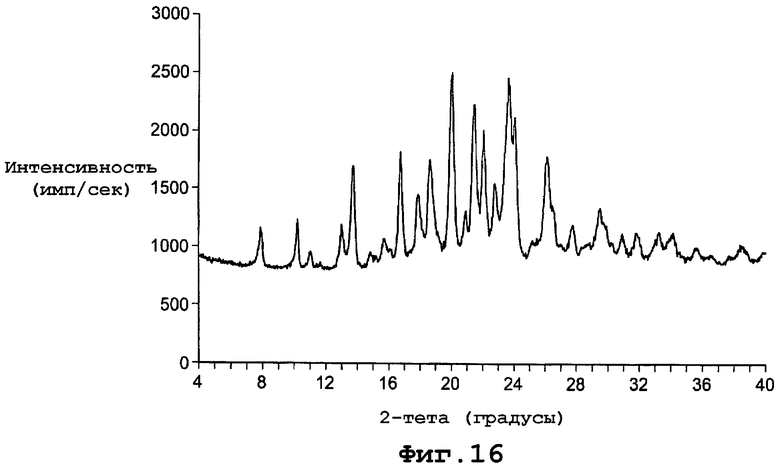
В другом воплощении данное изобретение представляет, по существу, чистый полиморф соединения, представленного формулой I, причем полиморф обозначен как форма Ibm-2, которая является смесью форм Ib и VI и имеет PXRD, содержащую пики при углах дифракции (2Θ), равные 12,9 и 13,8. Конкретнее форма полиморфа Ibm-2 имеет PXRD, содержащую пики при углах дифракции (2Θ), равные 12,9; 13,8; 20,1; 26,8. Еще конкретнее полиморф формы Ibm-2 имеет PXRD, содержащую пики при углах дифракции (2Θ) по существу, такие же, как и представленные на фигуре 16.
В еще одном аспекте данное изобретение относится к фармацевтическим композициям, каждая из которых содержит кристаллическую или аморфную форму соединения формулы I. Данное изобретение относится также к фармацевтической композиции, содержащей смесь, по меньшей мере, двух из любых форм полиморфа и аморфных форм.
В дополнительном аспекте данное изобретение представляет способы лечения рака, а также других болезненных состояний, связанных с нежелательным ангиогенезом и/или клеточной пролиферацией, включающие введение терапевтически эффективного количества полиморфа/аморфного соединения данного изобретения пациенту, нуждающемуся в таком лечении. Данное изобретение относится также к способу модуляции и/или ингибирования киназной активности VEGF-R (рецепторов фактора роста эндотелиальных клеток сосудов), FGF-R (рецепторов фактора роста фибробластов), комплекса CDK (циклинозависимой киназы), СНК1, LCK (известной так же, как лимфоцитоспецифическая тирозинкиназа), ТЕК (известной так же, как Tie-2), FAK (киназы фокальной адгезии) и/или фосфорилазкиназы путем введения соединения данного изобретения. Предпочтительные соединения данного изобретения обладают селективной киназной активностью, т.е. они обладают значительной активностью против одной или более из специфических киназ, в то же время обладая меньшей или минимальной активностью против одной или более из других киназ. В одном из предпочтительных воплощений данного изобретения полиморф/аморфные соединения данного изобретения представляют собой соединения, которые обладают, по существу, более высокой активностью против тирозинкиназы рецепторов VEGF-R, чем против тирозинкиназы FGF-R1 рецепторов. Данное изобретение относится также к способам модуляции активности тирозинкиназы рецепторов VEGF без значительной модуляции тирозинкиназной активности рецепторов FGF.
Соединения данного изобретения можно использовать преимущественно в комбинации с другими известными терапевтическими средствами. Например, полиморф/аморфные формы соединения формулы I, которые обладают противоангиогенной активностью, можно совместно вводить с цитотоксическими химиотерапевтическими средствами, такими как таксол, таксотере, винбластин, цис-платин, доксорубицин, адриамицин и тому подобное, для получения усиленного противоопухолевого действия. Аддитивное или синергидное повышение терапевтического эффекта может быть также получено совместным применением соединения данного изобретения, которое обладает противоангиогенной активностью с другими противоангиогенными средствами, такими как комбретастатин А-4, эндостатин, приномастат, целекоксиб, рофококсиб, ЕМD121974, IМ862, противо-VEGF моноклональные антитела и противо-KDR моноклональные антитела.
Краткое описание фигур
Описав таким образом данное изобретение в общих чертах, теперь обратимся к сопровождающим фигурам, где:
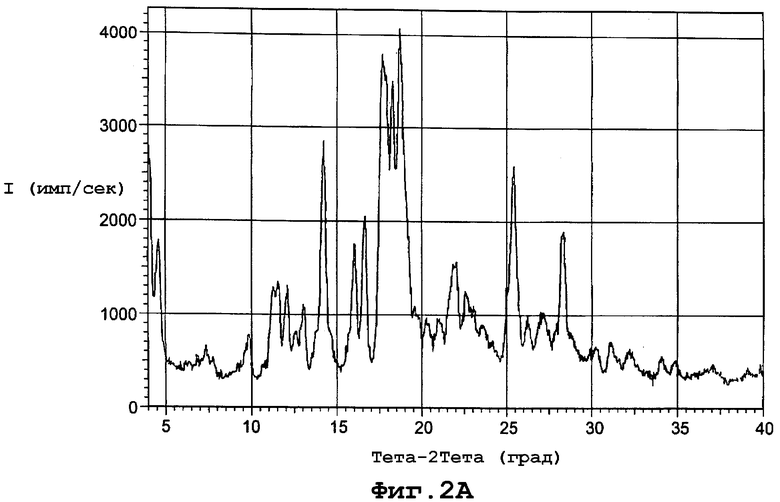
фиг. 1А является диаграммой порошковой рентгенограммы формы I полиморфа данного изобретения;
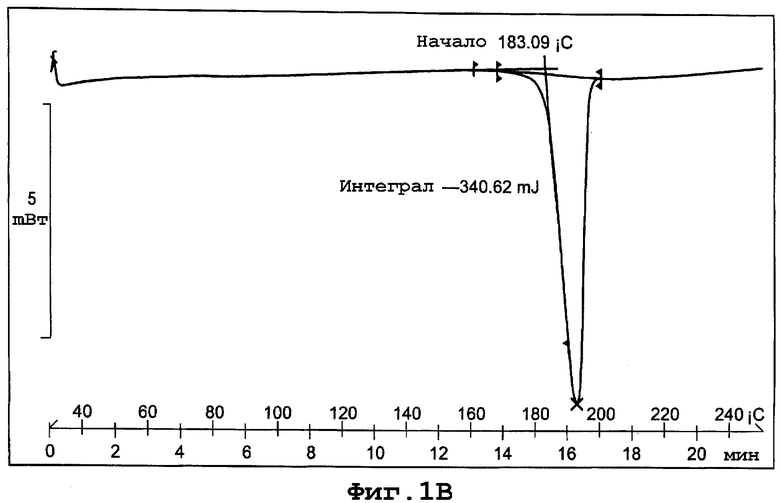
фиг. 1В является термограммой дифференциальной сканирующей калориметрии (DSC) формы I полиморфа данного изобретения;
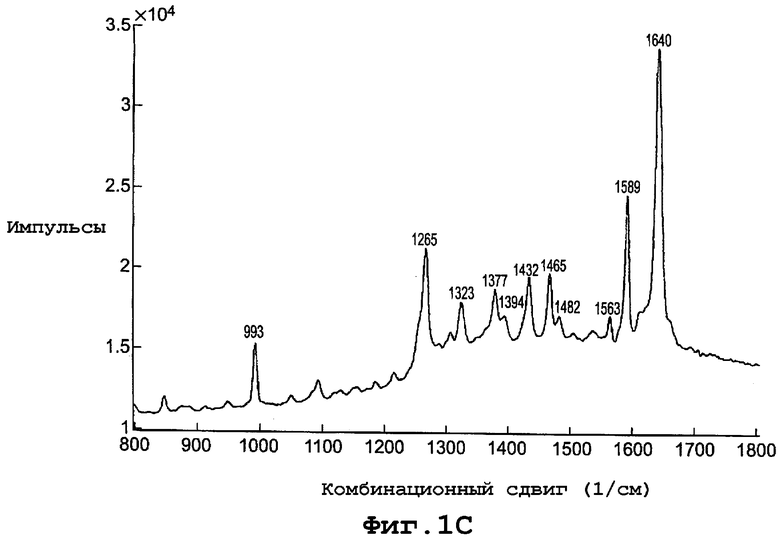
фиг. 1С является диаграммой спектрального комбинационного рассеяния формы I полиморфа данного изобретения;
фиг. 2А является диаграммой порошковой рентгенограммы формы II полиморфа данного изобретения;
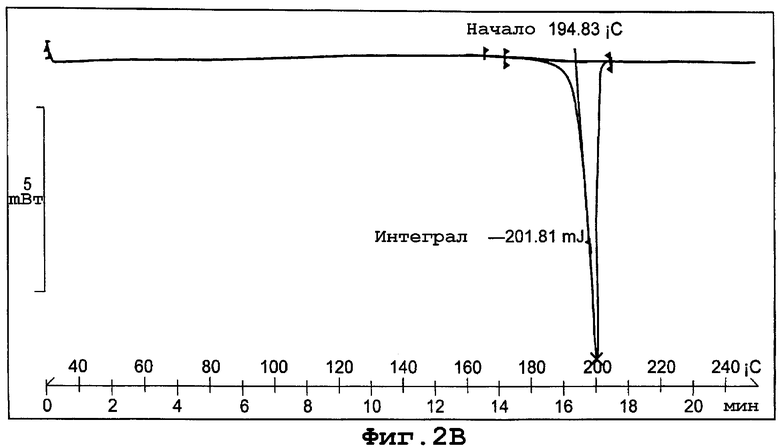
фиг. 2В является термограммой DSC формы II полиморфа данного изобретения;
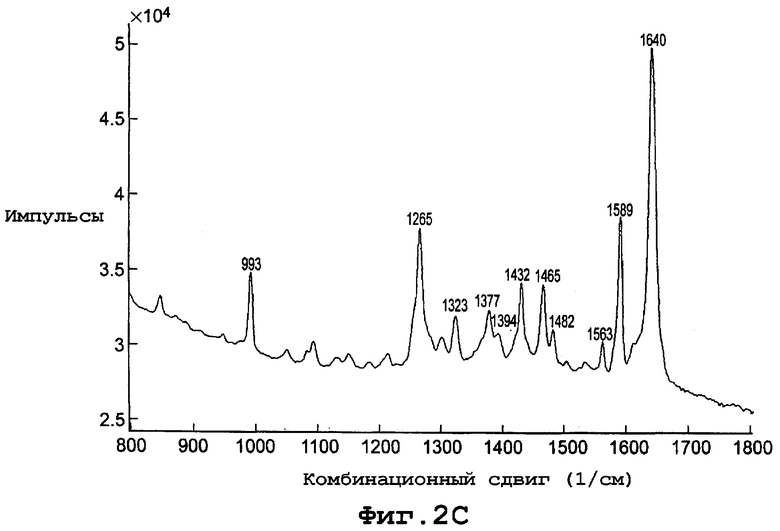
фиг. 2С является диаграммой спектрального комбинационного рассеяния формы II полиморфа данного изобретения;
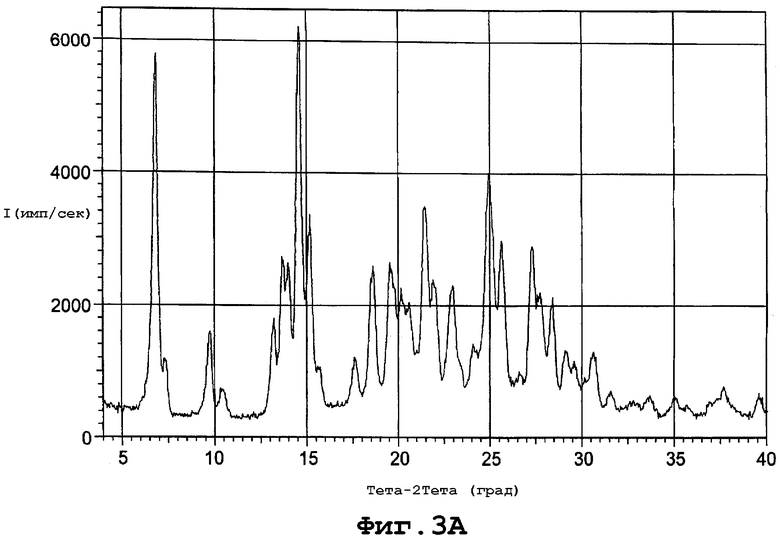
Фиг. 3А является диаграммой порошковой рентгенограммы формы III полиморфа данного изобретения;
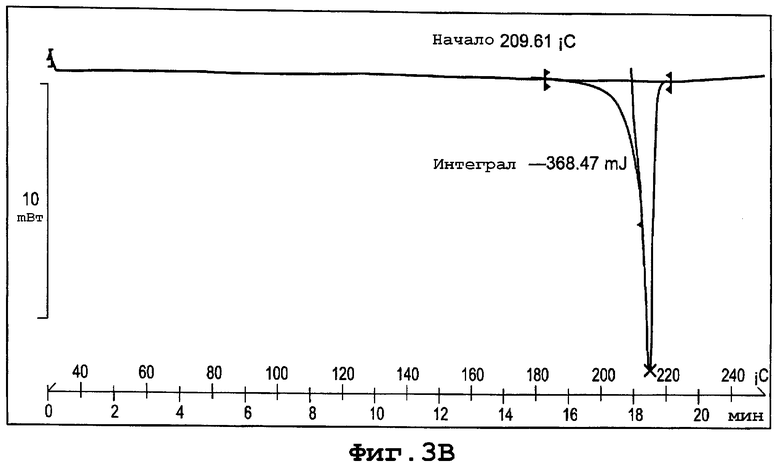
фиг. 3В является термограммой DSC формы III полиморфа данного изобретения;
фиг. 3С является диаграммой спектрального комбинированного рассеяния формы III полиморфа данного изобретения;
фиг. 4А является диаграммой порошковой рентгенограммы формы IV полиморфа данного изобретения;
фиг. 4В является термограммой DSC формы IV полиморфа данного изобретения;
фиг. 4С является диаграммой спектрального комбинированного рассеяния формы IV полиморфа данного изобретения;
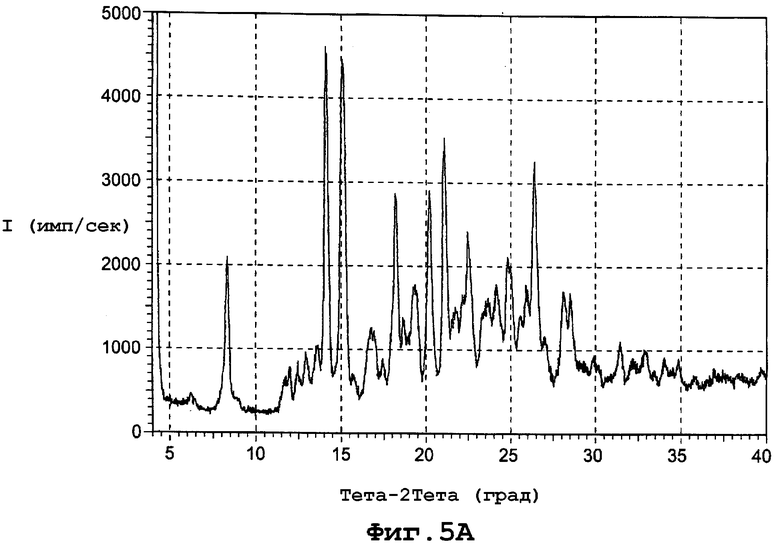
фиг. 5А является диаграммой порошковой рентгенограммы формы V полиморфа данного изобретения;
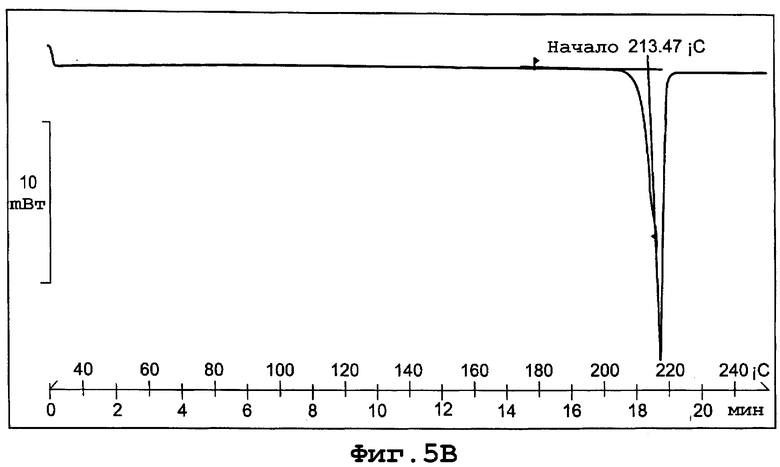
фиг. 5В является термограммой DSC формы V полиморфа данного изобретения;
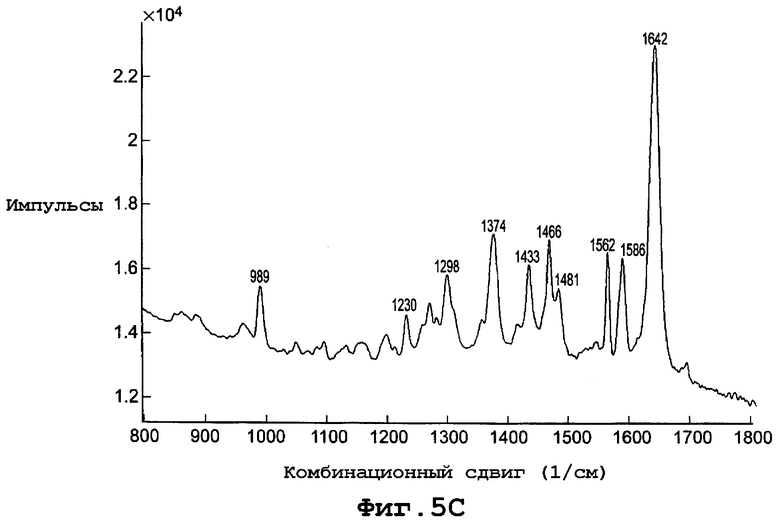
фиг. 5С является диаграммой спектрального комбинированного рассеяния формы V полиморфа данного изобретения;
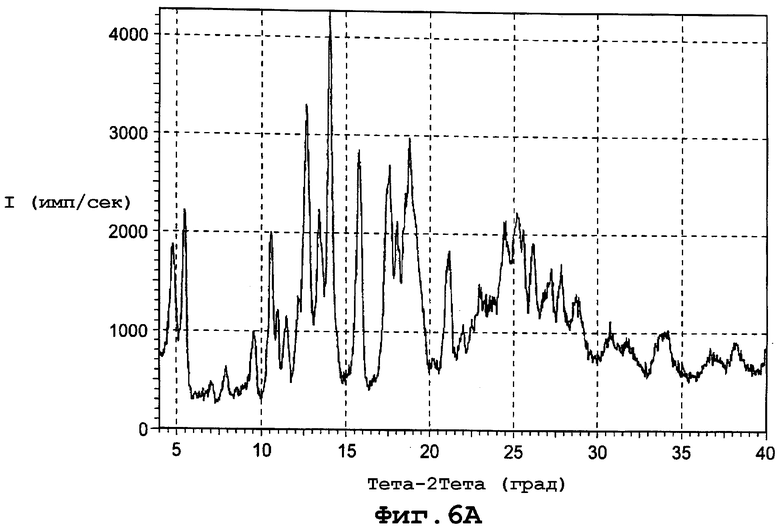
фиг. 6А является диаграммой порошковой рентгенограммы формы Ia полиморфа данного изобретения;
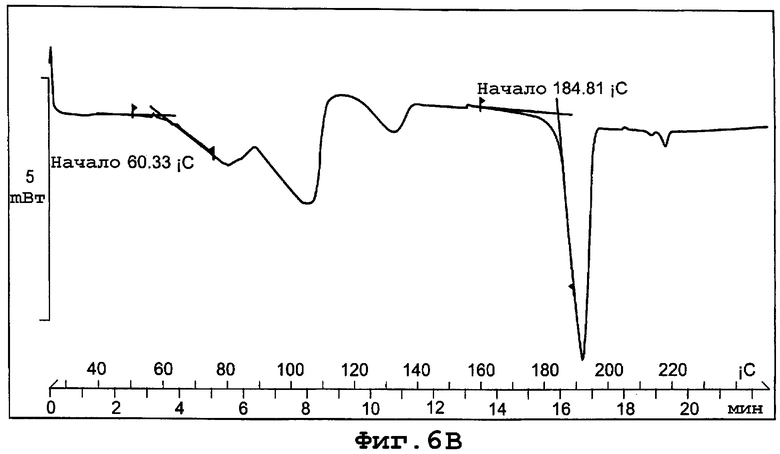
фиг. 6В является термограммой DSC формы Ia полиморфа данного изобретения;
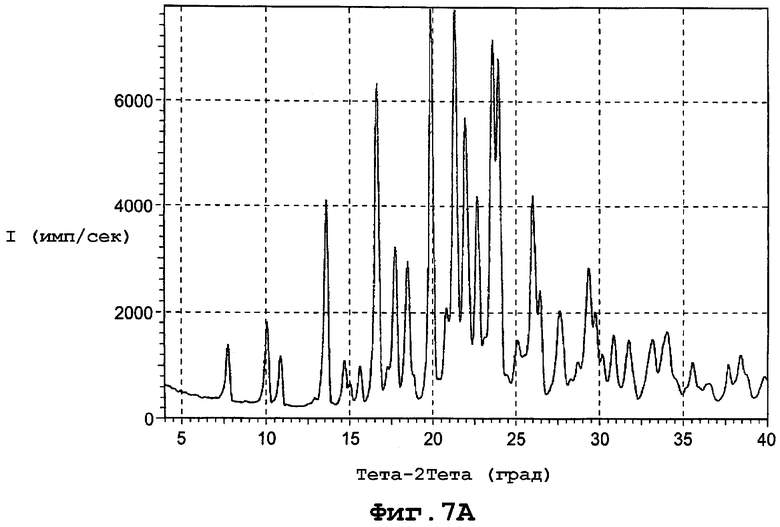
фиг. 7А является диаграммой порошковой рентгенограммы формы Ib полиморфа данного изобретения;
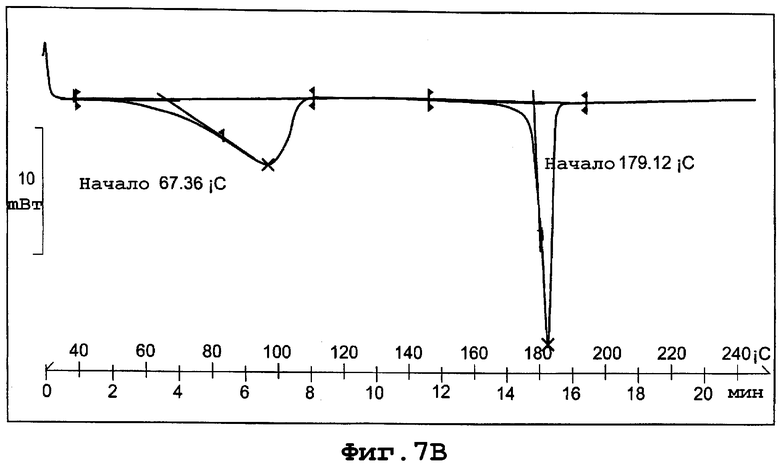
фиг. 7В является термограммой DSC формы Ib полиморфа данного изобретения;
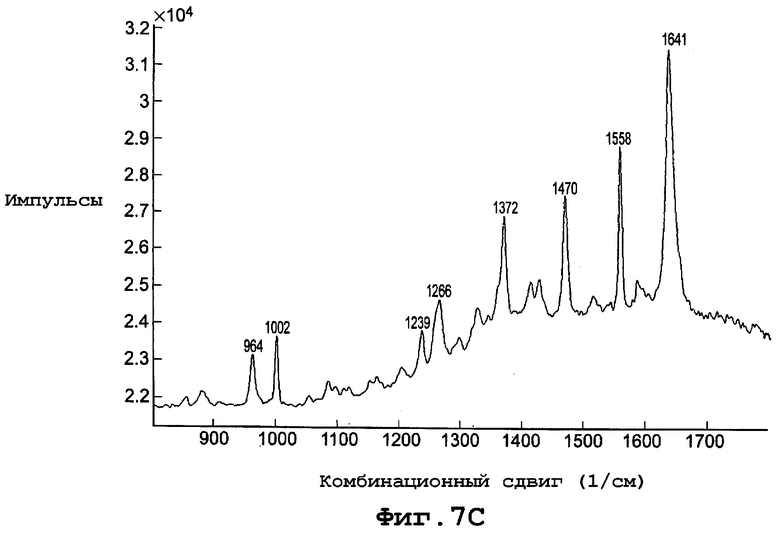
фиг. 7С является диаграммой спектрального комбинированного рассеяния формы Ib полиморфа данного изобретения;
фиг. 8А является диаграммой порошковой рентгенограммы формы IIa полиморфа данного изобретения;
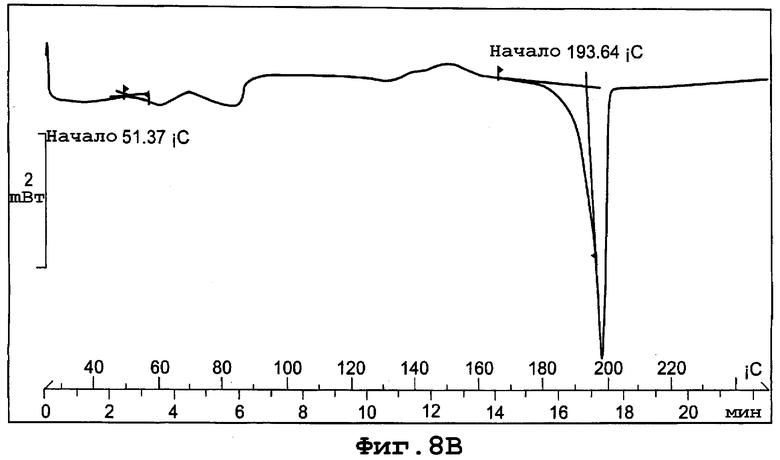
фиг. 8В является термограммой DSC формы IIa полиморфа данного изобретения;
фиг. 9А является диаграммой порошковой рентгенограммы формы IIb полиморфа данного изобретения;
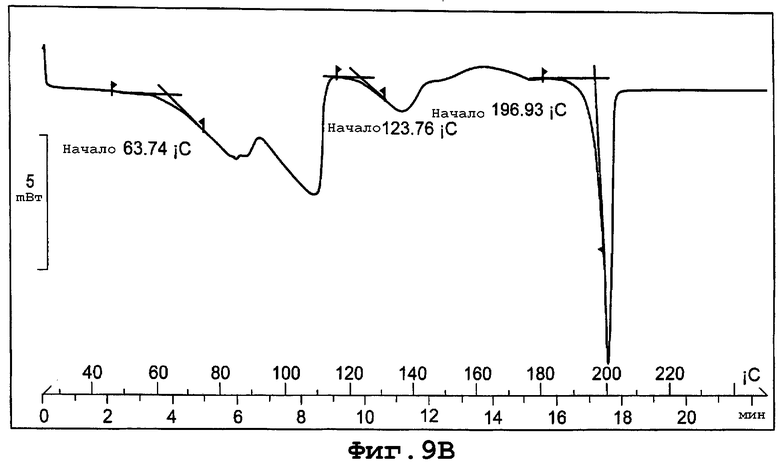
фиг. 9В является термограммой DSC формы IIb полиморфа данного изобретения;
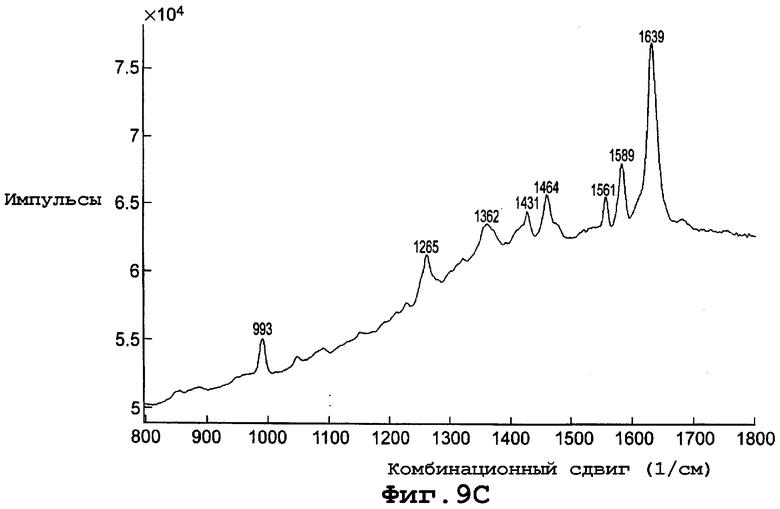
фиг. 9С является диаграммой спектрального комбинированного рассеяния формы IIb полиморфа данного изобретения;
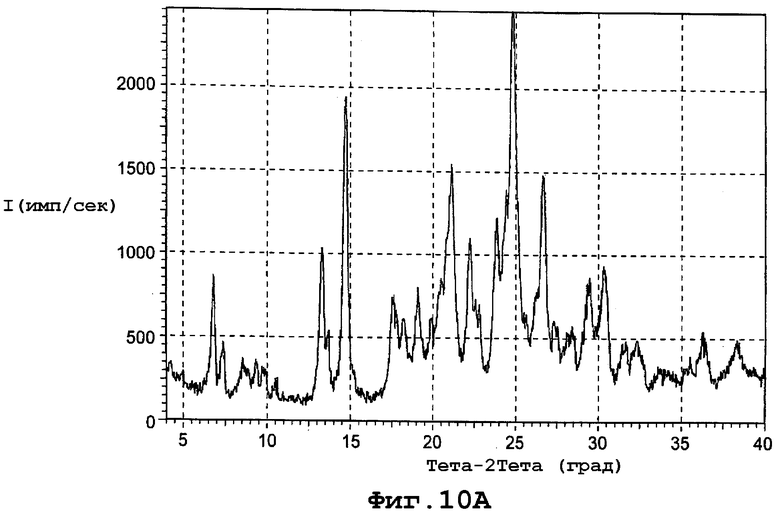
фиг. 10А является диаграммой порошковой рентгенограммы формы IIIa полиморфа данного изобретения;
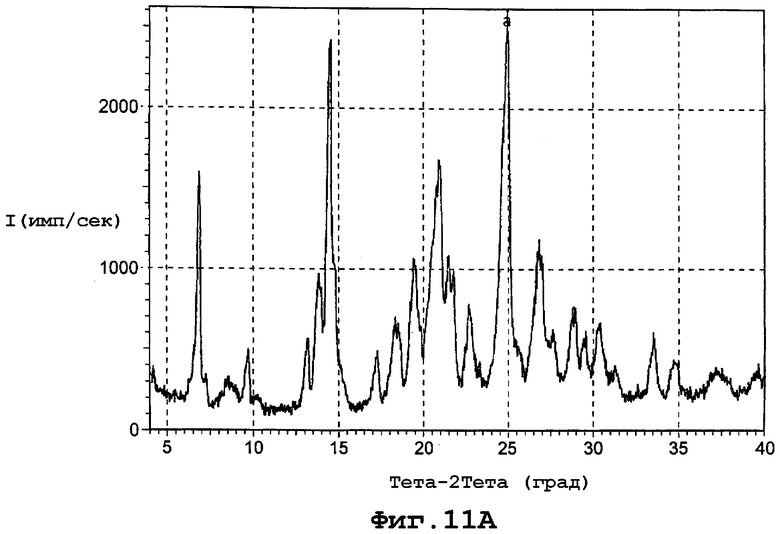
фиг. 11А является диаграммой порошковой рентгенограммы формы IIIb полиморфа данного изобретения;
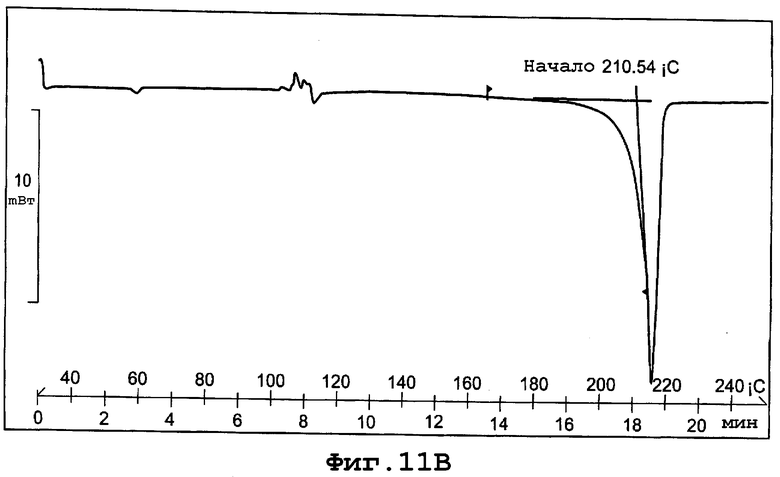
фиг. 11В является термограммой DSC формы IIIb полиморфа данного изобретения;
фиг. 11С является диаграммой спектрального комбинированного рассеяния формы IIIb полиморфа данного изобретения;
фиг. 12А является диаграммой порошковой рентгенограммы формы IVa полиморфа данного изобретения;
фиг. 12В является термограммой DSC формы IVa полиморфа данного изобретения;
фиг. 13А является диаграммой порошковой рентгенограммы формы Va полиморфа данного изобретения;
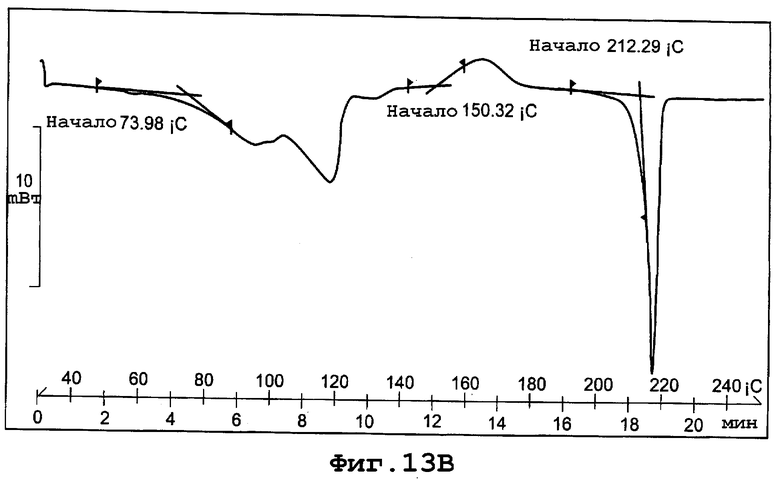
фиг. 13В является термограммой DSC формы Va полиморфа данного изобретения;
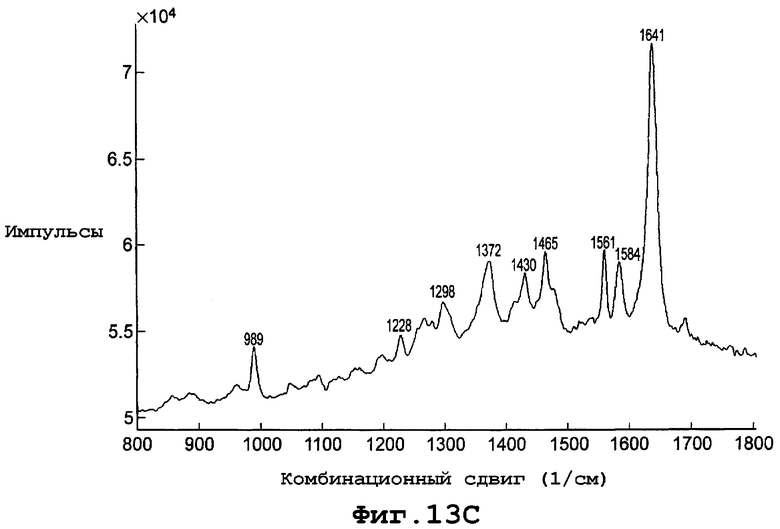
фиг. 13С является диаграммой спектрального комбинированного рассеяния формы Va полиморфа данного изобретения;
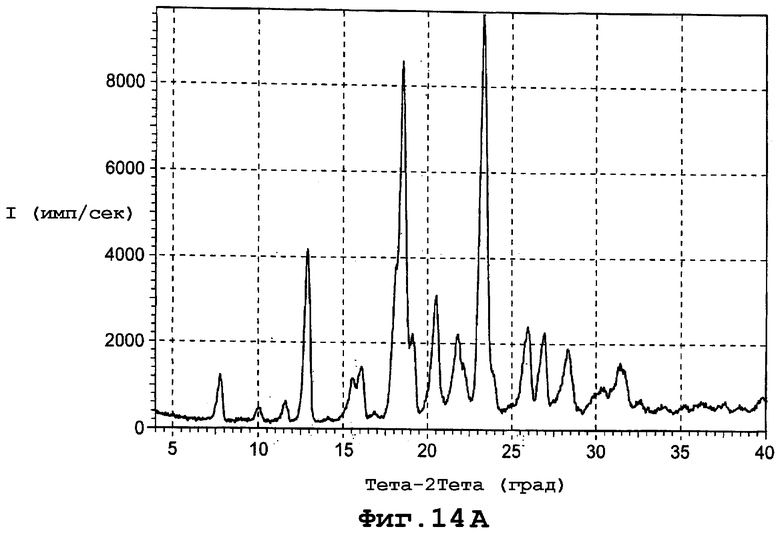
фиг. 14А является диаграммой порошковой рентгенограммы формы VI полиморфа данного изобретения;
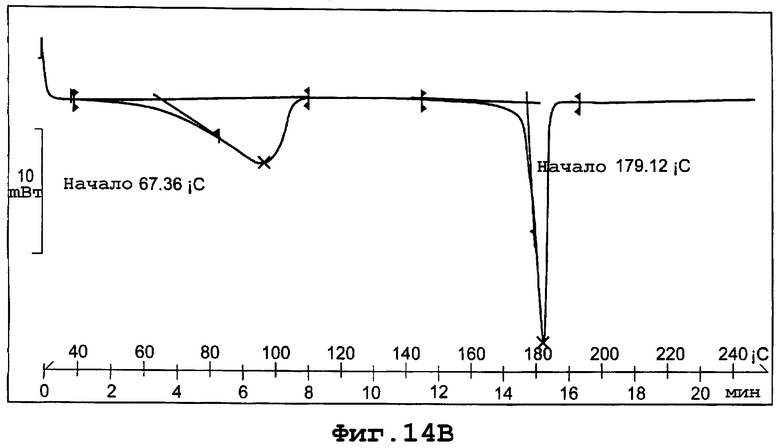
фиг. 14В является термограммой DSC формы VI полиморфа данного изобретения;
фиг. 14С является диаграммой спектрального комбинированного рассеяния формы VI полиморфа данного изобретения;
фиг. 15А является диаграммой порошковой рентгенограммы аморфной формы данного изобретения;
фиг. 15В является диаграммой спектрального комбинированного рассеяния аморфной формы данного изобретения; и
фиг. 16 является диаграммой порошковой рентгенограммы формы Ibm-2 полиморфа данного изобретения.
Подробное описание данного изобретения
Данное изобретение теперь будет описано более подробно. Данное изобретение, однако, может быть воплощено во многих разных формах и не должно истолковываться как ограниченное воплощениями, представленными здесь; точнее эти воплощения представлены так, что это описание будет исчерпывающим и полным и будет полностью представлять объем данного изобретения специалистам в данной области.
Определения
Следующие термины, которые использованы здесь, имеют указанные значения.
В соответствии с описанием и прилагаемой формулой изобретения формы единственного числа включают и множественное число объектов ссылки, если контекст ясно не диктует иное.
Термины «содержащий» или «включающий» использованы в открытом, не ограничивающем смысле.
Термин «полиморф» относится к кристаллической форме соединения с особой организацией пространственной решетки по сравнению с другими кристаллическими формами одного и того же соединения.
Термин «аморфное» относится к некристаллической форме соединения.
Термин «фармацевтически приемлемая соль» означает соль, которая сохраняет биологическую эффективность свободных кислот и оснований конкретного соединения и которая не является биологически или иначе нежелательной. Соединение данного изобретения может обладать только кислотными, только основными или обеими группами и соответственно реагируют с любым из ряда неорганических или органических оснований и неорганических и органических кислот с образованием фармацевтически приемлемой соли. Примеры фармацевтически приемлемых солей включают соли, полученные реакцией соединений данного изобретения с минеральной или органической кислотой, или неорганическим основанием, причем такие соли включают сульфаты, пиросульфаты, бисульфаты, сульфиты, бисульфиты, фосфтаты, двухзамещенные гидрофосфаты, однозамещенные гидрофосфаты, метафосфаты, пирофосфаты, хлориды, бромиды, йодиды, ацетаты, пропионаты, деканоаты, каприлаты, акрилаты, форматы, изобутираты, капроаты, гептаноаты, пропиолаты, оксалаты, малонаты, сукцинаты, субераты, себакаты, фумараты, малеаты, бутин-1,4-диоаты, гексин-1,6-диоаты, бензоаты, хлорбензоаты, метилбензоаты, динитробензоаты, гидроксибензоаты, метоксибензоаты, фталаты, сульфонаты, ксиленсульфонаты, фенилацетаты, фенилпропионаты, фенилбутираты, цитраты, лактаты, γ-гидроксибутираты, гликоляты, тартраты, метансульфонаты, пропансульфонаты, нафтален-1-сульфонаты, нафтален-2-сульфонаты и манделаты.
II. Полиморфные и аморфные формы соединения формулы I
Данное изобретение представляет несколько полиморфных кристаллических форм и аморфную форму соединения формулы I. Каждая кристаллическая или аморфная форма данного соединения может быть охарактеризована одним или более из следующих методов: порошковой рентгенограммой (т.е. пиками рентгеновской дифракции при разных углах дифракции (2Θ)), температурой начала плавления (и начала дегидратации для гидрированных форм), которые иллюстрируются эндотермами термограммы дифференциальной сканирующей калориметрии (DSC), диаграммой спектрального комбинационного рассеяния растворимостью в воде, устойчивостью к свету в условиях высокой интенсивности света по International Conference on Harmonization (ICH) и физической и химической стабильностью при хранении.
Картину порошковой рентгенограммы каждой полиморфной или аморфной формы данного изобретения определяли на рентгеновском дифрактометре Shimadzu XRD-6000, оборудованном Cu источником рентгеновского излучения, работающем при 40 кV и 50 мА. Образцы помещали в фиксатор образца, затем упаковывали и разглаживали предметным стеклом. Во время анализа образцы вращали со скоростью 60 об/мин и анализировали при углах 4 - 40° (Θ-2Θ) при 5°/мин с шагом 0,04° или при 2°/мин с шагом 0,02°. Если доступно ограниченное количество вещества, образцы помещали на силиконовую пластину (нулевой фон) и анализировали без вращения. Специалист в данной области поймет, что в положении пиков (2Θ) будет проявляться некоторая вариабельность от прибора к прибору, обычно такая как 0,1°. Соответственно, когда твердые формы данного изобретения описаны как имеющие порошковую рентгенограмму, по существу, такую же, как и показанная на данной фигуре, термин «по существу такая же», как подразумевается, охватывает такую вариабельность от прибора к прибору в положениях пиков дифракции.
Термограммы DSC получены на приборе Mettler Toledo DSC821θ при скорости сканирования 10°/мин по температурному интервалу 30-250°С. Образцы отвешивали в 40 мкл алюминиевые тигли, которые герметично закрывали и прокалывали единственное отверстие. Рассчитывали температуру начала плавления и, где применимо, температуру начала дегидратации.
В зависимости от нескольких факторов эндотермы, демонстрируемые соединениями данного изобретения, могут изменяться (на примерно 0,01-5°С при плавлении кристаллического полиморфа и на примерно 0,01-20°С при дегидратации полиморфа) выше или ниже эндотерм, представленных на прилагаемых фигурах. Факторы, ответственные за такое расхождение, включают скорость нагревания (т.е. скорость сканирования), при которой проводят анализ DSK, определяют начальную температуру хода DSC и устанавливают применяемый стандарт калибровки, калибровку прибора, относительную влажность и химическую чистоту образца. Для каждого данного образца наблюдаемые эндотермы также могут различаться от прибора к прибору; однако обычно они будут находиться в пределах, указанных здесь, при условии, что приборы калиброваны таким же образом.
Были получены спектры комбинационного рассеяния с использованием спектрофотометра комбинационного рассеяния с преобразованием Фурье Kaiser Optical Instruments, Ramen RXN1-785. Источником возбуждающего света был лазер Invictus NIR, работающий при длине волны 785 нм. Детектором был Andor CCD. Разрешение было равно 34 см-1.
Полиморфные или аморфные формы данного изобретения предпочтительно являются, по существу, чистыми, что означает, что каждая полиморфная или аморфная форма соединения формулы I включает менее 10%, предпочтительно менее 5%, предпочтительно менее 3%, предпочтительно менее 1% по весу примесей, включая другие полиморфные или аморфные формы данного соединения.
Твердые формы данного изобретения могут также существовать вместе в смеси. Смеси полиморфной и/или аморфной формы данного изобретения будет иметь пики дифракции рентгеновского излучения, характерные для каждого из полиморф и/или аморфных форм, представленных в смеси. Например, смесь двух полиморфных форм будут иметь диаграмму порошковой рентгенограммы, которая представляет собой поворот картин рентгеновской дифракции, соответствующая, по существу, чистым полиморфам.
А. Полиморфная форма I
Полиморфная форма I, безводная форма, может быть получена путем получения густой суспензии соединения формулы I в этаноле, а затем нагревания до кипячения с обратным холодильником в течение 30 минут с последующим медленным охлаждением до 23°С. Форма I имеет растворимость в воде, равную примерно 39 мкг/мл при рН 2 и примерно 0,4 мкг/мл при рН 7,4. Форма I устойчива к свету в условиях высокой интенсивности освещения по ICN и химически стабильна при 80°С и 40°С/75% ОВ в течение, по меньшей мере, 14 дней.
Форма I характеризуется диаграммой порошковой рентгенограммы с пиками в следующих примерных дифракционных углах (2θ): 4,80; 5,49; 7,06; 7,90; 9,52; 10,67; 12,33; 14,10; 15,08; 15,80; 18,12; 18,80; 19,72; 20,40; 21,09; 21,95; 23,00; 23,48; 24,52; 25,52; 26,16; 27,92; 28,36; 29,08; 29,88; 30,32; 30,96; 31,68; 33,59; 34,32; 34,72; 35,20; 36,64 и 38,00. Фигура 1А представляет диаграмму порошковой рентгенограммы для формы I.
Термограмма DSC для формы I, представленная на фигуре 1В, показывает начало эндотермы плавления кристаллов при примерно 183°С при скорости сканирования 10°С/минуту.
Диаграмма спектра комбинационного рассеяния для формы I, показанная на фигуре 1С, включает пики комбинационного сдвига (см-1) при примерно 993, 1265, 1323, 1377, 1394, 1432, 1465, 1482, 1563, 1589 и 1640.
В. Полиморфная форма II
Полиморфная форма II, безводная форма, может быть получена путем прямой кристаллизации раствора соединения формулы I в тетрагидрофуране при 60°С с помощью гексанов. Форма II имеет растворимость в воде примерно 19 мкг/мл при рН 2 и примерно 0,7 мкг/мл при рН 7,4. Форма II устойчива к свету в условиях высокой интенсивности освещения по ICH.
Форма II характеризуется диаграммой порошковой рентгенограммы с пиками в следующих примерных дифракционных углах (2θ): 4,65; 6,9200; 7,36; 7,76; 9,81; 11,41; 12,08; 12,60; 13,03; 13,72; 14,24; 14,72; 16,06; 16,66; 17,80; 18,32; 18,80; 19,68; 20,32; 21,05; 21,89; 22,64; 23,00; 23,60; 25,45; 26,30; 27,18; 28,34; 29,04; 30,21; 31,14; 32,24; 34,14; 34,91; 36,97; 39,21 и 39,92. Фигура 2А представляет диаграмму порошковой рентгенограммы для формы II.
Термограмма DSC для формы II, представленная на фигуре 2В, показывает начало эндотермы плавления кристаллов при примерно 195°С при скорости сканирования 10°С/минуту.
Диаграмма спектра комбинационного рассеяния для формы I, показанная на фигуре 2С, включает пики комбинационного сдвига (см-1) при примерно 993, 1265, 1323, 1377, 1394, 1432, 1465, 1482, 1563, 1589 и 1640.
С. Полиморфная форма III
Полиморфная форма III, безводная форма, может быть получена путем получения густой суспензии твердого соединения формулы I в минеральном масле при 192°С в течение 1,5 часов, с последующим промыванием гексаном и фильтрованием. Форма III имеет растворимость в воде, равную примерно 10 мкг/мл при рН 2 и примерно 0,6 мкг/мл при рН 7,4. Форма III устойчива к свету в условиях высокой интенсивности освещения по ICN.
Форма III характеризуется диаграммой порошковой рентгенограммы с пиками в следующих примерных дифракционных углах (2θ): 6,40; 6,87; 7,36; 9,73; 10,43; 13,20; 13,72; 14,04; 14,65; 15,20; 15,80; 17,60; 18,56; 19,56; 20,16; 20,56; 21,49; 21,96; 22,92; 23,40; 24,08; 24,98; 25,64; 27,32; 27,72; 28,35; 29,08; 29,56; 30,12; 30,58; 31,53; 33,58; 35,01; 36,84; 37,24; 37,60 и 39,51. Фигура 3А представляет диаграмму порошковой рентгенограммы для формы III.
Термограмма DSC для формы III, представленная на фигуре 3В, показывает начало эндотермы плавления кристаллов при примерно 210°С при скорости сканирования 10°С/минуту.
Диаграмма спектра комбинационного рассеяния для формы III, показанная на фигуре 3С, включает пики комбинационного сдвига (см-1) при примерно 991, 1261, 1379, 1431, 1589 и 1634.
D. Полиморфная форма IV
Форма IV, безводная форма, может быть получена путем кристаллизации соединения формулы I в этилацетате и этаноле с помощью NaHCO3:воды 1:1. Форма IV имеет растворимость в воде, равную примерно 7 мкг/мл при рН 2. Форма IV устойчива к свету в условиях высокой интенсивности освещения по ICN.
Форма IV характеризуется диаграммой порошковой рентгенограммы с пиками в следующих примерных дифракционных углах (2θ): 4,85; 7,95; 9,85; 11,51; 12,80; 13,53; 14,56; 14,92; 15,80; 16,32; 17,43; 18,08; 18,44; 19,31; 20,08; 21,08; 21,61; 22,64; 23,24; 23,84; 24,48; 25,08; 26,24; 27,02; 27,92; 28,76; 30,12; 30,72; 31,40; 32,52; 34,07; 37,48 и 38,20. Фигура 4А представляет диаграмму порошковой рентгенограммы для формы IV.
Термограмма DSC для формы IV, представленная на фигуре 4В, показывает начало эндотермы плавления кристаллов при примерно 118°С при скорости сканирования 10°С/минуту.
Диаграмма спектра комбинационного рассеяния для формы IV, показанная на фигуре 4С, включает пики комбинационного сдвига (см-1) при примерно 998, 1269, 1314, 1340, 1371, 1436, 1463, 1483, 1562, 1592 и 1644.
Е. Полиморфная форма V
Полиморфная форма V, безводная форма, может быть получена путем получения густой суспензии твердых веществ формы IV в густом минеральном масле при 130°С, а затем 180°С в течение примерно 1,5 часов с последующим промыванием гексаном и фильтрованием. Форма V имеет растворимость в воде, равную примерно 8 мкг/мл при рН 2 и примерно 0,2 мкг/мл при рН 7,4. Форма V устойчива к свету в условиях высокой интенсивности освещения по ICN.
Форма V характеризуется диаграммой порошковой рентгенограммы с пиками в следующих примерных дифракционных углах (2θ): 4,23; 8,38; 11,74; 12,00; 12,47; 12,95; 13,58; 14,17; 15,15; 16,76; 16,96; 17,44; 17,92; 18,28; 18,70; 19,37; 20,26; 21,16; 21,62; 21,84; 22,16; 22,54; 23,28; 23,64; 24,17; 24,84; 25,12; 25,58; 25,98; 26,48; 27,02; 28,16; 28,54; 29,14; 29,89; 31,40; 32,23; 32,66 и 39,68. Фигура 5А представляет диаграмму порошковой рентгенограммы для формы V.
Термограмма DSC для формы V, представленная на фигуре 5В, показывает начало эндотермы плавления кристаллов при примерно 210°С при скорости сканирования 10°С/минуту.
Диаграмма спектра комбинационного рассеяния для формы V, показанная на фигуре 5С, включает пики комбинационного сдвига (см-1) при примерно 989, 1230, 1298, 1374, 1433, 1466, 1481, 1562, 1586 и 1642.
F. Полиморфная форма Ia
Форма Ia, которая является гидратной формой, может быть получена путем взбалтывания густой суспензии соединения формы I в воде при комнатной температуре в течение семи дней. Форма Ia устойчива к свету в условиях высокой интенсивности освещения по ICN.
Форма Ia характеризуется диаграммой порошковой рентгенограммы с пиками в следующих примерных дифракционных углах (2θ): 4,84; 5,49; 7,07; 7,90; 9,55; 10,60; 10,96; 11,48; 12,20; 12,72; 13,48; 14,10; 14,56; 15,78; 17,54; 18,08; 18,52; 18,88; 19,44; 21,11; 21,93; 22,48; 23,06; 23,72; 24,20; 24,48; 25,20; 25,56; 26,12; 26,72; 27,12; 27,78; 28,75; 30,36; 30,68; 31,20; 31,64; 32,04; 34,64; 34,97; 36,16; 36,60; 36,92; 37,24; 37,68; 38,12; 38,48; и 39,80. Фигура 6А представляет диаграмму порошковой рентгенограммы для формы Ia.
Термограмма DSC для формы Ia, представленная на фигуре 6В, показывает начало эндотермы дегидратации при примерно 60°С и начало эндотермы плавления кристаллов при примерно 185°С при скорости сканирования 10°С/минуту.
G. Полиморфная форма Ib
Форма Ib, которая является моногидратом, может быть получена путем взбалтывания густой суспензии формы в воде при 90°С в течение трех дней или путем кристаллизации из этанола:воды при более 65°С. Форма Ib физически и химически стабильна в течение, по меньшей мере, трех месяцев при 60°С и 40°С/75%ОВ и устойчива к свету в условиях высокой интенсивности освещения по ICN.
Форма Ib характеризуется диаграммой порошковой рентгенограммы с пиками при следующих примерных дифракционных углах (2θ): 7,93; 10,23; 11,04; 13,12; 13,79; 14,88; 15,24; 15,81; 16,81; 17,40; 17,89; 18,64; 19,00; 20,11; 20,96; 21,53; 22,14; 22,87; 23,80; 24,16; 25,20; 26,20; 26,64; 27,76; 28,38; 28,84; 29,52; 29,92; 30,28; 30,92; 31,87; 32,80; 33,24; 34,07; 34,68; 35,74; 36,54 и 37,96. Фигура 7А представляет диаграмму порошковой рентгенограммы для формы Ib.
Диаграмма спектра комбинационного рассеяния для формы Ib, показанная на фигуре 7С, включает пики комбинационного сдвига (см-1) при примерно 964, 1002, 1239, 1266, 1372, 1470, 1558 и 1641.
Н. Полиморфная форма IIa
Форма IIa, моногидрат, может быть получена путем взбалтывания густой суспензии соединения формы I в воде при комнатной температуре в течение семи дней. Форма IIa устойчива к свету в условиях высокой интенсивности освещения по ICN.
Форма IIa характеризуется диаграммой порошковой рентгенограммы с пиками в следующих примерных дифракционных углах (2θ): 4,77; 7,64; 8,80; 9,82; 11,41; 12,75; 13,48; 14,23; 15,96; 16,64; 17,68; 18,76; 21,67; 22,85; 25,38; 27,16; 28,24; 30,12; 31,23; 32,16; 34,02; 34,80; 35,92; 36,92; 38,32 и 39,25. Фигура 8А представляет диаграмму порошковой рентгенограммы для формы IIa.
Термограмма DSC для формы IIa, представленная на фигуре 8В, показывает начало эндотермы дегидратации при примерно 51°С и начало эндотермы плавления кристаллов при примерно 194°С при скорости сканирования 10°С/минуту.
I. Полиморфная форма IIb
Форма IIb, дигидрат, может быть получена путем взбалтывания густой суспензии соединения формы II в воде при температуре 90°С в течение трех дней и затем при комнатной температуре в течение 17 дней. Форма IIb устойчива к свету в условиях высокой интенсивности освещения по ICN.
Форма IIb характеризуется диаграммой порошковой рентгенограммы с пиками при следующих примерных дифракционных углах (2θ): 4,80; 7,86; 8,73; 11,44; 12,70; 13,41; 14,33; 15,71; 16,60; 17,43; 18,32; 19,03; 20,08; 21,56; 21,88; 22,56; 23,10; 23,76; 24,40; 25,04; 25,56; 26,20; 26,64; 27,02; 27,80; 28,64; 30,63; 31,36; 31,80; 32,28; 33,88; 35,95; 37,03; 37,80; 38,16 и 39,88. Фигура 9А представляет диаграмму порошковой рентгенограммы для формы IIb.
Термограмма DSC для формы IIb, представленная на фигуре 9В, показывает начало эндотермы дегидратации при примерно 64°С и начало эндотермы плавления кристаллов при примерно 197°С при скорости сканирования 10°С/минуту.
Диаграмма спектра комбинационного рассеяния для формы IIb, показанная на фигуре 9С, включает пики комбинационного сдвига (см-1) при примерно 993, 1265, 1362, 1431, 1464, 1561, 1589 и 1639.
J. Полиморфная форма IIIa
Форма IIIa, дигидрат, может быть получена путем взбалтывания густой взвеси формы III в воде при комнатной температуре в течение семи дней или путем помещения формы III при 93% относительной влажности при комнатной температуре в течение десяти дней.
Форма IIIa характеризуется диаграммой порошковой рентгенограммы с пиками при следующих примерных дифракционных углах (2θ): 6,81; 7,36; 8,71; 9,37; 9,80; 10,51; 13,31; 13,72; 14,72; 15,28; 17,60; 18,20; 19,09; 19,92; 20,48; 21,03; 22,27; 22,68; 23,84; 24,36; 24,86; 25,60; 26,16; 26,66; 27,33; 28,22; 29,41; 30,29; 31,48; 32,27; 33,60; 35,35; 36,22 и 38,21. Фигура 10А представляет диаграмму порошковой рентгенограммы для формы IIIa.
К. Полиморфная форма IIIb
Форма IIIb, безводная форма, может быть получена путем сушки формы IIIa при 50°С под вакуумом.
Форма IIIb характеризуется диаграммой порошковой рентгенограммы с пиками при следующих примерных дифракционных углах (2θ): 6,28; 6,84; 7,36; 8,66; 9,66; 13,13; 13,80; 14,4718; 15,40; 17,21; 18,39; 19,46; 20,78; 21,56; 22,70; 24,81; 25,52; 26,79; 27,60; 28,80; 29,45; 30,32; 31,22; 33,47; 34,69; 37,16; 37,88 и 39,45. Фигура 11А представляет диаграмму порошковой рентгенограммы для формы IIIb.
Термограмма DSC для формы IIIb, представленная на фигуре 11В, показывает начало эндотермы плавления кристаллов при примерно 210°С при скорости сканирования 10°С/минуту.
Диаграмма спектра комбинационного рассеяния для формы IIIb, показанная на фигуре 11С, включает пики комбинационного сдвига (см-1) при примерно 993, 1267, 1311, 1326, 1378, 1436, 1466, 1481, 1563, 1592 и 1636.
L. Полиморфная форма IVa
Форма IVa, дигидрат, может быть получена путем взбалтывания густой взвеси формы IV в воде при комнатной температуре в течение семи дней. Форма IVa устойчива к свету в условиях высокой интенсивности освещения по ICN.
Форма IVa характеризуется диаграммой порошковой рентгенограммы с пиками при следующих примерных дифракционных углах (2θ): 4,85; 7,95; 9,85; 11,51; 12,80; 13,53; 14,56; 14,92; 15,80; 16,32; 17,43; 18,08; 18,44; 19,31; 20,08; 21,08; 21,61; 22,64; 23,24; 23,84; 24,48; 25,08; 26,24; 27,02; 27,92; 28,76; 30,12; 30,72; 31,40; 32,52; 34,07; 37,48 и 38,20. Фигура 12А представляет диаграмму порошковой рентгенограммы для формы IVa.
Термограмма DSC для формы IVa, представленная на фигуре 12В, показывает начало эндотермы дегидратации при примерно 63°С и начало эндотермы плавления кристаллов при примерно 123°С при скорости сканирования 10°С/минуту.
M. Полиморфная форма Va
Форма Va, дигидратная форма, может быть получена путем взбалтывания густой взвеси формы V в воде в течение семи дней. Форма IVa устойчива к свету в условиях высокой интенсивности освещения по ICN.
Форма Va характеризуется диаграммой порошковой рентгенограммы с пиками при следующих примерных дифракционных углах (2θ): 4,26; 4,82; 7,92; 8,42; 8,96; 11,45; 12,70; 13,40; 14,21; 15,21; 15,70; 16,64; 16,96; 17,30; 18,28; 19,16; 20,24; 21,14; 21,60; 22,56; 23,20; 23,80; 24,44; 24,96; 26,60; 27,08; 27,96; 28,56; 29,04; 30,62; 31,34; 32,27; 32,84; 33,92; 34,83; 35,90; 36,99 и 37,44. Фигура 13А представляет диаграмму порошковой рентгенограммы для формы Va.
Термограмма DSC для формы Va, представленная на фигуре 13В, показывает начало эндотермы дегидратации при примерно 74°С и начало эндотермы плавления кристаллов при примерно 211°С при скорости сканирования 10°С/минуту.
Диаграмма спектра комбинационного рассеяния для формы Va, показанная на фигуре 13С, включает пики комбинационного сдвига (см-1) при примерно 989, 1228, 1298, 1372, 1430, 1465, 1561, 1584 и 1641.
N. Полиморфная форма VI
Форма VI, безводная форма, может быть получена путем дегидратации формы Ib, такой как нагревание формы Ib при 140С в течение 10 минут. Форма VI является очень гигроскопичной и может быть легко превращена обратно в форму Ib в условиях влажности окружающей среды.
Форма VI характеризуется диаграммой порошковой рентгенограммы с пиками при следующих примерных дифракционных углах (2θ): 7,74; 10,00; 11,56; 12,85; 15,56; 16,04; 17,80; 18,47; 19,20; 20,43; 21,72; 22,16; 23,28; 24,00; 25,83; 26,79; 28,23; 29,88; 30,36; 31,36 и 39,69. Фигура 14А представляет диаграмму порошковой рентгенограммы для формы VI.
Термограмма DSC для формы VI, представленная на фигуре 14В, показывает начало эндотермы плавления кристаллов при примерно 179°С при скорости сканирования 10°С/минуту.
Диаграмма спектра комбинационного рассеяния для формы VI, показанная на фигуре 14С, включает пики комбинационного сдвига (см-1) при примерно 965, 993, 1201, 1230, 1267, 1320, 1368, 1412, 1426, 1469, 1557, 1587 и 1647.
О. Аморфная форма
Аморфная форма может быть получена разбавлением водой (примерно в соотношении 1:10) при добавлении каплями соединения формулы I в растворе в полиэтиленгликоле 400 или путем выпаривания в роторном испарителе раствора соединения формулы I в метаноле или в ТГФ, или лиофилизации раствора соединения формулы I в т-бутаноле.
Диаграмма порошковой рентгенограммы аморфной формы характеризуется типичным аморфным широким округлым пиком от 4 до 40 без острых пиков, характерных для кристаллических форм. Фигура 15А представляет диаграмму порошковой рентгенограммы для аморфной формы.
Диаграмма спектра комбинационного рассеяния для аморфной формы, показанная на фигуре 15В, включает пики комбинационного сдвига (см-1) при примерно 995, 1265, 1366, 1435, 1468, 1562, 1589 и 1640.
Р. Смеси
Кристаллические и аморфные формы, описанные выше, могут существовать также в смесях, в которых твердая форма существует в виде смеси, содержащей, по меньшей мере, две из твердых форм, обсужденных выше. Например, форма Ibm-2 является мета-стабильной формой, которая является смесью форм Ib и VI. Эта мета-стабильная форма может быть получена путем дегидратации формы Ib под вакуумом при температуре примерно 45°С или более. Частичная гидратация формы VI будет также приводить к метастабильной форме Ibm-2. Форма Ibm-2 будет превращаться в форму Ib при полной гидратации в условиях влажности окружающей среды. Форма Ibm-2 характеризуется диаграммой порошковой рентгенограммы с пиками, которые показаны на фигуре 16. Данная диаграмма соответствует диаграмме, которая является результатом сложения диаграмм формы Ib и формы VI. Термограмма DSC для формы Ibm-2 показывает начало эндотермы дегидратации при примерно 73°С и начало эндотермы плавления кристаллов при примерно 177°С при скорости сканирования 10°С/минуту.
III. Фармацевтические композиции данного изобретения
Активные вещества (т.е. полиморфные и аморфные формы соединения формулы I, описанной здесь, или их смеси) данного изобретения могут быть переработаны в фармацевтические композиции, пригодные для использования в ветеринарии и для медицинского применения у людей. Фармацевтические композиции данного изобретения содержат терапевтически эффективное количество активного вещества и один или более из инертных фармацевтически приемлемых носителей, и необязательно, любые другие терапевтические ингредиенты, стабилизаторы и тому подобное. Носитель(ли) должны быть фармацевтически приемлемыми в том смысле, что должны быть совместимыми с другими ингредиентами препарата и не быть вредными для принимающего препарат. Данные композиции могут дополнительно включать разбавители (растворители), буферы, связывающие вещества, дезинтегранты, загустители, улучшающие скольжение вещества, консерванты (включая антиоксиданты), улучшающие вкус и запах вещества, маскирующие неприятный вкус вещества, неорганические соли (например, хлорид натрия), антимикробные вещества (например, бензалкония хлорид), подсластители, антистатики, поверхностно-активные вещества (например, полисорбаты, такие как «твин 20» и «твин 80», и плуроники, такие как F68 и F88, доступные для приобретения у BASF), сложные эфиры сорбита, липиды (например, фосфолипиды, такие как лецитин и другие фосфтидилхолины, фосфатидилэтаноламины, жирные кислоты и сложные жирные эфиры, стероиды (например, холестерин)) и хелатирующие вещества (например, ЭДТА, цинк и другие такие подходящие катионы). Другие фармацевтические вспомогательные вещества и/или добавки, пригодные для использования в композициях по данному изобретению, перечислены в «Remington: The Science & Practice of Pharmacy», 19th ed., Williams & Williams (1995) и в «Phisician's Desk Reference», 52th ed., Medical Economics, Montvale, NJ (1998), и в «Handbook Pharmaceutical Excipients», Third Ed., Ed. A.H. Kibbe, Pharmaceutical Press, 2000. Активные вещества данного изобретения могут быть переработаны в композиции, включая пригодные для перорального, ректального, местного, назального, глазного или парентерального (включая внутрибрюшинные, внутривенные, подкожные или внутримышечные инъекции) введения.
Количество активного вещества в лекарственной форме будет меняться в зависимости от ряда факторов, включая дозированную форму, патологическое состояние, которое нужно лечить, целевую группу пациентов и других соображений, и будет обычно легко определяться специалистом в данной области. Терапевтически эффективное количество будет количеством, необходимым для модуляции, регуляции или ингибирования протеинкиназы. На практике оно будет меняться в широких пределах в зависимости от конкретного активного вещества, тяжести патологического состояния, которое нужно лечить, группы пациентов, стабильности препарата и тому подобного. Композиции будут обычно содержать где-то от примерно 0,001% по весу до примерно 99% по весу активного вещества, предпочтительно от примерно 0,01% до примерно 5% по весу активного вещества, и более предпочтительно от примерно 0,01% до 2% по весу активного вещества, и это будет также зависеть от относительных количеств наполнителей/добавок, содержащихся в композиции.
Фармацевтическую композицию данного изобретения вводят в обычной дозированной форме, изготовленной путем объединения терапевтически эффективного количества активного вещества в качестве активного ингредиента с одним или более из подходящих фармацевтических носителей по общепринятым методикам. Эти методы могут включать смешивание, гранулирование и прессование или растворение ингредиентов, как нужно для желаемого препарата.
Применяемый фармацевтический носитель может быть или твердым или жидким. Примеры твердых носителей включают лактозу, сахарозу, тальк, желатин, агар, пектин, акацию, стеарат магния, стеариновую кислоту и тому подобное. Примеры жидких носителей включают сироп, арахисовое масло, оливковое масло, воду и т.п. Подобным же образом носитель может включать замедляющие или пролонгирующие всасывание вещества, известные специалистам, такие как глицерилмоностеарат или глицерилдистеарат отдельно или с воском, этилцеллюлозой, гидроксипропилцеллюлозой, метилметакрилатом и т.п.
Можно использовать ряд фармацевтических форм. Так, если используют твердый носитель, препарат можно таблетировать, помещать в твердую желатиновую капсулу в порошковой или гранулированной форме, или изготавливать в виде драже или лепешек. Количество твердого носителя может меняться, но обычно будет составлять от примерно 25 мг до примерно 1 г. Если используют жидкий носитель, препарат может быть в форме сиропа, эмульсии, мягкой желатиновой капсулы, стерильных инъекционного раствора или инъекционной суспензии в ампуле или флаконе, или неводной жидкой суспензии.
Чтобы получить стабильную водорастворимую дозированную форму, фармацевтически приемлемую соль активного соединения растворяют в водном растворе органической или неорганической кислоты, таком как 0,3 М раствор янтарной кислоты или лимонной кислоты. Если растворимой формы соли нет в наличии, активное вещество может быть растворено в подходящем сорастворителе или комбинациях сорастворителей. Примеры подходящих сорастворителей включают, но не ограничиваются этим, спирт, пропиленгликоль, полиэтиленгликоль 300, полисорбат 80, глицерин и тому подобное в концентрациях, колеблющихся в интервале 0-60% от объема в целом. Композиция может быть также в виде раствора или в виде соли активного вещества в подходящем водном растворителе, таком как вода или изотонический раствор соли, или раствор глюкозы.
Понятно, что фактические дозировки активных веществ, используемые в композициях данного изобретения, будут меняться в соответствии с конкретным комплексом, который нужно использовать, конкретной создаваемой композицией, способом введения и конкретным местом, хозяином и заболеванием, которое нужно лечить. Специалисты в данной области, использующие обычные тесты для определения дозировки с учетом экспериментальных данных для какого-то вещества, могут установить оптимальные дозировки для данной совокупности условий. Для перорального введения примером обычно применяемой суточной дозировки является дозировка в интервале от 0,001 до примерно 1000 мг/кг веса тела, более предпочтительно от примерно 0,001 до примерно 50 мг/кг веса тела с курсами лечения, повторяемыми с соответствующими интервалами. Введение пролекарств обычно происходит в дозах на уровне, который по весу химически эквивалентен весовому уровню полностью активной формы.
Композиции данного изобретения могут быть получены методами, в общем известными специалистам в отношении получения фармацевтических композиций, например с использованием обычных методов, таких как смешивание, растворение, гранулирование, дражирование, растирание в порошок, эмульгирование, инкапсулирование, включение в массу или лиофилизация. Фармацевтические композиции могут быть получены обычным способом с использованием одного или более из физиологически приемлемых носителей, которые могут быть выбраны из наполнителей и вспомогательных веществ, которые облегчают переработку активных веществ в препараты и которые могут фармацевтически использоваться.
Соответствующая технология получения препарата зависит от выбранного пути введения. Для инъекций вещества данного изобретения могут быть изготовлены в виде водных растворов, предпочтительно в физиологически совместимых буферах, таких как раствор Хэнкса, раствор Рингера или буфер на основе физиологического раствора. Для введения через слизистые в препарате используют вещества для улучшения проникновения активного вещества в соответствии с барьером, через который оно должно проникнуть в организм. Такие вещества для улучшения проникновения в основном известны специалистам.
Что касается перорального введения, соединения могут быть легко переработаны в препарат путем соединения активных соединений с фармацевтически приемлемыми носителями, известными специалистам. Такие носители делают возможным переработать соединения данного изобретения так, чтобы изготовить препараты в виде таблеток, пилюль, драже, капсул, жидкостей, гелей, сиропов, густых суспензий, суспензий и тому подобного, для перорального приема пациентом, который нуждается в лечении. Фармацевтические препараты для перорального использования можно получить, используя твердый наполнитель в смеси с активным ингредиентом (веществом), необязательно, размалывая полученную смесь и перерабатывая смесь из гранул после добавления соответствующих вспомогательных веществ, если желательно, с получением таблеток или ядер драже. Подходящие вспомогательные вещества включают: наполнители, такие как сахара, включая лактозу, сахарозу, маннит или сорбит; и препараты целлюлозы, например кукурузный крахмал, пшеничный крахмал, рисовый крахмал, картофельный крахмал, желатин, камедь, метилцеллюлозу, гидроксипропилметилцеллюлозу, натрийкарбоксиметилцеллюлозу или поливинилпирролидон (ПВП). Если желательно, можно добавить дезинтегрирующие вещества, такие как структурированный поливинилпирролидон, агар или альгиновая кислота или ее соль, такая как альгинат натрия.
На ядрах драже создают соответствующее подходящее покрытие. Для этой цели можно использовать концентрированные растворы сахара, которые, по желанию, могут содержать аравийскую камедь, поливинилпирролидон, гель карбопол, полиэтиленгликоль и/или диоксид титана, глазирующие растворы и подходящие органические растворители и смеси растворителей. В таблетки или покрытия для драже могут быть добавлены красители и пигменты для идентификации или для того, чтобы придать отличие разным комбинациям активных веществ.
Фармацевтические препараты, которые можно использовать перорально, включают набиваемые капсулы, изготовленные из желатина, а также мягкие запаиваемые капсулы, изготовляемые из желатина и пластификатора, такого как глицерин или сорбит. Набиваемые капсулы могут содержать активные ингредиенты в смеси с такими наполнителями, как лактоза, связывающими веществами, такими как крахмалы, и/или улучшающими скольжение веществами, такими как тальк или стеарат магния, и, необязательно, стабилизаторами. В мягких капсулах активные вещества могут быть растворены или суспендированы в подходящих жидкостях, таких как жирные масла, жидкий парафин или жидкие полиэтиленгликоли. Кроме того, можно добавлять стабилизаторы. Все препараты для перорального введения должны быть в дозах, подходящих для такого введения. Для защечного введения композициям можно придавать форму таблеток или пастилок, изготовленных обычным способом.
Для введения интраназально или путем ингаляции соединения для применения по данному изобретению обычно доставляются в виде подачи жидкости для получения аэрозоля из упаковок под давлением или из небулайзера с использованием соответствующего пропеллента, например дихлордифторметана, трихлорфторметана, дихлортетрафторэтана, двуокиси углерода или другого подходящего газа. В случае аэрозольного препарата под давлением единица дозировки может определяться с помощью обеспечения клапаном для подачи отмеренного количества. Можно изготовить капсулы и катриджи из желатина для использования в ингаляторе или инсуффляторе или тому подобном, содержащие порошковую смесь данного соединения и подходящую порошковую основу, такую как лактоза или крахмал.
Соединения могут быть переработаны в лекарственную форму для парентерального введения путем инъекций, например путем нагрузочной инъекции или длительного вливания. Препараты для инъекции могут быть представлены в дозированной форме на одно введение, например в ампулах или в контейнерах, содержащих много доз, с добавленным консервантом. Композиции могут иметь такие формы, как суспензии, растворы или эмульсии в масляных или водных носителях, и могут содержать технологические вещества для получения препарата, такие как суспендирующие, стабилизирующие и/или диспергирующие вещества.
Фармацевтические препараты для парентерального введения включают водные растворы активных соединений в водорастворимой форме. Кроме того, суспензии активных веществ могут быть получены в виде соответствующих суспензий для инъекций в масле. Подходящие липофильные растворители или носители включают жирные масла, такие как кунжутное масло, или синтетические сложные эфиры жирных кислот, такие как этилолеат или триглицериды, или липосомы. Водные инъекционные суспензии могут содержать вещества, которые повышают вязкость суспензии, такие как натрийкарбоксиметилцеллюлоза, сорбит или декстран. По желанию, суспензия может также содержать подходящие стабилизаторы или вещества, которые повышают растворимость соединений, которые дают возможность приготовления высококонцентрированных растворов.
Для введения в глаза активное вещество доставляется в фармацевтически приемлемом для глаз носителе, так что соединение сохраняется в контакте с поверхностью глаза в течение достаточного периода времени, чтобы дать возможность соединению проникнуть в роговичную и внутреннюю области глаза, включая, например, переднюю камеру, заднюю камеру, внутриглазную жидкость, стекловидное тело, роговицу, радужную оболочку/цилиарную область, хрусталик, сосудистую оболочку/сетчатку и т.д. Фармацевтически приемлемый носитель для глаз может быть, например, мазью, растительным маслом или инкапсулирующим материалом. Соединение данного изобретения можно также вводить путем инъекции непосредственно в стекловидное тело или внутриглазную жидкость, или субтенально.
Альтернативно активный ингредиент может быть в порошковой форме для воспроизведения с помощью подходящего носителя, например стерильной апирогенной воды, перед применением. Данные соединения могут быть также переработаны в композиции для ректального введения, такие как суппозитории или удерживаемые клизмы, например, содержащие обычные основы для суппозиториев, такие как масло какао или другие глицериды.
В дополнение к препаратам, описанным выше, данные соединения можно также переработать в такие препараты, как депо-препарат. Такие длительно действующие препараты можно вводить путем имплантации (например, подкожно или внутримышечно) или путем внутримышечной инъекции. Так, например, с данными соединениями могут быть изготовлены препараты с подходящими полимерными или гидрофобными материалами (например, в виде эмульсии в приемлемом масле) или ионообменными смолами, или в виде труднорастворимых производных, например, в виде труднорастворимой соли.
Фармацевтическим носителем для гидрофобных соединений является система сорастворителей, содержащая бензиловый спирт, неполярное поверхностно-активное вещество, смешиваемый с водой органический полимер и водную фазу. Система сорастворителей может быть VPD системой сорастворителей. VPD является раствором 3% в/о бензилового спирта, 8% в/о неполярного поверхностно-активного вещества, полисорбата 80 и 65% в/о полиэтиленгликоля 300, с доведением до объема, приготовленном в абсолютном этаноле. Система сорастворителй VPD (VPD:5W) содержит VPD, разведенный 1:1 5% раствором глюкозы в воде. В этой системе сорастворителей хорошо растворяются гидрофобные соединения и она сама дает слабую токсичность при системном введении. Естественно, соотношения в системе сорастворителей могут значительно изменяться без нарушения ее характеристик по способности растворения и токсических свойств. Кроме того, вид компонентов сорастворителей может меняться: например можно использовать другие неполярные малотоксичные поверхностно-активные вещества вместо полисорбата 80; можно изменять размер фракции полиэтиленгликоля; можно заменять полиэтиленгликоль другими биосовместимыми полимерами, например поливинилпирролидоном; и декстрозу можно заменять другими сахарами или полисахаридами.
Альтернативно можно применять другие системы доставки гидрофобных фармацевтических соединений. Липосомы и эмульсии являются известными примерами носителей или основ для доставки гидрофобных лекарственных веществ. Можно также использовать некоторые органические растворители, такие как диметилсульфоксид, хотя обычно ценою большей токсичности. Кроме того, соединения можно доставлять, используя систему с длительным высвобождением, такую как полупроницаемые матрицы из твердых гидрофобных полимеров, содержащих терапевтическое средство. Были созданы различные длительно высвобождающие материалы и они известны специалистам. Капсулы с длительным высвобождением могут в зависимости от их химической природы высвобождать данные соединения в течение нескольких недель, вплоть до свыше 100 дней. В зависимости от химической природы и биологической стабильности терапевтического средства можно применить дополнительные стратегии для стабилизации белка.
Фармацевтические композиции могут также содержать подходящие твердые или гелеобразные носители, или вспомогательные вещества. Примеры таких носителей или вспомогательных веществ включают карбонат кальция, фосфат кальция, сахара, разные виды крахмала, производные целлюлозы, желатин и полимеры, такие как полиэтиленгликоли.
IV. Способ использования соединений данного изобретения
Соединения данного изобретения пригодны для опосредования активности протеинкиназ. Более конкретно эти соединения полезны в качестве противоангиогенезных средств и в качестве средств модуляции и ингибирования активности протеинкиназ, такой как активность, связанная с комплексами VEGF, FGF, CDK, TEK, CHK1, LCK, FAK и фосфорилазкиназой среди прочего, обеспечивая таким образом лечение рака и других заболеваний, связанных с клеточной пролиферацией, опосредуемой протеинкиназами у млекопитающих, включая людей.
Терапевтически эффективное количество веществ данного изобретения может вводиться обычно в форме фармацевтической композиции для лечения заболеваний, опосредуемых модуляцией или регуляцией протеинкиназ. «Эффективное количество», как подразумевается, означает, то количество вещества, которое при введении млекопитающему, нуждающемуся в таком лечении, является достаточным, чтобы осуществить лечение заболевания, опосредуемого активностью одной или более из протеинкиназ, таких как тирозинкиназы. Таким образом, терапевтически эффективное количество соединения данного изобретения является количеством, достаточным для модуляции, регуляции или ингибирования активности одной или более протеинкиназ, так что болезненное состояние, которое опосредуется этой активностью, снижается или облегчается. Эффективное количество данного соединения будет меняться в зависимости от таких факторов, как болезненное состояние и его тяжесть и вид, и состояния (например, вес) млекопитающего, нуждающегося в лечении, но, тем не менее, может быть обычным образом определено специалистом в данной области. «Лечение», как подразумевается, означает, по меньшей мере, облегчение болезненного состояния у млекопитающих, такого как и у людей, на которое влияет, по меньшей мере, частично, активность одной или более протеинкиназ, таких как тирозинкиназы, и включает: профилактику возникновения болезненного состояния у млекопитающего, особенно, когда млекопитающее, как обнаружено, предрасположено к этому болезненному состоянию, но оно еще не выявлено; модуляцию и подавление болезненного состояния и/или облегчение состояния при заболевании. Примеры болезненных состояний включают диабетическую ретинопатию, неоваскулярную глаукому, ревматоидный артрит, псориаз, возрастную дегенерацию желтого пятна (ВДЖП; AMD) и рак (солидные опухоли).
Активность соединений данного изобретения в качестве модуляторов активности протеинкиназ, такой как активность киназ, может быть определена любым из методов, доступных специалистам в данной области, включая исследования in vivo и/или in vitro. Примеры подходящих исследований по определению активности включают исследования, описанные у Parast C. et al., BioChemistry, 37, 16788-16801 (1998); Jeffry et al., Nature, 376, 313-320 (1995); WIPO International Publication No. WO 97/34876; и WIPO International Publication No. WO 96/14843.
V. Примеры
Следующие примеры даны для иллюстрации данного изобретения, но не должны рассматриваться как ограничения данного изобретения. Если не указано иначе, все температуры представлены в градусах Цельсия, и все части и проценты являются весовыми. Данные ВЭЖХ получены с использованием Hewlett Packard HP-1100 HPLC.
Пример 1
Полиморфная форма I
Из неочищенного вещества после синтеза (155 мг) соединения формулы I готовили густую суспензию в 5 мл этанола и затем нагревали с обратным холодильником в течение 30 мин. Образцу давали медленно остыть до 23°С. Твердые вещества собирали фильтрованием и сушили при 85°С под высоким вакуумом. Форму I подтверждали рентгеновской дифракцией, и чистота по ВЭЖХ составляла >98%.
Пример 2
Полиморфная форма II
Форму I из примера 1 растворяли в тетрагидрофуране при 60°С, а затем перекристаллизовывали путем постепенного добавления гексанов с получением формы II. Форму II подтверждали рентгеновской дифракцией (чистота по ВЭЖХ >98%).
Пример 3
Полиморфная форма III
Из формы I из примера 1 готовили густую взвесь в легком минеральном масле при 192°С и взбалтывали в течение 1 часа, а затем охлаждали до комнатной температуры. Твердые вещества собирали фильтрованием, промывали гексаном и затем сушили при 50°С под вакуумом. Форму III подтверждали рентгеновской дифракцией (чистота по ВЭЖХ >97%).
Пример 4
Полиморфная форма IV
Неочищенное вещество после синтеза соединения формулы I растворяли в этилацетате и этаноле. Перекристаллизацию выполняли добавлением NaHCO3:воды 1:1. Форму IV подтверждали рентгеновской дифракцией (чистота по ВЭЖХ >99%).
Пример 5
Полиморфная форма V
Твердое вещество формы IV из примера 4 суспендировали в тяжелом минеральном масле при 130°С и затем готовили густую суспензию при 180°С в течение полутора часов. Твердые вещества собирали фильтрованием, промывали гексаном и затем сушили под вакуумом. Форму V подтверждали рентгеновской дифракцией (чистота по ВЭЖХ >99%).
Пример 6
Полиморфная форма Ia
Из формы I из примера 1 готовили густую суспензию в воде (примерно 20-40 мг/мл) и взбалтывали при комнатной температуре в течение семи дней с получением формы Ia. Форму Ia подтверждали рентгеновской дифракцией (чистота по ВЭЖХ >99%).
Пример 7
Полиморфная форма Ib
Из формы I из примера 1 готовили густую суспензию в воде (примерно 20-40 мг/мл) и взбалтывали при 90°С в течение трех дней с получением формы Ib. Альтернативно форму Ib получали кристаллизацией из этанола:воды при 65°С. Форму Ib подтверждали рентгеновской дифракцией (чистота по ВЭЖХ >99%).
Пример 8
Полиморфная форма IIa
Из формы II из примера 2 готовили густую суспензию в воде (примерно 20-40 мг/мл) и взбалтывали при комнатной температуре в течение семи дней с получением формы IIa. Форму IIa подтверждали рентгеновской дифракцией (чистота по ВЭЖХ >99%).
Пример 9
Полиморфная форма IIb
Из формы II из примера 2 готовили густую суспензию в воде (примерно 20-40 мг/мл) и взбалтывали при 90°С в течение трех дней и затем при комнатной температуре в течение 17 дней с получением формы IIb. Форму IIb подтверждали рентгеновской дифракцией.
Пример 10
Полиморфная форма IIIa
Форму III из примера 3 помещали в условия 93% относительной влажности при комнатной температуре на десять дней и готовили густую суспензию в воде (примерно 20-40 мг/мл) и взбалтывали при комнатной температуре в течение семи дней с получением формы IIIa. Форму IIIa подтверждали рентгеновской дифракцией.
Пример 11
Полиморфная форма IIIb
Форму IIIa из примера 10 сушили при 50°С под вакуумом с получением формы IIIb. Форму IIIb подтверждали рентгеновской дифракцией.
Пример 12
Полиморфная форма IVa
Из формы IV из примера 4 готовили густую суспензию в воде (примерно 20-40 мг/мл) и взбалтывали при комнатной температуре в течение семи дней с получением формы IVa. Форму IVa подтверждали рентгеновской дифракцией и DSC.
Пример 13
Полиморфная форма Va
Из формы V из примера 5 готовили густую суспензию в воде (примерно 20-40 мг/мл) и взбалтывали при комнатной температуре в течение семи дней с получением формы Va. Форму Va подтверждали рентгеновской дифракцией.
Пример 14
Полиморфная форма VI
Форму Ib из примера 7 нагревали при 140°С в течение 10 минут с получением формы VI. Форму VI подтверждали рентгеновской дифракцией.
Пример 15
Аморфная форма
Аморфную форму получали путем разбавления в воде (примерно в отношении 1:10), при добавлении каплями соединения формулы I в растворе в полиэтиленгликоле 400 или получали выпариванием в роторном испарителе раствора соединения формулы I в метаноле или ТГФ, или получали лиофилизацией раствора соединения формулы I в т-бутаноле.
Пример 16
Полиморфная форма Ibm
Форму Ib из примера 7 нагревали при 50°С под вакуумом с получением формы Ibm-2, которая, как подтверждали рентгеновской дифракцией, являлась смесью формы Ib и формы VI полиморфа.
Пример 17
Применение Полиморфной формы Ib в препарате гиалуронатной суспензии
Гиалуронат натрия (1% вес/вес) растворяли в изотоническом буферном растворе фосфата натрия с рН 7,4, содержащем 0,85% хлорида натрия, 0,022 двухзамещенного фосфата натрия, 0,004% однозамещенного фосфата натрия и 97,15% воды с образованием вязкого раствора. Раствор затем стерилизовали фильтрованием. Затем добавляли микронизированную и стерилизованную форму Ib из примера 7 (0,1-1,0% вес/вес) с образованием гомогенной суспензии при помощи мягкого перемешивания лопастной мешалкой.
Пример 18
Применение полиморфной формы Ib в препарате суспензии с КМЦ
Натрийкарбоксиметилцеллюлозу (КМЦ) (0,5% вес/вес) растворяли в воде и затем стерилизовали фильтрованием. Затем добавляли соответствующее количество формы Ib из примера 7 (0,1-1,0% вес/вес) с образованием гомогенной суспензии взвихриванием и обработкой ультразвуком в течение до 10 минут.
Многие модификации и другие воплощения данного изобретения придут на ум специалисту в области, к которой принадлежит данное изобретение, обладающие преимуществами идей представленного выше описания. Поэтому должно быть понятно, что данное изобретение нельзя ограничивать описанными конкретными воплощениями, и что модификации и другие воплощения, как подразумевается, включены в объем прилагаемой формулы изобретения. Хотя здесь используются специфические термины, они используются только в общем и описательном смысле, а не в целях ограничения.
Изобретение представляет несколько полиморфных форм и аморфную форму {2-фтор-5-[3-(Е))-2-пиридин-2-илвинил)-1Н-индазол-6-иламино]фенил}амида 2,5-диметил-2Н-пиразол-3-карбоновой кислоты, фармацевтическую композицию, содержащую такие полиморфные или аморфные формы и способы использования таких фармацевтических композиций для лечения болезненных состояний, опосредуемых протеинкиназами, таких как рак и другие болезненные состояния, связанные с нежелательным ангиогенезом и/или клеточной пролиферацией, а также способ модуляции активности рецепторов протеинкиназы на основе полиморфных форм. Технический результат - получены полиморфные формы {2-фтор-5-[3-(Е))-2-пиридин-2-илвинил)-1Н-индазол-6-иламино]фенил}амида 2,5-диметил-2Н-пиразол-3-карбоновой кислоты, обладающие улучшенной растворимостью и биодоступностью при пероральном приеме. 20 н. и 2 з.п. ф-лы, 16 ил.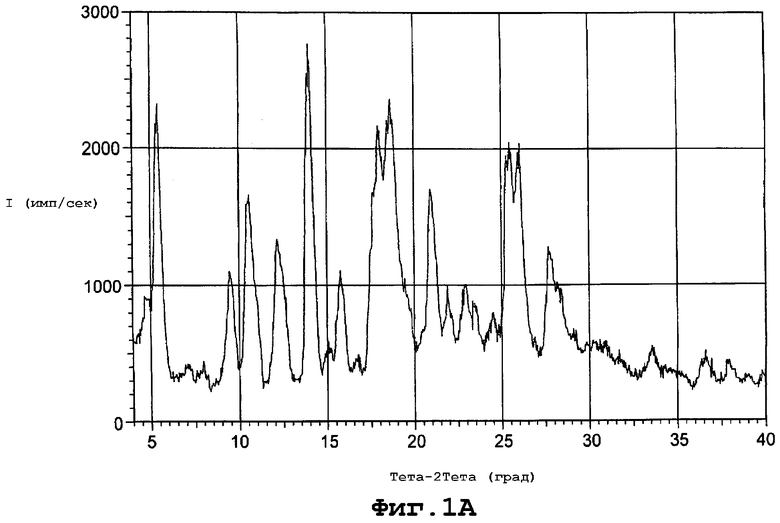
23 Способ по п.22, где рецептор протеинкиназы представляет собой рецептор VEGF.
| US 6531491 В1, 11.03.2003 | |||
| RU 2001124816 А, 20.06.2003. |
Авторы
Даты
2008-05-20—Публикация
2005-03-04—Подача