ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к устройству для латерально-диагонально-потокового многопараметрического анализа, в частности, в области иммуногематологии и серологии инфекционных заболеваний, предназначенному для одновременного качественного или количественного определения нескольких аналитов в одной жидкой пробе, которое содержит, по меньшей мере, одну мембрану с загрузочной зоной для нанесения жидкой пробы, по меньшей мере, две индикаторные зоны, которые могут вступать во взаимодействие с аналитом (или аналитами), и, по меньшей мере, одну абсорбционную зону, которая поглощает жидкость после ее прохождения через индикаторные зоны, причем индикаторные зоны находятся между загрузочной зоной и абсорбционной зоной; устройство отличается тем, что направления потоков от загрузочной зоны через соответствующие индикаторные зоны к абсорбционной зоне (дорожки) практически параллельны, и имеется, по меньшей мере, две различные дорожки.
Изобретение далее относится к способу определения нескольких аналитов в одной жидкой пробе, который включает в себя нанесение пробы на загрузочную зону мембраны устройства согласно настоящему изобретению, при этом количество пробы достаточно для того, чтобы обеспечить течение жидкости по направлению к абсорбционной зоне через индикаторные зоны и обеспечить возможность образования аналитами или их производными, содержащимися в жидкости пробы, комплексов в индикаторных зонах, в частности, для одновременного определения параметров клеток и плазмы, предпочтительно для одновременного проведения определения группы крови, серологического перекрестного контроля (перекрестной пробы сыворотки) и/или анализа для выявления антител; для одновременного проведения определения группы крови и определения серологических маркеров инфекционных заболеваний, имеющих значение при трансфузиях, а также для одновременного проведения определения группы крови и определения антител к другим клеткам крови, отличающимся от эритроцитов, в частности антител к тромбоцитам и антител к лимфоцитам.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Как известно, для того, чтобы предупредить риски осложнений, например, при переливании крови, в особенности риски несовместимости групп крови и заражения вирусами и/или бактериями, проводятся различные лабораторные анализы крови доноров и пациентов для получения компонентов крови, серологически и по группе крови совместимых с кровью реципиентов и не содержащих известных передаваемых патогенов. Существующие серологические тесты, как правило, включают в себя определение групп крови донора и реципиента, в частности определение групп крови по системе групп крови АВ0, определение резус-фактора и Келл-фактора, перекрестную пробу сывороток донора и реципиента, анализы на антитела для выявления регулярных антител у донора и реципиента, а также идентификацию антител реципиента при наличии нерегулярных антител. Также в связи с трансфузиями и трансплантациями проводят выявление антител к тромбоцитам и/или лимфоцитам.
Серологические анализы для выявления маркеров инфекционных заболеваний у донора, как известно, включают в себя стандартное определение антител, в частности антител к ВИЧ-1, ВИЧ-2, к HCV (вирусу гепатита С), к Treponema pallidum (возбудителю сифилиса), а также определение поверхностного антигена гепатита В (=HBsAg: поверхностный антиген гепатита В).
В ходе серологической диагностики групп крови обычно выявляют параметры, имеющие особое значение в связи с трансфузиями или геморрагической болезнью новорожденных (Morbus Hamoliticum Neonatorum; MHN; ГБН). При этом речь идет, среди прочего, о выявлении на поверхности эритроцитов тех антигенов, которые характерны для групп крови (определение группы крови). Другие важные системы антигенов находятся на тромбоцитах, гранулоцитах, лимфоцитах, которые также играют роль при трансфузии и трансплантации. При различии антигенов тромбоцитов и гранулоцитов у матери и плода у новорожденных могут возникнуть клинические картины болезни, сходные с ГБН. Далее речь идет о выявлении регулярных групповых антител (изоагглютининов) и нерегулярных групповых антител в сыворотке или плазме.
Изоагглютинины или регулярные антитела вырабатываются у всех людей вскоре после рождения и соответствуют группе крови АВ0-системы. Они направлены против тех антигенов А или В группы крови, которые отсутствуют у самих индивидуумов, то есть у людей с группой крови А имеются антитела к антигену В, у людей с группой крови В - антитела к антигену А, у людей с группой крови 0 имеются антитела к антигену А и к антигену В; у людей с группой крови АВ изоагглютининов нет. Регулярные антитела также называют полными антителами, поскольку они могут прямо агглютинировать эритроциты в NaCl-среде.
Нерегулярные, или аллоантитела, в отличие от изоагглютининов, вырабатываются при последующих иммунизациях, прежде всего - при переливании крови или беременности. Поэтому у большинства людей нет нерегулярных групповых антител. Нерегулярные антитела, связанные с переливанием крови, как правило, реагируют на тепло и относятся преимущественно к классу IgG. В отличие от регулярных антител они не способны вызывать прямую агглютинацию эритроцитов в NaCl-среде.
Как известно, для определения группы крови эритроциты исследуемого человека (донора или реципиента) соединяют с реактивами, которые содержат антитела, специфичные для групп крови. Обычно речь идет об анализах в жидких средах, при которых исследуемую смесь получают посредством смешивания пробы, содержащей эритроциты, с пробой, содержащей антитела к определенному признаку группы крови. Затем исследуемую смесь инкубируют в течение определенного периода времени в определенных условиях, а после завершения инкубации, сразу же или после этапа центрифугирования, визуально или с использованием оптических способов проверяют на наличие вероятной агглютинации или адсорбции эритроцитов. Преобладающим измерением конечной точки в серологии групп крови по-прежнему является гемагглютинация. Для каждой определяемой группы крови необходимо пипеткой нанести специальную смесь, то есть, например, для определения 9 важнейших групп крови А, В, D, С, с, Е, е, Cw и K необходимо, без учета контроля, 9 отдельных образцов.
Для перекрестной пробы сыворотки, как известно, используют реакции клеток с известной АВ0-группой крови (А1, А2, В, 0), которые инкубируют с сывороткой или плазмой исследуемого человека. После этапа центрифугирования визуально или с помощью оптических способов проверяют возможную агглютинацию эритроцитов. Для перекрестной пробы сыворотки с 4 указанными тестовыми клетками обычно необходимо нанести пипеткой 4 образца.
Для выявления нерегулярных антител, как известно, используют панель, обычно состоящую из 2 или 3 образцов клеток группы крови 0, объединенный профиль антигенов которых содержит важнейшие антигены, прежде всего антигены, относящиеся к системам групп крови Rh, Келла, Даффи, Кидда, MNS, Р, Левиса, Лютерана. Клеточный реагент соединяют с сывороткой или плазмой исследуемого человека, инкубируют и, после этапа центрифугирования, визуально или с помощью оптических способов проверяют возможную агглютинацию эритроцитов. Для определения в одной пробе пациента необходимо пипеткой нанести 2-3 образца.
Для идентификации нерегулярных антител, которую, как правило, проводят после позитивного анализа для выявления антител, используют панель, состоящую из 16 видов клеток группы крови 0, профиль антигенов которых включает важнейшие антигены, прежде всего антигены, относящиеся к системам групп крови Rh, Келла, Даффи, Кидда, MNS, Р, Левиса, Лютерана, в точно определенном соотношении. Клеточный реагент соединяют с сывороткой или плазмой исследуемого человека, инкубируют и визуально или с помощью оптических способов проверяют возможную агглютинацию эритроцитов. Для определения в одной пробе пациента необходимо пипеткой нанести до 16 образцов.
Так как основные нерегулярные антитела, имеющие отношение к трансфузии, относятся к IgG-типу и поэтому являются неполными, как правило, для того, чтобы иметь возможность обнаружить в качестве конечной точки гемагглютинацию, необходимо усиливать вышеописанные реакции, используемые для их выявления и идентификации. Наиболее широко используемым для этого реагентом является реагент, содержащий поликлональные антитела к гемоглобину человека, к которому часто добавляют антитела к комплементу (в типичном случае - антитела к C3d и/или к C3b).
Наиболее часто используемым способом выявления антител к тромбоцитам является так называемый MAIPA-тест (иммобилизация моноклональных антител на антигенах тромбоцитов). При этом исследуемые тромбоциты инкубируют с исследуемой сывороткой. После стадии промывки их инкубируют с моноклональным антителом, например специфическим антителом мыши к определенному гликопротеину тромбоцитов. Затем тромбоциты лизируют и разбавленный лизат переносят в реакционную лунку планшета для микротитрования, покрытую, например, антителами козы к антителам мыши. Антитело козы к антителам мыши связывает антитело мыши и связанный с ним комплекс тромбоцитарного гликопротеина и антитела человека. Антитело человека выявляют посредством добавления конъюгированного с ферментом антитела козы к IgG человека.
С помощью стандартных диагностических анализов можно определять либо клеточные, либо плазматические параметры. Для определения параметров составных частей крови первоначально необходимо разделить клетки и плазму.
Анализы с латеральными (поперечными) потоками в настоящее время часто используются в качестве экспресс-анализов, например в качестве тестов на беременность, для определения маркеров инфекционных заболеваний или для скрининга на наркотики. Оборудование для анализа с латеральными потоками состоит, как известно, из твердого носителя, на котором имеется загрузочная зона, куда наносят исследуемую пробу, разделительная мембрана, с которой соединены связывающие элементы, например акцепторные антитела или антигены, и на которой удается обнаружить реакции связывания, и поглощающая абсорбционная зона, которая вынуждает исследуемую пробу прямолинейно протекать через разделительную мембрану.
Стандартные тесты с латеральными потоками на испытательных мембранах описаны, как правило, с разделением, напоминающим хроматографическое. Аналит, содержащийся в пробе, специфически связывается с фиксированными на мембране связывающими элементами, которые, как правило, образуют расположенные друг за другом или накладывающиеся друг на друга ряды индикаторных зон. Образующийся в результате связывания комплекс становится видимым за счет индикаторных частиц, которые, как правило, уже присутствуют в сухом виде в определенном порядке на подушечке для высвобождения конъюгата. Подушечка для высвобождения конъюгата расположена между загрузочной зоной и мембраной. Предварительно нанесенные цветные индикаторные частицы покрыты, например, антителом к выявляемому аналиту.
Стандартным форматом анализа с боковыми потоками является так называемый «сэндвич-анализ», при котором как индикаторная зона, так и индикаторные частицы покрыты лигандами, ориентированными на определяемые аналиты, обычно антителами. При этом лиганд (связывающий элемент) иммобилизован на мембране. Реактив-детектор, обычно антитело, связанное с окрашенной полистирольной частицей или коллоидными металлами, депонирован в подушечке для высвобождения конъюгата и может оттуда вымываться. Этот комплекс служит индикаторной частицей. После нанесения пробы, подлежащей исследованию, она очень быстро увлажняет подушечку для высвобождения конъюгата, за счет чего индикаторные частицы мобилизируются. Индикаторные частицы мигрируют вместе с фронтом жидкости вдоль пористой мембраны. Находящийся в пробе аналит связывается антителом, которое находится на поверхности индикаторной частицы. Когда проба проходит через индикаторную зону, комплекс аналита и индикаторной частицы иммобилизуется в индикаторной зоне за счет реакции аналита с антителом, связанным в индикаторной зоне, что ведет к появлению видимого сигнала.
Следующим известным форматом анализа на мелкие аналиты с одной антигенной детерминантой, не способные связывать одновременно два антитела, является так называемый «конкурентный анализ». Связанный с поверхностью индикаторной частицы реагент-детектор в норме является молекулой, идентичной или аналогичной аналиту. Индикаторные частицы депонированы в подушечке для высвобождения конъюгата. Индикаторные частицы мигрируют вместе с фронтом жидкости вдоль пористой мембраны. Когда проба, содержащая аналит, и индикаторные частицы (которые также эффективно захватывают аналит) проходят через индикаторную зону, связывается часть молекул аналита, содержащихся в пробе, и часть индикаторных частиц. Чем больше аналита содержится в пробе, тем эффективнее он конкурирует за связывание с индикаторными частицами, и тем слабее становится сигнал.
Как известно, эти индикаторные частицы преимущественно состоят из коллоидного золота или из полистирола, которые получают способами, известными в данной области техники, и на которые наносят покрытие. В типичных форматах анализов с латеральными потоками аналиты определяют непрямыми способами. Под прямым определением аналита в контексте настоящего изобретения понимают, что аналит уже связан с индикаторной частицей (например, эритроцитом) естественным образом. В наиболее употребительном случае непрямого определения аналита проба, подлежащая анализу, содержит, как правило, в качестве аналитов не связанные с клетками, например плазматические, компоненты, и кроме пробы, подлежащей анализу, необходимы два реагента, а именно индикаторная частица и связывающий элемент. При непрямом определении аналит сначала связывается с выделившимися из подушечки для высвобождения конъюгата индикаторными частицами, после чего этот комплекс в ходе второй реакции со связывающим элементом иммобилизуется в индикаторных зонах.
При проведении стандартных анализов с латеральными потоками, в которых в качестве индикаторных частиц использовались эритроциты, связанные с аналитами, подлежащими определению, например с антигенами, специфичными для групп крови, до сих пор в индикаторных зонах антитела к соответствующим групповым антигенам, выполнявшие роль связывающих элементов, располагали в расположенных друг за другом или накладывающихся друг на друга полосах только в одной проточной дорожке, например анти-А и анти-В антитела к групповым антигенам А или В или антитела к антигену Rh-системы групп крови. При этом стандартные анализы с латеральными потоками обладают недостатком, состоящим в том, что эритроциты, связавшиеся с антителами, образуют барьер для потока других аналитов, подлежащих определению в данной пробе, например для других связанных с клетками антигенов. Из-за агглютинации или адсорбции клеток в полосах связывающих элементов, расположенных проксимально к загрузочной зоне, другие аналиты, в особенности клетки или фрагменты клеток, содержащиеся в пробе, подлежащей исследованию, невозможно беспрепятственно и явно разделить, и вследствие этого невозможно однозначно или полностью доказать их присутствие. Это может привести, например, у пациента с АВ Rh-позитивной D группой крови к ослаблению или устранению В- и D-полос, что может привести к неправильной интерпретации его группы крови как А Rh-отрицательной. Поэтому до сих пор в серологической диагностике групп крови намеренно не использовали анализы с латеральными потоками с более чем одной индикаторной зоной. Для измерения нескольких, в особенности клеточных и плазматических, параметров групп крови до сих пор нужно было проводить раздельные анализы отдельных параметров.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Задача изобретения состоит в том, чтобы преодолеть недостатки, существующие на современном уровне техники, прежде всего недостатки стандартных анализов с латеральными потоками, в которых используют расположенные друг за другом или накладывающиеся друг на друга индикаторные зоны, или зоны обнаружения, для одновременного измерения различных параметров пробы, более конкретно клеточных и плазматических параметров.
Эта задача согласно настоящему изобретению достигнута за счет устройства для одновременного качественного или количественного определения одного или нескольких аналитов в жидкой пробе или в нескольких жидких пробах, которое содержит, по меньшей мере, одну мембрану, содержащую загрузочную зону для нанесения жидкой пробы, по меньшей мере, одну группу индикаторных зон, состоящую, по меньшей мере, из двух индикаторных зон, которые могут взаимодействовать с аналитом или аналитами, и абсорбционную зону, которая поглощает жидкость после того, как она проходит через индикаторные зоны, причем индикаторные зоны расположены между загрузочной зоной и абсорбционной зоной;
это устройство отличается тем, что направления потоков от загрузочной зоны через соответствующие индикаторные зоны одной группы к абсорбционной зоне, которые представляют собой проточные дорожки, практически параллельны, и имеется, по меньшей мере, две различные дорожки.
Индикаторные зоны устройства согласно настоящему изобретению расположены на мембране и содержат связывающие элементы, которые захватывают или присоединяют к себе содержащиеся в пробе аналиты, подлежащие определению. В индикаторных зонах обнаруживаются реакции соединения между аналитом и связывающим элементом. В качестве особо предпочтительных связывающих элементов на пористую мембрану наносят антитела или фрагменты антител, лектины, антигены или эпитопы антигенов и/или клетки или фрагменты клеток. Каждая индикаторная зона предпочтительно содержит один элемент, связывающий один из исследуемых аналитов.
В одной из форм осуществления настоящего изобретения индикаторные зоны расположены так, что жидкость пробы при движении по проточной дорожке протекает не более чем через одну индикаторную зону. Например, индикаторные зоны могут быть расположены на мембране со смещением. При этом индикаторные зоны предпочтительно расположены в диагональном ряду, идущем от проксимальной стороны к дистальной или наоборот. Особые конструктивные решения являются V-образными, W-, М- или N-образными или перевернутыми V-образными, W-, М- или М-образными. В еще одной форме осуществления индикаторные зоны расположены параллельно рядом друг с другом в виде линейного ряда.
Только использование смещенных индикаторных зон с латеральным расположением обеспечивает возможность проведения мультипараметрического анализа с использованием в качестве индикаторных частиц эритроцитов. Особо предпочтительная форма осуществления с диагональным расположением обладает преимуществом, состоящим в том, что на устройство согласно настоящему изобретению можно нанести особенно практичную и легко читаемую маркировку результатов; так как каждый параметр, подлежащий определению, занимает определенное Х- или Y-положение, можно рассматривать устройство согласно настоящему изобретению как систему координат с ординатой (плоскость проточных дорожек) и абсциссой (плоскость загрузочной зоны).
В следующей форме осуществления изобретения более одного ряда индикаторных зон предпочтительно расположены диагонально от проксимальной стороны к дистальной или наоборот или, например, также V-образно, W-, М- или N-образно или в виде перевернутых букв V, W, М или N, в направлении течения друг за другом и/или со смещением вбок, и индикаторные зоны различных рядов либо разделены промежутками, так что жидкость пробы по каждой дорожке может протечь не больше чем через одну индикаторную зону, либо не разделены промежутками, так что жидкость пробы по каждой проточной дорожке может протечь больше чем через одну индикаторную зону.
Более одного ряда индикаторных зон, например два ряда индикаторных зон, на различном расстоянии от загрузочной зоны особо предпочтительно иметь тогда, когда в одной пробе цельной крови необходимо определить клеточные и плазматические параметры. В одной из форм осуществления изобретения, например при анализе с использованием в качестве пробы цельной крови, связывающие элементы выбирают так, что содержащиеся в плазме аналиты, например все виды антител, которые протекают в устройстве от загрузочной зоны к абсорбционной зоне через индикаторные области, связываются связывающими элементами в ряду индикаторных зон, расположенном проксимально по отношению к загрузочной зоне (т.е. вблизи нее). Связывающие элементы для выявления аналитов, связанных с клетками, например эритроцитарных антигенов, напротив, выбирают так, чтобы они связывались со связывающими элементами в ряду индикаторных зон, расположенных дистально по отношению к загрузочной зоне (т.е. в удалении от нее). При этой предпочтительной форме осуществления настоящего изобретения, кроме эритроцитов, предпочтительно используют дополнительный вид индикаторных частиц, предпочтительно изготовленных из коллоидного золота или полистирола, или фиксированные эритроциты. Эти индикаторные частицы, в частности, используют для того, чтобы выявить аналиты, не связанные с эритроцитами, например свободные антитела плазмы, в виде комплекса в индикаторной зоне. Если, например, используют два вида индикаторных частиц, один из которых не является эритроцитами, индикаторные зоны обоих рядов могут быть не разделены промежутками, или они могут быть расположены друг за другом в одной проточной дорожке. Предпочтительным при этом является такое расположение, при котором аналиты, определяемые в плазме, выявляются в проксимальных индикаторных зонах, а аналиты, связанные с эритроцитами, выявляются в дистальных индикаторных зонах. В форме осуществления настоящего изобретения с более чем одним рядом индикаторных зон, описанной ранее, где связывающие элементы каждого ряда реагируют или связываются с эритроцитами, являющимися индикаторными частицами, ряды индикаторных зон разделены промежутками или не расположены последовательно в одной проточной дорожке.
В следующей и особо предпочтительной форме осуществления настоящего изобретения более одного ряда индикаторных зон, предпочтительно в виде диагональных рядов, идущих по диагонали от проксимальной стороны к дистальной или наоборот, или в виде V-образных, W-, М- или М-образных рядов или рядов, имеющих форму перевернутых букв V, W, М или N, или, например, в виде рядов, идущих параллельно друг другу со смещением, расположены с двух сторон (например, под углом 180°) от центральной загрузочной зоны. Такое расположение выгодно, прежде всего, в том случае, если в пробе цельной крови необходимо определить клеточные и плазматические параметры.
В одной из форм осуществления настоящего изобретения, например в анализе с использованием в качестве пробы цельной крови, связывающие элементы выбраны так, что аналиты, содержащиеся в плазме, например каждый вид антител, которые проходят через устройство от загрузочной зоны к абсорбционной зоне через индикаторные зоны, связываются со связывающими элементами ряда индикаторных зон, расположенного с одной стороны загрузочной зоны. Связывающие элементы для выявления аналитов, связанных с клетками, например эритроцитарных антигенов, напротив, выбирают так, чтобы эти аналиты связывались связывающими элементами в ряду индикаторных зон, расположенных с противоположной стороны от загрузочной зоны. В этой предпочтительной форме осуществления настоящего изобретения, кроме эритроцитов, используют другие сорта индикаторных частиц, предпочтительно состоящих из коллоидного золота или полистирола. Эти индикаторные частицы, в частности, используют для того, чтобы выявить в индикаторной зоне в виде комплекса аналиты, не связанные с эритроцитами, например свободные антитела плазмы.
В предпочтительной форме осуществления изобретения загрузочная зона содержит две различные мембраны различной пористости. В этой предпочтительной форме осуществления настоящего изобретения, кроме эритроцитов, предпочтительно используют другие сорта индикаторных частиц, предпочтительно состоящих из коллоидного золота или полистирола. Эти индикаторные частицы, в частности, используют для того, чтобы выявить в индикаторной зоне в виде комплекса аналиты, не связанные с эритроцитами, например свободные антитела плазмы.
В предпочтительной форме осуществления изобретения загрузочная зона, кроме того, содержит две различные мембраны различной пористости. В этой предпочтительной форме осуществления изобретения, кроме эритроцитов, предпочтительно используют другие сорта индикаторных частиц, предпочтительно состоящих из коллоидного золота или полистирола. Эти индикаторные частицы, в частности, используют для того, чтобы выявить в индикаторной зоне в виде комплекса аналиты, не связанные с эритроцитами, например свободные антитела плазмы.
В особо предпочтительной форме осуществления изобретения загрузочная зона содержит одну мембрану или две мембраны различной пористости. Кроме того, одна из двух мембран содержит подушечку с конъюгатом, которая расположена между уплотнителем и индикаторными зонами. В этой предпочтительной форме осуществления изобретения, кроме эритроцитов, предпочтительно используют другие сорта индикаторных частиц, предпочтительно состоящих из коллоидного золота или полистирола. Эти индикаторные частицы, в частности, используют для того, чтобы выявить в индикаторной зоне в виде комплекса аналиты, не связанные с эритроцитами, например свободные антитела плазмы. Этот другой сорт индикаторных частиц, используемый в дополнение к эритроцитам, предпочтительно содержится в подушечке с конъюгатом в сухом виде. Кроме того, подушечка с конъюгатом служит для того, чтобы замедлить течение эритроцитов. Это приводит к тому, что при двустороннем расположении относительно одной общей загрузочной зоны в одном направлении создаются условия, оптимизированные для выявления клеточных свойств, а в другом направлении - оптимизированные условия для выявления плазматических свойств.
С использованием устройства согласно настоящему изобретению выполняют анализ с латеральным потоком, более конкретно серологическую диагностику групп крови, в котором в качестве индикаторных частиц используют эритроциты, и в одном испытательном устройстве можно одновременно определить несколько клеточных параметров, например эритроцитарные антигены или эпитопы антигенов, плазматические параметры и/или свойства клеток крови, более конкретно свойства составных частей цельной крови, в исследуемой пробе. Кроме того, таким образом получают наиболее простую в изготовлении и простую в обращении, более конкретно требующую малого числа серий опытов и не требующую подготовки пробы, а также требующую меньших затрат испытательную систему, с помощью которой можно одновременно определить различные клеточные параметры и/или плазматические параметры одной пробы или нескольких проб, подлежащих исследованию.
Эти преимущества устройство согласно настоящему изобретению обеспечивает в любой области медицинской диагностики, где необходимо одновременно определять различные клеточные параметры и плазматические параметры, особенно в области серологии групп крови и серологии инфекционных заболеваний, более конкретно для любой диагностики в рамках трансфузионной медицины, например для одновременного проведения определения группы крови, в ходе которого прежде всего определяют антигены, связанные с эритроцитами, или эпитопы антигенов, и перекрестной пробы сыворотки, в ходе которой прежде всего определяют регулярные антитела (изоагглютинины), и/или анализа на антитела, в ходе которого прежде всего определяют нерегулярные антитела, а также для одновременного проведения определения группы крови и определения важных при трансфузиях серологических маркеров инфекционных заболеваний, например антител к ВИЧ-1, ВИЧ-2, вирусу гепатита С, Treponema pallidum, а также поверхностного антигена вируса гепатита В (HBsAg), и для одновременного проведения определения группы крови и определения антител к другим клеткам крови, отличающимся от эритроцитов, более конкретно - антител к тромбоцитам и антител к лимфоцитам.
Для этого может быть использована кровь с антикоагулянтом или нативная цельная кровь, при этом перед определением нет необходимости обязательно отделять друг от друга эритроциты и фракцию сыворотки или плазмы. Определение может быть осуществлено в ручном формате, который не требует вообще никаких приборов (в том числе - электрического тока).
В предпочтительной форме осуществления устройства согласно настоящему изобретению индикаторные зоны, предпочтительно расположенные дистально относительно загрузочной зоны ряды индикаторных зон, содержат антитела, или фрагменты антител, или лектины, которые могут захватывать или связывать групповые антигены всех мыслимых систем групп крови, подлежащих определению, а значит - и несущие их клетки, содержащиеся в пробе крови. В качестве предпочтительных связывающих элементов в индикаторных зонах на пористой мембране, предпочтительно в ряду, расположенном дистально относительно других рядов индикаторных зон, используют антитела, фрагменты антител или лектины к антигенам или эпитопам антигенов, более конкретно относящихся к системам групп крови АВ0, Rh и Келла, например анти-А, анти-В, анти-D и анти-K. Предпочтительно в одной индикаторной зоне этого ряда индикаторных зон, предпочтительно в индикаторной зоне, расположенной дистально по отношению ко всем остальным индикаторным зонам этого ряда, помещают контрольный связывающий элемент (контроль = ctl), который посредством позитивной реакции подтверждает протекание пробы через индикаторные зоны. Контрольным связывающим элементом предпочтительно является поликлональное антиэритроцитарное антитело.
В этой предпочтительной форме осуществления устройства согласно настоящему изобретению в следующем, предпочтительно расположенном проксимально по отношению к загрузочной зоне, ряду индикаторных зон находятся антигены или эпитопы антигенов, которые захватывают или связывают регулярные антитела, содержащиеся в пробе. В качестве предпочтительных связывающих элементов на пористую мембрану наносят групповые антигены А1, А2, В, 0 или эпитопы этих антигенов, например эритроцитарные мембраны эритроцитов определенных групп крови (А1, А2, В, 0) или синтетически полученные вещества, характерные для групп крови. Предпочтительно в одной индикаторной зоне этого ряда индикаторных зон, предпочтительно в индикаторной зоне, расположенной дистально по отношению ко всем остальным индикаторным зонам этого ряда, помещают контрольный связывающий элемент (контроль = ctl), который посредством позитивной реакции подтверждает протекание пробы через индикаторные зоны. Контрольным связывающим элементом предпочтительно является антитело к IgG.
В этой предпочтительной форме осуществления устройство может содержать в дополнительном ряду индикаторных зон, предпочтительно расположенном проксимально по отношению к загрузочной зоне, антигены или эпитопы этих антигенов, которые захватывают или связывают нерегулярные антитела или их фрагменты в пробе. Для этого в качестве предпочтительных связывающих элементов на пористую мембрану наносят клеточные мембраны различных эритроцитарных препаратов нулевой группы крови, комбинированный антигенный профиль которых перекрывает (охватывает) те антигены, которые направлены против важнейших нерегулярных антител, существенных для переливания крови. Предпочтительно в одной индикаторной зоне этого ряда индикаторных зон, предпочтительно в индикаторной зоне, расположенной дистально по отношению ко всем остальным индикаторным зонам этого ряда, помещают контрольный связывающий элемент (контроль = ctl), который посредством позитивной реакции указывает протекание пробы через индикаторные зоны. Контрольным связывающим элементом предпочтительно является антитело к IgG.
В следующей предпочтительной форме осуществления устройства согласно настоящему изобретению индикаторные зоны, предпочтительно расположенные в дистальном по отношению к загрузочной зоне ряду индикаторных зон, содержат антитела, или фрагменты антител, или лектины, которые при определении группы крови могут захватывать или связывать антигены группы крови, подлежащие определению, и за счет этого связывать несущие их клетки, присутствующие в пробе. В качестве предпочтительных связывающих элементов в индикаторные зоны на пористой мембране, предпочтительно находящиеся в ряду, расположенном дистально по отношению к загрузочной зоне и другим рядам индикаторных зон, наносят антитела, или фрагменты антител, или лектины к антигенам или эпитопам антигенов системы групп крови АВ0, например анти-А, анти-В или анти-А и анти-В. Предпочтительно в одной индикаторной зоне этого ряда индикаторных зон, предпочтительно в индикаторной зоне, расположенной дистально по отношению ко всем остальным индикаторным зонам этого ряда, помещают контрольный связывающий элемент (контроль = ctl), который посредством позитивной реакции подтверждает протекание пробы через индикаторные зоны. Контрольным связывающим элементом предпочтительно является поликлональное антитело к эритроцитам.
В этой предпочтительной форме осуществления устройства согласно настоящему изобретению в еще одном ряду индикаторных зон, предпочтительно расположенном проксимально по отношению к загрузочной зоне, присутствуют мембраны тромбоцитов и/или лимфоцитов или составные части мембран в качестве связывающих элементов для выявления антитромбоцитарных/антилимфоцитарных антител.
В следующей предпочтительной форме осуществления устройства согласно настоящему изобретению индикаторные зоны, предпочтительно расположенные в дистальном по отношению к загрузочной зоне ряду индикаторных зон, содержат антитела, или фрагменты антител, или лектины, которые при определении группы крови могут захватывать или связывать антигены группы крови, подлежащие определению, и за счет этого связывать несущие их клетки, присутствующие в пробе. В качестве предпочтительных связывающих элементов в индикаторные зоны на пористой мембране, предпочтительно находящиеся в ряду, расположенном дистально по отношению к загрузочной зоне и другим рядам индикаторных зон, помещают антитела, или фрагменты антител, или лектины к антигенам или эпитопам антигенов системы групп крови АВ0, например анти-А, анти-В или анти-А и анти-В.
Предпочтительно в одной индикаторной зоне этого ряда индикаторных зон, предпочтительно в индикаторной зоне, расположенной дистально по отношению ко всем остальным индикаторным зонам этого ряда, помещают контрольный связывающий элемент (контроль = ctl), который посредством позитивной реакции подтверждает протекание пробы через индикаторные зоны. Контрольным связывающим элементом предпочтительно является поликлональное антитело к эритроцитам.
В этой предпочтительной форме осуществления устройства согласно настоящему изобретению в еще одном ряду индикаторных зон, предпочтительно расположенном проксимально по отношению к загрузочной зоне, присутствуют связывающие элементы для выявления инфекционных агентов, более конкретно полученные синтетическим путем пептиды или рекомбинантные антигены, экспрессированные с использованием рекомбинантных ДНК, которые включают в себя диагностически значимые последовательности поверхностных белков соответствующего маркера (обнаружение антител), или антитела, ориентированные против поверхностных белков инфекционных агентов (обнаружение антигенов).
При использовании устройства согласно настоящему изобретению для одновременного определения клеточных и плазматических параметров одной пробы не нужно раздельно наносить пипеткой образцы для каждого отдельного определения, а можно в одной пробе одновременно определить все желаемые параметры, более конкретно при одновременном проведении определения группы крови, перекрестной пробы сыворотки и/или анализа для выявления антител, или при одновременном проведении определения группы крови и определения значимых для трансфузии серологических маркеров инфекционных заболеваний, при этом определение группы крови можно сочетать с выявлением любого серологического маркера инфекционного заболевания, или при одновременном проведении определения группы крови и определения антител к другим клеткам крови, отличающимся от эритроцитов, более конкретно антител к тромбоцитам и антител к лимфоцитам.
Это обеспечивает исключительную рационализацию рабочих процессов. Кроме преимущества, состоящего в одновременном определении нескольких серологических параметров, следует назвать также практически полное исключение необходимости подготовки пробы, в отличие от стандартных анализов. Также значительно более удобным является считывание результатов, расположенных по диагонали. Например, с использованием устройства согласно настоящему изобретению можно в одном устройстве определять и считывать результаты определения группы крови, более конкретно АВ0-характеристик, перекрестной пробы сыворотки и анализа для выявления антител, или результаты определения группы крови, более конкретно АВ0-характеристик, и других иммуногематологических параметров, более конкретно антитромбоцитарных и/или антилимфоцитарных антител или их фрагментов, или результаты определения группы крови, более конкретно АВ0-характеристик, и серологических маркеров инфекционных заболеваний, более конкретно антител к бактериальным и/или вирусным факторам или их фрагментов или вирусных или бактериальных антигенов или эпитопов этих антигенов.
Двухмерное плоскостное представление результатов и стабильная конечная точка реакции благоприятствуют как считыванию результатов невооруженным глазом, так и автоматическому считыванию результатов с использованием общеупотребительных способов анализа изображений, например ПЗС-камер. Снижаются трудозатраты, даже при ручной обработке результатов. Устройство согласно настоящему изобретению также обеспечивает снижение загрязнения окружающей среды и экономические выгоды. Даже в экстренных ситуациях можно за короткое время в ходе одного единственного анализа провести, например, полное определение АВ0-группы крови, перекрестную пробу сыворотки и анализ для выявления нерегулярных антител или, например, полное определение АВ0-группы крови и определение серологических маркеров инфекционных заболеваний или определение антител к тромбоцитам/лимфоцитам.
С производственно-технической точки зрения конструкция с латерально-диагональными потоками обеспечивает значительные преимущества по сравнению с устройствами, соответствующими современному уровню техники, так как при этом значительно снижается расход используемых реагентов и обеспечивается определение нескольких исследуемых параметров, которые раньше определяли раздельно, в одном единственном устройстве.
С помощью устройства согласно настоящему изобретению выполняют анализ с латеральными потоками, более конкретно для иммуногематологической и инфекционно-серологической диагностики, в ходе которого в одном устройстве для проведения анализа одновременно можно определить в пробе, подлежащей анализу, несколько клеточных, более конкретно эритроцитарных, антигенов или эпитопов антигенов, плазматических параметров и/или свойств клеток крови, более конкретно составных частей цельной крови, для чего используют, по меньшей мере, два сорта индикаторных частиц, из которых, по меньшей мере, один сорт представляет собой эритроциты. Кроме того, таким образом обеспечивается максимально просто изготавливаемая и простая в эксплуатации, более конкретно из-за малого числа серий опытов и отсутствия необходимости в подготовке пробы, дешевая система для проведения анализов, с помощью которой можно одновременно в одной пробе определять различные клеточные параметры и/или плазматические параметры, более конкретно признаки группы крови, выявлять регулярные и нерегулярные антитела, антитела к тромбоцитам и/или лимфоцитам и/или серологические маркеры инфекционных заболеваний, в частности маркеры, имеющие значение в трансфузиологии.
Мембрана устройства согласно настоящему изобретению представляет собой пористую мембрану. Предпочтительными материалами для изготовления мембраны являются, например, нитроцеллюлоза (например UniSart производства компании Sartorius, HiFlow производства компании Millipore, Whatman, AE99 или FF85/100 производства компании Schleicher & Schuell), полиэтилен (Lateral Flo производства корпорации Porex) или нейлон (Novylon производства компании CUNO). Предпочтительно мембрана должна иметь поры как можно большего размера, так как высокая пористость мембран способствует проникновению в пористую структуру, например, клеточных компонентов пробы, подлежащей анализу, например эритроцитов. Особо предпочтительным является использование адсорбирующих мембран. Устройство согласно настоящему изобретению, тем не менее, не ограничивается этими свойствами. Предпочтительными являются все мембраны с высокой скоростью движения жидкости по капиллярам (капиллярной скоростью), при этом скорость движения жидкости по капиллярам - это время, которое требуется для того, чтобы раствор красителя прошел 40 мм по данной мембране. Особо предпочтительными являются мембраны со скоростью движения жидкости по капиллярам меньше 100.
В двусторонней форме осуществления изобретения с двумя различными мембранами одна из мембран предпочтительно имеет высокую скорость движения жидкости по капиллярам, предпочтительно меньше 100, а вторая мембрана предпочтительно имеет меньшую скорость движения жидкости по капиллярам, предпочтительно больше 100.
В предпочтительной форме осуществления изобретения за загрузочной зоной устройства согласно настоящему изобретению в направлении течения жидкости на пористой мембране размещают уплотнитель. Можно использовать двух- или трехмерные уплотнители, которые помещают на пористую мембрану, и за счет которых образуется загрузочная зона, изолированная от остальной поверхности пористой мембраны. Уплотнительный элемент согласно настоящему изобретению играет роль барьера для течения жидкости и обеспечивает направленное распределение жидкости пробы и используемых для анализа реактивов в пористой мембране. Кроме того, уплотнительный элемент согласно настоящему изобретению изолирует загрузочную зону для предотвращения нежелательного перехода жидкости в другие области устройства для проведения анализа с латеральными потоками.
Предпочтительными формами осуществления уплотнительных элементов являются форма перемычки, форма ванночки или форма воронки. Формирование уплотнительного элемента осуществляют в процессе вырезания из материала, используемого для изготовления уплотнительного элемента. В случае формы воронки или формы ванночки уплотнительный элемент имеет внутреннее отверстие, предпочтительными формами которого являются круглая, квадратная или прямоугольная, в случае формы воронки к нижней стороне (стороне контакта с мембраной) уплотнительный элемент суживается.
Предпочтительными материалами для изготовления уплотнительного элемента являются такие материалы, которые не поглощают воду (гидрофобные). В особой форме осуществления материалы с одной стороны покрыты слоем клеящего вещества, например, чувствительного к изменениям давления, или самоклеящегося акрилатного клея. Благодаря этому слою уплотнительный элемент может быть приклеен непосредственно к поверхности пористой мембраны. Альтернативно, уплотнительный элемент может быть соединен с корпусом устройства для проведения анализа с латеральными потоками, например приклеен, так что в этой форме осуществления корпус устройства для проведения анализа с латеральными потоками прижимает уплотнительный элемент к поверхности пористой мембраны, и за счет этого обеспечиваются функции уплотнительного элемента.
Предпочтительными материалами для изготовления двухмерных уплотнительных элементов являются любые формы клейких лент или клейких пленок (например, Tesa 4124 производства компании Beiersdorf AG, ARcare 7815 производства компании Adhesives Research).
Предпочтительными материалами для изготовления трехмерных уплотнительных элементов являются гибкие эластомерные материалы с закрытыми порами или гибкие силиконовые материалы с различными значениями толщины материалов, предпочтительно в диапазоне 3-5 мм (например, ячеистая резина EPDM140 производства компании Pitzner, силиконовый каучук или натуральный каучук с твердостью 40 или менее производства компании Castan).
Благодаря такой конструкции согласно настоящему изобретению устройство согласно настоящему изобретению способно воспринимать жидкие пробы, содержащие клетки, например цельную кровь, не отфильтровывая клетки. Далее, уплотнительный элемент обеспечивает возможность нанесения на пористую мембрану (в загрузочную зону) пробы большого объема без переполнения загрузочной зоны. При этом уплотнительный элемент способствует использованию адсорбционных свойств пористой мембраны. Кроме того, уплотнительный элемент гарантирует направленное течение пробы. Однако устройство согласно настоящему изобретению может хорошо функционировать как с уплотнительным элементом, так и без него.
Для абсорбционной зоны (абсорбционной подушечки) устройства согласно настоящему изобретению предпочтительны механически стабильные материалы, предпочтительно с абсорбцией воды в диапазоне 20-30 г/100 см2 (например, бумага Wicking, тип 300, производства компании Schleicher & Schull). Контакт между абсорбционной подушечкой и мембраной, обеспечивающей латеральный поток, в устройстве согласно настоящему изобретению обеспечивается за счет ее прижимания и перекрытия с пористой мембраной. Точное позиционирование абсорбционной подушечки на мембране осуществляется за счет приклеивания абсорбционной подушечки к опорному слою (подложке), к которому прикреплена мембрана, обеспечивающая латеральные потоки.
Подушечка с конъюгатом предпочтительно состоит из стекловолокна или целлюлозы и предпочтительно обладает свойством задерживать поток нативных эритроцитов.
В следующей форме осуществления настоящего изобретения компоненты устройства согласно настоящему изобретению с целью механического укрепления укладывают на подложку, или опорный слой. Тем не менее, устройство согласно настоящему изобретению может функционировать и без опорного слоя. Предпочтительными являются механически стабильные и не поглощающие воду материалы, предпочтительно с толщиной, равной 100 мкм или больше, которые с одной или с двух сторон покрыты слоем клеящего вещества, например, чувствительного к изменениям давления, или самоклеящегося акрилатного клея (например 0,005" Polyester W/GL-187, G&L). На опорном слое фиксируют пористую мембрану и абсорбционную подушечку. В случае опорного слоя, покрытого клеем с двух сторон, вторую клеящую сторону используют для фиксации устройства на других поверхностях, например внутри корпуса устройства для проведения анализа с латеральными потоками.
В следующей форме осуществления изобретения устройство согласно настоящему изобретению, либо с опорным слоем, на котором размещены компоненты устройства согласно настоящему изобретению, либо без него, вставлено в корпус, за счет чего мембранные компоненты прижимаются друг к другу, и корпус способствует выполнению своей функции уплотнительным элементом. Однако устройство согласно настоящему изобретению может одинаково хорошо функционировать как с корпусом, так и без корпуса.
Следующим объектом изобретения является применение устройства согласно настоящему изобретению для анализа крови, более конкретно для одновременного проведения определения группы крови, серологического перекрестного контроля (перекрестной пробы сыворотки) и/или анализа для выявления антител, и/или для одновременного проведения определения группы крови и выявления антител к инфекционным, более конкретно бактериальным и/или вирусным, агентам, и/или для одновременного проведения определения группы крови и выявления антител к другим клеткам крови, отличающимся от эритроцитов, более конкретно антитромбоцитарных или антилимфоцитарных антител, или фрагментов этих антител.
Эта задача согласно настоящему изобретению решена, прежде всего, за счет обеспечения способа определения нескольких аналитов или их производных в жидкой пробе, который включает в себя нанесение пробы на загрузочную зону мембраны устройства согласно настоящему изобретению, причем эту пробу наносят в количестве, достаточном для того, чтобы заставить жидкость пробы течь в направлении абсорбционной зоны через индикаторные зоны и чтобы заставить аналиты или их производные, содержащиеся в жидкой пробе, связываться в соответствующих индикаторных зонах или образовывать в индикаторных зонах комплексы.
В особой форме осуществления способа согласно настоящему изобретению одновременно проводят определение группы крови, перекрестной пробы сыворотки и/или анализа для выявления антител.
Например, цельную кровь или ее разведение наносят на загрузочную зону устройства. Все компоненты, направляемые уплотнительным элементом, проникают в пористую мембрану и проходят при миграции в направлении абсорбционной подушечки вначале область индикаторных зон для перекрестной пробы сыворотки, которые содержат фрагменты клеток А1, А2, В, 0, а также контрольную индикаторную зону, содержащую антитело к lgG/lgM. Изоагглютинины, присутствующие в сыворотке, соединяются с соответствующими антигенами, связанными с клетками. Сывороточный lgG связывается на элементе для контроля связывания (перекрестная проба сыворотки: сенсибилизация).
Антигены, связанные с клетками, мигрируют дальше к области индикаторных зон для определения группы крови, расположенной дистально по отношению к области индикаторных зон для перекрестной пробы сыворотки, в этой области в каждой индикаторной зоне иммобилизовано антитело к другому признаку группы крови (например, анти-А, анти-В, анти-АВ). Самая дистальная по отношению к загрузочной зоне индикаторная зона этой области содержит в качестве связывающего элемента, например, поликлональное антиэритроцитарное антитело. В этой области индикаторных зон эритроциты связываются со связывающими элементами, соответствующими определенным признакам группы крови. На контрольном связывающем элементе связываются эритроциты любой группы крови (определение группы крови).
На следующем этапе отмывания несвязанный материал вымывают из мембраны. На следующем этапе обнаружения с помощью синтетических частиц, покрытых антителами к lgG/lgM, выявляют иммобилизованные на связывающих элементах проксимального ряда индикаторных зон изоагглютинины и контрольные антитела (перекрестная проба сыворотки: обнаружение).
В другой форме осуществления способа согласно настоящему изобретению при одновременном проведении определения группы крови, перекрестной пробы сыворотки и/или анализа для выявления антител признаки группы крови определяют прямым способом, как описано выше, а перекрестную пробу сыворотки и/или анализ для выявления антител проводят как конкурентный анализ следующим образом.
Например, цельную кровь или ее разведение наносят на загрузочную зону устройства. Все компоненты, направляемые уплотнительным элементом, проникают в пористую мембрану и проходят в процессе миграции в направлении абсорбционной подушечки вначале область индикаторных зон для перекрестной пробы сыворотки, которые содержат фрагменты клеток групп крови А и В, а также контрольную индикаторную зону, содержащую фрагменты клеток группы крови 0. Изоагглютинины, присутствующие в сыворотке, соединяются с соответствующими антигенами, связанными с клетками. (Перекрестная проба сыворотки: сенсибилизация).
Антигены, связанные с клетками, мигрируют дальше к области индикаторных зон для определения группы крови, расположенной дистально по отношению к области индикаторных зон для перекрестной пробы сыворотки, в этой области в каждой индикаторной зоне иммобилизованы антитела к разным признакам группы крови (например, анти-А, анти-В, анти-D). Самая дистальная по отношению к загрузочной зоне индикаторная зона этой области содержит в качестве связывающего элемента, например, поликлональное антиэритроцитарное антитело. В этой области индикаторных зон эритроциты связываются со связывающими элементами, соответствующими определенным признакам группы крови. На контрольном связывающем элементе связываются эритроциты любой группы крови (определение группы крови).
На следующем этапе отмывания несвязанный материал вымывают из мембраны. На следующем этапе на загрузочную зону наносят суспензию различных синтетических частиц, которые покрыты анти-А-, анти-В- или анти-Н-антителами. Частицы могут связываться только с теми связывающими элементами в области индикаторных зон для проведения перекрестной пробы сыворотки, которые на этапе сенсибилизации не вступили в контакт с сывороточными агглютининами, то есть цветная полоса в этом случае показывает отсутствие соответствующего изоагглютинина. Например, в случае группы крови А (лица с изоагглютининами анти-В) клеточные фрагменты В-клеток блокируются изоагглютининами, что приводит к тому, что клеточные фрагменты А-клеток окрашиваются нанесенной впоследствии смесью синтетических частиц из-за присутствия среди них анти-А-частиц. Фрагменты клеток группы крови 0 окрашиваются в любых возможных ситуациях, так как они не блокируются изоагглютининами и поэтому всегда свободны для реакции с окрашенными анти-Н-частицами, из-за чего и в варианте конкурентного анализа используют контрольный элемент (перекрестная проба сыворотки: обнаружение).
В следующей форме осуществления способа согласно настоящему изобретению для одновременного проведения определения группы крови, перекрестной пробы сыворотки и/или анализа для выявления антител с прямым определением признаков группы крови и проведением перекрестной пробы сыворотки и/или анализа для выявления антител как конкурентного анализа поступают следующим образом.
Цельную кровь или ее разведение наносят на асимметричную загрузочную зону устройства, содержащую две различные пористые мембраны. При этом для одной пористой мембраны характерна меньшая скорость движения жидкости по капиллярам, чем для другой мембраны. Во втором случае между уплотнительным элементом и индикаторными зонами на мембране размещают подушечку с конъюгатом, которая содержит сухие анти-А/анти-В/анти-Н-частицы. Все компоненты, направляемые уплотнительным элементом, проникают в обе пористые мембраны, что обеспечивает следующий характер потоков:
«Сторона, содержащая только мембрану»: Все компоненты в процессе миграции в направлении соответствующей абсорбционной подушечки проходят через область индикаторных зон для определения группы крови, в которой в индикаторных зонах иммобилизованы антитела к различным признакам группы крови (например, анти-А, анти-В, анти-D). Наиболее дистальная по отношению к загрузочной зоне индикаторная зона этой области в качестве связывающего элемента содержит, например, поликлональное антиэритроцитарное антитело. В этой области индикаторных зон эритроциты связываются со связывающими элементами, которые соответствуют определенным признакам группы крови. На контрольном связывающем элементе связываются эритроциты любой группы крови.
«Сторона, содержащая мембрану и подушечку с конъюгатом»: Все компоненты после проникновения в мембрану и прохождения уплотнительного элемента вступают в контакт с подушечкой с конъюгатом, при этом клеточные компоненты задерживаются или тормозятся, а жидкие компоненты (плазма) могут беспрепятственно течь дальше. Последние вымывают анти-А/анти-В/анти-Н-частицы из подушечки с конъюгатом. Область индикаторных зон для перекрестной пробы сыворотки содержит фрагменты клеток групп крови А и В, а контрольный элемент - фрагменты клеток группы крови 0. Присутствующие в сыворотке изоагглютинины связываются с соответствующими антигенами, связанными с клетками, и конкурируют при этом за связывание с окрашенными анти-А- и анти-В-частицами. Это означает, что частицы могут быть связаны только в том случае, если соответствующий изоагглютинин отсутствует. Например, человек с группой крови А имеет анти-В-изоагглютинины, что приводит к тому, что фрагменты клеток группы крови В блокируются в области индикаторных зон, а окрашенными анти-А-частицами могут быть окрашены только фрагменты клеток группы А. Контрольный элемент, к которому не существует изоагглютининов, всегда остается незаблокированным и окрашивается содержащимися в смеси частиц из подушечки с конъюгатом анти-Н-частицами в виде видимых полос.
В следующей особой форме осуществления способа согласно настоящему изобретению одновременно проводится определение группы крови и определение антитромбоцитарных и/или антилимфоцитарных антител или их фрагментов.
Например, для определения антитромбоцитарных антител индикаторные зоны в области, расположенной проксимально по отношению к загрузочной зоне, содержат в качестве связывающих элементов фрагменты тромбоцитов, которые связывают содержащиеся в сыворотке антитромбоцитарные антитела (если они присутствуют в пробе). В остальном способ остается таким же, как описано в предыдущей форме осуществления способа согласно настоящему изобретению, в частности определение группы крови осуществляется так, как там описано.
В следующей особой форме осуществления способа согласно настоящему изобретению одновременно проводится определение группы крови и определение серологических маркеров инфекционных заболеваний, имеющих значение при трансфузии.
Например, для определения маркеров инфекционных заболеваний индикаторные зоны первой, проксимальной, области индикаторных зон содержат в качестве связывающих элементов синтетические пептиды и/или рекомбинатные белки, которые соответствуют последовательностям белков вирусных или бактериальных агентов (определение антител к маркерам инфекционных заболеваний, например антител к ВИЧ-1), а также антитела, ориентированные против белков-маркеров инфекционных заболеваний (определение антигенов, например HbsAg). Содержащиеся в сыворотке антитела или антигены на первом этапе связываются с соответствующими антигенами или антителами. В остальном способ остается таким же, как описано в предыдущей форме осуществления способа согласно настоящему изобретению, в частности определение группы крови осуществляется так, как там описано.
В способе согласно настоящему изобретению речь идет об аналитах, подлежащих определению, более конкретно об антигенах групп крови или об эпитопах антигенов, предпочтительно относящихся к системам групп крови АВ0, Rh, Келла, об антителах к антигенам групп крови или к эпитопам антигенов или о фрагментах этих антител, предпочтительно о регулярных антителах, нерегулярных антителах, об антителах к инфекционным агентам, о поверхностных антигенах инфекционных агентов и/или об антитромбоцитарных или антилимфоцитарных антителах или фрагментах этих антител.
Пробу, подлежащую анализу, например нативную кровь или кровь с добавлением антикоагулянта, или концентрат эритроцитов, или разбавленную суспензию эритроцитов, составные части крови или исследуемые жидкости, такие как контрольная сыворотка или контрольные клетки, наносят на загрузочную зону устройства согласно настоящему изобретению. Содержащиеся в пробе эритроциты, несущие аналит/аналиты, одновременно выполняют функцию индикаторных частиц.
Более конкретно, используют две группы индикаторных частиц. Одна из них состоит исключительно из эритроцитов для прямого выявления аналитов, связанных с эритроцитами. Вторая группа состоит из частиц любых мыслимых видов и комбинаций, с которыми могут происходить реакции связывания, предпочтительно из частиц, состоящих из коллоидного золота или полистирола, или фиксированных эритроцитов. В предпочтительной форме осуществления настоящего изобретения в ходе одного анализа используются различные индикаторные частицы, из которых, по меньшей мере, один сорт представляет собой нативные эритроциты.
ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Далее изобретение будет описано более подробно с использованием чертежей и примеров, не ограничивающих настоящее изобретение. На чертежах изображено следующее:
Фиг.1 - перспективное изображение устройства согласно настоящему изобретению для проведения анализа с латеральными потоками для одновременного проведения определения группы крови и перекрестной пробы сыворотки;
Фиг.2 - изображение в разобранном виде представленного на Фиг.1 устройства согласно настоящему изобретению для проведения анализа с латеральными потоками;
Фиг.3 - перспективное изображение устройства согласно настоящему изобретению для проведения анализа с латеральными потоками для одновременного проведения определения группы крови и перекрестной пробы сыворотки, изготовленного с использованием трехмерного уплотнительного элемента в форме перегородки;
Фиг.4 - изображение в разобранном виде представленного на Фиг.3 устройства согласно настоящему изобретению для проведения анализа с латеральными потоками;
Фиг.5 - перспективное изображение устройства согласно настоящему изобретению для проведения анализа с латеральными потоками для одновременного проведения определения группы крови и перекрестной пробы сыворотки, изготовленного с использованием трехмерного уплотнительного элемента в форме ванночки;
Фиг.6 - изображение в разобранном виде представленного на Фиг.5 устройства согласно настоящему изобретению для проведения анализа с латеральными потоками;
Фиг.7 - перспективное изображение устройства согласно настоящему изобретению для проведения анализа с латеральными потоками для одновременного проведения определения группы крови, перекрестной пробы сыворотки и анализа для выявления антител у реципиентов;
Фиг.8 - перспективное изображение устройства согласно настоящему изобретению для проведения анализа с латеральными потоками для одновременного проведения определения группы крови, перекрестной пробы сыворотки и анализа для выявления антител у доноров;
Фиг.9 - перспективное изображение устройства согласно настоящему изобретению для проведения анализа с латеральными потоками для одновременного проведения определения группы крови и выявления маркеров инфекционных заболеваний;
Фиг.10 - перспективное изображение устройства согласно настоящему изобретению для проведения анализа с латеральными потоками для одновременного проведения определения группы крови и выявления антител к тромбоцитарным антигенам;
Фиг.11 - перспективное изображение устройства согласно настоящему изобретению для проведения анализа с латеральными потоками с двусторонним течением для одновременного проведения определения группы крови и перекрестной пробы сыворотки;
Фиг.12 - изображение в разобранном виде представленного на Фиг.11 устройства согласно настоящему изобретению для проведения анализа с латеральными потоками.
На Фиг.1 в качестве примера приведено перспективное изображение устройства для проведения анализов с латеральными потоками согласно настоящему изобретению для одновременного проведения определения группы крови и перекрестной пробы сыворотки. В приведенном примере устройство состоит из опорного слоя 1, пористой мембраны 2, абсорбционной подушечки 3 и двумерного уплотнительного элемента 4, выполненного в форме перегородки. При этом пористая мембрана 2 зафиксирована на опорном слое 1, покрытом чувствительным к давлению акрилатным клеящим веществом. Абсорбционная подушечка 3 также зафиксирована на опорном слое 1, при этом часть абсорбционной подушечки 3 перекрывается с пористой мембраной 2. Зафиксированный на верхней стороне пористой мембраны 2 уплотнительный элемент 4 отделяет загрузочную зону 5 от остальной поверхности мембраны и обеспечивает направленное поступление жидкости пробы и анализируемых веществ в пористую мембрану 2. Между загрузочной зоной 5 и областью пористой мембраны 2, контактирующей с абсорбционной подушечкой 3, расположена область индикаторных зон 6. Она состоит из смещенных по диагонали относительно друг друга, расположенных в определенных положениях с координатами Х и Y, точечных индикаторных зон I-IX, причем индикаторные зоны I-V соответствуют области индикаторных зон для перекрестной пробы сыворотки, а индикаторные зоны VI-IX - области индикаторных зон для определения группы крови, и эти зоны состоят из следующих связывающих элементов:
Индикаторная зона V является контролем (ctl) для перекрестной пробы сыворотки и содержит антитела к IgG/IgM человека. Индикаторная зона IX является контролем (ctl) для определения группы крови и содержит поликлональные антитела к эритроцитам. Эти зоны расположены дистально по отношению ко всем остальным индикаторным зонам.
На Фиг.2 представлено в разобранном виде изображенное на Фиг.1 устройство для проведения анализов с латеральными потоками согласно настоящему изобретению, которое состоит из следующих компонентов: опорного слоя 1, пористой мембраны 2, абсорбционной подушечки 3 и уплотнительного элемента 4, при этом загрузочная зона 5 отделена от остальной мембраны, которая содержит область индикаторных зон 6, состоящую из областей индикаторных зон «Перекрестная проба сыворотки» и «Определение группы крови» с индикаторными зонами I-IX, расположенными со смещением друг относительно друга по диагонали.
На Фиг.3 в качестве примера приведено перспективное изображение устройства для проведения анализов с латеральными потоками согласно настоящему изобретению для одновременного проведения определения группы крови и перекрестной пробы сыворотки. В приведенном примере компоненты устройства соответствуют компонентам устройства, изображенного на Фиг.1, за исключением фиксированного на верхней стороне пористой мембраны 2, выполненного в форме трехмерной перегородки уплотнительного элемента 4.
На Фиг.4 представлено в разобранном виде изображенное на Фиг.3 устройство для проведения анализов с латеральными потоками согласно настоящему изобретению, которое состоит из следующих компонентов: опорного слоя 1, пористой мембраны 2, абсорбционной подушечки 3 и уплотнительного элемента 4, выполненного в форме трехмерной перегородки, при этом загрузочная зона 5 отделена от остальной мембраны, которая содержит область индикаторных зон 6, состоящую из областей индикаторных зон «Перекрестная проба сыворотки» и «Определение группы крови» с индикаторными зонами I-IX, расположенными со смещением друг относительно друга по диагонали.
На Фиг.5 в качестве примера приведено перспективное изображение устройства для проведения анализов с латеральными потоками согласно настоящему изобретению для одновременного проведения определения группы крови и перекрестной пробы сыворотки. В приведенном примере компоненты устройства соответствуют компонентам устройства, изображенного на Фиг.1, за исключением фиксированного на верхней стороне пористой мембраны 2 уплотнительного элемента 4, выполненного в форме трехмерной ванночки.
На Фиг.6 представлено в разобранном виде изображенное на Фиг.5 устройство для проведения анализов с латеральными потоками согласно настоящему изобретению, которое состоит из следующих компонентов: опорного слоя 1, пористой мембраны 2, абсорбционной подушечки 3 и уплотнительного элемента 4, выполненного в форме трехмерной ванночки, при этом загрузочная зона 5 отделена от остальной мембраны, которая содержит область индикаторных зон 6, состоящую из областей индикаторных зон «Перекрестная проба сыворотки» и «Определение группы крови» с индикаторными зонами I-IX, расположенными со смещением друг относительно друга по диагонали.
На Фиг.7 в качестве примера приведено перспективное изображение устройства для проведения анализов с латеральными потоками согласно настоящему изобретению для одновременного проведения определения группы крови, перекрестной пробы сыворотки и анализа для выявления антител у реципиентов. В приведенном примере устройство состоит из опорного слоя 1, пористой мембраны 2, абсорбционной подушечки 3 и двумерного уплотнительного элемента 4, выполненного в форме перегородки. При этом пористая мембрана 2 зафиксирована на опорном слое 1, снабженном чувствительным к давлению акрилатным клеящим веществом. Абсорбционная подушечка 3 также зафиксирована на опорном слое 1, при этом часть абсорбционной подушечки 3 перекрывается с пористой мембраной 2. Зафиксированный на верхней стороне пористой мембраны 2 уплотнительный элемент 4 отделяет загрузочную зону 5 от остальной поверхности мембраны и обеспечивает направленное поступление жидкости пробы и анализируемых веществ в пористую мембрану 2. Между загрузочной зоной 5 и областью пористой мембраны 2, контактирующей с абсорбционной подушечкой 3, расположена область индикаторных зон 6. Она состоит из смещенных по диагонали относительно друг друга, расположенных в определенных положениях с координатами Х и Y, точечных индикаторных зон I-XII, причем индикаторные зоны I-VIII соответствуют области индикаторных зон «Перекрестная проба сыворотки/Анализ для выявления антител», а индикаторные зоны IX-XII - области индикаторных зон «Определение группы крови», и эти зоны состоят из следующих связывающих элементов:
Индикаторная зона VIII является контролем (ctl) для перекрестной пробы сыворотки и анализа для выявления антител и содержит антитела к IgG/IgM человека. Индикаторная зона XII является контролем (ctl) для определения группы крови и содержит поликлональные антитела к эритроцитам. Она расположена дистально по отношению ко всем остальным индикаторным зонам.
На Фиг.8 в качестве примера приведено перспективное изображение устройства для проведения анализов с латеральными потоками согласно настоящему изобретению для одновременного проведения определения группы крови, перекрестной пробы сыворотки и анализа для выявления антител у доноров.
В приведенном примере устройство состоит из опорного слоя 1, пористой мембраны 2, абсорбционной подушечки 3 и двумерного уплотнительного элемента 4, выполненного в форме перегородки. При этом пористая мембрана 2 зафиксирована на опорном слое 1, снабженном чувствительным к давлению акрилатным клеящим веществом. Абсорбционная подушечка 3 также зафиксирована на опорном слое 1, при этом часть абсорбционной подушечки 3 перекрывается с пористой мембраной 2. Зафиксированный на верхней стороне пористой мембраны 2 уплотнительный элемент 4 отделяет загрузочную зону 5 от остальной поверхности мембраны и обеспечивает направленное поступление жидкости пробы и анализируемых веществ в пористую мембрану 2. Между загрузочной зоной 5 и областью пористой мембраны 2, контактирующей с абсорбционной подушечкой 3, расположена область индикаторных зон 6. Она состоит из смещенных по диагонали относительно друг друга, расположенных в определенных положениях с координатами Х и Y, точечных индикаторных зон I-Х, причем индикаторные зоны I-VI соответствуют области индикаторных зон «Перекрестная проба сыворотки/Анализ для выявления антител», а индикаторные зоны VII-X - области индикаторных зон «Определение группы крови», и эти зоны состоят из следующих связывающих элементов:
Индикаторная зона VI является контролем (ctl) для перекрестной пробы сыворотки и анализа для выявления антител и содержит антитела к IgG/IgM 20 человека. Индикаторная зона Х является контролем (ctl) для определения группы крови и содержит поликлональные антитела к эритроцитам. Она расположена дистально по отношению ко всем остальным индикаторным зонам.
На Фиг.9 в качестве примера приведено перспективное изображение устройства для проведения анализов с латеральными потоками согласно настоящему изобретению для одновременного проведения определения группы крови и выявления маркеров инфекционных заболеваний. В приведенном примере устройство состоит из опорного слоя 1, пористой мембраны 2, абсорбционной подушечки 3 и двумерного уплотнительного элемента 4, выполненного в форме перегородки. При этом пористая мембрана 2 зафиксирована на опорном слое 1, снабженном чувствительным к давлению акрилатным клеящим веществом. Абсорбционная подушечка 3 также зафиксирована на опорном слое 1, при этом часть абсорбционной подушечки 3 перекрывается с пористой мембраной 2. Зафиксированный на верхней стороне пористой мембраны 2 уплотнительный элемент 4 отделяет загрузочную зону 5 от остальной поверхности мембраны и обеспечивает направленное поступление жидкости пробы и анализируемых веществ в пористую мембрану 2. Между загрузочной зоной 5 и областью пористой мембраны 2, контактирующей с абсорбционной подушечкой 3, расположена область индикаторных зон 6. Она состоит из смещенных по диагонали относительно друг друга, расположенных в определенных положениях с координатами Х и Y, точечных индикаторных зон I-XII, причем индикаторные зоны I-VI соответствуют области индикаторных зон «Выявление маркеров инфекционных заболеваний», а индикаторные зоны VI I-XII - области индикаторных зон «Определение группы крови», и эти зоны состоят из следующих связывающих элементов:
Индикаторная зона VI является контролем (ctl) для выявления антител к инфекционным агентам и содержит антитела к IgG/IgM человека. Индикаторная зона XII является контролем (ctl) для определения группы крови и содержит поликлональные антитела к эритроцитам. Она расположена дистально по отношению ко всем остальным индикаторным зонам.
На Фиг.10 в качестве примера приведено перспективное изображение устройства для проведения анализов с латеральными потоками согласно настоящему изобретению для одновременного проведения определения группы крови и выявления антител к тромбоцитарным антигенам. В приведенном примере устройство состоит из опорного слоя 1, пористой мембраны 2, абсорбционной подушечки 3 и двумерного уплотнительного элемента 4, выполненного в форме перегородки. При этом пористая мембрана 2 зафиксирована на опорном слое 1, снабженном чувствительным к давлению акрилатным клеящим веществом. Абсорбционная подушечка 3 также зафиксирована на опорном слое 1, при этом часть абсорбционной подушечки 3 перекрывается с пористой мембраной 2. Зафиксированный на верхней стороне пористой мембраны 2 уплотнительный элемент 4 отделяет загрузочную зону 5 от остальной поверхности мембраны и обеспечивает направленное поступление жидкости пробы и анализируемых веществ в пористую мембрану 2. Между загрузочной зоной 5 и областью пористой мембраны 2, контактирующей с абсорбционной подушечкой 3, расположена область индикаторных зон 6. Она состоит из смещенных по диагонали относительно друг друга, расположенных в определенных положениях с координатами Х и Y, точечных индикаторных зон I-IX, причем индикаторные зоны I-III соответствуют области индикаторных зон «Выявление антител к тромбоцитарным антигенам», а индикаторные зоны IV-IX - области индикаторных зон «Определение группы крови», и эти зоны состоят из следующих связывающих элементов:
Индикаторная зона III является контролем (ctl) для выявления антител к тромбоцитарным антигенам и содержит антитела к IgG/IgM человека. Индикаторная зона IX является контролем (ctl) для определения группы крови и содержит поликлональные антитела к эритроцитам. Она расположена дистально по отношению ко всем остальным индикаторным зонам.
На Фиг.11 в качестве примера приведено перспективное изображение устройства для проведения анализов с латеральными потоками согласно настоящему изобретению с двунаправленными потоками для одновременного проведения определения группы крови и перекрестной пробы сыворотки. В приведенном примере устройство состоит из опорного слоя 1, пористой мембраны 2а для определения группы крови, отличающейся от пористой мембраны 2а пористой мембраны 2b для проведения перекрестной пробы сыворотки, абсорбционных подушечек 3а и 3b, трехмерного уплотнительного элемента 4, выполненного в форме ванночки, и подушечки с конъюгатом 6. При этом пористые мембраны 2а и 2b зафиксированы на опорном слое 1, снабженном чувствительным к давлению акрилатным клеящим веществом. Абсорбционные подушечки 3а и 3b также зафиксированы на опорном слое 1, при этом часть абсорбционных подушечек 3а и 3b перекрывается с пористыми мембранами 2а и 2b. Зафиксированный на верхней стороне пористых мембран 2а и 2b уплотнительный элемент 4 отделяет загрузочные зоны 5а и 5b от остальной поверхности мембран и обеспечивает направленное поступление жидкости пробы и анализируемых веществ в пористые мембраны 2а и 2b. Между загрузочной зоной 5а и областью пористой мембраны 2а, контактирующей с абсорбционной подушечкой За, расположена область индикаторных зон 7а («Определение группы крови»). Она состоит из смещенных по диагонали относительно друг друга, расположенных в определенных положениях с координатами Х и Y, точечных индикаторных зон I-VI, причем индикаторные зоны области индикаторных зон 7а состоят из следующих связывающих элементов:
Индикаторная зона VI является контролем (ctl) для определения группы крови и содержит поликлональные антитела к эритроцитам. Она расположена дистально по отношению ко всем остальным индикаторным зонам.
Между загрузочной зоной 5b и областью пористой мембраны 2b, контактирующей с абсорбционной подушечкой 3b, расположена область индикаторных зон 7b («Перекрестная проба сыворотки»). Она состоит из смещенных по диагонали относительно друг друга, расположенных в определенных положениях с координатами Х и Y, точечных индикаторных зон VII-IX, причем индикаторные зоны области индикаторных зон 7b состоят из следующих связывающих элементов:
На Фиг.12 в качестве примера приведено в разобранном виде изображенное на Фиг.11 устройство для проведения анализов с латеральными потоками согласно настоящему изобретению с двунаправленными потоками, которое состоит из следующих компонентов: опорного слоя 1, пористой мембраны 2а для определения группы крови, отличающейся от пористой мембраны 2а пористой мембраны 2b для проведения перекрестной пробы сыворотки, абсорбционных подушечек 3а и 3b, трехмерного уплотнительного элемента 4, выполненного в форме ванночки, и подушечки с конъюгатом 6. Загрузочная зона захватывает обе пористые мембраны и состоит из загрузочной зоны 5а на мембране 2а и загрузочной зоны 5b на мембране 2b;
от остальной поверхности пористых мембран 2а и 2b она отделена уплотнительным элементом 4, выполненным в форме ванночки. Мембрана 2а содержит область индикаторных зон 7а со смещенными по диагонали от проксимальной стороны к дистальной индикаторными зонами I-VI, тогда как мембрана 2b содержит область индикаторных зон 7b со смещенными по диагонали от проксимальной стороны к дистальной индикаторными зонами VII-IX.
ОПИСАНИЕ ПРИМЕРОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Пример 1: Одновременное определение группы крови (прямой анализ) и перекрестной пробы сыворотки (анализ с прямым связыванием)
Изготовление испытательных полосок
Испытательные полоски состоят из загрузочной зоны, области индикаторных зон и абсорбционной зоны. Мембраны сорта Millipore HiFlow Plus 065 разрезали на полосы размером 15 мм × 35 мм (ширина/длина; х/у) и наклеивали на опорный слой (подложку, например, производства компании G&L). В области индикаторных зон, которая состоит из области индикаторных зон «Перекрестная проба сыворотки» (расположена проксимально относительно загрузочной зоны) и области индикаторных зон «Определение группы крови» (расположена дистально относительно загрузочной зоны), со смещением по диагонали наносили точечно по 0,2 мл различных связывающих элементов с помощью дозатора, например, AD3200 (Biodot):
область индикаторных зон «Перекрестная проба сыворотки» - суспензии теней эритроцитов с характеристиками группы крови А1, группы крови А2, группы крови В и группы крови 0 (изготовленных из концентратов эритроцитов) и антитела к IgG/IgM человека (антитела козы к IgG человека, антитела козы к IgM человека, производства компании Sigma, I-3382, I-0759) в качестве контроля; область индикаторных зон «Определение группы крови» - анти-А-антитела - клон Birma-1 (производства компании Serologicals, TLJ0105); анти-В-антитела - клон ES-4 (производства компании Serologicals, NCA0201); анти-АВ-антитела - клоны АВ6, АВ26, АВ92 (производства компании Medion Diagnostics, 010062); антиэритроцитарные антитела (фракция антител IgG кролика к эритроцитам (RBC) человека, производства компании Rockland, 209-4139).
Размещение связывающих элементов области индикаторных зон «Перекрестная проба сыворотки» начинают с теней эритроцитов группы крови А в положении х=2,5 мм/у=10 мм. Все остальные связывающие элементы наносят последовательно со смещением на расстояния х=2,5 мм/у=1,5 мм относительно положения теней эритроцитов группы крови А1. Тени эритроцитов наносят в виде 0,1-0,5%-ной (объем/объем) суспензии в 15 мМ калийфосфатном буфере с рН 7,5, содержащем 10% (объем/объем) метанола, антитела к IgG/IgM человека - в виде смеси в соотношении 1:1 с концентрацией 50 мкг/мл в 15 мМ калийфосфатном буфере с рН 7,5, содержащем 10% (объем/объем) метанола.
Размещение связывающих элементов области индикаторных зон «Определение группы крови» начинают с анти-А-антитела в положении х=3 мм/у=20 мм. Все остальные связывающие элементы наносят последовательно со смещением на расстояния х=3 мм/у=1,5 мм от положения анти-А-антитела. Разведения антител выполняли в 15 мМ калийфосфатном буфере с рН 7,5, содержавшем 10% (объем/объем) метанола, следующим образом: анти-А-антитела 1:3, анти-В-антитела 1:2, анти-АВ-антитела 1:4 и антиэритроцитарные антитела 1:3.
После нанесения связывающих элементов мембраны в течение 20 минут сушили при 40°С, после чего хранили при постоянной влажности воздуха до проведения анализа. На дистальном относительно загрузочной зоны конце приклеивали абсорбционную подушечку размером 15 мм × 15 мм (Schleicher&Schull, 300) так, чтобы она перекрывала мембрану на 3 мм. Загрузочную зону отделяли от остальной мембраны приклеиванием клейкой ленты (Теза 4124) шириной 1-2 мм в положении у=5 через всю ширину мембраны.
Проведение анализа
В качестве проб крови использовали цельную кровь с добавлением антикоагулянта. Для собственно анализа на загрузочную зону наносили 100 мкл неразбавленной или разведенной в соотношении 1:3 буфером-разбавителем (Enlisstll, производства Medion Diagnostics, или Разбавитель 1, производства DiaMed) крови. Когда кровь покидала загрузочную зону, ее два раза промывали 100 мкл Enlisstll, чтобы удалить из мембраны несвязанные эритроциты. Затем на загрузочную зону наносили 50 мкл частиц золота, конъюгированных с антителами к IgG/A/M (20-40 нм, производства Arista Biologicals, CGIGA-0800, CGIGG-0800, CGIGM-0800), разведенными в соотношении 1:10 (объем/объем) в TBS с добавлением 0,08% желатина и 0,5% альбумина. Вместо частиц золота можно использовать также окрашенные частицы полистирола диаметром 100-400 нм, например, Merck Eurolab France/Estapor. После того как частицы золота покидают загрузочную зону, мембрану снова один или два раза промывают 100 мкл Enlisstll.
Результаты
а) Контроли: Результаты анализа считаются действительными, если антиэритроцитарный контроль (индикаторная зона IX, область индикаторных зон «Определение группы крови») обнаруживает явно положительный сигнал (красная точка) и если анти-IgG/IgM-контроль (индикаторная зона V, область индикаторных зон «Перекрестная проба сыворотки») окрашивается в характерный пурпурный цвет (частицы золота) или в цвет использованных полистироловых частиц.
б) Результаты анализа: В зависимости от наличия или отсутствия соответствующих антигенов групп крови в соответствующих положениях в области индикаторных зон «Определение группы крови» проявляются красные точки (положительная реакция) или почти белый цвет фона мембраны (отрицательная реакция). Соответствующие изоагглютинины можно обнаружить в области индикаторных зон «Перекрестная проба сыворотки» по характерной пурпурной окраске частиц золота или по цвету использованных частиц полистирола. При отсутствии какого-либо изоагглютинина в этих положениях не удается обнаружить сигналов, отличающихся от фона.
Пример 2: Одновременное определение группы крови (прямой анализ) и перекрестной пробы сыворотки (конкурентный анализ)
Изготовление испытательных полосок
Испытательные полоски состоят из загрузочной зоны, двух областей индикаторных зон, расположенных с двух сторон от загрузочной зоны, и двух абсорбционных зон. Мембраны сортов Millipore HiFlow Plus 065 и HiFlow Plus 140 разрезали на полосы размером 15 мм × 20 мм (ширина/длина; х/у) и наклеивали друг около друга на опорный слой (подложку, например, производства компании G&L). На мембрану HiFlow Plus 140 дополнительно приклеивали подушечку с конъюгатом, в которой находились сухие частицы золота, коагулированные с анти-А/анти-В/анти-Н-антителами, так, чтобы она располагалась между уплотнительным элементом (полоской клейкой ленты) и индикаторными зонами. Вместо частиц золота можно использовать также окрашенные частицы полистирола диаметром от 100 до 400 мкм, например, Merck Eurolab France/Estapor. В области индикаторных зон «Определение группы крови», расположенной на мембране HiFlow Plus 065, со смещением по диагонали наносили точечно с помощью дозатора, например, AD3200 (Biodot), по 0,2 мл следующих связывающих элементов: анти-А-антител - клон Birma-1 (производства компании Serologicals, TLJ0105); анти-В-антител - клон ES-4 (производства компании Serologicals, NCA0201); анти-АВ-антител - клоны АВ6, АВ26, АВ92 (производства компании Medion Diagnostics, 010062); антиэритроцитарных антител (фракция антител IgG кролика к эритроцитам (RBC) человека, производства компании Rockland, 209-4139).
Аналогично в области индикаторных зон «Перекрестная проба сыворотки», расположенной на мембране HiFlow Plus 140, наносили суспензии теней эритроцитов группы крови А, группы крови В и группы крови 0 (изготовленных из концентратов эритроцитов).
Размещение связывающих элементов области индикаторных зон «Перекрестная проба сыворотки» начинают с теней эритроцитов группы крови А в положении х=3 мм/у=10 мм. Все остальные связывающие элементы наносят последовательно со смещением на расстояния х=3 мм/у=1,5 мм относительно положения теней эритроцитов группы крови А1. Тени эритроцитов наносят в виде 0,1-0,5%-ной (объем/объем) суспензии в 15 мМ калийфосфатном буфере с рН 7,5, содержащем 10% (объем/объем) метанола.
Размещение связывающих элементов области индикаторных зон «Определение группы крови» начинают с анти-А-антител в положении х=2,5 мм/у=20 мм. Все остальные связывающие элементы наносят последовательно со смещением на расстояния х=2 мм/у=1,5 мм от положения анти-А-антител. Разведения антител выполняли в 15 мМ калийфосфатном буфере с рН 7,5, содержавшем 10% (объем/объем) метанола, следующим образом: анти-А-антитела 1:3, анти-В-антитела 1:2, анти-АВ-антитела 1:4 и антиэритроцитарные антитела 1:3.
После нанесения связывающих элементов мембраны в течение 20 минут сушили при 40°С, после чего хранили при постоянной влажности воздуха до проведения анализа. На обоих дистальных относительно загрузочной зоны концах приклеивали абсорбционные подушечки размером 15 мм × 15 мм (Schleicher&Schull, 300) так, чтобы они перекрывали соответствующие мембраны на 3 мм. Загрузочную зону отделяли от остальной мембраны приклеиванием клейкой ленты (Теза 4124) шириной 1-2 мм в положении у=5 через всю ширину мембраны.
Проведение анализа
В качестве проб крови использовали цельную кровь с добавлением антикоагулянта. Для собственно анализа на загрузочную зону наносили 100 мкл неразбавленной или разведенной в соотношении 1:3 буфером-разбавителем (Enlisstll, производства Medion Diagnostics, или Разбавителем 1, производства DiaMed) крови. Когда кровь покидала загрузочную зону, ее два раза промывали 100 мкл Enlisstll, чтобы удалить из мембраны несвязанные эритроциты.
Результаты
а) Контроли: Результаты анализа считаются действительными, если антиэритроцитарный контроль (область индикаторных зон «Определение группы крови») обнаруживает явно положительный сигнал (красная точка) и если контрольная зона с эритроцитами группы 0 (область индикаторных зон «Перекрестная проба сыворотки») окрашивается в характерный пурпурный цвет (частицы золота) или в цвет использованных полистироловых частиц.
б) Результаты анализа: В зависимости от наличия или отсутствия соответствующих антигенов групп крови в соответствующих положениях в области индикаторных зон «Определение группы крови» видны красные точки (положительная реакция) или почти белый цвет фона мембраны (отрицательная реакция). Соответствующие изоагглютинины можно обнаружить в области индикаторных зон «Перекрестная проба сыворотки» по отсутствию соответствующих полос. При отсутствии какого-либо изоагглютинина соответствующие полосы приобретают характерную окраску.
Пример 3: Одновременное определение группы крови, перекрестной пробы сыворотки и анализа для выявления антител у реципиентов
Изготовление испытательных полосок
Испытательные полоски состоят из загрузочной зоны, области индикаторных 30 зон и абсорбционной зоны. Мембраны сорта Millipore HiFlow Plus 065 разрезали на полосы размером 20 мм × 35 мм (ширина/длина; х/у) и наклеивали на опорный слой (подложку, например, производства компании G&L). В области индикаторных зон, которая состоит из области индикаторных зон «Перекрестная проба сыворотки/Выявление антител» (расположена проксимально относительно загрузочной зоны) и области индикаторных зон «Определение группы крови» (расположена дистально относительно загрузочной зоны), со смещением по диагонали наносили точечно по 0,2 мл различных связывающих элементов с помощью дозатора, например, AD3200 (Biodot):
в области индикаторных зон «Перекрестная проба сыворотки/Выявление антител» - суспензии теней эритроцитов с характеристиками группы крови А1, группы крови А2, группы крови В, группы крови 0, группы крови 0 с Rh-формулой R1R1 w (пробные клетки 1), группы крови 0 с Rh-формулой R2R2 (пробные клетки 2), группы крови 0 с Rh-формулой R1R1 (пробные клетки 3), а также антитела к IgG/IgM человека (антитела козы к IgG человека, антитела козы к IgM человека, производства компании Sigma, I-3382, I-0759) в качестве контроля; область индикаторных зон «Определение группы крови» - анти-А-антитела - клон Birma-1 (производства компании Serologicals, TLJ0105); анти-В-антитела - клон ES-4 (производства компании Serologicals, NCA0201); анти-АВ-антитела - клоны АВ6, АВ26, АВ92 (производства компании Medion Diagnostics, 010062); антиэритроцитарные антитела (фракция антител IgG кролика к эритроцитам (RBC) человека, производства компании Rockland, 209-4139).
Размещение связывающих элементов области индикаторных зон «Перекрестная проба сыворотки» начинают с теней эритроцитов группы крови А в положении х=3 мм/у=10 мм, размещение теней эритроцитов групп крови А2, В, 0 осуществляют последовательно со смещением на расстояния х=2 мм/у=1,5 мм относительно положения теней эритроцитов группы крови А1. Тени эритроцитов пробных клеток 1 наносят в положении х=11 мм/у=10 мм, тени эритроцитов пробных клеток 2 и 3, а также антитела к IgG/IgM человека - со смещением на расстояния х=2 мм/у=1,5 мм. Тени эритроцитов наносят в виде 0,1-0,5%-ной (объем/объем) суспензии в 15 мМ калийфосфатном буфере с рН 7,5, содержащем 10% (объем/объем) метанола, антитела к IgG/IgM человека в виде смеси в соотношении 1:1 с концентрацией 50 мкг/мл в 15 мМ калийфосфатном буфере с рН 7,5, содержащем 10% (объем/объем) метанола.
Размещение связывающих элементов области индикаторных зон «Определение группы крови» начинают с анти-А-антитела в положении х=4 мм/у=20 мм. Все остальные связывающие элементы наносят последовательно со смещением на расстояния х=3 мм/у=1,5 мм от положения анти-А-антитела. Разведения антител выполняли в 15 мМ калийфосфатном буфере с рН 7,5, содержавшем 10% (объем/объем) метанола, следующим образом: анти-А-антитела 1:3, анти-В-антитела 1:2, анти-АВ-антитела 1:4 и антиэритроцитарные антитела 1:3.
После нанесения связывающих элементов мембраны в течение 20 минут сушили при 40°С, после чего хранили при постоянной влажности воздуха до проведения анализа. На дистальном относительно загрузочной зоны конце приклеивали абсорбционную подушечку размером 20 мм × 15 мм (Schleicher&Schull, 300) так, чтобы она перекрывала мембрану на 3 мм. Загрузочную зону отделяли от остальной мембраны приклеиванием клейкой ленты (Tesa 4124) шириной 1-2 мм в положении у=5 через всю ширину мембраны.
Проведение анализа
В качестве проб крови использовали цельную кровь с добавлением антикоагулянта. Для собственно анализа на загрузочную зону наносили 120 мкл неразбавленной или разведенной в соотношении 1:3 или 1:6 буфером-разбавителем (Enlisstll, производства Medion Diagnostics, или Разбавителем 1, производства DiaMed) крови. Когда кровь покидала загрузочную зону, ее два раза промывали 100 мкл Enlisstll, чтобы удалить из мембраны несвязанные эритроциты. Затем на загрузочную зону наносили 75 мкл частиц золота, конъюгированных с антителами к IgG/A/M (20-40 нм, производства Arista Biologicals, CGIGA-0800, CGIGG-0800, CGIGM-0800), разведенными в соотношении 1:10 (объем/объем) в TBS с добавлением 0,08% желатина и 0,5% альбумина. Вместо частиц золота можно использовать также окрашенные частицы полистирола диаметром 100-400 нм, например, Merck Eurolab France/Estapor. После того как частицы золота покидают загрузочную зону, мембрану снова один или два раза промывают 100 мкл Enlisstll.
Результаты
а) Контроли: Результаты анализа считаются действительными, если антиэритроцитарный контроль (индикаторная зона XII, область индикаторных зон «Определение группы крови») обнаруживает явно положительный сигнал (красная точка) и если анти-IgG/IgM-контроль (индикаторная зона VIII, область индикаторных зон «Перекрестная проба сыворотки/Выявление антител») окрашивается в характерный пурпурный цвет (частицы золота) или в цвет использованных полистироловых частиц. Контроль с антителами к IgG/IgM должен в любом случае быть окрашенным, так что у человека с группой крови АВ, у которого нет нерегулярных антител, окрашивание этой зоны при полном отсутствии других сигналов в области индикаторных зон «Перекрестная проба сыворотки/Выявление антител» подтверждает правильность проведения анализа. Индикаторная зона IV (тени эритроцитов группы крови 0) является отрицательным контролем на изоагглютинины. Окрашивание этой индикаторной зоны означает, что, кроме агглютининов, должны присутствовать также нерегулярные антитела, то есть должна быть окрашена, по меньшей мере, одна из трех индикаторных зон V, VI, VII. Если это не так, результаты анализа недействительны.
б) Результаты анализа: В зависимости от наличия или отсутствия соответствующих антигенов групп крови в соответствующих положениях в области индикаторных зон «Определение группы крови» обнаруживаются красные точки (положительная реакция) или почти белый цвет фона мембраны (отрицательная реакция). Соответствующие изоагглютинины можно обнаружить в области индикаторных зон «Перекрестная проба сыворотки» по характерной пурпурной окраске частиц золота или по цвету использованных частиц полистирола. При отсутствии какого-либо изоагглютинина в этих положениях не удается обнаружить сигналов, отличающихся от фона. При наличии нерегулярного антитела одна, две или все три индикаторные зоны с тенями эритроцитов пробных клеток 1, 2 или 3 окрашиваются в характерный пурпурный цвет частицами золота или в цвет использованных частиц полистирола.
Пример 4: Одновременное определение группы крови, перекрестной пробы сыворотки и анализа для выявления антител у доноров
Изготовление испытательных полосок
В основном, структура испытательных полосок соответствует структуре испытательных полосок из примера 2. Размер мембраны Millipore HiFlow Plus 065 равен 15 мм × 35 мм (ширина/длина; х/у). Индикаторные зоны области индикаторных зон «Определение группы крови» соответствуют примеру 2. В области индикаторных зон «Перекрестная проба сыворотки/Выявление антител» с помощью дозатора, например, AD3200 (Biodot) точечно нанесено по 0,2 мкл следующих связывающих элементов:
суспензий теней эритроцитов с характеристиками группы крови А1, группы крови А2, группы крови В, группы крови 0, теней эритроцитов из смеси пробных клеток 1-3 (см. пример 2) и антител к IgG/IgM человека (антитела козы к IgG человека, антитела козы к IgM человека, производства компании Sigma, I-3382, I-0759) в качестве контроля.
Размещение связывающих элементов области индикаторных зон «Перекрестная проба сыворотки/Выявление антител» начинают с теней эритроцитов с характеристиками группы крови А1 в положении х=2,5 мм/у=10 мм, размещение теней эритроцитов с характеристиками групп крови А2, В, 0 осуществляют последовательно со смещением на расстояния х=2 мм/у=1,5 мм. Размещение теней эритроцитов смеси пробных клеток 1-3 осуществляют в положении х=10,5 мм/у=13 мм, антител к IgG/IgM человека - в положении х=12,5 мм/у=14,5 мм. Тени эритроцитов наносят в виде 0,1-0,5%-ных (объем/объем) суспензий в 15 мМ калийфосфатном буфере с рН 7,5, содержащем 10% (объем/объем) метанола, антитела к IgG/IgM человека - в виде смеси в соотношении 1:1 с концентрацией 50 мкг/мл в 15 мМ калийфосфатном буфере с рН 7,5 с добавлением 10% (объем/объем) метанола.
Размещение связывающих элементов области индикаторных зон «Определение группы крови» начинают с анти-А-антител в положении х=3 мм/у=20 мм. Все остальные связывающие элементы наносят последовательно со смещением на расстояния х=3 мм/у=1,5 мм от положения анти-А-антител. Разведения антител выполняли в 15 мМ калийфосфатном буфере с рН 7,5, содержавшем 10% (объем/объем) метанола, следующим образом: анти-А-антитела 1:3, анти-В-антитела 1:2, анти-АВ-антитела 1:4 и антиэритроцитарные антитела 1:3.
После нанесения связывающих элементов мембраны в течение 20 минут сушили при 40°С, после чего хранили при постоянной влажности воздуха до проведения анализа. На дистальном относительно загрузочной зоны конце приклеивали абсорбционную подушечку размером 15 мм × 15 мм (Schleicher&Schull, 300) так, чтобы она перекрывала мембрану на 3 мм. Загрузочную зону отделяли от остальной мембраны приклеиванием клейкой ленты (Tesa 4124) шириной 1-2 мм в положении у=6 через всю ширину мембраны.
Проведение анализа
Проведение анализа соответствует проведению анализа в примере 1.
Результаты
а) Контроли: Результаты анализа считаются действительными, если антиэритроцитарный контроль (область индикаторных зон «Определение группы крови») обнаруживает явно положительный сигнал (красная точка) и если контрольная зона с антителами к IgG/IgM (индикаторная зона VI, область индикаторных зон «Перекрестная проба сыворотки/Выявление антител») окрашивается в характерный пурпурный цвет (частицы золота) или в цвет использованных полистироловых частиц. Контроль с антителами к IgG/IgM должен в любом случае быть окрашенным, так что у человека с группой крови АВ, у которого нет нерегулярных антител, окрашивание этой зоны при полном отсутствии других сигналов в области индикаторных зон «Перекрестная проба сыворотки/Выявление антител» подтверждает правильность проведения анализа. Индикаторная зона IV (тени эритроцитов группы крови 0) является отрицательным контролем. Окрашивание этой индикаторной зоны означает, что, кроме агглютининов, должны присутствовать также нерегулярные антитела, то есть должна быть окрашена, по меньшей мере, одна из трех индикаторных зон V, VI, VII. Если это не так, результаты анализа недействительны.
б) Результаты анализа: В зависимости от наличия или отсутствия соответствующих антигенов групп крови в соответствующих положениях в области индикаторных зон «Определение группы крови» обнаруживаются красные точки (положительная реакция) или почти белый цвет фона мембраны (отрицательная реакция). Соответствующие изоагглютинины можно обнаружить в области индикаторных зон «Перекрестная проба сыворотки» по характерной пурпурной окраске частиц золота или по цвету использованных частиц полистирола. При отсутствии какого-либо изоагглютинина в этих положениях не удается обнаружить сигналов, отличающихся от фона. При наличии нерегулярного антитела одна, две или все три индикаторные зоны с тенями эритроцитов пробных клеток 1, 2 или 3 окрашиваются в характерный пурпурный цвет частиц золота или в цвет использованных частиц полистирола.
Пример 5: Одновременное определение группы крови и выявление маркеров инфекционных заболеваний
Изготовление испытательных полосок
Испытательные полоски состоят из загрузочной зоны, области индикаторных зон и абсорбционной зоны. Мембраны сорта Millipore HiFlow Plus 065 разрезали на полоски с размерами 15 мм × 35 мм (ширина/длина; х/у) и наклеивали на опорный слой (подложку, например, производства компании G&L). В области индикаторных зон, которая состояла из области индикаторных зоны «Выявление маркеров инфекционных заболеваний» (расположенной проксимально по отношению к загрузочной зоне) и области индикаторных зон «Определение группы крови» (расположенной дистально по отношению к загрузочной зоне), со смещением по диагонали с помощью дозатора, например, AD3200 (Biodot), точечно наносили по 0,2 мкл следующих связывающих элементов:
в индикаторной зоне «Выявление маркеров инфекционных заболеваний» - растворов рекомбинантных антигенов (сифилис; TpN 15, TpN 17, TpN 47), синтетических белков, состоящих из последовательностей гликопротеинов gp-14, gp-41 (ВИЧ-1; ВИЧ-0) и gp-36 (ВИЧ-2), рекомбинантных антигенов вируса гепатита С (HCV) (С-100, С-200, С33с, С22), моноклональных антител (к HBsAg), а также антител к IgG/IgM человека (антитела козы к IgG человека, антитела козы к IgM человека, производства компании Sigma, I-3382, I-0759) в качестве контроля; в области индикаторных зон «Определение группы крови» - анти-А-антитела - клон Birma-1 (производства компании Serologicals, TLJ0105); анти-В-антитела - клон ES-4 (производства компании Serologicals, NCA0201); анти-АВ-антитела - клоны АВ6, АВ26, АВ92 (производства компании Medion Diagnostics, 010062); анти-D-антитела - клоны LDM3/ESD1 (SNBTS), анти-CDE-антитела - клоны MS-24/MS-201/MS-80/MS-258 (производства компании Serologicals), антиэритроцитарные антитела (фракция антител IgG кролика к эритроцитам (RBC) человека, производства компании Rockland, 209-4139).
Размещение связывающих элементов области индикаторных зон «Выявление маркеров инфекционных заболеваний» начинают с синтетических пептидов с характеристиками ВИЧ-1 (gp-14, gp-41) в положении х=2,5 мм/у=10 мм. Все остальные связывающие элементы наносят последовательно со смещением на расстояния х=2 мм/у=1,5 мм от положения индикаторной зоны I. Связывающие элементы индикаторных зон I-V наносят в соответствующих концентрациях в 15 мМ калийфосфатном буфере с рН 7,5, содержащем 10% (объем/объем) метанола, антитела к IgG/IgM человека - в концентрации 50 мкг/мл в 15 мМ калийфосфатном буфере с рН 7,5 с добавлением 10% (объем/объем) метанола.
Размещение связывающих элементов области индикаторных зон «Определение группы крови» начинают с анти-А-антител в положении х=2,5 мм/у=20 мм. Все остальные связывающие элементы этой области индикаторных зон наносят последовательно со смещением на расстояния х=2 мм/у=1,5 мм от положения анти-А-антител. Разведения антител выполняли в 15 мМ калийфосфатном буфере с рН 7,5, содержавшем 10% (объем/объем) метанола, следующим образом: анти-А-антитела 1:3, анти-В-антитела 1:2, анти-АВ-антитела 1:4, антиэритроцитарные антитела 1:3.
После нанесения связывающих элементов мембраны в течение 20 минут сушили при 40°С, после чего хранили при постоянной влажности воздуха до проведения анализа. На дистальном относительно загрузочной зоны конце приклеивали абсорбционную подушечку размером 15 мм × 15 мм (Schleicher&Schull, 300) так, чтобы она перекрывала мембрану на 3 мм. Загрузочную зону отделяли от остальной мембраны приклеиванием клейкой ленты (Tesa 4124) шириной 1-2 мм в положении у=6 через всю ширину мембраны.
Проведение анализа
В качестве проб крови использовали цельную кровь с добавлением антикоагулянта. Для собственно анализа на загрузочную зону наносили 100 мкл неразбавленной или разведенной в соотношении 1:3 или 1:6 буфером-разбавителем (Enlisstll, производства Medion Diagnostics, или Разбавитель 1, производства DiaMed) крови. Когда кровь покидала загрузочную зону, ее два раза промывали 100 мкл Enlisstll, чтобы удалить из мембраны несвязанные эритроциты.
Затем на загрузочную зону наносили 50 мкл смеси частиц золота, конъюгированных с антителами к IgG/A/M (20-40 нм, производства Arista Biologicals, CGIGA-0800, CGIGG-0800, CGIGM-0800) и разведенных в соотношении 1:10 (объем/объем) в TBS с добавлением 0,08% желатина и 0,5% альбумина, а также частиц золота, конъюгированных с антителом к HBsAG (производства Arista Biologicals, ABHBS-0500) в подходящем разведении. Вместо частиц золота можно использовать также окрашенные частицы полистирола диаметром 100-400 нм, например, Merck Eurolab France/Estapor. После того как частицы золота покидают загрузочную зону, мембрану снова один или два раза промывают 100 мкл Enlisstll.
Результаты
Результаты анализа считаются действительными, если антиэритроцитарный контроль (область индикаторных зон «Определение группы крови») обнаруживает явно положительный сигнал (красная точка) и если контрольная зона с антителами к IgG/IgM (индикаторная зона VI, область индикаторных зон «Выявление маркеров инфекционных заболеваний») окрашивается в характерный пурпурный цвет (частицы золота) или в цвет использованных полистироловых частиц. В зависимости от наличия или отсутствия соответствующих антигенов групп крови в соответствующих положениях в области индикаторных зон «Определение группы крови» обнаруживаются красные точки (положительная реакция) или почти белый цвет фона мембраны (отрицательная реакция). При наличии антител к ВИЧ-1, ВИЧ-2, сифилису или поверхностному антигену гепатита В (HBsAg) соответствующая позиция окрашивается в характерный пурпурный цвет частицами и видна как пурпурная точка. Если в качестве индикаторных частиц использованы частицы полистирола, соответствующая позиция окрашивается в цвет использованных частиц полистирола. В наиболее частом случае, а именно в случае отрицательной реакции на все маркеры инфекционных заболеваний, окрашивается только контроль с антителами к IgG/IgM (индикаторная зона VI, область индикаторных зон «Выявление маркеров инфекционных заболеваний»).
Пример 6: Одновременное определение группы крови и выявление антител к тромбоцитарным антигенам
Изготовление испытательных полосок
Структура и размер испытательных полосок, в основном, соответствуют структуре испытательных полосок из примера 4. Область индикаторных зон состоит из области индикаторных зон «Определение группы крови» и области индикаторных зон «Выявление антител к тромбоцитарным антигенам». С помощью дозатора, например, AD3200 (Biodot) точечно наносили по 0,2 мкл следующих связывающих элементов:
в индикаторной зоне «Выявление антител к тромбоцитарным антигенам» - мембранных белков тромбоцитов группы крови 0 с определенными профилями НРА-антигенов, а именно НРА 1bb3aa5bb и НРА 1aa3bb5aa, а также антител к IgG/IgM человека (антитела козы к IgG
человека, антитела козы к IgM человека, производства компании Sigma, I-3382, I-0759) в качестве контроля; в области индикаторных зон «Определение группы крови» - анти-А-антитела - клон Birma-1 (производства компании Serologicals, TLJ0105); анти-В-антитела - клон ES-4 (производства компании Serologicals, NCA0201); анти-АВ-антитела - клоны АВ6, АВ26, АВ92 (производства компании Medion Diagnostics, 010062); анти-D-антитела - клоны LDM3/ESD1 (SNBTS), анти-CDE-антитела - клоны MS-24/MS-201/MS-80/MS-258 (производства компании Serologicals), антиэритроцитарные антитела (фракция антител IgG кролика к эритроцитам (RBC) человека, производства компании Rockland, 209-4139). В качестве альтернативы для мембранных белков тромбоцитов можно также нанести рекомбинантные антигены с соответствующими характеристиками (профилем НРА-антигенов).
Размещение связывающих элементов области индикаторных зон «Выявление антител к тромбоцитарным антигенам» начинают с мембранных белков с профилем НРА-антигенов 1bb3aa5bb в положении х=4 мм/у=10 мм. Все остальные связывающие элементы наносят последовательно со смещением на расстояния х=3,5 мм/у=2 мм от положения индикаторной зоны I. Связывающие элементы индикаторных зон I и II наносят в соответствующих концентрациях в 15 мМ калийфосфатном буфере с рН 7,5, содержащем 10% (объем/объем) метанола, антитела к IgG/IgM человека - в концентрации 50 мкг/мл в 15 мМ калийфосфатном буфере с рН 7,5 с добавлением 10% (объем/объем) метанола.
Размещение связывающих элементов области индикаторных зон «Определение группы крови» соответствует примеру 4.
После нанесения связывающих элементов мембраны в течение 20 минут сушили при 40°С, после чего хранили при постоянной влажности воздуха до проведения анализа. На дистальном относительно загрузочной зоны конце приклеивали абсорбционную подушечку размером 15 мм × 15 мм (Schleicher&Schull, 300) так, чтобы она перекрывала мембрану на 3 мм. Загрузочную зону отделяли от остальной мембраны приклеиванием клейкой ленты (Tesa 4124) шириной 1-2 мм в положении у=6 через всю ширину мембраны.
Проведение анализа
В качестве проб крови использовали цельную кровь с добавлением антикоагулянта. Для собственно анализа на загрузочную зону наносили 100 мкл неразбавленной или разведенной в соотношении 1:3 или 1:6 буфером-разбавителем (Enlisstll, производства Medion Diagnostics, или Разбавитель 1, производства DiaMed) крови. Когда кровь покидала загрузочную зону, ее два раза промывали 100 мкл Enlisstll, чтобы удалить из мембраны несвязанные эритроциты.
Затем на загрузочную зону наносили 50 мкл смеси частиц золота, конъюгированных с антителами к IgG/A/M (20-40 нм, производства Arista Biologicals, CGIGA-0800, CGIGG-0800, CGIGM-0800) и разведенных в соотношении 1:10 (объем/объем) в TBS с добавлением 0,08% желатина и 0,5% альбумина. Вместо частиц золота можно использовать также окрашенные частицы полистирола диаметром 100-400 нм, например, Merck Eurolab France/Estapor. После того как частицы золота покидают загрузочную зону, мембрану снова один или два раза промывают 100 мкл Enlisstll.
Результаты
Результаты анализа считаются действительными, если антиэритроцитарный контроль (область индикаторных зон «Определение группы крови») обнаруживает явно положительный сигнал (красная точка) и если контрольная зона с антителами к IgG/IgM (индикаторная зона III, область индикаторных зон «Выявление антител к тромбоцитарным антигенам») окрашивается в характерный пурпурный цвет (частицы золота) или в цвет использованных полистироловых частиц. В зависимости от наличия или отсутствия соответствующих антигенов групп крови в соответствующих положениях в области индикаторных зон «Определение группы крови» обнаруживаются красные точки (положительная реакция) или почти белый цвет фона мембраны (отрицательная реакция). При наличии антител к тромбоцитарным антигенам соответствующая позиция окрашивается в характерный пурпурный цвет частицами золота и видна как пурпурная точка. Если в качестве индикаторных частиц использованы частицы полистирола, соответствующая позиция окрашивается в цвет использованных частиц полистирола.
Пример 7: Количественное определение аналитов
На Фиг.13 и Фиг.14 показаны результаты исследования крови с использованием устройства и способа согласно изобретению, демонстрирующие осуществление количественного определения антигенов групп крови.
Кроме характерной слабой реакции D-недостаточного фенотипа, Фиг.13 дополнительно демонстрирует градацию между реакциями промежуточной интенсивности (Е и е) и сильными реакциями (с; В), которую можно различить невооруженным глазом. В-антиген имеет наиболее высокую плотность антигена и поэтому дает самую яркую полосу, с-антиген присутствует как гомозигота (в отсутствие в реакции С-антигена) и потому имеет большее количество антигена на поверхности клетки, чем Е- и е-антигены, которые являются гетерозиготными и, вследствие этого, проявляются в реакции с несколько пониженной интенсивностью.
На Фиг.14 видна сильная реакция D-антигена, а также А-антигена (высокое число антигенов по системе групп крови АВ0), с-антигена и Е-антигена (оба присутствуют как гомозиготы).
Анализ, показанный на Фиг.13, выявил низкое содержание D-антигенов на эритроцит, что свидетельствует о наличии D-недостаточного фенотипа. Анализ, показанный на Фиг.14, выявил высокое содержание D-антигенов на эритроцит, что свидетельствует о наличии D-нормального фенотипа.
Изобретение относится к исследованию и анализу биологических материалов. Устройство содержит мембрану с загрузочной зоной для нанесения жидкой пробы, по меньшей мере, две индикаторные зоны, которые могут взаимодействовать с аналитом (или аналитами), и, по меньшей мере, одну абсорбционную зону, которая поглощает жидкость после прохождения через индикаторные зоны. Индикаторные зоны расположены между загрузочной зоной и абсорбционной зоной. Направления потоков от загрузочной зоны через соответствующие индикаторные зоны к абсорбционной зоне (дорожки) практически параллельны. Имеется, по меньшей мере, две различные дорожки. Раскрыт способ определения нескольких аналитов или их производных в жидкой пробе, включающий нанесение пробы на загрузочную зону мембраны. Количество указанной пробы является достаточным для обеспечения движения жидкости пробы в направлении абсорбционной зоны через индикаторные зоны и обеспечения возможности образования аналитами или их производными комплексов в индикаторных зонах. Изобретение позволяет производить одновременное определение клеточных и плазматических параметров пробы. 5 н. 20 з.п. ф-лы, 14 ил., 7 табл.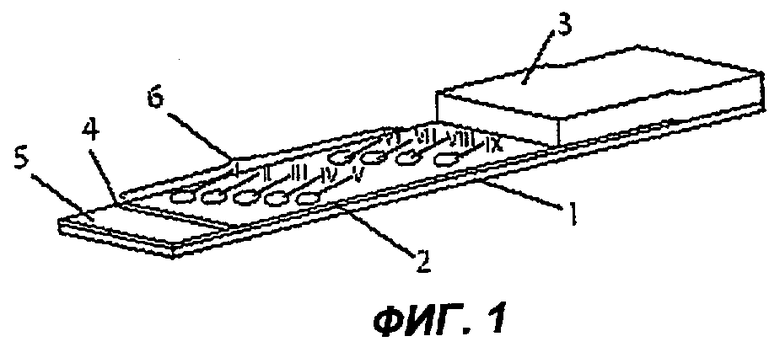
1. Устройство для одновременного количественного или качественного определения нескольких аналитов, по меньшей мере, один из которых представляет собой аналит, связанный с клетками, в жидкой пробе, причем для определения используют, по меньшей мере, два сорта индикаторных частиц, из которых, по меньшей мере, один сорт представляет собой клеточные частицы, включающее:
загрузочную зону (5) для нанесения жидкой пробы,
пористую мембрану (2), которая способствует проникновению клеточных компонентов, на которой имеется, по меньшей мере, две индикаторные зоны, способные вступать во взаимодействие с аналитом (или аналитами), и
по меньшей мере, одну абсорбционную зону (3), расположенную на мембране, которая поглощает жидкость после ее прохождения через индикаторные зоны,
причем индикаторные зоны расположены между загрузочной зоной (5) и абсорбционной зоной (3), при этом направления потоков от загрузочной зоны (5) через соответствующие индикаторные зоны к абсорбционной зоне (3) (дорожки) практически параллельны, и имеются, по меньшей мере, две разные дорожки.
2. Устройство по п.1, отличающееся тем, что индикаторные зоны расположены таким образом, что жидкость пробы по каждой дорожке проходит не более чем через одну индикаторную зону.
3. Устройство по п.1, отличающееся тем, что индикаторные зоны расположены в диагональном, V-образном, W-образном, М-образном, N-образном или прямолинейном порядке.
4. Устройство по п.1, отличающееся тем, что в направлении движения жидкости последовательно и/или рядом друг с другом расположено, по меньшей мере, два ряда индикаторных зон, и индикаторные зоны различных рядов разделены промежутками, так что жидкость пробы по каждой дорожке проходит не более чем через одну индикаторную зону.
5. Устройство по п.1, отличающееся тем, что в направлении движения жидкости последовательно и/или рядом друг с другом расположено, по меньшей мере, два ряда индикаторных зон, и индикаторные зоны различных рядов не разделены промежутками, так что жидкость пробы по каждой дорожке проходит более чем через одну индикаторную зону.
6. Устройство по п.1, отличающееся тем, что оно содержит, по меньшей мере, две группы индикаторных зон, которые расположены по разным направлениям потоков от загрузочной зоны.
7. Устройство по п.1, отличающееся тем, что индикаторные зоны содержат антитела, или фрагменты антител, или лектины, антигены или эпитопы антигенов и/или клетки или фрагменты клеток.
8. Устройство по п.1, отличающееся тем, что индикаторные зоны содержат, прежде всего, антитела или фрагменты антител к антигенам групп крови или эпитопам антигенов групп крови и мембраны или фрагменты эритроцитарных клеток групп крови A1, A2, В и/или 0.
9. Устройство по п.1, отличающееся тем, что индикаторные зоны содержат, прежде всего, антитела или фрагменты антител к антигенам групп крови или эпитопам антигенов групп крови и синтетические пептиды, рекомбинантные антигены и/или антитела или фрагменты антител к маркерам инфекционных заболеваний.
10. Устройство по п.1, отличающееся тем, что индикаторные зоны содержат, прежде всего, антитела или фрагменты антител к антигенам групп крови или эпитопам антигенов групп крови и фрагменты тромбоцитов и/или лимфоцитов.
11. Устройство по п.1, отличающееся тем, что мембрана (2) предпочтительно состоит из полиэтилена, нитроцеллюлозы или нейлона.
12. Устройство по п.1, отличающееся тем, что после загрузочной зоны (5) и перед индикаторными зонами на мембране (2) расположен, по меньшей мере, один уплотнительный элемент (4).
13. Устройство по п.1, отличающееся тем, что после уплотнительного элемента (4) и перед индикаторными зонами расположена, по меньшей мере, одна подушечка с конъюгатом.
14. Устройство по п.1, отличающееся тем, что компоненты устройства для повышения механической прочности укрепляют на опорном слое (1).
15. Устройство по п.1, отличающееся тем, что компоненты устройства собраны в одном корпусе.
16. Применение устройства, как оно определено в любом из пп.1-11, для анализа крови, в частности для одновременного проведения определения группы крови, перекрестной пробы сыворотки и/или анализа для выявления антител.
17. Применение устройства, как оно определено в любом из пп.1-11, для анализа крови, в частности для одновременного проведения определения группы крови и выявления серологических маркеров инфекционных заболеваний или их фрагментов.
18. Применение устройства, как оно определено в любом из пп.1-11, для анализа крови, в частности для одновременного проведения определения группы крови и выявления антител к клеткам крови, в частности антител к тромбоцитам или лимфоцитам, или их фрагментов.
19. Способ определения нескольких аналитов, по меньшей мере, один из которых представляет собой аналит, связанный с клетками, или их производных в одной жидкой пробе, включающий в себя:
нанесение пробы на загрузочную зону (5), по меньшей мере, одной мембраны (2) устройства, как оно определено в любом из пп.1-15, причем количество этой пробы достаточно для того, чтобы заставить жидкость пробы двигаться в направлении абсорбционной зоны (3) через индикаторные зоны, и чтобы заставить аналиты или их производные в жидкости пробы образовывать комплекс в индикаторных зонах, при этом используют, по меньшей мере, два сорта индикаторных частиц, из которых, по меньшей мере, один сорт представляет собой клеточные частицы.
20. Способ по п.19, отличающийся тем, что аналиты или их производные представляют собой антигены групп крови или эпитопы антигенов, антитела к антигенам групп крови или их фрагменты, антитела к тромбоцитам или лейкоцитам, или их фрагменты, антитела к инфекционным агентам или их фрагменты, или антигены инфекционных агентов или эпитопы этих антигенов.
21. Способ по п.19, отличающийся тем, что аналиты или их производные представляют собой антигены или эпитопы антигенов систем групп крови АВО, Rh и Келла.
22. Способ по п.19, отличающийся тем, что аналиты или их производные представляют собой антитела или фрагменты антител к тромбоцитам и/или лимфоцитам.
23. Способ по п.19, отличающийся тем, что аналиты или их производные представляют собой антитела или фрагменты антител к бактериальным и/или вирусным агентам, или вирусные или бактериальные антигены, или эпитопы этих антигенов.
24. Способ по п.19, отличающийся тем, что жидкие пробы предпочтительно состоят из цельной крови, концентрата клеток крови, сыворотки, плазмы и/или исследуемой жидкости, например контрольной сыворотки или контрольных клеток.
25. Способ по п.19, отличающийся тем, что в нем используют, по меньшей мере, два сорта индикаторных частиц, из которых, по меньшей мере, один сорт является эритроцитами.
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| US 6203757 B1, 20.03.2001 | |||
| US 2003045001 A1, 06.03.2003 | |||
| US 2003040021 A1, 27.02.2003 | |||
| УСТРОЙСТВО ДЛЯ ХРОМАТОГРАФИЧЕСКОГО АНАЛИЗА ДЛЯ ОБНАРУЖЕНИЯ И/ИЛИ ОПРЕДЕЛЕНИЯ АНАЛИТА В ОБРАЗЦЕ (ВАРИАНТЫ) | 1994 |
|
RU2124729C1 |
Авторы
Даты
2009-06-10—Публикация
2004-07-08—Подача