Изобретение относится к фармацевтической промышленности, а именно к твердой лекарственной форме амлодипина, обладающей антиангинальной и гипотензивной активностью, и к способу ее получения.
Амлодипин (2-[(2-аминоэтокси) метил]-4-(2-хлорфенил)-1, 4-дигидро-6-метил-3, 5-пиридин дикарбоновой кислоты 3-этил 5-метиловый эфир (в виде безилата)) относится к группе блокаторов «медленных» кальциевых каналов, обладающих антиангинальной и гипотензивной активностью.
Общедоступной информацией является то, что блокаторы «медленных» кальциевых каналов (БМКК), или антагонисты кальция, представляют собой лекарственные средства, избирательно блокирующие деятельность потенциал-зависимых кальциевых каналов, в результате чего ограничивается поступление ионов Са2+ в клетку. В основе механизма действия БМКК на молекулярном уровне является торможение входа ионов кальция внутрь клеток через цитоплазматические потенциал-зависимые кальциевые каналы L-типа (Кукес В.Г. Клиническая фармакология. М.: ГЭОТАР. Медиа, 2004). БМКК уже долгое время используются в терапевтической практике и широко известны практическим врачам. БМКК, имея хорошую переносимость, обладают весьма широким спектром фармакологических эффектов - антиангинальным (антиишемическим), антигипертензивным, антиаритмическим, антитромботическим и др.
Антагонисты кальция подразделяют на препараты первого и второго поколения. К первому поколению относят лекарственные средства, обладающие короткой продолжительностью действия активного вещества (нифедипин, верапамил, дилтиазем), в связи с чем их прием должен осуществляться 3 или 4 раза в день, чтобы гарантировать достаточные уровни действующего вещества в плазме крови. Однако многократный прием лекарственного препарата в день имеет риск, связанный с тем, что пациенты, принимающие большое число различных лекарств, могут забыть его принять.
Ко второму поколению антагонистов кальция относят лекарственные препараты, имеющие в своем составе активное вещество, способное длительно циркулировать в крови (амлодипин, фелодипин), и препараты с пролонгированным, замедленным и контролируемым высвобождением действующего вещества. Антагонисты кальция второго поколения требуют двукратного или однократного приема в день, что, безусловно, более предпочтительно.
Лекарственные средства амлодипина применяются при артериальной гипертензии, стенокардии напряжения, вазоспастической стенокардии (стенокардия Принцметала).
Механизм действия амлодипина обусловлен связыванием с дигидропиридиновыми рецепторами, в результате чего происходит блокирование кальциевых каналов и снижение трансмембранного перехода ионов кальция в клетку. Антиангинальное действие обусловлено расширением коронарных и периферических артерий и артериол, увеличением поступления кислорода в миокард. Гипотензивное действие обусловлено прямым вазодилатирующим влиянием на гладкие мышцы сосудов.
При приеме внутрь амлодипин медленно, но почти полностью абсорбируется из ЖКТ. Биодоступность составляет 60-65% (за счет эффекита «первого прохождения» через печень). Максимальная концентрация Сmax в плазме крови достигается через 6-9 ч. Концентрация стабильного равновесия достигается после 7 дней терапии. Амлодипин подвергается медленному, но экстенсивному метаболизму (90%) в печени с образованием неактивных метаболитов. Связывание с белками плазмы крови составляет 97-98%. Амлодипин проникает через ГЭБ. Т 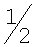 в среднем составляет 35 ч.
в среднем составляет 35 ч.
Выводится почками в виде метаболитов 60% и в неизмененном виде 10%; с желчью и через кишечник около 20-25% в виде метаболитов, а также с грудным молоком.
Рекомендуемый режим дозирования амлодипина составляет 5 мг свободного основания амлодипина (соответствует 6,944 мг безилата амлодипина) 1 раз в сутки. Доза максимально может быть увеличена до 10 мг свободного основания амлодипина (соответствует 13,889 мг безилата амлодипина) однократно в сутки. Эффект развивается через 1-2 ч после приема и продолжается около 24 ч.
Из патента US 4879303, опубликованного в 1989 г., известна таблетированная фармацевтическая композиция амлодипина безилата следующего состава (мг):
Как видно из таблицы, при низкой концентрации активного ингредиента (3,5 мас.%) общие массы таблеток слишком велики (200,0 и 400,0 мг соответственно), что обусловлено, вероятно, технологическими проблемами формования таблеток.
Большой вес, а следовательно, и размер таблетки, безусловно, являются недостатками известной композиции. Во-первых, пациент получает большое количество балластных веществ, оказывающих дополнительную нагрузку на его печень и почки. Во-вторых, размер таблетки относительно велик, а большие таблетки труднее глотать, особенно пожилым пациентам, которые являются основными потребителями препаратов амлодипина. В-третьих, вследствие высокого содержания вспомогательных компонентов в известной композиции затраты производственного процесса достаточно велики, а выход относительно низкий.
Из евразийского патента ЕА 6826 известны таблетки безилата амлодипина, характеризующиеся пониженным содержанием целевых добавок (микрокристаллической целлюлозы, смазывающего агента и разрыхляющего агента). Указанные таблетки содержат 4-6 мас.% безилата амлодипина в качестве активного ингредиента, 87-94 мас.% микрокристаллической целлюлозы, 1-5 мас.% разрыхляющего агента, 0,5-1,5 мас.% смазывающего агента и 0,2-1, 0 мас.% коллоидного диоксида кремния. Общие массы таблеток по известному изобретению при дозировке амлодипина 5 и 10 мг составляют соответственно 140,0 и 280,0 мг. К недостатку известной композиции (помимо также достаточно высокой общей массы таблеток) можно отнести использование в ее составе коллоидного диоксида кремния, на который по ГК XI существует ограничение в применении (не более 10 мас.%).
Настоящее изобретение решает задачу расширения арсенала средств заявленного назначения путем получения фармацевтической композиции амлодипина безилата в виде твердой лекарственной формы при использовании доступных вспомогательных веществ несложным в аппаратурном исполнении способом.
Поставленная задача решается тем, что твердая лекарственная форма, обладающая антиангинальным и гипотензивным действием, содержит амлодипин в виде его фармацевтической соли безилата, лактозу, крахмал картофельный, крахмал прежелатинизированный, натрия кроскармеллозу, стеариновую кислоту и/или ее соли при следующем соотношении компонентов, мас.%:
Общая масса таблетки в соответствии с заявляемым изобретением составляет 100 мг (для дозировки 5 мг амлодипина) и 150 мг (для дозировки 10 мг амлодипина).
Поставленная задача решается также способом получения твердой лекарственной формы, включающим перемешивание, увлажнение, грануляцию и сушку влажных гранул в кипящем псевдоожиженном слое части вспомогательных компонентов, их последующее смешивание с амлодипином и остальными целевыми добавками, опудривание и таблетирование с одновременным обеспыливанием полученных таблеток.
Технический результат изобретения заключается в значительном снижении общей массы таблеток (в 1,3-1,4 раза) и, как следствие, в увеличении в них содержания активного вещества при использовании недорогих и относительно безопасных целевых добавок, что дает дополнительные преимущества. Во-первых, вследствие меньшего размера таблеток облегчается их прием (глотание), в первую очередь, это относится к таблеткам с дозировкой 10 мг амлодипина. Этот аспект предлагаемого изобретения очень важен, особенно для пожилых пациентов, нуждающихся в таком лечении. Во-вторых, достигается снижение себестоимости данного производства. Кроме того, способ получения таблеток по настоящему изобретению является достаточно простым в аппаратурном оформлении.
Амлодипин обладает низкой растворимостью в кислой среде, что, безусловно, усложняет проблему выбора фармацевтически приемлемых и совместимых с ним вспомогательных компонентов с целью получения такой лекарственной формы, из которой бы его высвобождение происходило с достаточно высокой скоростью.
С другой стороны, твердая лекарственная форма амлодипина должна обладать достаточной механической прочностью, так как таблетирование, как правило, происходит на высокоскоростных прессах под давлением, а также хорошей стабильностью при хранении.
Кроме того, необходимо выбрать среди приемлемых такие целевые добавки, которые позволят сформировать таблетки удовлетворительного качества с пониженной общей массой.
Таким образом, выбор фармацевтически приемлемых целевых добавок для получения фармацевтической композиции амлодипина в твердой лекарственной форме для достаточного его высвобождения обусловлен необходимостью не только совместимости вспомогательных компонентов с амлодипином и возможностью формования прочной таблетки, но и достижения высокой скорости его высвобождения для обеспечения доступности для всасывания с одновременным снижением содержания целевых добавок и общей массы таблетки.
Основными формообразующими вспомогательными веществами в составе заявляемой твердой лекарственной формы являются лактоза, крахмал прежелатинизированный и крахмал картофельный в виде гранул, полученных в кипящем псевдоожиженном слое.
Формообразующие вещества обладают хорошей сыпучестью и прессуемостью, поэтому создают необходимую массу и объем и способствуют сохранению определенной формы таблетки. Использование в составе композиции в качестве наполнителя (помимо лактозы и крахмала картофельного) крахмала прежелатинизированного обусловлено его способностью к склеиванию в процессе грануляции, что способствует удерживанию отдельных частиц вместе и последующему образованию гранул и, как следствие, повышению прочности таблеток.
Применение лактозы, крахмала прежелатинизированного и крахмала картофельного в виде гранул как формообразующего вещества обусловлено еще и тем, что гранулят улучшает сжимаемость таблеточной массы.
Эта смесь в больших количественных соотношениях, чем заявленные, не обеспечивает хорошую скорость высвобождения активного вещества, а в меньших - ухудшается стабильность и формообразующие свойства таблетки.
В качестве вещества, обеспечивающего быстрое механическое разрушение таблетки в жидкой среде, способствующего скорейшему высвобождению амлодипина и раннему началу его всасывания, а следовательно, и оказанию лечебного эффекта, применяется натрия кроскармеллоза (примеллоза).
Действие натрия кроскармеллозы, как дезинтегранта, обусловлено тем, что благодаря своей высокой поглощающей способности она увеличивает пористость таблетки за счет образования гидрофильных пор, по которым жидкость проникает в таблетку и разрушает ее.
Присутствие натрия кроскармеллозы в заявленном количестве создает оптимальные условия для проникновения в поры жидкости и обеспечивает ускоренное растворение амлодипина безилата. При использовании меньшего количества натрия кроскармеллозы, чем заявлено, ухудшается растворимость таблетки и, как следствие, уменьшается скорость высвобождения активного вещества.
В качестве опудривающего вещества, защищающего пресс-инструмент от налипания таблеточной массы на стенки пуансонов и матриц и придающего таблеточной массе текучесть, используют стеариновую кислоту и/или ее соли, предпочтительно стеарат магния.
Использование магния стеарата в заявленных количествах обеспечивает равномерное истечение таблеточной массы из бункера в матрицу, что гарантирует точность дозирования амлодипина, способствует облегченному выталкиванию таблеток из матрицы, предотвращает образование царапин на гранях матриц, предотвращает налипание таблеточной массы на стенки пуансонов и матриц, а также слипание частичек между собой. Кроме того, скользящие вещества снимают электростатический заряд с частичек веществ, что также улучшает их сыпучесть.
Поскольку магния стеарат (как и стеариновая кислота) является гидрофобным веществом, то он затрудняет проникновение жидкости в пористую структуру таблетки, что ухудшает ее распадаемость. Поэтому большее, чем заявленное количество магния стеарата, ухудшает распадаемость, а меньшее количество ухудшает сыпучесть.
Заявляемое изобретение осуществляется следующим способом.
Пример 1
В гранулятор с кипящим псевдоожиженным слоем загружаются лактоза и крахмал прежелатинизированный. Порошки тщательно перемешиваются, смесь увлажняется предварительно приготовленным раствором крахмального клейстера при одновременном перемешивании и сушке полученных влажных гранул в кипящем псевдоожиженном слое. Затем полученные гранулы подвергаются процессу калибровки с помощью просеивания и измельчения.
Далее в смеситель загружается полученный на первой стадии гранулят, амлодипина безилат и натрия кроскармеллоза. Проводится тщательное перемешивание компонентов для достижения однородности их распределения в таблеточной массе и, как следствие, точности дозирования.
Смешивание является очень важной и довольно сложной технологической операцией, так как порошки обладают различными физико-химическими свойствами: дисперсностью, насыпной плотностью, влажностью, текучестью и др. Для равномерного распределения сыпучих компонентов смесь порошков гранулята, амлодипина безилата и натрия кроскармеллозы перемешивают в течение 90 мин.
Далее в смеситель загружают стеарат магния. После завершения смешивания и опудривания полученная однородная таблеточная масса направляется на стадию таблетирования.
Механическая прочность таблетки зависит от применяемого давления прессования при таблетировании. Согласно способу в заявленном изобретении используют преимущественно прогрессивное прессование, т.е. нарастающее постепенно, в ротационной таблеточной машине. Таблетирование осуществляется с одновременным обеспыливанием получаемых таблеток.
В качестве примера, иллюстрирующего изобретение, в таблице 1 представлен состав для двух дозировок лекарственного средства амлодипина безилата в твердой лекарственной форме, в частности, таблеток.
5
10
Полученные согласно заявленному изобретению таблетки соответствуют всем стандартам ГФ XI - обладают высокой прочностью - 35 Н, прочностью на истираемость - не менее 98,5%, а также хорошей стабильностью при хранении. Срок годности таблеток составляет 2 года.
При определении распадаемости таблеток, полученных согласно заявляемому изобретению, установлено, что все таблетки распадались за 0,21-0,41 мин, при этом на сетке диска частиц не оставалось, что соответствует требованиям ГФ XI, вып.2.
По данным, полученным в результате исследования показателя растворения таблетки, установлено, что все испытуемые серии препарата соответствуют установленным в ОФС требованиям (в раствор высвобождалось более 80% (Q) через 30 минут при распадаемости таблетки в течение не более 15 мин). Экспериментальные данные по распадаемости и растворению представлены в таблице 2.
Для установления чистоты препарата определяли «Посторонние примеси», используя метод ВЭЖХ, в условиях теста «Количественное определение». Все проведенные испытания по определению посторонних примесей в лекарственном препарате показали соответствие требованиям, заявленным в проекте ФСП, а именно: любой индивидуальной примеси - не более 0,3%. Суммарное содержание примесей - не более 0,6%.
В связи с малой дозировкой лекарственного средства (5 мг) проводили испытание на «Однородность дозирования» методом УФ-спектрофотометрии в условиях теста «Количественное определение». По результатам испытаний все таблетки соответствовали требованиям ГФ XI, вып.2, с.154 и были однородны по количественному содержанию.
Общая масса таблеток по настоящему изобретению составляет 100 и 150 мг для дозировок амлодипина 5 и 10 мг соответственно.
Тщательно подобранный качественный состав и количественные соотношения компонентов обуславливают получение таблеток амлодипина с пониженной общей массой (повышенной концентрацией активного вещества), высокую технологичность их производства с использованием доступных вспомогательных веществ при обеспечении высокой скорости распадаемости и быстрого высвобождения из таблетки активного вещества.
Настоящий способ обеспечивает полную механизацию процесса изготовления, его высокую производительность, чистоту и гигиеничность таблеток, точность дозирования и быстроту высвобождения амлодипина, хорошую стабильность твердой лекарственной формы при хранении.
Изобретение относится к области химико-фармацевтической промышленности и касается твердой лекарственной формы, обладающей антиангинальной и гипотензивной активностью, содержащей в качестве активного вещества амлодипина безилат и целевые добавки при следующем соотношении ингредиентов, мас.%: амлодипина безилат - 6-10, лактоза - 65-90, крахмал картофельный - 0,3-0,6, натрия кроскармеллозу - 1,5-3, стеариновая кислота и/или ее соли - 0,5-1, крахмал прежелатинизированный - остальное. Изобретение обеспечивает получение таблеток с пониженной общей массой. 2 н. и 6 з.п. ф-лы, 2 табл.
1. Твердая лекарственная форма, обладающая антиангинальной и гипотензивной активностью, содержащая амлодипина безилат в качестве активного вещества и целевые добавки, отличающаяся тем, что в качестве целевых добавок содержит лактозу, крахмал картофельный, крахмал прежелатинизированный, натрия кроскармеллозу, стеариновую кислоту и/или ее соли при следующем соотношении компонентов, мас.%:
2. Твердая лекарственная форма по п.1, отличающаяся тем, что содержание амлодипина безилата составляет 5 мг.
3. Твердая лекарственная форма по п.1, отличающаяся тем, что содержание амлодипина безилата составляет 10 мг.
4. Твердая лекарственная форма по п.1, отличающаяся тем, что в качестве соли стеариновой кислоты содержит стеарат магния.
5. Твердая лекарственная форма по п.1, отличающаяся тем, что выполнена в виде таблетки.
6. Способ получения твердой лекарственной формы по п.1, заключающийся в том, что лактозу и крахмал прежелатинизированный перемешивают в грануляторе и увлажняют раствором крахмального клейстера, сушат влажные гранулы, добавляют амлодипина безилат и натрия кроскармеллозу, тщательно перемешивают, опудривают стеариновой кислотой и/или ее солями и таблетируют с одновременным обеспыливанием таблеток.
7. Способ получения твердой лекарственной формы по п.6, отличающийся тем, что применяют грануляцию в кипящем псевдоожиженном слое.
8. Способ получения твердой лекарственной формы по п.6, отличающийся тем, что применяют метод прогрессивного прессования.
| Транспортер | 1928 |
|
SU6826A1 |
| US 4879303 А, 07.11.1989 | |||
| СТАБИЛИЗИРОВАННАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ БЛОКАТОР КАЛЬЦИЯ | 2001 |
|
RU2239432C2 |
| СТАБИЛЬНЫЙ ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ, СОДЕРЖАЩИЙ АМЛОДИПИНА БЕЗИЛАТ И АТЕНОЛОЛ | 1998 |
|
RU2188636C2 |
Даты
2009-06-27—Публикация
2008-02-18—Подача