Изобретение относится к лекарственным средствам, используемым в клинической онкологии, и касается фармацевтической композиции, содержащей пептид, обладающий противоопухолевым действием, которая может быть использована в клинической практике для лечения опухолей.
Современная медицина располагает достаточно обширным арсеналом лекарственных средств для лечения онкологических больных. Известно применение в клинической терапии опухолей препарата на основе циклического октапептида, выпускаемого фирмой «Сандос» (Н.Ф.Орел и др., ж. «Современная онкология», т.2, №1, 2000).
В клинической практике также широко применяют цитостатики: сарколизин, циклофосфан и цисплатин (Машковский М.Д. Лекарственные средства. Т.2. Харьков: Торсинг, 1997. С.437, 439, 458). Важно отметить, что при применении препаратов данной группы возможно серьезное побочное действие: нарушение функции почек, тошнота, рвота, потеря аппетита, головокружение, шум в ушах, понижение слуха, анафилактические реакции, лейкопения, тромбоцитопения, анемия, нейропатия с преимущественным поражением нервов нижних конечностей. В связи с этим существует значительное число противопоказаний к применению этой группы препаратов: нарушение функций почек и печени, угнетение костномозгового кроветворения, нарушение кровообращения, язвенная болезнь желудка и двенадцатиперстной кишки, беременность.
Тем не менее, в онкологии ведется активный поиск противоопухолевых лекарственных средств пептидной природы, проявляющих высокую специфическую активность и одновременно не имеющих серьезных противопоказаний и побочного действия.
Из уровня техники известны средства пептидной природы, обладающие противоопухолевым действием.
Известен пентапептид, обладающий противоопухолевой активностью М2 Val-Mval-Pro-Pro-NH-Bzl HCl (патент RU №2153504, 1995). Известно противоопухолевое средство, представляющее собой нетоксичный гексапептид формулы Leu-Val-Val-Тyr-Рrо-Трr (патент RU 2067870, 1993). Известно применение пептида H-Lys-Gln-OH для подавления роста опухолевых клеток (WO 86/04334 А1, опубл. 31.07.1986). Известна фармацевтическая композиция с использованием новых производных пептидов, которые обладают опухоль-ингибирующей активностью (патент RU 2116312, 1998).
Несмотря на то что известные средства пептидной природы обеспечивают потенциально улучшенные терапевтические возможности медикаментозного лечения опухолей, разработка новых средств пептидной природы остается актуальной.
Из уровня техники известен пептид глутамил-аспартил-глицин общей формулы: Н-Glu-Asp-Gly-OH (Регистрационный номер RN-75007-24-8 согласно STN int. BD Registry Chemical abstract).
Известно также, что пептид H-Glu-Asp-Gly-OH обладает стресспротекторным действием (патент RU №2304444, 2006).
При экспериментальном изучении пептида глутамил-аспартил-глицин общей формулы: H-Glu-Asp-Gly-OH было выявлено его ранее неизвестное свойство, проявляющееся в оказании противоопухолевого действия.
Настоящим изобретением поставлена и решена задача получения средства пептидной природы, обладающего противоопухолевым действием.
Технический результат изобретения заключается в проявлении пептидом глутамил-аспартил-глицин формулы: H-Glu-Asp-Gly-OH противоопухолевого действия, использование которого в качестве действующего вещества в фармацевтической композиции при онкологических заболеваниях оказывает противоопухолевое действие за счет торможения пролиферативной активности опухолевых клеток.
Для решения поставленной задачи и достижения указанного технического результата предложена группа изобретений, объединенных общим изобретательским замыслом.
В одном из своих аспектов настоящее изобретение относится к фармацевтической композиции, обладающей противоопухолевым действием, содержащей в качестве действующего вещества эффективное количество пептида глутамил-аспартил-глицин формулы: H-Glu-Asp-Gly-OH и фармацевтически приемлемый носитель.
При этом фармацевтическая композиция находится в форме, подходящей для парентерального введения.
В другом аспекте настоящее изобретение относится к средству, обладающему противоопухолевым действием, содержащему в качестве действующего вещества эффективное количество пептида глутамил-аспартил-глицин формулы: H-Glu-Asp-Gly-ОН и фармацевтически приемлемый носитель.
Пептид глутамил-аспартил-глицин формулы: H-Glu-Asp-Gly-OH получают классическим методом пептидного синтеза в растворе.
При экспериментальном изучении пептида глутамил-аспартил-глицин формулы: Н-Glu-Asp-Gly-OH выявлено, что он проявляет новую биологическую активность, проявляющуюся в оказании противоопухолевого действия.
Возможность объективного проявления технического результата при использовании изобретения подтверждена достоверными данными, содержащими сведения экспериментального характера, полученные по методикам, принятым в данной области.
Изучение биологической активности проводили на животных в экспериментальной модели рака Эрлиха с использованием штамма перевиваемых опухолей мышей линии SHR.
Понятие «фармацевтическая композиция» подразумевает различные лекарственные формы, содержащие пептид, которые могут найти лечебное применение в медицине в качестве средства, обладающего противоопухолевым действием.
Для получения фармацевтических композиций, отвечающих изобретению, эффективное количество пептида H-Glu-Asp-Gly-OH как действующее вещество смешивают с фармацевтически приемлемым носителем согласно принятым в фармацевтике способам компаундирования.
Понятие «эффективное количество» подразумевает использование такого количества действующего вещества, которое в соответствии с его количественными показателями активности и токсичности, а также на основании знаний специалиста должно быть эффективным в данной лекарственной форме.
В качестве носителя могут использоваться различные вещества в зависимости от лекарственной формы препарата, желаемой для введения в организм. Для парентерального введения в качестве носителя обычно используют физиологический раствор или стерильную воду.
Сущность изобретения поясняется таблицами.
В Таблице 1 представлено влияние фармацевтической композиции, содержащей в качестве действующего вещества пептид H-Glu-Asp-Gly-OH, на рост опухолей в экспериментальной модели рака Эрлиха у мышей линии SHR.
В Таблице 2 представлено влияние пептида H-Glu-Asp-Gly-OH, используемого в качестве действующего вещества в фармацевтической композиции, на морфологические и биохимические показатели периферической крови морских свинок при изучении хронической токсичности.
Изобретение иллюстрируется примером синтеза пептида глутамил-аспартил-глицин общей формулы: H-Glu-Asp-Gly-OH (пример 1), примером, подтверждающим противоопухолевое действие фармацевтической композиции, содержащей в качестве действующего вещества пептид H-Glu-Asp-Gly-OH (пример 2), а также примером изучения токсичности пептида H-Glu-Asp-Gly-OH, используемого в качестве действующего вещества в фармацевтической композиции (пример 3).
Пример 1. Синтез пептида H-Glu-Asp-Gly-OH
1. Название соединения: глутамил-аспартил-глицин.
2. Структурная формула H-Glu-Asp-Gly-OH
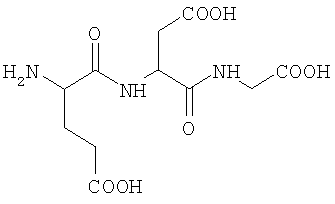
3. Брутто-формула без противоиона: C11H17N3O8.
4. Молекулярный вес без противоиона: 319,27.
5. Противоион: ацетат.
6. Внешний вид: белый аморфный порошок без запаха.
7. Способ синтеза: пептид получен классическим методом синтеза в растворе по схеме:
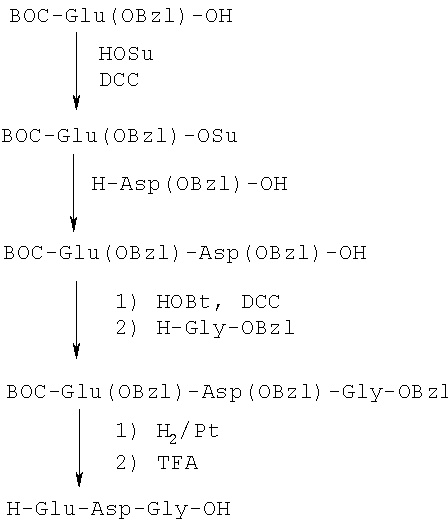
ВОС - трет.бутилоксикарбонильная группа,
OSu - N-оксисукцинимидный эфир,
DCC - N,N'-дициклогексилкарбодиимид,
OBzl - бензиловый эфир,
TFA - трифторуксусная кислота,
HOBt - N-оксибензотриазол.
Характеристики готового препарата:
- содержание основного вещества: 97,93% (по ВЭЖХ, 220 нм),
- ТСХ - индивидуален, Rf=0,45 (ацетонитрил-вода 1:2),
- содержание влаги: 6%,
- рН 0,01% раствора: 4,9,
- удельное оптическое вращение: [α]D 22: -31° (с=1, Н2О), "Polamat A", Carl Zeiss Jena.
Пример синтеза:
1) BOC-Glu(OBzl)-OSu, N-оксисукцинимидный эфир N-трет.бутилоксикарбонил-(γ-бензил)глутаминовой кислоты (I).
N-трет.бутилоксикарбонил-(γ-бензил)глутаминовую кислоту BOC-Glu(OBzl)-OH (33,7 г, 0,1 моль) растворяли в 50 мл N,N'-диметилформамида, охлаждали до температуры -10°С, добавляли при перемешивании охлажденные (4-6°С) растворы N,N'-дициклогексилкарбодиимида (23,0 г, 0,11 моль) в 30 мл N,N'-диметилформамида и N-гидроксисукцинимида (13,0 г, 0,11 моль) в 20 мл N,N'-диметилформамида. Реакционную смесь перемешивали в течение 12 ч при охлаждении льдом и далее в течение 1 суток при комнатной температуре. Выпавшую N,N'-дициклогексилмочевину отфильтровывали и полученный раствор активированного эфира использовали без выделения на следующей стадии.
2) BOC-Glu(OBzl)-Asp(OBzl)-OH, N-трет.бутилоксикарбонил-(γ-бензил)глутамил-(β-бензил)аспартат (II).
(β-Бензил) аспарагиновую кислоту H-Asp(OBzl)-OH (28,0 г, 0,12 моль) и 36 мл (0,12 моль) триэтиламина суспендировали в 50 мл N,N'-диметилформамида и перемешивали в течение 1 ч. Затем добавили порциями раствор активированного эфира BOC-Glu(OBzl)-OSu (I), полученный на предыдущей стадии. Реакционную смесь перемешивали при комнатной температуре в течение 2 суток. Затем подкисляли 0,5 н серной кислотой до рН 2-3 и экстрагировали этилацетатом 4х50 мл. Вытяжки объединяли и последовательно промывали 0,5 н H2SO4 3×50 мл, водой 2×50 мл, 5% раствором NaHCO3 2×50 мл, водой 2×50 мл, насыщенным раствором NaCl 2×50 мл. Органический слой сушили над Na2SO4, упаривали растворитель в вакууме, остаток кристаллизовали под гексаном. Получено 50 г продукта (92%). Rf=0,34 (бензол-ацетон 2:1).
3) BOC-Glu(OBzl)-Asp(OBzl)-Gly-OBzl (III), бензиловый эфир N-трет.бутилоксикарбонил-(γ-бензил)глутамил-(β-бензил)аспартил-глицина (III).
2,7 г (5 ммоль) дипептида и 0,95 г (7 ммоль) оксибензотриазола растворяли в тетрагидрофуране (10 мл) и охлаждали до температуры - 10°С. 1,44 г (7 ммоль) дициклогексилкарбодиимида растворяли в 5 мл тетрагидрофурана и охлаждали до той же температуры. 3,4 г (10 ммоль) тозилата бензилового эфира глицина растворяли в 10 мл тетрагидрофурана, добавляли 1,4 мл (10 ммоль) триэтиламина и охлаждали до той же температуры. При охлаждении на ледяной бане и интенсивном перемешивании объединяли растворы дипептида с оксибензотриазолом и карбодиимида, через 10 мин добавляли раствор тозилата бензилового эфира глицина. Реакционную смесь перемешивали в течение 3 ч при охлаждении льдом и в течение 1 суток при комнатной температуре. Выпавшую дициклогексилмочевину отфильтровывали, фильтрат упаривали в вакууме, остаток растворяли в этилацетате (100 мл). Раствор промывали последовательно 0,5 н серной кислотой, водой, 5% раствором бикарбоната натрия, водой, сушили над безводным сульфатом натрия. Этилацетат упаривали в вакууме, кристаллизация остатка в системе этилацетат/ гексан. Перекристаллизация из изопропанола. Получено после сушки в вакууме 2,74 г продукта (85%). Rf=0,78 (бензол-ацетон 1:1).
4) H-Glu-Asp-Gly-OH (IV), глутамил-аспартил-глицин.
Защищенный трипептид BOC-Glu(OBzl)-Asp(OBzl)-Gly-OBzl (III) (2,7 г) растворяли в смеси метиловый спирт - вода (4:1) (50 мл) и гидрировали над катализатором Pd/C (5%) в течение 4 ч. Катализатор отфильтровывали, растворитель упаривали в вакууме, остаток сушили в вакууме над KОН и P2O5. Далее продукт растворяли в 15 мл смеси хлористый метилен-трифторуксусная кислота (5:1) и выдерживали при комнатной температуре в течение 2 ч. Полноту прохождения реакции деблокирования контролировали по ТСХ в системе ацетонитрил-вода (1:3). Растворитель упаривали в вакууме, остаток сушили в вакууме над КОН.
Для очистки 300 мг препарата растворяли в 4 мл 0,01% трифторуксусной кислоты и подвергали высокоэффективной жидкостной хроматографии на колонке с обращенной фазой 50×250 мм Diasorb-130-C16T, 7 mkm. Хроматограф Beckman System Gold, 126 Solvent Module, 168 Diode Array Detector Module. Условия хроматографирования А: 0,1% TFA; В: MeCN/0,1% TFA, градиент В 0→50% за 100 мин. Объем пробы 5 мл, детекция при 215 нм, сканирование 190-600 нм, скорость потока 10 мл/мин. Отбирали фракцию основного пика. Растворитель упаривали в вакууме при температуре не выше 40°С, упаривание многократно (5 раз) повторяли с 10 мл 10% раствора уксусной кислоты.
Окончательно остаток растворяли в 20 мл деионизованной воды и лиофилизовывали. Получено 150 мг очищенного препарата в виде аморфного белого порошка без запаха.
5) Анализ готового препарата.
- Содержание основного вещества определяли методом ВЭЖХ на колонке Phenomenex С 18 LUNA 4,6×150 mm. A: 0,1% TFA, В: MeCN; grad.B 0-100% in 10 min. Скорость потока 1 мл/ мин. Детекция при 220 нм, сканирование 190-600 нм, проба 20µ1. Содержание основного вещества 97,93%.
- ТСХ: индивидуален, Rf=0,45 (ацетонитрил-вода 1:2, пластинки ПТСХ-П-В-УФ Sorbfil, силикагель СТХ-1ВЭ 8-12 мкм, проявление хлор/бензидин).
- Содержание влаги: 6% (гравиметрически по потере массы при сушке 20 мг при 100°С).
- рН 0,01% раствора: 4,9 (потенциометрически).
- Удельное оптическое вращение: [α]D 22: -31° (с=1, H2O), "Polamat A", Carl Zeiss Jena.
Пример 2. Изучение противоопухолевого действия фармацевтической композиции, содержащей пептид H-Glu-Asp-Gly-OH
Изучение противоопухолевого действия фармацевтической композиции, содержащей в качестве действующего вещества пептид H-Glu-Asp-Gly-OH, проводили на модели рака Эрлиха - штамма перевиваемых опухолей мышей, широко используемого для отбора и дальнейшего изучения противораковых средств.
Рак Эрлиха привили 80 мышам-самкам линии SHR под кожу правого бока в количестве 107 клеток в 0,1 мл физиологического раствора.
Спустя 48 часов после перевивки опухоли животных методом рандомизации разделили на 4 группы.
20 животным контрольной группы подкожно вводили по 0,2 мл стерильного физиологического раствора 5 раз в неделю в течение 1 месяца (всего 20 инъекций).
20 животным I подопытной группы вводили по 0,1 мкг на мышь, а 20 животным II подопытной группы - по 2 мкг на мышь пептида H-Glu-Asp-Gly-OH в 0,2 мл стерильного физиологического раствора 5 раз в неделю в течение 1 месяца (всего 20 инъекций).
20 животным группы сравнения однократно внутрибрюшинно вводили общепринятый цитостатический препарат цисплатин в дозе 5 мг/кг, используя его в качестве препарата сравнения.
Два раза в неделю у животных измеряли длину и ширину опухолевых узлов. Объем опухоли рассчитывали по формуле:
V=(a·b2)/2,
где а - больший, a b - меньший линейный размер узла.
Эффективность терапии оценивали по торможению роста опухоли. Процент торможения роста опухоли рассчитывали по формуле:
(VK-VO)/VK·100%,
где VK - средний объем опухоли у животных контрольной группы, a VO - средний объем опухоли у животных подопытной группы.
Результаты исследования влияния препаратов на рост солидного рака Эрлиха представлены в Таблице 1.
Из данных, приведенных в Таблице 1, следует, что при введении в указанных дозах и режимах фармацевтическая композиция, содержащая пептид H-Glu-Asp-Gly-OH в дозе 0,1 мкг/мышь на ранних стадиях проявляет статистически недостоверную (за исключением 18 дня роста опухоли) тенденцию к торможению роста опухоли, но на более поздних стадиях неэффективна.
Из данных, приведенных в Таблице 1, также следует, что введение фармацевтической композиции в дозе 2 мкг/мышь статистически достоверно тормозит рост рака Эрлиха на 71%.
Важно отметить, что в данном эксперименте препарат сравнения - цисплатин не более активен, чем фармацевтическая композиция, содержащая пептид H-Glu-Asp-Gly-OH в дозе 2 мкг/мышь: цисплатин статистически достоверно тормозит рост рака Эрлиха на 60%.
Таким образом, как видно из данных, представленных в Таблице 1, введение фармацевтической композиции, содержащей в качестве действующего вещества пептид H-Glu-Asp-Gly-OH в дозе 2 мкг/мышь, при подкожном введении 20-кратно оказывает противоопухолевое действие, выражающееся в торможении роста опухоли Эрлиха, сравнимое по эффективности с цитостатическим препаратом цисплатином.
Результаты, полученные при проведении исследований, свидетельствуют также о свойстве фармацевтической композиции, содержащей в качестве действующего вещества пептид H-Glu-Asp-Gly-OH, оказывать противоопухолевое действие.
Согласно изобретению фармацевтическая композиция, введенная в указанных дозах животным, обеспечивает противоопухолевый эффект. При этом дозы могут варьироваться в зависимости от природы и тяжести заболевания, веса пациента, сопутствующего лечения и других факторов, известных специалистам.
Вместе с тем, в основном, фармацевтическая композиция, содержащая в качестве действующего вещества пептид H-Glu-Asp-Gly-OH, согласно настоящему изобретению может быть введена в количестве 100 мкг/кг массы тела пациента (животного или человека) в виде одноразовой дозы. Предпочтительная доза для одного пациента, нуждающегося в таком лечении, составляет в пределах от 1 до 10 мг в день, а предпочтительный курс лечения составляет от 10 до 20 дней.
С целью подтверждения отсутствия токсичности пептида H-Glu-Asp-Gly-OH при указанных дозах введения ниже приводится пример 3.
Пример 3. Изучение токсичности пептида H-Glu-Asp-Gly-OH
Общетоксическое действие пептида H-Glu-Asp-Gly-OH, используемого в качестве действующего вещества в фармацевтической композиции, исследовали в соответствии с требованиями «Руководства по экспериментальному (доклиническому) изучению новых фармакологических веществ» (2000): острой токсичности при однократном введении препарата, а также подострой и хронической токсичности при длительном введении пептида.
Исследование по изучению острой токсичности проведено на 66 белых беспородных мышах-самцах массой 20-22 г. Животные были рандомизированно разделены на 6 равных групп. Препарат вводили животным однократно внутримышечно в дозах 1 мг/кг, 2 мг/кг, 3 мг/кг, 4 мг/кг, 5 мг/кг в 0,25 мл стерильного 0,9% раствора NaCl. Животным контрольной группы в том же объеме вводили 0,9% раствор NaCl.
Исследования по изучению подострой токсичности проведено на 64 белых беспородных крысах-самцах массой 180-220 г. Ежедневно однократно животным подопытных групп вводили препарат внутримышечно в течение 90 дней в дозах 1 мкг/кг, 0,1 мг/кг, 1 мг/кг в 0,5 мл стерильного 0,9% раствора NaCl. Животным контрольной группы вводили в том же объеме стерильный 0,9% раствор NaCl. До введения препарата, на 30, 60 и 90 сутки после начала введения препарата у животных исследовали морфологический состав и свойства периферической крови. При завершении эксперимента исследовали биохимические и коагулологические показатели крови.
Исследования по изучению хронической токсичности проводили в течении 6 месяцев, исходя из длительности рекомендуемого клинического назначения препарата, на 92 морских свинках-самцах массой 310-350 г. Животные подопытных групп получали ежедневно однократно внутримышечно пептид в течение 6 мес в дозах 1 мкг/кг, 0,1 мг/кг, 1 мг/кг в 0,5 мл стерильного 0,9% раствора NaCl. В контрольной группе животным вводили по аналогичной схеме стерильный 0,9% раствор NaCl в том же объеме. У животных в периферической крови общепринятыми методами определяли: количество эритроцитов, гемоглобина, ретикулоцитов, тромбоцитов, лейкоцитов, лейкоцитарную формулу, скорость оседания эритроцитов (СОЭ), резистентность эритроцитов. Наряду с этим определяли содержание в сыворотке крови общего белка по методу Лоури, калия и натрия методом плазменной спектрофотометрии. После завершения эксперимента проводили патоморфологическое исследование головного и спинного мозга, спинномозговых ганглиев, щитовидной железы, паращитовидных желез, надпочечников, семенников, гипофиза, сердца, легких, аорты, печени, почки, мочевого пузыря, поджелудочной железы, желудка, тонкой кишки, толстой кишки, тимуса, селезенки, лимфатических узлов, костного мозга.
При изучении острой токсичности установлено, что однократное введение исследуемого пептида животным в дозе, превышающей терапевтическую, рекомендованную для клинического применения, более чем в 5000 раз, не вызывает токсических реакций, что свидетельствует о большой терапевтической широте препарата.
Изучение подострой и хронической токсичности пептида свидетельствует об отсутствии побочных эффектов при длительном применении препарата в дозах, превышающих терапевтическую в 100-1000 раз. При исследовании влияния пептида на морфологический состав крови морских свинок установлено увеличение количества лейкоцитов через 3 месяца после начала введения препарата, которое нормализовалось к 6-му месяцу наблюдения (Таблица 2). Остальные показатели морфологического состава крови животных практически не изменялись. Не отмечено достоверного влияния препарата на СОЭ, резистентность эритроцитов и биохимические показатели сыворотки крови.
При оценке общего состояния животных, морфологических и биохимических показателей периферической крови, морфологического состояния внутренних органов, состояния сердечно-сосудистой и дыхательной систем, функции печени и почек патологические изменения в организме не обнаружены.
Отсутствие общетоксического действия позволяет рекомендовать фармацевтическую композицию, содержащую в качестве действующего вещества пептид H-Glu-Asp-Gly-OH, для проведения клинических испытаний в качестве лекарственного средства, используемого в клинической онкологии для лечения опухолей.
Изобретение относится к лекарственным средствам, используемым в клинической онкологии, и касается фармацевтической композиции, содержащей пептид, обладающий противоопухолевым действием, которая может быть использована в клинической практике для лечения опухолей. Предлагается фармацевтическая композиция и средство, обладающие противоопухолевым действием, содержащие в качестве действующего вещества эффективное количество пептида формулы H-Glu-Asp-Gly-OH и фармацевтически приемлемый носитель. При этом фармацевтическая композиция находится в форме, подходящей для парентерального введения. Заявленное изобретение обеспечивает противоопухолевое действие за счет торможения пролиферативной активности опухолевых клеток. 2 н. и 1 з.п. ф-лы, 2 табл.
1. Фармацевтическая композиция, обладающая противоопухолевым действием, содержащая в качестве действующего вещества эффективное количество пептида формулы H-Glu-Asp-Gly-OH и фармацевтически приемлемый носитель.
2. Фармацевтическая композиция по п.1, отличающаяся тем, что она находится в форме, подходящей для парентерального введения.
3. Средство, обладающее противоопухолевым действием, содержащее в качестве действующего вещества эффективное количество пептида глутамил-аспартил-глицин формулы H-Glu-Asp-Gly-OH и фармацевтически приемлемый носитель.
| ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО | 1993 |
|
RU2067870C1 |
| 0 |
|
SU75007A1 | |
| BD Registry Chemical abstract). | |||
Авторы
Даты
2009-07-27—Публикация
2007-11-26—Подача