Изобретение относится к лекарственным средствам для профилактики и лечения функциональных или стрессиндуцированных нарушений, возникающих при экстремальных воздействиях, и может быть использовано как средство, обладающее стресспротекторным действием.
Известно, что особенностью современной жизни является стресс, который включает в себя несколько проявлений, существенными из которых являются: адаптивная реакция организма; недостаточно адаптивная реакция; патологически зависимая адаптивная реакция от стресса; преждевременное старение организма, вызванное нервным, психическим и метаболическим истощением.
Из уровня техники неизвестны лекарственные средства, которые были бы эффективны для профилактики и лечения стресса во всех его проявлениях.
В зависимости от клинических проявлений стресса известно применение следующих препаратов: транквилизаторов, антидепрессантов, блокаторов бэта-адренергического рецептора, седативных и гипнотических средств, а также растительных адаптогенов.
Недостатками этих препаратов является то, что они применимы только для основного симптоматического лечения, они изменяют антистрессовые реакции адаптации организма и могут оказывать негативное побочное воздействие.
Известны композиции, включающие аминокислоты с витаминами или без них либо основанные на глутаматах (патент Румынии №76141) или на цистеине (патент Румынии №74505), аргинине (патент Франции №2494113), или составы, которые наряду с вышеуказанными аминокислотами содержат глицин, лизин, тирозин, орнитин, гистин (патент Франции №5937М, патент Румынии №76044).
К недостаткам указанных композиций можно отнести их неспецифическое действие и неспособность замедлять старение организма.
Указанные выше причины обусловливают необходимость разработки новых лекарственных средств.
Из уровня техники известен пептид глутамил-аспартил-глицин общей формулы: Н-Glu-Asp-Gly-OH (Регистрационный номер RN-75007-24-8 согласно STN int. BD Registry Chemical abstract).
При экспериментальном изучении пептида глутамил-аспартил-глицин общей формулы: H-Glu-Asp-Gly-OH было выявлено его ранее неизвестное свойство, проявляющееся в оказании стресспротекторного действия.
Настоящим изобретением поставлена и решена задача получения средства пептидной природы, обладающего стресспротекторным действием, фармацевтической композиции на его основе и способа ее применения.
Технический результат изобретения заключается в проявлении пептидом глутамил-аспартил-глицин формулы: H-Glu-Asp-Gly-OH стресспротекторного действия, применении его для изготовления фармацевтической композиции, содержащей этот пептид в качестве активного начала, использование которой позволяет регулировать уровень биогенных аминов в коре головного мозга и крови, влияя на экспрессию гена с-fos в различных структурах головного мозга и снижая активность энкефалиназ в крови, осуществляя таким образом стресспротекторное действие.
Возможность объективного проявления технического результата при использовании изобретения подтверждена достоверными данными, приведенными в примерах, содержащих сведения экспериментального характера, полученные в процессе проведения исследований по методикам, принятым в данной области, согласно которым экспериментальный стресс индуцировали у животных.
Настоящее изобретение относится к пептиду глутамил-аспартил-глицин общей формулы: H-Glu-Asp-Gly-OH последовательности 1 [SEQ ID NO:1], обладающему стресспротекторным действием.
Другой аспект настоящего изобретения касается фармацевтической композиции, обладающей стресспротекторным действием, содержащей в качестве активного начала эффективное количество пептида глутамил-аспартил-глицин общей формулы: H-Glu-Asp-Gly-OH [SEQ ID NO:1] и фармацевтически приемлемый носитель.
При этом фармацевтическая композиция находится в форме, подходящей для парентерального или интраназального введения.
Следующий аспект настоящего изобретения касается способа профилактики и/или лечения функциональных или стрессиндуцированных нарушений, возникающих при экстремальных воздействиях, заключающегося во введении пациенту фармацевтической композиции, содержащей в качестве активного начала эффективное количество пептида глутамил-аспартил-глицин общей формулы: H-Glu-Asp-Gly-OH последовательности 1 [SEQ ID NO:1] в дозе 0,01 - 100 мкг/кг массы тела, по крайней мере, один раз в день в течение периода, необходимого для достижения терапевтического эффекта.
При этом введение фармацевтической композиции осуществляют внутримышечно или интраназально капельно.
Пептид глутамил-аспартил-глицин общей формулы: H-Glu-Asp-Gly-OH получают классическим методом пептидного синтеза в растворе.
Изучение биологической активности проводили на интактных животных в экспериментальных моделях стресса с использованием сыворотки крови здоровых людей и на испытателях-добровольцах, подвергавшихся экстремальному воздействию пониженного парциального давления кислорода.
Понятие «фармацевтическая композиция» подразумевает различные лекарственные формы, содержащие новый пептид, которые могут найти лечебное применение в медицине в качестве средства, обладающего стресспротекторным действием.
Для получения фармацевтических композиций, отвечающих изобретению, эффективное количество пептида H-Glu-Asp-Gly-OH как активное начало смешивают с фармацевтически приемлемым носителем согласно принятым в фармацевтике способам компаундирования.
Понятие "эффективное количество" подразумевает использование такого количества активного начала, которое в соответствии с его количественными показателями активности и токсичности, а также на основании знаний специалиста должно быть эффективным в данной лекарственной форме.
Носитель может иметь различные формы, которые зависят от лекарственной формы препарата, желаемой для введения в организм.
Для парентерального введения носитель обычно включает физиологический раствор или стерильную воду, хотя могут быть включены другие ингредиенты, способствующие стабильности или для сохранения стерильности.
Для интраназального введения носитель обычно включает физиологический раствор или стерильную воду, хотя могут быть включены другие ингредиенты.
Сущность изобретения поясняется фигурами и таблицей.
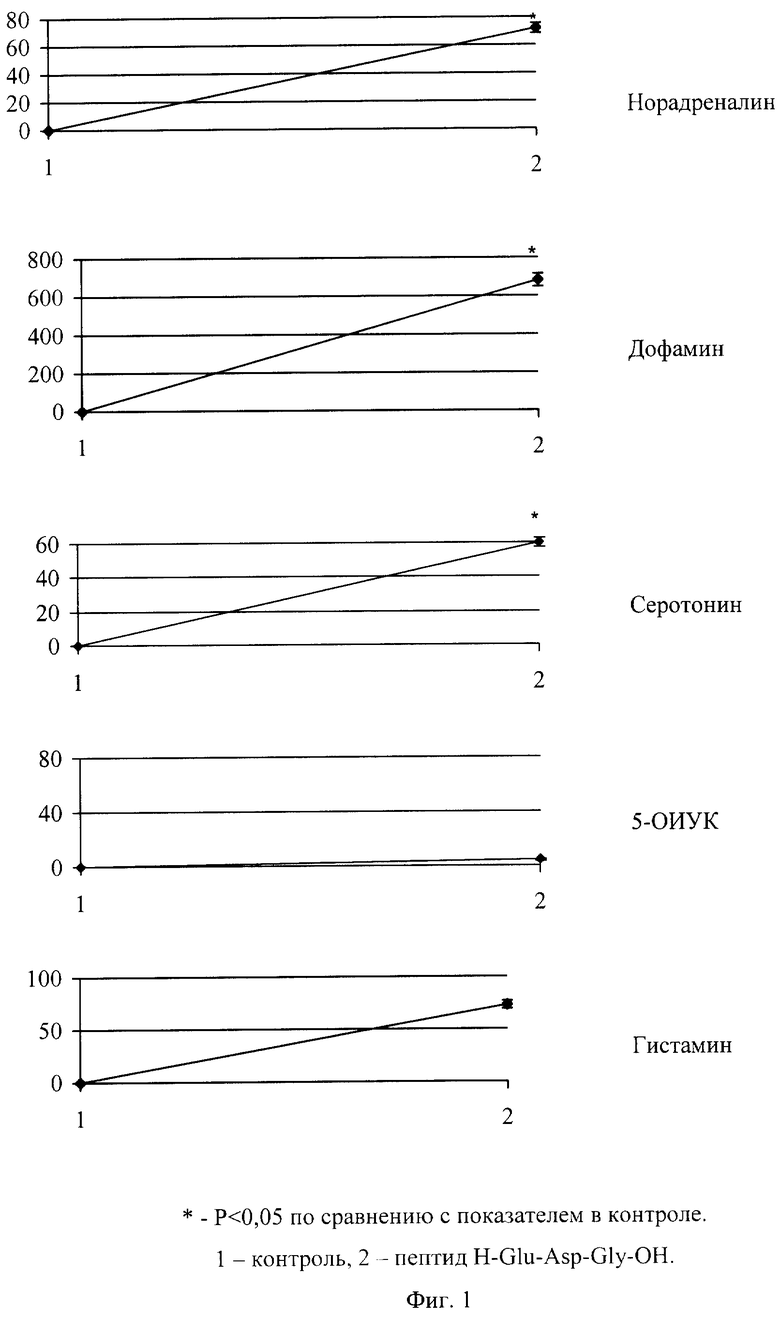
На Фиг.1 показано влияние пептида H-Glu-Asp-Gly-OH на уровень биогенных аминов в коре головного мозга крыс (в % по отношению к контролю).
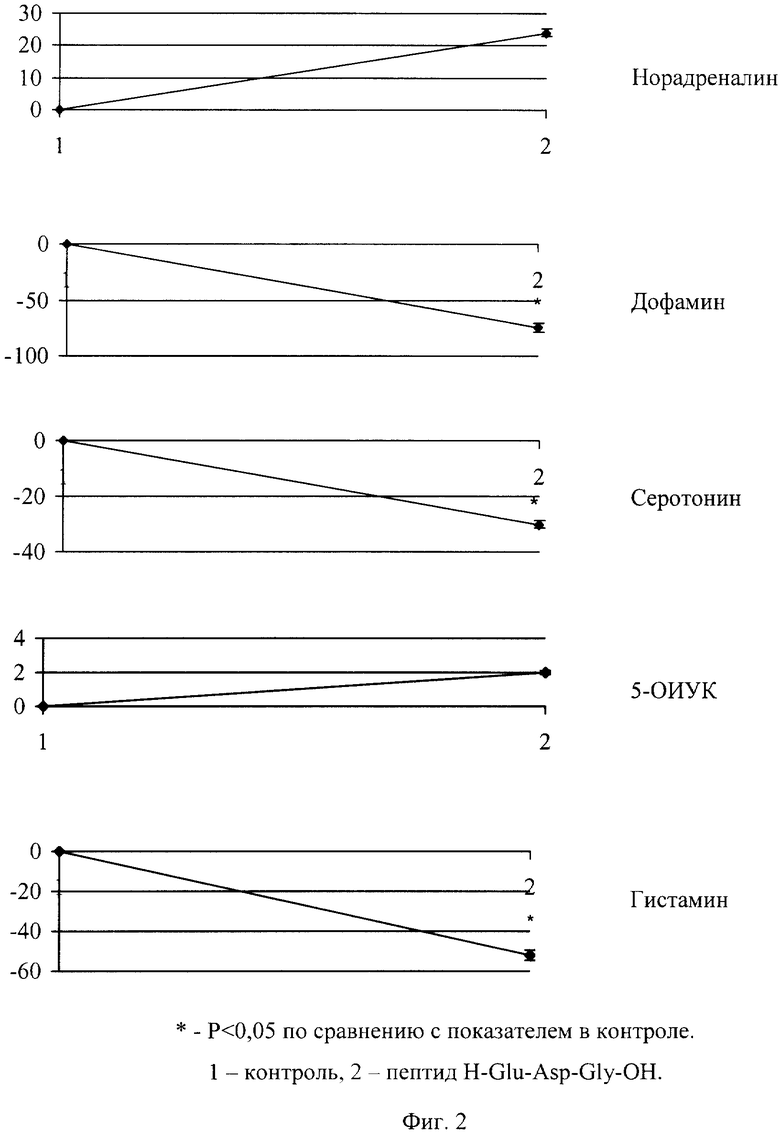
На Фиг.2 показано влияние пептида H-Glu-Asp-Gly-OH на уровень биогенных аминов в сыворотке крови крыс (в % по отношению к контролю).
На Фиг.3 представлено иммуногистохимическое определение содержания белка с-Fos в клетках эпифиза после осмотического стресса:
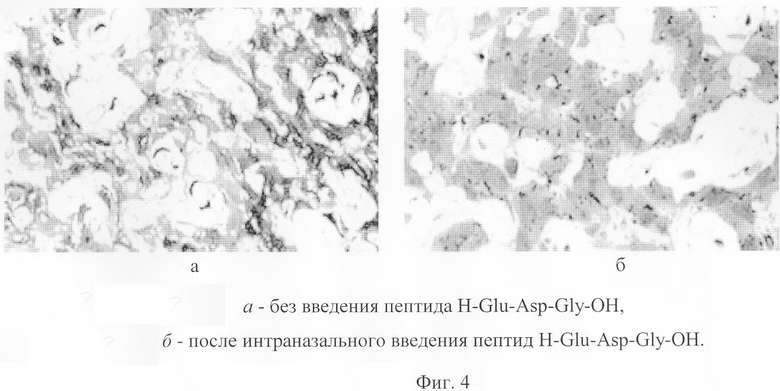
На Фиг.4 представлена паренхима эпифиза после осмотического стресса.
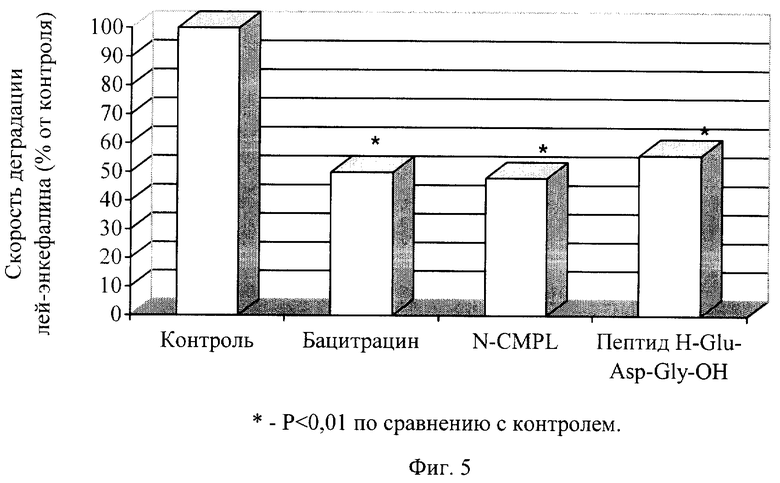
На Фиг.5 показано влияние пептида H-Glu-Asp-Gly-OH на энкефалиназную активность сыворотки крови людей.
В Таблице представлено влияние пептида H-Glu-Asp-Gly-OH на морфологические и биохимические показатели периферической крови морских свинок при изучении токсичности.
Изобретение иллюстрируется примером синтеза пептида глутамил-аспартил-глицин общей формулы: H-Glu-Asp-Gly-OH (пример 1), примерами, подтверждающими проявление биологической активности пептида (примеры 2, 3, 4, 5), примером изучения токсичности (пример 6), а также примером результатов клинического применения пептида, демонстрирующим его фармакологические свойства и подтверждающим возможность достижения профилактического и/или лечебного эффекта (пример 7).
Пример 1. Синтез пептида H-Glu-Asp-Gly-OH
1. Название соединения: глутамил-аспартил-глицин.
2. Структурная формула: Н-Glu-Asp-Cly-ОН
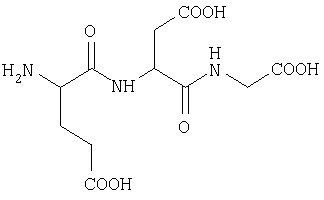
3. Брутто-формула без противоиона: С11Н17N3O8.
4. Молекулярный вес без противоиона: 319,27.
5. Противоион: ацетат.
6. Внешний вид: белый аморфный порошок без запаха.
7. Способ синтеза: пептид получен классическим методом синтеза в растворе по схеме:
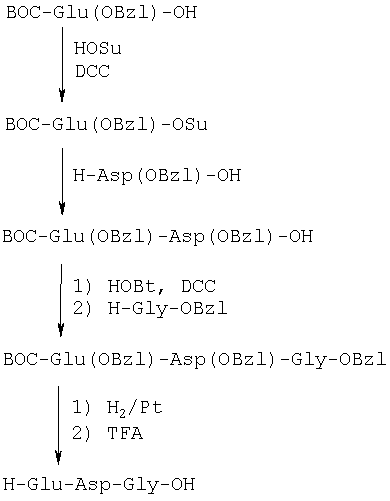
ВОС - трет.бутилоксикарбонильная группа,
OSu - N-оксисукцинимидный эфир,
DCC - N,N'-дициклогексилкарбодиимид,
OBzl - бензиловый эфир,
TFA - трифторуксусная кислота,
HOBt - N-оксибензотриазол.
Характеристики готового препарата:
- Содержание основного вещества: 97,93% ( по ВЭЖХ, 220 нм),
- ТСХ - индивидуален, Rf=0,45 (ацетонитрил-вода 1:2),
- Содержание влаги: 6%,
- рН 0,01% раствора: 4,9,
- Удельное оптическое вращение: [α]D 22: - 31° (с=1, H2O), "Polamat A", Carl Zeiss Jena.
Пример синтеза:
1) BOC-Glu(OBzl)-OSu, N-оксисукцинимидный эфир N-трет.бутилоксикарбонил-(γ-бензил)глутаминовой кислоты (I).
N-трет.бутилоксикарбонил-(γ-бензил)глутаминовую кислоту BOC-Glu(OBzl)-OH (33,7 г, 0,1 моль) растворяли в 50 мл N,N'-диметилформамида, охлаждали до температуры -10°С, добавляли при перемешивании охлажденные (4-6°С) растворы N,N'-дициклогексилкарбодиимида (23,0 г, 0,11 моль) в 30 мл N,N'-диметилформамида и N-гидроксисукцинимида (13,0 г, 0,11 моль) в 20 мл N,N'-диметилформамида. Реакционную смесь перемешивали в течение 12 ч при охлаждении льдом и далее в течение 1 суток при комнатной температуре. Выпавшую N,N'-дициклогексилмочевину отфильтровывали и полученный раствор активированного эфира использовали без выделения на следующей стадии.
2) BOC-Glu(OBzl)-Asp(OBzl)-OH, N-трет.бутилоксикарбонил-(γ-бензил)глутамил-(β-бензил)аспартат (II)
(β-Бензил) аспарагиновую кислоту H-Asp(OBzl)-OH (28,0 г, 0,12 моль) и 36 мл (0,12 моль) триэтиламина суспендировали в 50 мл N,N'-диметилформамида и перемешивали в течение 1 ч. Затем добавили порциями раствор активированного эфира ВОС-Glu(OBzl)-OSu (I), полученный на предыдущей стадии. Реакционную смесь перемешивали при комнатной температуре в течение 2 суток. Затем подкисляли 0,5 н. серной кислотой до рН 2-3 и экстрагировали этилацетатом 4×50 мл. Вытяжки объединяли и последовательно промывали 0,5 н. H2SO4 3×50 мл, водой 2×50 мл, 5% раствором NaHCO3 2×50 мл, водой 2×50 мл, насыщенным раствором NaCI 2×50 мл. Органический слой сушили над Na2SO4, упаривали растворитель в вакууме, остаток кристаллизовали под гексаном. Получено 50 г продукта (92%). Rf=0,34 (бензол-ацетон 2:1).
3) BOC-Glu(OBzl)-Asp(OBzl)-Gly-OBzl (III), бензиловый эфир N-трет.бутилоксикарбонил-(γ-бензил)глутамил-(β-бензил)аспартил-глицина (III)
2,7 г (5 ммоль) дипептида и 0,95 г (7 ммоль) оксибензотриазола растворяли в тетрагидрофуране (10 мл) и охлаждали до температуры -10°С. 1,44 г (7 ммоль) дициклогексилкарбодиимида растворяли в 5 мл тетрагидрофурана и охлаждали до той же температуры. 3,4 г (10 ммоль) тозилата бензилового эфира глицина растворяли в 10 мл тетрагидрофурана, добавляли 1,4 мл (10 ммоль) триэтиламина и охлаждали до той же температуры. При охлаждении на ледяной бане и интенсивном перемешивании объединяли растворы дипептида с оксибензотриазолом и карбодиимида, через 10 мин добавляли раствор тозилата бензилового эфира глицина. Реакционную смесь перемешивали в течение 3 ч при охлаждении льдом и в течение 1 суток при комнатной температуре. Выпавшую дициклогексилмочевину отфильтровывали, фильтрат упаривали в вакууме, остаток растворяли в этилацетате (100 мл). Раствор промывали последовательно 0,5 н. серной кислотой, водой, 5% раствором бикарбоната натрия, водой, сушили над безводным сульфатом натрия. Этилацетат упаривали в вакууме, кристаллизация остатка в системе этилацетат/гексан. Перекристаллизация из изопропанола. Получено после сушки в вакууме 2,74 г продукта (85%). Rf=0,78 (бензол-ацетон 1:1).
4) H-Glu-Asp-Gly-OH (IV), глутамил-аспартил-глицин
Защищенный трипептид BOC-Glu(OBzl)-Asp(OBzl)-Gly-OBzl (III) (2,7 г) растворяли в смеси метиловый спирт - вода (4:1) (50 мл) и гидрировали над катализатором Pd/C (5%) в течение 4 ч. Катализатор отфильтровывали, растворитель упаривали в вакууме, остаток сушили в вакууме над КОН и P2O5. Далее продукт растворяли в 15 мл смеси хлористый метилен-трифторуксусная кислота (5:1) и выдерживали при комнатной температуре в течение 2 ч. Полноту прохождения реакции деблокирования контролировали по ТСХ в системе ацетонитрил-вода (1:3). Растворитель упаривали в вакууме, остаток сушили в вакууме над КОН.
Для очистки 300 мг препарата растворяли в 4 мл 0,01% трифторуксусной кислоты и подвергали высокоэффективной жидкостной хроматографии на колонке с обращенной фазой 50×250 мм Diasorb-130-C16T, 7 mkm. Хроматограф Beckman System Gold, 126 Solvent Module, 168 Diode Array Detector Module. Условия хроматографирования А: 0,1% TFA; В: MeCN/0,1% TFA, градиент В 0 → 50% за 100 мин. Объем пробы 5 мл, детекция при 215 нм, сканирование 190-600 нм, скорость потока 10 мл/мин. Отбирали фракцию основного пика. Растворитель упаривали в вакууме при температуре не выше 40°С, упаривание многократно (5 раз) повторяли с 10 мл 10% раствора уксусной кислоты.
Окончательно остаток растворяли в 20 мл деионизованной воды и лиофилизовывали. Получено 150 мг очищенного препарата в виде аморфного белого порошка без запаха.
5) Анализ готового препарата
- Содержание основного вещества определяли методом ВЭЖХ на колонке Phenomenex С 18 LUNA 4,6×150 mm. A: 0,1% TFA, В: MeCN; grad. B 0-100% in 10 min. Скорость потока 1 мл/ мин. Детекция при 220 нм, сканирование 190-600 нм, проба 20 μl. Содержание основного вещества 97,93%.
- ТСХ: индивидуален, Rf = 0,45 (ацетонитрил-вода 1:2, пластинки ПТСХ-П-В-УФ Sorbfil, силикагель СТХ-1ВЭ 8-12 мкм, проявление хлор/бензидин).
- Содержание влаги: 6% (гравиметрически по потере массы при сушке 20 мг при 100°С).
- рН 0,01% раствора: 4,9 (потенциометрически).
- Удельное оптическое вращение: [α]D 22: -31°(с=1, Н2О), "Polamat A", Carl Zeiss Jena.
Пример 2. Влияние пептида H-Glu-Asp-Gly-OH на уровень биогенных аминов в коре головного мозга и сыворотке крови у крыс
Исследование проведено на 27 белых крысах обоего пола массой 300-320 г.
Пептид H-Glu-Asp-Gly-OH животным подопытных групп вводили внутрибрюшинно в дозе 2,5 мкг/кг массы тела в 0,5 мл стерильного физиологического 0,9% раствора NaCl ежедневно в течение 5 суток.
Крысам контрольной группы по аналогичной схеме вводили стерильный физиологический раствор в том же объеме.
После окончания введения препаратов животных декапитировали, затем в коре головного мозга и сыворотке крови определяли содержание норадреналина, дофамина, 5-оксииндолуксусной кислоты (5-ОИУК), серотонина и гистамина.
Установлено, что введение пептида животным способствовало значительным сдвигам в уровне биогенных аминов в коре головного мозга и сыворотке крови.
Так, после введения пептида H-Glu-Asp-Gly-OH крысам в коре головного мозга наблюдалось достоверное увеличение содержания норадреналина, дофамина и серотонина (Фиг.1).
При этом в сыворотке крови наблюдалось снижение содержания дофамина, серотонина и гистамина (Фиг.2).
Таким образом, в результате проведенного исследования установлено, что пептид H-Glu-Asp-Gly-OH оказывает модулирующее воздействие на содержание биогенных аминов в коре головного мозга и сыворотке крови, что свидетельствует о влиянии этого пептида на центральные и периферические механизмы регуляции стресса.
Пример 3. Влияние пептида H-Glu-Asp-Gly-OH на экспрессию гена c-fos в нейронах паравентрикулярного ядра гипоталамуса крыс при эмоциональном стрессе
Эмоциональный стресс усиливает экспрессию ранних генов в разных структурах мозга. Известным маркером активации нейрональных клеток является продукт гена немедленного ответа - c-Fos-белок, выполняющий функцию посредника между изменением характера транскрипции под действием стимула и реализацией информационного сигнала в долгосрочные фенотипические изменения. Белки семейства Fos активируются в нейронах в разное время после поступления стимула. Так, экспрессия c-fos мРНК начинается уже через несколько минут и достигает максимума через 30-60 мин после поступления стимула. Максимальный синтез c-Fos-белка наблюдается между 1-м и 3-м часом, а через 4-6 ч после предъявления стимула происходит снижение его синтеза в нейронах. Экспрессия гена c-fos в головном мозге животных, устойчивых и предрасположенных к эмоциональному стрессу, различна. Наиболее интенсивная экспрессия гена c-fos выявлена в структурах мозга (кора, миндалина, гипоталамус и ствол мозга) у предрасположенных к эмоциональному стрессу крыс. У особей, устойчивых к эмоциональному стрессу, в аналогичных условиях эксперимента экспрессия гена c-fos определялась только в инфралимбической коре и обонятельных ядрах.
В эксперименте изучали влияние пептида H-Glu-Asp-Gly-OH на экспрессию гена с-fos в паравентрикулярном ядре гипоталамуса (PVH) устойчивых и предрасположенных к эмоциональному стрессу животных, а также у крыс, подвергнутых эмоциональному стрессу.
Эксперименты были проведены на 28 крысах линии Вистар.
Поведение животных предварительно (для прогнозирования степени их устойчивости к эмоциональному стрессу) оценивали в тесте "открытое поле". Эффективность применения пептида H-Glu-Asp-Gly-OH изучали у устойчивых и предрасположенных к эмоциональному стрессу особей.
Пептид H-Glu-Asp-Gly-OH вводили внутрибрюшинно в дозах 0,1 и 0,01 мкг на крысу в 0,5 мл стерильного физиологического 0,9% раствора NaCl через 7-10 дней после первого теста. Через 1 ч после инъекции пептида животных подвергали 60-минутному эмоциональному стрессу, который создавали, ограничивая их подвижность.
Для идентификации клеток, содержащих белок Fos - продукт ранней экспрессии гена c-fos - провели иммуногистохимическое исследование срезов мозга с автоматизированным подсчетом Fos-позитивных клеток. Особенности индукции гена с-fos изучали в PVH.
Число Fos-позитивных клеток в PVH у крыс, прогностически устойчивых к эмоциональному стрессу, оказалось достоверно выше, чем у животных, предрасположенных к эмоциональному стрессу. Это отмечалось у крыс обеих контрольных групп (не подвергнутых стрессу и после эмоционального стресса).
Введение пептида H-Glu-Asp-Gly-OH в дозе 0,01 мкг приводило к увеличению количества Fos-позитивных нервных клеток у крыс, устойчивых к стрессу, не подвергавшихся стрессорному воздействию и на фоне стресса. Напротив, пептид H-Glu-Asp-Gly-OH в дозе 0,1 мкг способствовал снижению числа Fos-позитивных нервных клеток в PVH как у устойчивых, так и у предрасположенных к стрессу животных. На фоне стресса у устойчивых крыс пептид H-Glu-Asp-Gly-OH в дозе 0,1 мкг увеличивал количество Fos-позитивных нейронов.
Таким образом, были выявлены дозозависимые стресспротекторные эффекты пептида H-Glu-Asp-Gly-OH, проявляющиеся в усилении экспрессии гена c-fos и направленные на активацию нейронов и формирование адаптационных реакций.
Пример 4. Влияние пептида H-Glu-Asp-Gly-OH на содержание белка c-Fos в эпифизе крыс при осмотическом стрессе
Эпифиз наряду с гипоталамо-гипофизарным комплексом вовлекается в формирование множественных адаптационных ответов организма на стрессорное воздействие. При стрессе усиливается продукция эпифизом мелатонина и веществ пептидной природы, обладающих способностью ослаблять негативное воздействие на организм окислительного, осмотического, психического и других видов стресса.
Эпифиз принадлежит к нейрогемальным органам, лишенным гематоэнцефалического барьера, поэтому он очень чувствителен к высокомолекулярным биологически активным веществам, циркулирующим с мозговым кровотоком, особенно к пептидам. Уникальное положение обонятельной системы, химическая связь одновременно с окружающей средой и с ЦНС позволяет веществам неинвазивно проникать в мозговой кровоток и в нейрогемальные органы. Существует постоянная диффузия ликвора через подпаутинное пространство вдоль факторных нейронов к носовой подслизистой и носовой лимфатической системе.
В эксперименте изучали влияние пептида H-Glu-Asp-Gly-OH при интраназальном применении на содержания белка c-Fos в эпифизе крыс при стрессе. Для иммуногистохимического определения содержания белка c-Fos использовали интактных и подвергнутых 48-часовому осмотическому стрессу крыс, которым интраназально вводили пептид H-Glu-Asp-Gly-OH в дозе 0,5 мкг на животное в 0,1 мл стерильного физиологического 0,9% раствора NaCl (последняя инфузия проводилась за 2 ч до взятия материала). В это же время проводили светооптическое исследование состояния паренхимы эпифиза у животных всех групп.
Белок c-Fos является одним из триггеров, запускающих синтетические процессы в эпифизе при действии экстремальных факторов, в частности при стрессе. В наших опытах почти полное отсутствие белка c-Fos в эпифизе крыс при осмотическом стрессе, вероятно, было связано с хроническим характером этого стресса, поскольку наибольшее содержание продуктов гена c-fos наблюдается через 1-2 ч после воздействия стрессорного фактора. Хронический стресс подавляет активность гена c-fos в PVH из-за повышения в плазме крови уровня глюкокортикоидов.
Небольшое, но достоверное повышение содержания белка c-Fos в пинеалоцитах при стрессе наблюдалось только после интраназального введения пептида H-Glu-Asp-Gly-OH (Фиг.3).
Данный эффект пептида H-Glu-Asp-Gly-OH наблюдался только при стрессе. Это свидетельствует о том, что пептид H-Glu-Asp-Gly-OH участвует в пептидной саморегуляции деятельности эпифиза при экстремальных состояниях организма.
Было обнаружено, что белок c-Fos неравномерно содержится в разных пинеалоцитах. При стрессе выявляются кластеры (по 5-10 клеток), содержащие c-Fos в цитоплазме. Возможно, эти кластеры пинеалоцитов являются группами взаимодействующих клеток.
При оценке состояния паренхимы эпифиза было установлено, что возникающее при осмотическом стрессе расширение капилляров и перикапиллярного пространства (Фиг.4) частично устранялось интраназальным введением пептида H-Glu-Asp-Gly-OH.
Таким образом, пептид H-Glu-Asp-Gly-OH оказывает влияние на пинеальную железу при воздействии на организм экстремальных факторов. Пептид H-Glu-Asp-Gly-OH препятствует патологическим структурным изменениям паренхимы эпифиза при осмотическом стрессе и его действие на эпифиз опосредовано активацией системы определенных генов.
Пример 5. Влияние пептида H-Glu-Asp-Gly-OH на активность энкефалиназ в сыворотке крови людей
Целью данного исследования было определение опиоидной активности пептида Н-Glu-Asp-Gly-OH. Опиоидная активность может быть обусловлена как взамодействием пептидов с опиоидными рецепторами разного типа, так и ингибированием энкефалиназ, приводящим к соответствующему увеличению концентрации нативных энкефалинов.
Способность пептида H-Glu-Asp-Gly-OH влиять на активность ферментов деградации эндогенных опиоидных пептидов - энкефалинов оценивали в кинетических исследованиях по расщеплению малых концентраций (0,15 мкМ) [3H]Лей-энкефалина ферментами сыворотки крови человека. В качестве препаратов сравнения использовали общепринятые ингибиторы энкефалиназ М-карбоксиметил-Phe-Leu (N-CMPL) и бацитрацин. Определяли суммарную энкефалиназную активность сыворотки крови, полученной от 5 здоровых доноров, in vitro. Результаты оценивали после проведения 4 исследований.
На Фиг.5 показано влияние пептида H-Glu-Asp-Gly-OH на энкефалиназную активность сыворотки крови людей.
В результате исследования установлено, что пептид H-Glu-Asp-Gly-OH, добавленный в культуральную среду в конечной концентрации 10 мкг/мл, ингибировал активность энкефалиназ сыворотки крови (Фиг.5). Причем степень ингибирования была сравнима с таковой для N-CMPL (10 мкг/мл) и бацитрацина (50 мкг/мл).
Известно, что время ферментативной деградации энкефалинов в крови измеряется минутами, поэтому именно эти ферменты в наибольшей степени определяют периферические биологические эффекты эндогенных опиоидных пептидов. Применение пептида H-Glu-Asp-Gly-OH, ингибирующего активность энкефалиназ сыворотки крови, направлено на сохранение регуляторных свойств эндогенных опиоидных пептидов, что является основанием использования его для коррекции стрессиндуцированных нарушений.
Пример 6. Изучение токсичности пептида H-Glu-Asp-Gly-OH
Общетоксическое действие пептида H-Glu-Asp-Gly-OH исследовали в соответствии с требованиями «Руководства по экспериментальному (доклиническому) изучению новых фармакологических веществ» (2000): острой токсичности при однократном введении препарата, а также подострой и хронической токсичности при длительном введении пептида.
Исследование по изучению острой токсичности проведено на 66 белых беспородных мышах-самцах массой 20-22 г. Животные были рандомизированно разделены на 6 равных групп. Препарат вводили животным однократно внутримышечно в дозах 1, 2, 3, 4, 5 мг/кг в 0,25 мл стерильного 0,9% раствора NaCl. Животным контрольной группы в том же объеме вводили 0,9% раствор NaCl.
Исследования по изучению подострой токсичности проведено на 64 белых беспородных крысах-самцах массой 180-220 г. Ежедневно однократно животным подопытных групп вводили препарат внутримышечно в течение 90 дней в дозах 1 мкг/кг, 0,1 мг/кг, 1 мг/кг в 0,5 мл стерильного 0,9% раствора NaCl. Животным контрольной группы вводили в том же объеме стерильный 0,9% раствор NaCl. До введения препарата, на 30, 60 и 90 сутки после начала введения препарата у животных исследовали морфологический состав и свойства периферической крови. При завершении эксперимента исследовали биохимические и коагулологические показатели крови.
Исследования по изучению хронической токсичности проводили в течение 6 месяцев исходя из длительности рекомендуемого клинического назначения препарата на 92 морских свинках-самцах массой 310-350 г. Животные подопытных групп получали ежедневно однократно внутримышечно пептид в течение 6 мес в дозах 1 мкг/кг, 0,1 мг/кг, 1 мг/кг в 0,5 мл стерильного 0,9% раствора NaCl. В контрольной группе животным вводили по аналогичной схеме стерильный 0,9% раствор NaCl в том же объеме. У животных в периферической крови общепринятыми методами определяли: количество эритроцитов, гемоглобина, ретикулоцитов, тромбоцитов, лейкоцитов, лейкоцитарную формулу, скорость оседания эритроцитов (СОЭ), резистентность эритроцитов. Наряду с этим определяли содержание в сыворотке крови общего белка по методу Лоури, калия и натрия методом плазменной спектрофотометрии. После завершения эксперимента проводили патоморфологическое исследование головного и спинного мозга, спинномозговых ганглиев, щитовидной железы, паращитовидных желез, надпочечников, семенников, гипофиза, сердца, легких, аорты, печени, почки, мочевого пузыря, поджелудочной железы, желудка, тонкой кишки, толстой кишки, тимуса, селезенки, лимфатических узлов, костного мозга.
При изучении острой токсичности установлено, что однократное введение исследуемого пептида животным в дозе, превышающей терапевтическую, рекомендованную для клинического применения, более чем в 5000 раз, не вызывает токсических реакций, что свидетельствует о большой терапевтической широте препарата.
Изучение подострой и хронической токсичности пептида свидетельствует об отсутствии побочных эффектов при длительном применении препарата в дозах, превышающих терапевтическую в 100-1000 раз. При исследовании влияния пептида на морфологический состав крови морских свинок установлено увеличение количества лейкоцитов через 3 месяца после начала введения препарата, которое нормализовалось к 6-му месяцу наблюдения (Таблица). Остальные показатели морфологического состава крови животных практически не изменялись. Не отмечено достоверного влияния препарата на СОЭ, резистентность эритроцитов и биохимические показатели сыворотки крови.
При оценке общего состояния животных, морфологических и биохимических показателей периферической крови, морфологического состояния внутренних органов, состояния сердечно-сосудистой и дыхательной систем, функции печени и почек патологические изменения в организме не обнаружены.
Отсутствие общетоксического действия позволяет рекомендовать фармацевтическую композицию, содержащую в качестве активного начала пептид Н-Glu-Asp-Gly-OH, для проведения клинических испытаний.
Пример 7. Влияние пептида H-Glu-Asp-Gly-OH на функциональное состояние человека при воздействии пониженного парциального давления кислорода
Для оценки влияния пептида H-Glu-Asp-Gly-OH на функциональное состояние и работоспособность человека в экстремальных условиях воздействия пониженного парциального давления кислорода было обследовано 80 практически здоровых мужчин в возрасте 20-22 лет. Испытатели были разделены на 3 группы: в контрольную группу вошли 20 человек, в I и II основные - по 30 человек в каждой. В первый день исследования проводилось фоновое обследование, включавшее исследование дыхательной, сердечно-сосудистой и центральной нервной систем.
После окончания фонового обследования испытатели I основной группы начинали принимать фармацевтическую композицию, содержащую в качестве активного начала пептид H-Glu-Asp-Gly-OH интраназально капельно в дозе 5,0 мг в 1 мл физиологического раствора (I подгруппа), в дозе 100,0 мкг (II подгруппа) и в дозе 1,0 мкг в 1,0 мл физиологического раствора (III подгруппа) 3 раза в день в течение 2-х дней. Таким образом, испытатели I основной группы получали пептид H-Glu-Asp-Gly-OH интраназально в дозе 10 мг (I подгруппа), 200 мкг (II подгруппа) и 2 мкг (III подгруппа) на курс.
Испытатели II основной группы после окончания фонового обследования начинали принимать фармацевтическую композицию, содержащую в качестве активного начала пептид H-Glu-Asp-Gly-OH, внутримышечно в дозе 5,0 мг в 1 мл физиологического раствора (I подгруппа), в дозе 100,0 мкг (II подгруппа) и в дозе 1,0 мкг в 1,0 мл физиологического раствора (III подгруппа) ежедневно однократно в течение 2-х дней.
Испытатели контрольной группы получали плацебо в виде воды для инъекций.
На четвертый день эксперимента испытателей трех групп подвергали воздействию гипоксической гипоксии методом «подъема» в барокамере СБК-80 на высоту 5000 м с экспозицией 60 мин без дополнительного кислородного обеспечения. До начала подъема, в процессе и после окончания подъема испытателей обследовали по сокращенной схеме. На пятый день исследования проводилось заключительное итоговое обследование в полном объеме. Реактивная тревожность на протяжении исследования у всех испытателей соответствовала уровню умеренной тревожности (31-45 баллов). Однако в пределах этого уровня наблюдалась разнонаправленная динамика этого показателя у испытателей разных групп. После двухдневного применения фармацевтической композиции, содержащей в качестве активного начала пептид H-Glu-Asp-Gly-OH в разных дозировках, реактивная тревожность у испытателей снижалась на 10-13% в зависимости от дозировки и способа введения фармацевтической композиции по сравнению с испытателями контрольной группы. На следующий день после воздействия гипоксии реактивная тревожность у испытателей контрольной группы, принимавших плацебо, была на 9-10% выше исходных данных, а на фоне применения фармацевтической композиции, содержащей в качестве активного начала пептид H-Glu-Asp-Gly-OH в разных дозировках не зависимо от способа введения, соответствовала исходным показателям. Сходную динамику изменений имели показатели теста "САН" (самочувствие, активность, настроение).
В условиях гипоксической гипоксии субъективное состояние ухудшалось у испытателей трех групп, но в разной степени. У лиц, принимавших фармацевтическую композицию, содержащую в качестве активного начала пептид H-Glu-Asp-Gly-OH, субъективное состояние оставалось на исходном уровне при внутримышечном способе введения препарата в разных дозировках или ухудшалось на 4-5% у испытателей при интраназальном способе введения, тогда как у лиц, принимавших плацебо, - на 10-15%. На следующий день после гипоксии субъективное состояние испытателей, принимавших фармацевтическую композицию, содержащую в качестве активного начала пептид H-Glu-Asp-Gly-OH, было лучше исходных данных на 15% при внутримышечном способе введения или на 10% при интранальном способе введения, тогда как у лиц, принимавших плацебо, на 4-5% хуже. Следует отметить, что наиболее стабильные показатели регистрировались у лиц, получавших исследуемую композицию в дозировке 5,0 мг как при внутримышечном, так и при интраназальном способе введения.
Полученные данные свидетельствуют о том, что пептид H-Glu-Asp-Gly-OH оказывает заметное влияние на субъективное состояние испытателей, снижая эмоциональные и поведенческие проявления стресса, уменьшая тревожность, повышая активность, улучшая самочувствие, настроение. Объективно испытатели, принимавшие фармацевтическую композицию, содержащую в качестве активного начала пептид Н-Glu-Asp-Gly-OH в разных дозировках как внутримышечно, так и интраназально, лучше переносили гипоксическую гипоксию. Хорошая переносимость гипоксии отмечена у 80-90% испытателей, принимавших пептид H-Glu-Asp-Gly-OH, и только у 60% испытателей, принимавших плацебо.
Динамика частоты сердечных сокращений (ЧСС) была одинаковой у обследуемых всех групп. Под действием гипоксии ЧСС достоверно возрастала: у испытателей, принимавших фармацевтическую композицию, содержащую в качестве активного начала пептид H-Glu-Asp-Gly-OH, на 10-20% в зависимости от дозы и способа введения, а у лиц, принимавших плацебо, - на 30-40%. После окончания гипоксической пробы ЧСС у испытателей, принимавших фармацевтическую композицию, содержащую в качестве активного начала пептид H-Glu-Asp-Gly-OH, соответствовала исходным показателям, а у испытателей, принимавших плацебо, на 6-7% превышала их. Систолическое артериальное давление возвращалось к исходным данным у испытателей, принимавших фармацевтическую композицию, содержащую в качестве активного начала пептид H-Glu-Asp-Gly-OH, к 10-15-ой минуте в разных подгруппах, а у испытателей, принимавших плацебо, только после окончания гипоксии.
Динамика изменения диастолического артериального давления у испытателей была сходной: прирост в первые 10 минут действия гипоксии и постепенное снижение в дальнейшем. Физическая работоспособность в конце исследования возрастала по сравнению с фоновыми данными у всех испытателей, но в разной степени. Так, индекс физической работоспособности (PWC170) и максимальное потребление кислорода у испытателей, принимавших фармацевтическую композицию, содержащую в качестве активного начала пептид H-Glu-Asp-Gly-OH, увеличивались на 15-20% в зависимости от дозы и способа введения, а в группе плацебо - лишь на 10-11%. Особенностью действия пептида H-Glu-Asp-Gly-OH явилось снижение легочной вентиляции при дозированной физической нагрузке после воздействия гипоксии.
Из представленного материала видно, что функциональное состояние в процессе проведения гипоксической пробы у испытателей, принимавших фармацевтическую композицию, содержащую в качестве активного начала пептид H-Glu-Asp-Gly-OH в разных дозировках, было более адекватным с физиологической точки зрения, чем у испытателей, принимавших плацебо.
Таким образом, изучение эффективности применения пептида H-Glu-Asp-Gly-OH в исследованиях с участием испытателей-добровольцев, подвергавшихся "подъему" в барокамере на высоту 5000 м без дополнительного кислородного обеспечения, показало, что испытатели, принимавшие фармацевтическую композицию, содержащую в качестве активного начала пептид H-Glu-Asp-Gly-OH, лучше переносили гипоксическое воздействие как по объективным признакам, так и субъективно. Выявленный дозозависимый эффект позволяет рекомендовать применение исследуемой фармацевтической композиции в дозах от 5 мг до 1 мкг в 1 мл физиологического раствора как внутримышечно, так и интраназально в зависимости от степени нарушений функционального состояния испытателей.
Изменения физиологических показателей в группе испытателей, принимавших фармацевтическую композицию, содержащую пептид H-Glu-Asp-Gly-OH, были более сглаженными и характеризовались быстрым восстановлением до фоновых значений, что свидетельствует о стресспротекторных свойствах пептида H-Glu-Asp-Gly-OH.
72,9±3,1
73,6±2,8
73,1±3,4
72,3±2,9

Изобретение относится к лекарственным средствам для профилактики и лечения функциональных или стрессиндуцированных нарушений, возникающих при экстремальных воздействиях, и может быть использовано как средство, обладающее стресспротекторным действием. Предлагается пептид глутамил-аспартил-глицин общей формулы: H-Glu-Asp-Gly-OH последовательности 1 [SEQ ID NO:1], обладающий стресспротекторным действием. Предлагается фармацевтическая композиция, обладающая стресспротекторным действием, содержащая в качестве активного начала эффективное количество пептида глутамил-аспартил-глицин общей формулы: H-Glu-Asp-Gly-OH последовательности 1 [SEQ ID NO:1] и фармацевтически приемлемый носитель. Предлагается способ профилактики и/или лечения функциональных или стрессиндуцированных нарушений, возникающих при экстремальных воздействиях, заключающийся во введении пациенту фармацевтической композиции, содержащей в качестве активного начала эффективное количество пептида глутамил-аспартил-глицин общей формулы: H-Glu-Asp-Gly-OH последовательности 1 [SEQ ID NO:1] в дозе 0,01-100 мкг/кг массы тела, по крайней мере, один раз в день в течение периода, необходимого для достижения терапевтического эффекта. Изобретение раскрывает стресспротекторное действие пептида H-Glu-Asp-Gly-OH, применение его для изготовления фармацевтической композиции, использование которой позволяет регулировать уровень биогенных аминов в коре головного мозга и крови, влияя на эксперессию гена c-fos в различных структурах головного мозга и снижая активность энкефалиназ в крови, осуществляя таким образом стресспротекторное действие. 3 н. и 2 з.п. ф-лы, 5 ил., 1 табл.
| ЕР 1018341 A1, 05.02.1998 | |||
| АДАПТОГЕН СТРЕСС-КОРРЕКТОР И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 1999 |
|
RU2155064C1 |
| ПЕПТИДЫ, ОБЛАДАЮЩИЕ АНТИСТРЕССОРНЫМ, ПРОТИВОСУДОРОЖНЫМ И НЕЙРОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ | 1997 |
|
RU2115660C1 |
| СОСТАВ, ОБЛАДАЮЩИЙ СТРЕССОПРОТЕКТОРНЫМ И ПРОТИВОАТЕРОСКЛЕРОТИЧЕСКИМ ДЕЙСТВИЕМ | 1990 |
|
RU2033184C1 |
| ОПУСКНОЙ КОЛОДЕЦ | 1998 |
|
RU2134326C1 |
Авторы
Даты
2007-08-20—Публикация
2006-05-23—Подача