Настоящее изобретение относится к химии и химической технологии, а более конкретно - к синтезу представителей нового класса органических соединений, N,N'-дифторборильных комплексов N-(3-арил-2Н-изоиндол-1-ил)-N-(3-арил-1Н-изоиндол-1-илиден)аминов (3,3'-диарилазадиизоиндолилметенов). Эти соединения могут быть использованы, например, в качестве органических красителей и люминофоров, а также как фотосенсибилизаторы для фотодинамической терапии (ФДТ).
Известны дифторборильные комплексы тетраарилазадипиррометенов, получаемые обработкой соответствующих лигандов эфиратом трехфтористого бора в присутствии диизопропиламина в хлористом метилене при комнатной температуре (J.Killoran, L.Allen, J.F.Gallagher, D.F.O'Shea // Chem. Commun. 2002. p.1862-1863; A.Gorman, J.Killoran, CO'Shea, T.Kenna, W.M.Gallagher, F.D.O'Shea // J. Am. Chem. Soc. 2004. Vol.126. P.10619-10631). Синтезированные описанным способом соединения поглощают в спектральной области 480-580 нм и предложены для использования в качестве фотосенсибилизаторов для ФДТ. Существенным недостатком этих соединений как фотосенсибилизаторов является коротковолновая область их поглощения, что при проведении сеанса ФДТ не позволяет проникать в облучаемую опухоль достаточно глубоко и, как результат, снижает эффективность терапевтического воздействия.
В предлагаемом изобретении ставится задача синтеза эффективных фотосенсибилизаторов, поглощающих в ближней ИК-области спектра, для их использования в фотодинамической терапии.
Поставленная задача решена тем, что синтезирован ряд N,N'-дифторборильных комплексов N-(3-арил-2Н-изоиндол-1-ил)-N-(3-арил-1Н-изоиндол-1-илиден)аминов общей формулы
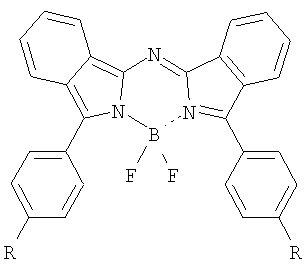
где R=H, C1-C4-алкил, OC1-C4-алкил, Ph, Br.
Указанная задача решается также тем, что предложенные соединения получают обработкой соответствующего лиганда эфиратом трехфтористого бора в присутствии вторичного или третичного амина в кипящем бензоле.
В соответствии с описанным способом получен ряд N,N'-дифторборильных комплексов, а именно N,N'-дифторборил-N-[(3-фенил-2Н-изоиндол-1-ил)-N-(3-фенил-1Н-изоиндол-1-илиден)]амин (I), N,N'-дифторборил-N-[3-(4-трет-бутилфенил)-2H-изоиндол-1-ил]-N-[3-(4-трет-бутилфенил)-1H-изоиндол-1-илиден]амин (II), N,N'-дифторборил-N-[3-(4-анизил)-2Н-изоиндол-1-ил)]-N-[3-(4-анизил)-1H-изоиндол-1-илиден]амин (III), N,N'-дифторборил-N-[3-(4-бутоксифенил)-2H-изоиндол-1-ил]-N-[3-(4-бутоксифенил)-1H-изоиндол-1-илиден]амин (IV), N,N'-дифторборил-N-[3-(4-бифенилил)-2H-изоиндол-1-ил]-N-[3-(4-бифенилил)-1Н-изоиндол-1-илиден]амин (V), N,N'-дифторборил-N-[(4-бромфенил)-2Н-изоиндол-1-ил]-N-[(4-бромфенил)-1H-изоиндол-1-илиден]амин (VI). Исходными соединениями для синтеза соединений (I-VI) служили соответствующие лиганды (VII-XII). N-(3-фенил-2H-изоиндол-1-ил)-N-(3-фенил-1H-изоиндол-1-илиден)амин (VII) и N-[3-(4-анизил)-2H-изоиндол-1-ил]-N-[3-(4-анизил)-1H-изоиндол-1-илиден]амин (IX) синтезированы по описанным в литературе методикам (H.Bredereck, H.W.Vollmann // Chem. Ber. 1972. B.105. N7. S.2271-2283). N-[3-(4-трет-Бутилфенил)-2H-изоиндол-1-ил)]-N-[3-(4-трет-бутилфенил)-1H-изоиндол-1-илиден]амин (VIII), N-[3-(4-бутоксифенил)-2H-изоиндол-1-ил]-N-[3-(4-бутоксифенил)-1H-изоиндол-1-илиден]амин (X), N-[3-(4-бифенилил)-2H-изоиндол-1-ил]-N-[3-(4-бифенилил)-1H-изоиндол-1-илиден]амин (XI) и N-[3-(4-бромфенил)-2H-изоиндол-1-ил]-N-[3-(4-бромфенил)-1H-изоиндол-1-илиден]амин (XII) синтезированы впервые.
Комплексы (I-VI) представляют собой кристаллические порошки от темно-зеленого до черного цвета с металлическим блеском, устойчивы на адсорбентах, вследствие чего протекание реакции можно анализировать методами тонкослойной хроматографии и электронной спектроскопии.
В отличие от тетраарилазадипиррометенов, сопряженная система которых содержит цепочку из двух пиррольных колец, хромофорная система молекул предлагаемых соединений характеризуется наличием сопряженной цепочки, построенной из двух остатков изоиндола, связанных друг с другом мостиком из атома азота, и двух фенильных заместителей в изоиндольных циклах. Поэтому в соответствии с длиной сопряженной цепочки диарилазадиизоиндолилметены обладают более глубоким цветом. В электронных спектрах поглощения N,N'-дифторборильных комплексов алкилдипиррометенов длинноволновая полоса находится в области 480-580 нм, а у их азааналогов - тетраарилазадипиррометенов - эта полоса смещена в область 650-690 нм. Спектры поглощения синтезированных дифторборильных комплексов (I-VI) характеризуются узкой длинноволновой полосой высокой интенсивности (lgε≈4.9) в ближней ИК-области спектра при 715-736 нм (Табл.1). На чертеже приведены электронные спектры поглощения комплексов (I-IV) в бензоле: 1 - (I), 2 - (II), 3 - (III), 4 - (IV). Параметры спектров поглощения соединений (V-VI) приведены в примерах 5 и 6 соответственно.
Настоящее изобретение иллюстрируется следующими примерами.
ПРИМЕР 1.
N-(3-Фенил-2Н-изоиндол-1-ил)-N(3-фенил-1Н-изоиндол-1-илиден)амин (VII).
К 12.8 г (0.1 моль) фталонитрила в 60 мл сухого бензола прибавляют при перемешивании раствор реактива Гриньяра - фенилмагнийбромида из 6.1 г (0.25 г-ат) магния и 26 мл бромбензола в 60 мл эфира при комнатной температуре и перемешивают смесь 1 ч. Реакционную колбу охлаждают до 0-5°С и осторожно разлагают избыток фенилмагнийбромида 20% раствором хлористого аммония, отгоняют растворители, а остаток подвергают перегонке с водяным паром. Осадок охлаждают, размельчают и кристаллизуют из смеси пиридин-MeOH. Получают 5.5 г (28%) фиолетового порошка с т.пл. 247-249°C, т.пл. лит. 247°C (H.Bredereck, H.W.Vollmann // Chem. Ber. 1972. B.105. N7. S.2271-2283). Электронный спектр поглощения (С6Н6), λмакс, нм (lgε): 656 (4.77), 429 пл. (3.12), 346 пл. (4.06), 303 (4.43).
N,N'-Дифторборил-N-(3-фенил-2H-изоиндол-1-ил)-N-(3-фенил-1H-изоиндолил-1-илиден)амин (I) получен взаимодействием 0.0001 моля лиганда (VII) с 0.0008 моля BF3·Et2O в присутствии 0.001 моля диизопропиламина в кипящем бензоле (0.41 моля) с выходом 70%, т.пл. 252-254°С. Электронный спектр поглощения (CHCl3), λмакс, нм (lgε): 715 (4.94), 657 пл. (4.33), 413 (3.73), 375 (3.97), 356 (3.98), 311 (4.32).
ПРИМЕР 2.
N-[3-(4-трет-Бутилфенил)-2H-изоиндол-1-ил]-N-[3-(4-трет-бутилфенил)-1H-изоиндол-1-илиден]амин (VIII) синтезирован из фталонитрила и трет-бутилфенилмагнийбромида с выходом 27% аналогично соединению (VII). Т.пл. 262-264°С. Электронный спектр поглощения (C6H6), λмакс, нм (lgε): 657 (4.75), 424 пл. (3.34), 343 пл. (4.15), 313 (4.53). N,N'-Дифтopбopил-N-[3-(4-тpeт-бyтилфeнил)-2H-изoиндoл-1-ил]-N-[3-(4-тpeт-бутил)-1H-изоиндол-1-илиден]амин (II) выделен из реакции лиганда (VIII) с BF3·Et2O аналогично (I) с выходом 73%, т.пл. 301-302°С. Электронный спектр поглощения (CHCl3), λмакс, нм (lgε): 724 (4.93), 662 пл. (4.34), 378 (3.96), 361 (3.95), 318 (4.34).
ПРИМЕР 3.
N-[(3-(4-Анизил-2H-изоиндол-1-ил)]-N-[3-(4-анизил)-1H-изоиндол-1-илиден]амин (IX) получен аналогично (I) из фталонитрила и 4-анизилмагнийиодида с выходом 17%. Т.пл. 198-200°С, т.пл. лит. 196°С (H.Bredereck, H.W.Vollmann // Chem. Ber. 1972. B.105. N7. S.2271-2283). Электронный спектр поглощения (C6H6), λмакс, нм (lgε): 662 (4.76), 444 пл. (3.13), 353 пл. (4.08), 319 (4.44).
N,N'-Дифторборил-N-[3-(4-анизил)-2H-изоиндол-1-ил]-N-[3-(4-анизил)-1H-изоиндол-1-илиден]амин (III) синтезирован аналогично (II) из лиганда (IX) с BF3·Et2O с выходом 62%, т.пл. 254-255°С. Электронный спектр поглощения (CHCl3), λмакс., нм (lgε): 733 (4.92), 669 пл. (4.26), 386 (4.17), 309 (4.26). Масс-спектр, m/z: 505 [М]+. Вычислено: M 505.332. Найдено, %: C 71.86; H 4.49. C30H22BF2N3O2. Вычислено, %: C 71.31; H 4.39.
ПРИМЕР 4.
N-[3-(4-Бутoкcифeнил)-2H-индоиндол-1-ил]-N-[3-(4-бутоксифенил)-1H-изoиндoл-1-илиден]амин (X) получен из фталонитрила и 4-бутоксифенилмагнийбромида с выходом 12%, т.пл. 209-211°С. Электронный спектр поглощения (C6H6), λмакс, нм (lgε): 670 (4.71), 442 пл. (3.35), 352 пл. (4.28), 319 (4.54). Масс-спектр, m/z. 542 [M]+. Вычислено: M 541.693. Найдено, %: C 79.42; H 6.45. C36H35N3O2. Вычислено, %: C 79.82; H 6.51. N,N'-Дифтopбopил-N-[3-(4-бyтoкcифeннл)-2H-изoиндoл-1-ил]-N-[3-(4-бутoкcифeнил)-1H-изоиндол-1-илиден]амин (IV) синтезирован из лиганда (X) и BF3·Et2O аналогично (I) с выходом 65%, т.пл. 182-183°С. Электронный спектр поглощения (CHCl3), λмакс, нм (lgε): 736 (4.95), 668 пл. (4.32), 389 (4.25), 310 (4.30).
ПРИМЕР 5.
N-[3-(4-Бифенилил)-2H-изоиндол-1-ил]-N-[3-(4-бифенилил)-1H-изоиндол-1-илиден]-амин (XI) синтезирован из фталонитрила и 4-бифенилилмагнийиодида с выходом 12%, т.пл. 320-322°С. Электронный спектр поглощения (C6H6), λмакс, нм (lgε): 679(4.71), 440 пл. (2.75), 347 (4.57). Масс-спектр, m/z 550 [M]+. Вычислено, М: 549.675. Найдено, %: N 6.86. C40H27N3. Вычислено, %: N 7.64.
N,N'-Дифтopбopил-N-[3-(4-бифeнилил)-2H-изoиндoл-1-ил]-N-[3-(4-бифeнилил)-1H-изоиндол-1-илиден]амин (V) синтезирован из лиганда (XI) и BF3·Et2O аналогично (I) с выходом 76%, т.пл. 318-320°С. Электронный спектр поглощения (CHCl3), λмакс нм (lgε): 735 (4.90), 668 пл. (4.15), 417 пл. (4.04), 345 (4.32). Масс-спектр, m/z 598 [M]+. Вычислено, М: 597.474.
ПРИМЕР 6.
N-[3-(4-Бромфенил)-2H-изоиндол-1-ил]-[3-(4-бромфенил)-1H-изоиндол-1-илиден]-амин (XII) выделен из реакции фталонитрила с 4-бромфенилмагнийбромидом с выходом 25%, т.пл. 280-282°С. Электронный спектр поглощения (C6H6), λмакс, нм (lgε): 656 (4.71), 435 пл. (3.56), 316 (4.50). Найдено, %: C 61.15; H 3.31; Br 29.50. C28H17B2N3. Вычислено, %: C 60.57; H 3.08; Br 28.78.
N,N'-Дифтopбopил-N-[3-[(4-бpoмфeнил)-2H-изoиндoл-1-ил]-N-[3-(4-бpoмфeнил)-1H-изоиндол-1-илиден]амин (VI) синтезирован из лиганда (XII) с выходом 86% аналогично соединению (I), т.пл. 274-276°С. Электронный спектр поглощения (CHCl3), λмакс, нм, (lgε): 725 (4.94), 660 пл. (4.29). 372 пл. (4.07), 351 (4.11), 324 (4.42). Найдено, %: N 6.97; Br 26.24. C28H16Br2F2N3. Вычислено, %: N 6.97; Br 26.50.
Предлагаемые соединения могут быть также получены с использованием в качестве аминов диэтиламина, триэтиламина, пиридина и 1,8-диазабицикло[5.4.0]-ундецен-7 (ДБУ).
ПРИМЕР 7.
Фотодинамическая активность комплексов (II) и (III) in vivo. Экспериментальные исследования проводят на мышах-самках линии BDF1 массой 20-22 г. В качестве экспериментальной опухоли используют модель перевиваемой саркомы S-37, привитой подкожно на наружную поверхность бедра нижней конечности. Сенсибилизированную опухоль облучают с помощью терапевтического аппарата для фотодинамической терапии АТО-1 с непрерывным спектром излучения (плотность мощности излучения 220 мВт/см2, плотность дозы 120 Дж/см2). Перед облучением шерсть над опухолью удаляют. Для контроля используют мышей-опухоленосителей, не подвергшихся какому-либо воздействию. Эффективность воздействия оценивают по изменению объема опухоли (Vоп) и рассчитанным исходя из него значениям торможения роста опухоли (ТРО).
Изучение in vivo биологической и фотодинамической активности комплекса (II) в водном растворе 4% Проксанола 268 проводят в дозах 1.2 и 6.2 мг/кг, комплекса (III) - в дозах 0.1, 0.5, 1.4 и 6.9 мг/кг. Растворы фотосенсибилизаторов вводят внутривенно, однократно на 6 день роста опухоли за 0.5 и 24 часа до проведения ФДТ. Количество животных в группах - от 4 до 7, продолжительность наблюдения - 20 дней.
Результаты испытаний представлены в Табл.2.
Комплекс (II) при его внутривенном введении в дозах 1.2 и 6.2 мг/кг в отсутствие облучения не подавляет рост экспериментальной опухоли. При облучении сенсибилизированных опухолей за 0.5 ч до сеанса ФДТ подавления роста опухоли также не отмечено. При проведении ФДТ через 24 ч после введения зарегистрирован биологически значимый антибластический эффект на протяжении всего периода наблюдения. Значения ТРО при дозе 6.2 мг/кг на 15-й день наблюдения составляют 98.5%, при дозе 1.2 мг/кг - 74.9%.
Значительная противоопухолевая эффективность ФДТ наблюдается и у комплекса (III), введенного за 0.5 ч до облучения опухоли. Высокие значения ТРО отмечены на протяжении 20 дней наблюдения при использовании его в дозах от 0.1 до 6.9 мг/кг (Табл.2).
Итак, предлагаемые в настоящем изобретении соединения - N,N'-дифторборильные комплексы N-(3-арил-2H-изоиндол-1-ил)-N-(3-арил-1H-изоиндол-1-илиден)аминов обладают высокой фотоиндуцированной активностью и представляют собой новый класс эффективных фотосенсибилизаторов, которые могут быть использованы для лечения опухолей методом ФДТ.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ N,N-БИС(5-АМИНО-3-АЛКИЛ-1,3,4-ТИАДИАЗОЛ-2-ИЛИДЕН)-2Н-ИЗОИНДОЛ-1,3-ДИАМИНОВ | 2015 |
|
RU2612259C1 |
| АЛКИЛТИОЗАМЕЩЕННЫЕ ФТАЛОЦИАНИНЫ, ИХ ЛЕКАРСТВЕННЫЕ ФОРМЫ И СПОСОБ ПРОВЕДЕНИЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2007 |
|
RU2340615C1 |
| N, N-БИС(5-АМИНО-3-ПЕНТИЛ-1,3,4-ТИАДИАЗОЛ-2-ИЛИДЕН)-2Н-ИЗОИНДОЛ-1,3-ДИАМИН | 2008 |
|
RU2373205C1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЗМЕТАЛЬНЫХ ТЕТРААЗАХЛОРИНОВ | 2012 |
|
RU2479586C1 |
| ФОТОСЕНСИБИЛИЗАТОР ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 1998 |
|
RU2164136C2 |
| СУЛЬФОЗАМЕЩЕННЫЕ ФТАЛОЦИАНИНЫ КАК ФОТОСЕНСИБИЛИЗАТОРЫ ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 1999 |
|
RU2183635C2 |
| ТЕТРААЗАХЛОРИНЫ КАК ФОТОСЕНСИБИЛИЗАТОРЫ ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2004 |
|
RU2278119C1 |
| ФОТОСЕНСИБИЛИЗАТОР, ЛИПОСОМАЛЬНАЯ ФОРМА ФОТОСЕНСИБИЛИЗАТОРА И СПОСОБ ПРОВЕДЕНИЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2004 |
|
RU2257898C1 |
| ПРОИЗВОДНЫЕ 13(1)-N-{2-[N-(КЛОЗО-МОНОКАРБАДОДЕКАБОРАН-1-ИЛ)-МЕТИЛ]АМИНОЭТИЛ}АМИД-15(2),17(3)-ДИМЕТИЛОВОГО ЭФИРА ХЛОРИНА e, ПРОЯВЛЯЮЩИЕ СВОЙСТВА ФОТОСЕНСИБИЛИЗАТОРА | 2009 |
|
RU2406726C1 |
| Фотосенсибилизатор для лечения рака предстательной железы и способ его получения | 2018 |
|
RU2670087C1 |
Изобретение относится к новому классу фотосенсибилизаторов для фотодинамической терапии - N,N'-дифторборильным комплексам N-(3-арил-2H-изоиндол-1-ил)-N-(3-арил-1H-изоиндол-1-илиден)аминов общей формулы
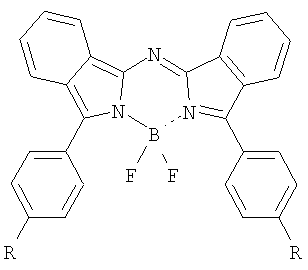
где R=H, C1-C4-алкил, OC1-C4-алкил, Ph, Br,
а также способу их получения, заключающемуся в обработке соответствующего лиганда эфиратом трехфтористого бора в присутствии вторичного или третичного амина в кипящем бензоле. Описываемые фотосенсибилизаторы обладают высокой фотоиндуцированной активностью и являются перспективными для практического применения в методе фотодинамической терапии. 2 н.п. ф-лы, 2 табл., 1 ил.
1. N,N'-Дифторборильные комплексы N-(3-арил-2H-изоиндол-1-ил)-N-(3-арил-1H-изоиндол-1-илиден)аминов общей формулы
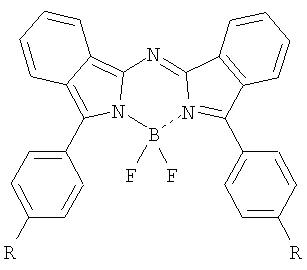
где R=H, C1-C4-алкил, OC1-C4-алкил, Ph, Br.
2. Способ получения соединений по п.1, заключающийся в обработке соответствующего лиганда эфиратом трехфтористого бора в присутствии вторичного или третичного амина в кипящем бензоле.
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСОВ НА ОСНОВЕ ТРЕХФТОРИСТОГО БОРА С АМИНАМИ | 0 |
|
SU368268A1 |
| A.GORMAN et al // J | |||
| Amer | |||
| Chem | |||
| Soc | |||
| Ударно-вращательная врубовая машина | 1922 |
|
SU126A1 |
Авторы
Даты
2009-08-20—Публикация
2008-01-14—Подача