Область техники, к которой относится настоящее изобретение.
Настоящее изобретение, в общем, относится к клеткам, полученным из жировой ткани, а более конкретно к полученным из жировой ткани стволовым и недифференцированным клеткам-предшественникам, способам использования полученных из жировой ткани стволовых и недифференцированных клеток-предшественников, композициям, содержащим полученные из жировой ткани стволовые и недифференцированные клетки-предшественники, и к системам для приготовления и использования полученных из жировой ткани стволовых и недифференцированных клеток-предшественников, которые используют для терапии сердечно-сосудистых заболеваний и расстройств.
2. Описание предшествующего уровня техники.
Сердечно-сосудистые заболевания и расстройства являются главной причиной смертности и потери трудоспособности в промышленно развитых странах. Только в одних США смертность в результате сердечно-сосудистых заболеваний составляет 40 процентов, и 58 миллионов американцев страдают от сердечно-сосудистых заболеваний (American-Heart-Association, 2002). Одним из основных факторов, делающих сердечно-сосудистые заболевания особенно распространенными, является неспособность сердца самовосстанавливаться в результате повреждения. Поскольку клетки сердечной мышцы, то есть клетки миокарда, не способны делиться вновь, заселять области повреждения, потеря сердечной клетки как результат повреждения или заболевания является почти совершенно необратимой (Аббат и др., 2002; Реме, 2000)
Из доступных видов терапии трансплантации сердца от человека человеку была самым эффективным видом в терапии тяжелых сердечно-сосудистых заболеваний и расстройств. Фактически одногодичная и пятигодичная выживаемость среднего реципиента сердечного трансплантата в настоящее время превышает 70 процентов. Однако, к сожалению, трансплантация является сильно ограниченным видом терапии по ряду причин, в частности, нехваткой соответствующих доноров, стоимостью процедуры и высокой вероятностью отторжения трансплантата и связанных проблем, например, инфекций, почечной дисфункции и раковых опухолей, связанных с иммунодепрессантом (American-Heart-Association, 2002).
Альтернативой трансплантации является использование регенеративной медицины для регенерации и восстановления поврежденных клеток сердечной мышцы. Регенеративная медицина использует в клинических целях способность стволовых клеток (то есть неспециализированных клеток тела) неограниченно самовосстанавливаться и развиваться в зрелые специализированные клетки. Стволовые клетки найдены в эмбрионах в течение ранних стадий развития, в ткани плода и некоторых зрелых органах и ткани (Пера и др., 2000). Эмбриональные стволовые клетки (называемые ниже как "ESC") не только содержат всю генетическую информацию об индивидууме, но также содержат потенциальную способность стать любой из клеток тканей тела. Таким образом, эти клетки имеют громадный потенциал для регенеративной медицины. Например, эмбриональные стволовые клетки могут быть выращены в специальных тканях, например сердце, легких или почках, которые могут быть затем использованы для регенерации поврежденных и больных органов (Ассади и др., 2004; Джекобсон и др., 2001; Одорико и др., 2001). Однако эмбриональные стволовые клетки, полученные из ткани, имеют клинические ограничения.
Поскольку эмбриональные стволовые клетки являются обязательно полученными из другого индивидуума, то есть эмбриона, имеется опасность того, что иммунная система реципиента отторгнет новый биологический материал. Хотя иммунодепрессивные лекарственные средства для предотвращения такого отторжения выпускаются на промышленной основе, также известно, что такие лекарственные средства блокируют требуемые иммунные реакции, например реакции против бактериальных инфекций и вирусов.
Кроме того, этические дебаты об источнике эмбриональных стволовых клеток, то есть эмбрионов, хорошо известны и представляют дополнительное и, возможно, непреодолимое препятствие в течение обозримого будущего.
Зрелые стволовые клетки (называемые ниже как "ASC") представляют альтернативу использованию эмбриональных стволовых клеток. Зрелые стволовые клетки в неактивном виде присутствуют во многих неэмбриональных тканях, потенциально готовые прореагировать на травму или другие деструктивные болезненные процессы восстановлением пораженной ткани (Арвидсон и др., 2002; Боннер-Вейр и Шарма, 2002; Кларк и Фризен, 2001; Кросби и Стрейн, 2001; Джанг и др., 2002а). Следует отметить, что появившееся научное доказательство показывает, что каждый индивидуум несет совокупность зрелых стволовых клеток, которые могут разделить с эмбриональными стволовыми клетками способность стать многими, если не всеми типами клеток и тканей (Янг и др., 2001; Джанг и др., 2002а; Джанг и др., 2002b; Шварц и др., 2002). Таким образом, зрелые стволовые клетки, подобно эмбриональным стволовым клеткам, имеют громадный потенциал для клинических применений регенеративной медицины.
Популяции зрелых стволовых клеток были обнаружены в костном мозге, коже, мышце, печени и головном мозге (Джанг и др., 2002b; Кросби и Стрейн, 2001). Однако концентрация зрелых стволовых клеток в этих тканях мала. Например, концентрация мезенхимальных стволовых клеток в костном мозге оценивается между 1 в 100000 и 1 в 1000000 ядерных клеток (Д′ Ипполито и др., 1999; Банфи и др., 2001; Фалла и др., 1993). Аналогичным образом, извлечение зрелых стволовых клеток из кожи включает в себя сложные серии этапов культивирования клеток в течение нескольких недель (Тома и др., 2001), а клиническое применение скелетных зрелых стволовых клеток, полученных из мышцы, требует двух-трехнедельной фазы культивирования (Хагидж и др., 2003). Таким образом, любое предложенное клиническое применение зрелых стволовых клеток из такой ткани требует увеличения числа клеток, чистоты и зрелости с помощью процессов очистки клеток и культивирования клеток.
Хотя этапы культивирования клеток могут обеспечить повышенное число, чистоту и зрелость клеток, они делают это при определенных затратах. Эти затраты могут включать в себя одну или более из следующих технических трудностей: потерю клеточной функции вследствие клеточного старения, потерю потенциально полезных нестволовых клеточных популяций, задержки в потенциальном применении клеток на пациентах, повышенные денежные затраты и повышенный риск загрязнения клеток микроорганизмами из окружающей среды в течение культивирования. В недавних исследованиях, рассматривающих терапевтический эффект зрелых стволовых клеток, полученных из костного мозга, использовали по существу весь мозг, чтобы преодолеть проблемы, связанные с культивированием клеток (Горвитц и др., 2001; Штамм и др., 2003; Штрауэр и др., 2002). Однако клинические выгоды были субоптимальными, результат практически полностью зависел от ограниченной дозы и чистоты доступных зрелых стволовых клеток.
В последнее время было показано, что жировая ткань может быть источником зрелых стволовых клеток (Зук и др., 2001; Зук и др., 2002). В отличие от костного мозга, кожи, мышцы, печени и головного мозга, жировая ткань сравнительно проста для получения в относительно больших количествах. Кроме того, было показано, что зрелые стволовые клетки, полученные из жировой ткани, обладают способностью генерировать множество тканей в искусственных условиях, включая кость, жир, хрящ и мышцу (Ашиян и др., 2003, Мицуно и др., 2002; Зук и др., 2001; Зук и др., 2002). Таким образом, жировая ткань представляет оптимальный источник для зрелых стволовых клеток для использования в регенеративной медицине. Однако на известном уровне техники отсутствуют пригодные способы получения зрелых стволовых клеток, полученных из жировой ткани. Существующие способы имеют ряд недостатков. Например, существующие способы не обладают способностью оптимальной аккомодации аспиратора для удаления жировой ткани. В существующих способах также отсутствует частичная или полная автоматизация от фазы получения жировой ткани до фаз обработки ткани (Кац и др., 2001а).
В существующих способах дополнительно отсутствует вместимость более 100 мл жировой ткани. В существующих способах еще дополнительно отсутствует частично или полностью замкнутая система от фазы получения жировой ткани до фаз обработки ткани. Наконец, в существующих способах отсутствует размещение компонентов для ослабления сопутствующих опасностей перекрестного загрязнения материалом от одной пробы к другой. Короче говоря, способы, соответствующие предшествующему уровню техники, получения зрелых стволовых клеток из жировой ткани не преодолевают технических трудностей, связанных с получением зрелых стволовых клеток из кожи, мышцы, печени и головного мозга, описанных выше.
В соответствии с этим при данном огромном терапевтическом потенциале зрелых стволовых клеток на известном уровне техники существует актуальная необходимость в устройстве, системе и способе получения зрелых стволовых клеток из жировой ткани, которая продуцирует популяцию зрелых стволовых клеток с повышенной продуктивностью, консистенцией и/или чистотой и так быстро и надежно с меньшей или несуществующей необходимостью в манипуляции после извлечения.
В идеальном случае такие устройство, система или способ будут производить зрелые стволовые клетки методом, пригодным для прямого размещения в реципиенте. Доступ к такому устройству, системе и способу в сочетании со способами и композициями, использующими зрелые стволовые клетки, полученные из жировой ткани, для терапии сердечно-сосудистых заболеваний и расстройств революционизирует терапию таких расстройств. При данной широкой распространенности сердечно-сосудистых заболеваний и недостатке возможностей современной терапии такая терапия крайне необходима.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Настоящее изобретение основано, по меньшей мере, частично на открытии того, что зрелые стволовые клетки, полученные из жировой ткани, могут быть использованы для терапии сердечно-сосудистых состояний, заболеваний или расстройств. Настоящее изобретение дополнительно основано на разработке устройств, систем и способов приготовления зрелых стволовых клеток и недифференцированных клеток-предшественников, полученных из жировой ткани. Кроме того, настоящее изобретение основано также на разработке способов и композиций зрелых стволовых клеток и недифференцированных клеток-предшественников, полученных из жировой ткани, для терапии сердечно-сосудистых состояний, заболеваний или расстройств. В соответствии с этим в одном варианте осуществления настоящее изобретение направлено на композиции, способы и системы для использования клеток, полученных из жировой ткани, которые размещают непосредственно в реципиенте вместе с добавками, необходимыми для стимулирования, возбуждения или поддержания терапевтического эффекта сердечно-сосудистой системы.
В одном варианте осуществления обработка жировой ткани имеет место в системе, которая поддержит замкнутый стерильный путь текучей среды/ткани. Этого достигают путем использования предварительно собранного соединенного агрегата из закрытых стерильных емкостей и трубопровода, обеспечивающих возможность переноса элементов ткани и текучей среды по замкнутому маршруту. Этот агрегат для обработки может быть связан с серией используемых реагентов (например, солевым раствором, ферментами и так далее), вводимых в устройство, которое может регулировать введение реагентов, температуру и синхронизацию обработки, освобождая, таким образом, операторов от необходимости вручную управлять процессом. В предпочтительном варианте осуществления вся процедура от экстракции ткани через процессинг и размещение в репициенте полностью будет выполняться в одном техническом средстве, фактически даже в одном помещении с пациентом, подвергающимся этой процедуре.
В соответствии с одним аспектом настоящего изобретения необработанную жировую ткань обрабатывают по существу до удаления зрелых адипоцитов и соединительной ткани, получая в соответствии с этим гетерогенное множество полученных из жировой ткани клеток, пригодных для размещения в теле реципиента. Клетки могут быть размещены в реципиенте в комбинации с другими клетками, тканью, фрагментами ткани или другими стимуляторами роста и/или дифференцировки клеток. В предпочтительном варианте осуществления клетки с любыми вышеупомянутыми добавками размещают в субъекте, из которого они были получены в контексте одной рабочей процедуры с намерением получения терапевтического эффекта для реципиента.
В одном варианте осуществления способ терапии пациента предусматривает: а) обеспечение устройства для удаления ткани; b) удаление жировой ткани из пациента при использовании устройства для удаления ткани, причем жировая ткань имеет концентрацию жировых клеток; е) обработку, по меньшей мере, части жировой ткани для получения концентрации стволовых клеток, которая отличается от концентрации стволовых клеток жировой ткани перед процессингом; и d) введение стволовых клеток и недифференцированных клеток-предшественников пациенту без удаления стволовых клеток и недифференцированных клеток-предшественников из устройства для извлечения клеток перед введением пациенту, используя несколько способов, известных обычным специалистам в этой области техники, включающих в себя без ограничения внутривенный, внутрикоронарный и эндомиокардиальный способы.
Устройство в соответствии с настоящим изобретением, описываемым в этой заявке, содержит а) емкость для сбора ткани, 1) принимающий ткань впускной порт, предназначенный для приема жировой ткани, удаленной из пациента, и 2) фильтр, расположенный в емкости и предназначенный для пропускания нежировой ткани, удаленной из пациента, b) смесительную емкость, соединенную с емкостью для сбора ткани для приема стволовых клеток, полученных из жировой ткани, без извлечения стволовых клеток из устройства для удаления ткани, и содержащую аддитивный порт для введения, по меньшей мере, одной добавки для смешивания со стволовыми клетками, содержащимися в ней, и с) выпускное отверстие, предназначенное для обеспечения клеткам в смесительной емкости быть извлеченными из устройства для сбора ткани с целью ведения пациенту.
Любой элемент или комбинация элементов, описываемых в этой заявке, включены в объем настоящего изобретения при условии, что эти элементы, включенные в любую такую комбинацию, не являются взаимно несовместимыми, как будет очевидно из контекста и знания одного из обычных специалистов в этой области техники. Дополнительные преимущества и аспекты настоящего изобретения становятся очевидными из следующего подробного описания.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг.1 - иллюстрация устройства для удаления ткани, предназначенной для процессинга жировой ткани.
Фиг.2 - иллюстрация емкости для сбора ткани устройства для удаления ткани, иллюстрируемого на фиг.1.
Фиг.3 - частичный разрез емкости для сбора ткани, иллюстрируемой на фиг.2.
Фиг.4 - иллюстрация процессорного устройства для автоматизации работы устройства для удаления ткани.
Фиг.5А и фиг.5В - иллюстрация экспрессии белка VEGF (5A) и PIGF (5B) посредством культивированных стволовых клеток, полученных из жира.
Фиг.6 - иллюстрация обнаружения эндотелиальных недифференцированных клеток-предшественников в популяциях стволовых клеток, полученных из жира.
Фиг.7А и фиг.7В - иллюстрация развития в искусственной среде сосудистых структур в нормальных (7А) и обработанных стрептоцотоцином (7В) мышах.
Фиг.8 - иллюстрация повышенной средней регенерации кровяного протока в мышах с ишемией задних конечностей, обработанных полученными из жира стволовыми клетками, по сравнению с негативным контролем.
Фиг.9А и фиг.9В - иллюстрация того, что увеличение дозы полученных из жира стволовых клеток улучшает приживление трансплантата и ангиогенез (9А) и показывает сохранение архитектуры жировой ткани в гистологической разновидности (9В).
Фиг.10 - иллюстрация гистологической временной последовательности приживления трансплантата полученных из жира стволовых клеток донора в области инфаркта миокарда.
Фиг.11 - иллюстрация двойного позитивного окрашивания для бетагалактозидазы и тяжелой цепи миозина. Выделенные клетки имеют голубое окрашивание бетагалактозидазы, демонстрируя их происхождение из клеток жировой ткани донора, и коричневое окрашивание, показывающее экспрессию тяжелой цепи миозина белка сердечной мышцы. Клетки, имеющие коричневое и голубое окрашивание (как показано стрелками), являются полученными из жировой ткани стволовыми клетками, которые взяты на фенотип клеток сердечной мышцы.
Фиг.12 - иллюстрация кластеров, полученных из жира стволовых клеток донора в области инфаркта миокарда после повреждения окклюзии/реперфузии в крысе.
ПОДРОБНОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Настоящее изобретение представляет, во первых, испытанные способы терапии сердечно-сосудистых состояний, заболеваний и расстройств при использовании полученных из жировой ткани стволовых клеток и недифференцированных клеток-предшественников. В частности, настоящее изобретение демонстрирует, что полученные из жировой ткани стволовые клетки и недифференцированные клетки-предшественники, соответствующие настоящему изобретению, (1) характеризуются факторами ангиогенного и артериогенного роста, включающими в себя фактор роста плаценты (PIGF) и фактор васкулярного эндотелиального роста (VEGF), (2) содержат эндотелиальные недифференцированные клетки-предшественники (ЕРС), которые имеют хорошо установленную функцию в образовании кровеносных сосудов, (3) выявляют в кровеносных сосудах az о, (4) поддерживают выживание в организме ишемической ткани, (5) возбуждают реперфузию после повреждения окклюзии/реперфузии задней конечности, (6) при инъецировании животным после травмы сердца в сердце и (7) при инъецировании животным после травмы сердца с дифференциацией кардинальных миоцитов. В соответствии с этим настоящее описание окончательно демонстрирует, что полученные из жировой ткани стволовые клетки и недифференцированные клетки-предшественники, соответствующие настоящему изобретению, пригодны для терапии сердечно-сосудистых заболеваний и расстройств.
Для того чтобы наше изобретение было легче понято, сначала будут определены некоторые термины. Дополнительные определения описаны в течение подробного описания.
Используемый в этой заявке термин «жировая ткань» относится к ткани, содержащей множество типов клеток, включая адипоциты (жировые клетки) и капиллярные клетки. Жировая ткань содержит стволовые клетки и недифференцированные эндотелиальные клетки-предшественники. В соответствии с этим жировая ткань относится к жиру, включающему в себя соединительную ткань, которая хранит жир.
Используемый в этой заявке термин «единица жировой ткани» относится к дискретному или поддающемуся измерению количества жировой ткани. Единица жировой ткани может быть измерена путем определения массы и/или объема единицы. Основываясь на данных, идентифицированных выше, единица процессированного липоаспирата, удаленного из пациента, имеет клеточный компонент, в котором, по крайней мере, 0,1% клеточного компонента составляют стволовые клетки. Со ссылкой на описание в этой заявке, единица жировой ткани может относиться ко всему количеству жировой ткани, удаленному из пациента. Таким образом, единица жировой ткани может комбинироваться с другой единицей жировой ткани для образования единицы жировой ткани, которая имеет массу и объем, то есть является суммой отдельных единиц.
Используемый в этой заявке термин «часть» относится к количеству материала, которая меньше целого. «Незначительная часть» относится к количеству, которое меньше 50%, а «основная часть» относится к количеству, которое больше 50%. Таким образом, единица жировой ткани, которая меньше всего количества жировой ткани, удаленной из пациента, является частью удаленной жировой ткани.
Используемый в этой заявке термин «стволовая клетка» относится к мультипотентным клеткам с потенциалом дифференцировки во множество других типов клеток, которые выполняют одну или более специальных функций и имеют способность самообновляться. Некоторые из стволовых клеток, описываемых в этой заявке, могут быть плюрипотентными.
Используемый в этой заявке термин «недифференцированные клетки-предшественники» относится к унипотентным, биопотентным или мультипотентным клеткам со способностью дифференцировки в одном или более типов клеток, которые выполняют одну или более специальных функций и которые имеют ограниченную способность или не обладают способностью к самообновлению. Некоторые из недифференцированных клеток-предшественников, описываемых в этой заявке, могут быть плюрипотентными.
Используемвый в этой заявке термин «число стволовых клеток» или «концентрация стволовых клеток» относится к числу колоний, наблюдаемых в клоногенном образце для анализа, в котором полученные из жировой ткани клетки (ADC) высеяны на чашки при низкой плотности клеток (<10000 клеток/колодец) и выращены в питательной среде, поддерживающей рост MSC (например, в среде DMEM/F12, дополненной 10% фетальной телячьей сыворотки, 5% лошадиной сыворотки и антибиотическими/антимикотическими агентами). Клетки выращивали в течение двух недель, после чего культуры подкрашивали гематоксилином и колонии более чем из 50 клеток считали как CFU-F. Концентрацию стволовых клеток вычисляли как число CFU-F, наблюдаемое на 100 высеянных ядерных клеток (например, 15 колоний, подсчитанных в стимулированных высеянных 1000 ядерных клеток (ADC) дает концентрацию стволовых клеток, умноженную на общее число полученных ядерных клеток (ADC). Высокий процент (~100%) CFU-F, выращенных из клеток (ADC) экспрессирует молекулу CD105 поверхности клетки, которая также экспрессируется полученными из костного мозга стволовыми клетками (Барри и др., 1999). CD105 также экспрессируется полученными из жировой ткани клетками (Зук и др., 2002).
Используемый в этой заявке термин «обработанный липоаспират» относится к жировой ткани, которая была обработана для отделения активного клеточного компонента (например, компонента, содержащего стволовые клетки и недифференцированные клетки-предшественники) от зрелых адипоцитов и соединительной ткани. На эту функцию ссылаются в этой заявке как на «полученные из жира клетки» или «ADC». Как правило, ADC относится к капле осадка, полученной благодаря промыванию и отделению клеток из жировой ткани. Каплю осадка, как правило, получают, благодаря центрифугированию суспензии из клеток, так что клетки агрегатируются на дне емкости центрифуги.
Используемая в этой заявке фраза «сердечно-сосудистое состояние, заболевание или расстройство» включает в себя все расстройства, отличающиеся недостаточной, нежелательной или ненормальной сердечной функцией, например, ишемическим сердечным заболеванием, гипертоническим сердечным заболеванием, гипертоническим сердечным заболеванием правой половины сердца, клапанным пороком, врожденным пороком сердца или любым состоянием, которое ведет к застойной сердечной недостаточности у субъекта, в частности, у человека. Недостаточная или ненормальная сердечная функция может быть результатом заболевания, травмы и/или старения. В качестве предпосылки, реакция на повреждение миокарда следует хорошо известным путем, в котором некоторые клетки умирают, тогда как другие входят в состояние гибернации, в котором они еще не мертвы, но являются дисфункциональными. За этим следует инфильтрация клеток воспаления, осаждение коллагена как части рубцевания, причем все это случается параллельно с врастанием внутрь новых кровеносных сосудов и увеличением степени продолжающегося умирания клеток. Используемый в этой заявке термин «ишемия» относится к любой локальной ишемии ткани вследствие уменьшения притока крови. Термин "ишемия миокарда" относится к нарушению кровообращения, вызванному коронарным атеросклерозом и/или неадекватной подачей кислорода к миокарду. Например, острый инфаркт миокарда представляет необратимый ишемический инсульт ткани миокарда. Этот инсульт происходит в результате окклюзивного (например, тромботического или эмболического) явления в коронарном кровообращении и создает среду, в которой метаболические требования миокарда превышают подачу кислорода к ткани миокарда.
Используемый в этой заявке термин "ангиогенез" относится к процессу, благодаря которому из существующей сосудистой сети и ткани генерируются новые кровеносные сосуды (Фолькман, 1995). Фраза "восстановление и реконструкция" относится к переформированию существующей сосудистой сети. Облегчение ишемии ткани резко зависит от ангиогенеза. Спонтанный рост новых кровеносных сосудов обеспечивает коллатеральное кровообращение в ишемической области и вокруг ишемической области, улучшает поток крови и облегчает симптомы, вызываемые ишемией. Как используется в этой заявке, термин "ангиогенный фактор" или "ангиогенный белок" относится к любому известному белку, способному содействовать росту новых кровеносных сосудов из существующей сосудистой сети ("ангиогенез"). Пригодные ангиогенные факторы для использования в настоящем изобретении включают в себя без ограничения фактор роста плаценты (Луттун и др., 2002), фактор стимулирования колонии макрофагов (Агариенейяд и др., 1995), фактор стимулирования колонии гранулоцитных макрофагов (Бушмен и др., 2003), фактор васкулярного эндотелиального роста (VEGF)-A, VEGF-A, VEGF-B, VEGF-C, VEGF-D, VEGF-E (Минтс и др., 2002), нейропилин (Ванг и др., 2003), фактор роста фибробласта (FGF)-l, FGF-2 (bFGF), FGF-3, FGF-4, FGF-5, FGF-6 (Ботта и др., 2000), Ангиопоэтин 1, Ангиопоэтин 2 (Сандберг и др., 2002), эритропоиетин (Рибатти и др., 2003), ВМР-2, ВМР-4, ВМР-7 (Карано и Филвароф, 2003), TGF-бета (Ксионг и др., 2002), IGF-1 (Шигематцу и др., 1999), Остеопонтин (Асоу и др., 2001), Плеиотропин (Бикен и др., 2000), Активин (Ламуил и др., 2002), эндотелии-1 (Багнато и Шпинелла, 2003) и их комбинации. Ангиогенные факторы могут действовать независимо или в комбинации друг с другом. Если они действуют в комбинации, то ангиогенные факторы могут также действовать синергетически, благодаря чему комбинированный эффект этих факторов больше, чем сумма эффектов отдельных факторов, взятых отдельно. Термин "ангиогенный фактор" или "ангиогенный белок" также охватывает функциональные аналоги таких факторов. Функциональные аналоги включают в себя, например, функциональные части факторов. Функциональные аналоги также включают в себя антиидиотипичные антитела, которые связываются с рецепторами факторов и, таким образом, подражают активности факторов в содействии ангиогенезу и/или реконструкции ткани. Способы генерирования таких антиидиотипических антител хорошо известны на предшествующем уровне техники и описаны, например, в документе WO 97/23510, содержание которого включено в эту заявку в качестве ссылки.
Ангиогенные факторы, используемые в настоящем изобретении, могут быть продуцированы или получены из любого соответствующего источника. Например, факторы могут быть очищены от их естественных источников или продуцированы синтетически или посредством рекомбинантной экспрессии. Эти факторы могут быть введены в форме плазмида экспрессии, кодирующего эти факторы. Структура пригодных плазмидов экспрессии хорошо известна на предшествующем уровне техники. Пригодные векторы для конструирования плазмидов экспрессии включают в себя, например, аденовирусные векторы, ретровирусные векторы, аденоассоциированные вирусные векторы, векторы RNA, липосомы, катионные липиды, лентивирусные векторы и транспозоны.
Используемый в заявке термин «артериогенез» относится к процессу увеличения роста коллатеральных артерий и/или других артерий из ранее существующих артериолярных соединений (Сармелиет, 2000; Шольц и др., 2001; Шольц и др., 2002). Более конкретно, артериогенез представляет собой включение новых и расширение имеющихся артерий благодаря пролиферации эндотелиальных и гладких миоцитов из существующих ранее артериолярных соединений, подающих кровь к ишемической ткани, новообразованию или месту воспаления.
Артериогенез является частью нормальной реакции на ишемию миокарда (Миллз и др., 2000; Монтеиро и др., 2003). Помимо всего прочего, обычная хирургическая технология шунтирования коронарной артерии (CABG) фактически является не более чем создание искусственного коллатерального сосуда (Сержант и др., 1997). Таким образом, процессы, которые увеличивают артериогенез после инфаркта улучшат поток крови к ишемической ткани, приводя в результате к уменьшению смертности клеток и уменьшению размера инфаркта. Эти улучшения приведут в результате к улучшению сердечной функции и терапевтическому эффекту.
Используемый в этой заявке термин «очистка» включает в себя уменьшение или ослабление, по меньшей мере, одного неблагоприятного эффекта или симптома сердечно-сосудистого состояния, заболевания или расстройства, то есть любого расстройства, характеризуемого недостаточной или нежелательной сердечной функцией.
Неблагоприятные эффекты или симптомы сердечных расстройств хорошо известны на предшествующем уровне техники и включают в себя без ограничения одышку, боль в груди, учащенные сердцебиения, головокружение, обморок, отек, цианоз, бледность, усталость и биологическая смерть.
Используемые попеременно в этой заявке термины "назначение", "введение" и "трансплантация" относятся к размещению ADC, соответствующего настоящему изобретению, в субъекте способом или путем, который приводит в результате, по меньшей мере, к частичной локализации ADC в требуемом месте. ADC может быть введен любым адекватным путем, который в результате приводит к подаче в требуемое местоположение в субъекте, где, по меньшей мере, часть клеток или компонентов клеток остаются жизнеспособными. Период жизнеспособности клеток после введения в субъект может быть коротким и составлять от нескольких часов, например 24 часов, до нескольких дней или нескольких лет.
Используемый в этой заявке термин "субъект" включает в себя теплокровных животных, предпочтительно млекопитающих, включая людей. В предпочтительном варианте осуществления субъектом является примат. Даже в более предпочтительном варианте осуществления субъектом является человек.
Далее ссылка будет делаться на деталь предпочтительных в настоящее время вариантов осуществления настоящего изобретения, примеры которого иллюстрируются на сопроводительных чертежах. Для ссылки на подобные или аналогичные детали на чертежах и в описании при любых обстоятельствах используют подобные или аналогичные ссылочные номера. Необходимо отметить, что чертежи приведены в упрощенном виде и в приблизительном масштабе. При ссылке на описание в этой заявке только для целей удобства и ясности относительно сопроводительных чертежей используются направляющие термины, например, верх, низ, вверх, вниз, поверх, над, под, ниже, сзади и спереди. Такие направляющие термины не должны толковаться, как каким-либо образом ограничивающие объем настоящего изобретения.
Хотя описание, приведенное в этой заявке, относится к определенным иллюстрируемым вариантам осуществления, должно быть очевидным, что эти варианты осуществления даны для примера, а не для какого-либо ограничения. Целью следующего подробного описания, хотя описываются примеры вариантов осуществления, является охват всех модификаций, альтернатив и эквивалентов вариантов осуществления, которые могут находиться в пределах сущности и объема настоящего изобретения, ограниченных формулой изобретения. Настоящее изобретение может найти практическое применение в связи с различными технологиями отделения клеток или ткани, которые обычно используются на известном уровне техники, и только так много обычно практикуемых этапов процесса включены в эту заявку, как это необходимо для обеспечения понимания настоящего изобретения.
В соответствии с этим в одном варианте осуществления настоящее изобретение направлено на клеточную популяцию в жировой ткани и системы и способы введения клеточной популяции в человека или животного для терапии сердечно-сосудистых заболеваний и расстройств. Клеточная популяция жировой ткани может быть использована как источник клеток для терапевтических применений.
Среди других вещей клетки могут быть использованы для регенеративной медицины, например, для лечения заболеваний с помощью регенерирующих клеток, включая сердечно-сосудистые заболевания и расстройства. Клетки популяции могут вводиться пациенту, страдающему сердечно-сосудистым заболеванием или расстройством, без других адипоцитов или соединительной ткани.
В частности, настоящее изобретение относится к получению клеток из жировой ткани и способам их использования, обладающих несколькими свойствами, которые могут сделать вклад в минимизацию вреда и содействовать восстановлению миокарда и регенерации в течение этого процесса. Они включают в себя среди прочего: способность синтезирования и выделения факторов роста, стимулирующих образование новых кровеносных сосудов; способность синтезирования и выделения факторов роста, стимулирующих выживание и пролиферацию клеток; способность пролиферировать и дифференцироваться в клетках, непосредственно участвующих в образовании новых кровеносных сосудов; способность прививать поврежденный миокард и подавлять образование рубцов (осаждение и перекрестное сшивание коллагена); способность пролиферировать и дифференцироваться в мышечные клетки, содействующие сократимости миокарда; и способность пролиферировать и дифференцировать клетки миокарда.
I. Способы настоящего изобретения
1. Способы получения обработанного липоаспирата (ADC)
Было обнаружено, что жировая ткань является особенно богатым источником стволовых клеток и недифференцированных клеток-предшественников. Это открытие может, по меньшей мере, частично упростить извлечение основного нестволового клеточного компонента жировой ткани, адипоцита. Таким образом, при изучении человека и животных, обработанный липоаспират (ADC) содержит стволовые клетки при концентрации, составляющей, по меньшей мере, 0,1%, а более типично - более 0,5%. В некоторых вариантах осуществления настоящего изобретения получен ADC, который содержит приблизительно 2-12% стволовых клеток. В еще одних вариантах осуществления АDС обработан для получения популяции клеток, в которой стволовые клетки составляют до 100% клеток в популяции. Чистота/концентрация стволовых клеток, получаемая в соответствии с настоящим изобретением, описываемая в этой заявке, существенно больше опубликованной концентрации 1 в 100000 (0,001%) в костном мозге (Дипполито и др., 1999; Банфи и др., 1993; Машлер и др., 2001). Кроме того, забор жировой ткани ассоциируется с меньшей травматичностью, чем забор подобного объема костного мозга (Нишимори и др., 2002). Кроме всего прочего, жировая ткань содержит эндотелиальные недифференцированные клетки-предшественники, которые способны обеспечивать терапию пациентам (смотри Асахара и др., 1999; Каузал и др., 2001; Каумото и др., 2003; Каумото и др., 2001).
В практике способов, описываемых в этой заявке, пациенту вводят клетки, которые получают из жировой ткани. Жировая ткань может быть получена любым способом, известным обычному специалисту в этой области техники. Например, жировая ткань может быть извлечена из пациента посредством липопластики, выполняемой с помощью всасывания, и эксцизионной липоэктомии. Помимо всего прочего, процедуры могут включать в себя комбинацию таких процедур, например, комбинацию эксцизионной липоэктомии и липопластики, выполняемой с помощью всасывания. Когда ткань или некоторая ее часть предназначена для реимплантации в пациента, жировая ткань должна быть собрана так, чтобы сохранить жизнеспособность клеточного компонента и чтобы минимизировать вероятность загрязнения ткани потенциально инфекционными организмами, например, бактериями и/или вирусами. Таким образом, экстракция ткани должна осуществляться стерильным или асептическим способом, чтобы минимизировать загрязнение. Для удаления жировой ткани из пациента может оказаться желательной липопластика, выполняемая с помощью всасывания, так как она обеспечивает минимально инвазивный способ коллектирования ткани с минимальной возможностью повреждения стволовых клеток, которое может быть связано с другими технологиями, например, с ультразвуковой липопластикой. Для процедур липопластики, выполняемой с помощью всасывания, жировую ткань коллектируют путем введения канюли в депо жировой ткани или вблизи депо жировой ткани, имеющегося у пациента, с последующим всасыванием жира в аспиратор. В одном варианте осуществления изобретения небольшая канюля может быть соединена со шприцем и жировая ткань может аспирироваться (отсасываться) при использовании силы руки (Аскен, 1990). Использование шприца или другого аналогичного устройства может оказаться желательным для получения относительно небольших количеств жировой ткани (например, от 0,1 мл до нескольких сот миллилитров жировой ткани). Процедуры, использующие такие относительно небольшие устройства, имеют то преимущество, что эти процедуры могут быть выполнены с использованием только местной анестезии, а не общей анестезии. Объемы жировой ткани, превышающие этот диапазон (например, более нескольких сотен миллилитров), могут потребовать общей анестезии, по решению донора и индивидуума, выполняющего процедуру коллектирования. Если требуется извлечь большие объемы жировой ткани, то в этой процедуре могут быть использованы относительно большие канюли и автоматизированные аспираторы (Коммоне и др., 2001).
Процедуры эксцизионной липоэктомии без ограничения предусматривают процедуры, в которых содержащие жировую ткань ткани (например, кожа) удаляют как несущественную часть процедуры; то есть, где основной целью хирургии является удаление ткани (например, кожи в операции при ожирении или в косметической хирургии) и в которых жировую ткань удаляют вместе с тканью, представляющей основной интерес.
Жировую ткань, которую удаляют из пациента, собирают в устройстве для дополнительной обработки. Как описано в этой заявке и в одном варианте осуществления, это устройство предназначено для обработки ткани для получения популяции клеток жировой ткани, которая содержит стволовые клетки и/или эндотелиальные недифференцированные клетки-предшественники. В других вариантах осуществления это устройство может быть стандартным устройством, которое, как правило, используют для сбора ткани врачами, выполняющими процедуру экстракции.
Количество отбираемой ткани будет зависеть от числа переменных, включающих без ограничения индексы массы тела донора, доступность мест получения жировой ткани, сопутствующие и предварительные лекарственные терапии и состояния (например, антикоагулянтную терапию) и клиническую цель, для которой коллектируют ткань.
Опыт с трансплантацией гемопоэтических стволовых клеток (полученные из костного мозга или пуповинной крови стволовые клетки, используемые для регенерации способности формирования клеток крови реципиента) показывает, что приживление трансплантата зависит от дозы клеток с пороговыми эффектами (Смит и Свитенхам, 1995; Баркер и др., 2001). Таким образом, вероятно, что общий принцип «чем больше, тем лучше» будет применим в пределах, устанавливаемых другими переменными, и что там, где это возможно, при получении будет отбираться как можно больше ткани.
Было обнаружено, что процент стволовых клеток в 100 мл жировой ткани, извлеченной из худого индивидуума, больше, чем извлеченных из донора, страдающего ожирением.
Это отражает эффект разбавления увеличенным содержанием жира у индивидуума, страдающего ожирением. Таким образом, в соответствии с одним аспектом настоящего изобретения может оказаться желательным получать большие количества ткани от доноров, имеющих избыточный вес, по сравнению с количествами, которые бы извлекались от более худых пациентов. Это наблюдение также показывает, что полезность настоящего изобретения не ограничивается индивидуумами с большими количествами жировой ткани.
Концентрированные стволовые клетки могут быть введены в композицию, содержащую полученные из жира стволовые клетки и/или эндотелиальные недифференцированные клетки-предшественники, по существу свободные от зрелых адипоцитов и соединительной ткани. В некоторых вариантах осуществления композиция имеет клеточный компонент, в котором, по меньшей мере, 0,1% клеток являются стволовыми клетками. В других вариантах осуществления композиция имеет клеточный компонент, в котором стволовые клетки содержат приблизительно 2-12% клеточного компонента. Более высокие концентрации стволовых клеток, например, до 100%, также включаются в разные композиции. Композиция может включать в себя дополнительные компоненты, например факторы клеточной дифференцировки, активаторы роста, иммунодепрессанты или медицинские устройства, как описано в этой заявке. Для получения некоторых композиций, в которых композиция главным образом содержит один тип клеток (например, полученные из жира стволовые клетки или полученные из жира эндотелиальные недифференцированные клетки-предшественники), может быть использован любой пригодный способ отделения других типов клеток, например использование специальных клеточных антител, которые распознают и связывают антитела, представленные на стволовых клетках или на эндотелиальных недифференцированных клетках-предшественниках.
Для большинства применений приготовление активной клеточной популяции потребует истощения жирного адипоцитного компонента жировой ткани. Этого, как правило, достигают посредством серии этапов промывки и дисагрегации, в которых ткань сначала промывают для уменьшения наличия свободных липидов (освобожденных разорванных адипоцитов) и элементов периферической крови (освобожденных из кровеносных сосудов, разрезанных в течение получения ткани), а затем дисагрегатируют до свободных неповрежденных адипоцитов и других клеточных популяций из матрицы соединительной ткани. В некоторых вариантах осуществления весь адипоцитный компонент или нестволовой клеточный компонент отделяют от стволового клеточного компонента жировой ткани. В других вариантах осуществления от стволовых клеток отделяют только часть или части адипоцитного компонента. Таким образом, в некоторых вариантах осуществления стволовые клетки могут быть введены с эндотелиальными недифференцированными клетками-предшественниками.
Промывка является факультативным, но предпочтительным этапом, в котором ткань смешивают с растворами для отмывки липидных и одноклеточных компонентов, например, компонентов в крови, остающихся за незатронутыми фрагментами жировой ткани. В одном варианте осуществления жировую ткань, которая удалена из пациента, смешивают с изотоническим солевым или другим физиологическим раствором (растворами) (например, Плазмалитет из компании Baxter Inc. или Нормозо (g) из Abbot Labs). Незатронутые фрагменты жировой ткани могут быть отделены от свободного липида и клеток с помощью любых средств, известных обычным специалистам в этой области техники, включающих в себя без ограничения фильтрацию, декантацию, седиментацию или центрифугирование.
В иллюстрируемом варианте осуществления настоящего изобретения жировую ткань отделяют от нежировой ткани посредством использования фильтра, расположенного в емкости для сбора ткани, как описано в этой заявке.
В других вариантах осуществления жировую ткань отделяют от нежировой ткани, используя емкость для сбора ткани. При этом используют технологии декантации, седиментации и/или центрифугирования для отделения материалов.
Целые фрагменты ткани затем дисагрегатируют при использовании любых стандартных технологий и способов, включая механическую силу (силы, возникающие при измельчении, или сдвиговые силы), ферментное расщепление одним или комбинированными протеолитическими ферментами, например коллагеназой, трипсином, липазой, либеразой H1, или элементами семейства блендзима, как описано в патенте США №5952215, и пепсином, или комбинации механических и ферментных способов. Например, клеточный компонент целых фрагментов ткани может быть дисагрегатирован с помощью способов, использующих опосредованную коллагеназой диссоциацию жировой ткани, подобных способам сбора сердечно-сосудистых эндотелиальных клеток в жировой ткани, как описано в патенте США №5372945. Другие способы, использующие коллагеназу, которые могут быть использованы при практическом использовании настоящего изобретения, описаны в патентах США №5830714 и №5952215, выданных Вильямсу и др. в 1995 году. Аналогичным образом, вместо коллагеназы может быть использована нейтральная протеаза, как описано в работе Твентимена и Юухаса, 1980. Кроме того, способы могут использовать комбинацию ферментов, например, комбинацию коллагеназы и трипсина, как описано в работе Русселла и др., 1976; или комбинацию фермента, например, трипсина, и механической диссоциации, как описано в работе Энгельхольма и др., 1985.
Активная клеточная популяция (процессированный липоаспират) может затем быть получена из дисагрегатированных фрагментов ткани путем уменьшения количества зрелых адипоцитов. Суспензия процессированного липоаспирата в жидкости, в которой дисагрегатирована жировая ткань, затем проходит в другую емкость, например, емкость для сбора клеток. Суспензия может проходить через один или более каналов к емкости для сбора клеток, благодаря использованию насоса, например перистальтического насоса, который извлекает суспензию из емкости для коллектирования ткани и побуждает ее направляться в емкость для сбора клеток. Другие варианты осуществления могут использовать гравитацию или вакуум, поддерживая в то же самое время замкнутую систему. Отделение клеток в суспензии может быть достигнуто посредством седиментации плавучей плотности, центрифугирования, отмучивания, фильтрации, дифференциального сцепления с твердофазными фракциями и вымывания из твердофазных фракций, выбора опосредованного антитела, различий в электрическом заряде, иммуномагнитных шариков, сортирования клеток активированных флуоресценцией (FACS) или другими средствами.
Примеры этих различных технологий и устройств для реализации этих технологий могут быть найдены в (Хемстрит и др., 1980; Швейцер и др., 1995; Грин и др., 2002; Принс и др., 2002; Ватт и др., 2002; Майнваринг и Роули, 1985; Гринберг и Хаммер, 2001) и в патентах США №6277060, №6221315, №6043066, №6451207, №5641622 и №6251295.
В иллюстрируемом варианте осуществления клетки в суспензии отделяют от бесклеточного компонента суспензии при использовании вращающегося мембранного фильтра. В других вариантах осуществления клетки в суспензии отделяют от бесклеточного компонента при использовании центрифуги. В одном таком примере варианта осуществления емкость для сбора клеток может быть гибким пакетом, который выполнен с возможностью размещения в центрифуге (например, вручную или посредством робота). В других вариантах осуществления гибкий пакет не используют.
После центрифугирования беслеточный компонент образует осадок, который может быть затем ресуспендирован с буферным раствором, так что клетки могут проходить через один или более каналов к смесительной емкости, как описано в этой заявке. Текучие ресуспендированные среды могут быть получены любым пригодным способом. Например, буферный раствор может быть введен в канал на емкости для сбора клеток или емкость для сбора клеток может содержать резерв буферного раствора, который может быть смешан с осадком из клеток, используя резерв. При использовании вращающегося мембранного фильтра ресуспензия является оптимальной, поскольку клетки остаются в объеме жидкости после процедуры отделения.
Хотя некоторые варианты осуществления настоящего изобретения относятся к способам полного дисагрегатирования жировой ткани для отделения активных клеток от зрелых адипоцитов и соединительной ткани, дополнительные варианты осуществления настоящего изобретения относятся к способам, в которых жировая ткань дисагрегатируется только частично. Например, частичное дисагрегатирование может быть выполнено одним или более ферментов, которые удаляют, по меньшей мере, из части жировой ткани раньше, чем это необходимо для полного дисагрегатирования тканей. Такой процесс может требовать меньшее время.
В одном особом варианте осуществления ткань промывают стерильным буферным изотоническим солевым раствором и инкубируют с коллагеназой при концентрации коллагеназы, температуре и времени, которых достаточно для обеспечения адекватного дисагрегатирования. В предпочтительном варианте осуществления используемый фермент коллагеназы будет одобрен соответствующим властным органом (например, Управлением по контролю за продуктами и лекарствами США) для употребления людьми. Пригодные препараты коллагеназы включают в себя рекомбинантную и нерекомбинантную коллагеназу. Нерекомбинантная коллагеназа может быть получена из компании F.Hoffmann-La Roche Ltd, Indianapolis, IN и/или из компании Advance Biofactures Corp., Lynbrook, NY. Рекомбинантная коллагеназа может быть также получена, как описано в патенте США №6475764.
В одном варианте осуществления растворы содержат коллагеназу в концентрациях от приблизительно 10 ед/мл до приблизительно 50 ед/мл и инкубируют при температуре, составляющей приблизительно 30-38°С, в течение от приблизительно 20 минут до примерно 60 минут. Эти параметры будут изменяться в соответствии с источником фермента коллагеназы и оптимизироваться эмпирически для того, чтобы обосновать то, что система эффективна при экстракции требуемой клеточной популяции в адекватном формате времени. Особенно предпочтительной концентрацией, временем и температурой является концентрация 20 ед/мл коллагеназы (смешанной с протеазе диспазе; Блендзиме 1, Роше), инкубированной в течение 45 минут при температуре, составляющей приблизительно 37°С. В альтернативном предпочтительном варианте осуществления используют 0:5 ед/мл коллагеназы (смешанной с протеазе диспазе; Блендзиме 3). В особенно предпочтительном варианте осуществления используемым ферментом коллагеназы является вещество, одобренное соответствующим властным органом для употребления людьми (например, Управлением по контролю за продуктами и лекарствами США). Используемая коллагеназа не должна содержать микроорганизмов и загрязнений, например, эндотоксина.
После дисагрегатирования активная клеточная популяция может быть промыта для удаления добавок и/или побочных продуктов процесса дисагрегатирования (например, коллагеназы и вновь выделенного свободного липида). После этого может быть увеличена концентрация активной клеточной популяции путем центрифугирования или другими способами, известными обычным специалистам в этой области техники, как описано выше. Эти этапы промывки/увеличения концентрации, проводимые после процессинга, могут быть проведены отдельно или одновременно.
В одном варианте осуществления увеличивают концентрацию клеток и удаляют коллагеназу путем пропускания клеточной популяции непрерывным потоком через вращающуюся мембранную систему или подобное устройство, например систему, описанную в патентах США №5034135 и №5234608.
Помимо сказанного выше, имеется множество способов промывки, которые могут быть использованы для дополнительной очистки активной клеточной популяции. Они включают в себя позитивную селекцию (выбор целевых клеток), негативную селекцию (избирательное удаление нежелательных клеток) или их комбинацию.
В одном варианте осуществления твердофазный материал с адгезивными свойствами, выбранный для обеспечения возможности для разного сцепления и/или элюирования субпопуляции клеток в обработанном липоаспирате, вводят в систему после этапа промывки клеток. Этот общий способ реализуют при клиническом переливании крови, в котором используют фильтры, дифференциально захватывающие лейкоциты, для уменьшения перелитых эритроцитов, содержащих лейкоциты (Соли и др., 2001).
Фильтры этого типа распространяются Полом Бедикалом (Leukogard RS and Purecell RCQ) и Асахи (RS2000). Дифференциальная адгезия также использовалась для позитивной селекции моноцитов (Бердель и др., 1982) и эпидермальных стволовых клеток (Бисенбах и Даннвальд, 2000). В этом варианте осуществления процессированный липоаспират будет пропущен через фильтрующий материал в состояниях течения и буфера, предварительно определенных для активации дифференциальной адгезии целевых клеток и нежелательных клеточных популяций. Для позитивной селекции фильтрующий материал и состояния обеспечат возможность предпочтительной адгезии целевых клеток, тогда как нежелательный материал будет свободно проходить через фильтр и вымываться избытком буфера. Целевые клетки будут элюированы из фильтра путем изменения условий, например, расхода, рН, ионной силы и/или наличия катионов, необходимых для адгезии. Фильтрующий материал может быть в виде трехмерной сетки, уплотненной кассеты мелких частиц, полых волокон или других элементов с большой площадью поверхности. В предпочтительном варианте осуществления такой фильтр будет интегральной частью агрегата одноразового использования, показанного на фиг.1, который будет вставлен в устройство, иллюстрируемое на фиг.4. Агрегат и устройство будут немного отличаться от примеров, иллюстрируемых на характерных чертежах; причем фиг.1 - для включения фильтра и корпуса, а фиг.4 - для обеспечения возможности вставки корпуса фильтра и трубопровода (включая клапаны), необходимые для сохранения замкнутого стерильного пути текучей среды.
В альтернативном варианте смесительная камера (компонент 108 фиг.4; компонент 30 фиг.1) может быть заменена фитингами и фильтром/корпусом соответственно.
Альтернативный вариант осуществления этого способа дифференциальной адгезии будет включать в себя использование антител и/или комбинаций антител, распознающих поверхностные молекулы дифференциально экспрессированы на целевых и нежелательных клетках. Селекция на основе экспрессии специфических маркеров поверхности клеток (или их комбинаций) является другой обычно используемой технологией, в которой антитела соединены (непосредственно или косвенно) с твердофазной опорной структурой (Гейзельгарт и др., 1996; Форманек и др., 1998; Граеплер и др., 1998; Кобари и др., 2001; Мор и др. Этот способ имеет очевидные применения при позитивной и негативной селекции, в которых, например, остаточные лейкоциты могут быть удалены, благодаря использованию антитела CD45).
Аналогичным образом, Рейес и др. использовали комплексную смесь антител в селекции мультипотентных зрелых недифференцированных клеток-предшественников из человеческого костного мозга (Рейес и др., 2001). Например, антитело, например, АР2 (Джойнер и др., 1999), которое характерно связано адипоцитами, может быть использовано для предпочтительного уменьшения остаточных адипоцитов (включающих в себя незрелые адипоциты и адипобласты). Позитивная селекция может быть реализована путем использования антител, характерных для целевой клеточной популяции (популяций). Например, Куирси и др. использовали антитела для рецептора фактора роста нерва для обогащения полученных из костного мозга мезенхимальных стволовых клеток (Куинси и др., 2002).
В одном варианте осуществления способа, основанного на применении антител, антитело (например, АР2) или комбинация антител (например, АР2, CD3, CD19, CD11b) будут введены в полученный липоаспират. Множество других антител и комбинаций антител станет очевидным для квалифицированного специалиста в этой области техники и эти примеры предусмотрены только для иллюстрации характерных вариантов осуществления. После инкубации в условиях, предварительно определенных для обеспечения возможность оптимальной связи этих антител с их родственными антигенами, клетки будут промыты посредством пропускания через вращающийся мембранный фильтр или другой вариант осуществления камеры для промывки клеток для удаления несвязанных избыточных антител. После этого клетки будут пропущены поверх твердофазной структуры, подобной той, которая была описана в вышеприведенном варианте осуществления, но в котором твердофазная структура соединена с вторичным антителом, способным надежно сцепляться с первичными антителами, в настоящее время связанными с поверхностью клеток. Целевые клетки, например, полученные из жировой ткани стволовые клетки, будут свободно проходить через фильтр вследствие отсутствия экспрессии антигенов поверхности клеток, распознаваемой выбранным антителом (смесью антител), создавая в соответствии с этим систему негативной селекции. В этом варианте осуществления агрегат одноразового использования (фиг.3) и устройство (фиг.4) будут предметами второстепенных модификаций, очень похожих на модификации, описанные в ссылке на вариант осуществления, описанный выше.
Вариант осуществления селекции, опосредованной антителом, может быть реализован очень похожим способом, предусматривающим введение третьей добавки, которая облегчает отделение клеток от твердофазной опоры. В этом варианте осуществления фермент-папаин или химопапаин может быть введен для расщепления молекул антитела и освобождения клеток из твердофазной опоры (Цивин и др., 1990). Другой альтернативой будет использование специальных пептидов, которые будут конкурировать с антигеном поверхности клеток для связи с антителами, как описано в патенте США №6017719, выданном Тсе-Лао и др.
В другом варианте осуществления осадок клеток может быть ресуспендирован, нанесен поверх (или под) материал текучей среды, образованный в непрерывном или прерывистом градиенте плотности, и размещен в центрифуге для отделения клеточной популяции на основе плотности клеток. Примеры сред, пригодных для образования таких градиентов, включают в себя вещество Percoll and Ficoll-Paque (Квиан и др., 1998; Смит и др., 2000) или Ficoll-Paque (Ленер и Холтер, 2002; Ван В и др., 2001). Этот вариант осуществления будет способным выделять некоторые остаточные популяции клеток крови и незрелые адипоциты (предадипоциты) из клеточной популяции.
В подобном варианте осуществления могут быть также использованы методы непрерывного потока, например, афереза (Смит, 1997) и очистки (с противотоком или без противотока) (Лаш и др., 2000; Ито и Шиномура, 2001). Такие механизмы использовали для фракционирования клеток крови, включая отделение эритроцитов на основе возраста (Лаш и др., 2000), а применение этого общего метода для дополнительной очистки клеток, представляющих интерес, от процессированного липоаспирата будет вполне очевидно для квалифицированных специалистов в этой области техники. Этот вариант осуществления может потребовать модификации устройства, иллюстрируемого на фиг.4, и агрегата одноразового использования, иллюстрируемого на фиг.3, так, чтобы устройство было выполнено интегрально с другим устройством, обеспечивающим способность афереза или отмучивания.
Адгезию к полимерному материалу после короткого периода расширения клеток также применяли в полученных из костного мозга зрелых стволовых клеточных популяциях (Джайзвел и др., 2000). В этом способе используют условия культивирования для предпочтительного расширения одной популяции, тогда как другие популяции сохраняются (и в соответствии с этим уменьшаются благодаря растущим селектированным клеткам) или теряются вследствие отсутствия требуемых условий роста. Секийя и др. описал условия, которые могут быть использованы в этом отношении для полученных из костного мозга стволовых клеток (Секийя и др., 2002). Этот метод (с дифференциальной адгезией и без дифференциальной адгезии к культуральному полимерному материалу ткани) может быть использован для дополнительного варианта осуществления настоящего изобретения. В этом варианте осуществления клетки удаляют из устройства, иллюстрируемого на фиг.4, и размещают в другом устройстве, обеспечивающем культуральный компонент клеток.
Оно может быть в виде стандартного лабораторного культурального инкубатора для ткани или устройством типа биореактора, например, описанного Цао и др. в патенте США №6001642 или Армстронгом и др. в патенте США №6238908. В альтернативном варианте осуществления смесительный компонент (компонент 108 устройства, иллюстрируемого на фиг.4; компонент 30 устройства, иллюстрируемого на фиг.3) может быть заменен биореактором, обеспечивающим возможность кратковременной адгезии и/или культивирования клеток процессированного липоаспирата. Этот альтернативный вариант осуществления обеспечит возможность интеграции биореактора в устройство и устранения необходимости удаления клеток из этого устройства и размещения в другом.
Иллюстрируемый способ получения обработанного липоаспирата.
На фиг.1 иллюстрируется пример устройства для удаления ткани, предназначенного для удаления жировой ткани у пациента. В широком варианте осуществления устройство 10 для удаления ткани содержит емкость 12 для коллектирования ткани и смесительную емкость 30, соединенную с емкостью 12 для коллектирования ткани.
Соединение между смесительной емкостью 30 и емкостью 12 для коллектирования ткани предпочтительно ограничивает замкнутую систему, в которой ткань, которая направляется из емкости 12 для сбора ткани к смесительной емкости 30, не подвергается воздействию внешней окружающей среды. Устройство 10 также содержит выпускное отверстие 32, которое предназначено для обеспечения возможности удаления концентрированных стволовых клеток из устройства 10 для коллектирования ткани для введения пациенту. Емкость 12 для сбора ткани содержит впускное отверстие 14 для коллектирования ткани и фильтр 16. Фильтр 16 расположен в емкости и предназначен для удерживания жировой ткани и для пропускания нежировой ткани, когда, например, ткани удаляют из пациента. Более конкретно, фильтр 16 обеспечивает возможность прохождения свободного жира крови и солевого раствора, тогда как удерживает фрагменты жировой ткани в процессе или в другом варианте осуществления после первоначального получения жировой ткани. В этом отношении фильтр 16 имеет множество пор одного размера или разных размеров, но в диапазоне размеров от приблизительно 20 нм до 5 мм. В предпочтительном варианте осуществления фильтр представляет собой полиэфирную сетку, разрешенную для применения в медицинских целях, толщиной, составляющей приблизительно 200 нм, с размером пор приблизительно 265 ед и приблизительно 47% открытой площади. Этот материал удерживает ткань в течение промывки, но позволяет клеткам выходить через сетку после дисагрегатирования ткани. Таким образом, когда ткань аспирируется из пациента, нежировая ткань может быть отделена от жировой ткани. Смесительная емкость 30 содержит аддитивный порт 31, который предназначен для обеспечения возможности пользователю управлять дополнительно к смесительной емкости 30 смешиванием со стволовыми клетками, содержащимися в смесительной емкости 30. В предпочтительном варианте осуществления размеры емкости 12 для коллектирования ткани должны быть такими, чтобы обеспечить возможность удерживания приблизительно одного литра фрагментов ткани в фильтре. В других вариантах осуществления емкость 12 для сбора ткани может иметь размеры для удержания большего или меньшего объема фрагментов ткани; например, емкость для коллектирования ткани может иметь размеры для хранения, по меньшей мере, 100 мл фрагментов жировой ткани и приблизительно до 2 л фрагментов жировой ткани.
Что касается дополнительных элементов, имеющихся в устройстве 10, иллюстрируемом на фиг.1, то впускное отверстие 14 для ткани соединено с канюлей 24 посредством трубопровода 22 для ограничения линии удаления ткани. В иллюстрируемом варианте осуществления канюля 24 является интегральной канюлей однократного использования для липосакции, а трубопровод является гибким трубопроводом. Канюля имеет такие размеры, чтобы вводиться в пациента для удаления из пациента жировой ткани. Трубопровод, используемый в устройстве, должен быть способным выдерживать отрицательное давление, связанное с липопластикой, выполняемой с помощью всасывания, для уменьшения вероятности схлопывания. Емкость 12 для сбора ткани также содержит порт 18 всасывания, расположенный на противоположной стороне фильтра 16 из впускного отверстия 14 для ткани. Порт 18 всасывания выполнен с возможностью соединения с аспиратором 20, который может работать вручную или автоматически. Аспиратор 20 может быть шприцом или может быть среди прочего электровакуумным устройством. Аспиратор 20 должен быть способным обеспечивать достаточное отрицательное давление в емкости 12 и канюли 24 для аспирирования ткани из пациента. Как иллюстрируется, аспиратор 20 соединен с портом 18 всасывания посредством трубопровода 22.
Иллюстрируется также устройство 10 для удаления ткани, содержащее емкость 26 для сбора клеток, позиционируемую между емкостью 12 для коллектирования ткани и смесительной емкостью 30. Емкость 26 для сбора клеток позиционирована в устройстве 10 так, чтобы клетки, например, стволовые клетки, проходили из емкости 12 для сбора ткани в емкость 12 для сбора клеток прежде, чем проходить в смесительную емкость 30. В иллюстрируемом варианте осуществления емкость 26 для сбора клеток соединена с емкостью 12 для сбора ткани посредством порта 48 сбора клеток. В одном варианте осуществления устройства 10 емкость 26 для сбора клеток содержит концентратор клеток (не показан), который облегчает отделение клеток в суспензии. Примером концентратора клеток является центрифуга, которая может отделять клетки от другого материала на основе, например, размера или плотности клеток.
Другим примером является вращающийся мембранный фильтр, как указано выше. Устройство 10 также иллюстрируется как содержащее фильтр 28, выполненный с возможностью пропускания клеток из емкости 26 для сбора клеток в смесительную емкость 30 и для предотвращения прохождения материала, который, например, крупнее клеток. Емкость 26 для сбора клеток также содержит выпускной патрубок к емкости 36 для отходов. Направление потока материала, содержащегося в емкости 26 для сбора клеток, определяется позиционированием одного или более клапанов, которые могут управлять движением потока материала к емкости 36 для отходов или смесительной емкости 30.
В иллюстрируемом варианте осуществления клеточный фильтр 28 содержит множество пор, имеющих диаметр или длину менее 200 нм. В некоторых вариантах осуществления поры могут иметь диаметры, которые меньше 200 нм. В других вариантах осуществления поры имеют диаметры между 20 и 200 нм. Клеточный фильтр 28 может отстоять от емкости 26 для сбора клеток или может быть размещен в емкости 26 для коллектирования клеток. Клеточный фильтр 28 может быть также интегрально образован в емкости 26 для сбора клеток. Дополнительные варианты осуществления устройства 10 не содержат фильтра 28.
Емкость для сбора клеток может быть получена из любого соответствующего материала. Например, емкость 26 для сбора клеток может быть пластиковым пакетом, например, таким как пакеты, обычно используемые при обработке крови в банках крови; или в других вариантах осуществления она может быть конструктивно жесткой. В некоторых вариантах осуществления емкость 26 для сбора клеток может содержать подготовительную камеру компонентов и камеру для промывки/отделения клеток.
В некоторых вариантах осуществления подготовительная камера компонентов включает в себя один или более портов для введения агентов, которые могут активизировать процесс отделения стволовых клеток для введения пациенту, например, факторов роста или буферных растворов для ресуспендирования клеток, как описано выше. В этих вариантах осуществления подготовительная камера компонентов включает в себя смеситель, предназначенный для смешивания или перемешивания в емкости клеток и добавок. Подготовительная камера компонентов также содержит один или более портов для удаления клеток, коллектированных в ней. Один порт может быть предусмотрен для пропускания клеток к смесительной емкости 30. Другие порты могут быть предусмотрены для направления клеток или части клеток к другим целям, например, имплантируемым материалам, включая костные фрагменты, или к устройствам для культивирования или очистки клеток. В одном варианте осуществления камера для промывки/отделения клеток содержит вращающийся мембранный фильтрующий компонент в качестве альтернативы центрифуге.
Устройство 10 также иллюстрируется как содержащее линию 34 возврата ткани, которая позиционирована для обеспечения канала из емкости 12 для коллектирования ткани в смесительную емкость 30. Таким образом, линия 34 возврата ткани пропускает или направляет ткань, содержащуюся в емкости 12, для сбора ткани в смесительной емкости 30, где ткань может быть смешена с клетками, полученными из емкости 26 для сбора клеток. В иллюстрируемом варианте осуществления линия 34 возврата ткани связана с емкостью 12 для сбора ткани для удаления жировой ткани, которая содержится в фильтре 16. Ткань пропускают или направляют через линию 34 возврата ткани при использовании одного или более насосов или аспираторов для перемешивания жировой ткани, которая была промыта, но не обязательно разделена на составляющие части.
В одном из вариантов осуществления устройство 10 содержит терморегулятор, который позиционирован относительно устройства 10 для регулирования температуры материала, содержащегося в емкости 12 для сбора ткани. В некоторых вариантах осуществления терморегулятор является нагревателем, а в других вариантах осуществления терморегулятор является охладителем. В дополнительных вариантах осуществления терморегулятор может быть способным переключаться между нагревателем и охладителем. Терморегулятор в устройстве может регулировать температуру жировой ткани, содержащейся в емкости 12 для сбора ткани, или может быть позиционирован для изменения температуры текучей среды, подаваемой к емкости 12 для сбора ткани. Было установлено, что нагрев жировой ткани облегчает ее разделение для увеличения отделения активного клеточного компонента. Помимо всего прочего, в некоторых вариантах осуществления требуется охлаждение части ткани, предпочтительно активного клеточного компонента, для обеспечения защиты клеткам. Даже небольшое охлаждение клеток может обеспечить пригодную защиту для увеличения выживания клеток в течение их обработки.
Выпускное отверстие 32 устройства 10 для удаления ткани иллюстрируется как являющееся компонентом смесительной емкости 30. В дополнительных вариантах осуществления выпускное отверстие 32 отстоит от смесительной емкости 30.
Выпускное отверстие 32 предпочтительно содержит укупорочное средство, которое сохраняет герметичность устройства 10 для удаления ткани, а в некоторых вариантах осуществления выпускное отверстие 32 содержит непроницаемую для текучей среды мембрану (например, мембрану, которая непроницаема для жидкости и воздуха). Выпускное отверстие 32 должно быть выполнено с возможностью пропускания композиции в смесительной камере 30 к пациенту при соответствующих условиях. Например, если для извлечения композиции используется шприц, то выпускное отверстие 32 должно быть способным принимать иглу шприца без ущерба для стерильности системы или композиции. В дополнительных вариантах осуществления, если выпускное отверстие соединено с устройством, которое предназначено для введения композиции, но не для извлечения композиции, например с канюлей, которая вводит композицию путем приложения положительного давления для смещения композиции через канюлю, выпускное отверстие 32 должно быть выполнено с возможностью разрешения композиции, содержащейся в смесительной емкости 30, проходить в канюлю. В других вариантах осуществления выпускное отверстие 32 может содержать устройство для введения композиции, или герметично соединено с устройством для введения композиции, например, иглу шприца или канюлю для введения композиции путем приложения положительного давления.
Устройство 10 для удаления ткани также иллюстрируется как содержащее емкость 36 для отходов, установленную для приема отходов из емкости 12 для сбора ткани. В иллюстрируемом варианте осуществления емкость 36 для отходов также соединена и установлена для приема отходов из емкости 26 для сбора клеток. Промывочная емкость 38 предусмотрена в гидродинамической связи с промывочной линией 39 для подачи промывочной жидкости, например, солевого раствора или любого другого пригодного буферного раствора, через промывочный порт 46 к емкости 12 для сбора ткани. Емкость 12 для сбора ткани также содержит входной воздушный патрубок 40 для регулирования величины давления в емкости 12 для сбора ткани. Аддитивная линия 42 предусмотрена на емкости 12 для обеспечения возможности введения добавки в емкость 12. В ссылке на способы, описываемые в этой заявке, аддитивная линия 42 предусмотрена для подачи одного или более ферментов к емкости 12 для облегчения отделения активного клеточного компонента от остатка жировой ткани, содержащегося в фильтре 16. Как иллюстрируется, аддитивная линия 42 содержит иглу 44, которая может быть использована для приема фермента из соответствующей емкости.
Конкретный вариант конструктивных элементов устройства 10 для удаления ткани иллюстрируется на фиг.2 и фиг.3, где аналогичными ссылочными номерами указаны аналогичные части. В конкретном варианте осуществления, иллюстрируемом на фиг.2 и фиг.3, емкость 12 для сбора ткани содержит корпус, изготовленный из поликарбоната, разрешенного для применения в медицине, содержащий конический фильтрующий пакет из полиэфира, разрешенного для применения в медицине, с размером сетки 275 мкм. Жесткая емкость для сбора ткани может иметь размер, составляющий приблизительно 0,125 дюйма. К внутренней области цилиндра имеется доступ через два порта для трубопровода всасывания, два порта с трубопроводом для соединения посредством технологии стерильной стыковки и два порта для доступа прокалывания иглой через резиновую мембрану. Подобная функциональность может быть достигнута с разными материалами, размерами сетки и числом и типами портов. Например, размеры отверстий сетки, составляющие менее 100 микрон или несколько тысяч микрон, будут решать одну задачу разрешения прохождения солевого раствора и клеток крови при удерживании агрегатов и фрагментов жировой ткани. Аналогичным образом, цель устройства может быть достигнута путем использования альтернативного жесткого полимерного материала, путем замены канюли одноразового использования канюлей многоразового использования или посредством многих других модификаций, которые будут известны квалифицированным специалистам в этой области техники. Однако в других вариантах осуществления устройства 10 для удаления ткани емкость 12 может содержать складной корпус, например, пакет для сбора ткани. В таких устройствах пакет предпочтительно предусмотрен с опорой, например, внутренней или внешней рамой, которая помогает уменьшить вероятность того, что пакет будет схлопываться при отсасывании из пакета.
Для уменьшения загрязнения в устройстве 10 для удаления ткани на различных линиях или трубопроводах для управления потоком материала через линии различных компонентов устройства может быть предусмотрен один или более зажимов 23. Зажимы 23 позволяют пользователю эффективно герметизировать различные области устройства 10 для удаления ткани. В предпочтительном варианте осуществления один или более компонентов устройства 10 являются элементами одноразового использования. Избежание повторного использования компонентов в этом варианте осуществления помогает уменьшить загрязнение, которое может быть связано с повторным использованием различных компонентов.
Помимо всего прочего, обеспечение компонентов в виде агрегата одноразового использования обеспечивает преимущество быть способным стерилизовать все компоненты одновременно, что может существенно уменьшить время, требуемое для практического использования способов, описываемых в этой заявке. В полностью или частично автоматизированных вариантах осуществления в дополнении к зажимам 23 или в качестве альтернативы зажимам 23 могут быть использованы клапаны с компьютерным управлением.
Помимо всего прочего, устройство 10 для удаления ткани может содержать дополнительные устройства или компоненты, которые среди прочего позволяют определять объем материала, удерживаемого в фильтре 16, для обеспечения возможности регистрации письменной информации, относящейся к процедуре экстракции или процессинга, или выполнения других дополнительных функций, например, присоединение устройства к стойке или размещение в течение работы.
Компоненты устройства 10 для удаления ткани должны быть сделаны из материалов, которые являются химически неактивными с биологическими текучими средами или тканями и химически неактивными с агентами, используемые при процессинге биологических текучих сред и тканей. Помимо всего прочего, материалы, из которых сделаны различные компоненты, должны быть способными выдерживать стерилизацию, например, посредством автоклавной обработки и облучением, включая без ограничения использование бета- или гамма-излучения. Трубопровод и рукоятка канюли могут быть выполнены из любого соответствующего материала, например, полиэтилена. Канюля может быть сделана из любого пригодного материала, включая нержавеющую сталь.
В соответствии с изобретением, описываемым в этой заявке, устройство 10 для удаления ткани обеспечивает получение замкнутой системы, которая удобна для удаления, процессинга и манипулирования зрелыми стволовыми клетками, обнаруженными в жировой ткани. Эта система может быть размещена вблизи пациента для удаления жировой ткани, а ткань может быть подвергнута процессингу, не требуя удаления ткани из системы. Таким образом, обеспечивается система, которая может обеспечивать получение свежих стволовых клеточных улучшенных композиций для пациента и уменьшать потенциальные опасности, связанные с культивированием и/или предохранением стволовых клеток.
В соответствии с этим описанием настоящее изобретение обеспечивает способ экстрагирования ткани из пациента при использовании следующих этапов: (1) подготовка пациента, как для традиционной липопластики, (2) перемещение канюли и устройства для удаления ткани из упаковочных материалов к стерильной области, (3) соединение насоса липоксации (со стандартной ловушкой и поточными микробными фильтрами) с адаптером шланга, ведущим из емкости для коллектирования ткани, (4) гарантирование, что винтовые зажимы трубопровода не сцепляются на портах всасывания емкости для сбора ткани, (5) использование канюли в качестве канюли нормальной липоксации для удаления нежелательной жировой ткани, (6) применение в ручном рабочем варианте осуществления винтовых зажимов двух трубопроводов для герметизации емкости для сбора ткани после того, как требуемое количество жировой ткани было собрано в соответствующей емкости, (7) гарантирование, что емкость для сбора ткани правильно помечена опознавательной биркой пациента, и регистрирование другой информации на бирке (дата и время процедуры и так далее) в соответствии с установленной практикой и (8) извлечение жировой ткани из пациента.
В соответствии с иллюстрируемым устройством 10 для удаления ткани ткань собирают непосредственно на этапах обработки путем присоединения трубопровода 22 к источнику 20 всасывания с расположенной линейно ловушкой для текучей среды и введения канюли 24 в место отсасывания жировой ткани. Жировую ткань затем аспирируют в емкость 12 для сбора ткани, где ее удерживают посредством фильтра 16, которым оборудована емкость 12. После сбора жировая ткань может быть промыта промывочной жидкостью, например стерильным изотоническим солевым раствором, содержащимся в промывочной емкости 38, вводимым в емкость 12 по промывочной линии 39. Если в иллюстрируемом варианте осуществления емкость 12 сделана из жесткого материала для поддержания сбора при всасывании, то воздух, подаваемый из корпуса в течение введения солевого раствора, может вентилироваться через входной воздушный патрубок 40.
В альтернативном варианте воздух может подаваться в емкость 36 для отходов или аналогичное место.
Как только ткань промыта, материалу отходов может быть разрешено поступить в емкость 36 для отходов.
После того, как ткань была собрана, игла 44 может быть введена в стерильную пробирку коллагенсодержащего раствора фермента, который затем проходит в емкость 12 для сбора ткани, где его смешивают с жировой тканью при температуре, составляющей приблизительно 37°С в течение 15-60 минут. При необходимости этап промывки может быть повторен и разделенная ткань может быть промыта с последующим выведением активной клеточной популяции для максимизации эффективности. В конце разделения ткани емкость 12 размещают вертикально для обеспечения возможности флотации адипоцитов. Затем потоку активной клеточной популяции дают возможность пройти в емкость 26 для сбора клеток, где клетки отделяют от коллагеназы и остаточного свободного липида. Клетки могут быть промыты и/или концентрированы любым способом, известным обычным специалистам в этой области техники, включая без ограничения последовательные центрифугирование/промывки, ресуспензии или механизмы непрерывного потока. После этого потоку концентрированных промытых клеток обеспечивают поступление в смесительную емкость 30, где они могут быть смешаны с целой тканью из линии 34 возврата ткани и/или другими предполагаемыми добавками перед удалением через выпускное отверстие 32 для введения пациенту. Материал, содержащийся в емкости 26 для сбора клеток, может быть отфильтрован при использовании клеточного фильтра 28 с последующей промывкой для увеличения удаления нежелательных остаточных клеток и агрегатов ткани, которые при применении могут провести к эмболии.
При необходимости для улучшения результатов в течение процессинга в различные емкости может быть введена одна или более добавок. Некоторые примеры добавок включают в себя агенты, которые оптимизируют промывку и разделение добавки, которые увеличивают жизнеспособность активной клеточной популяции в течение процесссинга, антимикробные агенты (например, антибиотики), добавки, которые разрушают адипоциты и/или эритроциты, или добавки, которые обогащают клеточные популяции, представляющие интерес (посредством дифференциальной адгезии к твердотельным фракциям или иначе активируют существенное уменьшение или обогащение клеточных популяций).
В вышеописанном варианте осуществления емкость 12 для сбора ткани является существенной для компонентов процессинга устройства 10 для удаления ткани. В альтернативном варианте отдельная емкость для коллектирования ткани, например, емкость, описанная в заявке на изобретение №10/242094, названной Сохранение неэмбриональных клеток из негемопоэтических тканей, поданной 12 сентября 2002 года, которая притязает на преимущество предварительной заявки США на изобретение №60/322070, поданной 14 сентября 2001 года, содержание которой включено в эту заявку в качестве ссылки, может быть целиком или частично использована с последующей передачей дисагрегатированного материала к компонентам процессинга. Дополнительные потенциальные емкости для коллектирования ткани описаны в патентах США №6316247 и №5372945.
Как показано выше, в некоторых вариантах осуществления настоящего изобретения способы могут быть автоматизированы путем обеспечения одного или более дополнительных устройств, которые могут автоматически реализовывать этапы способов. В таких вариантах осуществления устройство для обработки данных (например, микропроцессор или персональный компьютер) является устройством для частичной или полной автоматизации этапов, описанных выше. Примеры этапов, поддающихся такой автоматизации, включают в себя без ограничения управление входом и выходом текучих сред и тканей по конкретным маршрутам трубопроводов посредством управляющих насосов и клапанов системы или устройства для процессинга; детектирование блокировок с помощью датчиков давления; механизмы смешивания, измерение количества ткани и/или текучей среды для движения по конкретному маршруту при использовании объемных механизмов; поддержание температур различных компонентов при использовании терморегуляторов; промывку и концентрирование клеток и интеграцию процесса путем синхронизации и программных средств. В одном варианте осуществления программные средства могут регулировать параметры процесса для обеспечения возможности продуцирования клеточной популяции, получаемой в соответствии с параметрами, специально определенными оператором.
Таким образом, автоматическое устройство или устройства улучшают эффективность процедур и обеспечивают автоматическое получение жировой ткани и процессинг жировой ткани для введения пациенту.
На фиг.4 иллюстрируется одно конкретное автоматическое устройство. Емкость для сбора ткани (не показана) размещена в устройстве 100 при использовании кодированных цветом направляющих маркировок 112-118 для правильного совмещения и введения трубопровода в соответствующие дорожки. Устройство 100 содержит множество клапанов 105 и 108 и множество насосов 104 и 109. Трубопровод размещен в серии клапанов 105, 110 и насосов 104, 109, которые управляются интегральной микропроцессорной системой для координации потока текучей среды и ткани в соответствии с программой, определенной пользователем. Выбор программы опосредован через панель 106 интерфейса пользователя. Емкость для солевого раствора размещена на удерживающей конструкции 110 и присоединена к емкости для коллектирования ткани. Флакон или пробирку коллагеназы или другого средства или смеси (не показана) для диссоциации ткани вводят в емкость для коллектирования ткани в точке, указанной ссылочным номером 103. Пакет для отходов (не показан) вводят в удерживающую конструкцию 111, камеру разделения клеток/емкость для сбора клеток размещают в удерживающей конструкции 107, а смесительную емкость для смешивания ткани и клеток размещают в удерживающей конструкции 108. Емкость для сбора ткани размещают в камере 102 перемещения/инкубации.
Жировая ткань может быть собрана в емкости для сбора ткани, в то время как емкость находится в положении в устройстве или перед размещением в устройстве. Устройство может содержать необязательную прозрачную вставку 119 или другое приспособление, обеспечивающее возможность определения объема ткани в емкости для сбора ткани. В альтернативном варианте объем может определяться путем измерения массы материала, содержащегося в камере 102 возбуждения/инкубации (соответствующей емкости 12 для сбора ткани). Этот объем может визуально отображаться на экране 106 интерфейса пользователя.
После этого микропроцессор открывает клапаны 105 на линиях 114 и 115 и приводит в действие насосы 104 на линии 114 для введения солевого раствора в камеру 102 коллектирования и удаления отходов 115 в пакет 111 для отходов. В течение этого процесса камера сбора возбуждается покачиванием и поддерживается при запрограммированной температуре посредством подогревающих устройств, интегрированных в камеру 102. В некоторых вариантах осуществления при обработке ткани может использоваться подогретый солевой раствор, причем в этом случае роль подогревающего устройства камеры возбуждения/инкубации заключается скорее в поддержании температуры в заданной запрограммированной точке, чем в увеличении температуры.
Как только ткань промыта, некоторая фракция, составляющая от 0% до 100%, целой промытой жировой ткани может быть удалена из инкубационной камеры 102 путем приведения в действие насоса 109 и клапана 110 на линии 116. Извлеченный в это время материал удерживается в смесительной камере 108.
Средство 103 диссоциации вводят в материал, остающийся в камере 102, посредством открывания клапана 105 на линии 113, закрывая другие клапаны и приводя в действие насос 104 на линии 113. После введения средства 103 диссоциации камеру 102 возбуждают и поддерживают при температуре, как описано выше. При завершении запрограммированной инкубации период возбуждения удерживают для обеспечения возможности флотации адипоцитов. Для облегчения этого процесса может быть введен дополнительный солевой раствор.
После флотации адипоцитов клапаны на линиях 112 и 115 открывают для обеспечения возможности удаления целевой клеточной популяции из камеры 102 в камеру 107 для промывки клеток. Промытые клетки удаляют по линии 117 в смесительную камеру 108, надосадочную жидкость и промывочный раствор удаляют в камеру 111 для отходов по линии 118. Дополнительный солевой раствор пропускают в систему по линии 114 для завершения промывочного процесса. Клетки смешивают в камере 108 с любой незатронутой тканью, удаленной по линии 116 раньше в течение процессинга. Перемешивание может быть достигнуто с помощью средств, известных квалифицированным в этой области специалистам, без ограничения возбуждения покачиванием/инверсией камеры или посредством компрессии, работающей в импульсном режиме, или посредством движущихся роликов. Смешанный материал может быть затем удален через порт в смесительной камере агрегата одноразового использования.
Устройство содержит управляемый микропроцессором механизм для автоматизации процесса в соответствии с предварительно запрограммированными параметрами 106. Система будет также предусматривать использование датчиков давления для детектирования блокирований и аналогичные механизмы управления качеством и надежностью.
В предпочтительном варианте осуществления компонент программных средств системы будет предусматривать автоматизированный сбор данных "прогона программы", включающих в себя, например, серийные номера компонентов одноразового использования, измерения температуры и объема, объема ткани и параметры клеток, используемые дозы фермента, период инкубации, идентификатор оператора и так далее. В предпочтительном варианте осуществления устройства система считывания штрихового кода будет интегрирована для разрешения ввода данных этих параметров (например, серийный номер агрегата одноразового использования и предельный срок действия; серийный номер и срок годности коллагеназы, идентификаторы пациента/пробы и так далее) в контроллер устройства как часть документации процессинга. Это уменьшит количество ошибок ввода данных. Это устройство может быть просто встроено в систему контроллера при использовании универсальной последовательной шины или другой интерфейсный порт и систему, известную на предшествующем уровне техники. В этом случае устройство обеспечит интегральный контроль ввода данных и документацию процесса. Распечатанный отчет об этих параметрах будет частью определенных пользователем параметров программируемой работы устройства. Очевидно, это потребует интеграцию принтера (аппаратных средств и драйвера) или драйвера принтера в программные средства плюс интерфейсного соединителя выхода для принтера (например, порт универсальной соединительной шины) в аппаратные средства устройства.
В дополнительном варианте осуществления программные средства, входящие в контроллер, будут подсказывать пользователям этапы, необходимые для правильного введения трубопровода и других элементов в устройство.
Программные средства будут также инициировать автоматическую проверку для подтверждения правильного введения трубопровода, отсутствие блокировки и так далее.
Общий метод для процессинга в этом устройстве будет использовать те же параметры, как те, которые описаны в этой заявке для ручного процессинга клеток.
Много других устройств ступенчатых механизмов, используемых для процессинга клеток, будет очевидно квалифицированным специалистам в этой области техники, и настоящее описание включено только в качестве одного примера.
Например, смешивание ткани и солевого раствора в течение промывки и разделения может иметь место посредством возбуждения так, как это делается в приведенном примере или благодаря рециркуляции текучей среды. Промывка клеток может быть опосредована механизмом непрерывного потока, например, способом вращающейся мембраны, дифференциальной адгезией, дифференциальным центрифугированием (включая без ограничения дифференциальную седиментацию, скорость или градиентное разделение) или комбинацией средств. Аналогичным образом, дополнительные компоненты для обеспечения возможности дополнительной манипуляции клетками включает в себя введение факторов роста или других модификаторов биологической реакции (Линд, 1998; Ханада и др. 1997; Либерман и др., 1998), смешивание клеток с природными или синтетическими компонентами, предназначенными для имплантирования с клетками реципиенту (Фукуда, 2001; Содиан и др., 2002; Йе и др., 2000).
Манипуляция после процессинга может также включать в себя культивирование клеток (Каплан и Брудер, 2001; Де Агарте и др., 2003; Зук и др., 2001), генную трансплантацию (Ласки и др., 1990; Моризоно и др., 2003) или дополнительную очистку клеток (Гринберг и Хаммер, 2001; Майнваринг и Роули, 1985; Швейцер и др., 1995). Механизмы для выполнения таких функций могут быть интегрированы в устройство, иллюстрируемое на фиг.4, или могут быть встроены в отдельные устройства.
В дополнительных вариантах осуществления настоящего изобретения ткань, собранная в стандартной ловушке для жировой ткани, может быть перенесена в агрегат, предназначенный для обработки других тканей. Например, компания Baxter Inc. производит и продает серию пластиковых пакетов и фильтров, предназначенных для использования при получении трансплантата костного мозга («Набор для коллектирования костного мозга с гибкими предварительными фильтрами и линейными фильтрами», Product Code, 4R2107, патенты США №4346703 и №5724988). Этот набор пакетов содержит большой конический пакет с интегральным фильтром 8001 im, который может быть использован для промывания коллектированной жировой ткани. В этом примере фрагменты жировой ткани крупнее 800 tm будут удерживаться в пакете. Эти фрагменты могут быть затем промыты повторным введением отходов через порты под фильтром. Смешивание может быть достигнуто вручную или с помощью настольного покачивающего устройства, а нагревание может быть осуществлено с помощью электрогрелки.
В полости этого пакета может иметь место разделение ткани. После этого клетки будут пропущены через интегрированный фильтр с размером пор, составляющим 800 нм (а факультативно - через один или более фильтров с меньшим размером сетки, предусмотренных в наборе) и собраны в пакете для сбора (также предусмотренном в наборе). Этот пакет может быть затем размещен в центрифуге (например, в центрифуге типа Sorval RC-3C), где клетки могут быть последовательно промыты и концентрированы. Клетки могут быть также промыты при использовании существующих устройств для промывки клеток (разработанных для промывки продуктов человеческой крови), например, устройства, продаваемые компанией Baxter Inc. (Cytomate или Baxter CS3000) или компанией Cobe Inc. (Cobe Spectra). Элементы одноразового использования могут быть интегрированы при помощи фитингов, обеспечиваемых изготовителем, или они могут быть соединены путем использования стерильного соединительного устройства, производимого, например, в компании Terumo Inc. Аналогичным образом, механизмы, описанные в менее интегральном случае применения, могут быть соединены с центральным контроллером и смонтированы как компоненты более интегрального устройства. Перистальтический насос или батарея насосов может быть использована для автоматизации прохождения потока текучей среды с использованием ручного или автоматического зажима для открывания и закрывания путей прохождения потока текучей среды.
В предпочтительном варианте осуществления настоящего изобретения устройство для удаления ткани и агрегат для ее обработки будет расположен вблизи пациента, подвергаемого терапии, например, в операционной или в амбулаторном процедурном помещении (эффективно рядом с кроватью пациента). Это обеспечивает возможность осуществления быстрого и эффективного получения ткани и ее обработки, устранения возможности ошибок в транспортировке/маркировке образца и в соответствии с этим обеспечивает возможность выполнения всего процесса в течение одной хирургической процедуры.
Следующие примеры предусмотрены для демонстрации конкретных ситуаций и установочных параметров, когда может быть использована эта технология, и не предназначены для ограничения объема настоящего изобретения и формулы изобретения, включенной в это описание.
2. Способы терапии сердечно-сосудистых заболеваний и расстройств при использовании полученного липоаспирата (ADC).
Как показано в настоящем описании, в конкретном предпочтительном варианте осуществления, ADC в соответствии с настоящим изобретением может быть использован для терапии сердечно-сосудистых заболеваний и расстройств. Полученные из жировой ткани стволовые клетки и недифференцированные клетки-предшественники в соответствии с практикой и способами, соответствующими настоящему изобретению, имеют несколько свойств, которые могут повлиять на уменьшение и/или минимизацию повреждения и стимулировать восстановление миокарда или сердечно-сосудистой системы. Они среди прочего включают в себя способность синтезировать и секретировать факторы роста, стимулирующие выживание и пролиферацию клеток, способность пролиферировать и дифференцироваться в клетках, непосредственно участвующих в новом образовании кровеносных сосудов, способность уменьшать повреждения миокарда и препятствовать образованию рубцов (осаждение коллагена и перекрестное сшивание), способность пролиферировать и дифференцироваться в мышечных клетках, способных влиять на сократимость миокарда, и способность пролиферировать и дифференцироваться в клетках миокарда.
Вышеуказанные средства уменьшения и/или минимизации повреждения и стимулирования восстановления миокарда или сердечно-сосудистой системы при использовании полученных из жира зрелых стволовых клеток в соответствии с настоящим изобретением подробно описаны ниже в разделе Примеры настоящего описания. В частности, настоящее изобретение демонстрирует в первый раз, что полученные из жира стволовые клетки (или ADC) в соответствии с настоящим изобретением экспрессирует многочисленные ангиогенные факторы роста (PIGF) и фактор васкулярного эндотелиального роста (VEGF), содержат эндотелиальные недифференцированные клетки-предшественники (ЕРС), которые имеют хорошо установленную функцию в образовании кровеносных сосудов, развиваются в кровеносных сосудах в искусственных условиях, поддерживают выживание в организме ишемической ткани, вызывают реперфузию после повреждения окклюзии/реперфузии задней конечности, возвращаются в сердце при инъецировании в животных после повреждения сердца и дифференцируются в клетки экспрессирующие маркеры, совместимые с их дифференцировкой в сердечных миоцитах при инъецировании в животных после повреждения сердца.
В соответствии с этим, в одном аспекте настоящего изобретения получаемые из жировой ткани клетки экстрагигуют из жировой ткани донора и используют для извлечения терапевтической выгоды для поврежденного или дегенерированного миокарда или другой сердечно-сосудистой ткани с помощью одного или более механизмов, демонстрируемых в этой заявке. В предпочтительном варианте осуществления клетки экстрагируют из жировой клетки индивидуума, которому они должны быть имплантированы, уменьшая в соответствии с этим сложности, связанные с антигенными и/или иммуногенными реакциями на трансплантат.
Пациентов, как правило, подвергают анализу на повреждение или заболевание миокарда с помощью одной или более следующих процедур, выполняемых врачом или другим медицинским работником: история болезни пациента, физическое обследование и объективные данные, включающие без ограничения электрокардиограмму, эхокардиографию и так далее.
В одном варианте осуществления процедуру получения выполняют до приема пациентом каких-либо препаратов, предназначенных для уменьшения свертывания крови в связи с терапией инфаркта миокарда. Однако в некоторых вариантах осуществления пациент может принимать аспирин перед процедурой получения. Помимо всего прочего, один предпочтительный способ предусматривает получение жировой ткани до какой-либо попытки процедуры замены кровеносных сосудов. Однако, как очевидно специалистам в этой области техники, ожидается, что время воздействия должно изменяться и будет зависеть от нескольких факторов, включая среди прочего стабильность пациента, профиль коагуляции пациента, доступность провайдера и стандарты качества по уходу. В конечном счете, время воздействия будет определяться практикующим врачом, ответственным за назначение ухода за пораженным болезнью пациентом.
Объем жировой ткани, полученной из пациента, может изменяться до приблизительно 2000 куб. см, а в некоторых вариантах осуществления до приблизительно 3000 куб. см. Объем удаленного жира может изменяться от пациента к пациенту и будет зависеть от числа факторов, включающих в себя без ограничения возраст, телосложение, коагуляционный профиль, гемодинамическую стабильность, тяжесть инфаркта, сочетание заболевания и общее физическое состояние.
Клетки могут быть введены пациенту в любом случае поражения миокарда. Примеры таких случаев включают в себя без ограничения острый инфаркт миокарда (сердечный приступ), застойную сердечную недостаточность (либо как терапия, либо как подготовка к трансплантации и дополнение к хирургии коронарного шунтирования артерии). Клетки могут быть извлечены заранее и храниться при низкой температуре или они могут быть извлечены точно или приблизительно в нужное время. Как описано в этой заявке, клетки могут быть введены пациенту или нанесены непосредственно на поврежденную ткань или вблизи поврежденной ткани без дополнительной обработки или следующих дополнительных процедур для дополнительной очистки, модификации, стимулирования или иного изменения клеток. Например, клетки, полученные из пациента, могут быть введены пациенту без культивирования клеток перед введением их пациенту. В одном варианте осуществления получение жировой ткани будет выполняться рядом с пациентом. Для мониторирования клинического состояния пациента может быть использован гемодинамический мониторинг.
В соответствии с настоящим изобретением, описываемым в этой заявке, полученные из жира клетки могут быть доставлены к пациенту вскоре после получения жировой ткани из пациента. Например, клетки могут быть введены непосредственно после обработки жировой ткани для получения композиции полученных из жира стволовых клеток. В одном варианте осуществления предпочтительное время доставки должно иметь порядок от часов до дней после инфаркта, используя преимущество нейрогормональной среды, которая существует после повреждения сердца. В конечном счете, время доставки будет зависеть от доступности пациента и времени обработки требуемого для обработки жировой ткани. В другом варианте осуществления время для доставки может быть относительно более продолжительным, если клетки для реинфузии пациенту подвергают дополнительной модификации, очистке, стимуляции или другой манипуляции, как описано в этой заявке. Кроме того, полученные из жира клетки могут быть введены множество раз после инфаркта. Например, клетки могут вводиться непрерывно в течение продолжительного периода времени (например, часов) или могут быть введены в виде множества болюсных вливаний, растянутых по времени. В некоторых вариантах осуществления первоначальное введение клеток будет назначаться в пределах приблизительно 12 часов после инфаркта, например шести часов, а одна или более доз клеток будет вводиться в интервалах, составляющих 12 часов.
Число клеток, вводимых пациенту, может относиться, например, к клеточному выходу после обработки жировой ткани. Часть общего числа клеток может удерживаться для более позднего использования или храниться при низкой температуре. Кроме всего прочего, подаваемая доза будет зависеть от пути доставки клеток к пациенту. Меньше клеток может понадобиться при использовании эпикардинальных или эндокардинальных систем доставки, так как эти системы и способы могут обеспечивать самый прямой путь для терапии сердечно-сосудистых состояний. В одном варианте осуществления настоящего изобретения ожидается, что число клеток, например неочищенных клеток, доставляемых к пациенту, составляет приблизительно 5,5×10 клеток. Однако это число может быть изменено на порядки величин для достижения требуемого терапевтического эффекта.
Клетки могут также быть применены с добавками для увеличения, регулирования или иного направления предполагаемого терапевтического эффекта. Например, в одном варианте осуществления и как описано в этой заявке, клетки могут быть дополнительно очищены путем использования опосредованной антителом позитивной и/или негативной клеточной селекции для обогащения клеточной популяции для увеличения эффективности, уменьшения заболеваемости или для увеличения простоты процедуры. Аналогичным образом, клетки могут быть нанесены с биосовместимой матрицей, которая облегчает в организме тканевую инженерию благодаря поддержанию и/или направлению метаболического пути имплантированных клеток. В одном подобном случае клетки могут вводиться после генетической манипуляции так, чтобы экспрессировать генные продукты, которые, как предполагается, предназначены для стимулирования терапевтической реакции (реакций), обеспечиваемых клетками. Примеры манипуляций включают в себя манипуляции для регулирования (увеличения или уменьшения) экспрессии факторов, стимулирующих ангиогенез или образование или развитие сосудов (например, VEGF), экспрессии эволюционных генов, стимулирующих дифференцировку в специфические последовательности клеточных поколений (например, MyoD) или которые стимулируют рост и пролиферацию клеток (например, bFGF-1).
Клетки могут быть также подвергнуты клеточной культивации на материале клеточного каркаса перед имплантацией. Таким образом, полученные с помощью тканевой инженерии клапаны, желудочковые участки, перикар, кровеносные сосуды и другие структуры могут быть синтезированы на природных или синтетических материалах или клеточных каркасах при использовании ADC до введения или имплантирования реципиенту (Эшенхаген и др., 2002; Циммерман и др., 2004; Циммерман и др., 2002; Нереем и Энели, 2004). Фактически была продемонстрирована дифференцировка в искусственных условиях полученных из жира стволовых клеток и недифференцированных клеток-предщественников в экспрессирующих клетки маркерах сердечных миоцитов (Гаустад и др., 2004; Рангаппа и др., 2003).
3. Пути введения ADC для терапии сердечно-сосудистого заболевания и расстройства
В одном варианте осуществления предпочтительным является прямое введение клеток в место предполагаемого воздействия. Это может быть достигнуто прямой инъекцией во внешнюю поверхность сердца (эпикардиальное), прямой инъекцией в миокард через внутреннюю поверхность (эндокардиальное) посредством введения соответствующей канюли, посредством артериальной или венозной инфузии (включая механизмы ретроградного потока) или с помощью других средств, описанных в этой заявке или известных на предшествующем уровне техники. Пути введения, известные обычным специалистам в этой области техники, включают в себя без ограничения внутривенное, внутрикоронарное, эндомиокардиальное, эмпимиокардиальное, внутрижелудочковое, ретросинусное или внутривенное.
Как указано выше, клетки могут быть введены несколькими путями, включая системное введение посредством венозной или артериальной инфузии (влючая ретроградную инфузию) или прямой инъекцией в сердце. Системное введение, в частности, посредством периферийного венозного доступа имеет преимущество в том отношении, что оно является минимально инвазивным относительно природной перфузии сердца и способностью полученных из жировой ткани клеток попадать в место повреждения. Клетки могут быть введены одним болюсом, посредством медленной инфузии, или ступенчатыми сериями введений, отделенных несколькими часами, или обеспечиваемые клетки соответственно хранят несколько дней или недель. Клетки также могут быть введены путем использования зондирования так, чтобы первый проход клеток через сердце увеличивался благодаря использованию баллонов для управления потоком миокардиальной крови. Как при периферийном венозном доступе, клетки могут быть введены посредством катетеров одним болюсом или множеством меньших порций. Клетки могут быть также введены непосредственно в миокард посредством эпикардиальной инъекции. Это может быть выполнено при прямой визуализации в контексте процедуры вскрытого сердца (например, как в операции шунтирования коронарной артерии) или размещения внутрижелудочкового вспомогательного устройства. Катетеры, снабженные иглами, могут быть использованы для доставки клеток непосредственно в миокард эндокардиально, что обеспечило бы возможность менее инвазивных средств прямого введения.
В одном варианте осуществления путь доставки будет предусматривать внутривенную доставку посредством стандартного периферийного внутривенного катетера. В другом варианте осуществления клетки могут быть доставлены по внутрикоронарному пути, доступному с помощью обычно приемлемых способов. Поток клеток может регулироваться последовательным наполнением/опорожением дистального и проксимального баллонов, расположенных в сосудистой сети пациента, создавая в соответствии с этим кратковременные зоны отсутствия потока, что стимулирует клеточную прививку или клеточное терапевтическое действие. В другом варианте осуществления клетки могут доставляться эндокардиальным способом (на внутреннюю поверхность полости сердца), что может потребовать соответствующего катетера, а также способности визуализации или детектирования намеченной целевой ткани. В альтернативном варианте клетки могут доставляться эпикардиальным способом (на внешнюю поверхность сердца). Такая доствка может быть достигнута посредством непосредственно визуализации во время процедуры вскрытого сердца или тораскопическим способом, требующим специальных приборов для доставки клеток. Кроме того, клетки могут быть доставлены следующими путями одним или в комбинации с одним или более способами, идентифицированными выше как подкожный, внутримышечный, подъязычный, ретроградной коронарной перфузии, аппаратуры коронарного шунтирования, оборудования искусственной мембранной оксигенации (ЕСМО) и через перикардиальное окно.
В одном варианте осуществления клетки вводят пациенту как болюс внутрь сосуда или инфузионно. В другом варианте осуществления клетки могут быть ресуспендированы в искусственной или природной среде или клеточном каркасе ткани перед введением пациенту. Доза клеток, вводимая пациенту, будет зависеть от количества полученной жировой ткани и индекса массы тела донора (как меры количества доступной жировой ткани). Количество полученной ткани будет также определяться степенью миокардиального повреждения или дегенерации. Неоднократное лечение, использующее множество сборов ткани, или использование одного сбора с соответствующим хранением клеток между использованиями также предполагается настоящим изобретением.
Порции обработанного липоаспирата могут храниться перед введением пациенту. В течение кратковременного хранения (менее 6 часов) клетки могут храниться при комнатной температуре или ниже комнатной температуры в герметичной емкости с добавлением или без добавления питательного раствора.
Средневременное хранение (менее 48 часов) предпочтительно осуществляют при температуре 2-8°С в изоосмотическом буферном растворе (например, типа Плазмалитег) в емкости, содержащей или покрытой веществом, которое препятствует адгезии клеток. Более долговременное хранение предпочтительно осуществляют путем поддержания соответствующей криогенной температуры и хранят клетки в условиях, которые способствуют сохранению клеточной функции, как описано в заявке PCT/UA 02/29207, поданной 13 сентября 2002 года, и в предварительной заявке США №60/322070, поданной 14 сентября 2001 года, содержание которых включены в эту заявку в качестве ссылки.
В соответствии с одним аспектом настоящего изобретения, полученные из жировой ткани клетки, которые вводят пациенту, могут действовать как транспортные средства доставки фактора роста. Например, путем инженерии клеток для экспрессии одного или более факторов роста, пригодных для смягчения симптомов, связанных с сердечно-сосудистым расстройством или заболеванием, клетки могут быть введены пациенту и предназначены для освобождения одного или более факторов роста. Освобождение может быть обеспечено регулируемым образом в течение продолжительных периодов времени. Освобождение может регулироваться так, что фактор (факторы) роста освобождается импульсно или периодически так, чтобы имелись локальные подъемы в количестве фактора роста и/или локальные снижения в количестве фактора роста вблизи поврежденной области ткани.
Клетки, которые вводят пациенту, не только помогают восстановлению нарушенной функции тканей, но также обеспечивают реконструкцию поврежденных тканей.
Доставка клеток может иметь место без ограничения следующими местами: клиника, клиническое отделение, отдел по чрезвычайным ситуациям, больничная палата, отделение интенсивной терапии, операционная, комплекс помещений для катетеризации, комплекс радиологических помещений.
В одном варианте осуществления эффекты клеточной терапии были бы продемонстрированы, но не ограничены одной из следующих клинических мер: увеличенной сердечной функцией выброса, уменьшением сердечной недостаточности, уменьшенным размером инфаркта, уменьшенной соответствующей симптоматикой заболевания (отек легких, почечная недостаточность, аритмия), повышенной выносливостью к физической нагрузке или другими критериями качества жизни, а также уменьшением смертности. Эффекты клеточной терапии могут проявляться как ранние через несколько часов после процедуры и могут сохраняться в течение нескольких лет.
Пациенты, как правило, подвергаются мониторированию перед и в течение доставки клеток. Процедуры мониторирования включают в себя без ограничения: изучение свертывания, насыщение кислородом, гемодинамическое мониторирование и мониторирование сердечного ритма. После доставки клеток пациентам может потребоваться период приблизительно 24 часа мониторирования неблагоприятных явлений. Исследования по мониторированию могут включать в себя без ограничения оценку функциональной способности пациента (например, одышка при усилии, сердечная астма, стенокардия), эхокардиографию, изучение ядерной перфузии, магнитно-резонансную визуализацию, позитронную эмиссионную топографию и коронарную ангиографию.
Как было описано выше, в предпочтительном варианте осуществления ADC, то есть активную, полученную из жира стволовую клеточную популяцию, вводят непосредственно пациенту. Другими словами, активную клеточную популяцию, например стволовые клетки и/или эндотелиальные недифференцированные клетки-предшественники, вводят пациенту без удаления из системы или без оказания воздействия внешней окружающей среды на систему перед введением пациенту. Обеспечение замкнутой системы уменьшает возможность загрязнения материала, вводимого пациенту.
Таким образом, обработка жировой ткани в замкнутой системе обеспечивает преимущества перед существующими способами, поскольку активная клеточная популяция более вероятно является стерильной. В таком варианте осуществления только раз стволовые клетки и/или эндотелиальные недифференцированные клетки-предшественники подвергаются воздействию внешней окружающей среды или удаляются из системы - это когда клетки извлекаются в аппликатор и вводятся пациенту. В одном варианте осуществления аппликатор может быть частью замкнутой системы. Таким образом, клетки, используемые в этих вариантах осуществления, не подвергаются культивированию или хранению при криогенных температурах, а могут быть введены пациенту без дополнительной обработки или быть введены пациенту после смешивания с другими тканями и клетками.
В другом варианте осуществления, по меньшей мере, часть активной клеточной. популяции хранится для более поздней имплантации/инфузии. Эта популяция может быть разделена на более чем одну порцию или элемент, так что часть популяции стволовых клеток и/или эндотелиальных недифференцированных клеток-предшественников удерживается для более позднего использования, тогда как часть немедленно вводится пациенту. Среднесрочное/долгосрочное хранение всех или части клеток в банке клеток также находится в пределах объема настоящего изобретения, как описано в патентной заявке США №10/242094, названной «Сохранение неэмбриональных клеток из негемопоэтических тканей», поданной 12 сентября 2002 года, которая притязает на преимущемтво патентной заявки США №60/322070, поданной 14 сентября 2001 года, содержание которых включено в эту заявку в качестве ссылки. В конце обработки концентрированные клетки могут быть загружены в устройство доставки, например шприц, т.е. введены пациенту с помощью любого средства, известного обычным специалистам в этой области техники.
II. Фармацевтические композиции
Активная клеточная популяция может быть применена одна или в комбинации с другими клетками, тканью, фрагментами ткани, факторами роста, например VEGF, и другими известными ангиогенными или артериогенными факторами роста, биологически активными или инертными соединениями, рассасывающимися пластиковыми клеточными каркасами или другой добавкой, предназначенной для улучшения доставки, эффективности, приемлемости или функции популяции. Клеточная популяция может быть также модифицирована путем введения ДНК или путем размещения в клеточной культуре так, чтобы изменять, увеличить или дополнить функцию клеток для отклонения структурной или терапевтической цели. Например, технологии трансплантации генов для стволовых клеток известны обычным специалистам в этой области техники, как описано в работе (Моризоно и др., 2003; Моска и др., 2000) и могут включать в себя технологии вирусной трансфекции, а более конкретно, технологии трансплантации гена аденосателлитного вируса, как описано в работах (Вальтер и Штейн, 2000; Атаносопоулос и др., 2000). Как описано в работе (Мураматсу и др., 1998), могут быть также реализованы невирусные технологии.
В другом аспекте клетки могут быть скомбинированы с кодирующим ген проангиогенным и/или кардиомиогенным фактором (факторами) роста, которые обеспечивают возможность клеткам действовать как их собственный источник фактора роста в сердечном восстановлении и регенерации. Также могут быть использованы кодирующие ген антиапотические факторы или агенты. Дополнением гена (или комбинации генов) может быть без ограничения любая технология, известная из предшествующего уровня техники, например, аденовирусная трансдукция, «генные пушки», трансдукция, опосредованная липосомой, и трансдукция, опосредованная ретровирусом или лентивирусом, плазмид, аденосателлитный вирус. Клетки могут быть имплантированы вместе с материалом носителя, несущим транспортное средство доставки гена, способное освобождать и/или представлять гены клеткам по прошествии длительного времени так, чтобы трансдукция могла продолжаться или инициироваться сама по себе. В частности, если клетки и/или ткань, содержащую клетки, вводят пациенту, другому, чем пациент, из которого были получены клетки и/или ткань, то пациенту, принимающему клетки и/или ткань, для уменьшения, а предпочтительно для предотвращения отвержения трансплантата, может быть введен один или более иммунодепрессивных агентов. Используемый в этой заявке термин «иммунодепрессивное лекарственное средство или агент» относится к фармацевтическим веществам, которые подавляют нормальную иммунную функцию или изменяют с нормальной иммунной функцией. Примеры иммунодепрессантов, пригодных для использования со способами, описанными в этой заявке, включают в себя агенты, которые подавляют пути стимуляции Т-клеток/В-клеток, например, агенты, которые влияют на сопряжение Т-клеток и В-клеток по путям CTLA4 и В7, как описано в патенте США №20020182211. Предпочтительным иммунодепрессантом является циклоспорин А. Другие примеры включают в себя миофенилатмофетил, рапамицин и антитимоцит-глобулин. В одном варианте осуществления иммунодепрессивное лекарственное средство вводят, по меньшей мере, как один терапевтический агент. Иммунодепрессивное лекарственное средство вводят в композиции, которая совместима с путем введения, и вводится субъекту в дозе, достаточной для достижения требуемого терапевтического эффекта. В другом варианте осуществления иммунодепрессивное лекарственное средство вводят кратковременно в течение достаточного времени для стимулирования толерантности к ADC, соответствующего настоящему изобретению.
В некоторых вариантах осуществления настоящего изобретения клетки вводят пациенту с одним или более агентами клеточной дифференцировки, например, цитокинами и факторами роста. Примеры различных агентов клеточной дифференцировки описаны в работах (Джимба и др., 1995; Леннон и др., 1995; Маджумдар и др., 1998; Каплан и Голдберг, 1999; Огуши и Каплан, 1999; Питтенжер и др., 1999; Каплан и Брудер, 2001; Фукуда, 2001; Ворстер и др., 2001; Зук и др., 2001).
Настоящее изобретение дополнительно поясняется с помощью следующих примеров, которые никоим образом не должны восприниматься как дополнительное ограничение. Содержание всех приведенных ссылок, включая литературные ссылки, выданные патенты, опубликованные патентные заявки и патентные заявки, находящиеся в процессе совместного рассмотрения, указанные в этой заявке, включены в это описание в качестве ссылки.
ПРИМЕРЫ
ADC или активная популяция полученных из жира стволовых клеток, используемые в примерах, описываемых ниже, были получены способом (способами), описанным в этом описании, и/или способом (способами), описанным в заявке США №10/316127, названной «Системы и способы терапии пациентов обработанными клетками липоаспирата», поданной 9 декабря 2002 года, которая притязает на приоритет предварительной заявки США №60338856, поданной 7 декабря 2001 года, содержание которой включено в эту заявку в качестве ссылки.
ПРИМЕР 1: Экспрессия ангиогенного фактора роста, VEGF, посредством ADC.
Фактор эндотелиального роста (VEGF) является одним из главных регуляторов ангиогенеза (Наги и др., 2003; Фолкман, 1995). Фактор роста плаценты, другой член семейства VEGF, играет подобную роль как в ангиогенезе, так и артериогенезе посредством развития коллатеральных сосудов в ответ на увеличенную перфузию (Наги и др., 2003; Пипп и др., 2003; Шольц и др., 2003). В частности, трансплантация клеток дикого типа (PIGF+/+) в PIGF в модели « нокаутированной мыши» восстанавливает способность быстрого выздоровления от ишемии задних конечностей (Шольц и др., 2003).
При данной важности ангиогенеза и артериогенеза для процесса замены кровеносных сосудов экспрессию PIGF и VEGF посредством клеток ADC исследовали с помощью анализа ELISA (R& D Systems, Minneapolis, MN) при использовании клеток ADC от трех доноров. Один донор имел историю гипергликемии и диабет второго типа (состояние сильно связанное с заболеванием микро- и макрососудов, включая пациентов с заболеванием коронарной артерии). Клетки ADC от каждого донора были покрыты при 1000 клеток/см2 в среде DMEMIF-12 с добавлением 10% FCS и 5% HS и совместно культивированы. Плавающие на поверхности образцы были взяты и подвергнуты анализу на экспрессию белка PIGF и VEGF. Как показано на фиг.5А и фиг.5В, результаты показывают экспрессию VEGF (фиг.5А) и PIGF (фиг.5В) посредством полученных из жира стволовых клеток, соответствующих настоящему изобретению.
Эти данные показывают, что полученные из жировой ткани стволовые клетки и недифференцированные клетки-предшественники от нормальных пациентов и больного диабетом экспрессируют ангиогенные и артериогенные факторы роста. Это важно, так как пациенты больные диабетом, подвергаются повышенной опасности сердечно-сосудистого заболевания, а эти данные показывают, что клетки ADC сохраняют их ангиогенную способность при диабете. Таким образом, пациенты больные диабетом, могут получить ангиогенную пользу от своих собственных клеток ADC.
ПРИМЕР 2: ADC содержат клеточные популяции, которые участвуют в ангиогенезе. Известно участие в ангиогенезе эндотелиальных недифференцированных клеток-предшественников (ЕРС).
Циркуляция эндотелиальных недифференцированных клеток-предшественников была обнаружена в периферической крови, пуповинной крови, костном мозге, эмбриональной печени (Такахаши, 1999; Асахара, 1999; Асахара, 1997; Луманс, 2004; Шинтани, 2001; Ваза, 2001). Для определения концентрации ЕРС в полученных из жира стволовых клетках был сделан анализ ЕРС. Клетки ADC были размещены на покрытых фибронектином пластинах и культивированы в эндотелиальной клеточной среде в течение трех дней для удаления зрелых эндотелиальных клеток.
Несцепленные клетки были удалены и покрыты вновь. Через 14 дней колонии были идентифицированы окрашиванием FITC-сопряженным Ulex europaeus Agglutinin-1 (Vector Labs, Burlingame, CA) и помеченным Dil ацетилированным LDL (Molecular Probes, Eugene, OR). Как иллюстрируется на фиг.6, результаты показывают концентрацию ЕРС, составляющую приблизительно 500 ЕРС/106 клеток ADC.
Наличие ЕРС в клеточной популяции в полученных из жира клеток и недифференцированных клеток-предшественников показывает, что эта популяция может непосредственно участвовать в развитии новых кровеносных сосудов и усилении ангиогенеза и реперфузии, уменьшая в соответствии с этим длительность ишемии после инфаркта миокарда и застойной сердечной недостаточности.
ПРИМЕР 3: Развитие васкулярных структур в ADC ин витро.
Признанный на известном уровне техники анализ ангиогенеза представляет собой анализ, в котором эндотелиальные клетки, выращенные на питающем подслое фибробластов, развивают сложную сеть CD31-позитивных трубок, напоминающих нарождающуюся капиллярную сеть (Донован и др., 2001). ADC образуют подобные сети в отсутствии питающего подслоя (фиг.7А). Следует отметить, что клетки ADC, полученные от мышей, больных гликемией, с диабетом первого типа, индуцированным стрептозотоцином (STZ), через восемь недель после введения STZ, образуют подобные структуры с подобной концентрацией, как у необработанных мышей (фиг.7В).
Это важно, так как пациенты с диабетом подвергаются повышенной опасности сердечно-сосудистого заболевания, а эти данные показывают, что клетки ADC сохраняют их ангиогенную способность в условиях диабета. Таким образом, пациенты, страдающие диабетом, могут получить ангиогенную поддержку из своих собственных клеток ADC.
Короче говоря, результаты примеров 1-3, приведенных выше, показывают, что полученные из жира стволовые клетки содержат популяции клеток, которые могут стимулировать ангиогенез и артериогенез. Эти результаты также показывают, что полученные из жира стволовые клетки из донора, который является человеком, больным диабетом, или из обработанных STZ мышей, проявляющих длительную гипергликемию, вероятно, не имеют дефицита в клетках, которые стимулируют ангиогенез. Таким образом, жир может представлять резервуар регенеративных клеток, полезных для пациентов с диабетом, у которых риск сердечно-сосудистого заболевания существенно повышен.
ПРИМЕР 4: Развитие сосудистых структур в ADC в условиях организма.
Ин витро ангиогенный потенциал, хотя и является обещающим, является небольшим, если клетки не влияют на ангиогенную активность в организме. Хирургическое создание критической ишемии конечностей у грызунов является хорошо признанной моделью, в которой могут наблюдаться (Шаттмен, 2000; Шольц, 2002; Такаши, 1999) конкурентные процессы артериогенеза (восстановление и расширение коллатеральных сосудов в значительной степени в ответ на увеличенное усилие сдвига) и ангиогенеза (развитие новых сосудов в ответ на ишемию). Модель была использована в иммунодефицитных (NOD-SCID) мышах, в которых могла наблюдаться способность человеческих клеток возбуждать реперфузию. В частности, животные были анестезиированы кетамином и ксилазином (80 мг/кг, 7,5 мг/кг) и размещены на операционной поверхности в положении лежа на спине. Предоперационный кровоток определяли для обеих задних конечностей, как описано ниже. Животные были подготовлены бетадином, задрапированы обычным стерильным образом и размещены в циркуляционном водяном термостате. Был сделан односторонний разрез длиной 1,5 см, проходящий от места начала задней конечности до места, проксимального колену, для обнажения подвздошной артерии, проксимальной ее раздвоению в глубокую артерию бедра и поверхностную артерию бедра. Сосудистая сеть была перевязана шелковой лигатурой 3-0 на следующих участках: 1) в месте подвздошной артерии, проксимально раздвоению, 2) дистально месту начала глубокой артерии бедра, 3) проксимально ответвлению поверхностной артерии бедра. После наложения лигатуры эта сосудистая сеть была удалена. Затем было сделана попытка идентифицировать какие-либо очевидные колагерали, которые были лигированы и затем удалены. Рана и мышечный слой были закрыты викрилом
4-0, а кожа закрыта викролом 5-0. Животные после операции получали бупренорфином (0,5 мг/кг) и возвращены на циркуляционный водяной термостат в лежачем положении. Через 24 часа после хирургического вмешательства животным инъецировали клетки ADC 5×106 через хвостовую вену. NOD-SCID мышам были инъецированы человеческие донорные клетки, содержащие в одном исследовании клетки пациента, страдающего диабетом. Наблюдение велось в течение 14 дней после обработки.
В этих исследованиях обработанные ADC животные показали статистически значительное улучшение в сохранении структур конечностей (спасение конечностей; 2/3 необработанных мышей потеряло все нижние структуры задних конечностей по сравнению с 0/5 обработанных ADC животных) и восстановлении кровотока (фиг.8). Примечательнее всего то, что в NOD SCID мышах, получивших диабетические человеческие донорные клетки, на 14 день кровоток был восстановлен до 50% в обработанных животных по сравнению с 10% в необработанных животных (р<0.5). На 19 день имел место скачок, так что перфузия в экспериментальной конечности была больше, чем в контрольной. Эта реакция находится в пределах диапазона, наблюдаемого с клетками, полученными от двух нормальных (недиабетических) доноров (50-90%).
В этой модели восстановление кровотока обусловлено восстановлением и расширением коллатеральных сосудов, т.е. ангиогенезу в нижней конечности. Эти процессы также являются главными для восстановления кровотока в сердце после инфаркта. Таким образом, способность ADC стимулировать эти процессы в организме сильно поддерживает применение клеток ADC в лечении инфаркта миокарда. Также важно отметить то, что клетки ADC, полученные от диабетического донора (т.е. от пациента с высоким риском сердечно-сосудистого заболевания), также продемонстрировали эту активность.
ПРИМЕР 5: Увеличение дозы ADC связано с улучшением выживания трансплантата аутологической жировой ткани в пластической и реконструктивной хирургии (Фултон, 1998; Шиффман, 2001). Однако эта процедура ограничивается тем, что фрагменты жировой ткани трансплантируются без сосудистой поддержки, как результат, выживание трансплантата зависит от образования новых сосудов (Колеман, 1995; Эппли и др., 1990). Таким образом, трансплантируемая ткань ограниченно представляет ишемическую ткань.
Проводили исследование в крысах Фишера, в которые фрагменты жировой ткани трансплантировали в подкожное пространство поверх мышц внешнего бедра. В правую ногу трансплантировали 0,2 г одних фрагментов жировой ткани, а в левую ногу - 0,2 г фрагментов жировой ткани с добавкой полученных из жира стволовых клеток в трех различных дозах (1,7×10-1,3×10 клеток/трансплантат; три животных на дозу). После этого животные сохранялись в течение одного месяца, после чего животных умерщвляли и трансплантаты извлекали, взвешивали, фиксировали в формалине и внедряли в парафин для гистологического анализа.
Как иллюстрируется на фиг.9А, результаты показывают минимальное сохранение трансплантированной ткани в контрольной ноге и зависимое от дозы сохранение массы трансплантата в обработанной ноге.
Кроме того, иммуногистохимический анализ трансплантатов показал значительный неоангиогенез и перфузию в трансплантатах, обработанных полученными из жира стволовыми клетками (фиг.9В, стрелки). Это было связано с сохранением морфологии жировой ткани (фиг.9В).
Как указано выше, демонстрация того, что клетки ADC стимулируют выживание неадекватно обработанной ишемической ткани, является важным показателем клинического потенциала использования ADC при сердечно-сосудистом заболевании.
ПРИМЕР 6: Миокардиальное приживление трансплантата посредством ADC.
Криоповреждение миокарда является признанной хирургической моделью для исследования роли клеточной терапии в регенерации миокарда (Маршлинский и др., 1987). Для демонстрации способности клеток ADC восстанавливать поврежденный миокард и в соответствии с этим подавлять образование рубца (осаждение и перекрестное сшивание коллагена) было выполнено криоповреждение миокарда у мышей B6129SF1/J. Немедленно после повреждения 1 миллион клеток ADC (1,0×106), полученный из мышей ROSA26, которые являются трансгенными для гена lacZ, был инъецирован интравентрикулярно. Ткань сердца реципиента, окрашенная В-галактозидазой, обнаруживает присутствие полученных из жира стволовых клеток донора, благодаря окрашиванию в голубой цвет. Получали сердца мышей и подвергали обработке в следующих пяти временных точках после инъекции: 1 день, 7 день, 14 день, 28 день, 84 день. Как иллюстрируется на фиг.10, результаты показывают приживление трансплантата полученных из жира стволовых клеток донора в области нарушенного миокарда во всех точках, указанных выше. Фиг.10 демонстрирует гистологический график времени приживления трансплантата.
Важно, что иммуногистохимический анализ полученных от донора (бета-галактосидаза-позитив) клеток на 14 день показал, что многие полученные от донора клетки экспрессировали тяжелую цепь (фиг.11) миозина маркера сердечных миоцитов. Таким образом, клетки ADC могут быть способными пополнять сердечные миоциты, которые утеряны после сердечного приступа (инфаркта миокарда).
Для расширения этих находок изучали приживление трансплантата, полученного от донора липоаспирата в модели окклюзии/реперфузии крысы. В этой экспериментальной структуре, главная коронарная артерия иммунокомпетентной крысы Вистара была временно окклюзирована при использовании пролена 7-0 и небольшого кусочка силастиковой трубки, действующей как ловушка поверх артерии. Через один час окклюзию устраняли и обеспечивали возможность реперфузии крови к ишемическому миокарду. Эта модель более точно представляет механизмы повреждения и регенерации, имеющейся в человеческой клинической практике. Немедленно после реперфузии приблизительно 1 миллион клеток ADC (1×106), полученных от мышей Rosa 26, был инъецирован по интравентрикулярно. Сердца были получены через одну неделю после инъекции. Как иллюстрируется на фиг.12, результаты показывают приживление трансплантата полученных от донора клеток ADC.
ПРИМЕР 7: Терапия острого сердечного повреждения.
Острый инфаркт миокарда (сердечный приступ) приводит в результате к ишемическому повреждению миокарда.
Повреждение ткани может быть минимизировано посредством реперфузии поврежденной ткани и посредством регенерации ткани миокарда (Мудри и др., 1996; Орлик и др., 2003; Райнох и др., 2001; Штрауэр и др., 2002; Ассмус и др., 2002). Клеточная терапия с помощью клеток, полученных из жира, как описано в этой заявке, стремится обеспечить превосходный источник регенеративных клеток по сравнению с клеточной терапией с помощью клеток, полученных не из жира, например, полученных из костного мозга.
Предполагается что у пациента инфаркт миокарда. Допускается, что пациент находится в часе от инфаркта. Пациенту предписывается клеточная терапия с помощью клеток, полученных из жира. Исследуется габитус пациента с целью выявления места, пригодного для сбора жировой ткани. Места получения характеризуются, по меньшей мере, одним из следующих элементов: потенциальное пространство, ограниченное нормальными анатомическими структурами, нет главных сосудистых и висцеральных структур с риском для повреждения и простота доступа. Предпочтительными являются нетронутые места для получения, но предшествующее место получения не препятствует дополнительному получению жировой ткани. Потенциальные места получения ткани включают в себя без ограничения боковую и медиальную области бедра нижних конечностей, передний паннус брюшной стенки и билатеральные боковые области. Пациенту проводят подкожную инъекцию раствора распухающей текучей среды, содержащей комбинацию лидокаина, солевого раствора и эпинефина, например, в разных стандартных режимах дозирования. При использовании скальпеля (например, скальпель лезвии-11) в медиальной бедренной части правой и/или левой ноги пациента делают небольшую колотую рану для того, чтобы пересечь дермис. Лезвие поворачивают на 360 градусов для завершения раны. Канюлю с тупым кончиком (например, канюлю номер 14) вставляют в полость подкожной жировой ткани ниже реза. Канюлю соединяют с аспиратором, подключенным к источнику питания. Канюлю перемещают в полости жировой ткани для разрушения архитектуры соединительной ткани. Получают приблизительно 500 см3 аспирата. После извлечения жировой ткани с помощью стандартной хирургической технологии достигают остановки кровотечения и закрывают рану.
Липоаспират подвергают обработке в соответствии со способами, описанными в этой заявке выше для получения единицы концентрированных полученных из жира стволовых клеток. На основе обработки липоаспирата для пациента подбирают начальную дозу стволовых клеток в диапазоне между приблизительно 5,5×104 стволовых клеток и 5,5×105 стволовых клеток. Пациент получает две дополнительные дозы с 12 часовыми интервалами после первоначального введения. Стволовые клетки вводят пациенту через венозный центральный катетер. Для стимулирования клеточного приживления в целевой области поток стволовых клеток регулируют посредством баллона, распложенного ниже по технологической цепочке от целевого места, и посредством баллона, расположенного по технологической цепочке выше целевого места, для создания областей слабого или минимального потока крови.
Улучшения у пациента отмечаются в пределах приблизительно шести часов после процедуры введения стволовых клеток. Через несколько дней после процедуры введения стволовых клеток отмечается дополнительное улучшение состояния пациента, подтверждаемое фракцией выброса повышенного объема крови, уменьшенной степенью сердечной недостаточности, уменьшенным размером инфаркта, улучшенной выносливостью к физической нагрузке и другими критериями качества жизни.
Любой элемент или комбинация элементов, описанных в этой заявке, включены в объем настоящего изобретения при условии, что элементы, включенные в любую такую комбинацию, не являются взаимно несовместимыми, как будет очевидно из контеста этого описания и знания обычного специалиста в этой области техники. Для суммирования результатов настоящего изобретения были описаны некоторые аспекты, преимущества и новые элементы настоящего изобретения. Безусловно, должно быть очевидно, что не обязательно все такие аспекты, преимущества или элементы будут воплощены в любом конкретном варианте осуществления настоящего изобретения.
Дополнительные преимущества и аспекты настоящего изобретения очевидны из подробного описания и формулы изобретения.
Вышеописанные варианты осуществления были приведены в качестве примеров и настоящее изобретение не ограничено этими примерами. Квалифицированным специалистам в этой области техники будет очевидно множество изменений и модификаций описанных вариантов осуществления после знакомства с вышеизложенным описанием. Помимо всего прочего, квалифицированным специалистам в этой области техники станут очевидны другие комбинации, исключения, замены и модификации, принимая во внимание описание, приведенное в этой заявке. В соответствии с этим настоящее изобретение не ограничено описанными вариантами осуществления, а пунктами прилагаемой формулы изобретения.
Сумма публикаций и патентов приведена выше. Каждая из указанных публикаций и патентов включена во всей своей полноте в эту заявку в качестве ссылки.
| название | год | авторы | номер документа |
|---|---|---|---|
| СТВОЛОВЫЕ КЛЕТКИ И РЕШЕТКИ, ПОЛУЧЕННЫЕ ИЗ ЖИРОВОЙ ТКАНИ | 2000 |
|
RU2306335C2 |
| КЛЕТОЧНАЯ ТЕРАПИЯ ИШЕМИЧЕСКОЙ ТКАНИ | 2009 |
|
RU2535966C2 |
| ДИФФЕРЕНЦИРОВКА СТРОМАЛЬНЫХ КЛЕТОК, ПОЛУЧЕННЫХ ИЗ ЖИРОВОЙ ТКАНИ, В ЭНДОКРИННЫЕ КЛЕТКИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ И ИХ ИСПОЛЬЗОВАНИЕ | 2002 |
|
RU2351648C2 |
| СТРОМАЛЬНЫЕ КЛЕТКИ, ПОЛУЧЕННЫЕ ИЗ ЖИРОВОЙ ТКАНИ, ДЛЯ ЗАЖИВЛЕНИЯ ДЕФЕКТОВ РОГОВИЦЫ И ВНУТРИГЛАЗНЫХ ДЕФЕКТОВ И ИХ ИСПОЛЬЗОВАНИЕ | 2002 |
|
RU2331668C2 |
| КЛЕТКИ, ПРОИЗВОДНЫЕ ОТ КАРДИАЛЬНОЙ ТКАНИ | 2010 |
|
RU2642282C1 |
| КЛЕТКИ, ПРОИЗВОДНЫЕ ОТ КАРДИАЛЬНОЙ ТКАНИ | 2010 |
|
RU2662675C1 |
| КЛЕТКИ, ПРОИЗВОДНЫЕ ОТ КАРДИАЛЬНОЙ ТКАНИ | 2010 |
|
RU2583287C2 |
| АМНИОТИЧЕСКИЕ АДГЕЗИВНЫЕ КЛЕТКИ | 2009 |
|
RU2562154C2 |
| АДГЕЗИВНЫЕ КЛЕТКИ ЖИРОВОЙ ТКАНИ ИЛИ ПЛАЦЕНТЫ И ИХ ИСПОЛЬЗОВАНИЕ В ЛЕЧЕБНЫХ ЦЕЛЯХ | 2008 |
|
RU2709780C2 |
| БИОТРАНСПЛАНТАТ И СПОСОБ ЛЕЧЕНИЯ ЛЕГОЧНОЙ ГИПЕРТЕНЗИИ | 2004 |
|
RU2271817C1 |
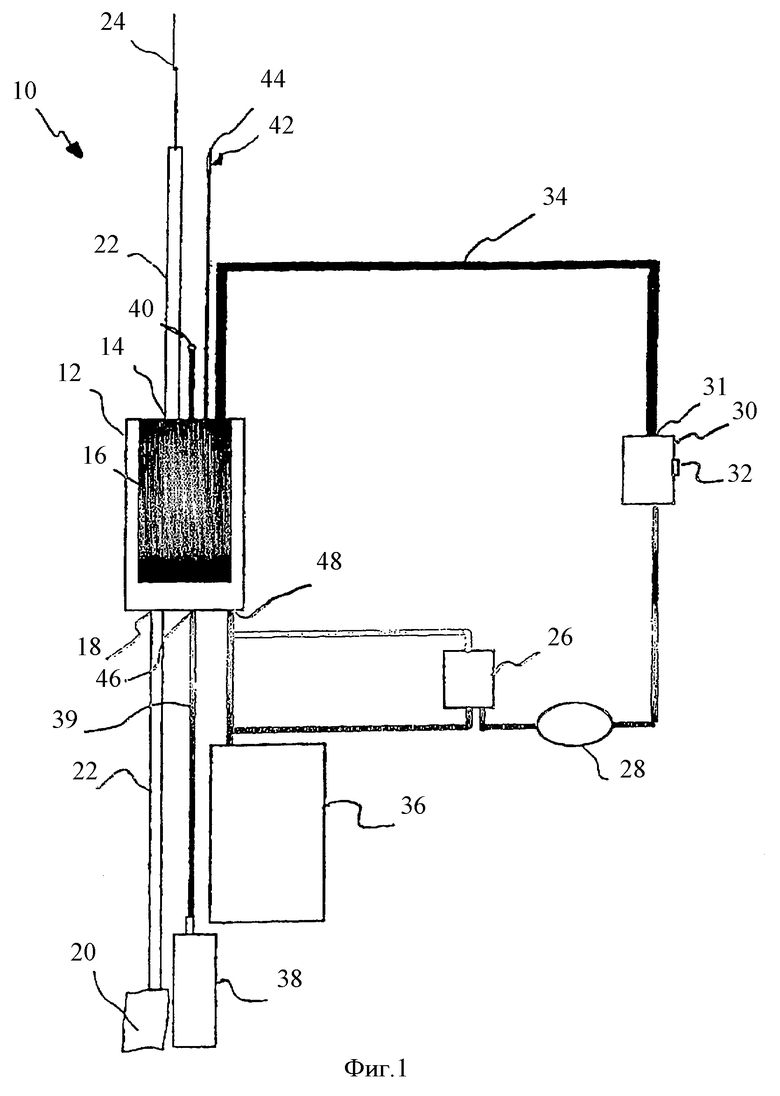
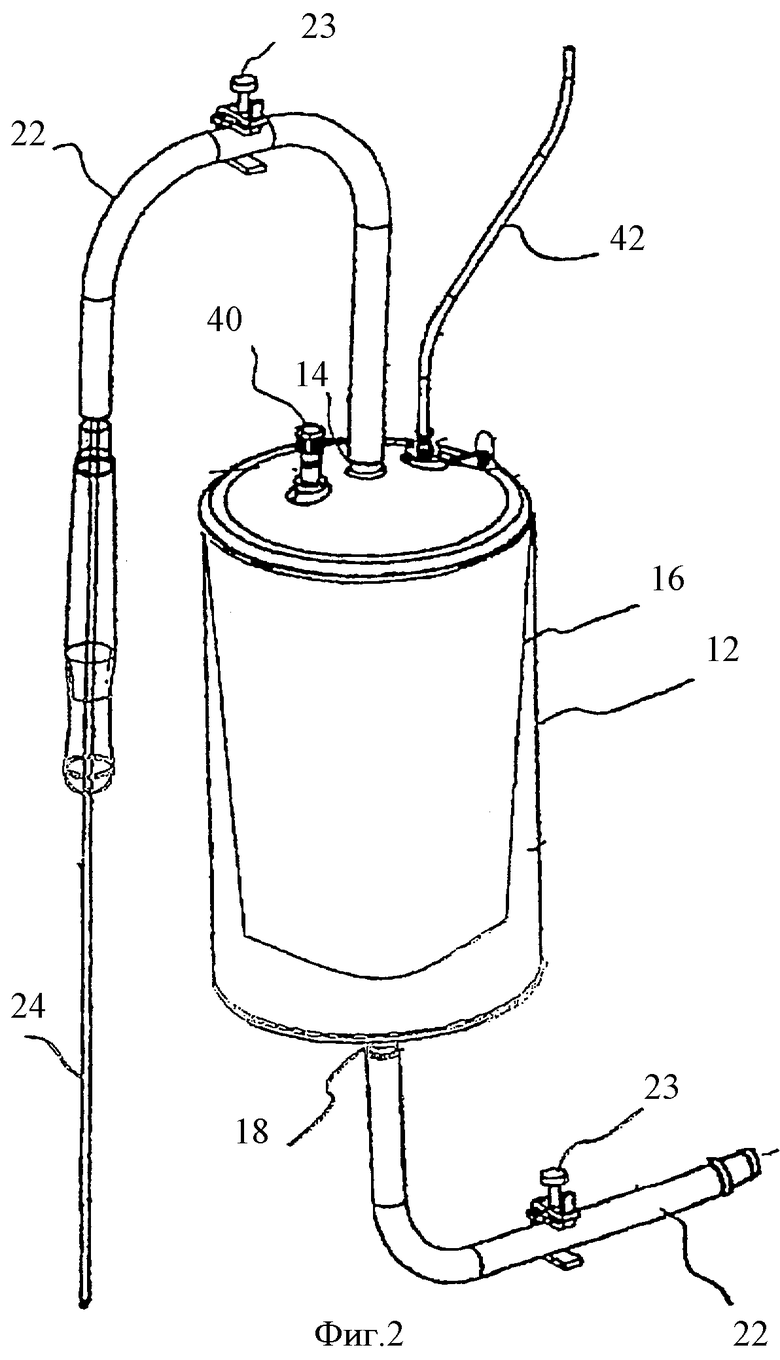
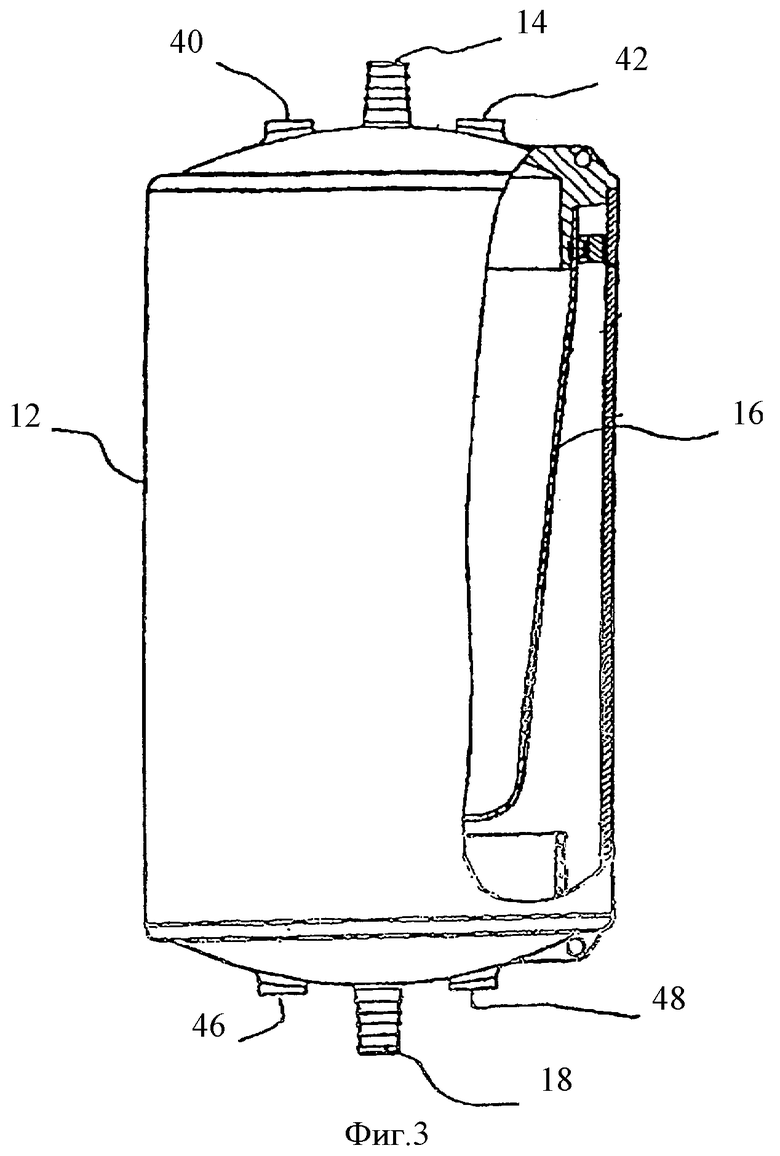
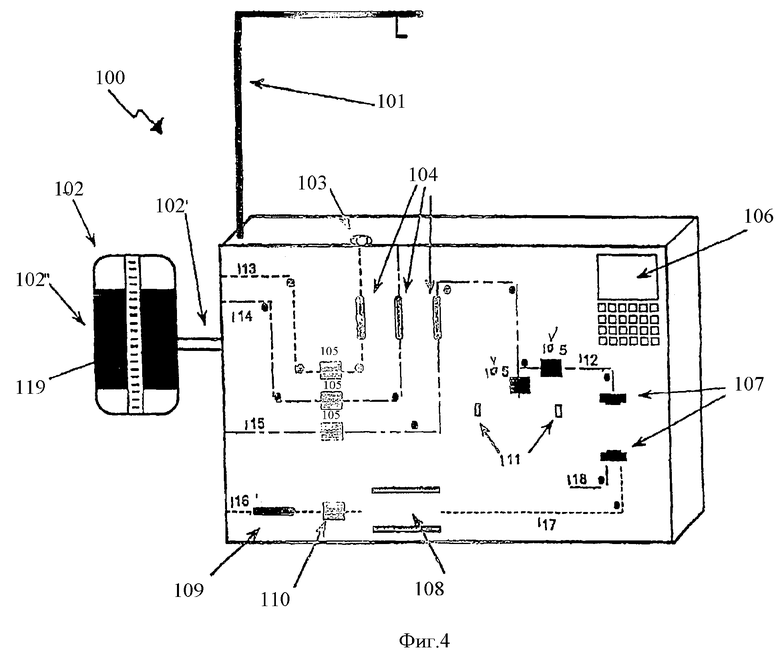
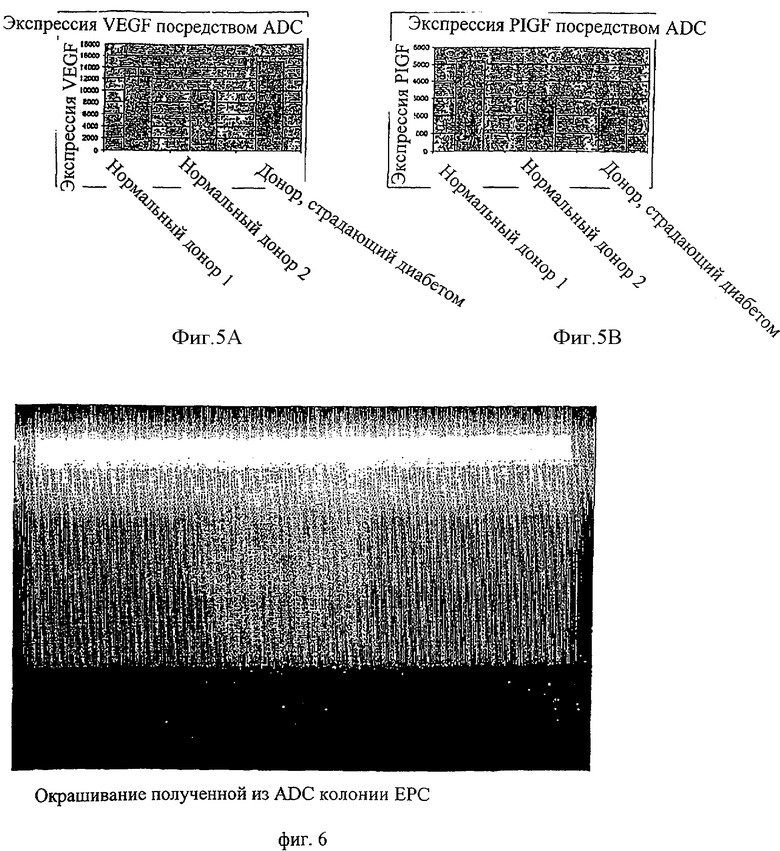

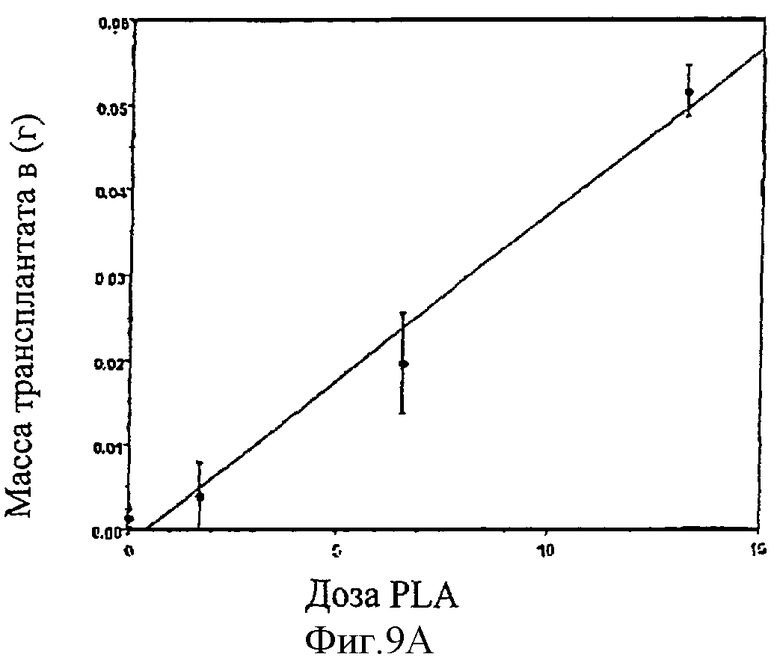

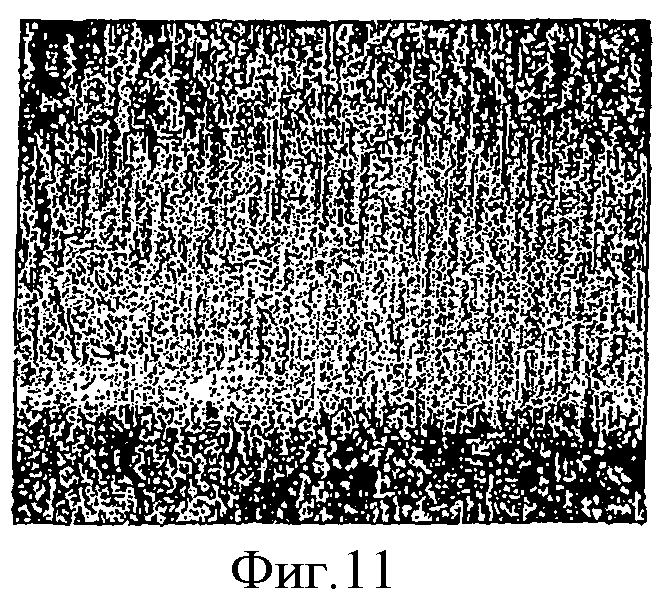
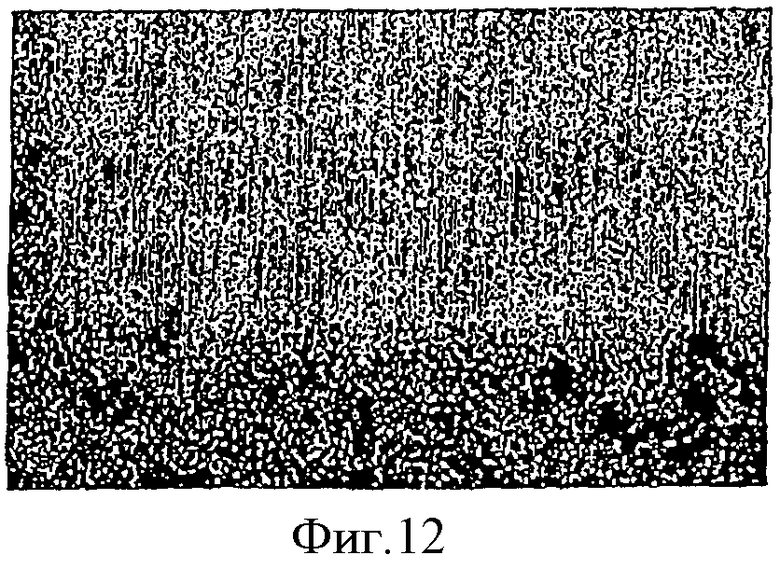
Изобретение относится к медицине, в частности к кардиологии, и касается лечения сердечно-сосудистых заболеваний. Для этого вводят композицию, состоящую из стволовых клеток и недифференцированных клеток-предшественников, полученных из жировой ткани в результате отделения зрелых адипоцитов и соединительной ткани. Это обеспечивает восстановление циркуляции крови в ишемизированной области. 27 з.п. ф-лы, 12 ил.
1. Применение композиции, состоящей из концентрированной клеточной популяции, представляющей собой стволовые клетки и недифференцированные клетки-предшественники, полученные в результате отделения зрелых адипоцитов и соединительной ткани от жировой ткани субъекта, для получения средства для восстановления циркуляции крови у субъекта, имеющего ишемическое состояние.
2. Применение по п.1, в котором указанная концентрированная клеточная популяция содержит не менее 500 эндотелиальных клеток-предшественников/миллион клеток, полученных из жира.
3. Применение по п.1, в котором указанное ишемическое состояние является ишемической болезнью сердца.
4. Применение по п.1, в котором указанное ишемическое состояние является инфарктом миокарда.
5. Применение по п.1, в котором указанный субъект страдает диабетом.
6. Применение по п.1, в котором указанный субъект страдает ожирением.
7. Применение по п.1, в котором указанная композиция содержит болюс указанных клеток, полученных из жира.
8. Применение по п.1, в котором указанная композиция обеспечивает от 55,000 до 550,000 стволовых клеток, выделенных из жировых.
9. Применение по п.1, в котором указанная композиция содержит один или более ангиогенных факторов.
10. Применение по п.1, в котором указанная клеточная популяция экспрессирует васкулярный эндотелиальный фактор роста (VEGF) во время культивирования.
11. Применение по п.1, в котором указанная клеточная популяция экспрессирует плацентарный фактор роста (ЗДПА) во время культивирования.
12. Применение по п.1, в котором указанная композиция содержит один или более артериогенных факторов.
13. Применение по п.1, в котором указанная композиция содержит один или более иммунодепрессивных лекарственных средств.
14. Применение по п.1, в котором указанные клетки, полученные из жира, не выращивают в клеточную культуру.
15. Применение по п.1, в котором указанные клетки, полученные из жира, выращивают в клеточную культуру.
16. Применение по п.1, в котором полученные из жира клетки выращивают в условиях культивирования, которые стимулируют дифференцировку к миоцитному фенотипу.
17. Применение по п.16, в котором указанный миоцитный фенотип является сердечным миоцитным фенотипом.
18. Применение по п.16, в котором миоцитный фенотип является скелетным миоцитным фенотипом.
19. Применение по п.16, в котором миоцитный фенотип является сосудистым миоцитным фенотипом гладкой мышцы.
20. Применение по п.15, в котором условия культивирования клеток стимулируют дифференцировку к эндотелиальному фенотипу.
21. Применение по п.15, в котором клеточная культура получена на клеточном каркасном материале для генерирования двухмерной или трехмерной структуры, которая может быть размещена на сердце или в сердце.
22. Применение по п.21, в котором клеточный каркасный материал способен рассасываться в организме.
23. Применение по п.1, в котором полученные из жира клетки модифицируют посредством генной трансплантации так, чтобы была изменена экспрессия одного или более генов в модифицированных полученных из жира клетках.
24. Применение по п.23, в котором указанная модификация приводит в результате к изменению уровня ангиогенеза в субъекте.
25. Применение по п.23, в котором модификация приводит в результате к изменению уровня артериогенеза в субъекте.
26. Применение по п.23, в котором модификация приводит в результате к изменению уровня апоптоза в субъекте.
27. Применение по п.26, в котором указанные модифицированные клетки-предшественники, выделенные из жировой ткани, могут дифференцироваться в сердечные миоциты с измененным апоптозом.
28. Применение по п.23, в котором модификация изменяет свойства хоминга указанных клеток, выделенных из жира.
| JACKSON КА et al | |||
| "Regeneration of ischemic cardiac muscle and vascular endothelium by adult stem cells" | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
| ПРОИЗВОДНЫЕ ФАКТОРА ИНГИБИРОВАНИЯ ЛИПОГЕНЕЗА И ИХ ПОЛУЧЕНИЕ | 1993 |
|
RU2138554C1 |
| US 2003069168, 10.04.2003 | |||
| WARNKE PH et al | |||
| Выращивание и пересадка индивидуального васкуляризованного костного трансплантата у мужчины | |||
| Опубликовано в журнале Lancet | |||
Авторы
Даты
2009-11-20—Публикация
2004-02-20—Подача