Изобретение относится к способу получения Cu/Zn/Al-катализаторов, к катализатору, который может быть получен этим способом, а также к его применению для синтеза метанола и риформинга метанола и для низкотемпературной конверсии моноксида углерода.
Cu/Zn/Al-катализаторы, которые катализируют превращение CO, CO2 и H2 в метанол, известны давно. Атомное соотношение между медью и цинком может у этих известных катализаторов меняться, причем обычно медь все же присутствует в избытке. Кроме того, часть цинкового компонента может быть заменена на кальций, магний и/или марганец. Оксид алюминия, применяющийся как термостабилизирующее вещество, также может быть частично заменен на оксид хрома.
Так, например, из документа DE 1 965 007 известен катализатор для низкотемпературного синтеза метанола. Для получения катализатора сначала из раствора подходящих солей цинка и меди добавлением карбонатов щелочных металлов высаживают соответствующий основный карбонат. Его отделяют от водной фазы, сушат и прокаливают, чтобы получить соответствующие оксиды. Затем оксиды цинка и меди смешивают с оксидом алюминия, причем получается суспензия оксидов, которая содержит не более 20% твердой фазы. Ее затем гомогенизируют, причем гомогенизация длится столько, чтобы диспергированные оксиды не осаждались в течение 2 часов. После гомогенизации смесь сушат, таблетируют и прокаливают. Чтобы преобразовать оксидную форму в катализатор, ее дополнительно восстанавливают в потоке водорода.
Из документа DE 2 302 658 A известен способ получения предшественника катализатора, который может применяться для синтеза метанола. Для получения предшественника катализатора сначала получают первый осадок, который содержит двухвалентный металл, например, цинк, а также трехвалентный металл, например, алюминий в форме какого-либо соединения, которое можно разложить термически до соответствующих оксидов. Подходящими соединениями являются, например, карбонаты или бикарбонаты. Далее получают второй осадок, который содержит соединения меди, которые можно разложить термически до оксидов. Оба осадка смешивают. За этим непосредственно следуют обычные этапы сушки и прокаливания, чтобы получить из металлических соединений оксиды и, по возможности, вызвать образование шпинельной структуры. Затем твердую фазу таблетируют. Чтобы перевести предшественник в активный катализатор, таблетки восстанавливают в потоке водорода.
В документе DE 2 056 612 A описан способ получения метанола, в котором реакция идет на катализаторе, содержащем цинк, медь и алюминий. Катализатор относится к ряду смешанных кристаллов формулы (CuxZny)Al2(OH)16 × CО3 × 4H2O, в которой x и y могут принимать численные значения от 0,5 до 5,5, а сумма x и y равна 6. Соединение со смешанными кристаллами осаждают из водного раствора, который содержит соли меди, цинка и алюминия, при добавлении щелочного карбоната, щелочного бикарбоната или их смеси. Атомное отношение суммы двухвалентных металлов меди и цинка к трехвалентному алюминию в ряду смешанных кристаллов постоянно и составляет 6:2. Для получения медь, цинк и алюминий в форме подходящих солей, предпочтительно нитратов, растворяют в воде, и притом в количественном соотношении, которое соответствует желаемому составу катализатора. Этот раствор нагревают до температуры от 50 до 100°C, предпочтительно от 70 до 100°C, и обрабатывают соответствующим нагретым водным раствором осадителя, например, карбонатом щелочного металла. Возникающий осадок отфильтровывают, моют и сушат. Высушенное соединение прокаливают при температурах в интервале от 200 до 500°C в течение 12-24 час. Прокаленный продукт формуют в таблетки и затем путем восстановления в потоке водорода переводят в активную форму катализатора.
В документе US 4,279,781 описан катализатор для синтеза метанола, который включает оксид меди и цинка, а также оксид металла для термической стабилизации, например, оксид алюминия. Отношение оксида меди к оксиду цинка в расчете на вес металла составляет от 2:1 до 3,5:1. Получение катализатора происходит через общее осаждение растворенных солей цинка, меди и алюминия, например, нитратов. Этим достигается тщательное перемешивание компонентов катализатора. Чтобы получить активную форму, предшественник катализатора восстанавливают в потоке водорода.
Из документа EP 0 125 689 A2 известен катализатор для синтеза метанола, который в качестве каталитически активных веществ содержит оксид меди и оксид цинка, а в качестве термостабилизирующего вещества - оксид алюминия. Катализатор отличается определенным распределением пор по радиусу, причем доля пор с диаметром от 20 до 75 Д (мезопоры) составляет по меньшей мере 20%, а доля пор с диаметром более 75 Д (макропоры) составляет самое большее 80%. Желательное распределение пор по радиусу может быть достигнуто тем, что при получении катализатора используется коллоидально диспергированный оксид или гидроксид алюминия. Для получения этих катализаторов каталитически активные компоненты оксид меди и оксид цинка осаждают из водных растворов соответствующих солей, например, нитратов, сульфатов, хлоридов, ацетатов, с помощью щелочных веществ в присутствии коллоидально диспергированного оксида или гидроксида алюминия. Продукт осаждения можно затем высушить, прокалить, прессовать в формованное изделие и при необходимости восстановить.
Из документа EP 0 152 809 A2 известен катализатор для синтеза метанола и спиртовой смеси, содержащей высшие спирты, который в виде оксидного предшественника содержит оксид меди и оксид цинка, которые путем восстановления по меньшей мере части оксида меди могут быть преобразованы в каталитически действующие компоненты, а также оксид алюминия как термостабилизирующeе вещество и по меньшей мере один щелочной карбонат или щелочной оксид. Доля пор с диаметром от 14 до 7,5 нм в оксидном предшественнике составляет от 20 до 70% от полного объема. Содержание щелочи составляет от 13 до 130×10-6 грамм-атомов щелочного металла на грамм оксидного предшественника. Компонент оксид алюминия получали из коллоидально диспергированного гидроксида алюминия. Для получения катализатора обычно применяют растворы нитратов меди и цинка и осаждение проводят предпочтительно водным раствором K2CО3. Концентрация раствора составляет предпочтительно от 5 до 20 вес.%. Вместо нитратов можно также исходить из соответствующих формиатов или ацетатов металлов. Осаждение можно осуществлять также с помощью раствора гидрокарбоната калия. Осаждение может проводиться периодически или непрерывно. Предпочтительно осаждение проводится путем непрерывного соединения раствора нитратов меди и цинка, содержащего коллоидально диспергированный гидроксид алюминия, с водным раствором K2CО3. Сразу после осаждения промытый осадок катализатора прокаливают и подщелачивают путем обработки раствором соединения щелочного металла. Подщелоченный предшественник катализатора после сушки прессуют способом, который сам по себе известен, с образованием формованного тела, причем может добавляться смазка, как графит. Чтобы перевести предшественник катализатора в активную форму, его восстанавливают водородом.
Из документа WO 03/053569 A1 известен катализатор для синтеза метанола, который содержит оксид меди и оксид цинка как каталитически действующие вещества, а также оксид алюминия как термостабилизирующее вещество. Для получения катализатора из раствора, который содержит соли Cu и Zn, а также часть соли Al, с помощью раствора щелочного карбоната или щелочного алюмината осаждают соответствующие гидроксокарбонаты или гидроксиды. Либо раствор солей Cu и Zn, либо раствор щелочного карбоната или щелочного алюмината содержит золь гидроксида алюминия. Полученный осадок отделяют от раствора, в котором происходило осаждение, моют, сушат и при необходимости прокаливают. При получении катализатора исходят предпочтительно из нитратов меди и цинка, которые осаждаются предпочтительно карбонатом натрия или алюминатом натрия.
В документе JP 2001-144779 описан медно-цинковый катализатор для реакции моноксида углерода и воды с получением диоксида углерода и воды, который получают тем, что раствор, содержащий формиат меди и формиат цинка, смешивают с водным раствором щелочного материала. Образующийся при этом осадок затем фильтруют, моют, сушат и прокаливают. Прокаленное твердое вещество взмучивают добавлением воды и наносят на поверхность подложки со структурой сот. В качестве связующего может применяться золь оксида алюминия или золь оксида циркония. Они могут добавляться во взвесь прокаленного осадка. При этом оксид алюминия распределен в катализаторе неоднородно, а находится только между частицами катализатора. Таким образом, его задачей является действовать только как связующее между содержащими медь и цинк частицами катализатора, а также подложки с сотовой структурой, и он не является активным компонентом катализатора.
Для получения Cu/Zn/Al-катализаторов для синтеза метанола в технически реализуемом способе применяются в основном нитраты цинка и меди благодаря своей хорошей растворимости в воде. При этом при осаждении скапливается отработанная вода, которая содержит большие количества нитрата натрия. При сбросе в поверхностные воды это привело бы к чрезмерной концентрации удобрений. Поэтому перед сбросом в поверхностные воды содержание водорастворимого азота в накапливающихся при получении катализаторов синтеза метанола отработанных водах должно быть существенно уменьшено.
Поэтому задачей изобретения является разработать способ получения Cu/Zn/Al-катализаторов, который, с одной стороны, позволяет заметно уменьшить содержание в отработанной воде соли, в частности, нитратов щелочного металла, и который, с другой стороны, предоставляет катализаторы для синтеза метанола, активность которых по меньшей мере сравнима с активностью катализатора, получаемого из нитратов металла.
Эта задача решена способом с отличительными признаками пункта 1 формулы изобретения. Выгодные формы реализации способа являются объектом зависимых пунктов.
В способе получения Cu/Zn/Al-катализаторов согласно изобретению сначала получают первый водный раствор, содержащий по меньшей мере формиат меди и формиат цинка. Далее получают второй раствор, который содержит осадитель. При этом под осадителем понимается реагент, который, прямо или косвенно, производит ионы, например, гидроксильные ионы и/или карбонатные ионы, с помощью которых можно осадить металлы, в частности, медь, цинк и алюминий. Первый раствор и/или второй раствор содержит золь/гель смесь гидроксида алюминия. При этом под золем гидроксида алюминия понимается тонкодисперсное распределение гидроксида алюминия в воде, в которой уже были образованы поликислоты путем конденсации гидроксида алюминия, однако при этом в водной фазе невооруженным глазом не видно никаких частиц, так что раствор является прозрачным. Под гелем гидроксида алюминия понимается дисперсия гидроксида алюминия в воде, причем уже образованы большие агломераты из поликислот, так что даже невооруженным глазом можно различить частицы, например, как помутнение водной фазы.
На стадии осаждения первый раствор и второй раствор соединяют, причем получается осадок. Осадок отделяют от водной фазы, причем водная фаза образует отработанную воду, которую проводят на переработку.
Осадок моют, пока содержание в нем щелочи не составит менее 500 частей/млн в расчете на прокаленный при 600°C катализатор. Затем осадок сушат, при необходимости прокаливают и мелют.
В способе согласно изобретению отработанной воды, содержащей нитраты, не образуется. Благодаря использованию формиата меди и формиата цинка в качестве водорастворимых солей меди и цинка отработанная вода содержит формиатные ионы, которые могут быть переработаны более простым путем. Благодаря применению формиатов нагрузка отработанной воды органическим материалом сохраняется относительно низкой. Это является преимуществом по сравнению с применением высших карбоновых кислот, таких как уксусная кислота, так как они из-за более высокого числа связей C-H повышают нагрузку отработанной воды органикой. Другим преимуществом является экономически выгодное получение муравьиной кислоты, которая необходима для получения формиатов меди и цинка, так что способ согласно изобретению выгоден также с экономической точки зрения.
Для способа согласно изобретению существенно, чтобы по меньшей мере часть алюминия вводилась в раствор, где проводится осаждение, в форме золя гидроксида алюминия, а другая часть - как гель гидроксида алюминия. При отказе от добавления золь/гель смеси гидроксида алюминия в раствор солей металлов падает выход продукта по весу в единицу времени (GZA, [кг метанола/{кг катализатора × час}]).
Осадок после отделения тщательно промывают, так чтобы содержание в нем щелочи, рассчитанное на прокаленный при 600°C оксидный катализатор, упало до значений меньше 500 частей/млн, предпочтительно меньше 400 частей/млн, в частности, до значений в интервале от 100 до 300 частей/млн. Скапливающуюся при этом промывочную воду можно объединить с содержащей формиат отработанной водой и при необходимости переработать. После промывки, сушки и при необходимости прокаливания оксидная форма катализатора еще обнаруживает остаточное содержание формиата менее 5 вес.%, предпочтительно от 0,5 до 4 вес.%, в частности, предпочтительно 1-2 вес.%. Содержание формиата можно определить, например, окислительным титрованием или количественным хроматографическим анализом, например, ВЭЖХ.
Помимо формиата меди и формиата цинка, первый водный раствор может также содержать также обычные промоторы, как, например, кальций, магний, марганец, церий, лантан, а также рутений или палладий. Кроме названных промоторов, могут также использоваться и другие промоторы. Промоторы вводятся предпочтительно также в форме своих формиатов предпочтительно в первый водный раствор. Их доля в оксидной форме катализатора, рассчитанная на оксид, составляет предпочтительно менее 10 вес.%, в частности менее 5 вес.%. Если в качестве промоторов используются благородные металлы, как рутений или палладий, то они предпочтительно содержатся в количестве менее 1 вес.%.
Как уже упоминалось, в способе согласно изобретению первый и/или второй раствор содержит золь/гель смесь гидроксида алюминия. В качестве исходного продукта для золь/гель смеси гидроксида алюминия может, например, использоваться продукт, имеющийся в продаже. Однако золь/гель смесь гидроксида алюминия можно также получить тем, что к разбавленному раствору соли алюминия добавляют немного гидроксида аммония, причем нагревания избегают, чтобы воспрепятствовать превращению в крупнодисперсные гидроксопроизводные. Согласно другому варианту, можно к раствору щелочного алюмината добавить незначительное количество кислоты, причем образуется золь/гель гидроксида алюминия. Предпочтительно золь/гель гидроксида алюминия содержится в первом водном растворе. Продукты, образующиеся из золь/гель гидроксида алюминия на следующих стадиях, служат как подложкой, так и термостабилизирующим веществом. Не привязываясь к этой теории, авторы изобретения предполагают, что при нагревании из золь/гель смеси гидроксида алюминия образуется трехмерная сетка, в свободных объемах которой располагаются кристаллы меди, относящиеся к активным компонентам, получающиеся после восстановления. Из-за этого усложняется дальнейшее срастание кристаллов меди при синтезе метанола, что повышает стабильность катализатора и его срок службы в технологических процессах.
Считается, что оксид цинка, во-первых, оказывает сильное влияние на образование активных компонентов, а во-вторых, благодаря своей частично игольчатой структуре способствует стабильности катализатора. Кроме того, оксид цинка действует как ловушка для ядовитых веществ, реагируя соединениями серы, которые могут случайно попадаться.
Присутствующие в известных случаях в качестве промоторов оксиды кальция, магния, марганца, церия и лантана также действуют стабилизирующе.
Первый раствор, который содержит смесь различных солей металлов, получают предпочтительно тем, что
- получают водный раствор формиата меди, полностью растворяя соль меди путем добавления муравьиной кислоты,
- получают водную дисперсию или раствор соли цинка,
- получают водный раствор соли алюминия, и
- раствор формиата меди, дисперсию или раствор соли цинка и раствор соли алюминия соединяют.
Если Cu/Zn/Al-катализатор должен еще модифицироваться промоторами, их можно вводить, например, в первый раствор. Промоторы могут добавляться в форме подходящих солей, например, как карбонаты, оксиды или гидроксиды. Сами по себе эти соли могут добавляться в любой момент времени, то есть в раствор формиата меди, в дисперсию или раствор соли цинка, или также после соединения раствора формиата меди и дисперсии или раствора соли цинка. Особенно дорогие промоторы, как благородные металлы, добавляются к суспензии предпочтительно на более позднем этапе процесса, например, перед распылительной сушкой, или напыляются тонкоизмельченными на сухой порошок после распылительной сушки.
При получении раствора формиата меди и цинка предпочтительно добавляется столько муравьиной кислоты, чтобы в расчете на использующееся количество соли меди и цинка, с учетом стехиометрии, муравьиная кислота находилась в избытке по меньшей мере на 10 моль%, предпочтительно от 10 до 20 моль%, в частности, предпочтительно от 14 до 16 моль%. Значение pH раствора формиата меди после добавления муравьиной кислоты предпочтительно составляет менее 3, предпочтительно менее 2,5.
В предпочтительном варианте реализации способа раствор или дисперсию соли цинка соединяют с раствором формиата меди. После соединения раствора или дисперсии формиата меди и соли цинка как медь, так и цинк находятся в растворе в форме их формиата. Полученный раствор имеет предпочтительно значение pH в диапазоне от 3,0 до 4,0, в частности, предпочтительно от 3,5 до 3,7. Затем к раствору меди с цинком добавляют раствор соли алюминия.
Раствор соли алюминия предпочтительно вводят в медно-цинковый раствор несколькими частями. При этом по меньшей мере первую часть раствора соли алюминия получают так, чтобы по меньшей мере первая доля соли алюминия растворялась в воде при добавлении муравьиной кислоты.
При получении первой части раствора соли алюминия предпочтительно действуют так, что, например, сначала растворяют в воде алюминат натрия, а затем добавляют столько муравьиной кислоты, чтобы значение pH составляло менее 5, предпочтительно от 4,5 до 2, в частности, от 4 до 3. Предпочтительно добавляют столько муравьиной кислоты, чтобы получить прозрачный раствор.
Далее, вторую часть раствора соли алюминия получают предпочтительно тем, что растворяют в воде вторую часть соли алюминия. При этом во вторую часть раствора соли алюминия муравьиную кислоту не добавляют. Для приготовления первого раствора, который содержит смесь всех солей металлов перед осаждением, в этом случае в водный медно-цинковый раствор предпочтительно вводят первую часть раствора соли алюминия и вторую часть раствора соли алюминия, предпочтительно разнесенными по времени.
Вторую часть раствора соли алюминия получают, например, тем, что NaAlO2 растворяют в воде. Значение pH водного раствора NaAlO2 составляет, в зависимости от избытка щелочи в исходном материале, от 11 до 14, предпочтительно от 12 до 13.
Доли первой и второй части раствора соли алюминия могут находиться, в расчете на содержание алюминия, в диапазоне от 0:100 до 100:0, предпочтительно от 1:99 до 99:1, особенно предпочтительно от 30:70 до 70:30 и, в частности, предпочтительно выбираются около примерно 50:50.
Получение растворов соли алюминия проводится предпочтительно при температурах ниже 40°C, в частности, предпочтительно ниже 30°C. Эту температуру также нельзя превышать, когда раствор соли алюминия вводится в медно-цинковый раствор, или в раствор формиата меди или в дисперсию, или в раствор соли цинка. Этим подавляется образование крупнодисперсных полимерных соединений алюминия. Под крупнодисперсными полимерными соединениями алюминия понимаются комплексные гидроксосоединения алюминия, которые образуют различимые глазом частицы, опускающиеся относительно быстро. Поэтому получение растворов проводится предпочтительно в котле, который оснащен соответствующим устройством охлаждения.
Солями алюминия, подходящими для применения в способе согласно изобретению, являются, например, ди- и триформиат алюминия, гидрат Al(NO3)3 или NaAlO2. Растворы соли алюминия имеют предпочтительно концентрацию алюминия в интервале от примерно 0,4 до примерно 1,1 моль/л, в частности, предпочтительно от примерно 0,9 до 1,1 моль/л. При этом верхние значения указанных интервалов определяются границами растворимости соли алюминия, тогда как нижние границы получаются из экономических соображений.
В качестве солей меди предпочтительно применяются такие соли, анионы которых являются оксидами, гидроксидами и карбонатом или их получаемыми восстановлением производными и которые в первом растворе или в оксидной форме катализатора больше не должны обнаруживаться индивидуально среди различимых элементов. Предпочтительно соль меди выбирается из CuO, Cu(OH)2 и Cu(OH)2 ×
CuCО3.
В качестве соли цинка предпочтительно выбирают также соединение цинка, анион которого в первом растворе или в оксидном предшественнике катализатора больше не обнаруживается как мешающий, предпочтительно как различимый элемент. Предпочтительно в качестве соли цинка выбирается ZnO.
Концентрация раствора формиата меди предпочтительно выбирается так, чтобы после соединения раствора формиата меди и раствора или дисперсии соли цинка концентрация меди устанавливалась в интервале от примерно 0,1 до примерно 0,5, в частности, предпочтительно от 0,3 до примерно 0,5 моль/л. Верхнее значение при этом определяется границей растворимости соли меди, а нижняя граница получается из экономических соображений, так как обработка разбавленных растворов приводит к повышенным объемам, что, например, влияет на определение размеров устройства, в котором реализуется способ согласно изобретению.
Концентрация соли цинка предпочтительно выбирается так, чтобы после соединения раствора формиата меди и раствора или суспензии соли цинка концентрация цинка предпочтительно лежала в интервале от примерно 0,1 до примерно 0,2 моль/л, предпочтительно от 0,15 до примерно 0,2 моль/л. Здесь также верхняя граница получается из растворимости соли цинка, а нижняя граница - из экономических соображений.
Раствор соли алюминия предпочтительно вводят в медно-цинковый раствор. Значение pH первого раствора, который предпочтительно содержит полное количество Cu, Zn и Al, при этом предпочтительно устанавливается на значение в интервале от 4,0 до 5,0, особенно предпочтительно от 4,2 до 4,4.
В качестве осадителя предпочтительно применяются основания щелочных металлов. В качестве оснований щелочного металла используются предпочтительно карбонаты щелочных металлов, гидрокарбонаты щелочных металлов или алюминаты щелочных металлов. В качестве щелочного металла предпочтительно применятся натрий. Если, например, как осадитель используется раствор соды, то концентрация содового раствора составляет предпочтительно от 80 г/л до 200 г/л, предпочтительно от 170 до 180 г/л.
Согласно другой форме реализации способа согласно изобретению в качестве осадителя используется пероксид водорода. Пероксид водорода вводится в первый раствор или дисперсию, который содержит медь, цинк и алюминий в форме их формиатов или гидроксоформиатов. Благодаря пероксиду водорода формиат окисляется в карбонат, так что в осадок выпадают металлы в форме их гидроксокарбонатов, карбонатов или гидроксидов. При окислении формиат-анионов сначала образуются анионы гидрокарбоната, а затем, при возрастающем значении pH, анионы карбоната. Использующиеся анионы металлов осаждаются последовательно в ряду Al-Cu-Zn как гидроксокарбонаты. Таким образом, можно отказаться от использования карбонатсодержащего щелочного раствора. Помимо пероксида водорода, могут применяться также другие подходящие окислители, например, озон.
Для получения оксидных предшественников катализаторов сначала соединяют первый и второй раствор, причем получают осадок. Осаждение предпочтительно проводят так, чтобы во время осаждения значение pH удерживалось в диапазоне от 3,5 до 7,5, предпочтительно от 6,0 до 7,0 в частности, предпочтительно 6,5 ± 0,1.
Температуру при осаждении удерживают предпочтительно в диапазоне от 25 до 95°C, в частности, предпочтительно от 50 до 75°C.
После смешения образованный осадок предпочтительно подвергают созреванию. Для этого можно, например, перевести суспензию, образовавшуюся при смешении первого и второго раствора, в резервуар для созревания, в котором суспензию можно вращать, например, подходящей мешалкой.
Созревание проводится предпочтительно в течение периода от 10 минут до 10 часов, в частности, предпочтительно от 1 до 5 часов.
При созревании суспензию предпочтительно выдерживают при повышенной температуре, причем созревание происходит, в частности, при температуре более 60°C, в частности, предпочтительно в диапазоне от 65 до 80°C.
Соединение первого и второго растворов предпочтительно проводят так, что растворы вводят параллельно в смесительный резервуар и там перемешивают. В этом резервуаре проводится грубое перемешивание, например, с помощью подходящей мешалки.
Однако предпочтительно, чтобы осаждение осуществлялось как непрерывное осаждение. Для этого предусмотрен имеющий соответствующие размеры смесительный резервуар, в который непрерывно подают первый и второй раствор и получающуюся смесь непрерывно отводят. Предпочтительно объем смесительного резервуара выбирают так, чтобы можно было осуществить непрерывный подвод первого и второго растворов в смесительный резервуар и непрерывный отвод смеси, причем время пребывания смеси составляет предпочтительно от примерно 0,1 секунды до 10 минут, особенно предпочтительно от примерно 1 до 120 секунд, в частности, предпочтительно от 1 до 20 секунд.
Время пребывания смеси в смесительном резервуаре сильно зависит от размеров смесительного резервуара и скорости потока. Соответствующие подходящие размеры смесительного резервуара, а также скорости подвода и отвода растворов или суспензии могут быть выбраны специалистом.
После осаждения и проведенном при необходимости этапе созревания осадок отделяют от водной фазы, для чего могут применяться обычные способы, например, фильтрация. Осадок затем промывают и сушат. Предпочтительно после сушки осадок прокаливают. Прокаливание проводится, в зависимости от используемого способа, при температурах предпочтительно от 140°C до 1000°C, в частности, предпочтительно от 170°C до 350°C в течение по меньшей мере 0,1 секунды, предпочтительно по меньшей мере 4 минут, особенно предпочтительно от 20 минут до 8 часов, в частности, предпочтительно от 30 минут до 4 часов. В зависимости от выбранных условий прокаливания оставшийся в осадке на фильтре формиат при кальцинировании удаляют по существу весь окислением на воздухе или путем внутримолекулярной окислительно-восстановительной реакции в инертном газе. В последнем случае Cu(HCO2)2 × H2O по всей вероятности сначала разлагается до H2 и CuC2O2. Затем оксалат меди реагирует до образования CO2 и элементарной меди. Прокаливание может проводиться в обычных устройствах. В промышленном производстве из-за лучшего теплопереноса применяются как пульсационные реакторы, так и реакторы с псевдоожиженным слоем катализатора как предпочтительные с точки зрения стоимости вращающиеся печи. Пульсационная сушилка делает возможными очень короткие времена сушки, в области менее 1 секунды, обычно в диапазоне от 0,1 секунды до 4 минут, причем могут применяться очень высокие температуры до 1000°C.
Прокаленный порошок можно при необходимости размолоть и затем с помощью обычных инструментов переработать, например, в таблетки или экструдаты. Однако можно также взмучить порошок, размолоть до очень маленьких размеров зерна и нанести полученную суспензию на подходящую подложку, например, соты. Для этого можно использовать обычные способы. При этом подходящий размер зерна устанавливают так, чтобы средний размер зерна D50 составлял от 10 нм до 10 мкм, в частности, предпочтительно от 100 нм до 5 мкм. Средний размер зерна можно определить, например, лазерной дифракцией. Подходящие катализаторы могут быть получены, например, с размером зерна, при котором значение D50 находится в интервале примерно 2-3 мкм.
Особое преимущество способа согласно изобретению состоит в том, что скапливающаяся после отделения осадка отработанная вода, содержащая формиаты, может быть обработана сравнительно простыми средствами. Для этого содержащую формиаты отработанную воду предпочтительно подвергают окислительной обработке, причем формиатные ионы окисляют в водном растворе, в зависимости от pH, в основном до карбоната, гидрокарбоната, диоксида углерода и воды. Содержание формиатов, например, в виде формиата натрия, в отработанной воде находится при технической реализации способа согласно изобретению в интервале от 0,2 до 1,5 моль/л, в частности, предпочтительно от 0,8 до 1,0 моль/л, но могут также присутствовать более высокие или более низкие концентрации формиата. Путем окислительной обработки отработанной воды можно снизить концентрацию формиата до значений менее 0,1 моль/л, предпочтительно от 0,01 до 0,075 моль/л, в частности, предпочтительно от 0,02 до 0,04 моль/л. Это соответствует снижению количества формиата, содержащегося в отработанной воде, более чем на 95%.
Согласно предпочтительной форме реализации для окислительной обработки к содержащей формиаты отработанной воде добавляют пероксид водорода. Пероксид водорода в содержащую формиаты отработанную воду добавляют предпочтительно в форме раствора, концентрация пероксида водорода в котором лежит в диапазоне примерно от 9 до 20 моль/л (примерно до 60 вес.%). Для случая, когда должны соблюдаться особые правила перевозки, концентрацию используемого раствора пероксида водорода можно повысить до более чем 90 вес.%. Предпочтительно пероксид водорода добавляют в избытке, причем добавленное количество в расчете на содержащийся в отработанной воде формиат выбирается в интервале от 160 до 200 моль%, в частности, предпочтительно от 160 до 170 моль%. Помимо пероксида водорода, могут также использоваться другие окислители, например, озон или раствор гипохлорита натрия. При выборе окислителя играет роль, например, себестоимость и законодательство об окружающей среде. В зависимости от законодательных ограничений и дополнительных доступных ступеней очистки при известных условиях не требуется окислять все количество формиатных ионов. Существенное снижение концентрации формиатных ионов химической окислительной обработкой может оказаться уже достаточным, и обработанная таким способом отработанная вода при необходимости может направляться, например, на ступень биологического осветления.
Обработку пероксидом водорода содержащей формиаты отработанной воды проводят предпочтительно при 20-95°C, в частности, предпочтительно при 50-80°C в диапазоне pH 4-8, в частности, предпочтительно от 5,0 до 6,5.
Согласно одной форме реализации способа по изобретению окислительная обработка содержащей формиаты отработанной воды проводится уже перед отделением осадка. Для этого можно, например, после этапа созревания добавить в суспензию подходящее количество пероксида водорода и отделять осадок только после существенного окислительного расщепления формиатных ионов. В альтернативной последовательности технологических стадий можно проводить добавление раствора пероксида водорода уже к раствору формиата, содержащему Cu, Zn, Al, причем осадитель (карбонатные ионы) получаются путем окисления из формиатных ионов.
Окислительную обработку отработанной воды путем добавления подходящего окислителя, как пероксид водорода, очень просто провести технически, и она позволяет также обработать отработанную воду, которая содержит относительно высокую концентрацию формиатных ионов. Однако возможно также, чтобы окислительная обработка проводилась исключительно биологической обработкой содержащей формиаты отработанной воды. При этом отработанная вода, содержащая формиаты, может при необходимости разбавляться до подходящей концентрации.
Окислительная обработке содержащей формиаты отработанной воды проводится предпочтительно так, чтобы концентрация формиата в отработанной воде после окислительной обработки была меньше 0,1 вес.%.
Если сравнивать Cu/Zn/Al-катализатор, полученный с применением формиата, с катализаторами, которые были получены, исходя из нитратов, то у катализатора, полученного способом согласно изобретению, оказывается лучшая или сравнимая активность и сравнимая селективность. Также долговременная стабильность катализатора, полученного с применением формиата, определенная при 250°C в тесте на синтез метанола, является несколько лучшей или по меньшей мере сравнимой со стабильностью катализатора, который был получен исходя из нитратов металлов. Поэтому объектом изобретения является также катализатор, который может быть получен вышеописанным способом.
Катализатор согласно изобретению в своей оксидной форме содержит менее 5 вес.%, предпочтительно от 0,5 до 4 вес.%, в частности, предпочтительно от 1 до 2 вес.% формиата, рассчитываемого как муравьиная кислота. Благодаря прокаливанию в мягких условиях можно сохранить структуру формиата, которая, согласно часто встречающемуся в катализе правилу "ключа и замка" может играть важную роль в достижении высокой активности. При прокаливании в щадящих условиях при примерно 170°C в течение 4 минут образуется катализатор, который имеет очень высокую активность при 250°C.
Катализатор согласно изобретению отличается высоким объемом мезопор. При этом доля мезопор с радиусом от 3,75 до 7,0 нм составляет предпочтительно более 30%, предпочтительно от 30 до 80% от всего объема пор. Полный объем пор включает объемы пор с радиусом от 3,75 до 7500 нм. Объем пор может быть определен по методу вдавливания ртути. Предпочтительно, полный объем пор, определенный для таблеток размером 6×4 мм, составляет 100 мм3/г -700 мм3/г, предпочтительно 250 мм3/г - 450 мм3/г.
Содержание меди, рассчитанное как CuO и отнесенное к весу оксидной формы катализатора, с учетом потери при прокаливании при 600°C, выбирается предпочтительно между 55 и 69 вес.%, в частности, предпочтительно 60 и 63 вес.%.
Содержание цинка, рассчитанное как ZnO и отнесенное к весу оксидной формы катализатора, с учетом потери при прокаливании при 600°C выбирается предпочтительно между 20 и 33 вес.%, в частности, предпочтительно между 25 и 31 вес.%.
Содержание алюминия, рассчитанное как Al2O3 и отнесенное к весу оксидной формы катализатора, предпочтительно выбирается между 5 и 20 вес.%, в частности, предпочтительно между 8 и 11 вес.%.
Процентные данные для содержания меди, цинка и алюминия рассчитаны на катализатор, прокаливавшийся три часа при 600°C.
Кроме того, катализатор согласно изобретению имеет в оксидной форме содержание щелочных ионов, в частности, ионов натрия, предпочтительно меньше 500 частей/млн, в частности, предпочтительно меньше 300 частей/млн, в частности, от 100 частей/млн до 300 частей/млн.
В своей оксидной форме катализатор согласно изобретению имеет удельную поверхность предпочтительно более 90 м2/г, в частности, предпочтительно более 100
м2/г.
Катализатор согласно изобретению может быть выполнен как формованное тело произвольного вида. Например, он может быть выполнен в виде колец, формованных тел с 3-20 отверстиями, таблеток с гладкой или волнистой наружной поверхностью или как соты. Размер формованного тела соответствует обычным значениям. Для получения формовок порошковый катализатор прессуют, при необходимости с добавлением смазки, как графит, например, в таблетки, например, размером 6×4 мм.
Перед применением катализатор переводят из оксидной формы в активную форму. Для этого оксид меди по меньшей мере частично восстанавливают до элементарной меди. Кроме того, оксидную форму катализатора согласно изобретению предпочтительно восстанавливают в потоке водорода. Активирование можно проводить непосредственно в реакторе синтеза и предпочтительно оно осуществляется тем, что сначала проводят восстановление с помощью инертного газа, такого, как азот, содержащего небольшое количество водорода. Азот сначала содержит обычно примерно 2,0 об.% H2. При этом температуру повышают, например, с 100 до 235°C в течение 16 часов. Затем содержание водорода повышают, причем, например, восстановление ведут с 2,0 об.% H2 (остальное N2) в течение 3 часов в интервале температур от 235 до 270°C. Завершение восстановительной обработки может проводиться с 99,9%-ным H2 в течение примерно 3 часов при температуре от 270°C до 300°C. Обычно катализатор активируют при объемной скорости примерно от 3000 до 4000 литров восстанавливающего газа в час на литр катализатора.
В восстановленном состоянии размер кристаллов меди равен предпочтительно примерно 4-12 нм, предпочтительно 5-7 нм.
Катализатор согласно изобретению подходит, в частности, для применения в синтезе метанола. Поэтому объектом изобретения является применение вышеописанного катализатора для синтеза метанола из CO, CO2 и H2. Синтез обычно проводится при температуре примерно от 200 до 320°C, предпочтительно от 210°C до 280°C, при давлении примерно от 40 до 150 бар, предпочтительно примерно от 60 до 100 бар, и при объемной скорости от примерно 2000 до 22000, предпочтительно от 8000 до 12000 литров синтез-газа в час на литр катализатора, причем синтез-газ может содержать примерно от 5 до 25, предпочтительно от 6 до 12 об.% CO, примерно от 4 до 10 об.% CO2, примерно от 10 до 30 об.% N2 плюс CH4 (инертные газы) и как остальное - H2.
Далее, катализатор согласно изобретению подходит для применения в риформинге метанола, а также в низкотемпературной конверсии моноксида углерода в диоксид углерода. Последняя реакция, называемая также низкотемпературным сдвигом (LTS), проходит при температурах в диапазоне примерно от 175 до 250°C, предпочтительно от 205 до 215°C и отношениях пар/газ в диапазоне примерно от 0,4 до 1,5 (норм. л/норм. л). Типичные сырьевые газовые смеси содержат примерно 3 об.% CO, 17 об.% CO2, 2 об.% N2 и 78 об.% H2, которые проводятся через реактор с объемной скоростью примерно от 2000 до 12000 л сухого газа (т.е. без воды) на литр катализатора в час. С хорошими катализаторами при объемной скорости 11200 ч-1 и отношении пара к газу приблизительно 1,5 достигаются степени превращения CO от 70 до 85%.
Далее изобретение подробнее поясняется на примерах.
Пример
(a) Получение раствора меди
5054 г суспензии Cu(OH)2 × CuCО3 (содержание Cu: 27,7 вес.%, что соответствует 1400 г Cu) диспергируют в 10-литровом химическом стакане и порциями смешивают с 85%-ной муравьиной кислотой (D=1,1856 г/см3), всего 2,399 мл, пока не прекратится выделение CO2. Раствор меди имеет pH 2,35 и температуру 55°C.
(b) Получение раствора Cu/Zn (предшественник первого раствора)
В 5-литровом химическом стакане из 781 г ZnO и 4000 мл H2O получают дисперсию ZnO. Суспензию соединяют с раствором меди, полученным согласно (a). При продолжающемся диспергировании порциями добавляют следующие 890 мл муравьиной кислоты и 33,6 л деминерализованной воды. Голубой, сначала слегка мутноватый раствор перемешивают до тех пор, пока он не станет совсем прозрачным.
(c) Получение раствора карбоната натрия (второй раствор)
Получают 24000 мл раствора Na2CО3, который имеет концентрацию примерно
180 г CО3/100 мл, и раствор нагревают до 70°C.
(d) Получение раствора I алюминия
В 5-литровую мешалку, оборудованную устройством охлаждения, в которой находится 2193 мл мягкой воды, добавляют 246,7 г NaAlO2. Раствор нагревают до температура максимум 30°C и затем порциями добавляют 350 мл муравьиной кислоты. Молочного цвета раствор имеет pH примерно 4,0.
(e) Получение раствора II алюминия
В мешалку, оборудованную устройством охлаждения, в которой находится 2,193 мл воды, порциями добавляют 246,7 г NaAlO2. При этом следят за тем, чтобы температура раствора не превышала 30°C. Смесь перемешивают до тех пор, пока не получится прозрачный раствор.
(f) Осаждение
Раствор, полученный согласно (b), переводят в первый накопительный бак смесительного устройства. Затем раствор I алюминия, полученный согласно (d), вводят в бак и там перемешивают при комнатной температуре до тех пор, пока соединенные растворы не станут полностью прозрачными. При необходимости можно добавить воду, чтобы устранить опалесцентность раствора. Перед началом осаждения раствор нагревают до 70°C. Примерно за 30 минут до начала осаждения полученный согласно (е) раствор II алюминия переводят в бак, причем образуется молочная, бледно-голубая суспензия.
Второй накопительный бак наполняют полученным согласно (c) раствором Na2CО3 и нагревают до 70°C.
Растворы, содержащиеся в первом и втором баках, одновременно подают в смесительное устройство и после выдерживания в течение примерно 20 с проводят оттуда в перепускной бак. Скорости закачивания устанавливаются так, что pH при осаждении составляет 6,5±0,1. Из смесительного устройства смесь поступает в перепускной бак. Из перепускного бака полученная суспензия проводится в резервуар для созревания, где она выдерживается при перемешивании при примерно 65°C. Осаждение заканчивается примерно через 35 минут. Затем установку промывают примерно 600 мл умягченной воды и температуру в резервуаре для созревания повышают до 70°C. По окончании процесса промывки суспензию выдерживают при перемешивании. Начало процесса созревания определяется концом процесса промывки. Использовавшиеся в примерах длительности созревания указаны в таблице 2.
По окончании созревания суспензию фильтруют, промывают умягченной водой до тех пор, пока остаточное содержание натрия в осадке на фильтре не упадет до менее чем 350 частей/млн, и полученную твердую фазу сушат в противотоке путем распылительной сушки с использованием однокомпонентной форсунки. В качестве подачи устанавливают суспензию с содержанием сухих веществ 30 вес.%. Температура горячего газа на входе составляет 330-350°C, температура продукта на выходе 110-120°C. Высушенный порошок затем прокаливают 50 минут при примерно 320°C либо в фарфоровой чашке в полочной печи, либо в работающей периодически лабораторной вращающейся трубчатой печи.
(г) Обработка отработанной воды
Скопившуюся при фильтрации и промывке отработанную воду обрабатывают пероксидом водорода, причем с помощью серной кислоты pH удерживают на уровне от 5 до 6,5, а температуру отработанной воды удерживают на уровне 70°C. При этом концентрацию формиата в отработанной воде устанавливают на значениях от 2,8 вес.% до 0,09 вес.%. Селективность, определяемая как число молей прореагировавшего формиата, отнесенное к числу молей используемого пероксида водорода, составляет примерно 60%.
Сравнительный пример
(a) Получение раствора нитрата меди/цинка
К 9,79 кг раствора нитрата меди, который содержит 1400 г меди, добавляют 781,25 г оксида цинка. Затем добавляют 2077 г азотной кислоты (58%-ной) и смесь перемешивают до тех пор, пока твердая фаза полностью не растворится.
(b) Получение раствора нитрата алюминия
В 1,5 л полностью умягченной воды растворяют 246,7 г Na2AlO2. Затем добавляют 1365 г азотной кислоты (58%) и перемешивают до тех пор, пока раствор не станет прозрачным. Полученный раствор нитрата алюминия добавляют к раствору нитрата меди и цинка и раствор Cu/Zn/Al нагревают до 60°C.
(c) Получение золя алюминия
В 1,5 л полностью умягченной воды в течение 30 минут при перемешивании растворяют 246,7 г Na2AlO2. Полученный раствор добавляют к раствору Cu/Zn/Al и смесь нагревают до 60°C.
(d) Осаждение
В первый накопительный бак смесительного устройства наливают смесь, полученную согласно (c). Во второй накопительный бак смесительного устройства наливают 25 л водного раствора, который содержит 172 г Na2CO3 на литр. Оба раствора одновременно закачивают в смесительный резервуар и оттуда смесь направляют в резервуар для созревания.
По окончании осаждения смесительный резервуар промывают полностью умягченной водой, температуру в резервуаре для созревания повышают до 70°C и осадок выдерживают от 1 до 4 часов. По окончания созревания суспензию фильтруют, промывают деминерализованной водой до тех пор, пока остаточное содержание натрия в осадке на фильтре не составит менее 350 частей/млн, и полученную твердую фазу сушат распылительной сушкой с применением однокомпонентной насадки в противотоке. Входная температура горячего газа составляет 330-350°C, температура продукта на выходе 110-120°C. Затем высушенный порошок прокаливают 50 минут при примерно 320°C либо в фарфоровой чашке в полочной печи, либо в работающей в периодическом режиме лабораторной вращающейся трубчатой печи.
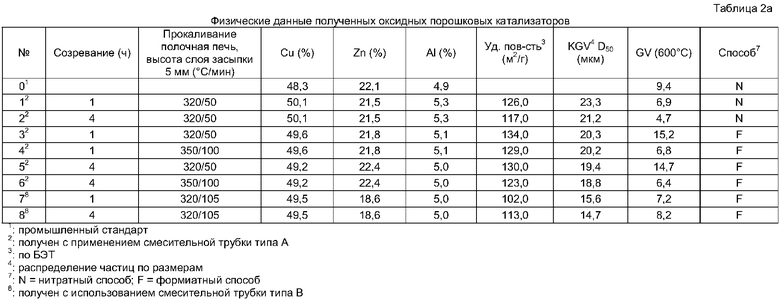
Осуществленные примеры осаждения, а также приводимые далее условия прокаливания сведены в таблицах 2a и 2b. В этих таблицах приведены также химические составы и физические параметры полученных предшественников оксидных катализаторов.
Определение физических параметров проводилось следующим образом:
Определение размеров кристаллов Cu:
Размеры кристаллов Cu определяют с помощью рентгеновской дифракции порошков (XRD). Рефлекс Cu (III) измеряют в диапазоне ~43,3° (2θ). Полуширина и интегральная интенсивность рефлекса рассчитывается по функции псевдоФойгта. Размер кристалла Cu рассчитывается с помощью функции Шеррера на основе рассчитанной полуширины.
Для подготовки к рентгенографическому определению размера кристалла оксидные катализаторы восстанавливают следующим образом:
2-5 г таблеток размером 6×4 мм нагревают в трубчатом реакторе с восстанавливающим газом (98% N2, 2% H2) от комнатной температуры до максимальной температуры при скорости нагрева 2°C/мин. Катализаторы, которые были получены из формиатов, нагревают до максимальной температуры 80-120°C. Катализаторы, которые были получены с использованием нитратов, греют сначала в течение ночи при 175°C. Затем в течение менее 2 часов устанавливают максимальную температуру: a) 180°C для катализаторов, полученных формиатным/карбонатным путем; b) 240°C для полученных нитратно/карбонатным путем. При удержании максимальной температуры содержание водорода в восстанавливающем газе повышают в конце до 100% в течение часа и затем образец восстанавливают еще 3 часа.
Определение удельной поверхности
Поверхность по БЭТ для порошкового оксидного катализатора, а также для таблеток размером 6 4 мм определяют по одноточечному методу адсорбции азота, согласно стандарту DIN 66132.
Определение потери при прокаливании
Если нужно определить потерю при прокаливании для таблеток, то их сначала размалывают в порошок. Исследуемый образец взвешивают во взвешенном фарфоровом тигле, который до этого нагревали 3 часа при 600°C в муфельной печи и затем охлаждали в эксикаторе до комнатной температуры. Тигель нагревали 3 часа в муфельной печи до 600°C и затем охлаждали в эксикаторе до комнатной температуры. Охлажденный тигель снова взвешивали и из разницы определяли потерю при прокаливании при 600°C.
Определение прочности на боковое сжатие
Прочность на боковое сжатие определяли согласно стандарту DIN EN 1094-5, издание 1995-09, огнестойкие изделия, предназначенные для изоляции - часть 5: Определение предела прочности на сжатие формованных изделий в холодном состоянии. Определение проводилось на стандартном приборе, как Schleuninger 6-D или ERWEKA TBH 310 MD согласно указаниям производителя прибора.
Для репрезентативного количества пробы в 100 таблеток в испытании на сопротивление продавливанию определялось давление прессования, прикладываемое к их цилиндрической оболочке, и с помощью имеющейся в приборе статистической программы рассчитывалось среднее значение, стандартное отклонение, а также минимальная и максимальная твердость. Распределение таблеток по твердости (N) представлялось графически.
Определение объема пор
Объем пор для порошковых оксидных катализаторов, а также таблеток размером 6×4 мм определяют по методу вдавливания ртути, следуя стандарту DIN 66133.
Определение содержания формиата
Примерно 10-20 г прокаленного порошка катализатора вводят в 300-миллилитровой колбе Эрлен-Мейера в (25+x) мл H2SO4 (25%) и растворяют при нагревании до примерно 70°C. Количество x мл H2SO4 (25%) определяется из минимально необходимого дополнительного количества серной кислоты, требуемого чтобы достичь полного растворения навески. Колбу наполняют дистиллированной водой до примерно 100 мл. Добавлением примерно от 2,5 до 25 мл NaOH (30%) устанавливают значение pH раствора 8-10. Затем раствор нагревают по меньшей мере еще 5 минут при 70°C. После этого добавляют 20 мл раствора KMnО4 (0,2 н) и раствор нагревают до легкого кипения по меньшей мере 30 мин. Горячий раствор подкисляют H2SO4 (25-50 мл) и добавляют 20 мл щавелевой кислоты (0,2 н), чтобы восстановить диоксид марганца и избыточный KMnO4 до Mn2+. Добавляемый раствор щавелевой кислоты должен точно соответствовать по количеству восстановительных эквивалентов окислительному эквиваленту раствора перманганата. Наконец, прозрачный раствор титруют 0,2 н KMnO4, пока не появится легкая розовая окраска.
Расчет:
Каждый мл израсходованного 0,2 н. раствора KMnO4 соответствует 4,5 мг формиата. Процентное содержание в образце формиата получается из:
[% формиата] = [(мл израсходованного 0,2 н. раствора KMnO4) × (4,5 мг формиата/мл 0,2 н. раствора KMnO4) × 100)/(навеска количества образца в мг]
Способ дает надежные результаты для концентраций формиата в титруемом растворе от 0,08 до 0,5 вес.% с погрешностями < +8%. Эти погрешности при применение 0,02 н. раствора перманганата можно снизить до +/-2%. Из-за зависимости точности метода от концентрации формиата, которая неизвестна, может потребоваться сначала взять навеску, соответствующую ожидаемому значению, чтобы после получения первого результата повторить титрование со скорректированной навеской, что даст в итоге концентрацию формиата в титруемом растворе в указанном выше диапазоне.
Содержание формиата в образцах из примеров 3 и 5 указано в таблице 1.
Физические свойства полученных катализаторов приведены в таблице 2. При этом таблица 2a относится к порошковым катализаторам, тогда как значения из таблицы 2b относятся к катализаторам, которые были формованы прессованием в таблетки с размерами 6×4 мм.
(м2/г)
(Н)5
(Е)
R=3,75-7500 нм
(мм3/г)
R=3,75-7 нм
(мм3/г)
(%)
%
6,7: объем пор определен по способу вдавливания Hg при 2000 бар
Испытание на активность по метанолу
Окисленные таблетки делили на четыре части, одной фракцией с размерами от 2,5 до 3,5 мм наполняли трубчатый реактор и после активирования подвергали стандартизированному испытанию на активность с периодическим изменением температур. При оценке весовой выход в единицу времени ((GZA), кг(метанола)/(кг(катализатора) × ч)) определяли как среднее значение для каждого периода постоянной температуры. В испытательной реакционной системе, состоящей из 6-16 отдельных труб, в одну из испытательных труб в качестве стандарта вводился катализатор C79-7 фирмы SÜd-Chemie AG, Германия, Мюнхен, и GZA, определенный для других образцов, устанавливали в каждом случае в отношении к значению для стандарта. Этот способ выгоден тем, что незначительные колебания, например, в составе синтез-газа для всех образцов одинаковы, и поэтому результаты разных опытов можно сравнивать друг с другом.
Побочные продукты определяли с помощью газ-хроматографического исследования образцов конденсата, к которым каждый раз добавляли внутренний стандарт. Установленные значения указаны также относительно значений, которые получены для стандарта.
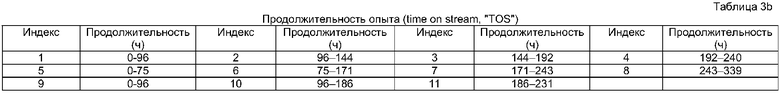
Результаты испытания на активность к метанолу приведены в таблице 3.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОНВЕРСИИ ОКСИДОВ УГЛЕРОДА | 2010 |
|
RU2524951C2 |
| Способ приготовления оксидных катализаторов | 2021 |
|
RU2781406C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА ДЛЯ ОБЕССЕРИВАНИЯ ПОТОКОВ УГЛЕВОДОРОДОВ | 2006 |
|
RU2361668C2 |
| Катализатор для селективного гидрирования диоксида углерода с получением метанола | 2023 |
|
RU2804195C1 |
| СПОСОБ СИНТЕЗА МЕТАНОЛА | 2010 |
|
RU2548006C2 |
| КАТАЛИЗАТОР КОНВЕРСИИ ВОДЯНОГО ГАЗА НИЗКОЙ ТЕМПЕРАТУРЫ | 2008 |
|
RU2491119C2 |
| Способ получения оксидного катализатора для дегидрирования органических веществ | 2021 |
|
RU2787818C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ СИНТЕЗА МЕТАНОЛА И КОНВЕРСИИ МОНООКСИДА УГЛЕРОДА | 2012 |
|
RU2500470C1 |
| МЕДЬЦИНКОВЫЙ КАТАЛИЗАТОР ДЛЯ НИЗКОТЕМПЕРАТУРНОЙ КОНВЕРСИИ ОКСИДА УГЛЕРОДА ВОДЯНЫМ ПАРОМ | 2014 |
|
RU2554949C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЛИТИЯ И ПЕРЕХОДНОГО МЕТАЛЛА С ПРИМЕНЕНИЕМ НАГРЕВАНИЯ | 2019 |
|
RU2790318C2 |
Изобретение относится к способу получения Cu/Zn/Al-катализаторов, к катализатору, полученному этим способом, а также к его применению для синтеза метанола, риформинга метанола и для низкотемпературной конверсии моноксида углерода. Описан способ получения Cu/Zn/Al-катализаторов, включающий получение первого водного раствора, который содержит по меньшей мере формиат меди и формиат цинка, второго раствора, который содержит осадитель, причем первый и/или второй раствор содержит золь/гель смесь гидроксида алюминия, затем на стадии 02осаждения оба раствора соединяют, полученный осадок отделяют от водной фазы, образующей отработанную воду, осадок промывают до тех пор, пока содержание щелочи, в расчете на прокаленный при 600°С катализатор, не станет меньше 500 частей /млн, и сушат. Описан катализатор, полученный этим способом, и его применение для синтеза метанола, риформинга метанола и конверсии моноксида углерода. Технический эффект - упрощение технологии получения катализатора и повышение его активности. 5 н. и 27 з.п. ф-лы, 5 табл.
1. Способ получения Cu/Zn/Al-катализаторов, отличающийся тем, что
получают первый водный раствор, который содержит по меньшей мере формиат меди и формиат цинка,
получают второй раствор, который содержит осадитель,
причем первый раствор и/или второй раствор содержит золь/гель смесь гидроксида алюминия,
на стадии осаждения первый раствор и второй раствор соединяют, причем получается осадок,
осадок отделяют от водной фазы, образующей отработанную воду, и
осадок промывают до тех пор, пока содержание щелочи, в расчете на прокаленный при 600°С катализатор, не станет меньше 500 ч./млн, и
затем осадок сушат.
2. Способ по п.1, отличающийся тем, что первый раствор получают путем
получения водного раствора формиата меди, в котором растворена соль меди без остатка путем добавления муравьиной кислоты,
получения водной дисперсии или раствора соли цинка,
получения водного раствора соли алюминия, и
соединения раствора формиата меди, дисперсии или раствора соли цинка и раствора соли алюминия.
3. Способ по п.2, где раствор формиата меди имеет значение pH ниже 3, предпочтительно ниже 2,5.
4. Способ по п.2, где раствор или дисперсию соли цинка соединяют с раствором формиата меди с образованием медно-цинкового раствора, причем полученный медно-цинковый раствор имеет pH в интервале от 3,0 до 4,0, предпочтительно от 3,5 до 3,7, и к медно-цинковому раствору добавляют раствор соли алюминия.
5. Способ по п.4, где раствор соли алюминия добавляют в нескольких парциальных растворах, причем по меньшей мере первую долю раствора соли алюминия получают так, что по меньшей мере первую часть соли алюминия растворяют в воде при добавлении муравьиной кислоты.
6. Способ по п.4, где вторую часть раствора соли алюминия получают так, что вторую часть соли алюминия растворяют в воде и для получения первого раствора первую часть раствора соли алюминия и вторую часть раствора соли алюминия добавляют к медно-цинковому раствору, предпочтительно разнесенными по времени.
7. Способ по п.2, отличающийся тем, что водный раствор соли алюминия, первую часть раствора соли алюминия и/или вторую часть раствора соли алюминия перед осаждением нагревают до температуры максимум 40°С, в частности максимум 30°С.
8. Способ по п.1, где во время стадии осаждения pH поддерживают в диапазоне от 3,5 до 7,5, предпочтительно от 6,0 до 7,0, в частности предпочтительно 6,5±0,1.
9. Способ по п.1, отличающийся тем, что соль меди выбирают из Cu(OH)2 и Cu(OH)2·CuCO3.
10. Способ по п.1, отличающийся тем, что в качестве соли цинка выбран ZnO.
11. Способ по п.1, где осадитель является щелочным основанием, предпочтительно щелочным карбонатом.
12. Способ по п.1, где осадитель является пероксидом водорода.
13. Способ по п.1, отличающийся тем, что осадок после осаждения подвергают созреванию.
14. Способ по п.13, отличающийся тем, что созревание проводят в течение от 10 мин до 10 ч, предпочтительно от 1 до 5 ч.
15. Способ по п.13, отличающийся тем, что созревание проводят при температуре выше 60°С, в частности, в интервале от 65 до 80°С.
16. Способ по п.1, отличающийся тем, что стадию осаждения проводят как непрерывное осаждение.
17. Способ по п.1, отличающийся тем, что первый раствор содержит медь и цинк в соотношении, выбранном от 1:99 до 99:1.
18. Способ по п.1, отличающийся тем, что осадок после сушки прокаливают.
19. Способ по п.18, где осадок прокаливают при температурах в интервале 140-1000°С, предпочтительно 170-350°С, в течение по меньшей мере 0,1 с, предпочтительно от 20 мин до 8 ч, в частности предпочтительно от 30 мин до 4 ч.
20. Способ по п.1, отличающийся тем, что отработанная вода содержит формиатные ионы и тем, что содержащую формиаты отработанную воду подвергают окислительной обработке, причем формиатные ионы окисляются в основном до карбоната, гидрокарбоната, диоксида углерода и воды.
21. Способ по п.20, отличающийся тем, что для окислительной обработки в содержащую формиаты отработанную воду добавляется пероксид водорода.
22. Способ по п.20, отличающийся тем, что окислительную обработку содержащей формиаты отработанной воды проводят перед отделением осадка.
23. Способ по п.20, отличающийся тем, что окислительную обработку проводят путем биологической обработки содержащей формиаты отработанной воды.
24. Катализатор, полученный способом по одному из пп.1-23, с содержанием формиата, в расчете на оксидный катализатор, менее 5%, предпочтительно 0,5-4%, в частности предпочтительно 1-2%.
25. Катализатор по п.24, отличающийся тем, что доля мезопор с радиусом 3,75-7,0 нм составляет более 30% от полного объема пор.
26. Катализатор по п.24, отличающийся тем, что содержание меди, рассчитанное на оксид меди и отнесенное к весу оксидного катализатора, выбирают между 55 и 69 вес.%.
27. Катализатор по п.24, отличающийся тем, что содержание цинка, рассчитанное на оксид цинка и отнесенное к весу оксидного катализатора, выбирают между 20 и 33 вес.%.
28. Катализатор по п.24, отличающийся тем, что содержание алюминия, рассчитанное на оксид алюминия и отнесенное к весу оксидного катализатора, выбирают между 5 и 20 вес.%.
29. Катализатор по п.24, отличающийся тем, что оксидный катализатор имеет содержание щелочных ионов меньше 500 ч./млн.
30. Применение катализатора по одному из пп.24-29 для синтеза метанола.
31. Применение катализатора по одному из пп.24-29 для риформинга метанола.
32. Применение катализатора по одному из пп.24-29 для низкотемпературной конверсии моноксида углерода в диоксид углерода.
| JP 2001321679 A, 20.11.2001 | |||
| 0 |
|
SU152809A1 | |
| Устройство для анализа случайных процессов | 1972 |
|
SU482753A1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА ДЛЯ ПРОЦЕССА КОНВЕРСИИ ОКСИДА УГЛЕРОДА ВОДЯНЫМ ПАРОМ | 1993 |
|
RU2046656C1 |
| Способ получения катализатора для конверсии окиси углерода | 1975 |
|
SU709163A1 |
Авторы
Даты
2009-11-20—Публикация
2006-05-02—Подача