Уровень техники, предшествующий изобретению
Настоящее изобретение относится к способу получения некоторых фенилсодержащих хлорсиланов, в котором используются алифатические или циклопарафиновые углеводородные растворители реакции сочетания.
Национальный стандарт по регулированию выбросов для опасных загрязнителей воздуха (NESHAP), известный как NESHAP для разнообразных органических соединений или норма MON, является постановлением, которое было опубликовано 10 ноября 2003 года Aгентством США по защите окружающей среды (АЗОС - US Environmental Protection Agency) (EPA), код 40 федеральных постановлений, раздел 63, подраздел FFFF. Согласно норме MON предмет нормы должен быть одобрен производителями и изготовителями химических продуктов к 10 ноября 2006 года. Многие предприятия в настоящий момент инициируют проведение мероприятий по одобрению норм MON, поскольку затронутые в документе операции могут потребовать значительных капиталовложений в новую технологию контроля за загрязнением воздуха, создания условий непрерывного мониторинга выбросов и информирования государственных и федеральных администраций о состоянии их одобрения.
Например, чтобы считаться основным источником загрязнения, предприятие должно обладать возможностью выбрасывать 10 тонн в год одного опасного загрязнителя воздуха (ОЗВ - Hazardous Air Pollutant) (HAP) или 25 тонн в год всех ОЗВ. Ароматические углеводородные соединения, такие как бензол, толуол и ксилол, находятся среди указанных в перечне ОЗВ. Однако другие углеводородные соединения, такие как алифатические и циклопарафиновые углеводороды, т.е. гептан и циклогексан, не находятся в списке ОЗВ и, следовательно, не подлежат контролю. Поэтому когда используется способ согласно изобретению, тогда в некоторых случаях могут не потребоваться дополнительные капиталовложения в любое предприятие, использующее настоящую технологию.
В свете вышеизложенного и согласно способу настоящего изобретения получены некоторые фенилсодержащие хлорсиланы, при получении которых обычно используемый в подобном процессе ароматический углеводородный растворитель реакции сочетания заменен на алифатический или циклопарафиновый углеводородный растворитель реакции сочетания. В частности, в качестве заменяющего растворителя реакции сочетания используют линейный или разветвленный цепочечный алкан
CnH2n+2, такой как н-гептан, вместо часто используемого в качестве растворителя реакции сочетания толуола, например, см. патент США № 6541651 (1 апреля 2003 года) и находящуюся в процессе одновременного рассмотрения предварительную заявку на патент США № 60/534443 (6 января 2004 года). В качестве растворителя реакции сочетания также может быть использован циклопарафиновый углеводород C2H2n.
Краткое изложение сущности изобретения
Настоящее изобретение относится к процессу Гриньяра получения фенилметилдихлорсиланов и дифенилметилхлорсиланов. В процессе реагенты, используемые в процессе Гриньяра, включают фенильный реактив Гриньяра, простой эфирный растворитель, трихлорсилан и алифатический или циклопарафиновый углеводородный растворитель реакции сочетания. Фенильный реактив Гриньяра представляет собой предпочтительно хлорид фенилмагния; простой эфирный растворитель представляет собой простой диалкиловый эфир, такой как простой диметиловый эфир, простой диэтиловй эфир (Et2O), простой этилметиловый эфир, простой н-бутилметиловый эфир, простой н-бутилэтиловый эфир, простой ди-н-бутиловый эфир, простой диизобутиловый эфир, простой изобутилметиловый эфир и простой изобутлэтиловый эфир; алифатический или циклопарафиновый углеводородный растворитель представляет собой предпочтительно н-гептан или циклогексан соответственно; и трихлорсилан представляет собой предпочтительно метилтрихлорсилан, фенилтрихлорсилан или винилтрихлорсилан.
Молярное отношение простого эфирного растворителя к фенильному реактиву Гриньяра составляет 2 к 5, молярное соотношение трихлорсилана к фенильному реактиву Гриньяра составляет 0,1 к 10, а молярное соотношение алифатического или циклопарафинового углеводородного растворителя реакции сочетания к фенильному реактиву Гриньяра составляет 3 к 7.
Было обнаружено, что при замене толуола н-гептаном, алифатическим или циклопарафиновым углеводородным растворителем как растворителем реакции сочетания система сорастворителей простой диэтиловый эфир/н-гептан позволяет очень эффективно осаждать хлорид магния. Использование данной системы простой диэтиловый эфир/н-гептан также обеспечило получение суспензий с очень низкой вязкостью, из которой можно быстро выделить хлорид магния, потому что была получена очень текучая реакционная смесь Гриньяра. Часто встречающийся второй слой мелкоизмельченного хлорида магния также исчезает. Анализ реакционной смеси газовой хроматографией (ГХ) показал, что система простой диэтиловый эфир/н-гептан действовала так же как система простой диэтиловый эфир/толуол с точки зрения образования продукта, если не лучше, потому что система простой диэтиловый эфир/н-гептан образовывала меньше побочных продуктов. Данные и другие признаки изобретения станут очевидными из дальнейшего анализа подробного описания изобретения.
Подробное описание изобретения
Как было использовано в тексте настоящего описания, термин «нормальное взаимодействие» относится к реакциям хлорида фенильного реактива Гриньяра с трихлорсиланом; термин «со-взаимодействие» относится к реакциям трихлорсилана фенильного реактива Гриньяра с фенилхлорсиланом; и термин «прямое взаимодействие» относится к реакциям фенильного реактива Гриньяра с фенилхлорсиланом. Сокращения Et, Me и Ph относятся к этилу, метилу и фенилу соответственно.
Процесс Гриньяра, использованный согласно настоящему изобретению, проиллюстрирован ниже химическими реакциями (I) и (II). Он показывает нормальное взаимодействие. н-Гептан также является одним из продуктов химической реакции (II), но н-гептан не показан в реакции.
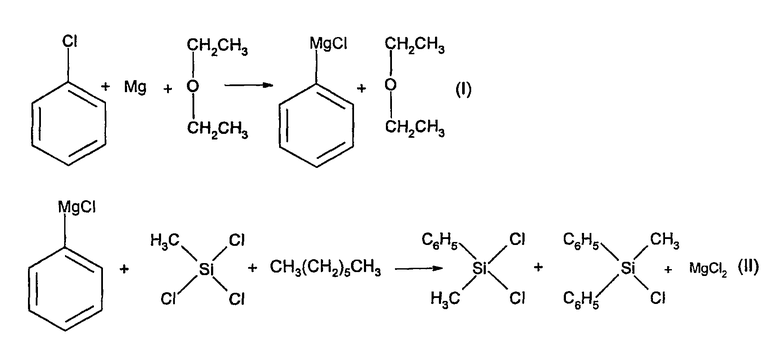
В химической реакции (I) фенилхлорид/хлорбензол (PhCl) соединяется с металлическим магнием (Mg) в присутствии простого диэтилового эфира (CH3-CH2-O-CH2-CH3) в качестве растворителя с получением хлорида фенилмагния (PhMgCl) в простом диэтиловом эфире. Хлорид фенилмагния в простом диэтиловом эфире после этого используется в химической реакции (II), где он соединяется с метилхлорсиланом (MeSiCl3) и предпочтительным растворителем реакции сочетания н-гептаном. Продуктами химической реакции (II) являются фенилметилдихлорсилан (PhMeSiCl2), дифенилметилхлорсилан (Ph2MeSiCl), хлорид магния и н-гептан.
Хлорсиланы, используемые согласно настоящему изобретению, обладают общей формулой RaSiX4-a, где каждый R может означать фенильную группу, метильную группу, винильную группу или атом водорода; X означает атом хлора или брома; и «a» принимает значение 0, 1 или 2. Некоторые подходящие и характерные хлорсиланы, которые могут быть использованы, включают тетрахлорид кремния, метилтрихлорсилан, диметилдихлорсилан, фенилметилдихлорсилан, фенилтрихлорсилан, дифенилдихлорсилан, винилтрихлорсилан, гидридтрихлорсилан, дивинилдихлорсилан, метилвинилдихлорсилан, фенилвинилдихлорсилан, гидридметилдихлорсилан, гидридфенилдихлорсилан, гидридвинилдихлорсилан и дигидриддихлорсилан.
Металлический магний, который может быть использован в настоящем изобретении, может быть любой из форм металла, используемой в настоящее время в реакции типа реакции Гриньяра. Например, металл может быть в форме порошка, хлопьев, гранул, опилок, куска или стружки. Контактирование металлического магния с фенилгалогенидом может быть осуществлено в реакторах стандартного типа, подходящих для протекания реакций типа реакции Гриньяра. Таким образом, реактор может представлять собой реактор периодического, полупериодического или непрерывного типа. Предпочтительным реактором является реактор непрерывного действия. Для лучших результатов среда для проведения настоящего способа должна быть инертной. Поэтому в предпочтительных условиях способа реактор продувают и полностью заполняют инертным газом, таким как азот или аргон.
Фенилгалогениды, которые могут быть использованы в настоящем изобретении, являются теми галогенидами формулы RX, где R представляет собой фенил, а X представляет собой атом хлора или брома. Предпочтительным фенилгалогенидом для настоящего изобретения является фенилхлорид (хлоробензол). Растворители для синтеза реактива Гриньяра включают простые диалкиловые эфиры, такие как простой диметиловый эфир, простой диэтиловый эфир, простой этилметиловый эфир, простой н-бутилметиловый эфир, простой н-бутилэтиловый эфир, простой ди-н-бутиловый эфир, простой диизобутиловый эфир, простой изобутилметиловый эфир и простой изобутилэтиловый эфир. Наиболее предпочтительным простым эфирным растворителем является простой диэтиловый эфир.
Растворителем реакции в реакции сочетания фенильного реактива Гриньяра PhMgCl с PhMeSiCl2 или MeSiCl3 согласно способу настоящего изобретения является алифатический или циклопарафиновый углеводород. В то время как н-гептан является предпочтительным растворителем реакции сочетания, также могут быть использованы и другие неразветвленные алканы, такие как, например, бутан, пентан, гексан, октан, нонан и декан. Как было указано ранее, циклопарафины, такие как циклобутан, циклопентан, циклогексан, циклогептан и их производные, такие как метилциклопентан и метилгексан, могут быть также использованы в качестве растворителя реакции сочетания. Фенильный реактив Гирньяра, такой как PhMgCl, может быть по желанию как синтезирован, так и закуплен на коммерческих условиях.
Примеры
Ниже представлены следующие примеры с целью более детально проиллюстрировать настоящее изобретение.
Сравнительный пример 1 - основная нормальная реакция сочетания с толуолом
В 1-литровой колбе с мешалкой смешивали 143,8 грамм толуола для высокоэффективной жидкостной хроматографии (ВЖХ) и 234,6 грамм MeSiCl3. Через 21 минуту добавляли 222 грамма PhMgCl в Et2O. Плотность PhMgCl составляла 0,91 грамм/мл, и приблизительная концентрация составляла 2,15 мл/л, как установлено методом обрыва реакции MeOH. Температура реакционной смеси достигала 61°С к концу 21-й минуты периода введения реагентов. Общая масса выделенного продукта составляла 572,6 грамм. Смесь жидкости и осадка помещали в 32-унциевую колбу и твердым веществам позволяли осесть. Общая высота жидкости и осадка составляла 9,7 сантиметра, в то время как высота одного осадка составляла 3,6 сантиметра. Плотность жидкости составляла 0,975 грамм/мл. Состав жидкости, определенный газовой хроматографией (ГХ), представлен в таблице 1.
Сравнительный пример 2 - Основная нормальная реакция сочетания с толуолом
В 1-литровой колбе с мешалкой смешивали 127,6 грамм ВЖХ толуола и 206,6 грамм MeSiCl3. Через 19 минут добавляли 215 грамм PhMgCl в Et2O. Плотность PhMgCl составляла 0,91 грамм/мл, и приблизительная концентрация составляла 1,96 моль/л, как было установлено методом обрыва реакции MeOH. Реакционная смесь достигала температуры 62°С к концу периода введения реагентов. Общая масса выделенного продукта составляла 523,4 грамм. Смесь жидкости и осадка помещали в 32-унциевую колбу и твердым веществам позволяли осесть. Общая высота жидкости и осадка составляла 8,8 сантиметра, в то время как высота одного осадка составляла 3,3 сантиметра. Плотность жидкости составляла 0,983 грамм/мл. Состав жидкости, определенный газовой хроматографией (ГХ), представлен в таблице 2.
Пример 3. Нормальная реакция сочетания с н-гептаном
В 1-литровой колбе с мешалкой смешивали 148,1 грамм ВЖХ н-гептана и 221,9 грамм MeSiCl3. Через 22 минуты добавляли 230 грамм PhMgCl в Et2O. Плотность PhMgCl составляла 0,91 грамм/мл, и концентрация составляла 1,96 моль/л, как было установлено методом обрыва реакции MeOH. Температура реакционной смеси достигала 59°С к концу периода введения реагентов. Общая масса выделенного продукта составляла 580,0 грамм. Смесь жидкости и осадка помещали в 32-унциевую колбу и твердым веществам позволяли осесть. Общая высота жидкости и осадка составляла 10,6 сантиметра, в то время как высота одного осадка составляла 4,1 сантиметра. Плотность жидкости составляла 0,874 грамм/мл. Состав жидкости, определенный газовой хроматографией (ГХ), представлен в таблице 3.
Пример 4. Нормальная реакция сочетания с н-гептаном
В 1-литровой колбе с мешалкой смешивали 148,8 грамм ВЖХ н-гептана и 222,4 грамм MeSiCl3. Через 21 минуту добавляли 230 грамм PhMgCl в Et2O. Плотность PhMgCl составляла 0,91 грамм/мл, и концентрация составляла 1,96 моль/л, как было установлено методом обрыва реакции MeOH. Реакционная смесь достигала температуры 58°С к концу периода введения реагентов. Общая масса выделенного продукта составляла 579,7 грамм. Смесь жидкости и осадка помещали в 32-унциевую колбу и твердым веществам позволяли осесть. Общая высота жидкости и осадка составляла 10,6 сантиметра, в то время как высота одного осадка составляла 3,9 сантиметра. Плотность жидкости составляла 0,879 грамм/мл. Состав жидкости, определенный газовой хроматографией (ГХ), представлен в таблице 4.
Различные изменения могут быть сделаны в соединениях, композициях и способах, описанных выше, но без отклонения от основных признаков настоящего изобретения. Варианты осуществления изобретения, конкретно представленные в настоящем описании, являются только пояснительными и не предназначены ограничивать объем притязаний изобретения за исключением прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ГРИНЬЯРА С ПОВЫШЕННЫМ СОДЕРЖАНИЕМ ДИФЕНИЛХЛОРСИЛАНОВ | 2004 |
|
RU2354660C2 |
| ПРОЦЕСС ГРИНЬЯРА С УВЕЛИЧЕННЫМИ ВЫХОДАМИ ДИФЕНИЛХЛОРСИЛАНОВ В КАЧЕСТВЕ ПРОДУКТОВ | 2004 |
|
RU2345084C2 |
| ПРОИЗВОДНОЕ АЛЮМИНИЯ ФОРМУЛЫ AL(CF) И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1995 |
|
RU2145607C1 |
| БЛОК-СОПОЛИМЕРЫ СОПРЯЖЕННЫХ ДИЕНОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И КОМПОЗИЦИЯ ПОКРЫТИЯ | 1993 |
|
RU2130032C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФТОРАРИЛМАГНИЕВОГО ПРОИЗВОДНОГО И СПОСОБ ПОЛУЧЕНИЯ (ФТОРАРИЛ) БОРАНОВОГО СОЕДИНЕНИЯ (ВАРИАНТЫ) | 1997 |
|
RU2159246C2 |
| ПОЛУЧЕНИЕ ЗАМЕЩЕННЫХ ИНДЕНОВ | 2003 |
|
RU2323921C2 |
| КАТАЛИТИЧЕСКАЯ СИСТЕМА, СОДЕРЖАЩАЯ РЕДКОЗЕМЕЛЬНЫЙ МЕТАЛЛОЦЕН | 2016 |
|
RU2729076C2 |
| ДИФОСФИНЫ И МЕТАЛЛОКОМПЛЕКСЫ | 2006 |
|
RU2408600C2 |
| АДДУКТЫ-АЛЬДЕГИДЫ В КАЧЕСТВЕ ПРОМЕЖУТОЧНЫХ ПРОДУКТОВ В СИНТЕЗЕ ПРОИЗВОДНЫХ ВИТАМИНА D | 1990 |
|
RU2036904C1 |
| КАТАЛИТИЧЕСКАЯ КОМПОЗИЦИЯ, МЕТАЛЛОЦЕНОВЫЙ КОМПЛЕКС И СПОСОБ ПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ | 1994 |
|
RU2156253C2 |
Изобретение относится к способу получения фенилсодержащих хлорсиланов на основе процесса Гриньяра. Техническая задача - разработка способа, в котором обычно используемый ароматический углеводородный растворитель реакции сочетания заменен на алифатический или циклопарафиновый. Предложен способ получения фенилметилдихлорсиланов и дифенилметилхлорсиланов по реакции Гриньяра, включающий взаимодействие фенильного реактива Гриньяра, простого эфирного растворителя, трихлорсилана и алифатического или циклопарафинового углеводородного растворителя реакции; молярное отношение простого эфирного растворителя к фенильному реактиву Гриньяра составляет 2 к 5, молярное отношение трихлорсилана к фенильному реактиву Гриньяра составляет 0,1 к 10, и молярное отношение алифатического или циклопарафинового углеводородного растворителя реакции к фенильному реактиву Гриньяра составляет 3 к 7. Предложенный способ более экологичен по сравнению со способом, проводимым с использованием ароматических углеводородных растворителей. 9 з.п. ф-лы, 4 табл.
1. Способ получения фенилметилдихлорсиланов и дифенилметилхлорсиланов по реакции Гриньяра, включающий взаимодействие фенильного реактива Гриньяра, простого эфирного растворителя, трихлорсилана и алифатического или циклопарафинового углеводородного растворителя реакции сочетания, при этом молярное отношение простого эфирного растворителя к фенильному реактиву Гриньяра составляет 2 к 5, молярное отношение трихлорсилана к фенильному реактиву Гриньяра составляет 0,1 к 10, и молярное отношение алифатического или циклопарафинового углеводородного растворителя реакции сочетания к фенильному реактиву Гриньяра составляет 3 к 7.
2. Способ по п.1, в котором фенильным реактивом Гриньяра является хлорид фенилмагния.
3. Способ по п.1 или 2, в котором простым эфирным растворителем является простой диалкиловый эфир, выбранный из группы, включающей простой диметиловый эфир, простой диэтиловый эфир, простой этилметиловый эфир, простой н-бутилметиловый эфир, простой н-бутилэтиловый эфир, простой ди-н-бутиловый эфир, простой диизобутиловый эфир, простой изобутилметиловый эфир и простой изобутилэтиловый эфир.
4. Способ по п.1, в котором трихлорсилан выбран из группы, включающей метилтрихлорсилан, фенилтрихлорсилан и винилтрихлорсилан.
5. Способ по п.1, в котором алифатический углеводородный растворитель реакции сочетания выбран из группы, включающей бутан, пентан, гексан, н-гептан, октан, нонан и декан.
6. Способ по п.1, в котором алифатический углеводородный растворитель реакции сочетания является н-гептаном.
7. Способ по п.1, в котором циклопарафиновый углеводородный растворитель реакции сочетания выбран из группы, включающей циклобутан, циклопентан, циклогексан, циклогептан, метилциклопентан и метилциклогексан.
8. Способ по п.1, в котором циклопарафиновый углеводородный растворитель реакции сочетания является циклогексаном.
9. Способ по п.3, в котором алифатический углеводородный растворитель реакции сочетания выбран из группы, включающей бутан, пентан, гексан, н-гептан, октан, нонан и декан.
10. Способ по п.3, в котором циклопарафиновый углеводородный растворитель реакции сочетания выбран из группы, включающей циклобутан, циклопентан, циклогексан, циклогептан, метилциклопентан и метилциклогексан.
| WO 03106465 A1, 24.12.2003 | |||
| WO 03084970 A1, 16.10.2003 | |||
| WO 03084967 A1, 16.10.2003 | |||
| Барабан для обработки металлургического скрапа | 1983 |
|
SU1120150A1 |
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕНИЛ- И МЕТИЛФЕНИЛХЛОРСИЛАНОВ | 1991 |
|
RU2015982C1 |
Авторы
Даты
2009-11-20—Публикация
2006-01-25—Подача