Область техники
Настоящее изобретение относится к системе арилфеноксидного катализатора для получения гомополимера этилена и сополимеров этилена и α-олефинов. Более конкретно настоящее изобретение относится к катализатору переходного металла 4-й группы, представленному формулой 1, каталитической системе, которая включает в себя катализатор на основе арилфеноксизамещенного переходного металла и алюминоксановый сокатализатор или сокатализатор из соединения бора, и способу получения гомополимера этилена или сополимеров этилена и α-олефинов с использованием такой каталитической системы. В катализаторе переходного металла производное циклопентадиена и арилфеноксид в качестве химически связанных лигандов локализованы вокруг переходного металла 4-й группы, арилфеноксидный лиганд замещен, по меньшей мере, одним арильным производным и локализован в его ортоположении и лиганды не сшиты друг с другом.
Формула 1
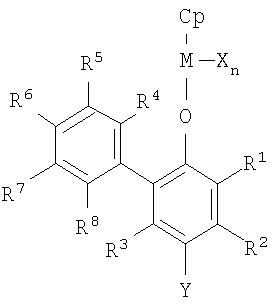
В формуле 1 М представляет собой переходный металл 4-й группы периодической таблицы;
Ср представляет собой циклопентадиеновую группу, способную образовывать η5-связь с центральным металлом, или ее производное;
R1, R2, R3, R4, R5, R6, R7 и R8 арилфеноксидного лиганда представляют собой независимо атом водорода, атом галогена, разветвленную или неразветвленную С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, силильную группу, которая содержит разветвленную или неразветвленную С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, С6-С30-арильную группу произвольно замещенную одним или несколькими атомами галогена, С7-С30-арилалкильную группу, произвольно замещенную одним или несколькими атомами галогена, алкоксигруппу, которая содержит С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, или С3-С20-алкилзамещенную или С6-С20-арилзамещенную силоксигруппу, необязательно с условием, что группы-заместители могут быть произвольно связаны с образованием кольца;
Х представляет собой один или два заместителя, независимо выбранных из группы, состоящей из атома галогена, С1-С20-алкильной группы, которая не является производным Ср, С7-С30-арилакильной группы, алкоксигруппы, которая содержит С1-С20-алкильную группу, С3-С20-алкилзамещенной силоксигруппы и амидогруппы, которая имеет С1-С20-угеводородную группу;
Y представляет собой атом водорода, атом галогена, разветвленную или неразветвленную С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, силильную группу, которая содержит неразветвленную или разветвленную С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, С6-С30-арильную группу, произвольно замещенную одним или несколькими атомами галогена, С7-С30-арилалкильную группу произвольно замещенную одним или несколькими атомами галогена, алкоксигруппу, которая содержит С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, или С3-С20-алкилзамещенную или С6-С20-арилзамещенную силоксигруппу, амидогруппу или фосфидогруппу, которая содержит С1-С20 углеводородную группу, или алкилзамещенную меркаптогруппу или нитрогруппу; и
n равно 1 или 2 в зависимости от степени окисления переходного металла.
Уровень техники
Общеизвестно, что каталитическую систему Циглера-Натта, которая включает в себя в качестве основного каталитического компонента соединения титана или ванадия и в качестве компонента-сокатализатора алкилалюминиевые соединения, применяли для получения гомополимера этилена или сополимеров этилена и α-олефинов. Однако каталитическая система Циглера-Натта невыгодна в том отношении, что хотя она обладает высокой активностью при полимеризации этилена, молекулярно-массовое распределение образовавшегося полимера находится в широких пределах, и, особенно, в том отношении, что сополимер этилена и α-олефина имеет неоднородное композиционное распределение вследствие активных центров гетерогенного катализатора.
Недавно была разработана металлоценовая каталитическая система, которая включает в себя металлоценовое соединение переходного металла 4-й группы в периодической таблице, такого как титан, цирконий или гафний, и метилалюминоксан в качестве сокатализатора. Поскольку металлоценовая каталитическая система является гомогенным катализатором, имеющим один тип каталитического активного центра, ее можно применять для получения полиэтилена, имеющего узкое молекулярно-массовое распределение и однородное композиционное распределение по сравнению с общепринятой каталитической системой Циглера-Натта. Например, в патентах ЕР №№320762 и 372632 и публикации выложенного патента Японии №№ Sho.63-092621, Hei.02-84405 и Hei.03-2347 описаны металлоценовые соединения, такие как Cp2TiCl2, Cp2ZrCl2, Cp2ZrMeCl, Cp2ZrMe2 или (этиленбистетрагидроинденил)ZrCl2, активированные метилалюминоксаном как сокатализатором, для полимеризации этилена при высокой каталитической активности, что делало, таким образом, возможным получение полиэтилена, имеющего молекулярно-массовое распределение (Mw/Mn) 1,5-2,0. Однако трудно получить полимер, имеющий высокую молекулярную массу, с использованием указанной выше каталитической системы. Особенно, если ее применяют для способа полимеризации в растворе, который проводят при высокой температуре 140°С или выше, активность полимеризации быстро понижается и доминирует реакция элиминирования β-водорода, поэтому она является неподходящей для получения полимера с высокой молекулярной массой, имеющего среднюю молекулярную массу (Mw) 100000 или более.
Между тем, неметаллоценовый катализатор с ограниченной геометрией (так называемый катализатор с одним активным центром), в котором переходный металл связан с лигандной системой в форме кольца, был предложен в качестве катализатора, который имеет высокую каталитическую активность и способен образовывать полимер, имеющий высокую молекулярную массу, при полимеризации только этилена или при сополимеризации этилена и α-олефина в условиях полимеризации в растворе.
В патентах ЕР №№0416815 и 0420436 предложена каталитическая система, в которой переходный металл соединяется с циклопентадиеновым лигандом и амидной группой в форме кольца, и в патенте ЕР №0842939 описан катализатор, в котором лиганд на основе фенола в качестве соединения-донора электронов соединяется с циклопентадиеновым лигандом в форме кольца. Однако поскольку циклизация лигандов вместе с соединением переходного металла протекает с очень низкими выходами во время синтеза катализатора с ограниченной геометрией, трудной является его реализация в коммерческих масштабах.
Между тем, пример неметаллоценового катализатора, который не является катализатором с ограниченной геометрией и который можно применять в условиях полимеризации в растворе при высокой температуре, описан в патенте США №6329478 и в публикации выложенного патента Кореи №2001-0074722. В патентах описан катализатор с одним активным центром, имеющий одно или несколько фосфиниминовых соединений в качестве лиганда, имеющий высокое превращение этилена во время сополимеризации этилена и α-олефинов в условиях полимеризации в растворе при высокой температуре от 140°С и выше. Однако для получения фосфиниминового лиганда можно применять ограниченный диапазон фосфиновых соединений и, поскольку эти соединения являются вредными для окружающей среды и человека, могут быть некоторые затруднения при получении их для получения олефиновых полимеров общего назначения. В патенте США №5079205 описан катализатор, имеющий бисфеноксидный лиганд, но он имеет слишком низкую каталитическую активность для коммерческого применения.
Помимо вышеуказанных примеров в Organometallic 1998, 17, 2152 (Nomura et al.) описан синтез неметаллоценового катализатора с лигандом на основе фенола и полимеризация с применением такого катализатора, в котором заместители фенольного лиганда ограничены только простыми алкильными заместителями, такими как изопропильная группа. С другой стороны, в J Organomet. Chem. 1999, 591, 148 (Rothwell, P. et al.) описан арилфеноксилиганд, но не предполагалось влияние арильного заместителя в ортоположении.
Описание изобретения
Техническая проблема
Для преодоления вышеуказанных проблем, имеющих место в предшествующем уровне техники, авторы настоящего изобретения провели экстенсивные исследования, которые привели к выводу, что катализаторы переходных металлов немостикового типа, в которых производные циклопентадиена и арилфеноксид, замещенный, по меньшей мере, одним арилпроизводным в его ортоположении, применяемые в качестве химически связанных лигандов, проявляют превосходную термическую стабильность. На основании вышеуказанного вывода был разработан катализатор, который применяют для получения гомополимера этилена или сополимеров этилена и α-олефинов, имеющих высокую молекулярную массу, при высокой активности его во время способа полимеризации в растворе при высокой температуре 80°С или выше, тем самым настоящее изобретение было выполнено.
В соответствии с этим задачей настоящего изобретения является предоставление катализатора с одним активным центром и способ полимеризации в растворе при высокой температуре с применением такого катализатора. Катализатор с одним активным центром включает в себя исходные материалы, благоприятные для окружающей среды, синтез катализатора является очень экономичным и термическая стабильность катализатора является превосходной. Способом полимеризации в растворе с применением такого катализатора можно легко и коммерчески выгодно получать гомополимер этилена или сополимеры этилена и α-олефина, имеющие различные физические свойства.
Техническое разрешение проблемы
Для выполнения вышеуказанной задачи аспект настоящего изобретения предлагает катализатор переходного металла на основе арилфеноксигруппы, представленный формулой 1, которая включает в себя производное циклопентадиена и арилфеноксид в качестве химически связанных лигандов вокруг переходного металла. Арилфеноксид замещен, по меньшей мере, одним арильным производным и локализован в его ортоположении и лиганды не сшиты друг с другом.
Формула 1
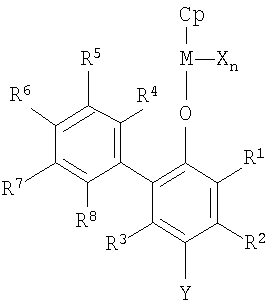
В формуле 1 М представляет собой переходный металл 4-й группы периодической таблицы;
Ср представляет собой циклопентадиеновую группу, способную образовывать η5-связь с центральным металлом, или ее производное;
R1, R2, R3, R4, R5, R6, R7 и R8 арилфеноксидного лиганда представляют собой независимо атом водорода, атом галогена, разветвленную или неразветвленную С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, силильную группу, которая содержит разветвленную или неразветвленную С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, С6-С30-арильную группу, произвольно замещенную одним или несколькими атомами галогена, С7-С30-арилалкильную группу, произвольно замещенную одним или несколькими атомами галогена, алкоксигруппу, которая содержит С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, или С3-С20-алкилзамещенную или С6-С20-арилзамещенную силоксигруппу, необязательно с условием, что группы-заместители могут произвольно образовывать кольца;
Х представляет собой два или более заместителей, независимо выбранных из группы, состоящей из атома галогена, С1-С20-алкильной группы, которая не является производным Ср, С7-С30-арилакильной группы, алкоксигруппы, которая содержит С1-С20-алкильную группу, С3-С20-алкилзамещенной силоксигруппы и амидогруппы, которая содержит С1-С20-углеводородную группу;
Y представляет собой атом водорода, атом галогена, разветвленную или неразветвленную С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, силильную группу, которая содержит неразветвленную или разветвленную С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, С6-С30-арильную группу, произвольно замещенную одним или несколькими атомами галогена, С7-С30-арилалкильную группу, произвольно замещенную одним или несколькими атомами галогена, алкоксигруппу, которая содержит С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, или С3-C20-алкилзамещенную или С6-С20-арилзамещенную силоксигруппу, амидогруппу или фосфидогруппу, которая содержит С1-С20-углеводородную группу, или С1-С20-алкилзамещенную меркаптогруппу или нитрогруппу, и
n равно 1 или 2 в зависимости от степени окисления переходного металла.
Другой аспект настоящего изобретения относится к каталитической системе, которая включает в себя катализатор переходного металла и соединение алюминия или бора в качестве сокатализатора.
Еще один аспект настоящего изобретения относится к способу получения полимеров этилена с применением катализатора переходного металла.
Благоприятные влияния
Система арилфеноксикатализатора согласно настоящему изобретению является благоприятной в том, что ею легко манипулировать и легко получать с применением благоприятных для окружающей среды исходных материалов с высоким выходом, и она имеет высокую каталитическую активность в условиях полимеризации в растворе при высокой температуре благодаря ее превосходной термической стабильности в процессе получения полимера, имеющего высокую молекулярную массу, таким образом, она является более полезной, чем общепринятый неметаллоценовый катализатор с одним активным центром. Следовательно, она является полезной для получения гомополимера этилена или сополимеров этилена и α-олефинов, имеющих различные физические свойства.
Краткое описание чертежей
Вышеуказанные и другие задачи, признаки и преимущества настоящего изобретения будут более лучше понятны из нижеследующего описания в сочетании с прилагаемыми чертежами, на которых:
на Фиг.1 показана кристаллическая структура катализатора (дихлор)(циклопентадиенил)(4-метил-2,6-бис(2'-изопропилфенил)фенокси)титана(IV) согласно настоящему изобретению; и
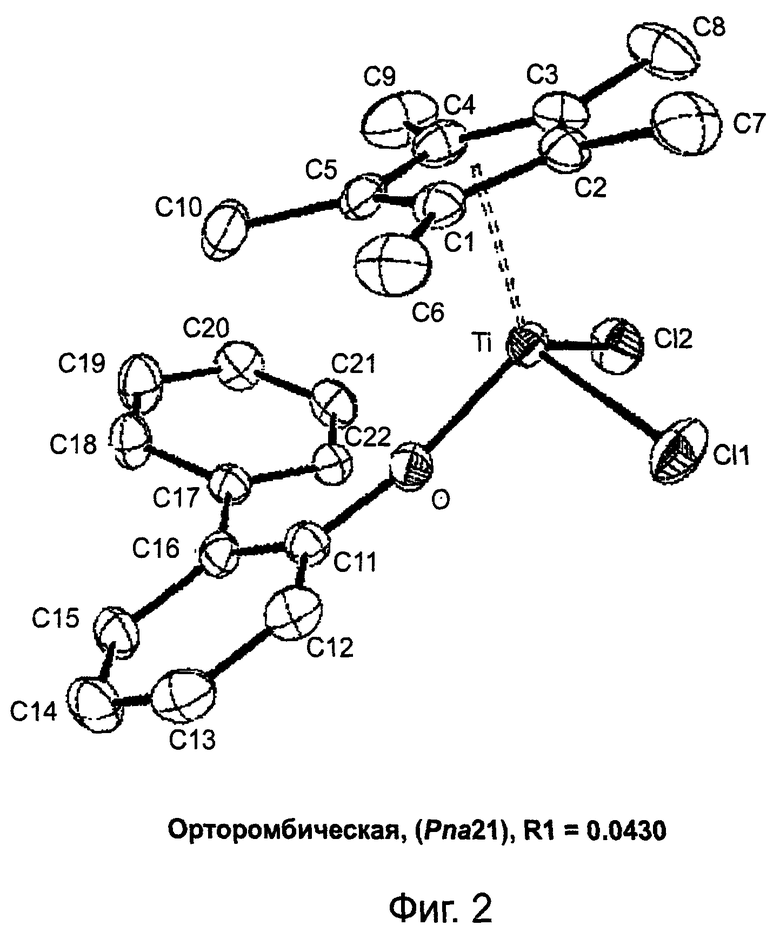
на Фиг.2 показана кристаллическая структура катализатора (дихлор)(пентаметилциклопентадиенил)(2-фенилфенокси)титана(IV) согласно настоящему изобретению.
Предпочтительный вариант осуществления изобретения
Ниже будет представлено подробное описание настоящего изобретения.
М катализатора переходного металла в формуле 1 предпочтительно представляет собой титан, цирконий или гафний. Кроме того, Ср представляет
собой анион циклопентадиена, способный образовывать η5-связь вместе с центральным металлом, или его производное. Подробно, примерами таких Ср являются циклопентадиенил, метилциклопентаденил, диметилциклопентадиенил, тетраметилциклопентадиенил, пентаметилциклопентадиенил, бутилциклопентадиенил, втор-бутилциклопентадиенил, трет-бутилметилциклопентадиенил, триметилсилилциклопентадиенил, инденил, метилинденил, диметилинденил, этилинденил, изопропилинденил, флуоренил, метилфлуоренил, диметилфлуоренил, этилфлуоренил и изопропилфлуоренил.
Что касается R1 R2, R3, R4, R5, R6, R7 и R8 арилфеноксидного лиганда, примером атома галогена являются атом фтора, хлора, брома и йода; и примером С1-С20-алкильной группы является метильная группа, этильная группа, н-пропильная группа, изопропильная группа, н-бутильная группа, втор-бутильная группа, трет-бутильная группа, н-пентильная группа, неопентильная группа, амильная группа, н-гексильная группа, н-октильная группа, н-децильная группа, н-додецильная группа, н-пентадецильная группа и н-эйкозильная группа, и предпочтительно, метильная группа, этильная группа, изопропильная группа, трет-бутильная группа и амильная группа. Алкильная группа может быть произвольно замещена одним или несколькими атомами галогена и примером ее является фторметильная группа, дифторметильная группа, трифторметильная группа, хлорметильная группа, дихлорметильная группа, трихлорметильная группа, бромметильная группа, дибромметильная группа, трибромметильная группа, йодметильная группа, дийодметильная группа, трийодметильная группа, фторэтильная группа, дифторэтильная группа, трифторэтильная группа, тетрафторэтильная группа, пентафторэтильная группа, хлорэтильная группа, дихлорэтильная группа, трихлорэтильная группа, тетрахлорэтильная группа, пентахлорэтильная группа, бромэтильная группа, дибромэтильная группа, трибромэтильная группа, тетрабромэтильная группа, пентабромэтильная группа, перфторпропильная группа, перфторбутильная группа, перфторпентильная группа, перфторгексильная группа, перфтороктильная группа, перфтордодецильная группа, перфторпентадецильная группа, перфторэйкозильная группа, перхлорпропильная группа, перхлорбутильная группа, перхлорпентильная группая, перхлоргексильная группа, перхлороктильная группа, перхлордодецильная группа, перхлорпентадецильная группа, перхлорэйкозильная группа, пербромпропильная группа, пербромбутильная группа, пербромпентилькая группа, пербромгексильная группа, пербромоктильная группа, пребромдодецильная группа, пербромпентадецильная группа или пербромэйкозильная группа. Среди них предпочтительной является трифторметильная группа. В R1 R2, R3, R4, R5, R6, R7 и R8 примером С1-С20-алкилзамещенной силильной группы является метилсилильная группа, этилсилильная группа, фенилсилильная группа, диметилсилильная группа, диэтилсилильная группа, дифенилсилильная группа, триметилсилильная группа, триэтилсилильная группа, три-н-пропилсилильная группа, триизопропилсилильная группа, три-н-бутилсилильная группа, три-втор-бутилсилильная группа, три-трет-бутилсилильная группа, триизобутилсилильная группа, трет-бутилдиметилсилильная группа, три-н-пентилсилильная группа, три-н-гексилсилильная группа, трициклогексилсилильная группа или трифенилсилильная группа и, предпочтительно, триметилсилильная группа, трет-бутилдиметилсилильная группа и трифенилсилильная группа. Примером С6-С30-арильной группы является фенильная группа, 2-толильная группа, 3-толильная группа, 4-толильная группа, 2,3-ксилильная группа, 2,4-ксилильная группа, 2,5-ксилильная группа, 2,6-ксилильная группа, 3,4-ксилильная группа, 3,5-ксилильная группа, 2,3,4-триметилфенильная группа, 2,3,5-триметилфенильная группа, 2,3,6-триметилфенильная группа, 2,4,6-триметилфенильная группа, 3,4,5-тетраметилфенильная группа, 2,3,4,5-тетраметилфенильная группа, 2,3,4,6-тетраметилфенильная группа, 2,3,5,6-тетраметилфенильная группа, пентаметилфенильная группа, этилфенильная группа, н-пропилфенильная группа, изопропилфенильная группа, н-бутилфенильная группа, втор-бутилфенильная группа, трет-бутилфенильная группа, н-пентилфенильная группа, неопентилфенильная группа, н-гексилфенильная группа, н-октилфенильная группа, н-децилфенильная группа, н-додецилфенильная группа, н-тетрадецилфенильная группа, бифенильная группа, флуоренильная группа, трифенильная группа, нафтильная группа или антраценильная группа и, предпочтительно, фенильная группа, нафтильная группа, бифенильная группа, 2-изопропилфенильная группа, 3,5-ксилильная группа и 2,4,6-триметилфенильная группа. Примером С7-С30-арилакильной группы является бензильная группа, (2-метилфенил)метильная группа, (3-метилфенил)метильная группа, (4-метилфенил)метильная группа, (2,3-диметилфенил)метильная группа, (2,4-диметилфенил)метильная группа, (2,5-диметилфенил)метильная группа, (2,6-диметилфенил)метильная группа, (3,4-диметилфенил)метильная группа, (4,6-диметилфенил)метильная группа, (2,3,4-триметилфенил)метильная группа, (2,3,5-триметилфенил)метильная группа, (2,3,6-триметилфенил)метильная группа, (3,4,5-триметилфенил)метильная группа, (2,4,6-триметилфенил)метильная группа, (2,3,4,5-тетраметилфенил)метильная группа, (2,3,4,6-тетраметилфенил)метильная группа, (2,3,5,6-тетраметилфенил)метильная группа, (пентаметилфенил)метильная группа, (этилфенил)метильная группа, (н-пропилфенил)метильная группа, (изопропилфенил)метильная группа, (н-бутилфенил)метильная группа, (втор-бутилфенил)метильная группа, (трет-бутилфенил)метильная группа, (н-пентилфенил)метильная группа, (неопентилфенил)метильная группа, (н-гексилфенил)метильная группа, (н-октилфенил)метильная группа, (н-децилфенил)метильная группа, (н-додецилфенил)метильная группа, (н-тетрадецилфенил)метильная группа, нафтилметильная группа или антраценилметильная группа и, предпочтительно, бензильная группа. Примером С1-С20-алкоксигруппы является метоксигруппа, этоксигруппа, н-пропоксигруппа, изопропоксигруппа, н-бутоксигруппа, втор-бутоксигруппа, трет-бутоксигруппа, н-пентоксигруппа, неопентоксигруппа, н-гексоксигруппа, н-октоксигруппа, н-додекоксигруппа, н-пентадексоксигруппа или н-эйкозоксигруппа и, предпочтительно, метоксигруппа, этоксигруппа, изопроксоксигруппа и трет-бутоксигруппа. Примером С3-С20-алкилзамещенной или С6-С20-арилзамещенной силоксигруппы является триметилсилоксигруппа, триэтилсилоксигруппа, три-н-пропилсилоксигруппа, триизопропилсилоксигруппа, три-н-бутилсилоксигруппа, три-втор-бутилсилоксигруппа, три-трет-бутилсилоксигруппа, триизобутилсилоксигруппа, трет-бутилдиметилсилоксигруппа, три-н-пентилсилокси группа, три-н-гексилсилоксигруппа, трициклогексилсилоксигруппа или трифенилсилоксигруппа и, предпочтительно, триметилсилоксигруппа, трет-бутилдиметилсилоксигруппа и трифенилсилоксигруппа. Вышеупомянутые группы-заместители могут быть произвольно замещены одним или несколькими атомами галогена.
В Х примером атома галогена является атом фтора, хлора, брома и йода и примером С1-С20-алкильной группы, которая не является производным Ср, является метильная группа, этильная группа, н-пропильная группа, изопропильная группа, н-бутильная группа, втор-бутильная группа, трет-бутильная группа, н-пентильная группа, неопентильная группа, амильная группа, н-гексильная группа, н-октильная группа, н-децильная группа, н-додецильная группа, н-пентадецильная группа и н-эйкозильная группа и предпочтительно метильная группа, этильная группа, изопропильная группа, трет-бутильная группа и амильная группа. Примером С7-С30-арилакильной группы является бензильная группа, (2-метилфенил)метильная группа, (3-метилфенил)метильная группа, (4-метилфенил)метильная группа, (2,3-диметилфенил)метильная группа, (2,4-диметилфенил)метильная группа, (2,5-диметилфенил)метильная группа, (2,6-диметилфенил)метильная группа, (3,4-диметилфенил)метильная группа, (4,6-диметилфенил)метильная группа, (2,3,4-триметилфенил)метильная группа, (2,3,5-триметилфенил)метильная группа, (2,3,6-триметилфенил)метильная группа, (3,4,5-триметилфенил)метильная группа, (2,4,6-триметилфенил)метильная группа, (2,3,4,5-тетраметилфенил)метильная группа, (2,3,4,6-тетраметилфенил)метильная группа, (2,3,5,6-тетраметилфенил)метильная группа, (пентаметилфенил)метильная группа, (этилфенил)метильная группа, (н-пропилфенил)метильная группа, (изопропилфенил)метильная группа, (н-бутилфенил)метильная группа, (втор-бутилфенил)метильная группа, (трет-бутилфенил)метильная группа, (н-пентилфенил)метильная группа, (неопентилфенил)метильная группа, (н-гексилфенил)метильная группой, (н-октилфенил)метильная группа, (н-децилфенил)метильная группа, (н-додециофенил)метильная группа, (н-тетрадецилфенил)метильная группа, нафтилметильная группа или антраценилметильная группа, и предпочтительно, бензильная группа. Примером С1-С20-алкоксигруппы является метоксигруппа, этоксигруппа, н-пропоксигруппа, изопропоксигруппа, н-бутоксигруппа, втор-бутоксигруппа, трет-бутоксигруппа, н-пентоксигруппа, неопентоксигруппа, н-гексоксигруппа, н-октоксигруппа, н-додекоксигруппа, н-пентадекоксигруппа или н-эйкозоксигруппа и предпочтительно метоксигруппа, этоксигруппа, изопроксоксигруппа и трет-бутоксигруппа. Примером С3-С20-алкилзамещенной силоксигруппы является триметилсилоксигруппа, триэтилсилоксигруппа, три-н-пропилсилоксигруппа, триизопропилсилоксигруппа, три-н-бутилсилоксигруппа, три-втор-бутилсилоксигруппа, три-трет-бутилсилокси группа, триизобутилсилокси группа, трет-бутилдиметилсилоксигруппа, три-н-пентилсилоксигруппа, три-н-гексилсилоксигруппа или трициклогексилоксигруппа и предпочтительно триметилсилоксигруппа и трет-бутилдиметилсилоксигруппа.
Примером амидогруппы или фосфидогруппы, имеющей С1-С20-углеводородную группу, является диметиламиногруппа, диэтиламиногруппа,
ди-н-пропиламиногруппа, диизопропиламиногруппа, ди-н-бутил аминогруппа, ди-втор-бутиламиногруппа, ди-трет-бутиламиногруппа, диизобутиламиногруппа, трет-бутилизопропиламиногруппа, ди-н-гексиламиногруппа, ди-н-октиламиногруппа, ди-н-дециламиногруппа, дифениламиногруппа, дибензиламидогруппа, метилэтиламидогруппа, метилфениламидогруппа, бензилгексиламидогруппа, бистриметилсилиламиногруппа или бис-трет-бутилдиметилсилиламиногруппа, или фосфидогруппа, которая замещена таким же алкилом. Среди них предпочтительными являются диметиламиногруппа, диэтиламиногруппа и дифениламидогруппа.
В Y примером атома галогена является атом фтора, хлора, брома и йода; и примером С1-С20-алкильной группы является метильная группа, этильная группа, н-пропильная группа, изопропильная группа, н-бутильная группа, втор-бутильная группа, трет-бутильная группа, н-пентильная группа, неопентильная группа, амильная группа, н-гексильная группа, н-октильная группа, н-децильная группа, н-додецильная группа, н-пентадецильная группа и н-эйкозильная группа и предпочтительно метильная группа, этильная группа, изопропильная группа, трет-бутильная группа и амильная группа. Примером С1-С20-алкильной группы, которая произвольно замещена одним или несколькими атомами галогена, является фторметильная группа, дифторметильная группа, трифторметильная группа, хлорметильная группа, дихлорметильная группа, трихлорметильная группа, бромметильная группа, дибромметильная группа, трибромметильная группа, йодметильная группа, дийодметильная группа, трийодметильная группа, фторэтильная группа, дифторэтильная группа, трифторэтильная группа, тетрафторэтильная группа, пентафторэтильная группа, хлорэтильная группа, дихлорэтильная группа, трихлорэтильная группа, тетрахлорэтильная группа, пентахлорэтильная группа, бромэтильная группа, дибромэтильная группа, трибромэтильная группа, тетрабромэтильная группа, пентабромэтильная группа, перфторпропильная группа, перфторбутильная группа, перфторпентильная группа, перфторгексильная группа, перфтороктильная группа, перфтордодецильная группа, перфторпентадецильная группа, перфторэйкозильная группа, перхлорпропильная группа, перхлорбутильная группа, перхлорпентильная группа, перхлоргексильная группа, перхлороктильная группа, перхлордодецильная группа, перхлорпентадецильная группа, перхлорэйкозильная группа, пербромпропильная группа, пербромбутильная группа, пербромпентильная группа, пербромгексильная группа, пербромоктильная группа, пербромдодецильная группа, пербромпентадецильная группа или пербромэйкозильная группа и предпочтительно трифторметильная группа. Кроме того, в Y примером С1-С20-алкилзамещенной силильной группы является метилсилильная группа, этилсилильная группа, фенилсилильная группа, диметилсилильная группа, диэтилсилильная группа, дифенилсилильная группа, триметилсилильная группа, триэтилсилильная группа, три-н-пропилсилильная группа, триизопропилсилильная группа, три-н-бутилсилильная группа, три-втор-бутилсилильная группа, три-трет-бутилсилильная группа, три-изобутилсилильная группа, трет-бутилдиметилсилильная группа, три-н-пентилсилильная группа, три-н-гексисилильная группа, трициклогексилсилильная группа или трифенилсилильную группу и предпочтительно триметилсилильная группа, трет-бутилдиметилсилильная группа и трифенилсилильная группа. Примером С6-С30-арильной группы является фенильная группа, 2-толильная группа, 3-толильная группа, 4-толильная группа, 2,3-ксилильная группа, 2,4-ксилильная группа, 2,5-ксилильная группа, 2,6-ксилильная группа, 3,4-ксилильная группа, 3,5-ксилильная группа, 2,3,4-триметилфенильная группа, 2,3,5-триметилфенильная группа, 2,3,6-триметилфенильная группа, 2,4,6-триметилфенильная группа, 3,4,5-триметилфенильная группа, 2,3,4,5-тетраметилфенильная группа, 2,3,4,6-тетраметилфенильная группа, 2,3,5,6-тетраметилфенильная группа, пентаметилфенильная группа, этилфенильная группа, н-пропилфенильная группа, изопропилфенильная группа, н-бутилфенильная группа, втор-бутилфенильная группа, трет-бутилфенильная группа, н-пентилфенильная группа, неопентилфенильная группа, н-гексилфенильная группа, н-октилфенильная группа, н-децилфенильная группа, н-додецилфенильная группа, н-тетрадецилфенильная группа, бифенильная группа, флуоренильная группа, трифенильная группа, нафтильная группа или антраценильная группа, и предпочтительно, фенильная группа, нафтильная группа, бифенильная группа, 2-изопропилфенильная группа, 3,5-ксилильная группа и 2,4,6-триметилфенильная группа. Примером С7-С30-арилакильной группы является бензильная группа, (2-метилфенил)метильная группа, (3-метилфенил)метильная группа, (4-метилфенил)метильная группа, (2,3-диметилфенил)метильная группа, (2,4-диметилфенил)метильная группа, (2,5-диметилфенил)метильная группа, (2,6-диметилфенил)метильная группа, (3,4-диметилфенил)метильная группа, (4,6-диметилфенил)метильная группа, (2,3,4-триметилфенил)метильная группа, (2,3,5-триметилфенил)метильная группа, (2,3,6-триметилфенил)метильная группа, (3,4,5-триметилфенил)метильная группа, (2,4,6-триметилфенил)метильная группа, (2,3,4,5-тетраметилфенил)метильная группа, (2,3,4,6-тетраметилфенил)метильная группа, (2,3,5,6-тетраметилфенил)метильная группа, (пентаметилфенил)метильная группа, (этилфенил)метильная группа, (н-пропилфенил)метильная группа, (изопропилфенил)метильная группа, (н-бутилфенил)метильная группа, (втор-бутилфенил)метильная группа, (трет-бутилфенил)метильная группа, (н-пентилфенил)метильная группа, (неопентилфенил)метильная группа, (н-гексилфенил)метильная группа, (н-октилфенил)метильная группа, (н-децилфенил)метильная группа, (н-додецилфенил)метильная группа, (н-тетрадецилфенил)метильная группа, нафтилметильная группа или антраценилметильная группа, и предпочтительно, бензильная группа. Примером С1-С20-алкоксигруппы является метоксигруппа, этоксигруппа, н-пропоксигруппа, изопропоксигруппа, н-бутоксигруппа, втор-бутоксигруппа, трет-бутоксигруппа, н-пентоксигруппа, неопентоксигруппа, н-гексоксигруппа, н-октоксигруппа, н-додекоксигруппа, н-пентадекоксигруппа или н-эйкозоксигруппа и предпочтительно метоксигруппа, этоксигруппа, изопропоксигруппа и трет-бутоксигруппа. Примером С3-С20-алкилзамещенной или С6-С20-арилзамещенной силоксигруппы является триметилсилоксигруппа, триэтилсилоксигруппа, три-н-пропилсилоксигруппа, триизопропилсилоксигруппа, три-н-бутилсилоксигруппа, три-втор-бутилсилоксигруппа, три-трет-бутилсилокси группа, триизобутилсилоксигруппа, трет-бутилдиметилсилоксигруппа, три-н-пентилсилоксигруппа, три-н-гексилсилоксигруппа, трициклогексилсилоксигруппа или трифенилсилоксигруппа и предпочтительно триметилсилоксигруппа, трет-бутилдиметилсилоксигруппа и трифенилсилоксигруппа. Вышеупомянутые группы-заместители могут быть замещены одним или несколькими атомами галогена. Кроме того, что касается Y, примером амидогруппы или фосфидогруппы, имеющей С1-С20-углеводородную группу, является диметиламиногруппа, диэтиламиногруппа, ди-н-пропиламиногруппа, диизопропиламиногруппа, ди-н-бутиламиногруппа, ди-втор-бутиламиногруппа, ди-трет-бутиламиногруппа, диизобутиламиногруппа, трет-бутилизопропиламиногруппа, ди-н-гексиламиногруппа, ди-н-октиламиногруппа, ди-н-дециламиногруппа, дифениламиногруппа, дибензиламидогруппа, метилэтиламидогруппа, метилфениламидогруппа, бензилгексиламидогруппа, бистриметилсилиламиногруппа, или бис-трет-бутилдиметилсилиламиногруппа, или фосфидогруппа, которая замещена таким же алкилом. Среди них предпочтительными являются диметиламиногруппа, диэтиламиногруппа и дифениламидогруппа. Примером С1-С20-меркаптогруппы является метилмеркаптан, этилмеркаптан, пропилмеркаптан, изопропилмеркаптан, 1-бутилмеркаптан или изопентилмеркаптан, и предпочтительно, этилмеркаптан и изопропилмеркаптан.
В репрезентативном способе синтеза комплекса переходного металла формулы 1 замещенный или незамещенный лиганд на основе арилфеноксида получают и подвергают реакции с соединением переходного металла 4-й группы, имеющим одно циклопентадиеновое производное. Для получения замещенного или незамещенного лиганда на основе арилфенола производное анизола, которое представлено формулой 2 и замещено одним или двумя атомами галогена, и замещенную или не замещенную арилбороновую кислоту, которая показана в формуле 3, подвергают реакции с органическим фосфиновым лигандом с применением соединения металла палладия в качестве катализатора в органическом растворителе при температуре предпочтительно от -20 до 120°С с образованием арилзамещенного производного анизола, и продукт подвергают реакции с трибромборным соединением в органическом растворителе предпочтительно при температуре в диапазоне от -78 до 50°С для получения арилзамещенного феноксидного лиганда. Таким образом, полученный лиганд подвергают реакции с гидридом натрия, алкиллитием или галогенидом алкилмагния в органическом растворителе предпочтительно при температуре в диапазоне от -78 до 120°С, так чтобы превратить в анионы и затем подвергают реакции обмена лиганда с соединением переходного металла 4-й группы, которое представленно формулой 4 и имеет одно производное цикдопентадиена, при температуре от -20 до 120°С при эквивалентом отношении реагентов. Образовавшийся продукт очищают, получая при этом компонент катализатора переходного металла на основе арилфеноксида.
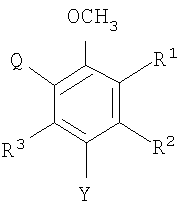
Формула 2
Формула 3
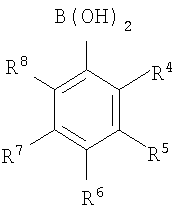
В вышеприведенной формуле 2 или 3 R1, R2, R3, R4, R5, R6, R7 и R8 представляют собой независимо атом водорода, атом галогена, разветвленную или неразветвленную С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, силильную группу, которая содержит разветвленную или неразветвленную С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, С6-С30-арильную группу, произвольно замещенную одним или несколькими атомами галогена, С7-С30-арилалкильную группу, произвольно замещенную одним или несколькими атомами галогена, С1-С20-алкилалкоксигруппу, произвольно замещенную одним или несколькими атомами галогена, или С3-С20-алкилзамещенную силоксигруппу или С6-С20-арилзамещенную силоксигруппу, необязательно с условием, что группы-заместители могут быть произвольно связаны с образованием колец; Q представляет собой атом галогена; и Y представляет собой атом водорода, атом галогена, разветвленную или неразветвленную С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, силильную группу, которая содержит неразветвленную или разветвленную С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, С6-С30-арильную группу, произвольно замещенную одним или несколькими атомами галогена, С7-С30-арилалкильную группу, произвольно замещенную одним или несколькими атомами галогена, С1-С20-алкилалкоксигруппу, произвольно замещенную одним или несколькими атомами галогена, С3-С20-алкилзамещенную силоксигруппу или С6-С20-арилзамещенную силоксигруппу, амидогруппу или фосфидогруппу, которая содержит С1-С20-углеводородную группу, или С1-С20-алкилзамещенную меркаптогруппу или нитрогруппу.
Формула 4
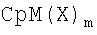
В формуле 4 Ср представляет собой циклопентадиенил, способный образовывать η5-связь вместе с центральным атомом металла, или его производное, М представляет собой переходный металл 4-й группы периодической таблицы, Х представляет собой атом галогена, С1-С20-алкильную группу, в которой нет производного Ср, С7-С30-арилалкильную группу, С1-С20-алкилалкоксигруппу, С3-С20-алкилзамещенную силоксигруппу или амидогруппу, имеющую С1-С20-угеводородную группу, и m равно 2 или 3 в зависимости от степени окисления переходного металла.
Между тем, для использования катализатора переходного металла формулы 1 в качестве активного компонента катализатора, который применяют для получения гомополимера этилена или сополимеров этилена и α-олефиновых сомономеров, Х-лиганд экстрагируют из комплекса переходного металла для превращения центрального атома металла в катионы, и алюминоксановые соединения или соединения бора, которые способны действовать как противоположные ионы, имеющие слабую связывающую способность, то есть анионы, применяют в качестве сокатализатора.
Хорошо известный в данной области техники алюминоксан, который представлен формулой 5 или 6, часто применяемый в качестве алюминоксанового соединения, применяют в настоящем изобретении.
Формула 5
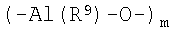
Формула 6
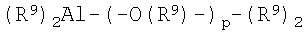
В вышеприведенных формулах R9 представляет собой С1-С20-алкильную группу и предпочтительно метильную группу или изобутильную группу, и m и р равны целым числам в диапазоне 5-20.
Для применения катализатора переходного металла настоящего изобретения в качестве активного катализатора отношение при смешивании двух компонентов устанавливают таким образом, чтобы молярное отношение центрального атома металла к атому алюминия предпочтительно было 1:20-1:10000 и более предпочтительно 1:50-1:5000.
Кроме того, соединения бора, которые можно применять в качестве сокатализатора настоящего изобретения, можно выбрать из соединений нижеследующих формул 7-9, как описано в патенте США №5198401.
Формула 7
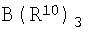
Формула 8
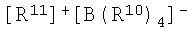
Формула 9
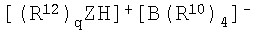
В вышеприведенных формулах В представляет собой атом бора, R10 представляет собой незамещенную фенильную группу или фенильную группу, замещенную 3-5 группами-заместителями, выбранными из группы состоящей из С1-С4-алкильной группы, которая замещена или не замещена атомом фтора, и С1-С4-алкоксигруппы, которая замещена или не замещена атомом фтора, R11 представляет собой циклический С5-С7-ароматический катион или алкилзамещенный катион, например, трифенилметильный катион, Z представляет собой атом азота или атом фосфора, R12 представляет собой С1-С4-алкильный радикал или анилиниевый радикал, который замещен двумя С1-С4-алкильными группами вместе с атомом азота, и q равно целому числу 2 или 3.
Примеры сокатализатора на основе бора включают в себя трис(пентафторфенил)боран, трис-(2,3,5,6-тетрафторфенил)боран, трис-(2,3,4,5-тетрафторфенил)боран,
трис-(3,4,5-трифторфенил)боран, трис-(2,3,4-трифторфенил)боран, фенилбис(пентафторфенил)боран, тетракис(пентафторфенил)борат, тетракис-(2,3,5,6-тетрафторфенил)борат, тетракис-(2,3,4,5-тетрафторфенил)борат, тетракис-(3,4,5-тетрафторфенил)борат, тетракис-(2,2,4-трифторфенил)борат, фенилбис(пентафторфенил)борат и тетракис-(3,5-бистрифторметилфенил)борат. Кроме того, примером комбинации вышеприведенных соединений является тетракис(пентафторфенил)борат ферроцения, тетракис(пентафторфенил)борат 1,1'-диметилферроцения, тетракис(пентафторфенил)борат серебра, трифенилметилтетракис(пентафторфенил)борат, трифенилметилтетракис-(3,5-бистрифторметилфенил)борат, тетракис(пентафторфенил)борат триэтиламмония, тетракис(пентафторфенил)борат трипропиламмония, тетракис(пентафторфенил)борат три(н-бутил)аммония, тетракис-(3,5-бистрифторметилфенил)борат три-(н-бутил)аммония, тетракис(пентафторфенил)борат N,N-диметиланилиния, тетракис(пентафторфенил)борат N,N-диэтиланилиния, тетракис(пентафторфенил)борат N,N-2,4,6-пентаметиланилиния, тетракис-(3,5-бистрифторметилфенил)борат N,N-диметиланилиния, тетракис(пентафторфенил)борат диизопропиламмония, тетракис(пентафторфенил)борат дициклогексиламмония, тетракис(пентафторфенил)борат трифенилфосфониум, тетракис(пентафторфенил)борат три(метилфенил)фосфония или тетракис(пентафторфенил)борат три(диметилфенил)фосфония и, предпочтительно, тетракис(пентафторфенил)борат N,N-диметиланилиния, тетракис(пентафторфенил)борат трифенилметилиния и трис(пентафтор)боран.
В каталитической системе, применяющей сокатализатор на основе бора, молярное отношение центрального атома металла к атому бора предпочтительно составляет 1:0,01-1:100 и более предпочтительно 1:0,5-1:5.
Между тем, если необходимо, можно применять смесь соединения бора и алюминийорганического соединения или смесь соединения бора и алюминоксанового соединения. В связи с этим соединение алюминия применяют для удаления полярных соединений, действующих в качестве каталитического яда, из растворителя для реакции, и это соединение может действовать в качестве алкилирующего агента, если Х каталитических компонентов представляет собой атом галогена.
Алюминийорганическое соединение представлено следующей формулой 10
Формула 10
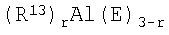
В вышеприведенной формуле R13 представляет собой С1-С8-алкильную группу, Е представляет собой атом водорода или атом галогена, и r равно целому числу в диапазоне 1-3.
Примером алюминийорганического соединения является триалкилалюминий, включающий в себя триметилалюминий, триэтилалюминий, трипропилалюминий, триизобутилалюминий и тригексилалюминий, диалкилалюминийхлорид, включающий в себя диметилалюминийхлорид, диэтилалюминийхлорид, дипропилалюминийхлорид, диизобутилалюминийхлорид и дигексилалюминийхлорид, алкиалюминийдихлорид, включающий в себя метилалюминийдихлорид, этилалюминийдихлорид, пропилалюминийдихлорид, изобутилалюминийдихлорид и гексилалюминийдихлорид, или диалкилалюминийгидрид, включающий в себя диметилалюминийгидрид, диэтилалюминийгидрид, дипропилалюминийгидрид, диизобутилалюминийгидрид и дигексилалюминийгидрид. Предпочтительным алюминийорганическим соединением является триалкилалюминий, наиболее предпочтительно триэтилалюминий и триизобутилалюминий.
В связи с этим молярное отношение центральный атом металла: атом бора: атом алюминия предпочтительно составляет 1:0,1-100:10-1000 и, более предпочтительно, 1:0,5-5:25-500.
Согласно другому аспекту настоящего изобретения в способе получения полимеров этилена с применением каталитической системы переходного металла катализатор переходного металла, сокатализатор и этилен или сомономер на основе винила контактируют друг с другом в присутствии предварительно выбранного органического растворителя. На этой стадии катализатор переходного металла и сокатализатор по отдельности загружают в реактор или их загружают в реактор после предварительного смешивания. Не имеется ограничений по условиям смешивания, таких как порядок добавления, температура или концентрация.
Примером органического растворителя, применяемого в способе, являются С3-С20-углеводороды, включающие в себя бутан, изобутан, пентан, гексан, гептан, октан, изооктан, нонан, декан, додекан, циклогексан, метилциклогексан, бензол, толуол или ксилол.
Подробно, при получении гомополимера этилена, то есть полиэтилена высокой плотности (HDPE), применяют только этилен в качестве мономера, и полимеризацию согласно настоящему изобретению проводят при давлении этилена 1-1000 атм. И, предпочтительно, 10-150 атм. Кроме того, температура реакции полимеризации составляет 80-300°С и предпочтительно 120-250°С.
Кроме того, когда получают сополимеры этилена и α-олефинов в качестве сомономеров применяют С3-С18-α-олефины вместе с этиленом, и С3-С18-α-олефины выбирают из группы, состоящей из пропилена, 1-бутена, 1-пентена, 4-метил-1-пентена, 1-гексена, 1-октена, 1-децена, 1-додецена, 1-гексадецена и 1-октадецена. Более предпочтительно, с этиленом сополимеризуют 1-бутен, 1-гексен, 1-октен или 1-децен. В связи с этим, давление этилена и температура полимеризации предпочтительно являются такими же, как в способе получения полиэтилена высокой плотности. Сополимеры этилена, полученные согласно настоящему изобретению, включают в себя 60 мас.% или более этилена, и предпочтительно, 75 мас.% этилена. Как описано выше, линейный полиэтилен низкой плотности (LLDPE), который получают с применением С4-С10-α-олефина как сомономера, имеет плотность 0,910-0,940 г/см3 и в связи с этим можно получить полиэтилен очень низкой или сверхнизкой плотности (VLDPE или ULDPE), имеющий плотность 0,910 г/см3 или меньше. Кроме того, во время получения гомополимера или сополимеров этилена согласно настоящему изобретению можно применять водород в качестве агента, регулирующего молекулярную массу, и гомополимер и сополимеры этилена обычно имеют среднюю молекулярную массу (Mw) 80000-500000.
Так как каталитическая система настоящего изобретения является гомогенной в реакторе полимеризации, она является предпочтительной для применения для способа полимеризации в растворе, которую проводят при температуре точки плавления или выше точки плавления полимера, который нужно получить. Однако, как описано в патенте США №4752597, катализатор переходного металла и сокатализатор можно нанести на носитель из пористого оксида металла, так чтобы применять в способе суспензионной полимеризации или способе газофазной полимеризации в качестве гетерогенной каталитической системы.
Способ реализации настоящего изобретения
Настоящее изобретение можно лучше понять при помощи следующих примеров, которые представлены для иллюстрации, но не должны истолковываться как ограничение настоящего изобретения.
Синтез всех лигандов и катализаторов проводили с применением стандартной методики Шленка или с применением сферического резервуара в атмосфере азота, если не описано иначе. Органические растворители, применяемые в реакциях, кипятили с обратным холодильником в присутствии металлического натрия и бензофенона для удаления влаги и перегоняли непосредственно перед их применением. Анализы 1Н ЯМР полученных лигандов и катализаторов проводили при нормальной температуре и 300 МГц на приборе Varian Oxford.
н-Гептан в качестве растворителя полимеризации пропускали через колонку, в которую загружали молекулярное сито 5А и активированный оксид алюминия, и через колонку пропускали очень чистый азот для удаления по существу всей влаги, кислорода и других ядов для катализатора перед применением растворителя. Образовавшиеся полимеры анализировали с применением следующих методов:
1. Индекс расплава (MI)
Измерение проводили на основе ASTM D 2839.
2. Плотность
Измерение проводили с применением колонки градиента плотности на основе ASTM D 2839.
3. Анализ точки плавления (Tm)
Измерение проводили с применением Dupont DSC2910 в атмосфере азота при скорости 10°C/мин в условиях 2-го нагревания.
4. Молекулярная масса и молекулярно-массовое распределение
Измерение проводили с применением прибора PL210 GPC, который оборудовали PL Mixed-BX+preCol, в растворителе 1,2,3-трихлорбензол при 135°С и скорости 1,0 мл/мин и молекулярную массу проверяли с применением стандартного материала полистирола PL.
5. Содержание α-олефина в сополимере (мас.%)
Измерение проводили с применением спектроскопа ядерного магнитного резонанса Bruker DRX500 125 МГц в смешанном растворителе 1,2,4-трихлорбензола/С6D6 (массовое отношение, 7/3) при 120°С на ядрах 13С ЯМР (Bibliography: Randal, J. С. JMS-Rev. Macromol. Chem. Phys. 1980, C29, 201).
Пример получения 1
Синтез 4-метил-2,6-бис-(2'-изопропилфенил)фенола
Смешанный раствор 1 мл воды и 4 мл диметоксиэтана добавляют в колбу, в которую уже добавили 2,6-дибром-4-метиланизол (400 мг, 1,43 ммоль), 2-изопропилфенилбороновую кислоту (720 мг, 0,23 ммоль), ацетат палладия (14 мг, 0,062 ммоль), трифенилфосфин (60 мг, 0,23 ммоль) и фосфат калия (940 мл, 4,43 ммоль), и затем смесь кипятят с обратным холодильником при нормальном давлении в течение 6 часов. После охлаждения до комнатной температуры к смеси добавляют водный раствор хлорида аммония (5 мл) и 10 мл диэтилового простого эфира для разделения органического слоя и экстракции остатков с применением диэтилового простого эфира. Отделенный органический слой сушат сульфатом аммония или летучие вещества затем удаляют, получая при этом 670 мг серого твердого 4-метил-2,5-бис-(2′-изопропилфенил)анизола. Таким образом полученный анизол растворяют в 5 мл метиленхлорида без дополнительной очистки, по каплям к раствору добавляют 3 мл трибромидабора (1 М раствор в метиленхлориде) при -78°С и реакцию проводят при медленном повышении температуры до нормальной температуры. После завершения реакции добавляют смешанный раствор воды (5 мл) и диэтилового простого эфира (10 мл) для отделения органического слоя и экстракции слоя водного раствора с применением диэтилового эфира (5 мл × 3) и отделенный органический слой сушат. Остатки, из которых летучие компоненты удаляли при пониженном давлении, очищают с применением трубки для хроматографии на силикагеле в смешанном растворителе из гексана и метиленхлорида, получая при этом 0,47 г белого твердого 4-метил-2,6-бис-(2′-изопропилфенил)фенола.
Выход: 95%, 1Н ЯМР (CDCl3) δ 1,12-1,19 (м, 12Н), 2,34 (с, 3Н), 2,93 (м, 2Н), 4,51 (с, 1Н), 6,95 (с, 2Н), 7,24 (д, 4Н), 7,42 (т, 4Н) м.д.
Синтез (дихлоро)(пентаметилциклопентадиенил)(4-метил-2,6-бис(2′-изопропилфенил)фенокси)титана(IV)
4-Метил-2,6-бис-(2′-изопропилфенил)фенол (344 мг, 1 ммоль) и гидрид натрия (72 мг, 3 ммоль) растворяют в 10 мл толуола и затем кипятят с обратным холодильником в течение 4 часов. Затем, проводят охлаждение до нормальной температуры и к полученному раствору медленно добавляют раствор (трихлоро)(пентаметилциклопентадиенил)титана(IV) (289 мг, 1 ммоль) в 5 мл толуола и смесь кипятят с обратным холодильником в течение 24 часов. После окончания реакции летучие вещества удаляют, промывку проводят с применением очищенного гексана, перекристаллизацию проводят с применением смешанного раствора толуол/гексан при -35°С, смесь фильтруют и сушку проводят при пониженном давлении, получая при этом 352 мг твердого красного продукта.
Выход: 67%, 1Н ЯМР(C6D6) δ 0,95-1,26 (м, 12Н), 1,62 (с, 15Н), 1,88 (с, 3Н), 3,17 (м, 2Н), 6,94-7,29 (м, 10Н) м.д.
Пример 1
300 мл н-гептана добавляют в реактор из нержавеющей стали, который был продут азотом, после достаточной сушки, и имел объем 500 мл, и к н-гептану добавляют 0,5 мл триизобутилалюминия (Aldrich) (200 мМ раствор в н-гептане). Температуру реактора затем повышают до 140°С и затем к смеси последовательно добавляют 0,2 мл (дихлор)(пентаметилциклопентадиенил)(4-метил-2,6-бис(2′-изопропилфенил)фенокси)
титана(IV) (5 мМ раствор в толуоле), полученного согласно примеру получения 1, и 0,3 мл трифенилметилинийтетракис(пентафторфенил)бората (99% Boulder Scientific) (5 мМ раствор в толуоле). Затем в реактор впрыскивают этилен до достижения давления в реакторе 30 атм и смесь непрерывно подают для полимеризации. Через 10 мин после начала реакции добавляют 10 мл этанола (включая 10 об.% водного раствора хлористоводородной кислоты) для завершения полимеризации, перемешивание проводят в течение 4 часов вместе с 1500 мл дополнительного этанола и продукты фильтруют и отделяют. Образовавшийся продукт сушат в вакуумном сушильном шкафу при 60°С в течение 8 часов, получая при этом 7,3 г полимера. Полимер имеет точку плавления 132,1°С и индекс расплава 0,001 г/10 мин или меньше и средневесовую молекулярную массу 393000 и молекулярно-массовое распределение 3,36, которые определяли посредством анализа гель-хроматографии.
Пример 2
15 мл 1-октена впрыскивают в реактор, который был таким же, как в примере 1, и полимеризацию затем проводили посредством такой же методике, как в примере 1, за исключением того, что 0,3 мл (дихлор)(пентаметилциклопентадиенил)(4-метил-2,6-бис(2′-изопропилфенил) фенокси)титана(IV) (5 мМ раствор в толуоле) и 0,45 мл трифенилметилинийтетракис(пентафторфенил)бората (Boulder Scientific) (5 мМ раствор в толуоле) добавляют после добавления 0,75 мл триизобутилалюминия (Aldrich) (200 мл раствор в н-гептане). Получают 4,0 г высушенного полимера. Средневесовая молекулярная масса была 175000 и молекулярно-массовое распределение было 5,91, которые определяли посредством анализа гель-хроматографией. Индекс расплава был 0,12 г/10 мин, температура плавления полимера была 114,7°С, плотность была 0,9215 и содержание 1-октена было 7,8 мас.%.
Пример получения 2
Синтез 4-метил-2-(2′-изопропилфенил)фенола
Смешанный раствор 1 мл воды и 4 мл диметоксиэтана добавляют в колбу, в которую уже добавили 2-бром-4-метиланизол (600 мг, 2,98 ммоль), 2-изопропилфенилбороновую кислоту (734 мл, 4,47 ммоль), ацетат палладия (16 мг, 0,074 ммоль), трифенилфосфин (72 мг, 0,27 ммоль) и фосфат калия (1,12 г, 5,28 ммоль), и затем смесь кипятят с обратным холодильником при нормальном давлении в течение 6 часов. После охлаждения до комнатной температуры к смеси добавляют водный раствор хлорида аммония (5 мл) и 10 мл диэтилового простого эфира для отделения органического слоя и экстракции остатков с применением диэтилового простого эфира. Отделенный органический слой сушат сульфатом аммония или летучие вещества затем удаляют, получая при этом 850 мг серого твердого 4-метил-2-(2'-изопропилфенил)анизола. Таким образом полученный анизол растворяют в 5 мл метиленхлорида без дополнительной очистки, по каплям к раствору добавляют 3 мл трибромидабора (1 М раствор в метиленхлориде) при -78°С и реакцию проводят при медленном повышении температуры до нормальной. После завершения реакции добавляют смешанный раствор воды (5 мл) и диэтилового простого эфира (10 мл) для отделения органического слоя и экстракции слоя водного раствора с применением диэтилового эфира (5 мл × 3) и отделенный органический слой сушат. Остатки, из которых летучие компоненты удаляли при пониженном давлении, очищают с применением трубки для хроматографии на силикагеле в смешанном растворителе из гексана и метиленхлорида, получая при этом 633 мг белого твердого 4-метил-2,6-(2'-изопропилфенил)фенола.
Выход: 95%, 1Н ЯМР (CDCl3) δ 1,10-1,21 (к, 6Н), 2,33 (с, 3Н), 2,91 (м, 1Н), 4,63 (с, 1Н), 6,87-7,51 (м, 7Н) м.д.
Синтез (дихлоро)(пентаметилциклопентадиенил)(4-метил-2-(2'-изопропилфенил)фенокси)титана(IV)
4-Метил-2-(2'-изопропилфенил)фенол (1 г, 4,41 ммоль) и гидрид натрия (318 мг, 13,25 ммоль) растворяют в 10 мл толуола и затем кипятят с обратным холодильником в течение 4 часов. Затем, проводят охлаждение до нормальной температуры и к полученному раствору медленно добавляют раствор (трихлоро)(пентаметилциклопентадиенил)титана(IV) (1,15 г, 4,0 ммоль) в 5 мл толуола и кипячение с обратным холодильником проводят в течение 24 часов. После окончания реакции летучие вещества удаляют, промывку проводят с применением очищенного гексана, перекристаллизацию проводят с применением смешанного раствора толуол/гексан при -35°С, смесь фильтруют и сушку проводят при пониженном давлении, получая при этом 1,53 г твердого красного продукта.
Выход: 67%, 1Н ЯМР (C6D6) δ=0,96-1,07 (м, 6Н), 1,76 (с, 15Н), 1,89 (с, 3Н), 2,99 (м, 1Н), 6,85-7,37 (м, 7Н) м.д.
Пример 3
Полимеризацию проводят посредством такого же метода, как в примере 2, за исключением того, что применяют 0,2 мл (дихлоро)(пентаметилциклопентадиенил)(4-метил-2-(2'-изопропилфенил) фенокси)титана(IV) (5 мМ раствор в толуоле), полученного согласно получению примера 2. Продукт сушат, получая при этом 5,5 г полимера. Полимер имеет точку плавления 132,1°С и индекс расплава 0,06 г/10 мин или меньше и средневесовую молекулярную массу 188000 и молекулярно-массовое распределение 4,30, которые определяли посредством анализа гель-хроматографией.
Пример получения 3
Синтез 4-метил-2,6-дифенилфенола
Смешанный раствор 1 мл воды и 4 мл диметоксиэтана добавляют в колбу, в которую уже добавили 2,6-дибром-4-метиланизол (400 мг, 1,43 ммоль), фенилбороновую кислоту (535 мл, 4,39 ммоль), ацетат палладия (14 мг, 0,062 ммоль), трифенилфосфин (60 мг, 0,23 ммоль) и фосфат калия (940 мг, 4,43 ммоль), и затем смесь кипятят с обратным холодильником при нормальном давлении в течение 6 часов. После охлаждения до комнатной температуры к смеси добавляют водный раствор хлорида аммония (5 мл) и 10 мл диэтилового простого эфира для отделения органического слоя и экстракции остатков с применением диэтилового простого эфира. Отделенный органический слой сушат сульфатом аммония или летучие вещества затем удаляют, получая при этом 420 мг серого твердого 4-метил-2,6-дифениланизола. Таким образом полученный анизол растворяют в 5 мл метиленхлорида без дополнительной очистки, по каплям к раствору добавляют 3 мл трибромидабора (1 М раствор в метиленхлориде) при -78°С и реакцию проводят при медленном повышении температуры до нормальной. После завершения реакции добавляют смешанный раствор воды (5 мл) и диэтилового простого эфира (10 мл) для отделения органического слоя и экстракции слоя водного раствора с применением диэтилового эфира (5 мл × 3) и отделенный органический слой сушат. Остатки, из которых летучие компоненты удаляли при пониженном давлении, очищают с применением трубки для хроматографии на силикагеле в смешанном растворителе из гексана и метиленхлорида, получая при этом 333 мг белого твердого 4-метил-2,6-дифенилфенола.
Выход: 89%, 1Н ЯМР (CDCl3) δ=2,36 (с, 3Н), 5,24 (с, 1Н), 7,01 (с, 2Н), 7,37 (т, 2Н), 7,47 (т, 4Н) м.д.
Синтез (дихлор)(пентаметилциклопентадиенил)(4-метил-2,6-дифенилфенокси)титана(IV)
4-Метил-2,6-дифенилфенол (400 мг, 1,53 ммоль) и гидрид натрия (110 мг, 4,60 ммоль) растворяют в 10 мл толуола и затем кипятят с обратным холодильником в течение 4 часов. Затем, проводят охлаждение до нормальной температуры и к полученному раствору медленно добавляют раствор (трихлор)(пентаметилциклопентадиенил)титана(IV) (376 мг, 1,30 ммоль) в 5 мл толуола и кипятят с обратным холодильником в течение 24 часов. После окончания реакции летучие вещества удаляют, промывку проводят с применением очищенного гексана, перекристаллизацию проводят с применением смешанного раствора толуол/гексан при -35°С, смесь фильтруют и сушку проводят при пониженном давлении, получая при этом 308 мг твердого красного продукта.
Выход: 46%, 1Н ЯМР(C6D6) δ=1,87 (с, 3Н), 1,67 (с, 15Н), 6,97-7,18 (м, 12Н) м.д.
Пример 4
Полимеризацию проводят посредством такого же метода, как в примере 2, за исключением того, что применяют 0,2 мл (дихлор)(пентаметилциклопентадиенил)(4-метил-2,6-дифенилфенокси)титана(IV) (5 мМ раствор в толуоле), полученного согласно получению примера 3. Продукт сушат, получая при этом 5,8 г полимера. Полимер имеет точку плавления 131,4°С, и индекс расплава 0,011 г/10 мин или меньше, и средневесовую молекулярную массу 349000, и молекулярно-массовое распределение 2,74, которые определяли посредством анализа гель-хроматографии.
Пример получения 4
Синтез (дихлор)(пентаметилциклопентадиенил)(2-фенилфенокси)титана(IV)
После растворения 0,86 мг 2-фенилфенола (5,07 ммоль) (Aldrich, 99%) в 40 мл толуола к раствору добавляют медленно по каплям при 0°С 2,4 мл бутиллития (2,5 М раствор в гексане). После проведения реакции при нормальной температуре в течение 12 часов раствор, в котором (трихлор)(пентаметилциклопентадиенил)титан(IV) (1,32 г, 4,56 ммоль) растворяли в 10 мл толуола, медленно по каплям добавляют в реакционный раствор при 0°С. После перемешивания, проводимого при нормальной температуре в течение 12 часов, проводили фильтрование, летучие компоненты удаляли и проводили перекристаллизацию с применением смешанного раствора толуол/гексан при -35°С, получая при этом 1,64 г твердого оранжевого продукта.
Выход: 85%, 1H-NMR (C6D6) δ=1,68 (с, 15Н), 6,82-7,26 (м, 9Н) м.д.
Пример 5
Полимеризацию проводят посредством такого же метода, как в примере 2, за исключением того, что применяют 0,2 мл (дихлор)(пентаметилциклопентадиенил)(2-фенилфенокси)титана(IV) (5 мМ раствор в толуоле), полученного согласно примеру получения 4. Продукт сушат, получая при этом 10,5 г полимера. Полимер имеет точку плавления 130,3°С, и индекс расплава 0,001 г/10 мин или меньше, и средневесовую молекулярную массу 303000, и молекулярно-массовое распределение 3,4, которые определяли посредством анализа гель-хроматографией.
Пример 6
Полимеризацию проводят посредством такого же метода, как в примере 2, за исключением того, что применяют 0,3 мл (дихлор)(пентаметилциклопентадиенил)(2-фенилфенокси)титана(IV) (5 мМ раствор в толуоле), полученного согласно примеру получения 4. 7,8 г полученного полимера сушат. Средневесовая молекулярная масса была 139000 и молекулярно-массовое распределение было 2,5, которые определяли посредством анализа гель-хроматографией. Индекс расплава был 0,2 г/10 мин или меньше и точка плавления была 118,7°С, плотность была 0,9197 и содержание 1-октена было 4,5 мас.%.
Пример получения 5
Синтез 2-изопропил-6-фенилфенола
Смешанный раствор 8 мл воды и 32 мл диметоксиэтана добавляют в колбу, в которую уже добавили 2-бром-6-изопропиланизол (1,98 г, 8,64 ммоль), фенилбороновую кислоту (2,10 г, 17,28 ммоль), ацетат палладия (96 мг, 0,43 ммоль), трифенилфосфин (0,225 г, 0,86 ммоль) и фосфат калия (11 г, 51,84 ммоль), и затем смесь кипятят с обратным холодильником при нормальном давлении в течение 12 часов. После охлаждения до комнатной температуры к смеси добавляют водный раствор хлорида аммония (15 мл) и 30 мл диэтилового простого эфира для разделения органического слоя и экстракции остатков с применением диэтилового простого эфира. Отделенный органический слой сушат сульфатом аммония, и летучие вещества затем удаляют, получая при этом 2 г серого твердого 2-изопропил-6-фениланизола. Таким образом полученный анизол растворяют в 15 мл метиленхлорида без дополнительной очистки, по каплям к раствору добавляют 12 мл трибромида бора (1 М раствор в метиленхлориде) при -78°С и реакцию проводят при медленном повышении температуры до нормальной в течение 12 часов. После завершения реакции добавляют смешанный раствор воды (15 мл) и диэтилового простого эфира (30 мл) для отделения органического слоя и экстракции слоя водного раствора с применением диэтилового эфира (5 мл × 3) и отделенный органический слой сушат. Остатки, из которых летучие компоненты удаляли при пониженном давлении, очищают с применением трубки для хроматографии на силикагеле в смешанном растворителе из гексана и метиленхлорида, получая при этом 1,72 г белого твердого 2-изопропил-6-фенилфенола.
Выход: 94%, 1H-NMR (CDCl3) δ=1,307 (д, 6Н), 3,45 (м, 1Н), 5,09 (с, 1Н), 6,95-7,43 (м, 8Н) м.д.
Синтез (дихлор)(пентаметилциклопентадиенил)(2-изопропил-6-фенилфенокси)титана(IV)
2-Изопропил-6-фенилфенол (700 мг, 3,28 ммоль) и гидрид натрия (236 мг, 9,84 ммоль) растворяют в 10 мл толуола, и затем раствор кипятят с обратным холодильником в течение 4 часов. Затем проводят охлаждение до нормальной температуры и к полученному раствору медленно добавляют раствор, в котором (трихлор)(пентаметилциклопентадиенил)титан(IV) (930 мг, 3,21 ммоль) растворен в 5 мл толуола, и кипячение с обратным холодильником проводят в течение 24 часов. После окончания реакции летучие вещества удаляют, промывку проводят с применением очищенного гексана, перекристаллизацию проводят с применением смешанного раствора толуол/гексан при -35°С, смесь фильтруют и сушку проводят при пониженном давлении, получая при этом 1,0 г твердого красного продукта.
Выход: 64%, 1H-NMR (C6D6) δ=1,324 (д, 6Н), 1,63 (с, 15Н), 3,53 (м, 1Н), 7,05-7,66 (м, 8Н) м.д.
Пример 7
Полимеризацию проводят посредством такого же метода, как в примере 2, за исключением того, что применяют 0,2 мл (дихлор)(пентаметилциклопентадиенил)(2-изопропил-6-фенилфенокси)титана(IV) (5 мМ раствор в толуоле), полученного согласно примеру получения 5. Продукт сушат, получая при этом 5,5 г полимера. Полимер имеет точку плавления 132,6°С, и индекс расплава 0,002 г/10 мин или меньше, и средневесовую молекулярную массу 390000, и молекулярно-массовое распределение 4,08, которые определяли посредством анализа гель-хроматографией.
Пример получения 6
Синтез 4-метил-2,6-бис(3′,5′-диметилфенил)фенола
Смешанный раствор 1 мл воды и 4 мл диметоксиэтана добавляют в колбу, в которую уже добавили 2,6-дибром-4-метиланизол (400 мг, 1,43 ммоль), 3,5-диметилфенилбороновую кислоту (658 мг, 4,39 ммоль), ацетат палладия (14 мг, 0,062 ммоль), трифенилфосфин (60 мг, 0,23 ммоль) и фосфат калия (940 мг, 4,43 ммоль), и затем смесь кипятят с обратным холодильником при нормальном давлении в течение 6 часов. После охлаждения до комнатной температуры к смеси добавляют водный раствор хлорида аммония (5 мл) и 10 мл диэтилового простого эфира для отделения органического слоя и экстракции остатков с применением диэтилового простого эфира. Отделенный органический слой сушат сульфатом аммония и летучие вещества удаляют, получая при этом 453 мг белого твердого 4-метил-2,6-бис-(3′,5′-диметилфенил) анизола (выход 96%). Таким образом полученный анизол растворяют в 5 мл метиленхлорида без дополнительной очистки, по каплям к раствору добавляют 3 мл трибромида бора (1 М раствор в метиленхлориде) при -78°С и реакцию проводят при медленном повышении температуры до нормальной температуры. После завершения реакции добавляют смешанный раствор воды (5 мл) и диэтилового простого эфира (10 мл) для отделения органического слоя и экстракции слоя водного раствора с применением диэтилового простого эфира (5 мл × 3) и отделенный органический слой сушат. Остатки, из которых летучие компоненты удаляли при пониженном давлении, очищают с применением трубки для хроматографии на силикагеле в смешанном растворителе из гексана и метиленхлорида, получая при этом 0,41 г белого твердого 4-метил-2,6-бис-(3′,5′-диметилфенил)фенола.
Выход: 92%, 1H-NMR (CDCl3) δ=1,55 (с, 3Н), 2,37 (с, 12Н), 5,35 (с, 1Н), 7,05 (с, 2Н), 7,15 (с, 4Н), 7,27 (4, 2Н) м.д.
Пример получения 7
Синтез 4-метил-2,6-бис-(бифенил)фенола
Смешанный раствор 1 мл воды и 4 мл диметоксиэтана добавляют в колбу, в которую уже добавили 2,6-дибром-4-метиланизола (400 мг, 1,43 ммоль), бифенилбороновую кислоту (870 мг, 4,39 ммоль), ацетат палладия (14 мг, 0,062 ммоль), трифенилфосфин (60 мг, 0,23 ммоль) и фосфат калия (940 мг, 4,43 ммоль), и затем смесь кипятят с обратным холодильником при нормальном давлении в течение 6 часов. После охлаждения до комнатной температуры к смеси добавляют водный раствор хлорида аммония (5 мл) и 10 мл диэтилового простого эфира для отделения органического слоя и экстракции остатков с применением диэтилового простого эфира. Отделенный органический слой сушат сульфатом аммония или летучие вещества затем удаляют, получая при этом 560 мг белого твердого 4-метил-2,6-бис-(бифенил)анизола (выход 95%). Таким образом полученный анизол растворяют в 5 мл метиленхлорида без дополнительной очистки, по каплям к раствору добавляют 3 мл трибромида бора (1 М раствор в метиленхлориде) при -78°С и реакцию проводят при медленном повышении температуры до нормальной температуры. После завершения реакции добавляют смешанный раствор воды (5 мл) и диэтилового простого эфира (10 мл) для отделения органического слоя и экстракции слоя водного раствора с применением диэтилового эфира (5 мл × 3) и отделенный органический слой сушат. Остатки, из которых летучие компоненты удаляли при пониженном давлении, очищают с применением трубки для хроматографии на силикагеле в смешанном растворителе из гексана и метиленхлорида, получая при этом 540 мг белого твердого 4-метил-2,6-бис-(бифенил)фенола.
Выход: 92%, 1Н-NMR (CDCl3) δ=2,39 (с, 3Н), 5,34 (с, 1Н), 7,16-7,72 (м, 20Н) м.д.
Синтез (дихлор)(пентаметилциклопентадиенил)(4-метил-2,6-бис(бифенил)фенокси)титана(IV)
4-Метил-2,6-бис-(бифенил)фенол (206 мг, 0,5 ммоль) и гидрид натрия (36 мг, 1,5 ммоль) растворяют в 10 мл толуола и затем раствор кипятят с обратным холодильником в течение 1 часа. Затем проводят охлаждение до нормальной температуры и к полученному раствору медленно добавляют (трихлор)(пентаметилциклопентадиенил)титан(IV) (130 мг, 0,45 ммоль), растворенный в 5 мл толуола, и смесь кипятят с обратным холодильником в течение 24 часов. После окончания реакции летучие вещества удаляют, промывание проводят с применением очищенного гексана, перекристаллизацию проводят с применением смешанного раствора толуол/гексан при -35°С, продукт фильтруют и сушку проводят при пониженном давлении, получая при этом 0,12 г твердого желтого продукта.
Выход: 42%, 1H-NMR (CDCl3) δ=1,60 (с, 15Н), 2,48 (с, 3Н), 7,08-8,15 (м, 20Н) м.д.
Пример получения 8
Синтез 4-метил-2,6-бис-(1′-нафтил)фенола
Смешанный раствор 1 мл воды и 4 мл диметоксиэтана добавляют в колбу, в которую уже добавили 2,6-дибром-4-метиланизол (700 мг, 2,63 ммоль), 1-нафтилбороновую кислоту (1,39 г, 8,07 ммоль), ацетат палладия (25 мг, 0,12 ммоль), трифенилфосфин (94 мг, 0,35 ммоль) и фосфат калия (1,9 г, 8,9 ммоль), и затем смесь кипятят с обратным холодильником при нормальном давлении в течение 6 часов. После охлаждения до комнатной температуры к смеси добавляют водный раствор хлорида аммония (5 мл) и 10 мл диэтилового простого эфира для отделения органического слоя и экстракции остатков с применением диэтилового простого эфира. Отделенный органический слой сушат сульфатом аммония и летучие вещества затем удаляют, получая при этом 880 мг серого твердого 4-метил-2,6-бис-(1′-нафтил)анизола (выход 89%). Таким образом полученный анизол растворяют в 10 мл метиленхлорида без дополнительной очистки, по каплям к раствору добавляют 5 мл трибромида бора (1 М раствор в метиленхлориде) при -78°С и реакцию проводят при медленном повышении температуры до нормальной температуры. После завершения реакции добавляют смешанный раствор воды (5 мл) и диэтилового простого эфира (10 мл) для отделения органического слоя и экстракции слоя водного раствора с применением диэтилового эфира (5 мл × 3) и отделенный органический слой сушат. Остатки, из которых летучие компоненты удаляли при пониженном давлении, очищают с применением трубки для хроматографии на силикагеле в смешанном растворителе из гексана и метиленхлорида, получая при этом 805 мг белого твердого 4-метил-2,6-бис-(1′-нафтил)фенола.
Выход: 85%, 1H-NMR (CDCl3) δ=2,41 (с, 3Н), 4,71 (с, 1Н), 7,21-7,92 (м, 16Н) м.д.
СРАВНИТЕЛЬНЫЙ ПРИМЕР ПОЛУЧЕНИЯ 1
Синтез (дихлор)(пентаметилциклопентадиенил)(2,6-ди-трет-бутилфенокси)титана(IV)
После растворения 600 мг 2,6-ди-трет-бутилфенола (2,91 ммоль) (Aldrich, 99%) в 30 мл диэтилового простого эфира к раствору медленно по каплям при -31°С добавляют 1,28 мл бутиллития (2,5 М раствор в гексане). Спустя 1 час перемешивание проводят при нормальной температуре в течение 6 часов. Образовавшуюся смесь растворяют в диэтиловом простом эфире и к смеси медленно по каплям при -30°С добавляют раствор (трихлор)(пентаметилциклопентадиенил)титана(IV) (752 мг, 2,60 ммоль) в 10 мл диэтилового простого эфира. Спустя 1 час перемешивание проводят при нормальной температуре в течение 6 часов. Растворитель удаляют из образовавшегося продукта и не содержащий растворитель продукт растворяют в 10 мл толуола и затем перекристаллизовывают, получая при этом 829 мг твердого красного продукта.
Выход: 69%, 1H-NMR (CDCl3) δ=1,37 (с, 18Н), 2,10 (с, 15Н), 6,50-7,20 (м, 3Н) м.д.
Сравнительный пример 1
Полимеризацию проводят посредством такого же метода, как в примере 1, за исключением того, что применяют 0,2 мл (дихлор)(пентаметилциклопентадиенил)(2,6-ди-трет-бутилфенокси)титана(IV) (5 мМ раствор в толуоле), полученного согласно примеру получения 1. Продукт сушат, получая при этом 1,4 г полимера. Полимер имеет точку плавления 133,1°С, и индекс расплава 0,25 г/10 мин или меньше, и средневесовую молекулярную массу 182000, и молекулярно-массовое распределение 5,76, которые определяли посредством анализа гель-хроматографией.
Сравнительный пример 2
Полимеризацию проводят посредством такого же метода, как в примере 2, за исключением того, что применяют 0,2 мл (триметил)(пентаметилциклопентадиенил)титана(IV) (97%, Strem) (5 мМ раствор в толуоле), 0,24 мл триизобутилалюминия (200 мМ раствор в н-гептане) (Aldrich) и 0,25 мл трифенилметилинийтетракис (пентафторфенил)бората (99%, Boulder Scientific) (5 мМ раствор в толуоле). Продукт сушат, получая при этом 3,0 г полимера. Полимер имеет точку плавления 132,0°С, и индекс расплава 0,16 г/10 мин или меньше, и средневесовую молекулярную массу 150000, и молекулярно-массовое распределение 5,47, которые определяли посредством анализа гель-хроматографией.
Сравнительный пример 3
Полимеризацию проводят посредством такого же метода, как в примере 3, за исключением того что применяют 0,4 мл (триметил)(пентаметилциклопентадиенил)титана(IV) (97%, Strem) (5 мМ раствор в толуоле), 1,0 мл триизобутилалюминия (200 мМ раствор в н-гептане)(Aldrich) и 0,6 мл трифенилметилинийтетракис (пентафторфенил)бората (99%, Boulder Scientific)(5 мМ раствор в толуоле). Получают 1,1 г высушенного полимера.
Сравнительный пример 4
Полимеризацию проводят посредством такого же метода, как в примере 1, за исключением того, что 0,2 мл рац-диметилсилилбис-(2-метилинденил)цирконийдихлорида (Boulder Scientific)(5 мМ раствор в толуоле) применяют в качестве каталитического компонента. Продукт сушат, получая при этом 25,0 г полимера. Полимер имеет точку плавления 132,5°С, и индекс расплава 4,4 г/10 мин или меньше, и средневесовую молекулярную массу 59000, и молекулярно-массовое распределение 8,9, которые определяли посредством анализа гель-хроматографией.
Сравнительный пример 5
Полимеризацию проводят посредством такого же метода, как в примере 3, за исключением того, что 0,3 мл рац-диметилсилилбис-(2-метилинденил)цирконийдихлорида (Boulder Scientific)(5 мМ раствор в толуоле) применяют в качестве каталитического компонента. Продукт сушат, получая при этом 15,0 г полимера. Полимер имеет точку плавления 123,2°С, и индекс расплава 110 г/10 мин или меньше, и средневесовую молекулярную массу 28000, и молекулярно-массовое распределение 12, которые определяли посредством анализа гель-хроматографией. Содержание 1-октена в полимере составляло 2,4 мас.%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОВРЕМЕННЫЕ КАТАЛИТИЧЕСКИЕ СИСТЕМЫ С ПЕРЕХОДНЫМ МЕТАЛЛОМ НА ОСНОВЕ ВНЕДРЕНИЯ СОМОНОМЕРА И ИСПОЛЬЗУЮЩИЕ ИХ СПОСОБЫ ПРИГОТОВЛЕНИЯ ГОМОПОЛИМЕРОВ ЭТИЛЕНА ИЛИ СОПОЛИМЕРОВ ЭТИЛЕНА И ОЛЕФИНОВ | 2011 |
|
RU2575004C2 |
| КАТАЛИТИЧЕСКИЕ СИСТЕМЫ НА ОСНОВЕ ПЕРЕХОДНЫХ МЕТАЛЛОВ И СПОСОБЫ ПОЛУЧЕНИЯ ГОМОПОЛИМЕРОВ ЭТИЛЕНА ИЛИ СОПОЛИМЕРОВ ЭТИЛЕНА И α-ОЛЕФИНОВ С ПРИМЕНЕНИЕМ ЭТИХ СИСТЕМ | 2009 |
|
RU2507210C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭЛАСТИЧНЫХ СОПОЛИМЕРОВ ЭТИЛЕНА И АЛЬФА-ОЛЕФИНОВ | 2009 |
|
RU2512536C2 |
| НОВОЕ ТЕТРААРИЛБОРАТНОЕ СОЕДИНЕНИЕ, ВКЛЮЧАЮЩАЯ ЕГО КАТАЛИТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ПОЛУЧЕНИЯ ГОМОПОЛИМЕРОВ ЭТИЛЕНА ИЛИ СОПОЛИМЕРОВ ЭТИЛЕНА И α-ОЛЕФИНА С ЕЕ ПРИМЕНЕНИЕМ | 2020 |
|
RU2801287C2 |
| ЭТИЛЕНОВЫЙ СОПОЛИМЕР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2009 |
|
RU2468039C2 |
| НОВОЕ МЕТАЛЛОЦЕНОВОЕ СОЕДИНЕНИЕ, СОДЕРЖАЩАЯ ЕГО КАТАЛИТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРОВ НА ОСНОВЕ ОЛЕФИНОВ С ЕЕ ПРИМЕНЕНИЕМ | 2012 |
|
RU2529020C2 |
| ПОЛИМЕР НА ОСНОВЕ ОЛЕФИНОВ С ИСКЛЮЧИТЕЛЬНОЙ СПОСОБНОСТЬЮ К ПЕРЕРАБОТКЕ | 2015 |
|
RU2670752C9 |
| ЭТИЛЕН/АЛЬФА-ОЛЕФИНОВЫЕ СОПОЛИМЕРЫ, ХАРАКТЕРИЗУЮЩИЕСЯ ПРЕВОСХОДНОЙ ПЕРЕРАБАТЫВАЕМОСТЬЮ | 2015 |
|
RU2671499C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОПОЛИМЕРА ЭТИЛЕН-α-ОЛЕФИНДИЕНА | 2012 |
|
RU2599626C2 |
| ВЫСОКОАКТИВНЫЙ И ВЫСОКОСЕЛЕКТИВНЫЙ КАТАЛИЗАТОР ОЛИГОМЕРИЗАЦИИ ЭТИЛЕНА И СПОСОБ ПОЛУЧЕНИЯ ГЕКСЕНА ИЛИ ОКТЕНА С ПРИМЕНЕНИЕМ ДАННОГО КАТАЛИЗАТОРА | 2010 |
|
RU2541528C2 |
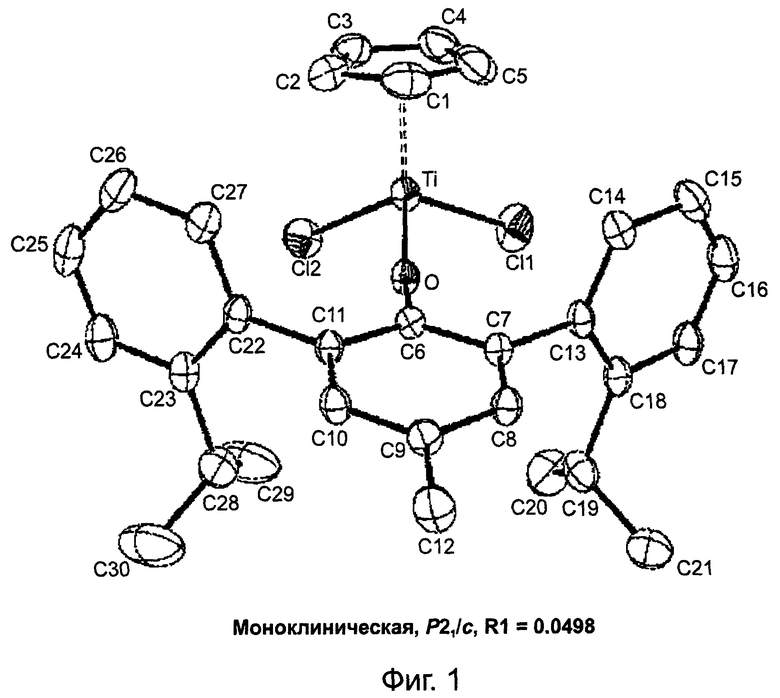
Настоящее изобретение описывает систему арилфеноксидного катализатора для получения гомополимера этилена, и сополимеров, и альфа-олефинов и способ производства гомополимера этилена, и сополимеров, и альфа-олефинов, имеющих высокую молекулярную массу при условии полимеризации раствора при высокой температуре с применением его же. Система катализатора включает катализатор на основе арилфеноксизамещенного переходного металла 4-й группы и алюминоксановый сокатализатор или сокатализатор из соединения бора. В катализаторе переходного металла производное циклопентадиена и арилфеноксид в качестве химически связанных лигандов локализованы вокруг переходного металла 4-й группы, арилфеноксидный лиганд замещен, по меньшей мере, одним арильным производным и локализован в его ортоположении и лиганды не сшиты друг с другом. Технический результат - катализатор содержит сырье, благоприятное для окружающей среды, его синтез экономичен, и его термальная стабильность превосходна. Он используется при получении гомополимера этилена и сополимеров и альфа-олефинов с разничными физическими свойствами в промышленных процессах полимеризации. 4 н. и 10 з.п. ф-лы, 2 ил.
1. Катализатор на основе арилфеноксида переходного металла, представленный формулой 1, который включает в себя производное циклопентадиена и арилфеноксид в качестве химически связанных лигандов вокруг переходного металла, причем арилфеноксид замещен, по меньшей мере, одним арильным производным, который находится в его ортоположении, и лиганды не сшиты друг с другом
формула (1)
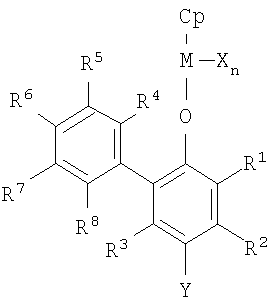
в формуле (1), М представляет собой переходный металл 4-й группы периодической таблицы;
Ср представляет собой циклопентадиеновую группу, способную образовывать η5-связь с центральным металлом, или ее производное;
R1, R2, R3, R4, R5, R6, R7 и R8 арилфеноксидного лиганда представляют собой независимо атом водорода, атом галогена, разветвленную или неразветвленную С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, силильную группу, содержащую разветвленную или неразветвленную С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, С6-С30-арильную группу произвольно замещенную одним или несколькими атомами галогена, С7-С30-арилалкильную группу, произвольно замещенную одним или несколькими атомами галогена, алкоксигруппу, которая содержит С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, или С3-С20-алкилзамещенную или С6-С20-арилзамещенную силоксигруппу и необязательно с условием, что группы-заместители могут произвольно образовывать кольца;
Х представляет собой одну или две группы, независимо выбранные из группы, состоящей из атома галогена, С1-С20-алкильной группы, которая не является производным Ср, С7-С30-арилакильной группы, алкоксигруппы, которая содержит С1-С20-алкильную группу, С3-С20-алкилзамещенную силоксигруппу и амидогруппу, которая имеет С1-С20-угеводородную группу;
Y представляет собой атом водорода, атом галогена, разветвленную или неразветвленную С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, силильную группу, которая содержит неразветвленную или разветвленную алкильную группу, произвольно замещенную одним или несколькими атомами галогена, С6-С30-арильную группу, произвольно замещенную одним или несколькими атомами галогена, С7-С30-арилалкильную группу произвольно замещенную одним или несколькими атомами галогена, алкоксигруппу, которая содержит С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, или С3-С20-алкилзамещенную или С6-С20-арилзамещенную силоксигруппу, амидогруппу или фосфидогруппу, которая содержит С1-С20 углеводородную группу, или алкилзамещенную меркаптогруппу или нитрогруппу;
n равно 1 или 2 в зависимости от степени окисления переходного металла.
2. Катализатор на основе арилфеноксида переходного металла по п.1, где М выбран из группы, состоящей из титана, циркония и гафния.
3. Катализатор на основе арилфеноксида переходного металла по п.1, где Ср представляет собой анион циклопентадиена, способный образовывать η5-связь с центральным атомом металла или его производного, причем циклопентадиенил или его производное выбрано из группы, состоящей из циклопентадиенила, метилциклопентаденила, диметилциклопентадиенила, тетраметилциклопентадиенила, пентаметилциелопентадиенила, бутилциклопентадиенила, втор-бутилциклопентадиенила, трет-бутилметилциелопентадиенила, триметилциклопентадиенила, инденила, метилинденила, диметилинденила, этилинденила, изопропилинденила, флуоренила, метилфлуоренила, диметилфлуоренила, этилфлуоренила и изопропилфлуоренила.
4. Катализатор на основе арилфеноксида переходного металла по п.1, где R1 R2, R3, R4, R5, R6, R7 и R8 арилфеноксидного лиганда независимо выбраны из группы, состоящей из атома водорода, атом галогена, метильной группы, этильной группы, изопропильной группы, трет-бутильной группы, амильной группы, триметилсилильной группы, трет-бутилдиметилсилильной группы, трифенилсилильной группы, фенильной группы, нафтильной группы, бифенильной группы, 2-изопропилфенильной группы, 3,5-ксилильной группы, 2,4,6-триметилфенильной группы, бензильной группы, метоксигруппы, этоксигруппы, изопропоксигруппы, трет-бутоксигруппы, триметилсилокси группы, трет-бутилдиметилсилоксигруппы, трифенилсилоксигруппы, трифторметилгруппы и пентафторметилгруппы.
5. Катализатор на основе арилфеноксида переходного металла по п.1, где один или несколько Х арилфеноксидного лиганда выбраны из группы, состоящей из атома галогена, метильной группы, этильной группы, изопропильной группы, трет-бутильной группы, амильной группы, бензильной группы, метоксигруппы, этоксигруппы, изопропоксигруппы, трет-бутоксигруппы, триметилсилокси группы, трет-бутилдиметилсилоксигруппы, бутилдиметилсилоксигруппы, диметиламиногруппы и диэтиламиногруппы.
6. Катализатор на основе арилфеноксида переходного металла по п.1, где Y арилфеноксидного лиганда выбран из группы, состоящей из атома водорода, атома галогена, метильной группы, этильной группы, изопропильной группы, трет-бутильной группы, амильной группы, триметилсилильной группы, трет-бутилдиметилсилильной группы, фенильной группы, нафтильной группы, бифенильной группы, 2-изопропилфенильной группы, 3,5-ксилильной группы, 2,4,6-триметилфенильной группы, бензильной группы, метоксигруппы, этоксигруппы, изопропоксигруппы, трет-бутоксигруппы, триметилсилоксигруппы, диметилсилоксигруппы, трифенилсилоксигруппы, трифторметилгруппы, пентафторфенилгруппы, диметиламиногруппы, диэтиламиногруппы, этилмеркаптангруппы, изопропилмеркаптангруппы и нитрогруппы.
7. Система арилфеноксидного катализатора для получения гомополимера этилена или сополимера этилена и α-олефина включает в себя катализатор переходного металла, который включает в себя производное циклопентадиена и арилфеноксид в качестве химически связанных лигандов вокруг атома переходного металла, причем арилфеноксид замещен, по меньшей мере, одним арильным производным, который находится в его ортоположении, и лиганды не сшиты друг с другом, и алюминоксан или соединение бора в качестве сокатализатора, где катализатор переходного металла представлен формулой (1)
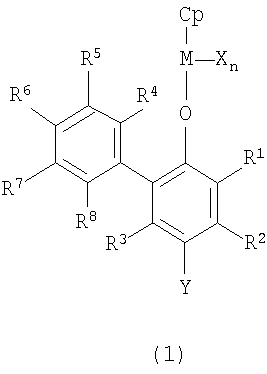
где М представляет собой переходный металл 4-й группы периодической таблицы;
Ср представляет собой циклопентадиеновую группу, способную образовывать η5-связь с центральным металлом, или ее производное;
R1, R2, R3, R4, R5, R6, R7 и R8 арилфеноксидного лиганда представляют собой независимо атом водорода, атом галогена, разветвленную или неразветвленную С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, силильную группу, содержащую разветвленную или неразветвленную С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, С6-С30-арильную группу произвольно замещенную одним или несколькими атомами галогена, С7-С30-арилалкильную группу, произвольно замещенную одним или несколькими атомами галогена, алкоксигруппу, которая содержит С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, или С3-С20-алкилзамещенную или С6-С20-арилзамещенную силоксигруппу и необязательно с условием, что группы-заместители могут произвольно образовывать кольца;
Х представляет собой одну или две группы, независимо выбранные из группы, состоящей из атома галогена, С1-С20-алкильной группы, которая не является производным Ср, С7-С30-арилакильной группы, алкоксигруппы, которая не является С1-С20-алкильной группы, С3-С20-алкилзамещенной силоксигруппы и амидогруппы, которая имеет С1-С20-угеводородную группу;
Y представляет собой атом водорода, атом галогена, разветвленную или неразветвленную С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, силильную группу, которая содержит неразветвленную или разветвленную алкильную группу, произвольно замещенную одним или несколькими атомами галогена, С6-С30-арильную группу, произвольно замещенную одним или несколькими атомами галогена, С7-С30-арилалкильную группу произвольно замещенную одним или несколькими атомами галогена, алкоксигруппу, которая содержит С1-С20-алкильную группу, произвольно замещенную одним или несколькими атомами галогена, или С3-С20-алкилзамещенную или С6-С20-арилзамещенную силоксигруппу, амидогруппу или фосфидогруппу, которая содержит С1-С20 углеводородную группу, или алкилзамещенную меркаптогруппу или нитрогруппу;
n равно 1 или 2 в зависимости от степени окисления переходного металла.
8. Система арилфеноксидного катализатора по п.7, где алюминоксановый сокатализатор предстален формулой 5 или 6 и молярное отношение центрального атома металла к алюминию составляет 1:50-1:5000
формула (5)
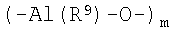
формула (6)
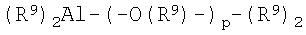
где R9 представляет собой С1-С4-алкильную группу, и каждый из m и р равен целому числу в диапазоне 5-20.
9. Система арилфеноксидного катализатора по п.7, где соединение бора в качестве сокатализатора выбрано из группы, состоящей из группы N,N-диметиланилинийтетракис(пентафторфенил)бората, трифенилметилинийтетракис(пентафторфенил)бората и трис(пентафтор) борана.
10. Система арилфеноксидного катализатора по п.7, где соединение бора в качестве сокатализатора дополнительно смешивают с алюминоксаном или органическим алкилалюминиевым соединением, так чтобы молярное отношение центральный атом металла: атом бора: атом алюминия было 1:0,5-5:25-500.
11. Система арилфеноксидного катализатора по п.10, где алюминоксан выбран из группы, состоящей из соединений, представленный формулой 5 или 6, и органическое алкилалюминиевое соединение выбрано из группы, состоящей из соединений, представленных формулой (10)
формула (5)
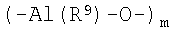
формула (6)
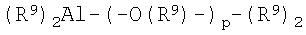
где R9 представляет собой С1-С20-алкильную группу и предпочтительно метальную группу или изобутильную группу и m и р равны целому числу в диапазоне 5-20
формула (10)
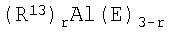
где R13 представляет собой С1-С8-алкильную группу, Е представляет собой атом водорода или атом галогена и г равно целому числу в диапазоне 1-3.
12. Система арилфеноксидного катализатора по п.11, где органическое алкилалюминиевое соединение представляет собой триэтилалюминий или триизобутилалюминий.
13. Способ получения гомополимера этилена или сополимера этилена и α-олефина с применением катализатора на основе арилфеноксида переходного металла по п.1, где давление мономеров этилена в реакционной системе составляет 10-150 атм и температура полимеризации 120-250°С.
14. Способ получения гомополимера этилена или сополимера этилена и α-олефина с применением катализатора на основе арилфеноксида переходного металла по п.7, где сомономером, который применяют для проведения полимеризации вместе с этиленом является один или несколько сомономеров, выбранных из группы, состоящей из 1-бутена, 1-гексена, 1-октена и 1-децена, и содержание этилена в сополимере составляет 60 мас.% или более.
| Чугунный экономайзер с вертикально-расположенными трубами с поперечными ребрами | 1911 |
|
SU1978A1 |
| Шеститрубный элемент пароперегревателя в жаровых трубках | 1918 |
|
SU1977A1 |
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| Металлический водоудерживающий щит висячей системы | 1922 |
|
SU1999A1 |
| КОМПОНЕНТ КАТАЛИЗАТОРА, КАТАЛИЗАТОР ПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ (ВАРИАНТЫ), СПОСОБ ПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ | 1996 |
|
RU2156260C2 |
Авторы
Даты
2009-11-27—Публикация
2005-10-14—Подача