Изобретение относится к медицине, а именно к реконструктивной хирургии, и может быть использовано при реконструкции костных структур различных типов и размеров путем замещения костных дефектов биоинертными керамическими материалами.
Известен способ костно-реконструктивного лечения нижней челюсти у детей (RU №2201159), включающий костно-реконструктивное лечение с использованием имплантата, выполненного из пористой керамики. К причинам, по которым использование известного способа не приводит к техническим результатам заявляемого изобретения, можно отнести следующие:
- применение известного способа ограничено рамками, указанными в названии изобретения;
- использование в качестве имплантата пористого керамического материала, выполненного в виде монолитного блока, невозможно при необходимости моделирования костного дефекта сложной конфигурации.
Известен также способ внедрения дентальных имплантатов (RU 2176489), заключающийся в том, что костную пластику осуществляют с помощью аллотрансплантата в виде двух слоев деминерализованного костного матрикса с помещенным между ними измельченным матриксом в комбинации с гидроксиапатитом. К причинам, по которым использование известного способа не приводит к техническим результатам заявляемого изобретения, можно отнести следующие:
- применение аллогенного трансплантата (чужеродная ткань) сопряжено с высоким риском иммунных реакций отторжения и инфицирования,
- невозможность применения при реконструкции сложных костных дефектов, требующих адекватного моделирования,
- технические трудности фиксации имплантата из за различной структуры используемых материалов.
Наиболее близким способом того же назначения является способ герметизации и пластики дефекта основания черепа (RU №2174825), включающий пластику дефекта твердой мозговой оболочки и костного дефекта основания черепа. При этом в качестве трансплантата твердой мозговой оболочки используют широкую фасцию бедра, а костный дефект основания черепа закрывают конгруэнтным аутотрансплантатом или имплантатом из гидроксиапатита. Принят в качестве прототипа. Однако известный способ обладает рядом недостатков, препятствующих достижению указанных ниже лечебных результатов, а именно:
- невозможность изоляции структур головного мозга от прямого контакта с гранулами гидроксиапатита при сквозных костных дефектах основания черепа,
- свободное размещение гранул гидроксиапатита не помещенных в «контейнер» не обеспечивает стабильного положения гранул в операционной полости и, следовательно, адекватного замещения костного дефекта и выполнения опорной функции утраченных костных структур,
- возможные затруднения при фиксации трасплантата к окружающим тканям.
Заявляемое изобретение направлено на решение задачи реконструкции костных структур различных типов и размеров, в том числе - основания черепа, челюстно-лицевой зоны и опорно-двигательной системы путем замещения костных дефектов биоинертными керамическими материалами.
Использование в клинической практике заявляемого способа позволяет достичь нескольких технических (лечебных) результатов:
- восстановление каркасной функции,
- предотвращение реакции отторжения;
- возможность моделирования имплантата в соответствии с размером и формой имеющегося дефекта;
- изоляция жизненно важных органов,
- улучшение косметических результатов.
Указанные технические (лечебные) результаты при осуществлении изобретения достигаются за счет того, что также как в известном способе осуществляют замещение костного дефекта с помощью гидроксиапатита. Особенность заявляемого способа заключается в том, что в костном дефекте размещают биологический контейнер, сформированный из свободного апоневротического лоскута, выкроенного из широчайшей фасции бедра, заполненный гранулированным пористым гидроксиапатитом.
Сущность изобретения заключается в следующем.
Использование в качестве имплантируемого материала для замещения костных дефектов пористых биоинертных биокерамических материалов, в частности гранул гидроксиапатита, обеспечивает биологическую активность имплантируемого материала, а именно: высокие адгезивные свойства по отношению к клеткам, сочетание свойств остеокондуктивности и остеоиндуктивности, регулируемость скорости растворения при замещении костной тканью, неоваскуляризацию, способность поддерживать пролиферацию и дифференцировку клеток из окружающей живой ткани, скорость резорбции, сравнимую со скоростью образования костной ткани. Однако до сегодняшнего дня является проблемой осуществление моделирования имплантата в соответствии с размером и формой имеющегося дефекта. Особенно это касается костных структур различных типов и размеров, в том числе - основания черепа, челюстно-лицевой зоны и опорно-двигательной системы.
Авторами заявляемого изобретения разработан метод такого индивидуального моделирования. Из широчайшей фасции бедра выкраивают свободный апоневротический лоскут, из которого формируют биологический контейнер и заполняют его пористыми гранулами гидроксиапатита с размером пор от 200 до 600 мкм. Использование гранул с указанным размером пор является оптимальными, т.к. размер пор менее 200 мкм не позволяет обеспечить адекватное проникновение в гранулы биологических потоков и остеогенных клеток, а наличие пор более 600 мкм резко уменьшает прочностные характеристики гранул. Затем готовый контейнер размещают в костном дефекте. Использование в качестве стенки контейнера аутологичной ткани - фрагмента широчайшей фасции бедра, предотвращает реакцию отторжения. Гистологическая структура ткани обеспечивает высокую пластичность «биологического контейнера» при достаточной прочности ткани, проницаемость для биологических сред организма, а также возможность трехмерного равномерного заполнения костного дефекта, то есть позволяет осуществлять индивидуальное моделирование составного имплантата. В процессе регенерации костной ткани с помощью «биологического контейнера», заполненного пористыми гранулами гидроксиапатита, достигается адекватная интеграция трансплантата.
При этом формирование апоневротического лоскута из широчайшей фасции бедра не сопровождено с обширной хирургической травмой и не ведет к функциональным нарушениям конечности.
Способ осуществляют следующим образом.
По латеральной поверхности бедра на границе верхней и средней трети производят линейный разрез кожи и подкожной клетчатки. Подкожную клетчатку широко отсепаровывают от широчайшей фасции бедра и разводят крючками, создавая окно для дальнейших манипуляций. Широчайшую фасцию бедра рассекают по средней линии и отсепаровывают от подлежащих мышц в латеральном направлении и отсекают по задней поверхности бедра. Донорскую рану на бедре ушивают послойно с дренированием мягких тканей. Далее из полученного свободного апоневротического лоскута моделируют контейнер в соответствии с формой и размером дефекта реконструируемых тканей посредством наложения шва по периферии контура, оставляя небольшое окно. Через неушитую часть контейнер заполняют гранулированным пористым гидроксиапатитом в объеме, необходимом для замещения костного дефекта, и ушивают наглухо. Сформированный имплантат переносят в область дефекта костных тканей челюстно-лицевой зоны, черепа или опорно-двигательной системы и фиксируют узловыми швами к окружающим тканям и дополнительно укрывают покровными тканями.
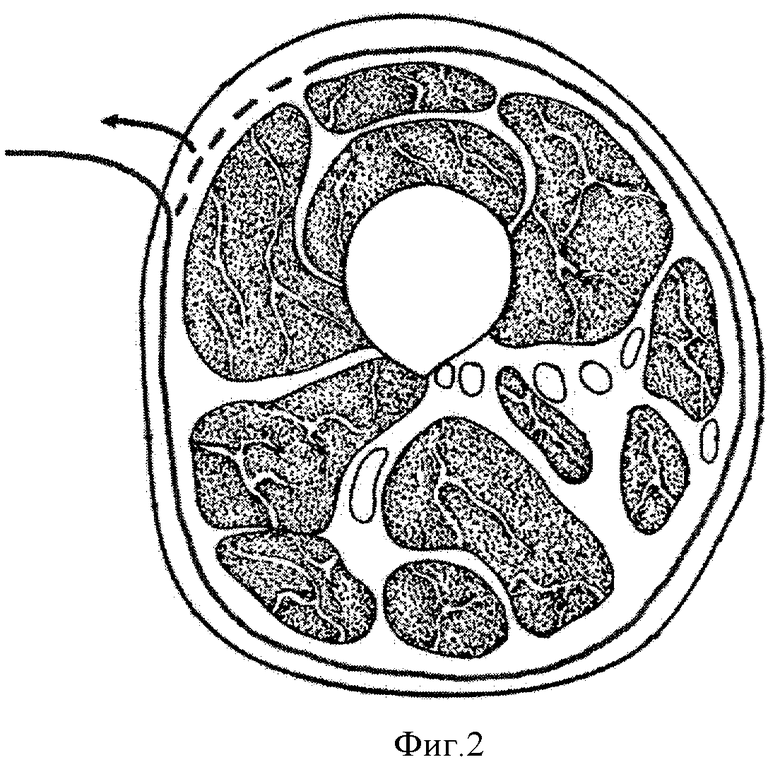
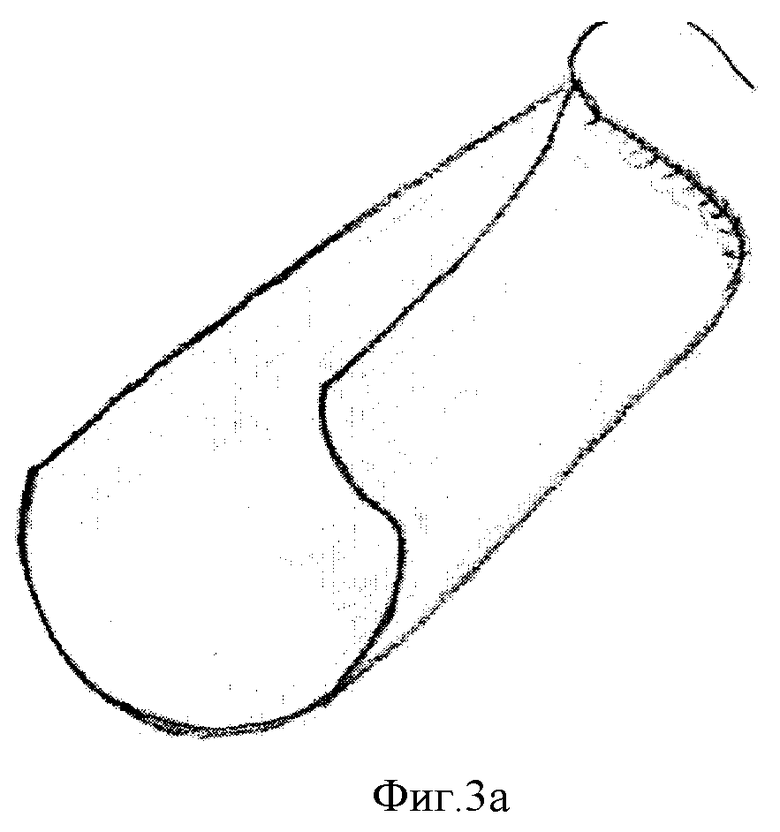
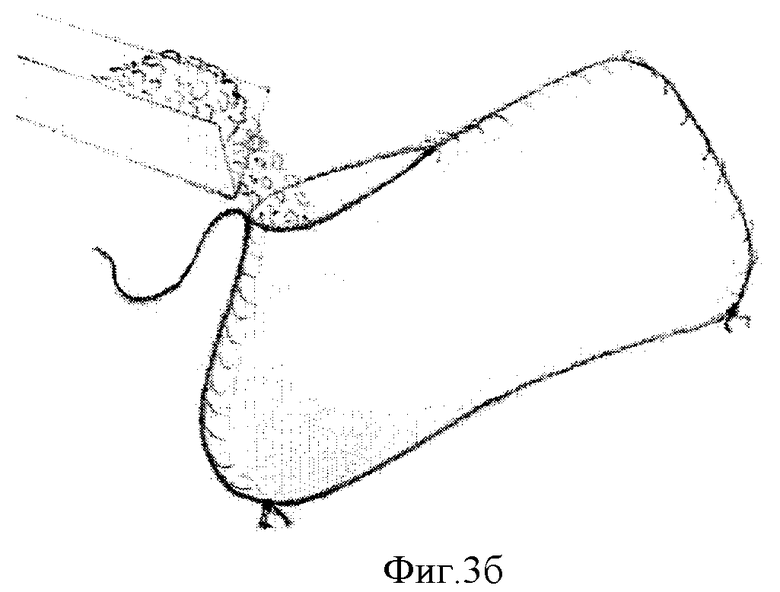
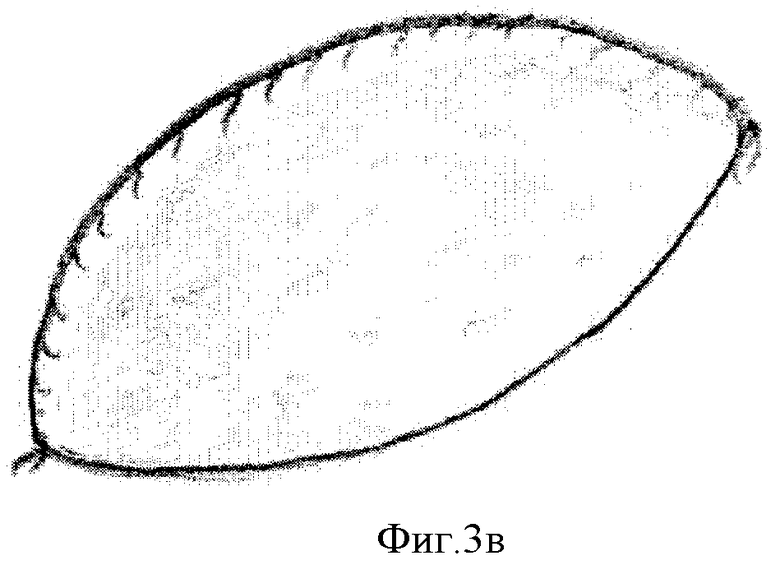
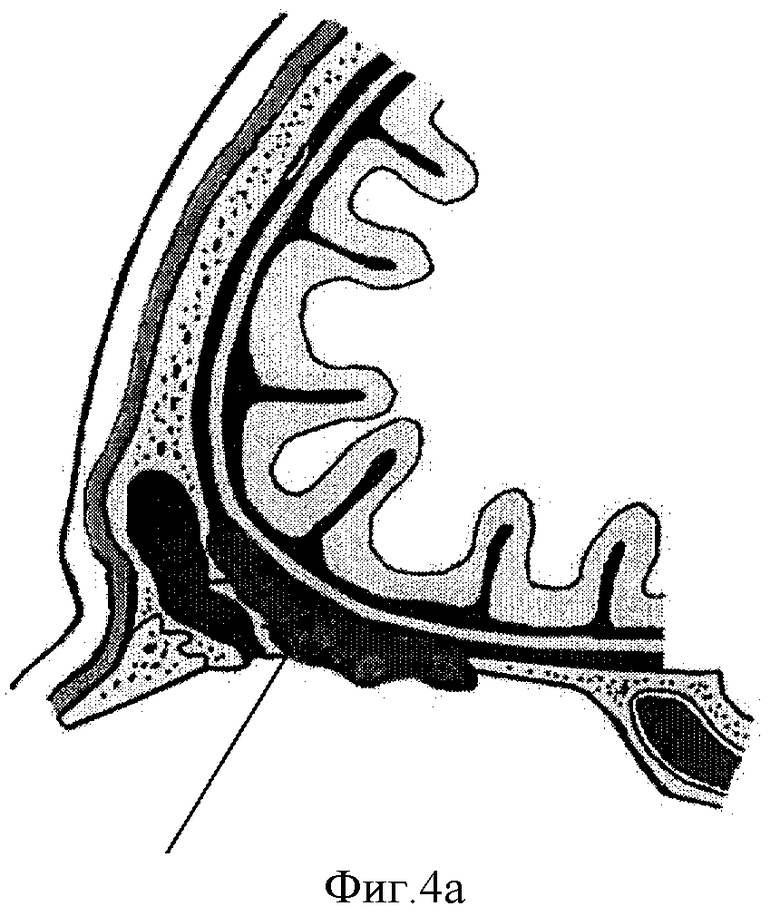
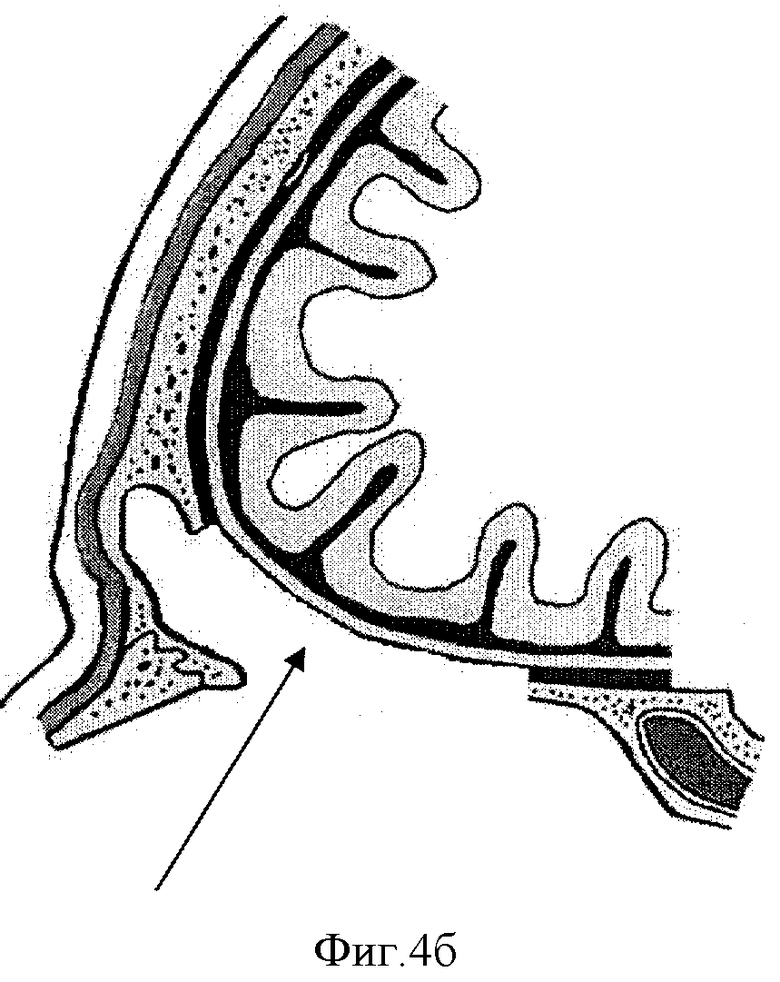
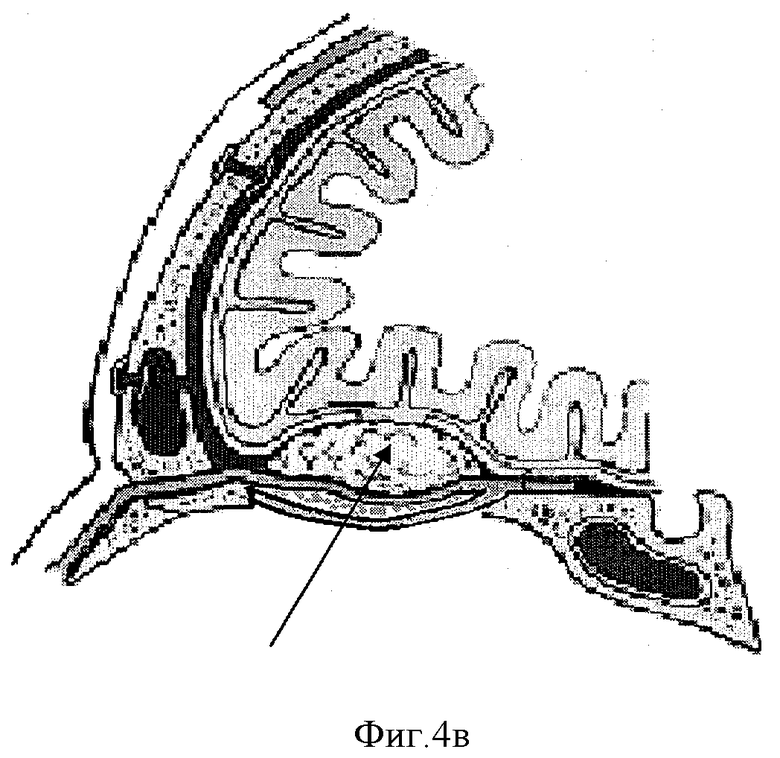
Схема изготовления составного имплантата представлена на Фиг.1-4. На Фиг.1 представлен кожный разрез по передней поверхности бедра с отсепаровкой кожи, на Фиг.2 - мобилизация широчайшей фасции бедра, на Фиг.3а-3в - формирование «контейнера» из широчайшей фасции бедра: Фиг.3а - сшивание лепестков фасции, 3б - заполнение «контейнера» гранулами гидроксиапатита, 3в - ушивание «контейнера» наглухо. На Фиг.4а-4в представлена схема размещения «контейнера» с гранулами в костном дефекте: Фиг.4а - схема поражения опухолью основания черепа (стрелкой указана опухоль), Фиг.4б - операционный дефект (стрелкой указан дефект основания черепа), Фиг.4в - схема замещения костного дефекта основания черепа (стрелкой указан «контейнер с гранулами гидроксиапатита»).
Примеры выполнения.
1. Замещение костного дефекта основания черепа.
Больной П., 45 лет, диагноз: Рак решетчатого лабиринта T4N0Mo. Состояние после нерадикального хирургического лечения в сентябре 2003 года. Остаточная опухоль. Состояние после курса предоперационной лучевой терапии в декабре 2003 года СОД - 36 Гр. Состояние после хирургического лечения в 10 февраля 2004 года в объеме краниофациальной резекции.
Из анамнеза: больным себя считает с марта 2003 года, когда отметил появление заложенности носа, ввиду присоединившихся кровянистых выделений из носа в сентябре 2003 года обследован в О.Д. г.Липецк, выполнена резекция носовой перегородки и удаление «полипа» полости носа. Гистологически - злокачественное образование, в связи с чем направлен в МНИОИ им. П.А.Герцена.
С 02.12.03 года по 30.12.03 - проведен курс ДЛТ на область опухолевого поражения РОД - 2 Гр до СОД - 36 Гр. Вторым этапом комбинированного лечения 10.02.2004 года больному выполнена операция: Видеоассистированная краниофациальная резекция, возмещение костного дефекта гранулами гидроксиапатита, пластика свободным апоневротическим лоскутом. Операционный доступ к опухоли решетчатого лабиринта осуществлен двойным доступом: бикоронарным и трансназальным. После мобилизации и удаления опухоли решетчатого лабиринта сформирован свободный апоневротический лоскут из широчайшей фасции бедра левой нижней конечности. Рана на мягких тканях левой нижней конечности ушита послойно с активным дренированием. Из свободного апоневротического лоскута сформирован «контейнер» заполненный гранулами гидроксиапатита, который помещен в область резецированных тканей основания черепа и фиксирован узловыми швами к окружающими тканями. Дополнительно операционная рана укрыта ротированными тканями скальпа. Послеоперационный период протекал без осложнений. Донорская рана на левой нижней конечности зажила первичным натяжением, дренаж удален на 3-й сутки после операции. Больной активизирован, нарушения опорной функции конечности не отмечено. Заживление операционной раны головы без осложнений, дыхание через верхние дыхательные пути не затруднено, питание через рот в полном объеме. При обследовании через 1 год без данных за местный рецидив. Больной в настоящее время находится под динамическим наблюдением. Социально адаптирован.
2. Замещение дефекта рукоятки грудины.
Больной К., 47 лет. Диагноз: хондросаркома рукоятки грудины IA стадии, T1N0M0G1.
Из анамнеза: в октябре 2003 г при обследовании по месту жительства выявлена саркома грудины, в связи с чем направлен в МНИОИ им. П.А.Герцена.
05.01.04 г выполнена операция: Резекция грудины с послойной реконструкцией. Произведена медиастинотомия на уровне III реберно-грудинного сочленения с обеих сторон. На этом уровне выполнена остеотомия грудины. Поэтапно пересечены II и III ребра с обеих сторон кнаружи от краев грудины на 2-3 см. Препарат удален, дефект грудины составил 11·7 см. Выполнена послойная реконструкция грудины с использованием контейнера из широкой фасции правого бедра с гранулами гидроксиапатита. Произведено послойное ушивание раны. Левая большая грудная мышца мобилизована на сосудистой ножке, ротирована и фиксирована в проекции передней стенки грудины. Операционная рана ушита послойно наглухо с активным дренированием. Течение послеоперационного периода гладкое, без осложнений. При контрольном обследовании через 1 год без данных за рецидив. Больной социально адаптирован, вернулся к активной трудовой деятельности.
Заявляемый способ обладает значительными преимуществами и отвечает критериям патентоспособности.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОФИЛАКТИКИ ТРАВМАТИЧЕСКИХ ПОВРЕЖДЕНИЙ ДЛИННЫХ ТРУБЧАТЫХ КОСТЕЙ | 2014 |
|
RU2574139C1 |
| Способ восстановления циркулярных дефектов диафиза кости | 2016 |
|
RU2614888C1 |
| СПОСОБ ПЛАСТИКИ КОСТНОГО ДЕФЕКТА ОСНОВАНИЯ ЧЕРЕПА | 2019 |
|
RU2722406C1 |
| СПОСОБ РЕКОНСТРУКЦИИ ОБШИРНЫХ ДЕФЕКТОВ ДНА ПЕРЕДНЕЙ ЧЕРЕПНОЙ ЯМКИ | 2014 |
|
RU2570619C1 |
| Способ реконструкции основания передней черепной ямки при выполнении блок-резекции распространенной опухоли переднего отдела основания черепа | 2019 |
|
RU2730955C1 |
| СПОСОБ КОСТНОЙ ПЛАСТИКИ АЛЬВЕОЛЯРНОГО ОТРОСТКА ВЕРХНЕЙ ЧЕЛЮСТИ И АЛЬВЕОЛЯРНОЙ ЧАСТИ НИЖНЕЙ ЧЕЛЮСТИ | 2017 |
|
RU2661039C1 |
| СПОСОБ УСКОРЕНИЯ РЕГЕНЕРАЦИИ КОСТНОЙ ТКАНИ ПРИ ПРОВЕДЕНИИ ОСТЕОСИНТЕЗА | 2009 |
|
RU2410050C2 |
| СПОСОБ ПЛАСТИКИ ОБШИРНЫХ ПОСТРЕЗЕКЦИОННЫХ ОКОНЧАТЫХ ДЕФЕКТОВ СТЕНОК ГРУДНОЙ КЛЕТКИ И/ИЛИ СВОДА ЧЕРЕПА | 2009 |
|
RU2393808C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ИМПЛАНТАТА ДЛЯ ЗАМЕЩЕНИЯ ДЕФЕКТОВ КОСТЕЙ ЧЕРЕПА ПРИ ГРУБЫХ КОСМЕТИЧЕСКИХ ДЕФЕКТАХ В ВИСОЧНОЙ ОБЛАСТИ И ИМПЛАНТАТ ДЛЯ ЗАМЕЩЕНИЯ ДЕФЕКТОВ КОСТЕЙ ЧЕРЕПА ПРИ ГРУБЫХ КОСМЕТИЧЕСКИХ ДЕФЕКТАХ В ВИСОЧНОЙ ОБЛАСТИ | 2020 |
|
RU2740567C1 |
| СПОСОБ УСТРАНЕНИЯ КОМБИНИРОВАННЫХ ДЕФЕКТОВ ВЕРХНЕЙ ЧЕЛЮСТИ С ИСПОЛЬЗОВАНИЕМ ИНДИВИДУАЛЬНОГО ЭНДОПРОТЕЗА | 2024 |
|
RU2831787C1 |

Изобретение относится к травматологии и ортопедии и может быть применимо для замещения костных дефектов. Размещают в костном дефекте биологический контейнер, сформированный из свободного апоневротического лоскута, выкроенного из широчайшей фасции бедра, заполненный гранулированным пористым гидроксиапатитом. В частном случае размер пор гранулированного гидроксиапатита составляет от 200 до 600 мкм. Способ позволяет восстановить каркасную функцию, моделировать трансплантат по размеру дефекта. 1 з.п. ф-лы, 8 ил.
1. Способ замещения костного дефекта с помощью гидроксиапатита, отличающийся тем, что в костном дефекте размещают биологический контейнер, сформированный из свободного апоневротического лоскута, выкроенного из широчайшей фасции бедра, заполненный гранулированным пористым гидроксиапатитом.
2. Способ по п.1, отличающийся тем, что размер пор гранулированного гидроксиапатита составляет от 200 до 600 мкм.
| СПОСОБ ЛЕЧЕНИЯ ОСКОЛЬЧАТЫХ ПЕРЕЛОМОВ ДЛИННЫХ ТРУБЧАТЫХ КОСТЕЙ | 2003 |
|
RU2253393C1 |
| US 7371410, 13.05.2008 | |||
| Способ исправления пайкой сломанных алюминиевых предметов | 1921 |
|
SU223A1 |
| Способ сужения чугунных изделий | 1922 |
|
SU38A1 |
| Клозетный промывной бак | 1928 |
|
SU11758A1 |
| БАГРАТАШВИЛИ В.Н | |||
| и др | |||
| Синтез новых минерал-полимерных композитов для имплантологии | |||
Авторы
Даты
2009-12-10—Публикация
2008-09-23—Подача