Настоящее изобретение относится к способу производства пероксида водорода посредством реагирования (химического взаимодействия) органического медиатора на катоде с образованием восстановленного медиатора и реагирования этого восстановленного медиатора с кислородом с образованием пероксида водорода.
Наиболее распространенный способ промышленного производства пероксида водорода представляет собой антрахиноновый способ, включающий в себя поочередное гидрирование и окисление антрахинонов и/или тетрагидроантрахинонов в рабочем растворе. Хотя он и очень эффективный, этот способ является сложным в работе и требует разнообразного оборудования. До сих пор не было предложено конкурентоспособных альтернативных способов для крупномасштабного производства пероксида водорода.
Электрохимическое производство щелочного раствора пероксида водорода посредством восстановления кислорода на катоде описывается, например, в патенте США 6322690.
Электрохимическое производство щелочного раствора пероксида водорода посредством восстановления кислорода на катоде и одновременное получение хлората натрия описано в работе E. E. Kalu и C. Oloman. "Simultaneous electrosynthesis of alkaline hydrogen peroxide and sodium chlorate", Journal of Applied Electrochemistry 20 (1990), 932-940.
E.L. Gyenge и C.W. Oloman описывают в работах "Electrosynthesis hydrogen peroxide and acid solutions by mediated oxygen reduction in three-phase (aqueous/organic/gaseous) system Part I: Emulsion structure, electrode kinetics and batch electrolysis", Journal of Applied Electrochemistry (2003), 33(8), 655-663, и "Electrosynthesis hydrogen peroxide and in acid solutions by mediated oxygen reduction in three-phase (aqueous/organic/gaseous) system. Part II: Experiments in flow-by fixed-bed electrochemical cells with three-phase flow", Journal of Applied Electrochemistry (2003), 33(8), 665-674, производство пероксида водорода посредством электровосстановления 2-этил-9,10-антрахинона до соответствующего антрагидрохинона, растворенного в органической фазе, эмульгированной в воде. Антрагидрохинон подвергается реакции с газообразным кислородом с получением пероксида водорода.
Патент США 4515664 описывает способ электролитического образования пероксида водорода в электролитической ячейке с твердым полимерным электролитом.
Патент Японии JP 61-284591 и патент США 4067787 описывают производство пероксида водорода посредством восстановления водорастворимого производного антрахинона в водном растворе с последующей реакцией с кислородом.
A. Huissoud и P. Tissot описывают в "Electrochemical reduction of 2-ethyl-9,10-anthraquinone on reticulated vitreous carbon and mediated formation hydrogen peroxide", Journal of Applied Electrochemistry (1998), 28(6), 653-657, электрохимическое восстановление 2-этил-9,10-антрахинона в диметоксиэтане, содержащем 5% воды и 0,1 моль/литр тетрафторбората тетраэтиламмония.
Электрохимическое восстановление кислорода на углеродном катоде с привитым антрахиноном описывается, например, в WO 02/02846, Mirkhalaf, Fakhradin; Tammeveski, Kaido; Schiffrin, David J., "Substituent effects on electrocatalytic reduction of oxygen on quinone-modified glassy carbon electrodes", Phys. Chem.Chem.Phys.(2004), 6(6), 1321-1327, и Vaik, Katri; Schiffrin, David J.; Tammeveski, Kaido; "Electrochemical reduction of oxygen on anodically pre-treated and chemically grafted glassy carbon electrodes in alkaline solutions", Electrochemistry Communications (2004), 6(1), 1-5.
Vaik, Katri; Sarapuu, Ave; Tammeveski, Kaido; Mirkhalaf, Fakhradin; Schiffrin, David J. в "Oxygen reduction on phenanthrenequinone-modified glassy carbon electrodes in 0,1 M KOH", Journal of Electroanalytical Chemistry (2004), 564(1-2), 159-166, описывают использование катода с привитым фенантренхиноном.
WO 03/004727 описывает электросинтез органических соединений посредством электрохимического превращения соединения в присутствии электролита, содержащего ионную жидкость комнатной температуры, и извлечения продукта.
Задачей изобретения является создание способа производства пероксида водорода, который может осуществляться на сравнительно простом оборудовании.
Другой задачей изобретения является создание способа производства пероксида водорода, включающего в себя электрохимическое восстановление медиатора.
Еще одной задачей изобретения является создание способа производства пероксида водорода посредством опосредованного (непрямого) электрохимического восстановления кислорода без необходимости в контактировании катода с газообразным кислородом.
В соответствии с изобретением было найдено, что возможно решить эти задачи в способе производства пероксида водорода, включающем в себя:
обеспечение электрохимической ячейки, содержащей анод и катод;
контактирование катода с электролитом, содержащим по меньшей мере один органический медиатор, растворенный в по меньшей мере частично органической сплошной жидкой фазе, содержащей по меньшей мере частично органическую соль и нейтральный сорастворитель, причем упомянутая соль содержит по меньшей мере один вид органического катиона и/или органического аниона, упомянутая сплошная жидкая фаза имеет электропроводность при условиях способа по меньшей мере примерно 0,1 Cм/м, более предпочтительно по меньшей мере примерно 1 Cм/м, наиболее предпочтительно по меньшей мере примерно 3 Cм/м;
реагирование органического медиатора на катоде с образованием по меньшей мере одной восстановленной формы этого медиатора;
реагирование упомянутой по меньшей мере одной восстановленной формы медиатора с кислородом с образованием пероксида водорода.
Органический медиатор представляет собой вещество, способное электрохимически реагировать на катоде с образованием одной или нескольких восстановленных форм, которые в свою очередь способны реагировать с предпочтительно молекулярным кислородом и преобразовываться обратно в свою исходную форму, тем самым делая возможным циклический процесс. Реакция восстановленных форм медиатора с кислородом предпочтительно происходит в присутствии протонов. Однако в отсутствие подходящего источника протона является возможным образование пероксидных солей, например Na2O2, которые впоследствии могут быть гидролизованы с получением пероксида водорода. Не ограничиваясь какой-либо теорией, предполагается, что схема реакции образования пероксида водорода включает в себя перенос двух электронов и двух протонов, происходящий в отдельных или комбинированных одновременных реакциях, и предполагается вовлечение в качестве промежуточных частиц O2 -·, HOO-· и HOO-.
Примеры классов органических веществ, формирующих окислительно-восстановительные системы и пригодных в качестве медиаторов, включают в себя хиноны, флавохиноны, производные пиридина, такие как никотинамиды, и кетоны.
Пригодные для использования хиноны включают молекулы, содержащие (бензо)хиноновый фрагмент (орто- или пара-формы), среди которых антрахиноны, тетрагидроантрахиноны, нафтохиноны, бензохиноны и их производные являются предпочтительными. Антрахиноны, нафтохиноны и бензохиноны предпочтительно являются замещенными, например алкилзамещенными, подобно 2-алкил-9,10-антрахинонам. Конкретные примеры включают в себя 2-этил-9,10-антрахинон, 2-трет-бутил-9,10-антрахинон, 2-гексенил-9,10-антрахинон, эвтектические смеси алкил-9,10-антрахинонов, смеси 2-амил-9,10-антрахинонов, все они имеют высокую стабильность. Конкретные примеры алкилзамещенных нафтохинонов включают в себя 2-метил-1,4-нафтохинон, 2-этил-1,4-нафтохинон, 2-пропил-1,4-нафтохинон, 2-трет-бутил-1,4-нафтохинон, 2-трет-амил-1,4-нафтохинон, 2-изо-амил-1,4-нафтохинон, 2,3-диметил-1,4-нафтохинон. Другие примеры заместителей, пригодных для управления реакционной способностью и растворимостью хинонов, включают в себя -SO3H/-SO3 -, -PO2R-, -OPO3R-, -NO2, -OCH3, -SO2CH3, -OPh, -SPh, -SO2Ph, -COOH/-COO-, -CN, -OH, -COCH3, -F, -Cl, -Br, -CF3, -NH2/-NH3 +, -NRH/-NRH2 +, -NR2/-NR2H+, -NR3 +, -PH2/-NH3 +, -SR2 +, -PRH/-PRH2 +, -PR2/-PR2H+ и -PR3 +, R предпочтительно представляют собой независимо друг от друга необязательно замещенный алкил, алкенил, арил или водород. Антрахинон может быть одно- или многозамещенным некоторым сочетанием вышеуказанных и/или других заместителей. Также является возможным использовать производные хинона с несущими общий заряд заместителями, придающими молекуле ионный характер. Конкретные примеры замещенных не алкилами производных хинона включают в себя антрахинон-2-сульфонат, 5,6,7,8-тетрагидро-9-10-антрахинон-2-сульфонат, антрахинон-2,6-дисульфонат, нафтохинон-2-сульфонат, 2-метокси-1,4-нафтохинон, 2-этокси-1,4-нафтохинон, 2-амино-антрахинон, 2-амино-нафтохинон, 2-(алкиламино)-антрахинон, 2-(диалкиламино)-антрахинон, 2-(триалкиламмоний)-антрахинон, 2-(алкиламино)-нафтохинон, 2-(диалкиламино)-нафтохинон, 2-(триалкиламмоний)-нафтохинон. Нафтохиноны могут, например, быть замещенными в любом положении на боковом кольце, например нафтохинон-6-сульфонат или 6-триалкиламмонийнафтохинон. Также может быть выгодным один заместитель на каждом кольце, например 6-амил-нафтохинон-2-сульфонат или 6-этил-2-триэтиламмонийнафтохинон. Соответствующими примерами для бензохинона являются бензохинон-2-сульфонат и 2-(этил,диметил)аммоний. Также могут быть использованы антрахиноны и нафтохиноны с частично гидрированными боковыми кольцами, например 1,2,3,4-тетрагидроантрахинон, 5,6,7,8-тетрагидро-2-этил-антрахинон, 5,6,7,8-тетрагидронафтохинон. Это также применимо к замещенным антра- и нафтохинонам, включая те, которые соответствуют указанным выше типам.
В случае когда хинон является замещенным и содержит одну или более необязательно замещенную алкильную, алкенильную или арильную группы, является предпочтительным, чтобы эти группы независимо друг от друга имели от 1 до 12 атомов углерода, наиболее предпочтительно от 1 до 8 атомов углерода. Если присутствует более чем одна такая группа, то они предпочтительно имеют смешанную длину цепей. Алкильная, алкенильная и арильная группы также могут быть замещенными, например, одной или более гидроксильной группой.
Хиноны, включая антрахиноны, тетрагидроантрахиноны, нафтохиноны, бензохиноны и их производные, могут быть восстановлены до соответствующих гидрохинонов посредством последовательного присоединения двух электронов и двух протонов. Наряду с хиноном и гидрохиноном, как предполагается, присутствует и является активным ряд промежуточных форм, подобных семихиноновому радикалу и семихиноновому аниону, а также основные формы кислого гидрохинона. Все эти восстановленные формы могут реагировать с кислородом и вносить вклад в общую реакцию, давая пероксид водорода и исходный хинон.
Другие медиаторные системы, способные восстанавливать кислород до супероксида и впоследствии пероксида водорода, включают в себя флавохиноны, например флавин (см., например, H. Tatsumi и др. в работе "Mechanistic study of autooxidation of reduced flavin and quinone compounds", Journal of Electroanalytical Chemistry (1998), 443, 236-242), и производные пиридина, подобные никотинамиду, и их производные.
Другие медиаторные системы образуются кетонами и соответствующими им спиртами. Кетон может электрохимически восстанавливаться до соответствующего спирта, который реагирует с кислородом с образованием пероксида водорода и исходного кетона. Предпочтительными являются вторичные спирты и в особенности фенильные. Пригодные для использования спирты включают в себя изопропиловый спирт, бензиловый спирт, дифенилметанол, метилфенилметанол. Также могут использоваться вторичные спирты, дополнительно содержащие несущую заряд группу.
Содержание органического медиатора, включая его восстановленные формы, в по меньшей мере частично органической сплошной жидкой фазе предпочтительно составляет по меньшей мере примерно 0,1 мас.%, более предпочтительно по меньшей мере примерно 1 мас.%, наиболее предпочтительно по меньшей мере примерно 3 мас.%. Оно ограничивается сверху только растворимостью, которая зависит от используемого медиатора и состава жидкой фазы, но во многих случаях может достигать примерно 10 мас.%, или примерно 20 мас.%, или даже более. В том варианте осуществления, где значительная часть пероксида водорода образуется вне ячейки, содержание органического медиатора предпочтительно составляет по меньшей мере примерно 1 мас.%, более предпочтительно по меньшей мере примерно 3 мас.%, наиболее предпочтительно по меньшей мере примерно 10 мас.%.
По меньшей мере частично органическая сплошная жидкая фаза предпочтительно содержит по меньшей мере примерно 20 мас.%, более предпочтительно по меньшей мере примерно 50 мас.%, наиболее предпочтительно по меньшей мере примерно 80 мас.% органических компонентов и в крайних случаях может по существу не содержать неорганических компонентов. Однако является предпочтительным, чтобы содержалось по меньшей мере примерно 5 мас.%, наиболее предпочтительно по меньшей мере примерно 20 мас.% неорганических компонентов. Такие неорганические компоненты могут, например, представлять собой неорганические ионы солей, образованных как органическими, так и неорганическими ионами.
По меньшей мере частично органическая сплошная жидкая фаза содержит по меньшей мере частично органическую соль, содержащую по меньшей мере один вид органического катиона и/или органического аниона. Ее содержание в сплошной жидкой фазе предпочтительно составляет от примерно 20 мас.% до примерно 99 мас.%, более предпочтительно от примерно 40 мас.% до примерно 95 мас.%, наиболее предпочтительно от примерно 60 мас.% до примерно 90 мас.%.
По меньшей мере частично органическая сплошная жидкая фаза содержит нейтральный сорастворитель, такой как вода или низкомолекулярный спирт, подобный метанолу, этанолу, пропанолу или их смесям, среди которых вода является предпочтительной. Его содержание предпочтительно составляет вплоть до примерно 50 мас.%, наиболее предпочтительно от примерно 1 до примерно 20 мас.%. Особенно предпочтительное содержание может, например, составлять от примерно 1 до примерно 5 мас.% или от примерно 5 до примерно 10 мас.%.
По меньшей мере частично органическая соль может выбираться из группы солей, именуемых ионными жидкостями, т.е. широкого класса жидкостей, состоящих по существу из ионов. Ионная жидкость может быть простой и содержать один вид анионов и один вид катионов или же может быть сложной и содержать смесь различных анионов и/или различных катионов. Некоторые ионные жидкости имеют низкую температуру плавления и пренебрежимо малое давление паров вблизи или ниже комнатной температуры и часто называются ионными жидкостями комнатной температуры. Такие ионные жидкости обычно остаются жидкими в широком диапазоне температур.
По меньшей мере частично органическая соль может также выбираться из солей, которые сами по себе не классифицируются как ионные жидкости, но имеют такие свойства, когда присутствуют вместе с нейтральным сорастворителем, таким как вода или низкомолекулярный спирт, подобный метанолу, этанолу или пропанолу. Массовое отношение соли к сорастворителю предпочтительно составляет от примерно 1:1 до примерно 1000:1, более предпочтительно от примерно 2:1 до примерно 100:1, наиболее предпочтительно от примерно 5:1 до примерно 20:1.
Является предпочтительным использовать такую по меньшей мере частично органическую соль, которая сама по себе или в сочетании с нейтральным сорастворителем образует жидкую фазу при атмосферном давлении ниже примерно 130°C, предпочтительно ниже примерно 100°C, наиболее предпочтительно ниже примерно 80°C. Кроме того, парциальное давление этой соли при 100°C предпочтительно составляет ниже примерно 10 кПа, более предпочтительно ниже примерно 1 кПа, наиболее предпочтительно ниже 0,1 кПа (исключая парциальное давление необязательного нейтрального сорастворителя).
Жидкость с подходящими физическими свойствами может содержать одну по меньшей мере частично органическую соль или смесь двух или более по меньшей мере частично органических солей в сочетании с нейтральными сорастворителями. Она также может содержать анионы и катионы, которые сами не образуют солей с подходящими свойствами.
По меньшей мере частично органическая соль может быть образована из различных сочетаний катионов и анионов, среди которых по меньшей мере один вид ионов является органическим. Эти ионы предпочтительно являются одновалентными. Примеры катионов включают в себя 1-алкил-3-метилимидазолий, 1-бутил-3-метилимидазолий [BMIM], 1-этил-3-метилимидазолий [EMIM], 1,2,3-триметилимидазолий, н-алкилпиридиний, н-бутилпиридиний [BPY], пирролидиний, гуанидиний и алкилгуанидиний, изоуроний, PR4 +, NPR4 +, SR3 +, тетраметиламмоний, холин, кокомоний и их смеси, R предпочтительно представляют собой независимо друг от друга необязательно замещенный алкил, алкенил, арил или водород. Другие примеры включают в себя замещенные хиноны, обозначаемые здесь [Q-NR3 +] и [Q-PR3 +], где Q означает хинон, такой как антрахинон, нафтохинон или бензохиноны, а R является таким же, как выше. Примеры анионов включают в себя гексафторфосфат [HFP], тетрафторборат [TFB], фторсульфонат, гексафторантимонат гексафторарсенат, хлоралюминат, бромалюминат, бис(трифторметилсульфонил)имид, трис(трифторметилсульфонил)метид, трицианометид, дицианамид, нонафторбутансульфонат, трифторметансульфонат, 2,2,2-трифторэтансульфонат, нитрат, сульфат, фосфат, RPO4 2-, R2PO4 -, R2PO2 - (например, диалкилфосфинат), перхлорат, ацетат, алкилсульфонат, бис(2-этилгексил)натрия сульфосукцинат, диэтиленгликольмонометилэфирсульфат, алкилолигоэфирсульфат, пивалат, тетраалкилборат, пропионат, сукцинат, сахаринат, гликолят, стеарат, лактат, малат, тартрат, цитрат, аскорбат, глютамат, бензоат, салицилат, метансульфонат, толуолсульфонат и их смеси, R является таким же, как и выше. Другие примеры включают в себя замещенные хиноны, обозначаемые здесь [Q-(O)-SO3 -] и [Q-(O)-PO3R-], где Q означает хинон, такой как антрахинон, нафтохинон или бензохиноны, (O) обозначает необязательный кислород (например, сульфат/сульфонат и фосфат/фосфонат), а R является таким же, как и выше.
В случае когда любой катион или анион содержит одну или более необязательно замещенную алкильную, алкенильную или арильную группы, является предпочтительным, чтобы эти группы независимо друг от друга имели от 1 до 12 атомов углерода, наиболее предпочтительно от 1 до 8 атомов углерода. Если присутствует более чем одна такая группа, то они предпочтительно имеют смешанную длину цепей. Алкильная, алкенильная и арильная группы также могут быть замещенными, например, одной или более гидроксильной группой.
Примеры солей, пригодных для настоящего изобретения, включают в себя любую комбинацию следующих катионов: [1,3-диалкилимидазолий], [триалкиламмоний], [тетраалкиламмоний], [триалкилфосфоний], [тетраалкилфосфоний], [алкилпиридиний], [холин], [Q-NR3 +] и [Q-PR3 +], в сочетании с любым из следующих анионов: [сульфат], [фосфат], [алкилсульфат], [алкилсульфонат], [диалкилфосфат], [алкилфосфонат], [Q-(O)-SO3 -] и [Q-(O)-PO3R-], где Q, (O) и R определены так же, как и выше.
Конкретные комбинации групп включают в себя [1,3-диалкилимидазолий][алкилсульфонат], такой как любая из следующих: [1-бутил-3-метилимидазолий][метил-SO3 -], [1-этил-3-метилимидазолий][этилсульфонат], [1-гексил-3-метилимидазолий][тозилат], [1-бутил-3-метилимидазолий][антрахинон-2-сульфонат] или [1-бутил-3-метилимидазолий][5-трет-амилнафтохинон-2-сульфонат]; [тетраалкиламмоний][Q-(O)-SO3 -], такие как любой из следующих: [метил,триэтиламмоний], [5-трет-амил-нафтохинон-2-сульфонат], [метил,диэтил,бутиламмоний][антрахинон-2-сульфонат] или [холин][5-амил-бензохинон-2-сульфонат]; или [Q-NR3 +][алкилсульфонат], такой как [5,6,7,8-тетрагидроантрахинон-2-аминий, н,н,н-(метил,диэтил)][метилсульфонат]; [тетраалкилфосфоний][диалкилфосфат], такой как любой из следующих: [этилтрибутилфосфоний][диэтилфосфат], [фенилтриэтилфосфоний][диизобутилфосфат].
Не ограничиваясь конкретными комбинациями групп, возможно множество комбинаций, таких как любая из следующих: [триизобутил(метил)фосфоний][тозилат], тригексил(тетрадецил)фосфоний][бис-2,4,4-триметилпентилфосфинат] [тетрабутиламмоний][метансульфонат][1-этил-3-метилимидазолий] [HFP], [трипентилсульфоний][дипентил,бензиламмоний], [бензохинон-2-аминий-н,н,н-диэтил,фенил][5,6,7,8-тетрагидро-9,10-антрахинон-2-сульфонат], [холин][5-этокси-1,4-нафтохинон-6-сульфат], [н-пропилпиридиний][сахаринат].
В дополнение к упомянутым выше могут использоваться также и другие виды имеющихся в продаже или известных иным образом ионных жидкостей или солей, имеющих такие свойства в сочетании с нейтральным сорастворителем.
Может также быть возможным использование соли, где по меньшей мере один из ионов также действует в качестве медиатора, который подвергается реакции на катоде до получения восстановленной формы и таким образом принимает участие в циклическом процессе получения пероксида водорода. В этом случае используемый медиатор может частично или полностью состоять из ионов такой соли. Примеры включают в себя соли, содержащие катион или анион замещенного хинона или производного никотинамида, такого как те, которые упомянуты выше.
Использование по меньшей мере частично органической соли, как описано выше, в сплошной фазе электролита обеспечивает преимущества комбинирования высокой растворимости органических медиаторов, подобных хинонам, с хорошей электропроводностью. Другим преимуществом является очень низкая воспламеняемость, дающая возможность безопасно осуществлять реакцию с кислородом при более высоких концентрациях кислорода и при более высокой температуре, чем было бы возможно в случае обычных воспламеняющихся растворителей. Также является простым отделение пероксида водорода от них, например, посредством выпаривания или экстракции и тем самым получение пероксида водорода либо высокой чистоты, либо в подлежащей дальнейшей переработке смеси с выбранным соединением, например с водой. Другой пример представляет собой смесь метанол/пероксид водорода для использования в качестве реагента в реакции эпоксидирования. Использование ионных жидкостей для образования среды, пригодной для осуществления реакций с участием пероксида водорода, было описано в работе B. Chhikara et al. "Oxidation of alcohols with hydrogen peroxide catalyzed by new imidazolium ion based phosphotungstate complex in ionic liquid", Journal of Catalysis 230 (2005, 436-439).
По меньшей мере частично органическая сплошная жидкая фаза электролита может также содержать дополнительные компоненты. Примеры включают в себя одну или более органическую или неорганическую кислоты, подобные муравьиной кислоте, уксусной кислоте, монохлоруксусной кислоте, бензойной кислоте, сульфоновым кислотам, фосфоновым кислотам, азотной кислоте, серной кислоте, хлористоводородной кислоте, йодистоводородной кислоте, бромистоводородной кислоте, перхлорной кислоте или фосфорной кислоте. Примеры других необязательных добавок включают в себя стабилизаторы пероксида водорода, эмульгаторы, ингибиторы коррозии, противовспениватели, буферы, усилители проводимости, понизители вязкости и тому подобное. Примеры стабилизаторов пероксида водорода включают те, которые широко используются, такие как фосфорная кислота, комплексообразующие агенты на основе фосфоновой кислоты, защитные коллоиды, подобные станнату щелочного металла, и поглотители радикалов, подобные пиридинкарбоновым кислотам. Примеры комплексообразующих агентов на основе фосфоновой кислоты включают в себя 1-гидроксиэтилиден-1,1-дифосфоновую кислоту, 1-аминоэтан-1,1-дифосфоновую кислоту, аминотри(метиленфосфоновую кислоту), этилендиаминтетра(метиленфосфоновую кислоту), гексаметилендиаминтетра(метиленфосфоновую кислоту), диэтилентриаминпента(метиленфосфоновую кислоту), диэтилентриамингекса(метиленфосфоновую кислоту), 1-аминоалкан-1,1-дифосфоновые кислоты (такие как морфолинметандифосфоновая кислота, н,н-диметиламинодиметилдифосфоновая кислота, аминометилдифосфоновая кислота), продукты их реакций и их соли, предпочтительно натриевые соли.
Является предпочтительным, чтобы по меньшей мере частично органическая жидкая фаза имела вязкость при рабочих условиях ниже примерно 100 мПа·с, более предпочтительно ниже примерно 30 мПа·с, а наиболее предпочтительно ниже примерно 10 мПа·с. Кроме того, из-за опасностей, связанных с обращением с по существу чистым пероксидом водорода, извлеченный продукт предпочтительно представляет собой смесь пероксида водорода с водой или низкомолекулярными спиртами, например метанолом. Парциальное давление при 100°C жидких компонентов, которые не составляют часть смеси-продукта, предпочтительно должно быть ниже примерно 10 кПа, более предпочтительно ниже примерно 1 кПа, наиболее предпочтительно ниже 0,1 кПа.
Электрохимическая ячейка может содержать одну единственную камеру для анода и катода или может быть разделенной (диафрагменной) и содержащей отдельные анодную и катодную камеры необязательно с одной или несколькими камерами в промежутке между ними, например электродиализный пакет, делающий возможным осуществление любого известного электродиализа. Средство для разделения этих камер может представлять собой неселективный физический барьер, например пористую мембрану или диафрагму, или же оно может быть селективно проницаемым для определенных частиц, таких как катионы или анионы. Также может использоваться сочетание мембран, такое как биполярные мембраны, позволяющие разделять воду на протоны и гидроксид-ионы. Неселективные барьеры могут, например, изготавливаться из асбеста, керамики, стекла, полиолефинов, политетрафторэтилена (ПТФЭ), поливинилхлорида (ПВХ) и тому подобного. Катионселективные мембраны могут, например, изготавливаться из органических полимеров, таких как ПТФЭ, полистирол, стирол/дивинилбензол или винилпиридин/дивинилбензол, модифицированный кислотными группами, подобными сульфонату, карбоксилату или фосфонату. Анионселективные мембраны могут, например, изготавливаться из органических полимеров, таких как ПТФЭ, полистирол, стирол/дивинилбензол или винилпиридин/дивинилбензол, модифицированный основными группами, подобными четвертичному аммонию. Биполярные мембраны могут содержать проницаемую для анионов мембрану и проницаемую для катионов мембрану, наслоенные вместе, необязательно со слоем катализатора между ними. Ионселективные и биполярные мембраны имеются в продаже, например, под товарными знаками Nafion™, Flemium™, Neosepta bipolar®.
Электролит в катодной камере или ячейке, если не имеется отдельной катодной камеры, может содержать одну, две или более жидких фаз. В системе с одной жидкой фазой имеется только по меньшей мере частично органическая жидкая фаза электролита, хотя неорганические частицы могут включаться в нее до той степени, в которой они растворимы в ней. В системе с двумя жидкими фазами имеется также преимущественно водная фаза, которая может быть эмульгирована или просто смешана в сплошной по меньшей мере частично органической жидкой фазе. Если имеется более чем одна жидкая фаза, то компоненты в электролите будут распределяться между этими фазами в зависимости от их свойств растворимости. В дополнение к жидкой фазе или фазам может также присутствовать газ и/или твердые вещества.
Если используется ячейка с одной единственной камерой, то один и тот же электролит, как правило, вступает в контакт как с анодом, так и с катодом. Чтобы дать возможность электролитам с различным составом вступать в контакт с анодом и катодом, может использоваться разделенная ячейка. Однако это также может достигаться без какого-либо физического барьера в ячейке посредством использования таких составов анолита и католита, которые образуют отдельные жидкие фазы, и необязательно используя разность плотностей для образования различных слоев, контактирующих соответственно с анодом и катодом. Является также возможным использовать различия в свойствах смачивания для образования водного слоя на гидрофильной поверхности анода и органического слоя на гидрофобной поверхности катода. Поверхности электродов могут быть целенаправленно модифицированы для создания подходящих условий смачивания. Для предотвращения медленного растворения жидкой пленки может быть преимущественным обеспечение того, что соседняя жидкая фаза является насыщенной компонентами жидкой фазы, составляющей эту пленку. Одним из способов обеспечения этого является создание эмульсии этой второй фазы. Химическая прививка молекул к поверхности представляет собой второй способ управления составом вблизи поверхности электрода.
В электролите, контактирующем с анодом, по меньшей мере один компонент окисляется. Имеется несколько возможных вариантов осуществления, которые могут выбираться посредством выбора состава электролита и материала анода.
В одном варианте осуществления, пригодном как для однокамерных ячеек, так и для разделенных ячеек, вода подвергается реакции на аноде с образованием кислорода и протонов. Кислород и образовавшиеся протоны могут использоваться при реакции с восстановленным медиатором с образованием пероксида водорода. Если ячейка является разделенной, то анолит предпочтительно содержит раствор NaOH или KOH. pH предпочтительно выше примерно 7, например от примерно 8 до примерно 14. Предпочтительно температура составляет от примерно 20 до примерно 100°C, наиболее предпочтительно от примерно 30 до примерно 90°C.
В другом варианте осуществления, наиболее пригодном для разделенной ячейки, электролит в контакте с анодом содержит хлорид-ионы, которые подвергаются реакции на аноде с образованием хлора. Образовавшийся хлор может выделяться как таковой или гидролизоваться в воде с образованием хлорноватистой кислоты, которая может подвергаться реакции далее с образованием хлората. Анолит предпочтительно содержит раствор NaCl или KCl, возможно, в сочетании с соответствующими хлоратами, NaClO3 или KClO3. Если pH составляет ниже примерно 4, то преобладающий продукт представляет собой Cl2. При более высоком pH образовавшийся Cl2 гидролизуется и образуется хлорноватистая кислота. pH от примерно 4 до примерно 10 в объеме анолита является предпочтительным для получения хлората щелочного металла, такого как хлорат натрия, который, таким образом, может быть получен одновременно с пероксидом водорода. Предпочтительно температура составляет от примерно 20 до примерно 100°C, наиболее предпочтительно от примерно 40 до примерно 90°C.
Еще в одном варианте осуществления, наиболее пригодном для разделенной ячейки, серная кислота, бисульфат или сульфат щелочного металла или аммония в электролите подвергается электролизу на аноде до кислоты Каро, пероксомоносерной кислоты H2SO5, или пероксодисерной кислоты, H2S2O8, или соответствующей пероксосоли. Эти вещества могут использоваться как таковые, например, при выщелачивании или гидролизоваться в воде с получением пероксида водорода и серной кислоты или соответствующей соли щелочного металла. Анолит предпочтительно содержит водный раствор сульфата. pH зависит от выбора катиона, если это H+, то pH предпочтительно составляет ниже примерно 3, если это NH4 +, то pH предпочтительно составляет от примерно 4 до примерно 9, если это щелочной металл типа Na+, то pH может быть выше примерно 8.
В еще одном варианте осуществления, наиболее пригодном для разделенной ячейки, карбоновая кислота или ее соль окисляется в присутствии воды с получением соответствующей перкислоты и протонов. Возможные карбоновые кислоты включают в себя муравьиную кислоту, уксусные кислоты, пропионовую кислоту и бензойную кислоту. Анолит предпочтительно содержит водный раствор карбоновой кислоты, подобной перуксусной кислоте, при pH предпочтительно между 3 и 8 или соль щелочного металла, подобную ацетату калия или натрия, при pH между 8 и 12.
Еще в одном варианте осуществления, наиболее пригодном для разделенной ячейки, метанол или другое органическое вещество, подобное этанолу, формальдегиду, природному газу, используется в анолите предпочтительно в смеси с водой и окисляется с получением, главным образом, диоксида углерода и протонов. Эта анодная реакция как таковая является хорошо известной и используется в метанольных топливных элементах прямого действия, и она вносит вклад в уменьшение напряжения ячейки и тем самым общего потребления электроэнергии. Анолит предпочтительно содержит смесь метанола и воды, и pH предпочтительно составляет от примерно 1 до примерно 7.
Еще в одном варианте осуществления, наиболее пригодном для разделенной ячейки, водород окисляется на аноде, предпочтительно газодиффузионном электроде, в присутствии воды с получением протонов, которые могут переноситься к катоду через проницаемую для катионов мембрану. Также и эта реакция известна для топливных элементов и вносит вклад в уменьшение количества электрической энергии, необходимой для проведения общих реакций. Анолит предпочтительно содержит фосфорную кислоту и предпочтительно имеет pH от примерно 1 до примерно 6.
Еще в одном варианте осуществления для разделения анодной и катодной камер используется биполярная мембрана, обеспечивающая расщепление воды. Гидроксид, образующийся внутри такой мембраны, переносится в анодную камеру, в то время как образующиеся протоны переносятся в катодную камеру, где они могут реагировать с образованием пероксида водорода или любой из восстановленных форм участвующего в процессе медиатора, например гидрохинона, или любых из промежуточных форм такого медиатора. На аноде может протекать любая реакция, включая те, которые указаны выше, например с анолитом, содержащим любой из NaOH, KOH или NH3 и имеющим предпочтительный pH от примерно 8 до примерно 14 или содержащим хлорид-ионы и имеющим предпочтительный pH от примерно 5,5 до примерно 8. Одна возможная реакция представляет собой окисление водорода на газодиффузионном электроде в анолите, предпочтительно содержащем KOH и предпочтительно имеющем pH от примерно 8 до примерно 14.
В рамках настоящего изобретения также являются возможными и другие анодные реакции, такие как разрушение различных продуктов отходов, электрохимическое окисление белого щелока (сульфатной варочной жидкости) с получением, например, полисульфидов или диоксида серы, опосредованное окисление антрацена до антрахинона или нафталина до нафтохинона, например, с использованием окислительно-восстановительных пар Cr(III)/Cr(VI) или Ce(III)/Ce(IV) или электролиз слабого черного щелока, например, с генерированием кислорода.
В такой ячейке температура и давление предпочтительно задают так, что электролит представляет собой жидкость. Высокая температура способствует низкой вязкости, высокой электропроводности и высоким скоростям массопереноса, в то время как низкая температура способствует стабильности пероксида водорода и компонентов в электролите. Как правило, температура предпочтительно составляет от примерно 0 до примерно 200°C, более предпочтительно от примерно 40 до примерно 150°C, наиболее предпочтительно от примерно 60 до примерно 100°C. Давление предпочтительно составляет от примерно 10 до примерно 30000 кПа, более предпочтительно от примерно 80 до примерно 2000 кПа, наиболее предпочтительно от примерно 100 до примерно 800 кПа. Если ячейка содержит более чем одну камеру, то условия в разных камерах могут быть одинаковыми или различными, хотя является предпочтительным работать в указанных выше пределах во всех камерах ячейки.
Реакция одной или более восстановленных форм медиатора и кислорода с получением пероксида водорода может происходить внутри ячейки, или в отдельной емкости, или в сочетании их обеих, приводя к образованию пероксида водорода в по меньшей мере частично органической фазе электролита и повторному образованию медиатора для участия в другом реакционном цикле. Как правило, к электролиту, содержащему восстановленный медиатор, добавляют молекулярный кислород, но часть его может происходить от кислорода, образовавшегося в ходе анодных реакций и перенесенного через электролит в ячейке необязательно через мембрану или выделенного в виде отдельного потока и повторно введенного в ячейку. Молекулярный кислород может быть добавлен растворенным в жидкости или в виде любого кислородсодержащего газа, такого как воздух, обогащенный кислородом воздух или по существу чистый кислород. Добавление по меньшей мере части кислорода в виде газа непосредственно в ячейку обеспечивает преимущество улучшения перемешивания, а также может создавать газ-лифт для переноса электролита из ячейки, альтернативно вносить вклад в отгонку пероксида водорода из электролита. Добавление кислорода непосредственно в ячейку может сделать возможным завершение полного каталитического цикла медиатора внутри ячейки, по существу устраняя необходимость выводить поток, содержащий восстановленную форму медиатора, и подавать поток, содержащий медиатор. Реакции получения пероксида водорода облегчаются за счет присутствия протонов, которые могут происходить из любого доступного источника, такого как вода, гидрохинон, протоны, образующиеся на аноде, или любая кислота, которая была добавлена к электролиту. Если реакция с кислородом происходит в отдельной емкости, условия в ней, подобные температуре, давлению и т.д., могут быть теми же самыми, как и те, которые преобладают в ячейке, или отличающимися от них. Температура предпочтительно находится в пределах температуры окружающей среды, например примерно 20°C, до верхнего предела, определяемого либо воспламеняемостью растворителя, либо стабильностью пероксида водорода, например до примерно 70°C. Давление предпочтительно составляет от примерно атмосферного до примерно 5 бар манометрического давления. Как правило, является предпочтительным использование барботажной колонны, либо насадочной, либо с ситчатыми тарелками. Предпочтительно кислородсодержащий газ подают снизу, а жидкость протекает либо снизу вверх, либо сверху вниз.
Для отделения пероксида водорода от электролита могут использоваться различные способы, такие как выпаривание, экстракция или мембранные технологии. Такое разделение может иметь место в ячейке, в отдельном оборудовании, из которого оставшийся электролит затем рециркулируют назад в ячейку, или в их сочетании.
В одном варианте осуществления пероксид водорода выпаривают из по меньшей мере частично органической фазы электролита, предпочтительно вместе с водой и необязательно с другими летучими веществами, которые могут присутствовать. Выпаривание может осуществляться непосредственно из ячейки или из отдельной емкости, например, путем отгонки вместе с любым газом, например кислородом, воздухом или азотом, или посредством дистилляции при атмосферном или субатмосферном давлении. Низкое давление паров упомянутой по меньшей мере частично органической соли и других органических веществ, необязательно присутствующих в электролите и не образующих часть желательной смеси-продукта, облегчает использование технологий выпаривания для отделения пероксида водорода. В этом варианте осуществления является возможным получение содержащего пероксид водорода потока продукта высокой чистоты без сложных стадий очистки.
В другом варианте осуществления пероксид водорода экстрагируют из по меньшей мере частично органической жидкой фазы любым подходящим растворителем, таким как вода или метанол. Могут быть применены все широко используемые технологии экстракции, такие как один или несколько смесителей-отстойников, колонны с ситчатыми тарелками, колонны со слоем насадки. Если используется электролит, также содержащий преимущественно водную фазу, то пероксид водорода будет автоматически обогащаться в этой фазе, которая может извлекаться в качестве продукта, альтернативно подвергаться дистилляции или другому виду очистки и рециркулироваться назад в ячейку.
В еще одном варианте осуществления используется мембранное разделение. Примеры таких способов включают в себя мембранную экстракцию, первапорацию (испарение через полупроницаемую мембрану) и нанофильтрацию.
Еще в одном варианте осуществления пероксид водорода не извлекают из электролита, а используют непосредственно в качестве реагента при производстве других химикатов. Электролит, остающийся после таких реакций, может затем быть рециркулирован в ячейку.
Способ предпочтительно осуществляют непрерывно, либо с протеканием электролита через ячейку, либо при непрерывном отделении пероксида водорода от электролита в ячейке. Является предпочтительным обеспечить надлежащее перемешивание, особенно вокруг катода, например, за счет продувки газом, механического перемешивания, циркуляции электролита или их сочетаний. Продувку газом предпочтительно проводят кислородом или кислородсодержащим газом, таким как воздух. В ячейке с по существу вертикальным потоком вдувание газа может также создавать газ-лифт, усиливающий перенос электролита через ячейку, альтернативно отгонке пероксида водорода необязательно вместе с водой или любым другим компонентом, который является летучим при температуре и давлении эксплуатации.
Для предотвращения вредного накопления примесей от исходных химикатов или продуктов разложения, образующихся в побочных реакциях, в некоторых случаях может оказаться желательным выпускать часть электролита из системы и/или очистка с помощью различных способов, подобных электродиализу, адсорбции, перекристаллизации, осаждению, промывке, ионному обмену, выпариванию или отгонке с использованием газа-носителя, реакционной регенерации с кислотной/основной или восстановительной/окислительной стадиями.
Поскольку в ходе побочной реакции на катоде может образовываться газообразный водород, может быть полезным включение газоанализатора и устройства для продувки инертным газом.
Температура может регулироваться любыми подходящими средствами, например посредством теплообменников при любом соответствующем потоке. Охлаждение также может осуществляться посредством выпаривания, например, в электрохимической ячейке и последующей конденсации паров. Если испарительное охлаждение осуществляется с помощью воды, может быть полезным добавление воды специально для этой цели.
Могут использоваться различные виды катодов. Является предпочтительным, чтобы катод изготавливался из материала, подавляющего паразитные реакции, такие как выделение водорода, прямое восстановление кислорода до воды и разложение органического медиатора, ионной жидкости или образовавшегося пероксида водорода. В большинстве случаев является предпочтительным использование катода с гидрофобной поверхностью. Примеры материалов для катода включают в себя материалы на основе углерода, подобные легированному бором алмазу, графиту, стеклообразному углероду, высокоориентированному пиролитическому графиту, сетчатому углероду и проводящим полимерам. Примеры проводящих полимеров включают в себя поли(пара)фенилен, полипиррол, политиофен и полианилин. Проводящий полимер может наноситься в виде тонкой пленки с предпочтительной толщиной от примерно 0,1 до примерно 100 мкм на любую пригодную подложку, такую как Pt или нержавеющая сталь. Полимерная пленка может быть получена посредством химического синтеза или предпочтительно посредством электросинтеза. Конкретный пример представляет собой катод, полученный с помощью электросинтеза пленки полипиррола на нержавеющей стали. Другие примеры катодных материалов включают в себя металлы, подобные железу, стали, свинцу, никелю, титану или платине, или проводящие оксиды металлов, такие как PbO2, NiO2, Ti4O7, NiCo2O4 или RuO2. Другие примеры включают в себя электрокаталитические катоды из материала, подобного титану или титановому сплаву, покрытого полностью или частично частицами благородных металлов, подобных золоту, платине, палладию, или с привитыми катализаторами для антрахинонов.
Анод также может изготавливаться из многих видов материалов. Хотя многие металлы как таковые не являются термодинамически стабильными, пригодными для использования являются оксиды, например, платины, свинца, никеля, титана, тантала и ниобия. Также могут использоваться графитовые и электрокаталитические аноды, подобные DSA (анод со стабильными размерами), предпочтительно полученные посредством покрытия материала, подобного титану или титановому сплаву, каталитическими металлами и/или оксидами металлов.
Для окисления воды при высоких pH, предпочтительно от примерно 8 до примерно 15, предпочтительные материалы представляют собой сталь или никель, покрытые отложениями с высокой площадью поверхности из никеля или другого каталитического металла, подобного платине, или из смешанных оксидов типа шпинели или перовскита. Для окисления воды при низких pH, предпочтительно от примерно 1 до примерно 7, предпочтительными являются DSA-аноды, например титан или титановый сплав, покрытый Ta2O5/IrO2.
Для окисления хлорида предпочтительными являются DSA-аноды, такие как титан или титановый сплав, покрытый, например, RuO2/TiO2, RuO/TiO2/IrO2 или Pt/Ir.
Для окисления сульфата и бисульфата предпочтительные материалы представляют собой Pt, Pt/Ta/Ag и PbO2.
Для окисления карбоновых кислот до перкарбоновых кислот предпочтительные материалы представляют собой Pt, Au или углерод.
Для окисления метанола предпочтительные материалы представляют собой смешанные оксиды типа шпинели или перовскита, необязательно содержащие любой из Pt и Ru.
Для окисления водорода предпочтительные материалы представляют собой углерод на связке ПТФЭ в сочетании с одним или более благородными металлами, углеродную или графитовую шерсть, покрытую одним или более благородными металлами, или смешанные оксиды типа шпинели или перовскита.
Катод и анод могут изготавливаться с различными геометрическими формами и могут, например, принимать форму плоского листа или пластины, искривленной (неплоской) поверхности, криволинейной поверхности, перфорированной пластины, тканой проволочной сетки, растянутого сетчатого листа, стержня или трубки. Однако анод и катод предпочтительно имеют плоскую форму, наиболее предпочтительно в виде листа, сетки или пластины.
Может использоваться любая традиционная конструкция ячейки предпочтительно с как можно меньшим расстоянием между анодом и катодом. Разделенная ячейка может, например, быть типа "с нулевым зазором", где по меньшей мере один из электродов прижимается к мембране, разделяющей ячейку.
Типичная производственная установка включает в себя множество ячеек для достижения желаемой производительности. Ячейки могут быть скомпонованы однополярным или биполярным образом в электролизер в соответствии с любой обычной конструкцией.
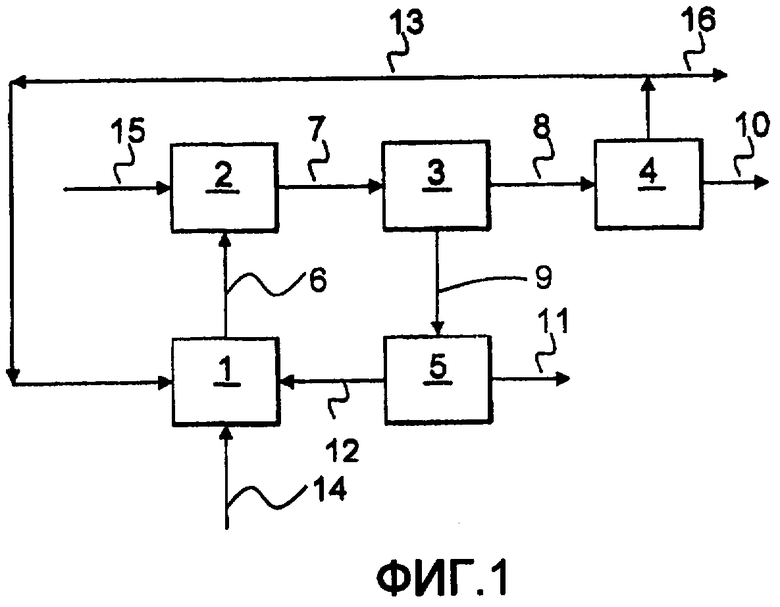
Теперь варианты осуществления изобретения будут описываться дополнительно в связи с прилагаемыми схематическими чертежами. Однако объем изобретения не ограничивается этими вариантами осуществления. Фиг.1 показывает схематическую конфигурацию катодной части способа, в то время как Фиг.2, 3 и 4 показывают схематические конструкции различных электрохимических ячеек.
Обращаясь к Фиг.1, электрохимическое восстановление медиатора происходит в по меньшей мере частично органической сплошной фазе электролита в камере 1 ячейки, которая может представлять собой катодную камеру или однокамерную ячейку. Исходный поток 14 снабжает камеру 1 ячейки любыми веществами, которые потребляются в этом способе, такими как кислород, или извлекаются в любом нерециркулируемом потоке продукта, такими как вода или инертный газ, подобный азоту. Если присутствует кислород, то в камере 1 ячейки также может происходить реакция между восстановленной формой или формами медиатора и кислородом с получением пероксида водорода или пероксида щелочного металла. Если эта реакция протекает до достаточно большой степени, то является достаточным удалить пероксид водорода вместе, например, с водой в потоке 6. Если реакция с получением пероксида водорода или пероксида щелочного металла является незавершенной, то электролит отводят и реакцию завершают до желательной степени в реакторе 2 окисления, куда может подаваться дополнительный кислород 15. Полученный в результате поток 7 содержит пероксид водорода или пероксид щелочного металла в одной или нескольких формах в зависимости от используемых условий, например в виде пара или растворенный в жидкой фазе. Если присутствуют как газовая, так и по меньшей мере одна жидкая фаза, то их направляют в газожидкостный сепаратор 3, из которого газовый поток 8 направляют в конденсор 4. Продукт пероксид водорода 10 отводят из конденсора 4, в то время как остающийся газ 13, например кислород, водяной пар и другие необязательные компоненты, либо рециркулируют в любую точку, где может использоваться кислород, такую как камера 1 ячейки или реактор 2 окисления, либо выпускают через 16. Поток 9 жидкости из сепаратора 3 рециркулируют в камеру 1 ячейки. Если поток 9 жидкости содержит пероксид водорода, то сначала его направляют в сепаратор 5, который может представлять собой, например, установку экстракции или установку мембранного разделения. Здесь этот поток 5 разделяют на поток 11 продукта, содержащий пероксид водорода, и рециркулируемый поток 12, содержащий по меньшей мере частично органический электролит.
Различные установки, проиллюстрированные на Фиг.1, могут быть скомбинированы множеством способов. Например, кислород может вводиться в камеру 1 ячейки различными способами, например, отдельно или вместе с любым жидким исходным или рециркулируемым потоком. Кислород также может вводиться в некотором месте над электродами для разделения электрохимических реакций и окисления. Реактор 2 окисления и газожидкостный сепаратор 3 могут быть объединены, например, посредством использования барботажной колонны. Если условия эксплуатации заданы так, что газ не образуется и только жидкая фаза извлекается из камеры 1 ячейки, то газожидкостный сепаратор 3 и конденсор 4 могут отсутствовать.
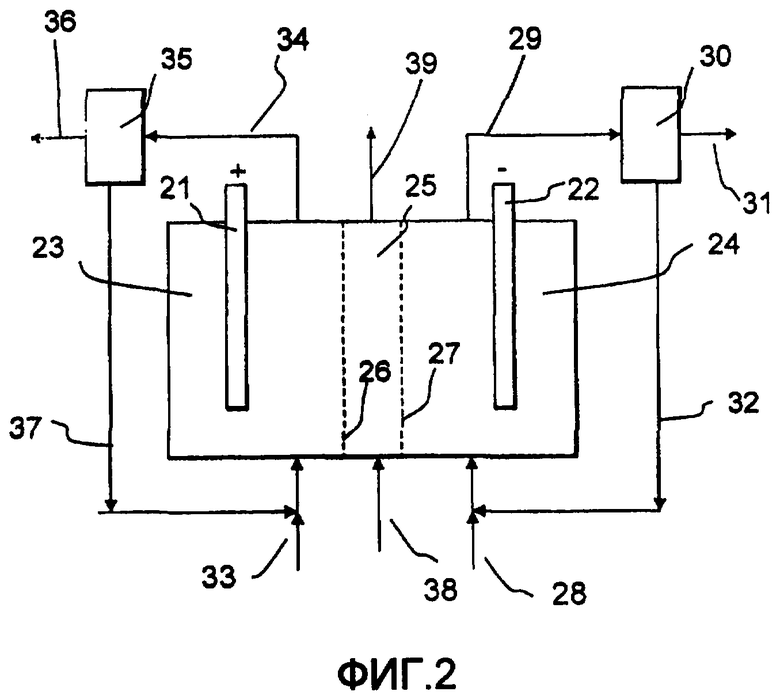
Обращаясь к Фиг.2, электрохимическая ячейка, работающая в соответствии с изобретением, содержит анод 21 в анодной камере 23 и катод 22 в катодной камере 24. Ячейка также содержит среднюю камеру 25, отделенную от анодной и катодной камер 23, 24 ионселективными мембранами 26, 27. В одном варианте осуществления мембрана 26 является проницаемой для анионов, а мембрана 27 является проницаемой для катионов. В другом варианте осуществления обе мембраны 26, 27 являются проницаемыми для катионов. В катодной камере 24 удерживается католит, содержащий органический медиатор согласно изобретению. Кислородсодержащий газ подают с помощью входного потока 28 в катодную камеру 24, а выходной поток 29, содержащий пероксид водорода и/или восстановленный медиатор, направляют в установку 30, где происходит дальнейшая переработка. Такая дальнейшая переработка может включать в себя окисление восстановленного медиатора с получением пероксида водорода и его отделение, приводящее к получению потока 31 продукта, содержащего пероксид водорода и необязательно другие вещества, такие как вода, которые могут оставаться в конечном продукте, и другие, которые могут отделяться позднее, из рециркулируемого потока 32, содержащего, например, католит с органическим медиатором, полученным посредством окисления его восстановленных форм. Анодная камера 23 запитывается входным потоком 33, который может иметь различные составы в зависимости от желаемых реакций. Анолит, содержащий продукты реакции, отводят в выходном потоке 34 в сепаратор 35 продукта, из которого отводят продукт 36, а оставшийся электролит 37 рециркулируют в анодную камеру 23. Среднюю камеру 25 запитывают с помощью входного потока 38 предпочтительно водным раствором, состав которого зависит от желаемых общих реакций. Выходной поток 39 из средней камеры 25 может рециркулироваться или использоваться любым другим образом.
Если ячейка по Фиг.2 используется в варианте осуществления, где обе мембраны 26, 27 являются катионселективными, и вода подвергается реакции на аноде 21 с образованием кислорода и протонов, то анолит предпочтительно состоит из воды и подходящего электролита, такого как KOH или NaOH. Кислород отводят вместе с анолитом с помощью выходного потока 34 и отделяют от него в сепараторе 35. Оставшийся анолит 37 рециркулируют в анодную камеру 23, в то время как кислород может переноситься в катодную камеру 24 или отдельную установку для окисления восстановленного медиатора с образованием пероксида водорода. Протоны из анолита переносятся в среднюю камеру 25 через катионселективную мембрану 26. Среднюю камеру 25 предпочтительно запитывают с помощью входного потока 38 предпочтительно водным раствором, содержащим протоны или катионы, подобные ионам натрия, которые могут переноситься через катионселективную мембрану 27 в катодную камеру 24. Примеры таких растворов представляют собой растворители, подобные воде, содержащие HCl, HxPO3 (3-x)-, HxSO4 (2-x)-, NaClO3 или уксусную кислоту.
Если ячейка по Фиг.2 используется в варианте осуществления, где мембрана 26 является анионселективной, мембрана 27 является катионселективной, а хлорид подвергается реакции на аноде с образованием хлора, который может гидролизоваться далее с образованием хлората, то анолит предпочтительно представляет собой водный раствор, содержащий NaCl, NaClО3 или соответствующие калиевые соли KCl или KClO3 и необязательно буфер, такой как хромат, дихромат или любая другая подходящая соль. Поток 34 продукта-анолита отводят и направляют в сепаратор 35 продукта, где хлорат щелочного металла кристаллизуют и извлекают 36, в то время как оставшийся электролит рециркулируют 37 в анодную камеру 23. Можно также предусмотреть установку (не показана) для дополнительных реакций с образованием хлората в извлекаемом потоке 34 продукта перед кристаллизацией. В одном варианте среднюю камеру 39 предпочтительно запитывают с помощью входного потока 38 растворителем, подобным воде, содержащим HCl или NaCl, и хлорид-ионы переносятся через анионселективную мембрану 26 в анодную камеру 23, где они потребляются на аноде 21 с образованием хлора на первой стадии. Затем в катодную камеру 23 подают Na+ или K+ с помощью входного потока 33, например, в форме NaOH или KOH. В другом варианте среднюю камеру 25 с помощью входного потока 38 запитывают OH-, например, в виде NaOH или KOH, причем гидроксид-ионы будут переноситься через анионселективную мембрану 26, а затем с помощью входного потока 33 подают хлорид-ионы, например, в виде NaCl. В любом варианте катионы, как правило, Na+ или H+, переносятся из средней камеры 25 через катионселективную мембрану 27 в катодную камеру 24.
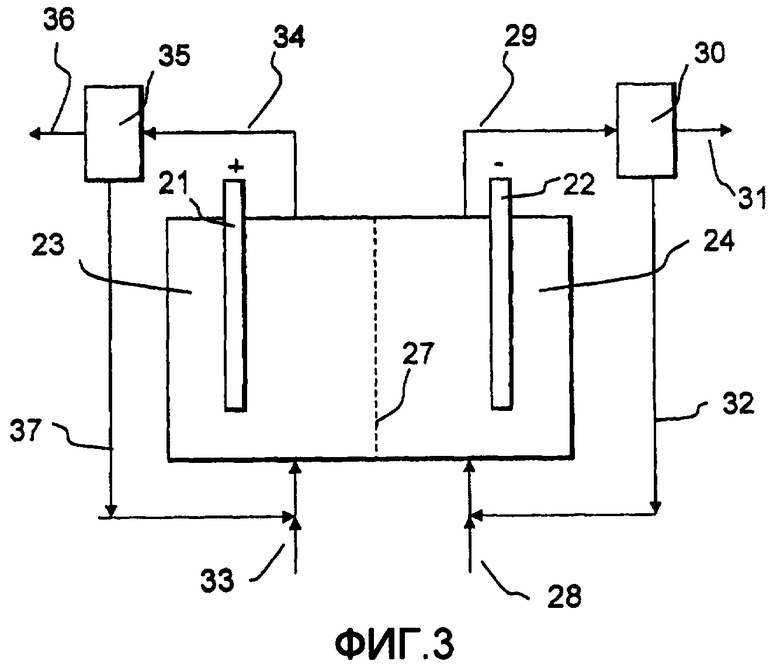
Обращаясь к Фиг.3, электрохимическая ячейка, работающая в соответствии с изобретением, содержит анод 21 в анодной камере 23 и катод 22 в катодной камере 24. Однако в отличие от ячейки по Фиг.2 здесь имеется только одна ионселективная мембрана 27, которая предпочтительно является катионселективной, а средней камеры нет. Во всех других отношениях эта ячейка является идентичной ячейке по Фиг.2, к описанию которой отсылается читатель.
Если ячейка по Фиг.3 снабжается катионселективной мембраной 27 и используется в варианте осуществления, где хлорид реагирует на аноде 21 с образованием хлора, который гидролизуется далее с образованием хлората, то анолит предпочтительно представляет собой водный раствор, содержащий NaCl, NaClO3 или соответствующие калиевые соли KCl или KClO3 и буфер, такой как хромат или любая другая подходящая соль. NaCl или KCl подают в анодную камеру 23 с помощью входного потока 33, в то время как катионы, такие как Na+ или H+, переносятся через мембрану 27 в катодную камеру 24. Для компенсации убыли Na+ или K+ через мембрану 27 и нейтрализации H+, образовавшегося при анодных реакциях, может оказаться полезным добавлять некоторое количество NaOH или KOH в любом подходящем месте, например во входной поток 33 или рециркулируемый поток 37. Во всех других отношениях, подобных манипуляциям с потоком 34 продукта и рециркулируемым потоком 37, работа является эквивалентной соответствующему варианту осуществления, реализованному в ячейке по Фиг.2, к описанию которого отсылается читатель.
Если ячейка по Фиг.3 снабжена катионселективной мембраной 27 и используется в варианте осуществления для разложения продуктов отходов, таких как SO2, то его подают в анодную камеру вместе с водой с помощью потока 33 и окисляют на аноде 21 с образованием серной кислоты, растворяющейся в воде и извлекаемой с помощью потока 34 продукта. Любые протоны или другие присутствующие катионы проходят через мембрану 27 в катодную камеру 24.
Если ячейка по Фиг.3 снабжается катионселективной мембраной 27 и используется в варианте осуществления, где водород окисляется до протонов на газодиффузионном аноде 21, снабженном катализатором, то протоны переносятся через мембрану 27 в катодную камеру 24 и облегчают образование пероксида водорода. Анолит, содержащий, например, фосфорную кислоту, может циркулировать через анодную камеру 23 без извлечения какого-либо продукта, и тогда установка 35 разделения может быть исключена.
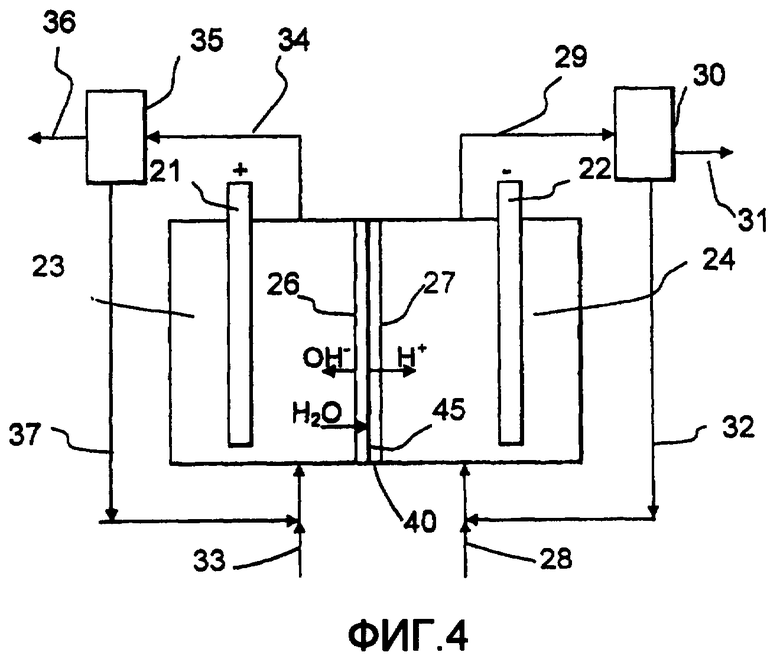
Обращаясь к Фиг.4, электрохимическая ячейка, работающая в соответствии с изобретением, содержит анод 21 в анодной камере 23 и катод 22 в катодной камере 24. Однако в отличие от ячейки по Фиг.2 средняя камера здесь заменена биполярной мембраной 40, разделяющей камеры 23, 24 ячейки. Биполярная мембрана 40 содержит анионселективную мембрану 26 и катионселективную мембрану 27, наслоенные вместе с двух сторон слоя катализатора 45. Вода из анолита проходит в слой катализатора, где она расщепляется на протоны, проходящие в катодную камеру 24, и гидроксид-ионы, проходящие в анодную камеру 23. Во всех других отношениях эта ячейка является идентичной ячейкам по Фиг.2 и 3, к описаниям которых отсылается читатель.
Если ячейка по Фиг.4 используется в варианте осуществления, где вода подвергается реакции на аноде 21 с образованием кислорода и протонов, то анолит предпочтительно состоит из воды и подходящего электролита, такого как NaOH или KOH, и кислород отводят вместе с анолитом с помощью выходного потока 34. Внутри биполярной мембраны вода расщепляется на протоны и гидроксид-ионы. Протоны перемещаются в катодную камеру 24 и облегчают окисление восстановленного медиатора с образованием пероксида водорода, в то время как гидроксид-ионы перемещаются в анодную камеру 23 и нейтрализуются протонами от анодных реакций. Во всех других отношениях, подобных манипуляциям с потоком 34 продукта и рециркулируемым потоком 37, работа эквивалентна соответствующему варианту осуществления, реализованному в ячейке по Фиг.2, к описанию которого отсылается читатель.
Если ячейка по Фиг.4 используется в варианте осуществления, где хлорид реагирует на аноде 21 с образованием хлора, который подвергается реакции далее с образованием хлората, то анолит предпочтительно представляет собой водный раствор, содержащий NaCl, NaClO3 или соответствующие калиевые соли KCl или KClO3 и буфер, такой как хромат или любая другая подходящая соль. NaCl или KCl подают в анодную камеру 23 с помощью входного потока 33. Внутри биполярной мембраны вода расщепляется на протоны и гидроксид-ионы. Протоны перемещаются в катодную камеру 24 и облегчают окисление восстановленного медиатора с образованием пероксида водорода, в то время как гидроксид-ионы перемещаются в анодную камеру 23, облегчая гидролиз хлора. Во всех других отношениях, подобных манипуляциям с потоком 34 продукта и рециркулируемым потоком 37, работа эквивалента соответствующим вариантам осуществления, реализованным в ячейке по Фиг.2, к описанию которой отсылается читатель.
Во всех вариантах осуществления, описанных на Фиг.2-4, катодный процесс может быть одинаковым, то есть представлять собой восстановление медиатора на катоде 22 и перенос катионов, подобных H+ или Na+, из средней камеры 25 или анодной камеры 23 через катионселективную мембрану 27. Если кислород образуется и извлекается из анодной камеры 23, он может переноситься в катодную камеру 24 или в отдельную установку для окисления восстановленной формы медиатора, образующейся в катодной камере 24.
Настоящее изобретение теперь будет описываться дополнительно с помощью следующих далее примеров. Если не указано иное, то все доли и процентные содержания относятся к долям и процентам по массе.
Пример 1. Раствор, содержащий 25 мл ионной жидкости 1-бутил-3-метил-имидазолий гексафторфосфата [BMIM] [HFP] с 0,1 г 2-этил-9,10-антрахинона (EAQ) в качестве медиатора залили в небольшой реактор и нагрели до 60°C. В этот раствор в течение 30 минут вдували газообразный азот, насыщенный водой, для растворения газов в растворе и для насыщения раствора водой до оценочной концентрации примерно 3-5 мас.%. Поверх органической фазы добавляли водную фазу, содержащую 0,05 M H2SO4, для подачи протонов. Катод из круглой платиновой сетки с диаметром 3 см помещали в органическую фазу, а анод из платиновой сетки помещали в отдельную камеру, содержащую 10 мМ водного раствора NaOH. Анодная и катодная камеры были разделены неселективной керамической мембраной (диафрагмой). Католит перемешивали с помощью магнитного бруска, расположенного в органической фазе в катодной камере. Для отслеживания катодного потенциала в катодную камеру вблизи катода помещали электрод сравнения (Metrohm 6.0726.110 Ag/AgCl).
В качестве первого испытания к ячейке в течение 10 минут прикладывали ток примерно 30 мА, что давало увеличение потенциала на уровне примерно 1 В по сравнению с электродом сравнения. В анодной камере образовывался кислород. Катод становился красноватым по цвету, что было предположительно связано с комплексом восстановленной формы EAQ. После этого измеряли концентрацию пероксида водорода, что дало ноль мг/л. Затем через раствор продували кислород и в водной фазе в катодной камере наблюдали концентрацию пероксида водорода 5 мг/л.
Из этих результатов можно сделать вывод, что кислород не восстанавливался на катоде с образованием пероксида водорода, а вместо этого сначала должен был восстанавливаться EAQ, который затем подвергался реакции с кислородом с образованием пероксида водорода.
Пример 2. В сходной установке, как и в примере 1, в качестве католита использовали двухфазную систему: нижнюю фазу из 50 мл [BMIM] [HFP] с оценочным содержанием воды примерно 3-5 мас.% и с 0,8 г EAQ, растворенного в ней, и верхнюю фазу из 40 мл 0,5 M раствора H2SO4. В нижней фазе располагался катод из стальной сетки с площадью примерно 13 см2, в то время как в верхнюю фазу непрерывно барботировали кислород. Анодную камеру с 10 мМ NaOH, как описано в примере 1, погружали в раствор. При температуре 68°C между анодом и катодом пропускали ток 0,2 A в течение 30 минут, что давало почти черный раствор из-за восстановленного EAQ. Затем измеряли содержание пероксида водорода в водной фазе и использовали его в качестве основы для вычисления выхода по току для образования пероксида водорода, который был равен 22% (то есть не включая пероксид водорода, остающийся в фазе [BMIM] [HFP]).
Пример 3. Использовали такую же установку и условия, как и в примере 1, за исключением того, что кислоту в водной фазе в катодной камере заменили на фосфорную кислоту с концентрацией 2 мас.%, а вместо Ag/AgCl использовали каломельный электрод сравнения. Между анодом и катодом прикладывали ток и наблюдали накопление пероксида водорода. Через 100 минут измеряли концентрацию пероксида водорода в водной фазе и находили ее равной примерно 250 мг/л.
Пример 4. Использовали такую же установку и условия, как и в примере 2, за исключением того, что анодная камера содержала водный раствор 150 г/л NaCl и 10 г/л дихромата натрия. Во время эксперимента к анолиту добавляли несколько капель NaOH (1 M) для поддержания pH между 6 и 7. В катодной камере образовывался пероксид водорода, как описано в примере 2. В анодной камере хлорид окислялся до хлора, который в конечном итоге образовывал хлорат. Через 20 минут эксперимент прекратили и вычислили выход по току для образования хлората, составивший 59%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОИЗВОДСТВА ПЕРОКСИДА ВОДОРОДА И ХЛОРАТА | 2006 |
|
RU2375500C2 |
| ЭЛЕКТРОХИМИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ АЗОТНЫХ УДОБРЕНИЙ | 2008 |
|
RU2479558C2 |
| ЭЛЕКТРОЛИЗНАЯ СИСТЕМА ДЛЯ ЭЛЕКТРОХИМИЧЕСКОЙ УТИЛИЗАЦИИ ДИОКСИДА УГЛЕРОДА С ПРОТОНОДОНОРНЫМ БЛОКОМ И СПОСОБ ВОССТАНОВЛЕНИЯ | 2016 |
|
RU2685421C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЩЕЛОЧНОГО РАСТВОРА ПЕРОКСИДА ВОДОРОДА И ДИОКСИДА ХЛОРА | 2000 |
|
RU2221741C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРЕКИСИ ВОДОРОДА | 2010 |
|
RU2494960C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРОКСИДА ВОДОРОДА | 2007 |
|
RU2458856C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭЛЕМЕНТАРНОЙ СЕРЫ ИЗ СЕРОВОДОРОДА И ЦИКЛИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ ПЕРЕКИСИ ВОДОРОДА | 1994 |
|
RU2099280C1 |
| УСТРОЙСТВО ДЛЯ ОЧИСТКИ ВОЗДУХА В ЖИЛЫХ И ПРОИЗВОДСТВЕННЫХ ПОМЕЩЕНИЯХ ОТ ВРЕДНЫХ ПРИМЕСЕЙ | 2012 |
|
RU2494790C1 |
| СПОСОБ ПОВЫШЕНИЯ ЧИСТОТЫ ГИДРОКСИДОВ ЧЕТВЕРТИЧНОГО АММОНИЯ ЭЛЕКТРОЛИЗОМ | 2001 |
|
RU2282488C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТАНА И КИСЛОРОДА | 2009 |
|
RU2407825C1 |
Изобретение относится к способу производства пероксида водорода, включающему в себя обеспечение электрохимической ячейки, содержащей анод и катод; контактирование катода с электролитом, содержащим по меньшей мере один органический медиатор, растворенный в по меньшей мере частично органической сплошной жидкой фазе, содержащей по меньшей мере частично органическую соль и нейтральный сорастворитель, реагирование органического медиатора на катоде с образованием по меньшей мере одной восстановленной формы этого медиатора; и реагирование упомянутой по меньшей мере одной восстановленной формы медиатора с кислородом с образованием пероксида водорода. Причем частично органическая соль содержит по меньшей мере один вид органического катиона и/или органического аниона, упомянутая сплошная жидкая фаза имеет электропроводность при условиях способа, по меньшей мере, примерно 0,1 См/м. Технический результат: производство пероксида водорода посредством опосредованного электрохимического восстановления кислорода без необходимости в контактировании катода с газообразным водородом, которое может осуществляться на сравнительно простом оборудовании и включает в себя электрохимическое восстановление медиатора. 20 з.п. ф-лы, 4 ил.
1. Способ производства пероксида водорода, включающий в себя обеспечение электрохимической ячейки, содержащей анод и катод; контактирование катода с электролитом, содержащим по меньшей мере один органический медиатор, растворенный в по меньшей мере частично органической сплошной жидкой фазе, содержащей по меньшей мере частично органическую соль и нейтральный сорастворитель, причем упомянутая соль содержит по меньшей мере один вид органического катиона и/или органического аниона, содержание упомянутой по меньшей мере частично органической соли в упомянутой сплошной жидкой фазе составляет от примерно 20 мас.% до примерно 99 мас.%, и упомянутая сплошная жидкая фаза имеет электропроводность при условиях способа, по меньшей мере, примерно 0,1 См/м; реагирование органического медиатора на катоде с образованием по меньшей мере одной восстановленной формы этого медиатора; и реагирование упомянутой по меньшей мере одной восстановленной формы медиатора с кислородом с образованием пероксида водорода.
2. Способ по п.1, в котором нейтральный сорастворитель присутствует в упомянутой по меньшей мере частично органической сплошной жидкой фазе электролита в количестве вплоть до примерно 50 мас.%.
3. Способ по п.2, в котором нейтральный сорастворитель присутствует в упомянутой по меньшей мере частично органической сплошной жидкой фазе электролита в количестве от примерно 1 до примерно 20 мас.%.
4. Способ по любому из пп.1-3, в котором сорастворитель представляет собой воду.
5. Способ по любому из пп.1-3, в котором органический медиатор выбирают из группы, состоящей из хинонов, флавохинонов, производных пиридина и кетонов.
6. Способ по п.5, в котором органический медиатор выбирают из группы, состоящей из хинонов, содержащих (бензо)хиноновый фрагмент.
7. Способ по п.6, в котором органический медиатор выбирают из группы, состоящей из антрахинонов, тетрагидроантрахинонов, нафтохинонов, бензохинонов и их производных.
8. Способ по любому из пп.1-3, в котором содержание органического медиатора, включая восстановленные формы, в упомянутой по меньшей мере частично органической сплошной жидкой фазе составляет, по меньшей мере, примерно 1 мас.%.
9. Способ по любому из пп.1-3, в котором упомянутая по меньшей мере частично органическая соль сама по себе или в сочетании с нейтральным сорастворителем образует жидкую фазу при атмосферном давлении ниже примерно 130°С.
10. Способ по любому из пп.1-3, в котором упомянутая по меньшей мере частично органическая соль при 100°С имеет парциальное давление ниже примерно 10 кПа.
11. Способ по любому из пп.1-3, в котором упомянутая по меньшей мере частично органическая соль содержит катион, выбранный из группы, состоящей из 1-алкил-3-метилимидазолия, 1-бутил-3-метилимидазолия [BMIM], 1-этил-3-метилимидазолия [EMIM], 1,2,3-триметилимидазолия, н-алкилпиридиния, н-бутилпиридиния [BPY], пирролидиния, гуанидиния и алкилгуанидиния, изоурония, PR4 +, NR4 +, SR3 +, тетраметиламмония, холина, кокомония и их смесей, R представляют собой, независимо друг от друга, необязательно замещенный алкил, алкенил или арил, или водород.
12. Способ по любому из пп.1-3, в котором упомянутая по меньшей мере частично органическая соль содержит катион, выбранный из группы, состоящей из замещенных хинонов.
13. Способ по любому из пп.1-3, в котором упомянутая по меньшей мере частично органическая соль содержит анион, выбранный из группы, состоящей из гексафторфосфата [HFP], тетрафторбората [TFB], фторсульфоната, гексафторантимоната, гексафторарсената, хлоралюмината, бромалюмината, бис(трифторметилсульфонил)имида, трис(трифторметилсульфонил)метида, трицианометида, дицианамида, нонафторбутансульфоната, трифторметансульфоната, 2,2,2-трифторэтансульфоната, нитрата, сульфата, фосфата, RPO4 2-, R2PO4 -, R2PO2 - (например, диалкилфосфината), перхлората, ацтетата, алкилсульфоната, бис(2-этилгексил)натрия сульфосукцината, диэтиленгликольмонометилэфирсульфата, алкилолигоэфирсульфата, пивалата, тетраалкилбората, пропионата, сукцината, сахарината, гликолята, стеарата, лактата, малата, тартрата, цитрата, аскорбата, глютамата, бензоата, салицилата, метансульфоната, толуолсульфоната и их смесей, R представляют собой, независимо друг от друга, необязательно замещенный алкил, алкенил или арил, или водород.
14. Способ по любому из пп.1-3, в котором упомянутая по меньшей мере частично органическая соль содержит анион, выбранный из группы, состоящей из замещенных хинонов.
15. Способ по любому из пп.1-3, в котором упомянутая по меньшей мере частично органическая соль содержит катион, выбранный из группы, состоящей из [1,3-диалкилимидазолия], [триалкиламмония], [тетраалкиламмония], [триалкилфосфония], [тетраалкилфосфония], [алкилпиридиния], [холина], [Q-NR3 +] и [Q-PR3 +], и анион, выбранный из группы, состоящей из [сульфата], [фосфата], [алкилсульфата], [алкилсульфоната], [диалкилфосфата], [алкилфосфоната], [Q-(O)-SO3 -] и [Q-(O)-PO3R-], где Q представляет собой хинон, (О) представляет собой необязательный кислород, и R представляет собой, независимо друг от друга, необязательно замещенный алкил, алкенил или арил, или водород.
16. Способ по любому из пп.1-3, в котором электрохимическая ячейка содержит отдельные анодную и катодную камеры.
17. Способ по любому из пп.1-3, в котором электролит в катодной камере или ячейке, если нет отдельной катодной камеры, содержит единственную жидкую фазу.
18. Способ по любому из пп.1-3, в котором к упомянутой по меньшей мере частично органической фазе электролита, содержащей восстановленный медиатор, добавляют молекулярный кислород, что приводит к образованию пероксида водорода в электролите.
19. Способ по п.18, в котором, по меньшей мере, часть этого кислорода добавляют к упомянутой по меньшей мере частично органической фазе электролита, содержащей восстановленный медиатор, в виде газа непосредственно в электрохимическую ячейку.
20. Способ по любому из пп.1-3, в котором пероксид водорода выпаривают из упомянутой по меньшей мере частично органической фазы электролита.
21. Способ по любому из пп.1-3, в котором пероксид водорода экстрагируют из упомянутой по меньшей мере частично органической жидкой фазы.
| HUISSOUD A | |||
| et | |||
| al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| J | |||
| applied electrochemistry | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| KR 100341886 B1, 12.06.2002 | |||
| СПОСОБ ПОЛУЧЕНИЯ ПЕРОКСИДА ВОДОРОДА АНТРАХИНОНОВЫМ МЕТОДОМ И КОМПОЗИЦИЯ ДЛЯ ПОЛУЧЕНИЯ ПЕРОКСИДА ВОДОРОДА | 2000 |
|
RU2196106C2 |
| US 4515664 A, 07.05.1985 | |||
| GLYENCE E.L | |||
| et | |||
| al | |||
| Electrosynthesis of hydrogen peroxide in | |||
Авторы
Даты
2010-01-27—Публикация
2006-06-02—Подача