Изобретение относится к способу получения пероксида водорода антрахиноновым методом, в котором рабочий раствор содержит определенную смесь антрахинонов и тетрагидроантрахинонов. Изобретение также относится к композиции, содержащей смесь антрахинонов, используемых в качестве рабочего раствора при получении пероксида водорода.
Антрахиноновый метод является наиболее общим способом получения пероксида водорода. Согласно такому способу замещенные антрахиноны и/или тетрагидроантрахиноны, растворенные в смеси подходящих органических растворителей, так называемом рабочем растворе, подвергают гидрированию с образованием соответствующих гидрохинонов. Затем полученные гидрохиноны окисляют кислородом (обычно воздухом) обратно в хиноны с одновременным образованием пероксида водорода, который затем можно экстрагировать водой, тогда как хиноны возвращают с рабочим раствором на стадию гидрирования.
Антрахиноновый метод описан в литературе, например в энциклопедии Kirk-Othmer, "Encyclopedia of chemical technology", 4-е изд., т.13, стр. 961-995.
Наиболее решающей стадией антрахинонового метода является гидрирование. Существующие проблемы главным образом состоят в минимизации потерь антрахинонов и тетрагидроантрахинонов на нежелательные побочные реакции и в достижении высокой концентрации гидрохинонов в рабочем растворе. Было установлено, что для преодоления указанных проблем важным фактором является состав рабочего раствора.
В WO 95/28350 раскрывается получение пероксида водорода с использованием рабочего раствора, главным образом состоящего из тетрагидроэтил- и тетрагидроамилатрахинонов в среде органических растворителей.
В WO 98/28225 раскрывается получение пероксида водорода с использованием рабочего раствора, состоящего из этил- и амилантрахинонов в среде органических растворителей.
Авторами изобретения была обнаружена возможность получения рабочего раствора, обладающего высокой растворимостью, позволяющего использовать высокие концентрации гидрохинонов, кроме этого рабочий раствор также обладает устойчивостью к побочным реакциям в ходе стадии гидрирования.
Таким образом, настоящее изобретение относится к способу получения пероксида водорода антрахиноновым способом, включающим чередующиеся стадии гидрирования и окисления антрахинонов и тетрагидроантрахинонов в рабочем растворе. Рабочий раствор, подлежащий гидрированию, содержит смесь алкилзамещенных антрахинонов и алкилзамещенных тетрагидроантрахинонов, которые растворены по крайней мере в одном органическом растворителе, в котором 10-55 мол.%, предпочтительно 20-50 мол. %, от общего количества антрахинонов и тетрагидроантрахинонов замещены одной амиловой группой, а молярное соотношение алкилзамещенных тетрагидроантрахинонов и алкилзамещенных антрахинонов составляет по крайней мере 1:1, предпочтительно приблизительно от 2:1 до приблизительно 50:1, наиболее предпочтительно приблизительно от 3:1 приблизительно до 20:1. В некоторых случаях удобнее работать при молярном соотношении лишь приблизительно до 9:1, однако возможно также использовать рабочие растворы, практически не содержащие алкилзамещенных антрахинонов.
Амилзамещенные антрахиноны и амилзамещенные тетрагидроантрахиноны главным образом получают из 2-трет-амил- и/или 2-изо-втор-амилзамещенного антрахинона и тетрагидроантрахинона, предпочтительно из их смеси. Также предпочтительно, чтобы 45-90 мол.%, наиболее предпочтительно 55-80 мол.%, антрахинонов и тетрагидроантрахинонов были замещены одной или несколькими другими алкильными группами, наиболее предпочтительно содержащими, в целом, 1-4 углеродных атомов, особенно предпочтительно одной этильной группой. Наиболее предпочтительно, чтобы алкилзамещенные антрахиноны и тетрагидроантрахиноны представляли собой монозамещенные вещества, предпочтительно в положении 2.
Использование амилзамещенного антрахинона и амилзамещенного тетрагидроантрахинона в рабочем растворе означает, что соответствующие гидрохиноны образуются на стадии гидрирования. Поскольку амилзамещенные гидрохиноны обладают значительно более высокой растворимостью, чем другие алкилзамещенные гидрохиноны, возникает возможность достижения высокой степени гидрирования без риска осаждения гидрохинонов в рабочем растворе, даже при сравнительно низких концентрациях амилзамещенных хинонов. Однако высокие степени гидрирования могут быть достигнуты лишь в том случае, когда используется достаточно большое количество тетрагидроантрахинонов. Кроме этого, при низких концентрациях тетрагидроантрахинонов увеличиваются потери активных хинонов на образование продуктов деградации. Может также происходить нежелательное осаждение.
Если используют слишком высокое количество амилзамещенного антрахинона и амилзамещенного тетрагидроантрахинона, плотность рабочего раствора становится слишком высокой, что будет затруднять экстракцию пероксида водорода водой после стадии окисления. Было обнаружено, что плотность понижается, если мольная доля амилзамещенных хинонов в общем количестве хинонов поддерживается на низком значении. Предпочтительно, когда рабочий раствор имеет плотность при 20oС 910-980 кг/м3, более предпочтительно 930-970 кг/см3. Кроме этого, получение амилзамещенного антрахинона более сложно, чем получение этилзамещенного антрахинона, что делает его наиболее дорогостоящим ингредиентом рабочего раствора.
Молярное соотношение между алкилзамещенными тетрагидроантрахинонами и алкилзамещенными антрахинонами в выдержанном рабочем растворе (рабочий раствор, который использовали для получения пероксида водорода в течение, по крайней мере, шести месяцев) обычно имеет близкую величину для антрахинонов, замещенных различными алкильными группами. Молярные отношения для каждой алкильной группы, предпочтительно, отличаются менее чем в 2,5 раза, наиболее предпочтительно менее чем в 1,7 раз.
Алкилзамещенные тетрагидроантрахиноны обычно получают из β-тетрагидроантрахинонов, однако, могут использоваться и некоторые α-тетрагидроантрахиноны.
Помимо прямого или косвенного гидрирования в гидрохиноны протекает большое число вторичных реакций. Так, например, антрагидрохиноны могут дополнительно реагировать с образованием тетрагидроантрагидрохинонов, которые на стадии окисления превращаются в тетрагидроантрахиноны, вследствие чего повышается их количество в рабочем растворе. Это означает, что при запуске процесса настоящего изобретения исходный рабочий раствор может содержать лишь небольшие количества тетрагидроантрахинонов или не содержать их совсем, поскольку они будут образовываться автоматически в ходе реакции. По мере достижения желательных концентраций антрахинонов и тетрагидроантрахинонов по крайней мере часть рабочего раствора обычно подвергают обработке с целью дегидрирования обратного дегидрирования тетрагидроантрахинонов в антрахиноны.
Также происходит прямое или косвенное образование таких нежелательных побочных продуктов, как эпоксиды, октагидроантрахиноны, оксантроны, антроны и диантроны. Некоторые из таких соединений, например эпоксиды, могут быть превращены обратно в антрахиноны, тогда как другие продукты, например диантроны, составляют необратимую потерю активного рабочего раствора. Было обнаружено, что образование нежелательных побочных продуктов может быть минимизировано в том случае, если молярное соотношение между тетрагидроантрахинонами и антрахинонами поддерживается в указанных пределах.
Предпочтительно, чтобы рабочий раствор, подлежащий гидрированию, практически не содержал незамещенных антрахинонов и тетрагидроантрахинонов, поскольку было установлено, что эти соединения обладают плохой растворимостью и легко образуют октагидроантрагидрохинон, который трудно подвергается окислению с образованием пероксида водорода. Особенно предпочтительно, чтобы рабочий раствор, подлежащий гидрированию, в основном состоял из алкилзамещенных соединений, наиболее предпочтительно, когда он представляет собой смесь амил- и этилзамещенного антрахинона с тетрагидроантрахиноном в по крайней мере одном органическом растворителе, предпочтительно содержащем менее 100 кг/м3, наиболее предпочтительно менее 50 кг/м3 таких соединений, как эпоксиды и другие продукты деградации, образующиеся из антрахинонов и/или растворителей, некоторые из которых даже трудно идентифицировать.
Указанный по меньшей мере один органический растворитель, предпочтительно представляет собой смесь одного или более хиноновых растворителей с одним или более, по крайней мере, двумя гидрохиноновыми растворителями. Подходящие хиноновые растворители могут включать ароматические, алифатические или нафтеновые углеводороды, например бензол, такие алкилированные или полиалкилированные бензолы, как трет-бутилбензол или триметилбензол, такие алкилированные толуолы или нафтены, как трет-бутилтолуол или метилнафталин. Подходящие гидрохиноновые растворители могут включать алкилфосфаты (например, триоктилфосфат), алкилфосфонаты, сложные эфиры алкилциклогексанола, N,N-диалкилкарбонамиды, тетраалкилмочевины (например, тетрабутилмочевина), N-алкил-2-пирролидоны и высококипящие спирты, предпочтительно содержащие 8-9 углеродных атомов (например, ди-изобутилкарбинол). Наиболее предпочтительные гидрохиноновые растворители выбирают из алкилфосфатов, тетраалкилмочевин, производных циклической мочевины и алкилзамещенных капролактамов. Особенно предпочтительные гидрохиноновые растворители описаны в патентах США 4800073 и 4800074, и они включают такие алкилзамещенные капролактамы, как октилкапролактам и такие производные циклической мочевины, как N,N'-диалкилзамещенная алкиленмочевина.
Стадию гидрирования обычно осуществляют путем контактирования рабочего раствора с газообразным водородом в присутствии катализатора, при температуре приблизительно от 0 до, примерно, 100oС, предпочтительно от приблизительно 40 до приблизительно 75oС, и при абсолютном давлении от приблизительно 100 до приблизительно 1500 кПа, предпочтительно от приблизительно 200 до приблизительно 600 кПа. Степень гидрирования (выраженная числом молей гидрохинонов в расчете на 1 м3 рабочего раствора) обычно составляет приблизительно от 350 до приблизительно 800, предпочтительно приблизительно от 400 до приблизительно 650.
В качестве активного катализатора могут применяться, например, металл, выбранный из группы, состоящей из никеля, палладия, платины, родия, рутения, золота, серебра или их смесей. Предпочтительные металлы представляют собой палладий, платину и золото, причем особенно предпочтительными являются палладий или смеси, содержащие по крайней мере 50 вес.% палладия. Активный катализатор может использоваться в свободной форме, например палладиевая чернь, суспендированная в рабочем растворе, или может быть нанесен на такой твердый носитель, как частицы, применяемые в виде суспензии или неподвижного слоя. Однако особенно предпочтительно применять катализатор в виде активного металла на монолитном носителе, например, в соответствии с описанием патентов US 4552748 и 5063043. Предпочтительные носители выбирают из диоксида кремния и оксида алюминия.
До или после стадии гидрирования по крайней мере часть рабочего раствора регенерируют в одну или несколько стадий с целью удаления воды с тем, чтобы поддерживать заданное соотношение между тетрагидроантрахинонами и антрахинонами, превратить часть нежелательных побочных продуктов со стадии гидрирования или окисления обратно в активные компоненты и удалить другие нежелательные побочные продукты. Регенерация может представлять собой фильтрацию, выпаривание воды и обработку пористым адсорбентом и катализатором на основе оксида алюминия.
Другие стадии процесса получения пероксида водорода, например окисление кислородом и экстракция водой, могут осуществляться традиционным способом, описанным в литературе.
Кроме этого, настоящее изобретение относится к композиции, применяемой в качестве рабочего раствора при производстве пероксида водорода антрахиноновым способом. Такая композиция включает смесь алкилзамещенных антрахинонов и алкилзамещенных тетрагидроантрахинонов, растворенных, в по крайней мере одном органическом растворителе, в котором 10-55 мол.%, предпочтительно 20-50 мол. %, антрахинонов и тетрагидроантрахинонов замещены амиловой группой, а молярное соотношение алкилзамещенных тетрагидроантрахинонов и алкилзамещенных антрахинонов составляет по крайней мере 1:1, предпочтительно приблизительно от 2: 1 до приблизительно 50:1, наиболее предпочтительно от приблизительно 3:1 до приблизительно 20:1. На приведенное описание процесса ссылаются в том, что касается необязательных и предпочтительных признаков композиции.
Настоящее изобретение далее будет описано дополнительно со ссылкой на следующие примеры, которые, однако, не следует интерпретировать как ограничение объема изобретения.
Пример 1
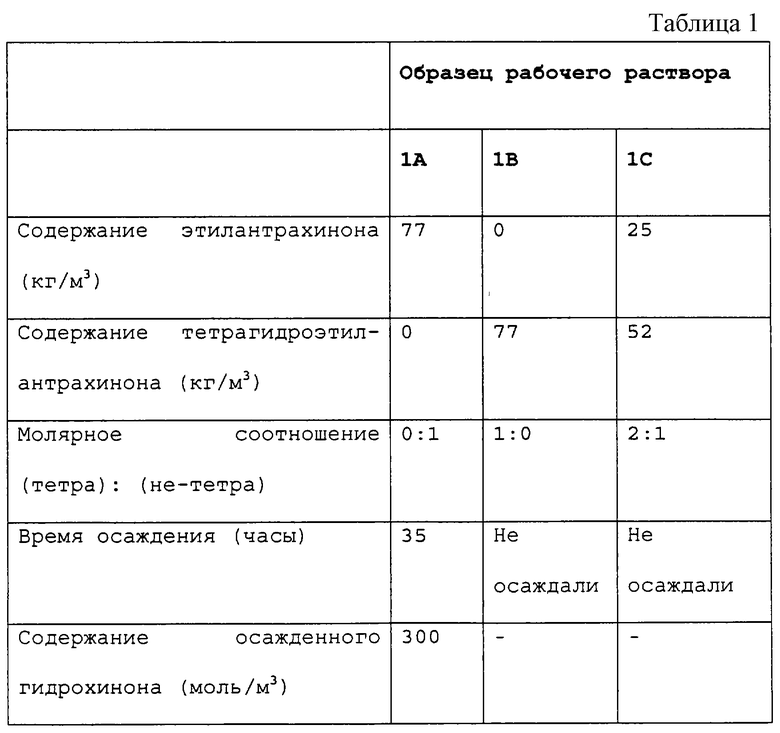
Три различных рабочих раствора, 1А, 1В и 1С, готовили растворением этилантрахинона и β-тетрагидроэтилантрахинона с применением одинаковой смеси растворителей (22 об. % тетрабутилмочевины, 3 об.% триоктилфосфата, 75 об.% триметилбензола). Каждый раствор гидрировали в реакторном блоке, содержащем неподвижный слой палладиевого катализатора на носителе из диоксида кремния. 2,5 л рабочего раствора использовали в реакторе в условиях циркуляции при 30oС. Большой избыток водорода пропускали через реактор при давлении 420 кПа (абс. ) до практически полного гидрирования хинона в гидрохинон. Полученные результаты представлены в таблице 1.
Из представленных результатов видно, что осаждение гидрированного хинона происходит при более низких концентрациях в случае этилантрахинона, по сравнению с его тетрагидроформой и смесью обеих форм.
Пример 2
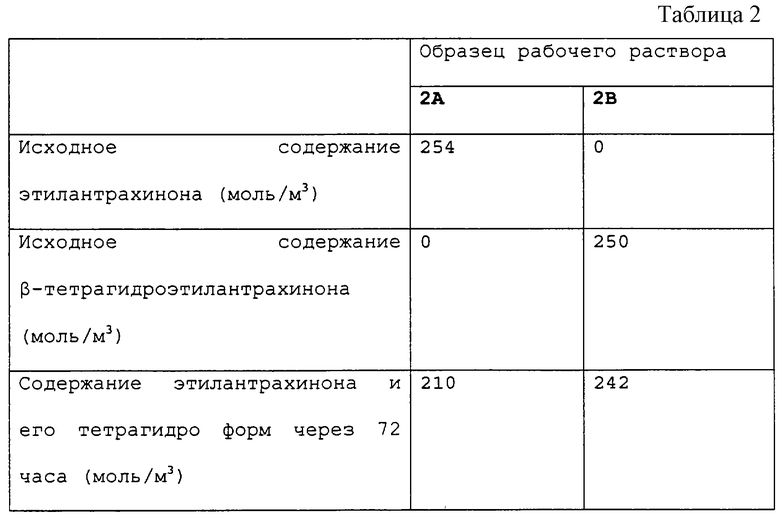
Два различных рабочих раствора, 2А и 2В, готовили растворением этилантрахинона и β-тетрагидроэтилантрахинона с применением смеси растворителей, состоящей из 25% тетрабутилмочевины и 75% триметилбензола (по объему). Каждый раствор гидрировали в лабораторном реакторе с суспензией палладиевого катализатора на носителе из диоксида кремния. 50 мл рабочего раствора использовали в условиях циркуляции в реакторе при 50oС. Водород подавали в реактор под давлением 250 кПа (абс.). Практически весь хинон гидрировался в гидрохинон менее чем за час. Гидрирование продолжали в течение 72 ч. Состав реакционной среды определяли методом ГХ-анализа, и полученные результаты представлены в таблице 2.
Из представленных данных можно сделать вывод, что этилантрахинон более подвержен деградации в ходе гидрирования, чем его тетрагидроформа.
Пример 3
Образец выдержанного рабочего раствора, отработавшего более одного года, извлекали из антрахинонового рабочего цикла, и было обнаружено, что такой раствор содержит также обычные продукты деградации. Осаждение гидрохинона исследовали с использованием образца как такового (образец 3А) и также после добавления дополнительного количества хинона. В качестве добавляемого хинона применяли β-тетрагидроэтилантрахинон (образец 3В), амилантрахинон (образец 3С) или β-тетрагидроамилантрахинон (образец 3D). Для каждого образца получали по несколько концентраций гидрохинона в результате гидрирования в лабораторном реакторе с использованием водорода и палладиевого катализатора. Образцы выдерживали при низкой температуре (от, примерно, -10 до +15oС) с целью получения осадка. За максимальную концентрацию гидрохинона принимали те образцы, в которых осадок быстро исчезал при нагревании до комнатной температуры. Концентрацию гидрохинона определяли титрованием образовавшегося пероксида водорода при окислении образца кислородом и экстракции его водой. Исходный образец рабочего раствора главным образом содержал β-форму тетрагидроэтилантрахинона, однако присутствовало небольшое количество α-формы. Амиловая группа в добавленном хиноне представляла 2-трет-пентил, а также 2-втор-изопентил (небольшая часть). Растворителем в рабочем растворе служила смесь тетрабутилмочевины и смешанных ароматических углеводородов технического сорта (главным образом углеводороды С9 и С10). Полученные результаты представлены в таблице 3.
Из полученных результатов можно сделать вывод о том, что умеренное добавление тетрагидроамилантрахинона повышает максимальное содержание гидрохинона до более высокого значения без опасности осаждения.
Пример 4
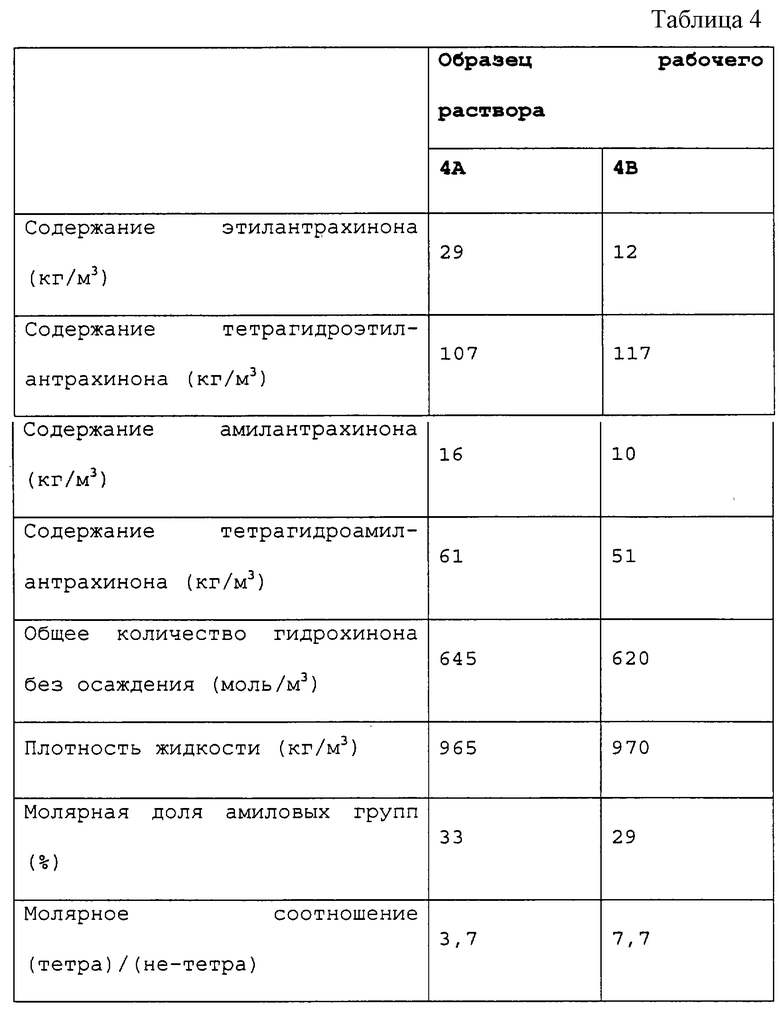
Из антрахинонового реакционного цикла отбирали два образца выдержанного рабочего раствора, отработавшего более 9 месяцев, причем такой раствор содержал также обычные продукты деградации. В качестве растворителей использовали смесь тетрабутилмочевины (образец 4А) или октилкапролактама (образец 4В) со смешанными ароматическими углеводородами технического сорта (главным образом, углеводороды С9 и С10). В обоих образцах присутствовало также небольшое количество триоктилфосфата. Композицию растворителей слегка модифицировали путем выпаривания и добавления растворительных компонентов с тем, чтобы получить подходящее количество растворителя, содержащего до 1/3 по объему гидрохинонового растворителя (тетрабутилмочевина или октилкапролактам), причем оставшееся количество представляло собой растворитель хинона. Осаждение гидрохинона изучали по методике, описанной в примере 3. Полученные результаты представлены в таблице 4.
Из полученных результатов можно сделать вывод, что очень высокая степень гидрирования может быть достигнута без опасности осаждения, даже при относительно низких концентрациях амилантрахинона и тетрагидроамилантрахинона.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПЕРОКСИДА ВОДОРОДА И КОМПОЗИЦИЯ ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2001 |
|
RU2235680C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРОКСИДА ВОДОРОДА | 2007 |
|
RU2458856C2 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА, КАТАЛИЗАТОР И СПОСОБЫ ПОЛУЧЕНИЯ ПЕРОКСИДА ВОДОРОДА | 1998 |
|
RU2150322C1 |
| ЭЛЕКТРОСИНТЕЗ ПЕРОКСИДА ВОДОРОДА | 2006 |
|
RU2380460C2 |
| СПОСОБ ПРОИЗВОДСТВА ПЕРОКСИДА ВОДОРОДА И ХЛОРАТА | 2006 |
|
RU2375500C2 |
| НОСИТЕЛЬ КАТАЛИЗАТОРА, СПОСОБ ЕГО ПОЛУЧЕНИЯ, СУСПЕНЗИЯ ДЛЯ ИСПОЛЬЗОВАНИЯ ПРИ ЕГО ПОЛУЧЕНИИ, КАТАЛИЗАТОР И ЕГО ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ ПЕРОКСИДА ВОДОРОДА | 2001 |
|
RU2215578C2 |
| СПОСОБ ПРОИЗВОДСТВА ПЕРОКСИДА ВОДОРОДА | 2012 |
|
RU2609474C2 |
| МЕТОД ПРОИЗВОДСТВА ПЕРОКСИДА ВОДОРОДА | 2012 |
|
RU2616701C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРОКСИДА ВОДОРОДА И НОСИТЕЛИ РЕАКЦИИ ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1999 |
|
RU2220903C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЩЕЛОЧНОГО РАСТВОРА ПЕРОКСИДА ВОДОРОДА И ДИОКСИДА ХЛОРА | 2000 |
|
RU2221741C1 |

Изобретение предназначено для химической промышленности. Пероксид водорода получают атрахиноновым методом, чередуя стадии гидрирования и окисления смеси алкилзамещенных антрахинонов и алкилзамещенных тетрагидроантрахинонов, растворенных по крайней мере в одном органическом растворителе. В этой смеси 10-55 мол. % алкилзамещенных антрахинонов и алкилзамещенных тетрагидроантрахинонов замещены амиловой группой. Молярное соотношение алкилзамещенных тетрагидроантрахинонов и алкилзамещенных антрахинонов по крайней мере 1:1, предпочтительно 50: 1. От 55 до 80 мол.% антрахинонов и тетрагидроантрахинонов замещены одной этильной группой. Органическим растворителем может быть один или более гидрохиноновых растворителей из группы, включающей алкилфосфаты, тетраалкилмочевины, производные циклической мочевины и алкилзамещенные капролактамы. Композиция, содержащая указанную смесь, практически свободна от незамещенного антрахинона и тетрагидроантрахинона. Рабочий раствор обладает высокой растворимостью, позволяет использовать высокие концентрации гидрохинонов, устойчив к побочным реакциям в ходе гидрирования. 2 с. и 8 з.п. ф-лы, 4 табл.
| US 5399333 А, 21.03.1995 | |||
| СПОСОБ ПОЛУЧЕНИЯ ПЕРЕКИСИ ВОДОРОДА | 1971 |
|
SU421174A3 |
| US 4800073 А, 24.01.1989 | |||
| US 4800074 А, 24.01.1989 | |||
| Приспособление к трактору для замера обработанной площади | 1937 |
|
SU62559A1 |
| МАШИНА ДЛЯ ОБРАЗОВАНИЯ В ГРУНТЕ ВЫЕМКИ ТИПА КОТЛОВАНА | 0 |
|
SU286610A1 |
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
Авторы
Даты
2003-01-10—Публикация
2000-11-21—Подача