ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к способу получения пероксида водорода в электрохимической ячейке катодным восстановлением кислорода. Изобретение также относится к получению диоксида хлора.
УРОВЕНЬ ТЕХНИКИ
Щелочные растворы пероксида водорода обычно используют для отбелки и/или делигнификации целлюлозной волокнистой массы. Пероксид водорода обычно получают на больших предприятиях, используя антрахиноновый способ, и транспортируют на целлюлозные комбинаты. Антрахиноновый способ является очень эффективным, однако требует значительных капиталовложений и не пригоден в случае производства в небольшом объеме на месте потребления пероксида водорода.
Электрохимическое получение щелочных растворов пероксида водорода раскрыто в патенте США 5702585 "Способ получения смесей каустической соды и пероксида водорода путем восстановления кислорода", а также в работах Р.С. Foller et al, Journal of Applied Electrochemistry, 25 (1995), pp.613-627; С. Oloman "Electrochemical Processing for the Pulp and Paper Industry", The Electrochemical Consultancy 1996, pp.143-152. Однако ни в одном из этих документов не раскрыт способ, который был бы достаточно гибким для того, чтобы получать различные соотношения NaOH:H2О2 в сочетании с возможностью получения одного или более других химических продуктов, которые можно было бы использовать на целлюлозных предприятиях.
Диоксид хлора также представляет собой широко используемый на целлюлозном производстве отбеливающий агент. Вследствие химической неустойчивости диоксида хлора его всегда получают непосредственно на месте потребления, для этого коммерчески используют множество разнообразных способов, например такие, как описано в патенте США 5770171, патенте США 5091166, патенте США 5091167 и документе ЕР 612686. Большинство коммерческих процессов включают взаимодействие хлората натрия с минеральной кислотой, обычно серной кислотой, и восстанавливающим агентом, таким как хлорид-ионы, диоксид серы, метанол или пероксид водорода, в кислой реакционной среде. В качестве побочного продукта обычно получают сульфат натрия, либо в виде кислого или нейтрального твердого сульфата натрия, либо в форме кислого остающегося раствора. На многих современных целлюлозных производствах сульфатный побочный продукт рассматривают как бесполезные отходы, которые необходимо удалять, хотя все еще имеется необходимость в некотором количестве сульфата для приготовления варочного щелока.
Образование сульфатного побочного продукта может быть снижено или полностью исключено путем замены части или всего количества хлората натрия хлорноватой кислотой, как описано в WO 93/25470. Также возможно электрохимически подкислять получаемый твердый сульфат натрия, как описано в патенте США 5198080, или электрохимически подкислять отработанную реакционную среду, без кристаллизации, как описано в патенте США 5487881. Однако ни один из этих методов до настоящего времени коммерчески не используется.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Целью настоящего изобретения является создание электрохимического способа получения щелочного раствора пероксида водорода, который мог бы быть использован в разнообразных процессах отбеливания, например, таких как отбелка и/или делигнификация целлюлозной волокнистой массы, в частности, в последовательных технологических процессах ECF (без использования элементарного хлора) и в последовательных технологических процессах TCF (полностью без использования хлора в каком-либо виде), или для осветления целлюлозной массы.
Другой целью настоящего изобретения является создание электрохимического способа получения щелочных растворов пероксида водорода, согласно которому получают один или более других химических продуктов, которые могли бы быть использованы на целлюлозных предприятиях, в частности подкисленный раствор, содержащий хлорат, пригодный для использования при получении диоксида хлора.
Еще одной целью настоящего изобретения является создание электрохимического способа получения щелочных растворов пероксида водорода, согласно которому один или более побочных продуктов получения диоксида хлора могут быть использованы в качестве сырья, пригодного для переработки.
Еще одной целью настоящего изобретения является создание электрохимического способа получения пероксида водорода и диоксида хлора, который отличается гибкостью в отношении количества получаемого побочного продукта - сульфата.
Эти цели достигаются при осуществлении способа, определенного прилагаемой формулой изобретения.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Согласно одному из своих аспектов изобретение относится к непрерывному способу получения щелочного раствора пероксида водорода и подкисленного раствора соли щелочного металла в электрохимической ячейке, включающей анодное отделение, снабженное анодом, и катодное отделение, снабженное катодом для восстановления кислорода. Способ включает следующие стадии:
(a) подачу водного раствора соли щелочного металла, содержащего хлорат, в анодное отделение;
(b) взаимодействие на аноде указанного раствора соли щелочного металла для получения Н+ и образования в анодном отделении подкисленного водного раствора соли щелочного металла;
(c) перенос Н+ и ионов щелочного металла из анодного отделения в катодное отделение;
(d) подачу кислорода или содержащей кислород жидкости и воды в катодное отделение;
(e) взаимодействие на катоде указанного кислорода и воды с образованием водного щелочного раствора, содержащего в катодном отделении пероксид водорода (Н2О2) и гидроксид щелочного металла (МОН);
(f) удаление подкисленного водного раствора соли щелочного металла, образованного в анодном отделении;
(g) удаление щелочного водного раствора пероксида водорода, образованного в катодном отделении;
причем молярное соотношение МОН:Н2О2 для результирующего продукта, содержащего гидроксид щелочного металла и пероксид водорода, в катодном отделении на стадии (е) поддерживается на уровне от приблизительно 0,1:1 до приблизительно 2:1, подходящим образом, от приблизительно 0,1:1 до приблизительно 1,8:1, предпочтительно от приблизительно 0,1:1 до приблизительно 1,7:1, наиболее предпочтительно от приблизительно 0,5:1 до приблизительно 1,7:1. М относится к щелочному металлу, например, такому как натрий, калий или их смесь, среди указанных металлов наиболее предпочтительным является натрий.
Термины - катодное отделение и анодное отделение при использовании в настоящем описании также включают возможный рециркуляционный контур для анолита (электролита в прианодной области) и католита (электролита в прикатодной области). Анодное и катодное отделение подходящим образом разделяются, по меньшей мере, одной перегородкой, например, такой как мембрана или диафрагма, проницаемой для Н+ и ионов щелочного металла, но предпочтительно непроницаемой для таких анионов, как гидроксиди пергидроксил-ионы. Перегородка представляет собой, по меньшей мере, одну ионообменную мембрану, наиболее предпочтительно, по меньшей мере, одну катионообменную мембрану. Предпочтительными являются обычные полимерные ионообменные мембраны, но также могут быть использованы ионообменные мембраны с высокой проницаемостью, такие как керамические мембраны. В большинстве случаев используют ячейки с двумя отделениями, но также могут быть приняты во внимание ячейки, включающие одно или более отделение между анодным и катодным отделениями.
Может быть использован любой восстанавливающий кислород катод, хотя предпочтительным является, когда катод выполнен из углерода, например графита или сажи, возможно в сочетании с другими введенными в его состав материалами, например, такими как инертные химически стойкие полимеры (например, PTFE политетрафторэтилен) или каталитически активные материалы (например, золото, цинк или подобные им материалы), причем последние подходящим образом могут быть использованы в виде частичного покрытия на углероде. Вследствие низкой растворимости кислорода в католите в качестве катода предпочтителен трехмерный электрод. Одна из групп трехмерных электродов включает неподвижные слои высокой пористости, например, сетчатые слои (например, Reticulated Vitreous Carbon), слои из частиц или материал типа войлока (материал типа войлока на основе графита) или слои из нетканых волокон (например, углеродных волокон), все эти материалы являются коммерчески доступными. Эти типы неподвижных слоев могут быть выполнены в виде катода для струйного течения жидкости. Другая группа трехмерных электродов включает микропористые, возможно слоистые, электроды, допускающие диффузию газов, которые, например, могут быть выполнены из пористого углерода. Такие газодиффузионные электроды являются коммерчески доступными и схожи с электродами, которые используют, например, в топливных элементах.
В качестве анода может быть использован любой обычный тип электродов, например, такой как анод из титана, покрытого оксидами драгоценных металлов, например DSA O2 TM, или газовые электроды, такие как поляризованные водородные аноды.
Водный раствор, подаваемый в анодное отделение на стадии (а), представляет собой необязательно кислый раствор, содержащий хлорат щелочного металла, также необязательно содержащий сульфат щелочного металла и/или другие соли щелочного металла. Раствор подходящим образом содержит от приблизительно 0,5 моль/л солей щелочного металла вплоть до насыщенного раствора, предпочтительно, от приблизительно 1 до приблизительно 12 моль/л солей щелочного металла. Кислотность предпочтительно составляет от приблизительно 0 до приблизительно 11 Н, более предпочтительно, от приблизительно 0 до приблизительно 9 Н. Согласно одному из предпочтительных воплощений изобретения раствор получают непосредственно или косвенным образом из генератора диоксида хлора. Например, раствор, содержащий щелочной металл, может представлять собой отработанную кислую реакционную среду из генератора диоксида хлора, необязательно дополнительно подкисленную электрохимическими методами, или нейтральный или кислый сульфат щелочного металла, полученный в качестве побочного продукта при получении диоксида хлора. В соответствии с другим предпочтительным воплощением изобретения раствор предпочтительно по существу нейтрального хлората щелочного металла подают в анодное отделение.
На аноде находящаяся в растворе вода взаимодействует на стадии (b) с образованием при этом H+ и, как правило, также кислорода. Как полагают, имеет место следующая реакция:
Н2О --> 2H+ + 1/2 O2 + 2е-.
Разность потенциалов в ячейке приводит на стадии (с) к перемещению катионов по направлению к катоду. Таким образом, как ионы щелочного металла, так и ионы H+ переносятся из анодного отделения в катодное отделение. Однако все количество образовавшихся ионов Н+ не переносится, при этом соответственно в анодном отделении остается раствор продукта - подкисленной соли щелочного металла, который предпочтительно содержит сульфат, хлорат или их смесь.
Кислород может подаваться в катодное отделение на стадии (d) совместно с подаваемым католитом, подходящим образом при достаточно высоком давлении для того чтобы, по меньшей мере, частично быть растворенным в католите, например, при давлении от приблизительно 100 до приблизительно 2000 кПа. Высокое давление повышает плотность тока, но также повышает и стоимость ячейки вследствие более сложной конструкции. Если в качестве катода используется газодиффузионный электрод, кислород предпочтительно подают в виде газа, наиболее предпочтительно вместе с парами воды, в газовую камеру, из которой он диффундирует внутрь катода. Некоторое количество кислорода может представлять собой вторичный кислород, взятый из кислорода, образовавшегося на аноде на стадии (b). Также возможно использовать кислород, образующийся при получении диоксида хлора при использовании пероксида водорода в качестве восстанавливающего агента.
На стадии (е) вода и кислород взаимодействует на катоде с образованием при этом пергидроксил- и гидроксид-ионов.
Как полагают, имеет место следующая реакция:
H2O+О2+2е- --> HO2 -+ОН-.
Вместе с H+ и ионами щелочного металла, перенесенными из анодного отделения, продукты реакции будут образовывать водный раствор продукта в катодном отделении, содержащий пероксид водорода и гидроксид щелочного металла, соответствующим образом с концентрацией от приблизительно 1 до приблизительно 15 мас.%, предпочтительно от приблизительно 2 до приблизительно 10 мас.% пероксида водорода, и соответствующим образом от приблизительно 2 до приблизительно 20 мас.%, предпочтительно от приблизительно 4 до приблизительно 15 мас. % гидроксида щелочного металла. Молярное соотношение МОН:Н2О2 в получаемом продукте, содержащем гидроксид щелочного металла и пероксид водорода, зависит от соотношения количества ионов щелочного металла к количеству ионов Н+, перенесенных из анодного отделения, которое определяется соответствующим соотношением в анодном отделении. Путем регулировки кислотности раствора соли щелочного металла, получаемого в анодном отделении, может быть проконтролировано молярное соотношение МОН:Н2О2. Кроме того, устанавливая заданную продолжительность пребывания в анодном отделении, можно контролировать степень конверсии и кислотность получаемого раствора щелочного металла, и таким образом, также контролировать молярное соотношение МОН:Н2О2, получаемое в катодном отделении. Низкое молярное соотношение, т.е. значительное количество пероксида водорода дает возможность использовать раствор для большинства способов отбеливания, например таких, как в последовательных технологических процессах ECF (без использования элементарного хлора) и в последовательных технологических процессах TCF (полностью без использования хлора в каком-либо виде), или для осветления целлюлозной массы. С другой стороны, это требует низкого молярного соотношения количества ионов щелочного металла к количеству ионов Н+, перенесенных в катодное отделение, что снижает коэффициент использования тока. Предпочтительно оперировать со степенью конверсии ионов щелочного металла в Н+ в анодном отделении, равной от приблизительно 0,05 до приблизительно 90%, наиболее предпочтительно от приблизительно 0,1 до приблизительно 80%, отчасти в зависимости от того, соль какого щелочного металла используют. В случае раствора хлората натрия степень конверсии соответствующим образом составляет от приблизительно 2 до приблизительно 80%, предпочтительно от приблизительно 7 до приблизительно 60%, наиболее предпочтительно от приблизительно 7 до приблизительно 40%. Коэффициент использования тока для получения гидроксида щелочного металла (соответствует коэффициенту использования тока для переноса ионов щелочного металла из анодного в катодное отделение) составляет предпочтительно от приблизительно 3 до приблизительно 85%, наиболее предпочтительно от 20 до почти 70%.
На стадиях (f) и (g) растворы продуктов, полученных в анодном и катодном отделениях, просто удаляют. Подкисленный раствор щелочного металла, полученный в анодном отделении, может быть затем использован в качестве сырья для получения диоксида хлора, в то время как щелочной раствор пероксида водорода, полученный в катодном отделении, может быть затем использован для отбеливания и/или делигнификации целлюлозной массы.
Во многих случаях может быть выгодно соединить две или более ячейки, как описано выше, последовательным образом. Затем возможно последовательно подавать только анолит (со стадии (f) в первой ячейке на стадию (а) в последующей ячейке), только католит (со стадии (g) в первой ячейке на стадию (d) в последующей ячейке) или как анолит, так и католит.
Щелочной металл, о котором идет речь в настоящем описании, подходящим образом представляет собой натрий, калий или их смеси, предпочтительно, натрий.
Предпочтительное осуществление изобретения относится к непрерывному способу получения пероксида водорода и одновременному получению диоксида хлора посредством восстановления хлорат-ионов в кислой реакционной среде, поддерживаемой в реакторе, и включает следующие стадии:
(i) получение щелочного раствора пероксида водорода и подкисленного раствора соли щелочного металла путем выполнения стадий от (а) до (g), как описано выше;
(ii) подачу в реакционную среду, имеющуюся в реакторе, подкисленного водного раствора соли щелочного металла, удаленного из анодного отделения на указанной выше стадии (f);
(iii) восстановление хлорат-ионов в реакционной среде с получением при этом диоксида хлора предпочтительно с использованием восстанавливающего агента, наиболее предпочтительно пероксида водорода; и
(iv) удаление диоксида хлора из реактора.
При таком осуществлении изобретения раствор соли щелочного металла на стадии (а) соответствующим образом имеет концентрацию от приблизительно 0,5 моль/л вплоть до насыщенного раствора, предпочтительно от приблизительно 2 до приблизительно 12 моль/л, наиболее предпочтительно, от приблизительно 3 до приблизительно 8 моль/л. В том случае, если раствор представляет собой раствор хлората щелочного металла, кислотность предпочтительно составляет от приблизительно 0 до приблизительно 5 Н, наиболее предпочтительно, от приблизительно 0 до приблизительно 4 Н. В том случае, если раствор представляет собой раствор смеси сульфата и хлората, кислотность соответствующим образом составляет от приблизительно 0 до приблизительно 11 Н, наиболее предпочтительно от приблизительно 0,5 до приблизительно 9 Н.
Особенно предпочтительно подавать на стадии (а) в анодное отделение по существу нейтральный раствор хлората щелочного металла, получая таким образом смесь хлорноватой кислоты и хлората щелочного металла, которую удаляют на стадии (f) и используют в качестве сырья на стадии (ii).
Диоксид хлора может быть получен на стадии (iii) и (iv) в соответствии с любым известным способом, согласно которому восстанавливают хлорат-ионы, с использованием восстанавливающего агента или электрохимическим способом, включая способы, которые описаны в упоминавшихся ранее патенте США 5770171, патенте США 5091166, патенте США 5091167 и WO 93/25470. Эти предпочтительные способы включают подачу в кислую реакционную среду серной кислоты, восстанавливающего агента, предпочтительно метанола, пероксида водорода или их смеси, хлората щелочного металла и/или хлорноватой кислоты. В реакционной среде, предпочтительно, поддерживаемой при давлении ниже атмосферного, хлорат-ионы восстанавливаются до диоксида хлора, который удаляют в виде газа, в то время как сульфат щелочного металла образуется в виде побочного продукта, обычно как твердый кислый или нейтральный сульфат натрия. Также возможно получать диоксид хлора при по существу атмосферном давлении, как описано в ЕР 612686, или путем использования других восстанавливающих агентов как одного, так и смеси, например, такого как хлорид-ионы, диоксид серы, или органические вещества, например этанол, изопропанол, другие спирты и формальдегид. Кислотность подкисленного раствора соли щелочного металла, подаваемого на стадию (ii), определяет количество серной кислоты, которая должна быть подана, и таким образом также - количество образующегося побочного продукта - сульфата. В соответствии с этим, возможно регулировать осуществление способа таким образом, чтобы получать такое количество побочного продукта - сульфата, которое необходимо на каждом конкретном целлюлозном производстве.
Конечное количество побочного продукта - сульфата, образующегося при получении диоксида хлора, также может быть снижено при использовании его раствора в качестве сырья, подаваемого в анодное отделение на стадии (а), в сочетании с хлоратом щелочного металла. Подкисленный раствор соли щелочного металла, который удаляют на стадии (g) и подают на стадию (ii), будет тогда представлять собой смесь, содержащую сульфат щелочного металла, серную кислоту, хлорат щелочного металла и хлорноватую кислоту. Количество серной кислоты, добавляемой из внешних источников, будет в этом случае снижено в той мере, которая зависит от степени превращения в анодном отделении на стадии (b). Таким образом, также и в этом случае возможно контролировать конечный выход образующегося побочного продукта - сульфата, и регулировать его в зависимости от требований для каждого конкретного целлюлозного производства.
Согласно варианту такого осуществления изобретения отработанная реакционная среда, полученная при производстве диоксида хлора на стадии (iii), выводится из реактора, предпочтительно по существу без кристаллизации солей щелочного металла, и используется в качестве сырья, подаваемого в анодное отделение на стадии (а). Этот водный раствор будет в этом случае соответствующим образом содержать сульфат щелочного металла, хлорат щелочного металла и соответственно иметь кислотность от приблизительно 0,5 до приблизительно 11 Н, предпочтительно от приблизительно 3 до приблизительно 9 Н, наиболее предпочтительно от приблизительно 3 до приблизительно 8 Н. Концентрация сульфата составляет соответственно от 0,5 моль/л до насыщенного раствора, предпочтительно от приблизительно 1 до приблизительно 8 моль/л, наиболее предпочтительно от приблизительно 1 до приблизительно 6 моль/л, в то время как концентрация хлората составляет соответственно от 0,5 моль/л до насыщенного раствора, предпочтительно от приблизительно 1 до приблизительно 5 моль/л, наиболее предпочтительно от приблизительно 1 до приблизительно 4 моль/л. Предпочтительно молярное соотношение Н+: SО4 2- составляет от приблизительно 0,5 до приблизительно 1,5, наиболее предпочтительно от приблизительно 0,7 до приблизительно 1,3. Степень конверсии ионов щелочного металла с образованием ионов Н+ в анодном отделении предпочтительно составляет от приблизительно 0,05 до приблизительно 20%, наиболее предпочтительно от приблизительно 0,1 до приблизительно 10%. Подкисленный раствор соли щелочного металла затем используется в качестве сырья на стадии (ii). Возможно в результате по существу избежать конечного образования побочного продукта - сульфата. Весь способ может осуществляться таким же точно образом, как способ, описанный в упоминавшемся ранее патенте US 5487881, с тем исключением, что стадия электрохимического подкисления осуществляется так, как описано выше, и таким образом, также связана с одновременным получением щелочного раствора пероксида водорода.
Согласно еще одному варианту осуществления изобретения отработанная реакционная среда, полученная при производстве диоксида хлора на стадии (iii), выводится из реактора, в котором осуществлялось получение диоксида хлора, таким же самым образом и точно такого же предпочтительного состава, как описано выше. Удаляемая реакционная среда сначала электрохимически подкисляется в ячейке, в которой также получают гидроксид щелочного металла, после чего подкисленная реакционная среда дополнительно подкисляется в электрохимической ячейке согласно стадии (i) и, в заключение, используется в качестве подаваемого сырья на стадии (ii). Этот вариант выполнения способа может быть осуществлен также, как в патенте US 5487881, с тем исключением, что подкисление отработанной реакционной среды проводят, по меньшей мере, в две стадии, причем первая стадия включает одновременное получение гидроксида щелочного металла, а вторая стадия включает одновременное получение щелочного раствора пероксида водорода. Также может быть описан вариант непрерывного способа получения пероксида водорода и одновременного получения диоксида хлора путем восстановления хлорат-ионов в кислой реакционной среде, поддерживаемой в реакторе, способ включает:
(i) получение щелочного раствора пероксида водорода и подкисленного раствора соли щелочного металла путем выполнения стадий от (а) до (g), как описано выше;
(ii) подачу в реакционную среду в реакторе подкисленного водного раствора соли щелочного металла, удаленного из анодного отделения на стадии (f) стадии (i);
(iii) восстановление хлорат-ионов в реакционной среде с получением при этом диоксида хлора;
(iv) удаление диоксида хлора из реактора;
(v) удаление отработанной реакционной среды из реактора;
(vi) подкисление отработанной реакционной среды со стадии (v) в электрохимической ячейке при одновременном получении гидроксида щелочного металла; и
(vii) использование подкисленной реакционной среды со стадии (vi) в качестве сырья, подаваемого на стадию (а) стадии (i).
Путем варьирования получения гидроксида щелочного металла на различных стадиях, от стадии (i) до стадии (vi), может быть отрегулировано получение чистого гидроксида щелочного металла, а также соотношение гидроксида щелочного металла к пероксиду водорода таким образом, чтобы отвечать конкретным требованиям на каждом отдельном целлюлозном производстве. Также возможно в значительной степени избежать образования в результате осуществления способа побочного продукта-сульфата.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг. 1 схематически представлена электрохимическая ячейка для получения подкисленного раствора соли щелочного металла и щелочного раствора пероксида водорода. На фиг.2 схематически представлена карта технологического процесса получения диоксида хлора, гидроксида щелочного металла и щелочного раствора пероксида водорода.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНОГО СПОСОБА ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Некоторые предпочтительные способы осуществления изобретения будут далее описаны более подробно со ссылкой на чертежи.
На фиг.1 представлена ячейка 1 с двумя отделениями, с анодным отделением 2, включающим рециркуляционный контур 7 и снабженным анодом 3 марки DSATM, и с катодным отделением 4, включающим рециркуляционный контур 8 и снабженным восстанавливающим кислород газодиффузионным катодом 5. Отделения 2 и 4 отделяются катионообменной мембраной 6. Рядом с газодиффузионным катодом 5 находится газовая камера 9. Если используется другой тип трехмерного катода, газовую камеру 9 обычно исключают.
В действии, кислый водный раствор 21 сульфата натрия и хлората натрия, содержащий соответственно Na+, H+, СlO3 -, SO4 2- и H2O, непрерывно подают в анодное отделение 2. Этот раствор 21 может, например, представлять собой отработанную реакционную среду из реактора, в котором осуществляют получение диоксида хлора. На аноде 3 Н2О расщепляется на О2 и H+, таким образом, дополнительно повышая кислотность раствора. Вследствие наличия разности потенциалов в ячейке некоторые из ионов Na+ и H+ перемещаются из анодного отделения 2, через мембрану 6, в катодное отделение 4. В результате этого водный раствор, образовавшийся в анодном отделении 2, и циркулирующий по замкнутому контуру 7, т.е. анолит будет содержать те же самые компоненты, что и питающий раствор, но характеризоваться более высоким содержанием H+ и более низким содержанием Na+. Часть этого раствора выводится в виде продукта 22 вместе с кислородом.
Одновременно влажный кислород, т. е. О2 и H2O в виде газа непрерывно подаются в катодное отделение 4, тогда как католит, содержащий NaOH, H2О2 и Н2О, циркулирует по замкнутому контуру 8. Газообразные компоненты диффундируют в катод 5 и взаимодействуют с образованием ОН- и НО2 -, которые, соединяясь с Na+ и H+, переносятся из анодного отделения 2 через мембрану 6 и образуют пероксид водорода и гидроксид натрия. Часть католита выводится в виде продукта 23, в то время как компенсирующее количество воды подается в замкнутый контур 8.
Работа ячейки с другим типом трехмерного катода, нежели газодиффузионный электрод, осуществляется аналогичным образом, хотя кислород подают не в газовую камеру, а в католит, в котором кислород, по меньшей мере, частично растворяется. Давление в катодном отделении в этом случае составляет от приблизительно 100 до приблизительно 2000 кПа, при этом предпочтительно, чтобы в анодном отделении давление было незначительно выше, поскольку это повысит надежность, если произойдет просачивание через мембрану и возможно также повысит коэффициент использования тока.
Согласно одному из режимов работы раствор натриевой соли в анодном отделении 2 имеет следующий состав: 4,2 моль/л сульфата, 3,5 моль/л хлората и кислотность составляет 5,2 Н. При использовании газодиффузионного катода 5, без катализатора, изготовленного из углерода, обладающего площадью поверхности от низкой до средней, подавая в избытке влажный кислород и работая при плотности тока приблизительно 500 А/м2, а также поддерживая постоянную концентрацию анолита на уровне щелочности, соответствующей 6 мас.% NaOH, конечный продукт в катодном отделении 4 будет представлять собой продукт 23, характеризующийся молярным соотношением NaOH: H2О2, равным приблизительно 1,6, и концентрацией гидроксида натрия, равной 6 мас.%. Степень конверсии из Na+ в Н+ составит 1,6% при подаваемом токе 270 А мин на литр анолита, в то время как коэффициент использования тока для образования гидроксида натрия составит приблизительно 65%.
В соответствии с другим режимом работы - подкислении нейтрального раствора хлората натрия по существу свободного от сульфата, раствор в анодном отделении 2 содержит 5 моль/л хлората и имеет кислотность 0,5 Н. При использовании газодиффузионного катода 5 без катализатора, изготовленного из углерода, обладающего площадью поверхности от низкой до средней, подавая в избытке влажный кислород и работая при плотности тока приблизительно 500 А/м2, а также поддерживая постоянную концентрацию анолита на уровне щелочности, соответствующей 6 мас.% NaOH, конечный продукт в катодном отделении 4 будет представлять собой продукт 23, характеризующийся молярным соотношением NаОН: Н2O2, равным 1,4, и концентрацией гидроксида натрия, равной 6 мас.%. Степень конверсии из Na+ в Н+ составит 10%, в то время как коэффициент использования тока для образования гидроксида натрия составит 60%.
На фиг.2 представлен вариант процесса одновременного получения диоксида хлора, пероксида водорода и гидроксида натрия. В реактор для получения диоксида хлора 10, работающий как описано в упоминавшемся ранее патенте США 5487881, и включающий водную кислую реакционную среду, содержащую Na+, Н+, СlO3 - и SO4 2-, осуществляют непрерывную подачу NаСl3, Н2O2 и кислого водного раствора 22, содержащего Na+, Н+, СlO3 - и SO42-. В реакторе 10 СlO3 - взаимодействует с Н2O2 и Н+ с образованием при этом СlO2 и O2, которые выводят в виде газов. Отработанную реакционную среду 20, по существу того же самого состава, что и среда внутри реактора 10, удаляют без кристаллизации и подают в электрохимическую ячейку 11, также производя операции таким образом, как описано в патенте США 5487881, и получая таким образом подкисленный раствор 21, содержащий те же самые компоненты, что и питающий раствор 20, но с более высоким содержанием Н+ и с более низким содержанием Na+. Одновременно в ячейке 11 получают гидроксид натрия из воды и ионов натрия, извлекаемых из питающего раствора 20. Количество получаемого гидроксида натрия возрастает со степенью конверсии подкисления. В соответствии с предпочтительным способом подкисление раствора 20 с получением раствора 21 завершается в анодном отделении ячейки с двумя отделениями 11, разделенной катионообменной мембраной, в то время как гидроксид натрия образуется в катодном отделении. Подкисленный раствор 21 подают в анодное отделение ячейки 1, как показано на фиг. 1, и проводят описанные выше операции. Подкисленный раствор продукта 22 затем возвращают в реактор получения диоксида хлора 10, таким образом устраняя необходимость в подаче кислоты из внешних источников и исключая образование в результате осуществления процесса побочного продукта - сульфата. Газообразные СlO2 и O2, удаляемые из реактора 10, передают в абсорбер 12, в котором СlO2 абсорбируется водой, в то время как O2 перемещается в ячейку 1 и используется для получения Н2O2 и NaOH. Посредством варьирования степени подкисления в двух ячейках 11 и 1 получение гидроксида натрия и пероксида водорода может быть отрегулировано для того, чтобы соответствовать требованиям, выдвигаемым в каждом конкретном случае.
Изобретение далее будет проиллюстрировано посредством следующего примера, который, однако, не следует интерпретировать как ограничивающий объем изобретения. Если не указано иное, то все части и проценты относятся к частям и процентам по массе.
Пример
Хлорноватую кислоту и щелочной пероксид водорода получают одновременно в лабораторной ячейке, содержащей два отделения и снабженной анодом Ti/DSA (240 см2), восстанавливающим кислород катодом, выполненным из графитового войлока (поверхность внешняя 240 см2, истинная 104 см2), и катионообменной мембраной NafionTM 450. Водный раствор хлората натрия и хлорноватой кислоты подают в анодное отделение, в то время как водный раствор гидроксида натрия и кислорода подают в катодное отделение. На выпуске анолита температура составляет приблизительно 35-40oС, а давление - приблизительно 240-500 кПа. На выпуске католита температура составляет приблизительно 40-44oС, а давление - приблизительно 101-450 кПа. Из практических соображений ячейка работает с однократным прохождением католита, в то время как анолит, выходящий из ячейки, подвергается рециркуляции и частично нейтрализуется с использованием гидроксида натрия перед повторным введением в анодное отделение. Образцы анолита и католита отбирают у соответствующих выпускных отверстий и анализируют, оценивая коэффициент использования тока (С.Е.) для образования пероксида водорода и транспорт натрия через мембрану (соответствует образованию гидроксида натрия). В приведенной ниже таблице представлены стационарные значения для различных режимов работы.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ПОЛУЧЕНИЯ ДИОКСИДА ХЛОРА | 1991 |
|
RU2112817C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРЕКИСИ ВОДОРОДА | 2010 |
|
RU2494960C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДНОГО ПОДКИСЛЕННОГО РАСТВОРА, СОДЕРЖАЩЕГО ХЛОРАТНЫЕ ИОНЫ, СПОСОБ ЭЛЕКТРОХИМИЧЕСКОЙ ОБРАБОТКИ ВОДНОГО РАСТВОРА СМЕСИ СОЛЕЙ ЩЕЛОЧНЫХ МЕТАЛЛОВ, СПОСОБ ПОЛУЧЕНИЯ ДВУОКИСИ ХЛОРА | 1991 |
|
RU2108413C1 |
| СПОСОБ ПРОИЗВОДСТВА ПЕРОКСИДА ВОДОРОДА И ХЛОРАТА | 2006 |
|
RU2375500C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДВУОКИСИ ХЛОРА | 1994 |
|
RU2084557C1 |
| ЭЛЕКТРОСИНТЕЗ ПЕРОКСИДА ВОДОРОДА | 2006 |
|
RU2380460C2 |
| СПОСОБ И УСТРОЙСТВО ДЛЯ ПРОИЗВОДСТВА ДИОКСИДА ХЛОРА | 2005 |
|
RU2350550C1 |
| УСТРОЙСТВО ДЛЯ ПОЛУЧЕНИЯ ПРОДУКТОВ ЭЛЕКТРОЛИЗА РАСТВОРА ХЛОРИДА ЩЕЛОЧНОГО МЕТАЛЛА | 2018 |
|
RU2769053C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРАТА ЩЕЛОЧНОГО МЕТАЛЛА | 2003 |
|
RU2317351C2 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОГО ОКИСЛЕНИЯ БРОМИДА ДО БРОМА | 2003 |
|
RU2316616C2 |
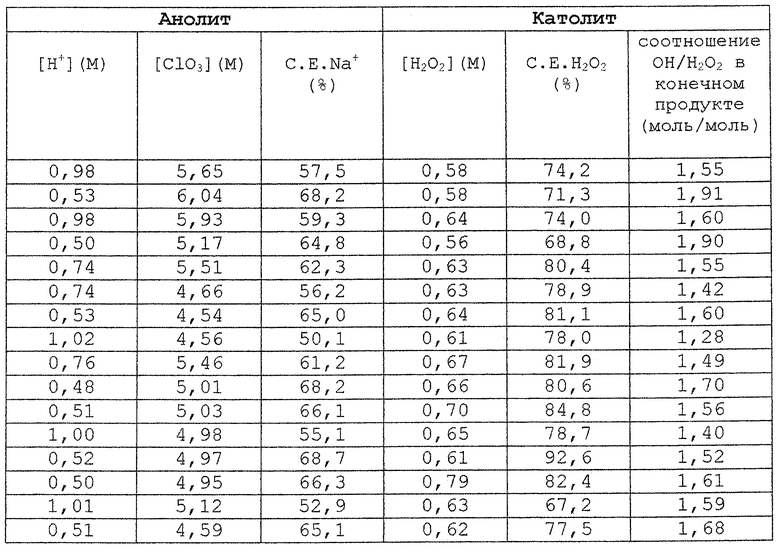
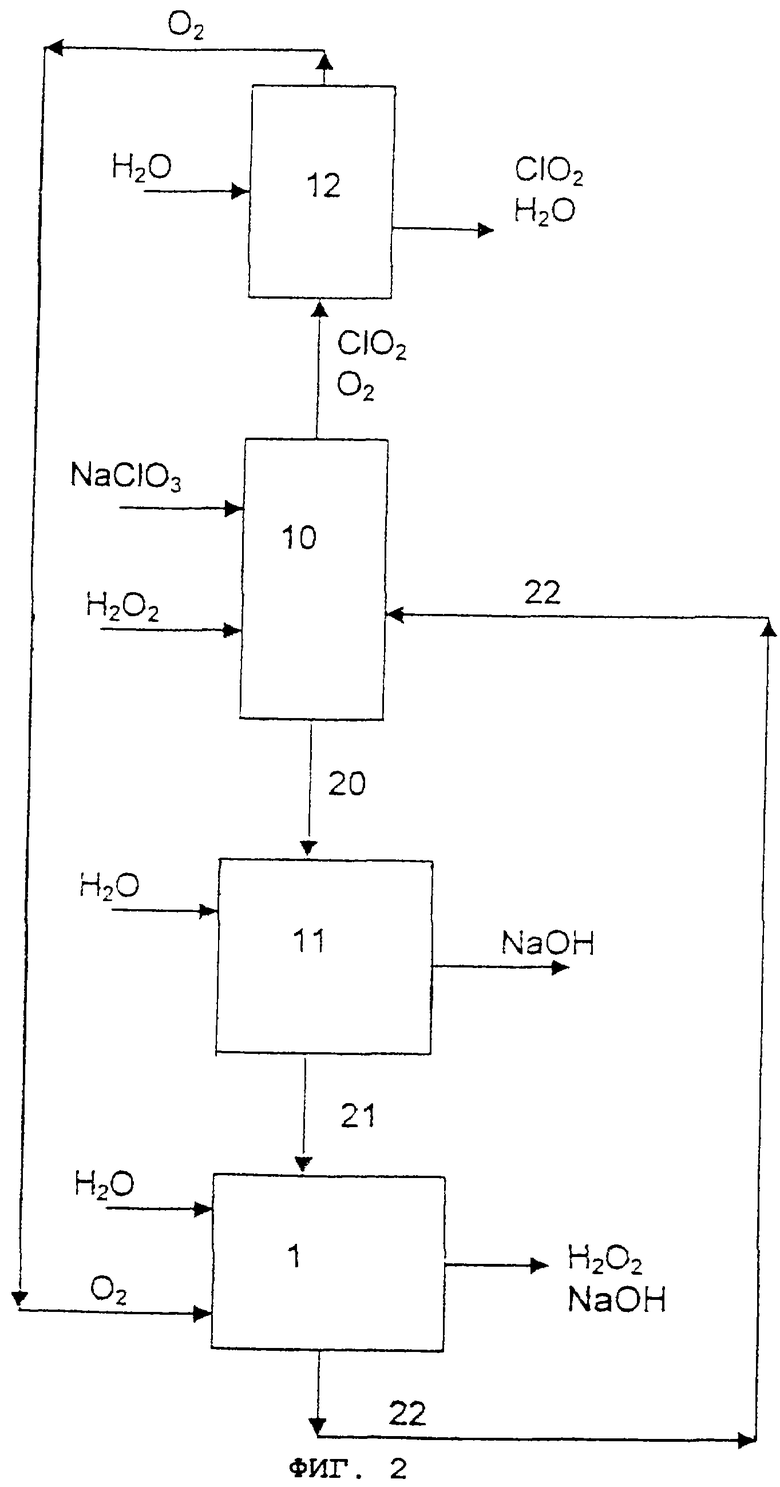
Изобретение предназначено для химической и целлюлозно-бумажной промышленности и может быть использовано при получении отбеливателей. Водный раствор соли щелочного металла, содержащий хлорат 21, подают в анодное отделение электрохимической ячейки 1. Кислород и воду подают в катодное отделение электрохимической ячейки 1. Катодное и анодное отделения разделены катионообменной мембраной. Часть щелочного раствора Н2О2, полученного в электрохимической ячейке 1, отбирают в качестве целевого продукта, а часть возвращают в анодное отделение электрохимической ячейки 1. Подкисленный раствор соли щелочного металла 22 подают в реактор 10 для получения ClO2. Смесь ClO2 и кислорода из реактора 10 направляют в абсорбер 12, где ClO2 абсорбируется водой, а кислород выводят и направляют в катодное отделение электрохимической ячейки 1. Отработанную реакционную среду 20 из реактора 10 подают в электрохимическую ячейку 11 с получением NaOH и водного раствора соли щелочного металла, содержащего хлорат 21, который снова направляют в анодное отделение электрохимической ячейки 1. Изобретение позволяет получить Н2О2 и ClO2 в одном непрерывном технологическом процессе, регулировать соотношение МОН: Н2О2 и количество сульфатов как побочного продукта. 3 с. и 10 з.п.ф-лы, 1 табл., 2 ил.
| US 5702585 А, 30.12.1997 | |||
| Способ получения неорганическогопЕРЕКиСНОгО СОЕдиНЕНия | 1979 |
|
SU827600A1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДНОГО ПОДКИСЛЕННОГО РАСТВОРА, СОДЕРЖАЩЕГО ХЛОРАТНЫЕ ИОНЫ, СПОСОБ ЭЛЕКТРОХИМИЧЕСКОЙ ОБРАБОТКИ ВОДНОГО РАСТВОРА СМЕСИ СОЛЕЙ ЩЕЛОЧНЫХ МЕТАЛЛОВ, СПОСОБ ПОЛУЧЕНИЯ ДВУОКИСИ ХЛОРА | 1991 |
|
RU2108413C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРОКСОСОЕДИНЕНИЙ | 1997 |
|
RU2121526C1 |
| US 5091167 A, 25.02.1992 | |||
| US 5198080 A, 30.03.1993 | |||
| US 5487881 А, 30.01.1996 | |||
| US 5770171 А, 23.06.1998. | |||
Авторы
Даты
2004-01-20—Публикация
2000-11-01—Подача