Изобретение относится к области химии и биохимии, в частности, к способу получения чистого хондроитин-6-сульфата, который может быть использован в медицине, фармакологии, биохимии.
Хондроитин-6-сульфат (ХС-6) является полисахаридом линейного строения, относится к классу кислых гликозаминогликанов (ГАГ), преимущественно локализован в сухожилиях, связках, межпозвоночных дисках, как правило, в смеси с другими ГАГ: гиалуроновой кислотой (ГК), хондроитин-4-сульфатом (ХС-4) или дерматансульфатом (ДС). Хондроитинсульфаты (ХС) обладают хондропротективным действием и входят в состав мази "Хондроксид" для лечения остеоартритов, являются действующим веществом препаратов "Румалон" (для лечения ревматоидных артритов), "Хонсурид" (для ускорения репаративных процессов).
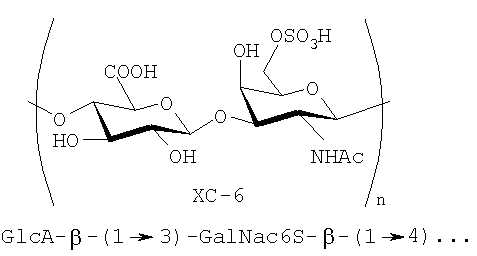
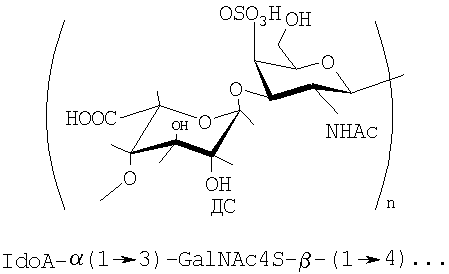
В смеси ХС-6/ДС, выделяемой из пупочных канатиков новорожденных, ХС-6 является доминирующим компонентом, состоит из повторяющихся остатков D-глюкуроновой кислоты и сульфатированного галактозамина, по структуре похож на ДС, дисахаридное звено которого состоит из остатков L-идуроновой кислоты и галактозамина, сульфатированного по С4-ОН-группе. Вследствие одинакового заряда на макромолекулах не удается достичь разделения ХС-6 и ДС с помощью анион-обменной хроматографии, которая является препаративным методом очистки и разделения ГАГ на классы.
Из литературы известно, что наиболее успешно извлечение индивидуального ХС-6 из его смеси, например, с ХС-4 достигается с помощью ферментативной обработки смеси с целью расщепления ХС-4 на низкомолекулярные фрагменты, от которых целевой ХС-6 легко очищается. В качестве источника фермента используют препарат, приготовленный из хвостового плавника головастика [Silbert J.E., DeLuka S. // J. Biol. Chem. 1970. V.245. №6. P.1506-1508].
Задачей предлагаемого изобретения является способ получения чистого ХС-6 из пупочных канатиков новорожденных (извлеченную щелочной экстракцией из пупочных канатиков новорожденных смесь ХС-6/ДС очищают от белков и сопутствующей гиалуроновой кислоты на колонке с ДЕАЕ-целлюлозой, как описано в работе [Понеделькина И.Ю., Одинокова В.Н., Вахрушева E.С., Голикова М. Т., Халилова Л.М., Джемилева У.М. // Биоорган. химия. 2005. Т.31. №1. С.90-95.]). Способ заключается в следующем. Смесь ХС-6/ДС окисляют в водной среде системой реагентов 2,2,6,6-тетраметилпиперидиний-1-оксил (TEMПO)-NaClO-NaBr (pH 10.2, 0-5°С, 1 час), затем смесь продуктов окисления выделяют осаждением тремя объемами этилового спирта с последующим разделением их на хроматографической колонке с ДЕАЕ-целлюлозой, используя в качестве элюента водные растворы NaCl возрастающей концентрации 0.2→0.6 М с шагом 0.05. Из фракции с 0.55-0.6 М NaCl с выходом 35 мас.% получают чистый ХС-6. Побочными продуктами являются элюированные 0.4-0.5 М NaCl гибридные полисахариды, образовавшиеся во время окисления и состоящие, по-видимому, из фрагментов ХС-6 и окисленного ДС (схема). Снижение ионной силы растворов NaCl при элюировании гибридного продукта обусловлено, вероятно, происходящими в процессе окисления деструктивными изменениями углеводного скелета ХС, отмечавшимися ранее при окислении ГК в тех же условиях [Jiang В., Drouet E., Milas М., Rinaudo М. // Carbohydr. Res. 2000. V.327. P.455-461].
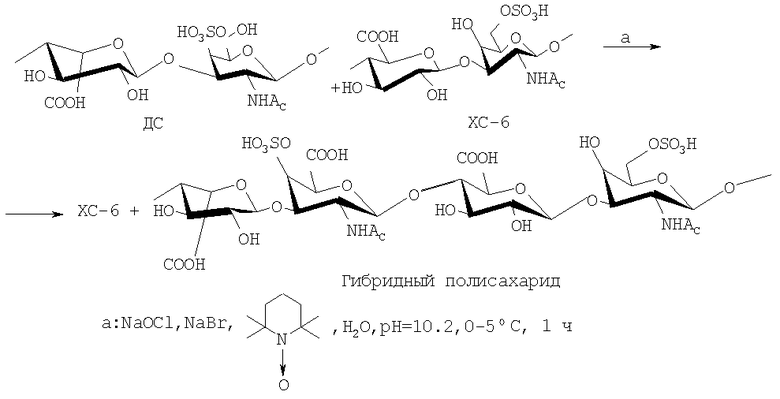
Реагент ТЕМПО-NaClO-NaBr широко используется в органическом синтезе при окислении спиртов и альдегидов. В химии полисахаридов он нашел применение сравнительно недавно: известны примеры окисления первичных гидроксигрупп до карбоксильных в целлюлозе [1], хитине [2], хитозане [3], циклодекстрине [4], мальтодекстрине [5], пуллулане [6], крахмале [7], гиалуроновой кислоте [8].
Источники информации
1. Tahiri С., Vignon M.R. // Cellulose. 2000. V.7. P.177-188.
2. Chang P.S., Robyt J.F. //J. Carbohydr. Chem. 1996. V.15. P.819-830.
3. Yoo S.H., Lee J.S., Park S.Y., Kim Y.S., Chang P.S., Lee H.G. // Int. J. Biol. Macromol. 2005. V.35. P.27-31.
4. Fraschini С., Vignon M.R. // Carbohydr. Res. 2000. V.328. P.585-589.
5. Thaburet J.-F., Merbouh N., Ibert M, Marsais F., Queguiner G. // Carbohydr. Res. 2001. V.330. P.21-29.
6. de Nooy A.E.J., Besemer A.C., van Bekkum H. // Carbohydr. Res. 1995. V.269. P.89-98.
7. Bragd P.L., Besemer A.C., van Bekkum H. // Carbohydr. Res. 2000. V. 328. P. 355-363.
8. JiangB., Drouet E., Milas M., Rinaudo M. // Carbohydr. Res. 2000. V.327. P.455-461.
Для окисления смесей ХС с последующим разделением окисленных продуктов на индивидуальные компоненты реагент TEMPO-NaClO-NaBr ранее не применялся.
Пример. Смесь ХС-6/ДС (302 мг, 0.6 ммоль), NaBr (12.4 мг, 0.12 ммоль) и ТЕМПО (1.0 мг, 0.0065 ммоль) растворяют в 48 мл воды, охлаждают до 0-5°С, затем при интенсивном перемешивании приливают 13% раствор NaClO (0.98 мл, 1.68 ммоль), pH раствора доводят до 10.2 и в течение часа поддерживают это значение с помощью 0.2 н. NaOH. Из реакционной смеси продукт окисления выделяют осаждением 3 объемами этилового спирта, осадок отделяют центрифугированием, растворяют в 5 мл воды, наносят на колонку с ДЕАЕ-целлюлозой (1×20 см) и промывают растворами NaCl возрастающих концентраций 0.2→0.6 М с шагом 0.05. Из каждой фракции с колонки спиртовым осаждением выделяют продукт, анализируют его методом ЯМР-спектроскопии. В результате из элюатов с 0.4-0.5 М получают гибридный полисахарид (схема), из элюатов с 0.55-0.6 М NaCl выделяют индивидуальный ХС-6 (106 мг, 35 мас.%), 1Н и 13С-ЯМР спектры которого идентичны приведенным в работах [Bociek S.M., Darke A.H., Welti D., Rees D.A. // Eur. J. Biochem. 1980. V.109. P.447-456; Welti D., Rees D.A., Welsh J. // Eur. J. Biochem. 1979. V.94. P.505-514]. 1H ЯМР (400 MHz, D2O, 20°C): δ 2.03 (s, 3Н, СН3СОN, CS-6). 13С ЯМР (100.6 MHz, D2O, 20°C): δ 175.9, 175.5 (C=O), 104.9 (Cl-GlcA), 102.0 (Cl-GalNAc6SO3), 73.4-82.9 (C2-GlcA, C3-C5), 68.6 (C6-GalNAc6
SO3), 52.7 (C2-GalNAc6SO3), 23.7 (CH3CON).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ОБЛАДАЮЩИХ ПОНИЖЕННОЙ РАСТВОРИМОСТЬЮ В ВОДЕ ПЛЕНОЧНЫХ МАТЕРИАЛОВ НА ОСНОВЕ МОДИФИЦИРОВАННЫХ АМИНОСАЛИЦИЛОВЫМИ КИСЛОТАМИ КАРБОКСИЛСОДЕРЖАЩИХ ПОЛИСАХАРИДОВ | 2007 |
|
RU2343932C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННЫХ АРАБИНОГАЛАКТАНОВ | 2007 |
|
RU2359975C2 |
| ПРОИЗВОДНЫЕ ГИАЛУРОНОВОЙ КИСЛОТЫ С ПОНИЖЕННОЙ БИОДЕГРАДИРУЕМОСТЬЮ | 2007 |
|
RU2350625C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОКИСЛЕННОГО ПРОИЗВОДНОГО ГИАЛУРОНОВОЙ КИСЛОТЫ И СПОСОБ ЕГО МОДИФИКАЦИИ | 2010 |
|
RU2559447C2 |
| Способ очистки хондроитин сульфата | 2015 |
|
RU2693262C2 |
| НЕНАСЫЩЕННЫЕ ПРОИЗВОДНЫЕ ПОЛИСАХАРИДОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2725500C1 |
| КОНЪЮГАТ ГИАЛУРОНОВОЙ КИСЛОТЫ С НОВОКАИНОМ С АМФОТЕРНЫМИ СВОЙСТВАМИ | 2011 |
|
RU2473351C2 |
| СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННОГО ДЕРМАТАНСУЛЬФАТА | 2005 |
|
RU2318830C2 |
| СПОСОБ ПОЛУЧЕНИЯ МУЛЬТИПОТЕНТНЫХ МЕЗЕНХИМНЫХ СТРОМАЛЬНЫХ КЛЕТОК ИЗ ПУПОЧНОГО КАНАТИКА НОВОРОЖДЕННОГО | 2020 |
|
RU2744301C1 |
| ГЛАЗНЫЕ КАПЛИ | 1999 |
|
RU2163123C2 |
Изобретение относится к химии, точнее к препаративной биохимии. Предложен способ получения хондроитин-6-сульфата из пупочных канатиков новорожденных, заключающийся в том, что выделенную из пупочных канатиков смесь хондроитин-6-сульфата с дерматансульфатом окисляют реагентом 2,2,6,6-тетраметилпиперидиний-1-оксил-NaClO-NaBr при pH 10.2 и температуре 0-5°С в течение 1 часа с последующим осаждением продуктов окисления тремя объемами этилового спирта и их разделением на хроматографической колонке с ДЕАЕ-целлюлозой с использованием в качестве элюента водных растворов NaCl возрастающей концентрации 0.2→0.6 М с шагом 0.05. Изобретение обеспечивает получение чистого хондроитин-6-сульфата с выходом 35 мас.%, остальные продукты представляют собой гибридные полисахариды, состоящие из окисленного по первичным группам дерматансульфата и хондроитин-6-сульфата.
Способ получения хондроитин-6-сульфата из пупочных канатиков новорожденных, заключающийся в том, что выделенную из пупочных канатиков смесь хондроитин-6-сульфата с дерматансульфатом окисляют реагентом 2,2,6,6-тетраметилпиперидиний-1-оксил-NaClO-NaBr при pH 10.2 и температуре 0-5°С в течение 1 ч с последующим осаждением продуктов окисления тремя объемами этилового спирта и их разделением на хроматографической колонке с ДЕАЕ-целлюлозой с использованием в качестве элюента водных растворов NaCl возрастающей концентрации 0.2→0.6 М с шагом 0.05.
| DANISHEFSKY I et al | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Preparative Biochemistry, 1971, 1 (2), 133-40 | |||
| HELTING TORSTEN et al | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Biochimica et Biophysica Acta, 1968, 170 (2), 301-8 | |||
| CATINI CLAUDIO et al | |||
| The glycosaminoglycans in the human | |||
Авторы
Даты
2010-03-10—Публикация
2008-02-20—Подача