Настоящее изобретение относится к органическим соединениям, к их получению и применению в качестве фармацевтических препаратов.
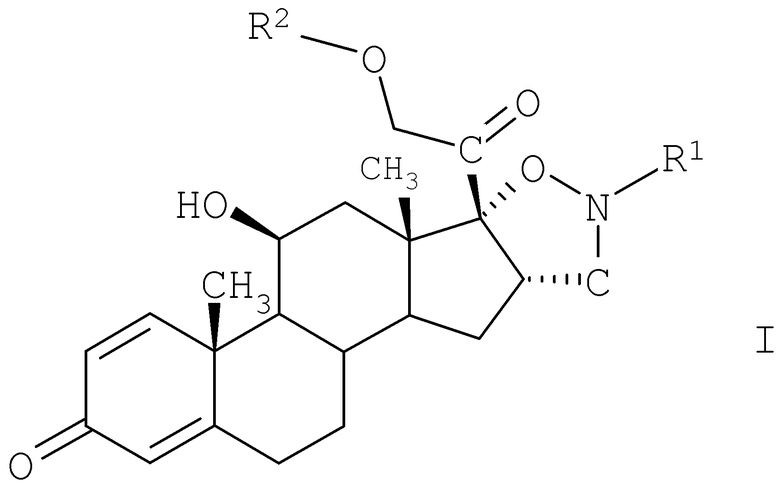
Одним объектом настоящего изобретения являются соединения формулы I
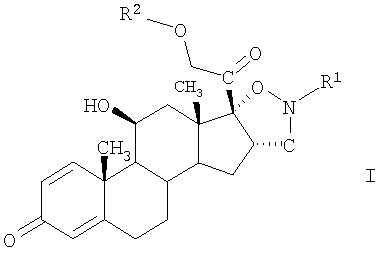
в свободной форме или в форме соли,
где R1 выбирают из группы, включающей С1-С8алкил и С3-С8циклоалкил, а
R2 выбирают из группы, включающей водород, С2-C8алкилкарбонил и С3-С8циклоалкилкарбонил.
Термины, используемые в описании, имеют следующие значения.
"С1-С8алкил" означает алкил с прямой или разветвленной цепью, содержащий 1-8 атомов углерода. Предпочтительно С1-С8алкил означает С1-С4алкил.
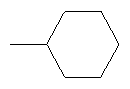
"С3-С8циклоалкил" означает циклоалифатическую группу, содержащую 3-8 атомов углерода, например циклопропил, метилциклопропил, циклобутил, метилциклобутил, циклопентил, циклогексил, метилциклогексил, диметилциклогексил или циклогептил, предпочтительно С2-С6циклоалкил.
"С2-С8алкилкарбонил" означает карбонил, замещенный С2-С8алкилом, указанным выше. Предпочтительной группой С2-С8алкилкарбонил является С2-С4алкилкарбонил.
"С3-С8циклоалкилкарбонил" означает карбонил, замещенный циклоалифатической группой, содержащей 3-8 атомов углерода, например циклопропил-, метилциклопропил-, циклобутил-, метилциклобутил-, циклопентил-, циклогексил-, метилциклогексил-, диметилциклогексил- или циклогептил- или циклооктилкарбонил, предпочтительно С3-С6циклоалкилкарбонил.
Если не указано иное, подразумевается, что термин «включает» или «включающий», используемый в описании заявки и в пунктах формулы изобретения, означает включение указанного целого процесса или стадии или группы целого процесса или стадии, но не исключает любого другого целого процесса или стадии или группы целого процесса или стадии.
Соединения формулы I образуют кислотно-аддитивные соли, прежде всего фармацевтически приемлемые кислотно-аддитивные соли.
Фармацевтически приемлемые кислотно-аддитивные соли соединения формулы I включают соли неорганических кислот, например галогенводородных кислот, таких как фтористоводородная кислота, хлористоводородная кислота, бромистоводородная кислота или иодистоводородная кислота, азотная кислота, серная кислота, фосфорная кислота, и органических кислот, например алифатических монокарбоновых кислот, таких как муравьиная кислота, уксусная кислота, трифторуксусная кислота, пропионовая кислота и масляная кислота, алифатических оксикислот, таких как молочная кислота, лимонная кислота, винная кислота или яблочная кислота, дикарбоновые кислоты, такие как малеиновая кислота или янтарная кислота, ароматические карбоновые кислоты, такие как бензойная кислота, пара-хлорбензойная кислота, дифенилуксусная кислота или трифенилуксусная кислота, ароматические гидроксикислоты, такие как орто-оксибензойная кислота, пара-оксибензойная кислота, 1-оксинафталин-2-карбоновая кислота или 3-оксинафталин-2-карбоновая кислота, и сульфоновых кислот, таких как метансульфоновая кислота или бензолсульфоновая кислота. Указанные соли получают из соединений формулы I известными способами.
Предпочтительные соединения формулы I включают такие соединения, где R1 выбирают из группы, включающей С1-С8алкил и С3-С8циклоалкил, a R2 выбирают из группы, включающей водород и С2-С8алкилкарбонил.
Предпочтительны прежде всего соединения формулы I, в которых R1 выбирают из группы, включающей С1-С4алкил и С3-С6циклоалкил, а R2 выбирают из группы, включающей водород и С2-С4алкилкарбонил.
Более предпочтительные соединения формулы I описаны в примерах.
Другим объектом настоящего изобретения является способ получения соединений формулы I, указанных выше, включающий
(1) (А) получение соединений формулы I, где R2 означает водород, гидролизом соответствующего эфира или
(В) получение соединений формулы I, где R2 выбирают из группы, включающей С2-С8алкилкарбонил и С3-С8циклоалкилкарбонил, ацилированием соответствующего соединения формулы I, где R2 означает водород, и
(2) выделение полученных соединений формулы I в свободной форме или в форме соли.
Способ по варианту (А) проводят с использованием известных методик гидролиза сложных эфиров с образованием соответствующих спиртов. Обычно сложный эфир гидролизуют водным раствором неорганического карбоната, например карбоната натрия, предпочтительно карбоната калия.
Предпочтительно реакцию проводят в протонном растворителе, например в метаноле, при температуре от 0°С до комнатной температуры.
Способ по варианту (В) проводят с использованием известных методик ацилирования спиртов с образованием соответствующего эфира. Обычно спирты вводят в реакцию с ангидридом, например изомасляным ангидридом, в основном растворителе, например пиридине, или в растворителе, содержащеим основание, при температуре от 0°С до 35°С.
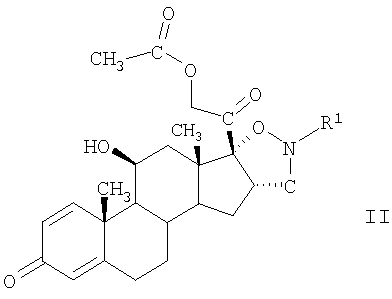
Третьим объектом настоящего изобретения являются новые промежуточные соединения формулы II
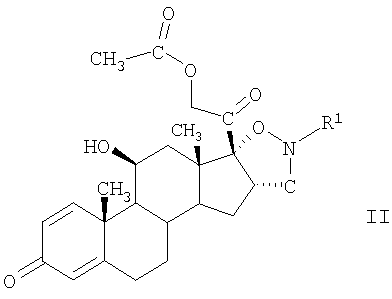
в свободной форме или в форме соли,
где R1 выбирают из группы, включающей С2-С8алкил и С3-С8циклоалкил.
Указанные соединения используются в качестве исходных сложных эфиров в способе по варианту (А).
Соединения формулы II получают по реакции соединения формулы III
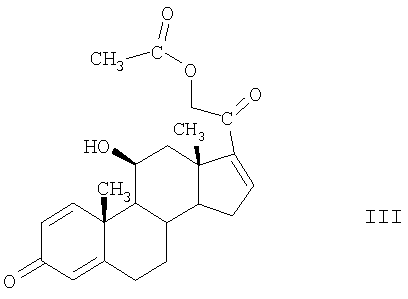
с соединением формулы IV
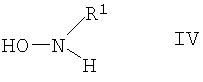
где R1 выбирают из группы, включающей С2-С8алкил и С3-С8циклоалкил, в присутствии параформальдегида и основания, предпочтительно вторичного амина, такого как диизопропиламин, по известным методикам получения изоксазолидина циклоприсоединением нитрона. Обычно реакцию проводят в протонном растворителе, например этаноле. Обычно реакцию проводят при повышенной температуре, например от 60°С до 85°С.
Соединение формулы III является известным соединением или его можно получить из преднизолона способом, описанным в статье Yoon и др., Steroids, 60,445-451 (1995).
Соединения формулы IV являются коммерческими продуктами или их можно получить способом, описанным в статье Tetrahedron Letters, 28, 2993-2994 (1987).
Соединения формулы I в свободной форме можно превратить в форму соли и наоборот обычным способом. Соединения в свободной форме или в форме соли можно получить в форме гидратов или сольватов, содержащих растворитель, который использовали для кристаллизации.
Соединения формулы I выделяют из реакционной смеси и очищают известным способом.
Соединения формулы I используются в качестве фармацевтических препаратов. Следовательно, в изобретении предлагаются соединения формулы I для применения в качестве фармацевтических препаратов. Соединения формулы I обладают ценными фармакологическими свойствами. Например, они обладают высоким противовоспалительным действием, которое можно продемонстрировать по их связыванию с глюкокортикоидным рецептором, по ингибированию синтеза TNF-α и его высвобождения в клеточной линии макрофагов человека.
Связывание с глюкортикоидным рецептором оценивают с использованием следующего анализа.
Рекомбинантный GR человека экспрессировали в инфицированных бакуловирусом клетках насекомых Sf-9, полученных из Panvera (Madison, WI, США), а анализ проводили в буферном растворе для анализа, содержащем GR и флуоресцентный лиганд FluormoneТМ-GSl (200 нМ раствор в метаноле). Анализ проводили в 384-луночных планшетах при последовательном добавлении растворов анализируемого соединения в воде (2 мкл) при серийном разведении исходных растворов ДМСО, лиганда FluormoneТМ-GS1 (2,2 нМ раствор в буферном растворе для анализа, 10 мкл) и раствор GR (8,8 нМ в буферном растворе для анализа, 10 мкл). Смесь инкубировали без доступа света при комнатной температуре в течение 1 ч и измеряли поляризацию флуоресценции на планшет-ридере при волне возбуждения 485 нм и волне испускания 530 нм. Концентрацию анализируемого соединения на половине максимума сдвига поляризации принимали за IC50. Графики зависимости получали с использованием программы OriginТМ, а значения Ki рассчитывали по уравнению Ченга-Прусофф (Cheng-Prussoff). По данным указанного анализа соединения, описанные в примерах 1, 2, 3 и 4, характеризовались величинами Ki 0,5, 1,4, 0,4 и 0,2 нМ соответственно.
Ингибирование синтеза TNF-α и его высвобождения в клетках оценивают с использованием следующего анализа.
Клеточную линию макрофагов человека U937 получали из Американской коллекции клеточных культур (Rockville MD) и культивировали в среде RPMI 1640 (фирма Gibco UK), содержащей 10% ЭТС (фирма Gibco UK). Плотность клеток составляла 4×105 клеток/мл, а клетки дифференцировали в присутствии миристата/ацетата форбала (РМА, 20 нг/мл) в течение 4 ч. РМА удаляли промывкой и прикрепленные к планшету клетки инкубировали в течение 48 ч при 37°С в термостате с высокой влажностью в атмосфере 5% СО2. Дифференцированные клетки U937 удаляли при использовании буферного раствора для диссоциации клеток (фирма Gibco UK) и плотность клеток доводили до 1×106 клеток/мл. Суспензию клеток переносили в 96-луночные культуральные планшеты (по 100 мкл в лунку), добавляли по 50 мкл среды или раствора соединения в диметилсульфоксиде при соответствующей концентрации. Предварительную инкубацию проводили в течение 20 мин при 37°С, клетки стимулировали добавлением липополисахарида (ЛПС, фирма Sigma, 10 нг/мл), инкубировали в течение 24 ч при 37°С в термостате с высокой влажностью в атмосфере 5% СО2 и собирали супернатант. Концентрацию TNFα в супернатантах определяли методом сэндвич-ИФА с использованием двух моноклональных антител, узнающих различные эпитопы цитокина (фирма Pharmingen UK). Связывание второго антитела анализировали ступенчатой инкубацией в присутствии конъюгата стрептавидин/щелочная фосфатаза (фирма Sigma UK) и динатриевой соли 4-нитрофенилфосфата. Оптическую плотность измеряли при 405 нм, а концентрацию цитокина рассчитывали по калибровочной кривой, полученной по результатам серийных разведений рекомбинантного TNFα в качестве стандарта. Построение графиков и рассчет значений IС50 проводили с использованием программы OriginТМ. По данным указанного анализа соединения, описанные в примерах 1, 2, 3 и 4, характеризовались величинами IC50 1,16, 4,95, 0,89 и 3,57 нМ соответственно.
Благодаря противовоспалительной активности соединения формулы I используются при лечении воспалительных состояний, прежде всего воспалительных или обструктивных заболеваний дыхательных путей. Способ лечения по изобретению является симптоматическим или профилактическим.
Воспалительные или обструктивные заболевания дыхательных путей по настоящему изобретению включают астму любого типа или этиологии, включая как наследственную (неаллергическую) астму, так и приобретенную (аллергическую) астму, легкую форму астмы, астму средней степени тяжести, тяжелую форму астмы, бронхиальную астму, астму, вызванную физическими нагрузками, профессиональную астму и бактериальную астму. Лечение астмы включает лечение субъектов, например детей в возрасте младше 4 или 5 лет, у которых наблюдается симптоматическое свистящее дыхание или с диагнозом «дети с одышкой» и которые относятся к категории пациентов первостепенного медицинского значения, и которых в настоящее время относят к астматикам в ранней фазе. Такое астматическое состояние называют «синдромом детей со стерторозным дыханием».
Профилактическое действие при лечении астмы наглядно проявляется в снижении частоты или тяжести симптоматических приступов, например острых астматических приступов или приступов бронхостеноза, в улучшении функционирования легких или повышении гиперреактивности дыхательных путей. Кроме того, профилактическое действие проявляется как снижение необходимости в другом симптоматическом лечении, предназначенном для подавления или остановки приступов астмы при их наличии, например, необходимости в противовоспалительном (например, кортикостероидном) или бронходилятаторном лечении. Профилактика при лечении астмы, прежде всего, необходима для субъектов, подверженных «утренним приступам». «Утренние приступы» являются известным астматическим синдромом, проявляющимся у большинства астматиков, который характеризуется астматическими приступами, например, между приблизительно 4 и 6 ч утра, т.е. через значительный промежуток времени после любого предшествующего введения симптоматического астматического терапевтического средства.
Другие воспалительные или обструктивные заболевания и состояния дыхательных путей по настоящему изобретению включают острое повреждение легких (ALI), острый респираторный дистресс-синдром у взрослых пациентов (ARDS), хроническое обструктивное заболевание легких, хроническую непроходимость дыхательных путей или легких (COPD, COAD или COLD), включая хронический бронхит или связанную с ним одышку, эмфизему, также как и обострение гиперреактивности дыхательных путей вследствие применения других лекарственных средств, прежде всего, другого ингаляционного медикаментозного лечения. Настоящее изобретение можно также использовать при лечении бронхитов любого типа или этиологии, включая острый, арахноидальный, катаральный, крупозный, хронический или гнойный туберкулезный бронхит. Кроме того, воспалительные или обструктивные заболевания дыхательных путей по настоящему изобретению включают пневмокониоз (воспалительное заболевание легких, которое обычно связано с профессиональной деятельностью, сопровождающееся в большинстве случаев хронической или острой обструкцией дыхательных путей, а также возникающее при повторном вдыхании пыли) любого типа или этиологии, включая, например, алюминоз, антракоз, асбестоз, халикоз, птилоз, сидероз, силикоз, табакоз и биссиноз.
В связи с характерной противовоспалительной активностью соединения формулы I можно также использовать при лечении нарушений, связанных с эозинофилами, например ацидоцитоза, прежде всего нарушений дыхательных путей, связанных с эозинофилами (например, включающих патологическую эозинофильную инфильтрацию легочных тканей), включая гиперэозинофилию, т.е. воздействие на дыхательные пути и/или легкие, а также, например, нарушения дыхательных путей, связанные с эозинофилами, являющиеся следствием или сопровождающиеся синдромом Леффлера, эозинофильную пневмонию, паразитическую (прежде всего, многоклеточные метазоа) инвазию (включая тропический ацидоцитоз), бронхолегочный аспергилломикоз, нодозный полиартрит (включая синдром Чарга-Страусса), эозинофильную гранулему и нарушения, связанные с эозинофилами, воздействующие на дыхательные пути вследствие реакции на лекарственные препараты.
Соединения формулы I можно также использовать при лечении воспалительных заболеваний кожи, например, включающих псориаз, контактный дерматит, атопический дерматит, гнездную алопецию, экссудативную эритему, герпетиформный дерматит, склеродерму, витилиго, аллергический ангиит, крапивницу, буллезный пемфигоид, красную волчанку, пузырчатку, приобретенный буллезный эпидемолиз и другие воспалительные заболевания кожи.
Соединения формулы I можно также использовать для лечения других заболеваний или состояний, ассоциированных с воспалительным процессом, например для лечения заболеваний и состояний глаз, таких как конъюнктивит, сиккативный кератоконъюнктивит и сезонный конъюнктивит, заболеваний носоглотки, включая аллергический ринит, а также воспалительных состояний желудочно-кишечного тракта, например воспаления кишечника, такого как язвенный колит и болезнь Крона.
Соединения формулы I можно также использовать в качестве агентов для сочетанной терапии в комбинации с другими лекарственными средствами для лечения заболеваний дыхательных путей, прежде всего противовопалительными бронхолитическими, антигистаминными и противокашлевыми лекарственными средствами, прежде всего при лечении обструктивных или воспалительных заболеваний дыхательных путей, указанных выше, например, в качестве стимуляторов терапевтической активности таких лекарственных средств или в качестве средств, обеспечивающих снижение требуемой дозы или побочного действия таких лекарственных средств. Соединение формулы I можно смешивать с другими лекарственными средствами в фиксированной фармацевтической композиции или их можно вводить отдельно, до или одновременно или после другого лекарственного средства. Следовательно, изобретение включает комбинацию агента по изобретению, указанного выше, с противовоспалительным, бронхолитическим, антигистаминовым или противокашлевым лекарственным средством, причем указанный агент по изобретению и указанное лекарственное средство содержатся в одной или в разных фармацевтических композициях.
Такие противовоспалительные лекарственные средства включают антагонисты LTB4, такие как BIIL 284, СР-195543, DPC11870, этаноламид LTB4, LY 293111, LY 255283, CGS025019C, СР-195543, ONO-4057, SB 209247, SC-53228 и другие, описанные в US 5451700; антагонисты LTD4, такие как монтелукаст, пранлукаст, зафирлукаст, акколат, SR2640, Wy-48,252, ICI 198615, МК-571, LY-171883, Ro 24-5913 и L-648051; ингибиторы PDE4, такие как циломиласт (Ariflo®, фирма GlaxoSmithKline), рофлумиласт (фирма Byk Gulden), V-11294А (фирма Napp), BAY19-8004 (фирма Bayer), SCH-351591 (фирма Schering-Plough), арофиллин (фирма Almirall Prodesfarma), PD189659/PD168787 (фирма Parke-Davis), AWD-12-281 (фирма Asta Medica), CDC-801 (фирма Celgene), SelCID(TM) CC-10004 (фирма Celgene), VM554/UM565 (фирма Vernalis), T-440 (фирма Tanabe), KW-4490 (фирма Kyowa Hakko Kogyo), и другие, описанные в WO 92/19594, WO 93/19749, WO 93/19750, WO 93/19751, WO 98/18796, WO 99/16766, WO 01/13953, WO 03/104204, WO 03/104205, WO 03/39544, WO 04/000814, WO 04/000839, WO 04/005258, WO 04/018450, WO 04/018451, WO 04/018457, WO 04/018465, WO 04/018431, WO 04/018449, WO 04/018450, WO 04/018451, WO 04/018457, WO 04/018465, WO 04/019944, WO 04/019945, WO 04/045607 и WO 04/037805; агонисты A2A, такие, как описанные в ЕР 1052264, ЕР 1241176, ЕР 409595А2, WO 94/17090, WO 96/02543, WO 96/02553, WO 98/28319, WO 99/24449, WO 99/24450, WO 99/24451, WO 99/38877, WO 99/41267, WO 99/67263, WO 99/67264, WO 99/67265, WO 99/67266, WO 00/23457, WO 00/77018, WO 00/78774, WO 01/23399, WO 01/27130, WO 01/27131, WO 01/60835, WO 01/94368, WO 02/00676, WO 02/22630, WO 02/96462 и WO 03/086408; антагонисты А2B, такие как описанные в WO 02/42298, и агонисты (β)-2-адренорецептора, такие как албутерол (салбутамол), метапротеренол, тербуталин, салметерол, фенотерол, прокатерол, и прежде всего формотерол, кармотерол и их фармацевтически приемлемые соли, и соединения (в свободной форме или в форме соли, или в форме сольвата) формулы I, описанные в WO 0075114, которая включена в описание заявки в виде ссылки, предпочтительно соединения, описанные в примерах, прежде всего соединения формулы
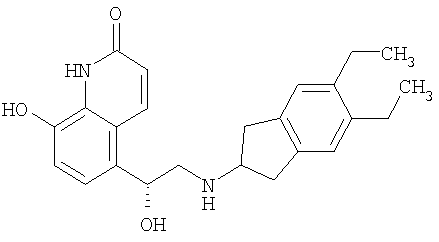
и их фармацевтически приемлемые соли, а также соединения (в свободной форме или в форме соли, или в форме сольвата) формулы I, описанные в WO 04/16601, а также соединения, описанные в ЕР 1440966, JP 05025045, WO 93/18007, WO 99/64035, US 2002/0055651, WO 01/42193, WO 01/83462, WO 02/66422, WO 02/70490, WO 02/76933, WO 03/24439, WO 03/42160, WO 03/42164, WO 03/72539, WO 03/91204, WO 03/99764, WO 04/16578, WO 04/22547, WO 04/32921, WO 04/33412, WO 04/37768, WO 04/37773, WO 04/37807, WO 04/39762, WO 04/39766, WO 04/45618 WO 04/46083 и WO 04/80964.
Такие бронхолитические средства включают антихолинергические или антимускариновые агенты, прежде всего ипратропий бромид, окситропий бромид, соли тиотропия и CHF 4226 (фирма Chiesi), и гликопирролят, а также соединения, описанные в ЕР 424021, US 3714357, US 5171744, WO 01/04118, WO 02/00652, WO 02/51841, WO 02/53564, WO 03/00840, WO 03/33495, WO 03/53966, WO 03/87094, WO 04/018422 и WO 04/05285.
Такие противовоспалительные и бронхолитические средства включают лекарственные средства с двойной противовоспалительной и бронхолитической активностью, прежде всего агонист (β-2 адренорецептора/мускариновый антагонист, такой, как описано в US 2004/0167167, WO 04/74246 и WO 04/74812.
Такие совместные терапевтические антигистаминовые лекарственные средства включают гидрохлорид цетиризина, ацетаминофен, фумарат клемастина, прометазин, лоратидин, деслоратидин, дифенгидрамин и гидрохлорид фексофенадина, активастин, астемизол, азеластин, эбастин, эпинастин, мизоластин и тефенадин, а также соединения, описанные в JP 2004107299, WO 03/099807 и WO 04/026841.
Комбинации агентов по изобретению и одного или более ингибиторов PDE4, агонистов A2A, антагонистов А2B, агонистов β-2-адренорецептора и/или антагонистов LTD4 можно использовать, например, при лечении COPD или прежде всего астмы. Комбинации агентов по изобретению и одного или более антихолинергических или антимускариновых агентов, ингибиторов PDE4, агонистов A2A, антагонистов А2B, агонистов β-2-адренорецептора и/или антагонистов LTB4 можно использовать, например, при лечении астмы или прежде всего COPD.
В соответствии с вышеизложенным в изобретении предлагается способ лечения воспалительного состояния, прежде всего воспалительного или обструктвного заболевания дыхательных путей, который включает введение субъекту, прежде всего человеку, который нуждается в лечении, эффективного количества соединения формулы I, описанного выше. Другим объектом изобретения является применение соединения формулы I, описанного выше, для получения лекарственного средства, предназначенного для лечения воспалительного состояния, прежде всего воспалительного или обструктвного заболевания дыхательных путей.
Соединения формулы I можно вводить любым приемлемым способом, например перорально, например, в форме таблетки или капсулы, парентерально, например внутривенно, ингаляцией, например, при лечении воспалительных или обструктивных заболеваний дыхательных путей, интраназально, например, для лечения аллергического ринита, местно на кожу, например, при лечении атопического дерматита или ректально, например, при лечении воспалительного заболевания кишечника.
Другим объектом изобретения является фармацевтическая композиция, включающая в качестве активного ингредиента соединение формулы I, необязательно в смеси с фармацевтически приемлемым разбавителем или носителем. Композиция может содержать другой терапевтический агент, такой как бронзолитическое или противовоспалительное лекарственное средство, указанное выше. Такие композиции получают с использованием обычных разбавителей или эксципиентов по известным методикам. Пероральные лекарственные формы включают таблетки и капсулы. Препараты для местного применения включают кремы, мази, гели или системы для трансдермальной доставки, например пластыри. Композиции для ингаляции включают аэрозоль или другие распыляемые препараты или составы в виде сухих порошков.
Композиции в форме аэрозоля предпочтительно содержат, например, фторированный углеводород (HFA), такой как HFA134a или HFA227 или их смесь, и могут содержать один или более известных сорастворителей, таких как этанол (до 20 мас.%), и/или один или более ПАВ, таких как олеиновая кислота или сорбитантриолеат, и/или один или более наполнителей, таких как лактоза. Композиция в форме сухого порошка предпочтительно содержит, например, соединение формулы I с диаметром частиц до 10 мкм, необязательно в смеси с разбавителем или носителем, таким как лактоза, с частицами с требуемым распределением по размеру, и соединение для защиты от увлажнения, например стеарат магния, обычно в количестве 0,05-1,5%. Композиции, включающая состав для распыления, предпочтительно содержит, например, соединение формулы I, растворенное или суспендированное в носителе, содержащем воду, сорастворитель, такой как этанол или пропиленгликоль, и стабилизатор, например ПАВ.
Изобретение включает (А) соединение формулы I в форме для ингаляции, например в форме аэрозоля или другой дисперсной композиции или состава для ингаляции, например, в микронизированной форме, (В) лекарственное средство для ингаляции, включающее соединение формулы I в форме для ингаляции, (С) фармацевтический продукт, включающий соединение формулы I в форме для ингаляции в усройстве для ингаляции, (D) ингаляционное устройство, содержащее соединение формулы I в форме, пригодной для ингаляции.
Дозы соединений формулы I, используемые по настоящему изобретению, изменяются в зависимости от конкретного состояния, подлежащего лечению, требуемого результата и способа введения. В общем случае, пригодная суточная доза для введения ингаляцией составляет приблизительно от 0,005 до 10 мг, при пероральном введении суточная доза составляет приблизительно от 0,05 до 100 мг.
Изобретение иллюстрируется следующими примерами.
Примеры 1-5
Соединения формулы I приводятся в следующей таблице. Способы их получения описаны ниже. В таблице также указаны данные масс-спектрометрии (МН+). Соединения приводятся в свободной форме.

Пример 1
В смесь 2-((4аR,5S,6аS,6bR,9аS)-5-гидрокси-4а,6а-диметил-2-оксо-8-пропил-2,4а,4b,5,6,6а,8,9,9а,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-6b-ил)-2-оксоэтилового эфира уксусной кислоты (пример 6) (0,082 г, 0,173 ммоля) в метаноле (2 мл) добавляли водный раствор карбоната калия (0,563 г, 4,08 ммоля в 2 мл Н2O). Реакционную смесь перемешивали в течение 2 ч, затем разбавляли водой и подкисляли. Продукт экстрагировали дихлорметаном, экстракт сушили над сульфатом натрия и концентрировали на роторном испарителе, при этом получали требуемый продукт, (4аR,5S,6аS,6bR,9аS)-5-гидрокси-6b-(2-гидроксиацетил)-4а,6а-диметил-8-пропил-4а,4b,5,6,6а,6b,8,9,9а,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-2-он.
Пример 2
(4аR,5S,6аS,6bR,9аS)-5-Гидрокси-6b-(2-гидроксиацетил)-4а,6а,8-триметил-4a,4b,5,6,6a,6b,8,9,9a,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-2-он получали из соединения, указанного ниже, по методике, описанной в примере 1.
2-((4аR,5S,6аS,6bR,9аS)-5-Гидрокси-4а,6а,8-триметил-2-оксо-2,4а,4b,5,6,6а,8,9,9а,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-6b-ил)-2-оксоэтиловый эфир уксусной кислоты описан в статье Green и др., J. Med. Chem., 25, 1492-1495 (1982).
Пример 3
(4аR,5S,6аS,6bR,9аS)-8-Бутил-5-гидрокси-6b-(2-гидроксиацетил)-4а,6а-диметил-4а,4b,5,6,6а,6b,8,9,9а,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-2-он получали из соединения, описанного в примере 7, по методике, описанной в примере 1.
Пример 4
(4аR,5S,6аS,6bR,9аS)-8-Циклогексил-5-гидрокси-6b-(2-гидроксиацетил)-4а,6а-диметил-4а,4b,5,6,6а,6b,8,9,9а,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-2-он получали из соединения, описанного в примере 8, по методике, описанной в примере 1.
Пример 5
Смесь (4аR,5S,6аS,6bR,9аS)-8-циклогексил-5-гидрокси-6b-(2-гидроксиацетил)-4а,6а-диметил-4а,4b,5,6,6а,6b,8,9,9а,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-2-она (0,054 г, 0,115 ммоля) и изомасляного ангидрида (0,019 г, 0,121 ммоля) в пиридине (0,5 мл) перемешивали в течение ночи. Реакционную смесь нагревали при 35°С в течение 2 ч, затем добавляли 0,01 г изомасляного ангидрида и температуру смеси понижали до комнатной температуры. Через 1 ч реакционную смесь разбавляли соляной кислотой и продукт экстрагировали СН2Сl2. Органический слой сушили и концентировали на роторном испарителе. Неочищенный продукт очищали хроматографией, при этом получали требуемый продукт, 2-((4аR,5S,6аS,6bR,9аS)-8-циклогексил-5-гидрокси-4а,6а-диметил-2-оксо-2,4а,4b,5,6,6а,8,9,9а,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-6b-ил)-2-оксоэтиловый эфир изомасляной кислоты.
Примеры 6-8
Соединения формулы II приводятся в следующей таблице. Способы их получения описаны ниже. Таблица включает данные масс-спектрометриии (МН+). Соединения приводятся в свободной форме.
Пример 6
Смесь 2-((10R,11S,13S)-11-Гидрокси-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15-декагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтилового эфира уксусной кислоты (0,576 г, 1,5 ммоля), н-пропилгидроксиламина (0,166 г, 1,5 ммоля), диизопропиламина (0,166 г, 1,65 ммоля) и параформальдегида (0,029 г, 0,97 ммоля) в этаноле (25 мл) нагревали при 85°С в течение 20 ч. Реакционную смесь выливали в воду и продукт экстрагировали дихлорметаном. Эстракт сушили над сульфатом натрия и концентрировали на роторном испарителе, при этом получали требуемый продукт, 2-((4аR,5S,6аS,6bR,9аS)-5-гидрокси-4а,6а-диметил-2-оксо-8-пропил-2,4а,4b,5,6,6а,8,9,9а,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-6b-ил)-2-оксоэтиловый эфир уксусной кислоты.
Пример 7
2-((4аR,5S,6аS,6bR,9аS)-8-Бутил-5-гидрокси-4а,6а-диметил-2-оксо-2,4а,4b,5,6,6а,8,9,9а,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-6b-ил)-2-оксоэтиловый эфир уксусной кислоты получали по методике, описанной в примере 6.
Пример 8
2-((4аR,5S,6аS,6bR,9аS)-8-Циклогексил-5-гидрокси-4а,6а-диметил-2-оксо-2,4а,4b,5,6,6а,8,9,9а,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-6b-ил)-2-оксоэтиловый эфир уксусной кислоты получали по методике, описанной в примере 6.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИОКСИДАНТНЫМИ, ГЕПАТОПРОТЕКТОРНЫМИ И ПРОТИВОВОСПАЛИТЕЛЬНЫМИ СВОЙСТВАМИ | 2010 |
|
RU2436793C1 |
| МОДУЛЯТОРЫ SHIP1 И ОТНОСЯЩИЕСЯ К НИМ СПОСОБЫ | 2014 |
|
RU2679805C2 |
| β-ЛАКТАМЫ | 1995 |
|
RU2143435C1 |
| РЕГУЛЯТОРЫ-ПРОИЗВОДНЫЕ СТЕРОИДОВ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2797408C2 |
| НОВЫЕ ОПТИЧЕСКИ АКТИВНЫЕ 4-ГИДРОКСИ-2-АЗА-9,10-АНТРАХИНОНЫ, ОБЛАДАЮЩИЕ ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2010 |
|
RU2436775C1 |
| НОВАЯ КРИСТАЛЛИЧЕСКАЯ ФОРМА СОЕДИНЕНИЯ-БЛОКАТОРА ПРОНИЦАЕМОСТИ СОСУДОВ | 2020 |
|
RU2809162C2 |
| КРИСТАЛЛИЧЕСКАЯ МОДИФИКАЦИЯ ПАРА-МЕТОКСИАНИЛИДА 6-ГИДРОКСИ-4-ОКСО-2,4-ДИГИДРО-1Н-ПИРРОЛО[3,2,1-ij]ХИНОЛИН-5-КАРБОНОВОЙ КИСЛОТЫ | 2012 |
|
RU2480468C1 |
| Способ получения производных бензо/с/хинолина или их фармацевтически приемлемых солей | 1981 |
|
SU1098520A3 |
| БЕНЗИЛУРСОНАТ - ПРОТИВОВОСПАЛИТЕЛЬНОЕ И ГЕПАТОПРОТЕКТОРНОЕ СРЕДСТВО | 2010 |
|
RU2430106C1 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБЫ ПРИМЕНЕНИЯ ПРОИЗВОДНЫХ 4-ПРЕГЕНЕН-11β-17-21-ТРИОЛ-3,20-ДИОНА | 2012 |
|
RU2683775C2 |
Описаны соединения формулы I

в свободной форме или в форме соли, где R1 и R2 имеют значения, указанные в описании заявки, которые используются для лечения воспалительных состояний, прежде всего воспалительных или обструктивных заболеваний дыхательных путей. В заявке также описаны фармацевтические композиции, содержащие указанные соединения, и способы получения указанных соединений. 3 н. и 2 з.п. ф-лы.
1. Соединение формулы I

в свободной форме или в форме соли, где
R1 выбирают из группы, включающей С1-С8алкил и С3-С8циклоалкил, а
R2 выбирают из группы, включающей водород, С2-С8алкилкарбонил.
2. Соединение по п.1, где
R1 выбирают из группы, включающей С1-С8алкил и С3-С8циклоалкил, а
R2 выбирают из группы, включающей водород, С2-С4алкилкарбонил.
3. Соединение по п.1, которое означает
(4аR,5S,6аS,6bR,9аS)-5-гидрокси-6b-(2-гидроксиацетил)-4а,6а-диметил-8-пропил-4а,4b,5,6,6а,6b,8,9,9а,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-2-он,
(4аR,5S,6аS,6bR,9аS)-5-гидрокси-6b-(2-гидроксиацетил)-4а,6а,8-триметил-4a,4b,5,6,6a,6b,8,9,9a,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-2-он,
(4аR,5S,6аS,6bR,9аS)-8-бутил-5-гидрокси-6b-(2-гидроксиацетил)-4а,6а-диметил-4а,4b,5,6,6а,6b,8,9,9а,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-2-он,
(4аR,5S,6аS,6bR,9аS)-8-циклогексил-5-гидрокси-6b-(2-гидроксиацетил)-4а,6а-диметил-4а,4b,5,6,6а,6b,8,9,9а,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-2-он,
2-((4аR,5S,6аS,6bR,9аS)-8-циклогексил-5-гидрокси-4а,6а-диметил-2-оксо-2,4a,4b,5,6,6a,8,9,9a,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-6b-ил)-2-оксоэтиловый эфир изомасляной кислоты,
2-((4аR,5S,6аS,6bR,9аS)-5-гидрокси-4а,6а-диметил-2-оксо-8-пропил-2,4а,4b,5,6,6а,8,9,9а,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-6b-ил)-2-оксоэтиловый эфир уксусной кислоты,
2-((4аR,5S,6аS,6bR,9аS)-8-бутил-5-гидрокси-4а,6а-диметил-2-оксо-2,4а,4b,5,6,6а,8,9,9а,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-6b-ил)-2-оксоэтиловый эфир уксусной кислоты или
2-((4аR,5S,6аS,6bR,9аS)-8-циклогексил-5-гидрокси-4а,6а-диметил-2-оксо-2,4а,4b,5,6,6а,8,9,9а,10,10а,10b,11,12-тетрадекагидро-7-окса-8-азапенталено[2,1-а]фенантрен-6b-ил)-2-оксоэтиловый эфир уксусной кислоты.
4. Фармацевтическая композиция, обладающая противовоспалительной активностью, включающая в качестве активного ингредиента соединение по любому из пп.1-3, необязательно в смеси с фармацевтически приемлемым разбавителем или носителем.
5. Способ получения соединений формулы I по п.1, включающий (1) (А) получение соединений формулы I, где R2 означает водород, гидролизом соответствующего эфира или
(В) получение соединений формулы I, где R2 означает С2-С8алкилкарбонил, ацилированием соответствующего соединения формулы I, где R2 означает водород, и
(2) выделение полученных соединений формулы I в свободной форме или в форме соли.
| TAESSOO KWON et al // J | |||
| Med.Chem | |||
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
| US 3349084 A, 24.10.1967 | |||
| US 4232013 A, 04.11.1980. | |||
Авторы
Даты
2010-04-27—Публикация
2005-07-13—Подача