В настоящей заявке испрашивается приоритет в связи с заявкой серийный номер №60/530891, поданной 22 декабря 2003 г., и с заявкой серийный номер №60/606897, поданной 3 сентября 2004 г., которые полностью включены в настоящее описание в качестве ссылок.
Область изобретения
Настоящее изобретение в основном относится к лигандам никотиновых ацетилхолиновых рецепторов (nAChR), активации nAChR и лечению заболеваний, связанных с недостаточностью функции никотиновых рецепторов ацетилхолина или с их аномальной функцией, прежде всего в ткани мозга. Настоящее изобретение относится также к новым соединениям, например, к индолам, 1H-индазолам, 1,2-бензизоксазолам и 1,2-бензизотиазолам, которые являются лигандами рецепторов подтипа nAChR, к способам получения указанных соединений, композициям, включающим указанные соединения, и к способам применения указанных композиций.
Предпосылки создания настоящего изобретения
Известно 2 вида рецепторов нейромедиаторов, таких как ацетилхолин: мускариновые рецепторы и никотиновые рецепторы в зависимости от селективности действия мускарина и никотина, соответственно. Мускариновые рецепторы являются рецепторами, сопряженными с G-белком. Никотиновые рецепторы являются членами семейства лиганд-активируемых ионных каналов. При их активации возрастает ионная проводимость никотиновых ионных каналов.
Никотиновый белок-рецептор α-7 образует гомопентамерный канал in vitro, который характеризуется высокой проницаемостью для ряда катионов (например, Са++). Каждый никотиновый рецептор α-7 содержит 4 трансмембранных домена, а именно M1, М2, М3 и М4. Полагают, что домен М2 выстилает стенки канала. Сравнение аминокислотных последовательностей свидетельствует о высокой степени консервативности никотинового рецептора α-7 в процессе эволюции. Аминокислотная последовательность домена М2, который выстилает канал, идентична для тканей из различных источников от курицы до человека. Описание рецепторов α-7 приведено в статьях, например, Revah и др., Nature, 353, 846-849 (1991); Gaizi и др., Nature, 359, 500-505 (1992); Fucile и др., PNAS 97 (7), 3643-3648 (2000); Briggs и др., Eur. J. Pharmacol., 366 (2-3). 301-308 (1999) и Gopalakrishnan и др., Eur. J. Pharmacol., 290 (3), 237-246 (1995).
Никотиновые рецепторные каналы α-7 экспрессируются в различных отделах мозга и включены в большинство важных биологических процессов в центральной нервной системе (ЦНС), включая обучение и память. Никотиновые рецепторы α-7 локализованы в пресинптических и в постсинаптических окончаниях и предположительно включены в процесс модулирующей синаптической трансмиссии. В связи с этим в настоящее время являются актуальными новые соединения, действующие в качестве лигандов для рецепторов nAChR подтипа α-7, предназначенные для лечения заболеваний, связанных с поврежденными никотиновыми ацетилхолиновыми рецепторами или их аномальной функцией.
Настоящее изобретение относится к новым соединениям, которые являются лигандами для рецепторов nAChR подтипа α-7, способам получения таких соединений, композициям, включающим такие соединения, и к способам их применения.
Подробное описание настоящего изобретения
Настоящее изобретение включает соединения формул I, II или III:
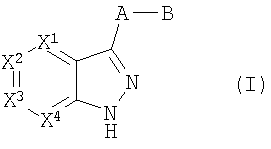
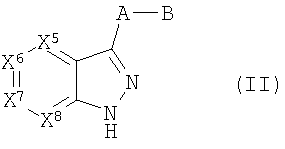
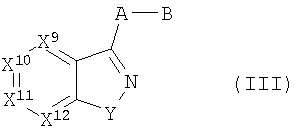
где
А означает -CH2- или
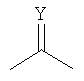 ,
,
В означает
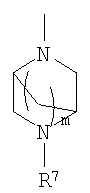 ;
;
Y означает О или S;
X1-X4 каждый независимо означает СН, CR1 или N, причем по крайней мере один из Х1-Х4 означает N,
X5-X8 каждый независимо означает СН, CR2 или N, причем по крайней мере один из Х5-Х8 означает N,
X9-X12 каждый независимо означает СН, CR3 или N, причем по крайней мере один из X9-X12 означает N,
R1, R2 и R3 каждый независимо означает
Н,
C1-С6алкил (например, СН3), который незамещен или замещен одной или более группами F, Cl, Br, I, CN, ОН, алкокси, содержащий от 1 до 4 атомов углерода (например, ОСН3), NR4R5, SH, SR4, SOR4, С3-С8циклоалкил, SO2R4, SO2NR4R5, Ar, Het или комбинации указанных групп,
С2-С6алкенил, который незамещен или замещен одной или более группами F, Cl, Br, I, CN, ОН, алкокси, содержащий от 1 до 4 атомов углерода (например, ОСН3), NR4R5, SH, SR4, SOR4, С3-С8циклоалкил, SO2R4, SO2NR4R5, Ar, Het или комбинации указанных групп,
С2-С6алкинил, который незамещен или замещен одной или более группами F, Cl, Br, I, CN, ОН, алкокси, содержащий от 1 до 4 атомов углерода (например, ОСН3), NR4R5, SH, SR4, SOR4, С3-С8циклоалкил, SO2R4, SO2NR4R5, Ar, Het или комбинации указанных групп,
С3-С8циклоалкил, который незамещен или замещен одной или более группами F, Cl, Br, I, CN, ОН, алкокси, содержащий от 1 до 4 атомов углерода (например, ОСН3), NR4R5, SH, SR4, SOR4, незамещенный С3-С8циклоалкил, SO2R4, SO2NR4R5, Ar, Het или комбинации указанных групп,
галоген (например, F, Cl, Br, I),
CN, NO2, NR4R5, SH, SR4, SOR4, SO2R4, SO2NR4R5, NR4SO2R5, CONR4R5, COOR4, NR4COR5, NR4CO2R5, NR4CONR4R5,
Ar,
Het или
R6O-;
R4 и R5 каждый независимо означает Н или
Ar, Ar-С1-С4алкил, Het, С1-С4алкил (например, СН3), С3-С8циклоалкил (например, циклопропил), или С4-С8циклоалкилалкил (например, циклопропилметил), каждый из которых незамещен или замещен одной или более группами F, Cl, Br, I, CN, ОН, алкокси, содержащий от 1 до 4 атомов углерода (например, ОСН3), моноалкиламино, диалкиламино (например, диэтиламино), С3-С8циклоалкил или комбинации указанных групп,
R6 означает
Н,
C1-С6алкил (например, СН3), который незамещен или замещен одной или более группами F, Cl, Br, I, CN, ОН, алкокси, содержащий от 1 до 4 атомов углерода (например, ОСН3), NR4R5, SH, SR4, SOR4, С3-С8циклоалкил, SO2R4, SO2NR4R5, Ar, Het или комбинации указанных групп,
С3-С6алкенил, который незамещен или замещен одной или более группами F, Cl, Br, I, CN, ОН, алкокси, содержащий от 1 до 4 атомов углерода (например, ОСН3), NR4R5, SH, SR4, SOR4, С3-С8циклоалкил, SO2R4, SO2NR4R5, Ar, Het или комбинации указанных групп,
С3-С6алкинил, который незамещен или замещен одной или более группами F, Cl, Br, I, CN, ОН, алкокси, содержащий от 1 до 4 атомов углерода (например, ОСН3), NR4R5, SH, SR4, SOR4, С3-С8циклоалкил, SO2R4, SO2NR4R5, Ar, Het или комбинации указанных групп,
С3-С8циклоалкил, который незамещен или замещен одной или более группами F, Cl, Br, I, CN, ОН, алкокси, содержащий от 1 до 4 атомов углерода (например, ОСН3), NR4R5, SH, SR4, SOR4, незамещенный С3-С8циклоалкил, SO2R4, SO2NR4R5, Ar, Het или комбинации указанных групп,
С4-С8циклоалкилалкил, который незамещен или замещен одной или более группами F, Cl, Br, I, CN, ОН, алкокси, содержащий от 1 до 4 атомов углерода (например, ОСН3), NR4R5, SH, SR4, SOR4, незамещенный С3-С8циклоалкил, SO2R4, SO2NR4R5, Ar, Het или комбинации указанных групп,
Ar или
Het;
R7 означает Н или
С1-С4алкил (например, СН3), который незамещен или замещен одной или более группами F, Cl, Br, I, CN, ОН, алкокси, содержащий от 1 до 4 атомов углерода (например, ОСН3), NR4R5 или комбинации указанных групп,
m равно 1, 2 или 3;
Ar означает арильную группу, содержащую от 6 до 10 атомов углерода, которая незамещена или замещена одной или более группами: алкил, содержащий от 1 до 8 атомов углерода, алкокси, содержащий от 1 до 8 атомов углерода, галоген (F, Cl, Br или I, предпочтительно F или Cl), диалкиламино, в котором каждый алкильный фрагмент содержит от 1 до 8 атомов углерода, амино, циано, гидроксил, нитро, галогенированный алкил, содержащий от 1 до 8 атомов углерода, галогенированный алкокси, содержащий от 1 до 8 атомов углерода, гидроксиалкил, содержащий от 2 до 8 атомов углерода, гидроксиалкокси, содержащий от 2 до 8 атомов углерода, алкенилокси, содержащий от 3 до 8 атомов углерода, алкилтио, содержащий от 1 до 8 атомов углерода, алкилсульфинил, содержащий от 1 до 8 атомов углерода, алкилсульфонил, содержащий от 1 до 8 атомов углерода, моноалкиламино, содержащий от 1 до 8 атомов углерода, циклоалкиламино, в котором циклоалкильная группа содержит от 3 до 7 атомов углерода и необязательно является замещенной, арилокси, в котором арильный фрагмент содержит от 6 до 10 атомов углерода (например, фенил, нафтил, бифенил) и необязательно является замещенным, арилтио, в котором арильный фрагмент содержит от 6 до 10 атомов углерода (например, фенил, нафтил, бифенил) и необязательно является замещенным, циклоалкилокси, в котором циклоалкильная группа содержит от 3 до 7 атомов углерода и необязательно является замещенной, сульфо, сульфониламино, ациламидо (например, ацетамидо), ацилокси (например, ацетокси), карбокси, алкоксикарбонил, алкиламинокарбонил или комбинации указанных групп, и
Het означает гетероциклическую группу, полностью насыщенную, частично насыщенную или полностью ненасыщенную, содержащую от 5 до 10 атомов в цикле, в котором по крайней мере 1 атом в составе цикла является атомом N, О или S, который является незамещенным или замещенным одним или более атомами галогена (F, Cl, Br или I, предпочтительно F или Cl), группами: арил, содержащий от 6 до 10 атомов углерода (например, фенил, нафтил, бифенил) и необязательно замещенный, арилалкил, содержащий от 6 до 10 атомов углерода в арильном фрагменте и от 1 до 4 атомов углерода в алкильном фрагменте, гетероциклическая группа, которая является полностью насыщенной, частично насыщенной или полностью ненасыщенной и содержит от 5 до 10 атомов в цикле, в котором по крайней мере 1 атом в составе цикла является атомом N, О или S, алкил, содержащий от 1 до 8 атомов углерода, алкокси, содержащий от 1 до 8 атомов углерода, циано, трифторметил, нитро, оксо, амино, моноалкиламино, содержащий от 1 до 8 атомов углерода, диалкиламино, в котором каждая алкильная группа содержит от 1 до 8 атомов углерода, алкоксикарбонил, алкиламинокарбонил или комбинации указанных групп, и
фармацевтически приемлемые соли указанных соединений.
В другом варианте осуществления настоящего изобретения в формулах I, II и III R4 и R5 каждый независимо означает Н, Ar, Het или С1-С4алкил (например, СН3), который является незамещенным или замещенным одним или более группами: F, Cl, Br, I, CN, ОН, алкокси, содержащий от 1 до 4 атомов углерода (например, ОСН3), моноалкиламино, диалкиламино (например, диэтиламино), С3-С8циклоалкил или их комбинации, а R1, R2 и R3 не означают NR4CO2R5 или NR4CONR4R5.
Термин алкил, использованный в данном контексте, означает прямой или разветвленный алифатический углеводородный радикал, содержащий предпочтительно от 1 до 4 атомов углерода. Пригодные алкильные группы включают метил, этил, пропил, изопропил, бутил, втор-бутил и трет-бутил.
Термин «алкокси» означает группы алкил-O-, в которых алкильный фрагмент предпочтительно содержит от 1 до 4 атомов углерода. Пригодные алкоксигруппы включают метокси, этокси, пропокси, изопропокси, изобутокси и втор-бутокси.
Термин «циклоалкил» означает циклический, бициклический или трициклический насыщенный углеводородный радикал, содержащий от 3 до 8 атомов углерода. Пригодные циклоалкильные группы включают циклопропил, циклобутил, циклопентил и циклогексил. Другие пригодные циклоалкильные группы включают спиропентил, бицикло[2.1.0]пентил и бицикло[3.1.0]гексил.
Циклоалкильные группы замещены группами: С1-С4алкил, С1-С4алкокси, гидроксил, амино, моноалкиламино, содержащий от 1 до 4 атомов углерода, и/или диалкиламино, в котором каждая алкильная группа содержит от 1 до 4 атомов углерода.
Термин «циклоалкилалкил» означает циклоалкилалкильные радикалы, в которых значения фрагментов циклоалкил и алкил описаны выше. Пригодные примеры включают циклопропилметил и циклопентилметил.
Термин «арил», в качестве группы или заместителя в целом, или в качестве фрагмента группы или заместителя означает ароматичекий карбоциклический радикал, содержащий от 6 до 10 атомов углерода, если не указано иное. Пригодные арильные группы включают фенил, нафтил и бифенил. Замещенные арильные группы включают описанные выше арильные группы, которые замещены одним или более атомами галогена, группами алкил, гидрокси, алкокси, нитро, метилендиокси, этилендиокси, амино, алкиламино, диалкиламино, гидроксиалкил, гидроксиалкокси, карбокси, циано, ацил, алкоксикарбонил, алкилтио, алкилсульфинил, алкилсульфонил, фенокси и ацилокси (например, ацетокси).
Термин «арилалкил» означает арилалкильный фрагмент, в котором значения фрагментов арил и алкил определены выше. Пригодные примеры включают бензил, 1-фенетил, 2-фенетил, фенпропил, фенбутил, фенпентил и нафтилметил. Ar-алкил означает также арилалкильный фрагмент, в котором значение арильного фрагмента соответствует определению группы Ar. Пригодные примеры включают бензил и фторбензил.
Термин «гетероциклические группы» означают насыщенные, частично насыщенные или полностью ненасыщенные гетероциклические группы, содержащие 1, 2 или 3 цикла и от 5 до 10 атомов углерода в составе всех циклов, в которых по крайней мере один из атомов в составе циклов является атомом N, О или S. Предпочтительно, гетероциклическая группа содержит от 1 до 3 гетероатомов в составе цикла, которые выбирают из N, О и S. Пригодные насыщенные и частично насыщенные гетероциклические группы включают, без ограничения перечисленным, тетрагидрофуранил, тетрагидротиенил, пирролидинил, пиперидинил, пиперазинил, морфолинил, изоксазолинил и т.п. Пригодные гетероарильные группы включают, без ограничения перечисленным, фурил, тиенил, пирролил, пиразолил, имидазолил, пиридил, пиримидинил, индолил, хинолинил, изохинолинил, нафтиридинил и т.п. Другие примеры пригодных гетероциклических групп включают 2-хинолинил, 1,3-бензодиоксил, 2-тиенил, 2-бензофуранил, 2-бензотиофенил, 3-тиенил, 2,3-дигидро-5-бензофуранил, 4-индолил, 4-пиридил, 3-хинолинил, 4-хинолинил, 1,4-бензодиоксан-6-ил, 3-индолил, 2-пирролил, 3,4-1,2-бензопиран-6-ил, 5-индолил, 1,5-бензоксепин-8-ил, 3-пиридил, 6-кумаринил, 5-бензофуранил, 2-изоимидазол-4-ил, 3-пиразолил и 3-карбазолил.
Замещенные гетероциклические группы означают гетероциклические группы, описанные выше, замещенные в одном или более положениях группами, например, галоген, арил, алкил, алкокси, циано, трифторметил, нитро, оксо, амино, алкиламино и диалкиламино.
Фрагменты, замещенные одним или более заместителями, предпочтительно содержат от 1 до 3 заместителей, прежде всего 1 или 2 заместителя, которые выбирают из описанных примеров заместителей. Галогенированные фрагменты, такие как галогенированные алкильные группы, предпочтительно означают фторированные фрагменты и включают пергалогенированные фрагменты, такие как трифторметил.
В соединениях формулы I R1 предпочтительно означает Н, OR6, NR4R5, NR4COR5, NR4CONR4R5, CF3, Br, тиенил, который незамещен или замещен (например, 2-тиенил, 3-тиенил и метилтиенил, такой как 2-(4-метил)тиенил и 2-(5-метил)тиенил), фурил, который незамещен или замещен (например, 2-фурил, 3-фурил и метилфурил, такой как 2-(5-метил)фурил), фенил, который незамещен или замещен (например, фторфенил, такой как 3-фторфенил и 4-фторфенил), метоксифенил, такой как 4-метоксифенил, тиазолил, такой как 2-тиазолил, 2-(4-метил)тиазолил и 2-(5-метил)тиазолил, оксазолил, такой как 2-оксазолил, и пиранил, такой как 4-тетрагидропиранил и 3,6-дигидропиран-4-ил.
В соединениях формулы II R2 предпочтительно означает Н, OR6, CF3, Br, тиенил, который незамещен или замещен (например, 2-тиенил, 3-тиенил и метилтиенил, такой как 2-(4-метил)тиенил и 2-(5-метил)тиенил), фурил, который незамещен или замещен (например, 2-фурил, 3-фурил и метилфурил, такой как 2-(5-метил-фурил), или фенил, который незамещен или замещен (например, фторфенил, такой как 3-фторфенил и 4-фторфенил, и метоксифенил, такой как 4-метоксифенил).
В соединениях формулы III R3 предпочтительно означает Н, циклопропил или OR6.
R4 предпочтительно означает Н или метил, a R5 предпочтительно означает H, метил, циклопропил, циклопентил, циклопропилметил, пропил или Ar-метил.
R6 предпочтительно означает метил, этил, CF3, CHF2, циклопентил или циклопропилметил.
R7 предпочтительно означает Н, метил или этил.
В соединениях формул I, II и III А предпочтительно означает -СО-. В соединениях формул I, II и III m предпочтительно равно 1 или 2.
Ar предпочтительно означает незамещенный или замещенный фенил (например, фторфенил, такой как 3-фторфенил и 4-фторфенил, и метоксифенил, такой как 4-метоксифенил).
Het предпочтительно означает незамещенный или замещенный тиенил (например, 2-тиенил, 3-тиенил, и метилтиенил, такой как 2-(4-метил)тиенил и 2-(5-метил)тиенил), или незамещенный или замещенный фурил (например, 2-фурил, 3-фурил, и метилфурил, такой как 2-(5-метил)фурил).
В формуле I каждый Х1-X4 предпочтительно означает СН или CR1. В формуле II каждый Х4-X8 предпочтительно означает СН или CR2. В формуле III каждый Х9-X12 предпочтительно означает СН или CR3.
Согласно одному объекту настоящего изобретения соединения формул I, II и III выбирают из следующих соединений:
гидрохлорид 3-[(1S,4S)-2,5-диазабицикло[2.2.1]гепт-2-илкарбонил]-1Н-индазола,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазол,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(трифторметокси)-1Н-индазола,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(трифторметил)-1Н-индазола,
гидрохлорид 5-бром-3-[(1S,4S)-2,5-диазабицикло[2.2.1]гепт-2-илкарбонил]-1Н-индазола,
формиат 5-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
гидрохлорид 6-бром-3-[(1S,4S)-2,5-диазабицикло[2.2.1]гепт-2-илкарбонил]-1Н-индазола,
формиат 6-этокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола,
формиат 6-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола,
6-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазол,
формиат 7-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(2-тиенил)-1Н-индазола,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(4-метил-2-тиенил)-1Н-индазола,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(5-метил-2-тиенил)-1Н-индазола,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-фенил-1Н-индазола,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(2-тиенил)-1Н-индазола,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(3-тиенил)-1Н-индазола,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(4-метил-2-тиенил)-1Н-индазола,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(5-метил-2-фурил)-1Н-индазола,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(5-метил-2-тиенил)-1Н-индазола,
формиат 5-(2-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиат 5-(3-фторфенил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1H-индазола,
формиат 5-(4-фторфенил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиат 5-(4-метоксифенил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1 ]гепт-2-ил]карбонил}-1Н-индазола,
формиат 6-(2-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1 ]гепт-2-ил]карбонил}-1Н-индазола,
формиат 6-(3-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
3-{[(1S,4S)-5-этил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(3-тиенил)-1Н-индазола,
формиат 5-(3-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-бром-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1H-индазол и их фармацевтически приемлемых солей.
Согласно одному аспекту настоящего изобретения соединения формул I, II и III выбирают из следующих соединений:
гидрохлорид 3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-6-(1,3-тиазол-2-ил)-1Н-индазола,
3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-6-(1,3-тиазол-2-ил)-1Н-индазол,
3-[(1S,4S)-(2,5-диазабицикло[2.2.1]гепт-2-илкарбонил]-1Н-индазол,
гидрохлорид 3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-1Н-индазола,
3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-1Н-индазол,
формиат 3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазола,
3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол,
формиат 3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-6-(1,3-тиазол-2-ил)-1Н-индазола,
3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-6-(1,3-тиазол-2-ил)-1H-индазол,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(1,3-тиазол-2-ил)-1H-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(1,3-тиазол-2-ил)-1Н-индазол,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(2-тиенил)-1Н-индазол,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(3-тиенил)-1Н-индазол,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(4-метил-2-тиенил)-1Н-индазол,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(5-метил-2-тиенил)-1Н-индазол,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(трифторметокси)-1Н-индазол,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-фенил-1Н-индазол,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(1,3-оксазол-2-ил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(1,3-оксазол-2-ил)-1Н-индазол,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(1,3-тиазол-2-ил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(1,3-тиазол-2-ил)-1Н-индазол,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(2-тиенил)-1Н-индазол,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(3-тиенил)-1Н-индазол,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(4-метил-1,3-тиазол-2-ил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(4-метил-1,3-тиазол-2-ил)-1Н-индазол,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(4-метил-2-тиенил)-1Н-индазол,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(5-метил-1,3-тиазол-2-ил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(5-метил-1,3-тиазол-2-ил)-1Н-индазол,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(5-метил-2-фурил)-1Н-индазол,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(5-метил-2-тиенил)-1Н-индазол,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(тетрагидро-2Н-пиран-4-ил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(тетрагидро-2Н-пиран-4-ил)-1Н-индазол,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(трифторметокси)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(трифторметокси)-1Н-индазол,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(трифторметил)-1Н-индазол,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-7-(трифторметокси)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-7-(трифторметокси)-1Н-индазол,
5-(2-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
5-(3-фторфенил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
5-(3-фурил)-3-{[(1S,4S)-5-метал-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
5-(4-фторфенил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
5-(4-метоксифенил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1H-индазол,
формиат 5-(циклопентилокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-(циклопентилокси)-3-{[(1S,4S)-5-метал-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил)-1Н-индазол,
формиат 5-(циклопропилметокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло [2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-(циклопропилметокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
5-амино-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол,
5-амино-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(1,3-тиазол-2-ил)-1Н-индазол,
5-бром-3-{[(1S,4S)-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
5-гидрокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
формиат 5-метокси-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазола,
гидрохлорид 3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-5-метокси-1Н-индазола,
3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-5-метокси-1Н-индазол,
формиат 5-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
6-(2-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
формиат 6-(3,6-дигидро-2Н-пиран-4-ил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
6-(3,6-дигидро-2Н-пиран-4-ил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
6-(3-фурил)-3-{((1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
формиат 6-(циклопентилокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
6-(циклопентилокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
формиат 6-циклопропил-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола,
6-циклопропил-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазол,
6-этокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазол,
гидрохлорид 3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-6-метокси-1Н-индазола,
3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-6-метокси-1Н-индазол,
формиат 6-метокси-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1H-индазола,
6-метокси-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол,
гидрохлорид 6-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиат 6-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1 ]гепт-2-ил]карбонил}-1Н-индазола,
6-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
7-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазол,
формиат N-(3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил)-N'-пропилмочевины,
N-(3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил)-N'-пропилмочевина,
формиат N-{3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-ил}циклопропанкарбоксамида,
N-{3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-ил}циклопропанкарбоксамид,
формиат N-{3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-ил}-N'-пропилмочевины,
N-{3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-ил}-N'-пропилмочевина,
и их фармацевтически приемлемых солей.
Согласно одному объекту настоящего изобретения соединения формул I, II и III выбирают из следующих соединений:
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизоксазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизоксазол,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(4-метил-1,3-тиазол-2-ил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(4-метил-1,3-тиазол-2-ил)-1Н-индазол,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(5-метил-1,3-тиазол-2-ил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(5-метил-1,3-тиазол-2-ил)-1Н-индазол,
формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(тетрагидро-2Н-пиран-4-ил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(тетрагидро-2Н-пиран-4-ил)-1Н-индазол,
формиат 5-(3,6-дигидро-2Н-пиран-4-ил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-(3,6-дигидро-2Н-пиран-4-ил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
формиат 5-(дифторметокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-(дифторметокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
формиат 6-(дифторметокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло [2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
6-(дифторметокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
формиат 7-фтор-6-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
7-фтор-6-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол,
формиат N-(3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил)циклопропанкарбоксамида,
N-(3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил)циклопропанкарбоксамид,
формиат N-(4-фторбензил)-N'-(3-{[(1S,4S)-5-метил-2,5-диазабицмкло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил)мочевины,
N-(4-фторбензил)-N'-(3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил)мочевина,
формиат N-(4-фторбензил)-N'-{3-[5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-ил}мочевины,
N-(4-фторбензил)-N'-{3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-ил}мочевина,
N-(циклопропилметил)-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-амин,
N-(циклопропилметил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-амин,
формиат N,N-диметил-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-амина,
N,N-диметил-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-амин,
формиат N,N-диметил-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-амина,
N,N-диметил-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-амин,
формиат N,N-диметил-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-6-амина,
N,N-диметил-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-6-амин,
формиат N-циклопентил-N'-(3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил)мочевины,
N-циклопентил-N'-(3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил)мочевина,
формиат N-циклопентил-N'-{3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-ил}мочевины,
N-циклопентил-N'-{3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-ил}мочевина,
и их фармацевтически приемлемых солей.
Предпочтительные объекты включают фармацевтические композиции, содержащие соединение по настоящему изобретению и фармацевтически приемлемый носитель и, необязательно, другой активный агент, как описано ниже; способ стимулирования или активирования ингибирования альфа-7-никотиновых рецепторов, которое, например, определяют стандартным методом анализа или описанным в данном контексте методом, in vitro или in vivo (с использованием животного, например, на модели животного, или с участием млекопитающего или человека), способ лечения неврологического синдрома, например, потери памяти, прежде всего долговременной потери памяти, нарушения или снижения познавательной способности, ухудшения памяти и т.п., способы лечения патологических состояний, модулированных активностью альфа-7 никотинового рецептора, у млекопитающего, например, у человека, например, как указано в данном контексте.
Соединения по настоящему изобретению получают по стандартным методикам. Некоторые из известных способов, которые можно использовать, описаны ниже. Все исходные материалы являются описанными соединениями или их получают по стандартным методикам из известных исходных материалов.
Синтез исходных соединений описан в находящейся на рассмотрении заявке №10/669645, поданной 25 сентября 2003 г., полное содержание которой включено в данное описание в качестве ссылки.
Кислоты, используемые при получении бициклоамида, являются коммерческими продуктами, их получают по методикам, описанным в литературе, или способы их получения описаны ниже. Например, индазол-3-карбоновая кислота является коммерческим препаратом. Броминдазолсодержащие кислоты получают также из соответствующих изатинов с использованием гидролиза в щелочных условиях, диазотирования и восстановления (Snyder H.R. и др., J.Am.Chem.Soc., 74, 2009 (1952)). Бензизоксазол-3-карбоновую кислоту получают также из 2,5-дибромнитробензола при взаимодействии с диэтилмалонатом, омылении, декарбоксилировании, с последующей переэтерификацией, взаимодействием с изоамилнитритом в щелочных условиях, гидрированием и омылением (Angell R.M., Baldwin I.R., Bamborough P., Deboeck N.M., Longstaff T., Swanson S, WO 04010995 A1). 3-Бензизотиазолкарбоновую килоту получают из тиофенола при взаимодействии с оксалилхлоридом и хлоридом алюминия с последующей обработкой гидроксиламином, пероксидом водорода и гидроксидом натрия. Бициклоамины, используемые при получении бициклоамидов, являются коммерческими препаратами, их получают по методикам, описанным в литературе, или способы их получения описаны ниже. Например, гидрохлорид (1S,4S)-2-трет-бутилоксикарбонил-2,5-диазабицикло[2.2.1]гептана является коммерческим препаратом. (1S,4S)-2-метил-2,5-диазабицикло[2.2.1 ]гептан получают при восстановлении трет-бутилкарбамата в присутствии литий-алюминий гидрида или по последовательности реакций восстановительного аминирования с последующим удалением защитных групп. 2,5-Диазабицикло[2.2.2]октан получают, как описано в статьях (Newman H., J. Heterocyclic. Chem., 11, 449 (1974); Sturm P.A., Henry D.W., J.Med.Chem., 17, 481 (1974)). 2-Метил-2,5-диазабицикло[2.2.2]октан получают из диэтилового эфира 2,5-диаминогександиовой кислоты при циклизации промежуточного N-бензилпроизводного, восстановлении третичных амидов, гидрировании, избирательном введении защитных групп, восстановительном аминировании и удалении защитных групп.
Бициклоамиды получают по реакции конденсации кислот с бициклоамином и HBTU или HOBt в присутствии EDCI в ДМФА, или превращением кислот в соответствующие хлорангидриды, а затем по реакции с бициклоамином (Масоr J.E., Gurley D., Lanthom Т., Loch J., Mack R.A., Mullen G., Tran O., Wright N., Macor J.E., Bioorg. Med. Chem. Lett., 9, 319 (2001). Конденсацию в большинстве случаев проводят при комнатной температуре в течение 4-8 ч. Аналоги тиоамидов получают из амидов при взаимодействии с реагентом Лавессона (Wipf P., Kim Y., Goldstein D.M., J.Am. Chem. Soc., 117, 11106 (1995)). Аналоги бициклометиленаминов получают из бициклоамидов по стандартным методикам восстановления, как описано, например, ниже. Полученные аддукты выделяют и очищают по стандартным методикам, таким как хроматография или перекристаллизация, известным специалистам в данной области техники.
Специалистам в данной области техники известно, что соединения формул I-III существуют в виде различных таутомерных и геометрических изомеров. Все указанные соединения, включая цис-изомеры, транс-изомеры, диастереомерные смеси, рацематы, нерацемические смеси энантиомеров, практически чистые и чистые энантиомеры включены в объем настоящего изобретения. Практически чистые энантиомеры содержат не более 5 мас.% соответствующего противоположного энантиомера, предпочтительно не более 2%, и наиболее предпочтительно не более 1%.
Оптические изомеры получают при разделении рацемических смесей по стандартным методикам, например, при образовании диастереомерных солей с использованием оптически активной кислоты или основания или при образовании ковалентных диастереомеров. Примеры соответствующих кислот включают винную, диацетилвинную, дибензоилвинную, дитолуоилвинную и камфарсульфоновую кислоту. Смеси диастереоизмеров разделяют на индивидуальные диастереомеры на основе их физических и/или химических различий по методикам, известным специалистам в данной области техники, например, с использованием хроматографии или фракционной кристаллизации. Оптически активные основания или кислоты затем выделяют из разделенных диастереомерных солей. Другой способ разделения оптических изомеров включает использование хиральной хроматографии (например, с использованием колонок хиральной ЖХВР), с использованием методов модификации или без них, причем методы модификации выбирают для повышения эффективности разделения энантиомеров. Пригодные колонки для хиральной ЖХВР выпускаются фирмой Diacel, например, такие как Chiracel OD и Chiracel OJ и т.п., которые характеризуются стандартной селективностью. Используют также ферментативное разделение, после стандартной модификации или без нее. Оптически активные соединения формул I-III получают с использованием оптически активных исходных материалов для хирального синтеза в условиях реакции, которые исключают рацемизацию.
Специалистам в данной области техники известно также, что соединения можно использовать в различных обогащенных изотопных формах, например, обогащенных по содержанию 2Н, 3Н, 11С, 13С и/или 14С. В одном предпочтительном варианте соединения дейтерируют. Такие дейтерированные формы получают по методикам, описанным в патентах США №5846514 и 6334997. Как описано в указанных патентах США, использование дейтерированных соединений приводит к улучшению эффективности и повышению продолжительности действия лекарственных средств.
Замещенные дейтерием соединения синтезируют с использованием различных методов, описанных в книге Dean Dennis С., Editor. Recent Advances in the Synthesis and Applications of Radiolabeled Compounds for Drug Discovery and Development (Curr., Pharm. Des., 6 (10) (2000)), 110, CAN 133:68895 AN 2000:473538 CAPLUS; Kabalka George W., Varma Rajender S., The synthesis of radiolabeled compounds via organometaleic intermediates. Tetrahedron, 45 (21), 6601-21 (1989) CODEN: TETRAB ISSN:0040-4020. CAN 112:20527 AN 1990:20527 CAPLUS, и Evans E. Anthony, Synthesis of radiolabeled compounds, J. Radioanal. Chem., 64 (1-2), 9-32 (1981), CODEN: JRACBN ISSN:0022-4081, CAN 95:76229 AN 1981:476229 CAPLUS.
Настоящее изобретение относится также к применимым формам соединениям, как описано в данном контексте, таким как фармацевтически приемлемые соли или пролекарства всех соединений по настоящему изобретению, для которых можно получить соли или пролекарства. Фармацевтически приемлемые соли включают соли, которые получают при взаимодействии соединения в форме основания с неорганической или органической кислотой с образованием соли, например, солей хлористоводородной кислоты, серной кислоты, фосфорной кислоты, метансульфоновой кислоты, камфорсульфоновой кислоты, щавелевой кислоты, малеиновой кислоты, янтарной кислоты, лимонной кислоты, муравьиной кислоты, бромистоводородной кислоты, бензойной кислоты, винной кислоты, фумаровой кислоты, салициловой кислоты, миндальной кислоты и карбоновой кислоты. Фармацевтически приемлемые соли включают также соли, в которых соединение в форме кислоты взаимодействует с соответствующим основанием с образованием соли, например, солей натрия, калия, кальция, магния, аммония и холина. Специалистам в данной области техники известно, что кислотно-аддитивные соли соединений по настоящему изобретению получают при взаимодействии соединений с соответствующей неорганической или органической кислотой по любой из известных методик. В другом варианте, соли щелочных и щелочно-земельных металлов получают при взаимодействии соединений по настоящему изобретению в соответствующими основаниями по любой из известных методик.
Ниже приведены примеры кислотно-аддитивных солей, которые получают при реакции с неорганическими или органическими кислотами: ацетаты, адипаты, альгинаты, цитраты, аспартаты, бензоаты, бензолсульфонаты, бисульфаты, бутираты, камфораты, диглюконаты, циклопентанпропионаты, додецилсульфаты, этансульфонаты, глюкогептаноаты, глицерофосфаты, гемисульфаты, гептаноаты, гексаноаты, фумараты, гидробромиды, гидроиодиды, 2-гидроксиэтансульфонаты, лактаты, малеаты, метансульфонаты, никотинаты, 2-нафталинсульфонаты, оксалаты, пальмоаты, пектинаты, персульфаты, 3-фенилпропионаты, пикраты, пивалаты, пропионаты, сукцинаты, тартраты, тиоцианаты, тозилаты, мезилаты и ундеканоаты.
Полученные соли предпочтительно являются фармацевтичеки приемлемыми для введения млекопитающим. Однако фармацевтически неприемлемые соли соединений являются пригодными для использования в качестве промежуточных соединений, например, для выделения соединения в виде соли и затем для превращения его обратно в свободное основание при обработке щелочным реагентом. Свободное основание затем при необходимости превращают в фармацевтически приемлемую кислотно-аддитивную соль.
Соединения по настоящему изобретению вводят в отдельности или в качестве активного ингредиента в составе композиции. Таким образом, настоящее изобретение включает также фармацевтические композиции соединений формул I-III, содержащие, например, один или более фармацевтически приемлемых носителей.
Методики получения различных композиций, пригодных для введения соединений по настоящему изобретению, описаны в ряде известных работ. Примеры возможных композиций и методик описаны, например, в книге Handbook of Pharmaceutical Excipients, American Pharmaceutical Association (последнее издание)); Pharmaceutical Dosage Forms: (Tablets (под ред. Lieberman, Lachman и Schwartz), последнее издание Marcel Dekker, Inc., Remington's Pharmaceutical Sciences (под ред. Arthur Osol), 1553-1593 (последнее издание).
С учетом стимулирующей активности в отношении рецептора α-7 и, предпочтительно, высокой степени селективности соединения по настоящему изобретению вводят пациентам, нуждающимся в стимуляции рецепторов α-7. Введение проводят в соответствии с состоянием пациента, например, назальным, парентеральным (подкожно, внутривенно, внутримышечно, внутригрудинно или с помощью вливания) способом, с помощью ингаляции, ректальным способом, вагинальным, местным или введением в глаз.
Для введения соединений по настоящему изобретению используют различные твердые лекарственные формы для перорального введения, включающие такие твердые формы, как таблетки, гелевые капсулы, капсулы, таблетки в виде капсул, гранулы, лепешки и порошки. Соединения по настоящему изобретению вводят в отдельности или в комбинации с различными фармацевтически приемлемыми носителями, разбавителями (такими, как сахароза, маннит, лактоза, крахмалы) и эксципиентами, известными в данной области техники, включая, без ограничения перечисленным, суспендирующие агенты, солюбилизирующие агенты, буферные агенты, связующие, дезинтегрирующие агенты, консерванты, красители, отдушки, замасливатели и т.п. Введение соединений по настоящему изобретению с использованием капсул, таблеток и гелей с замедленным высвобождением также характеризуется определенным преимуществом,
Для введения соединений по настоящему изобретению используют также различные жидкие лекарственные формы для перорального применения, включающие водные и неводные растворы, эмульсии, суспензии, сиропы и эликсиры. Такие лекарственные формы содержат также пригодные инертные разбавители, известные в данной области техники, такие как вода, и пригодные эксципиенты, известные в данной области техники, такие как консерванты, смачивающие агенты, подсластители, отдушки, а также агенты для эмульгирования и/или суспендирования соединений по настоящему изобретению. Соединения по настоящему изобретению вводят, например, внутривенно, в виде изотонического стерильного раствора. Используют также другие виды жидких лекарственных форм.
Суппозитории для ректального введения соединений по настоящему изобретению получают при смешивании соединения с пригодным эксципиентом, таким как масло какао, салицилаты и полиэтиленгликоли. Композиции для вагинального введения представляют собой пессарии, тампоны, кремы, гели, пасты, пены или спреи, содержащие активный ингредиент и пригодные носители, известные в данной области техники.
Фармацевтические композиции для местного введения используют в виде кремов, мазей, линиментов, лосьонов, эмульсий, суспензий, гелей, растворов, паст, порошков, спреев и капель, пригодных для введения через кожу, глаза, уши или носоглотку. Местное введение осуществляют также чрескожным способом с использованием чрескожных пластырей.
Получают также аэрозольные композиции, пригодные для введения ингаляцией. Например, для лечения заболеваний дыхательных путей соединения по настоящему изобретению вводят ингаляцией в форме порошка (например, тонкоизмельченного порошка) или в форме распыленных растворов или суспензий. Аэрозольные композиции выпускают в баллонах, содержащих смесь соединений с пригодными пропеллентами под давлением.
Соединения вводят в виде индивидуального активного агента или в комбинации с другими фармацевтическими агентами, такими как другие агенты, которые используют при лечении нарушения познавательных способностей и/или потери памяти, например, другие агонисты α-7, ингибиторы PDE4, блокаторы кальциевых каналов, мускариновые модуляторы m1 и m2, модуляторы рецепторов аденозина, модуляторы амфакинов NMDA-R, модуляторы mGluR, модуляторы допамина, модуляторы серотонина, каннабиноидные модуляторы и ингибиторы холинэстеразы (например, донепезил, ривастигимин и глантанамин). В таких комбинациях каждый активный ингредиент вводят в соответствии с его стандартной дозировкой или в более низкой дозе по сравнению с его стандартной дозой.
Соединения по настоящему изобретению используют в сочетании с «положительными модуляторами», которые увеличивают эффективность агонистов никотиновых рецепторов. Положительные модуляторы описаны, например, в заявках WO 99/56745, WO 01/32619 и WO 01/32622. Такую комбинированную терапию используют при лечении состояний/заболеваний, связанных со сниженной трансмиссией никотиновых рецепторов.
Соединения по настоящему изобретению используют также в комбинации с соединениями, которые связываются с пептидами Аβ и таким образом ингибируют связывание пептидов с рецепторами подтипа α7nAChr (см., например, заявку WO 99/62505).
Настоящее изобретение включает также способы лечения, включающие активацию никотиновых рецепторов α-7. Таким образом, настоящее изобретение включает способы селективного активирования/стимулирования никотиновых рецепторов α-7 у животных, например, у млекопитающих, прежде всего, у человека, причем такое активирование/стимулирование оказывает терапевтическое действие, например, такое активирование приводит к ослаблению симптомов состояний, включающих неврологические синдромы, такие как потеря памяти, прежде всего долгосрочной памяти. Такие способы включают введение животному, нуждающемуся в таком лечении, прежде всего млекопитающему, предпочтительно человеку, эффективного количества соединения формул I-III, в отдельности или в виде компонента в составе композиции, как описано в данном контексте.
В одном объекте способа по настоящему изобретению предлагается способ лечения пациента (например, млекопитающего, такого как человек), страдающего от патологического состояния (например, от нарушения памяти), причем способ включает введение пациенту соединения формул I, II или III. Предпочтительно, патологическое состояние включает снижение активности никотинового ацетилхолинового рецептора.
В другом объекте способа по настоящему изобретению предлагается способ лечения или профилактики заболевания или состояния, возникшего в результате нарушения функции трансмиссии никотиновых ацетилхолиновых рецепторов у млекопитающих, например, у человека, причем способ включает введение пациенту эффективного количества соединения формул I, II или III.
В одном объекте способа по настоящему изобретению предлагается способ лечения или профилактики заболевания или состояния, возникшего в результате нарушения или недостаточности функции никотиновых ацетилхолиновых рецепторов, предпочтительно рецепторов α7nACh у млекопитающих, например, у человека, причем способ включает введение пациенту эффективного количества соединения формул I, II или III.
В другом объекте способа по настоящему изобретению предлагается способ лечения или профилактики заболевания или состояния, возникшего в результате подавления функции трансмиссии никотиновых ацетилхолиновых рецепторов у млекопитающих, например, у человека, причем способ включает введение количества соединения формул I, II или III, достаточного для активации рецепторов α7nACh.
В одном объекте способа по настоящему изобретению предлагается способ лечения или профилактики психотического нарушения, нарушения познавательной способности (например, ухудшение памяти) или нейродегенеративного заболевания у млекопитающих, например, у человека, причем способ включает введение эффективного количества соединения формул I, II или III.
В другом объекте способа по настоящему изобретению предлагается способ лечения или профилактики заболевания или состояния, возникшего в результате потери холинергических синапсов у млекопитающих, например, у человека, причем способ включает введение эффективного количества соединения формул I, II или III.
В одном объекте способа по настоящему изобретению предлагается способ лечения или профилактики нейродегенеративного нарушения при активации рецепторов α7nACh у млекопитающих, например, у человека, причем способ включает введение эффективного количества соединения формул I, II или III.
В другом объекте способа по настоящему изобретению предлагается способ защиты нейронов млекопитающих, например, человека, от нейротоксического действия, вызванного активацией рецепторов α7nACh, причем способ включает введение эффективного количества соединения формул I, II или III.
В одном объекте способа по настоящему изобретению предлагается способ лечения или профилактики нейродегенеративного нарушения путем ингибирования связывания пептидов Аβ с рецепторами α7nACh у млекопитающих, например, у человека, причем способ включает введение эффективного количества соединения формул I, II или III.
В другом объекте способа по настоящему изобретению предлагается способ защиты нейронов млекопитающих, например, человека, от нейротоксического действия пептидов Аβ, причем способ включает введение эффективного количества соединения формул I, II или III.
В одном объекте способа по настоящему изобретению предлагается способ ослабления ингибирования холинэргической функции, вызванного действием пептидов Аβ, у млекопитающих, например, у человека, причем способ включает введение эффективного количества соединения формул I, II или III.
Соединения по настоящему изобретению являются никотиновыми лигандами типа α-7, предпочтительно агонистами, прежде всего частичными агонистами никотинового ацетилхолинового рецептора α-7. Способы определения активности никотинацетилхолина описаны в данной области техники (см., например, статью Davies A.R. и др., "Characterisation of the binding of [3H]methyllycaconitine: a new radioligand for labelling alpha 7-type neuronal nicotinic acetylcholine receptors," Neuropharmacology, 38(5), 679-90 (1999)). Соединения в качестве агонистов рецепторов nAChR α-7 применяют для профилактики и лечения ряда заболеваний и состояний, связанных с центральной нервной системой. Никотиновые ацетилхолиновые рецепоры являются рецепторами типа лиганд-гастрол, входящими в состав ионных каналов, и состоят из 5 белковых субъединиц, которые образуют центральную ионнопроводящую полость. В настоящее время известно 11 нейрональных субъединиц рецептора nAChR (α2-α9 и β2-β4). Существует также 5 других субъединиц, которые экспрессируются в периферийной нервной системе (α1, β1, γ, δ, ε).
Подтипы рецепторов nAChR могут образовывать гомопентамер или гетеропентамер. В настоящее время наибольший интерес представляет гомопентамерный рецептор подтипа α7, состоящий из 5 субъединиц α7. Рецепторы α7nAChR характеризуются высоким сродством к никотину (агонист) и α-бунгаротоксину (антангонист). Установлено, что агонисты α7nAChR можно применять при лечении психотических заболеваний, нейродегенеративных заболеваний и нарушений памяти и т.п. Несмотря на то, что никотин является известным агонистом, существует необходимость в разработке других агонистов рецепторов α7nAChR, прежде всего селективных агонистов, которые характеризуются меньшей токсичностью или сниженным побочным действием по сравнению с никотином.
Анабазеин, т.е. 2-(3-пиридил)-3,4,5,6-тетрагидропиридин, является природным токсином, выделенным из некоторых морских червей (немертины) и муравьев (см., например, в статье Кеm и др., Toxicon, 9:23 (1971). Анабазеин является высокоэффективным активатором никотиновых рецепторов млекопитающих, см. Статью Kem, Amer. Zoologist, 25, 99 (1985)). Некоторые аналоги анабазеина, такие как анабазин и DMAB (3-[4-(диметиламино)бензилиден]-3,4,5,6-тетрагидро-2',3'-бипиридин), известны также в качестве агонистов никотинового рецептора (см. патент США №5602257 и заявку WO 92/15306). Один аналог анабазеина, (Е-3-[2,4-диметоксибензилиден]анабазеин, известный также как GTS-21 и DMXB (см., например, патент США №5741802), является селективным частичным агонистом рецептора α7-nAChR, свойства которого подробно описаны. Например, установлено, что аномальное сенсорное ингибирование наблюдается при сенсорной процессинговой недостаточности у больных шизофренией, а GTS-21 приводит к повышению сенсорного ингибирования при взаимодействии с рецепторами α7-nAChRs (см., например, статью Stevens и др., Psychopharmacology, 136, 320-27 (1998)).
Другим известным селективным агонистом рецептора α7-nAChR является трописетрон, т.е. 1αH, 5αН-тропан-3α-илиндол-3-карбоксилат (см. статью J.Е.Macor и др., "The 5-НТ3-Antagonist Tropisetron (ICS 205-930) is a Potent and Selective A7 Nicotinic Receptor Partial Agonist", Bioorg. Med. Chem. Lett., 319-321, 2001).
Показано, что агенты, которые связываются с никотиновыми ацетилхолиновыми рецепторами, пригодны при лечении и/или профилактике различных заболеваний и состояний, прежде всего нарушения психики, нейродегенеративных заболеваний, вызванных дисфункцией холинергической системы, и состояний, связанных с нарушениями памяти и/или познавательной способности, включающих, например, шизофрению, тревожные состояния, мании, депрессии, маниакальные депрессии (примеры нарушения психики), болезнь Туретта, болезнь Паркинсона, болезнь Гентингтона (примеры нейродегенеративных заболеваний), нарушения познавательной способности (такие как болезнь Альцгеймера, деменция с тельцами Леви, боковой амиотрофический склероз, нарушения памяти, потери памяти, недостаточности познавательной способности, недостаточность внимания, гиперактивное состояние неостаточности внимания), а также при лечении никотиновой зависимости, последствий отказа от курения, при лечении болей (например, в качестве болеутоляющих средств), обеспечение нейрозащиты, при лечении страха перед полетом на самолете, при лечении воспалений или сепсиса (см., например, заявки на выдачу патентов США № WO 97/30998, WO 99/03850, WO 00/42044, WO 01/36417; статьи Holladay и др., J.Med. Chem., 40 (26), 4169-94 (1997), Schmitt и др., Annual Reports Med. Chem., гл.5, 41-51 (2000), Stevens и др., Psychopharmatology, 136: 320-27 (1998) и Shytle и др., Molecular Psychiatry, 7, 525-535 (2002)).
Таким образом, в настоящем изобретении предлагается способ лечения пациента, прежде всего человека, страдающего от психотических заболеваний, нейродегенеративных заболеваний, вызванных дисфункцией холинергической системы, и состояний, связанных с нарушениями памяти и/или познавательной способности, включающих, например, шизофрению, тревожные состояния, мании, депрессии, маниакальные депрессии (примеры нарушения психики), синдром Туретта, болезнь Паркинсона, болезнь Гентингтона (примеры нейродегенеративных заболеваний), и/или нарушения познавательной способности (такие как болезнь Альцгеймера, деменция с тельцами Леви, боковой амиотрофический склероз, нарушения памяти, потери памяти, недостаточность познавательной способности, недостаточность внимания, гиперактивное состояние недостаточности внимания), причем способ включает введение пациенту эффективного количества соединения формул I-III.
Нейродегенеративные заболевания, описанные в способах по настоящему изобретению, включают, без ограничения перечисленным, лечение и/или профилактику болезни Альцгеймера, болезни Пика, деменции с диффузными тельцами Леви, прогрессирующего супрануклеарного паралича (синдром Стила-Ричардсона), мультисистемной дегенерации (синдром Шая-Дрейджера), заболеваний двигательных нейронов, включающих боковой амиотрофический склероз, дегенеративную атаксию, корковую базальную дегенерацию, комплексное заболевание боковой амиотрофический склероз - болезнь Паркинсона - деменция (комплекс Гуама), подострый склеротичный панэнцефалит, заболевание Гетингтона, болезнь Паркинсона, синуклеинопатии, первичную прогрессирующую афазию, стриатонигральную дегенерацию, заболевание Мачадо-Джозефа/спинально-церебеллярную атаксию типа 3, оливомостомозжечковые дегенерации, заболевание Жиля де ла Туретта, бульбарный паралич, псевдобульбарный паралич, спинно-мышечная атрофия, спинно-бульбарная мышечная атрофия (заболевание Кеннеди), первичный боковой склероз, семейная спастическая параплегия, болезнь Верднига-Хоффмана, болезнь Кудельберга-Веландера, болезнь Тея-Сакса, болезнь Сандхоффа, семейная спастическая болезнь, болезнь Вольфарта-Кудельберга-Веландера, спазматический парапарез, прогрессирующая мультифокальная лейкоэнцефалопатия, прионовые болезни (такие как заболевания Крейтцфельдта-Якоба, Герстманна-Штройслера-Шейнкера, болезнь куру и фатальная наследственная бессонница), и нейродегенеративных заболеваний, возникающих вследствии ишемии или инфаркта головного мозга, включая эмболическую окклюзию и тромботическую окклюзию, а также внутричерепные кровоизлияния всех видов (включая, без ограничения перечисленным, эпидуральное, субдуральное, субарахноидальное и внутримозговое) и внутричерепные и внутрипозвоночные повреждения (включающие, без ограничения перечисленным, контузию, проникновение, сдвиг, сжатие и разрыв).
Агонисты рецепторов α-7nAChR, такие как соединения по настоящему изобретению, используют также при лечении возрастной деменции и других деменций и состояний, характеризующихся потерей памяти, включающих возрастное ослабление памяти, слабоумие, мультиинфарктную деменцию, диффузный отек белого вещества (болезнь Бинсвангера), деменцию эндокринной или метаболической природы, деменцию, вызванную травмой головы и диффузным повреждением мозга, деменцию при синдроме боксеров и деменцию при лобном синдроме (см., например, заявку на выдачу патента WO 99/62505). Таким образом, в настоящем изобретении предлагается способ лечения пацинта, прежде всего человека, страдающего от возрастной деменции или других деменций и состояний, характеризующихся ослаблением памяти, включающий введение пациенту эффективного количества соединения формул I-III.
Таким образом, в одном варианте настоящего изобретения предлагается способ лечения пациентов, страдающих от нарушений памяти вследствие, например, легкой степени нарушения познавательной способности, связанной с возрастом, болезни Альцгеймера, шизофрении, болезни Паркинсона, болезни Гентингтона, болезни Пика, болезни Крейтцфельда-Якоба, депрессии, старения, травм головы, инсульта, гипоксии ЦНС, мозгового слабоумия, мультиинфарктной деменции и других неврологических состояний, а также ВИЧ и сердечно-сосудистых заболеваний, причем способ включает введение пациенту эффективного количества соединения формул I-III.
Установлено, что амилоидный белок-предшественник (АРР) и выделенные из него пептиды Аβ, например, пептиды Aβ1-40, Aβ1-42, и другие фрагменты включены в патологические процессы при болезни Альцгеймера. Пептиды Аβ1-42 не только включены в процесс нейротоксичности, но и ингибируют холинергическую медиаторную функцию. Было установлено также, что пептиды Аβ связываются с рецепторами α-7nAChR. Таким образом, агенты, блокирующие связывание пептидов Аβ с рецепторами α-7nAChR, можно использовать при лечении нейродегенеративных заболеваний (см, например, заявку WO 99/62505). Кроме того, стимуляция рецепторов α-7nAChR защищает нейроны от циотоксичности, связанной с действием пептидов Аβ (см., например, статью Kihara Т. и др., Ann. Neurol., 42, 159 (1997).
Таким образом, в одном варианте настоящего изобретения предлагается способ лечения и/или профилактики деменции у пациента, страдающего болезнью Альцгеймера, включающий введение субъекту терапевтически эффективного количества соединения формул I-III для ингибирования связывания амилоидного бета-пептида (предпочтительно. Аβ1-42) с рецепторами nAChR, предпочтительно рецепторами α-7nAChR, более предпочтительно рецепторами α-7nAChR человека (а также способ лечения и/или профилактики других клинических проявлений болезни Альцгеймера, которые включают, без ограничения перечисленным, недостаточность познавательной способности и нарушение речи, апраксию, депрессию, галлюцинации и другие невропсихиатрические симптомы и признаки, а также нарушения двигательной моторики и походки.
В настоящем изобретении предлагается также способ лечения других амилоидозных заболеваний, например, наследственной церебральной ангиопатии, не-невропатического наследственного амилоидоза, синдрома Дауна, макроглобулинемии, вторичной семейной средиземноморской лихорадки, синдрома Макла-Уэлса, множественной миеломы, панкреатического и сердечного амилоидозов, хронической гемодиализной антропатии и амилоидозов Финниша и Иова.
Никотиновые рецепторы включены также в процесс ответной реакции организма на потребление алкоголя. Таким образом, агонисты рецепторов α-7nAChR можно использовать при лечении синдромов, возникающих при отказе от употребления алкоголя, и при лечении отравления. Таким образом, в одном варианте настоящего изобретения предлагается способ лечения пациента с синдромами отказа от алкоголя, или от отравления, причем способ включает введение пациенту эффективного количества соединения формул I-III.
Агонисты рецепторов подтипа α-7nAChR можно также использовать для нейрозащиты от повреждений, вызванных инсультами, ишемией и глутамат-индуцированной экситотоксичностью. Таким образом, в одном варианте настоящего изобретения предлагается способ лечения пациента, обеспечивающий нейрозащиту от повреждений, вызванных инсультами, ишемией и глутамат-индуцированной экситотоксичностью, включающий введение пациенту эффективного количества соединения формул I-III.
Как указано выше, агонисты рецепторов подтипа α-7nAChR можно также использовать при лечении никотиновой зависимости, включающей отказ от курения, боли и лечение страха перед полетом, ожирения, диабета, воспаления и сепсиса. Таким образом, в одном варианте настоящего изобретения предлагается способ лечения пациента, страдающего от никотиновой зависимости, включающей отказ от курения, боли и лечения страха перед полетом, ожирения и/или диабета, или способ, облегчающий отказ от курения у пациента, включающий введение пациенту эффективного количества соединения формул I-III.
Кроме того, меченные производные соединений формул I-III (например, С11 или r F18 меченные производные) вследствие их сродства к рецепторам α-7nAChR используют для получения изображения (томографии) рецепторов, например, в ткани мозга. Таким образом, использование таких меченных агентов при получении изображения рецепторов in vivo возможно, например, с использованием метода позитронной эмиссинной томографии (PET).
Ухудшение памяти проявляется при снижении способности усваивать новую информацию и/или неспособности вспомнить запомненную ранее информацию. Ухудшение памяти является первичным симптомом деменции, а также может быть симптомом болезни Альцгеймера, шизофрении, болезней Паркинсона, Гентингтона, Пика, Крейтцфельда-Якоба, ВИЧ, сердечно-сосудистых заболеваний, травм головы, а также ухудшения познавательной способности, связанного с возрастом.
Таким образом, в одном варианте настоящего изобретения предлагается способ лечения пациента, страдающего, например, от снижения познавательной способности средней степени (MCI), сосудистой деменции (VaD), ухудшения познавательной способности, связанного с возрастом (AACD), амнезии, вызванной операциями на открытом сердце, остановкой сердца, и/или после общего наркоза, недостаточности памяти, вызванной действием введенных анестетиков, ухудшения познавательной способности, вызванного недостатком сна, синдрома хронической усталости, нарколепсии, деменции, вызванной СПИД, ухудшения познавательной способности, вызванного эпилепсией, синдрома Дауна, деменции, вызванной алкоголизмом, ухудшения памяти, вызванного приемом лекарственных средств/реагентов, деменции легионеров (синдром боксеров) и деменции у животных (например, собак, кошек, лошадей и т.п.), причем способ включает введение пациенту эффективного количества соединения формул I-III.
Дозы соединений по настоящему изобретению зависят от ряда факторов, включающих конкретный синдром, который подвергается лечению, тяжесть симптома, способ введения, частоту введения дозы, конкретное используемое соединение, эффективность, токсикологический профиль, фармакокинетический профиль соединения и наличие побочных отрицательных воздействий и других факторов.
Соединения по настоящему изобретению вводят млекопитающим, прежде всего человеку, при этом уровень стандартных доз является известным для агонистов никотиновых рецепторов α-7, таких как указанные выше известные агонисты никотиновых рецепторов α-7. Соединения вводят, например, в виде однократных или многократных доз, пероральным способом в количестве, например, 0,0001-10 мг/кг/сут, например, 0,01-10 мг/кг/сут. Лекарственная форма содержит, например, 1-200 мг активного компонента. Соединения вводят внутривенно в виде однократных или многократных доз.
Следует понимать, что при описании методик по настоящему изобретению ссылки на определенные буферные растворы, среду, реагенты, клетки, культуральные условия и т.п. не ограничивают объем настоящего изобретения и в указанный объем включены все родственные материалы, которые являются очевидными для специалистов в данной области техники. Например, в большинстве случаев один буферный раствор можно заменить другим буферным раствором, одну культуральную среду на другую, и при этом получить аналогичные результаты. Специалисты в данной области техники могут без проведения дополнительных экспериментов определить необходимость таких замен для оптимизации способов и методик по настоящему изобретению.
Следующие примеры иллюстрируют настоящее изобретение и не ограничивают его объем. Следует понимать, что при применении описанных в примерах методик возможны изменения и модификации различных вариантов осуществления изобретения.
Полное описание всех заявок на выдачу патента, патентов и публикаций, цитированных выше и ниже, включено в описание настоящего изобретения в качестве ссылок.
Примеры
Все спектры ЯМР измеряли при 300 МГц на приборе ЯМР Bruker Instruments, если не указано иное. Константы взаимодействия (J) приведены герцах (Гц), а величины химического сдвига указаны по отношению к сигналу TMS (80,00 част./млн). Реакции при микроволновом облучении проводили в микроволновом реакторе Personal Chemistry Optimizer™ в сосудах объемом 2,5 мл или 5 мл для микроволнового реактора Personal Chemistry. Все реакции проводили при 200°С в течение 600 с при фиксированном времени включения, если не указано иное. Для хроматографии использовали ионно-обменную смолу на основе сульфокислоты (SCX) фирмы Varian Technologies. Аналитическую ЖХВР проводили на колонках 4,6 мм × 100 мм Xterra RP18, 3,5 мкм (элюент: градиент (0,1% муравьиной кислоты)/ацетонитрил (0,1% муравьиной кислоты) от 20:80 до 80:20 вода, в течение 6 мин, если не указано иное.
Получение кислот
В следующих методиках (1-10) подробно описано получение индазол-, бензизоксазол- и бензизотиазолкарбоновых кислот, которые не являются коммерческими препаратами.
Методика 1
Получение 6-нитроиндазол-3-карбоновой кислоты и ее конденсация с бициклооснованиями с образованием нитрозамещенных производных
В сосуд для микроволнового реактора объемом 5 мл загружали 3-иод-6-нитроиндазол (1 ммоль), цианид меди (I) (2 ммоля) и N,N-диметилформамид (3 мл), сосуд закрывали и облучали в микроволновом реакторе при 185°С в течение 600 с. Реакционную смесь распределяли между этилацетатом (100 мл) и водой (100 мл), смесь фильтровали через целит. Органический слой собирали, промывали солевым раствором, сушили (сульфат магния) и концентрировали, при этом получали 122 мг смеси 3-циано-6-нитроиндазола и 6-нитроиндазола (10:1) в виде твердого вещества желтого цвета. Полученную смесь 3-циано-6-нитроиндазола и 6-нитроиндазола (10:1) растворяли в 10н. гидроксиде натрия и полученный раствор ярко-оранжевого цвета нагревали при 100°С в течение 1 ч.
Затем смесь охлаждали до комнатной температуры и осторожно подкисляли 3н. хлористоводородной кислотой до рН 1. Твердое вещество отделяли и растирали в EtOAc, при этом получали 51 мг 6-нитроиндазол-3-карбоновой кислоты в виде твердого вещества коричневого цвета. Полученную кислоту конденсировали с бициклооснованием по методике А.
6-Нитро-1H-индазол-3-карбоновую кислоту получали описанным выше способом.
Методика 2
Нитрование индазолкарбоновой кислоты и ее конденсация с бициклооснованиями с образованием нитрозамещенных производных
Этиловый эфир индазол-3-карбоновой кислоты (73,7 ммоля) растворяли в 20 мл конц. серной кислоты и полученную реакционную смесь охлаждали до 0°С, затем в течение 1 ч по каплям добавляли смесь конц. серной кислоты (12 мл) и 70% азотной кислоты (12 мл). Полученную смесь перемешивали при 0°С в течение 1 ч и выливали в измельченный лед (200 г). Твердое вещество отделяли фильтрованием в вакууме, промывали несколькими порциями воды и сушили в вакууме. Высушенное твердое вещество суспендировали в 250 мл ацетонитрила и полученную смесь кипятили с обратным холодильником в течение 2 ч. Затем смесь охлаждали до комнатной температуры, твердое вещество отделяли и сушили в вакууме, при этом получали этиловый эфир 5-нитроиндазол-3-карбоновой кислоты (53%) в виде бесцветного твердого вещества. Кислоту, полученную в условиях щелочного гидролиза, конденсировали с бициклооснованием по методике A. (Org. Synthesis, Coll. т.1, стр.372.)
5-Нитро-1H-индазол-3-карбоновую кислоту получали описанным выше способом.
Методика 3
Взаимодействие индазолариллития с кетонами и конденсация с бициклооснованиями с образованием гетероциклических производных
Трет-бутиловый эфир 6-броминдазол-3-карбоновой кислоты получали из кислоты при взаимодействии с 2-кратным избытком ди-трет-бутилдикарбоната с последующей обработкой гидроксидом натрия. В суспензию гидрида натрия (60% дисперсия в минеральном масле, 4,8 ммоля) в тетрагидрофуране (40 мл) при 0°С медленно добавляли раствор трет-бутилового эфира 6-броминдазол-3-карбоновой кислоты (4,0 ммоля) в тетрагидрофуране (4 мл). После перемешивания при 0°С в течение 0,5 ч смесь охлаждали до -78°С и добавляли 1,7М раствор трет-бутиллития в пентане (5,1 ммоля). Полученную смесь выдерживали при -78°С в течение 0,5 ч, затем по каплям добавляли раствор тетрагидропиран-4-она (5 ммолей) в тетрагидрофуране (1 мл). Смесь перемешивали при -78°С в течение 1 ч и нагревали до 0°С. Реакцию останавливали добавлением насыщенного водного раствора хлорида аммония и смесь распределяли между этилацетатом (100 мл) и водой (100 мл). Органический слой отделяли, промывали солевым раствором (50 мл), сушили (сульфат магния) и концентрировали. Остаток очищали хроматографией (элюент: этилацетат/гексан, 70:30), при этом получали трет-бутиловый эфир 6-(4-гидрокситетрагидропиран-4-ил)-1Н-индазол-3-карбоновой кислоты (68%) в виде бесцветного твердого вещества.
Трет-бутиловый эфир 6-(4-гидрокситетрагидропиран-4-ил)-1Н-индазол-3-карбоновой кислоты (0,86 ммоля) растворяли в трифторуксусной кислоте (3 мл) и смесь выдерживали при комнатной температуре в течение 16 ч. Растворитель упаривали в вакууме и остаток растирали в этилацетате, при этом получали 6-(3,6-дигидро-2Н-пиран-4-ил)-1Н-индазол-3-карбоновую кислоту (76%). Кислоту конденсировали с бициклооснованием по методике А.
Трет-бутиловый эфир 6-(4-гидрокситетрагидропиран-4-ил)-1Н-индазол-3-карбоновой кислоты (1,0 ммоля) растворяли в трифторуксусной кислоте (5 мл), триэтилсилане (2 мл) и дихлорметане (3 мл), полученную смесь кипятили с обратным холодильником в течение 16 ч. Растворитель упаривали в вакууме и остаток растирали в этилацетате, при этом получали 6-(тетрагидропиран-4-ил)-1H-индазол-3-карбоновую кислоту (60%) в виде твердого вещества желто-коричневого цвета. Кислоту конденсировали с бициклооснованием по методике А.
Следующие кислоты получали по описанному способу:
6-(3,6-дигидро-2Н-пиран-4-ил)-1Н-индазол-3-карбоновая кислота,
6-(тетрагидро-2Н-пиран-4-ил)-1Н-индазол-3-карбоновая кислота.
Методика 4
Превращение замещенных изатинов в соответствующие индазол-3-карбоновые кислоты
Превращение замещенных изатинов в соответствующие индазол-3-карбоновые кислоты проводили аналогично тому, как описано для индазол-3-карбоновой кислоты, Snyder H.R. и др., J. Am. Chem. Soc. 74, 2009 (1952). Замещенный изатин (22,1 ммоля) разбавляли 1н. гидроксидом натрия (24 мл) и нагревали при 50°С в течение 30 мин. Полученный раствор темно-красного цвета нагревали до КТ и выдерживали в течение 1 ч. Реакционную смесь охлаждали до 0°С и при указанной температуре обрабатывали раствором нитрита натрия (22,0 ммоля) в воде (5,5 мл). Полученный раствор при 0°С добавляли в интенсивно перемешиваемый раствор серной кислоты (2,3 мл) в воде (45 мл) с помощью пипетки, погруженной ниже уровня раствора серной кислоты. Добавление проводили в течение 15 мин, затем реакционную смесь выдерживали в течение еще 30 мин. В реакционную смесь в течение 10 мин добавляли охлажденный (0°С) раствор дигидрата хлорида олова (II) (52,7 ммоля) в конц. хлористоводородной кислоте (20 мл) и смесь выдерживали в течение 60 мин. Полученный твердый осадок отделяли фильтрованием, промывали водой и сушили, при этом получали продукт с количественным выходом. Полученный материал обладал достаточной чистотой (по данным 1Н ЯМР и МС-ЖХ) и его использовали на следующей стадии без дополнительной очистки. В другом варианте кислоту перекристаллизовывали из уксусной кислоты, при этом получали очищенный материал.
Следующие кислоты получали по описанному способу:
5-броминдазол-3-карбоновая кислота,
6-броминдазол-3-карбоновая кислота,
5-трифторметоксииндазол-3-карбоновая кислота,
6-трифторметилиндазол-3-карбоновая кислота,
5-метоксииндазол-3-карбоновая кислота.
Методика 5
Получение замещенных бензизотиазол-3-карбоновых кислот из соответствующих тиофенолов
В раствор 3-метокситиофенола (3,75 г, 26,7 ммоля) в эфире (20 мл) по каплям добавляли оксалилхлорид (3,7 мл, 43 ммоля). Смесь кипятили с обратным холодильником в течение 1,5 ч, охлаждали до КТ и концентрировали в вакууме. Полученное масло желтого цвета растворяли в дихлорметане (50 мл), охлаждали до 0°С и порциями добавляли хлорид алюминия (4,30 г, 32,0 ммоля). Полученную смесь кипятили с обратным холодильником в течение 30 мин, охлаждали до КТ и при перемешивании выливали в лед. Органический слой отделяли и последовательно промывали насыщенным водным раствором бикарбоната натрия, водой и солевым раствором. Органический слой сушили над сульфатом магния, фильтровали и концентрировали в вакууме. Остаток очищали хроматографией (элюент: этилацетат/гексан, 4:1), при этом получали 6-метокси-1-бензотиофен-2,3-дион (2,46 г, 47%) в виде твердого вещества оранжевого цвета.
В смесь диона (86 мг, 0,44 ммоля) в 30% водном растворе гидроксида аммония (2,0 мл) добавляли 35% водный раствор пероксида водорода (0,2 мл) и реакционную смесь выдерживали в течение 12 ч. Полученный твердый осадок розового цвета отделяли фильтрованием, промывали водой и сушили в высоком вакууме, при этом получали 6-метоксибензизотиазол-3-карбоксамид (39 мг, 42%).
В раствор амида (1,14 г, 5,46 ммоля) в метаноле (100 мл) добавляли 10н. гидроксид натрия (12 мл). Смесь кипятили с обратным холодильником в течение 12 ч, охлаждали до КТ и подкисляли медленным добавлением конц. хлористоводородной кислоты до рН<2. Органический слой экстрагировали дихлорметаном (2х) и сушили над сульфатом натрия. Неочищенный продукт очищали хроматографией (элюент: дихлорметан/метанол/муравьиная кислота, 300:50:1), при этом получали 6-метоксибензизотиазол-3-карбоновую кислоту (1,02 г, 89%) в виде твердого вещества розового цвета.
Следующие кислоты получали по описанному способу:
бензо[d]изотиазол-3-карбоновая кислота,
6-бромбензо[d]изотиазол-3-карбоновая кислота,
5-бромбензо[d]изотиазол-3-карбоновая кислота,
5-метоксибензо[d]изотиазол-3-карбоновая кислота,
6-метоксибензо[d]изотиазол-3-карбоновая кислота,
7-метоксибензо[d]изотиазол-3-карбоновая кислота,
6-этоксибензо[d]изотиазол-3-карбоновая кислота,
Методика 6
Конденсация бромированных эфиров бензотиазол-3-карбоновой кислоты и бронированных эфиров индазол-3-карбоновой кислоты в присутствии реактива Гриньяра с образованием алкил- и гетероциклических замещенных кислот.
Раствор бромида циклопропилмагния (25,0 ммоля, 3,7 экв., 0,5М) в тетрагидрофуране разбавляли тетрагидрофураном (60 мл) и обрабатывали при КТ раствором хлорида цинка (25,0 ммоля, 3,7 экв., 0,5М) в тетрагидрофуране. Через 10 мин в полученную суспензию добавляли бромированный этиловый эфир бензизотиазол-3-карбоновой кислоты (0,30 ммоля) и хлорид бис(трифенилфосфин)палладия (II) (0,95 ммоля, 0,1 экв.). Реакционную смесь выдерживали при температуре окружающей среды в течение 1 ч, а затем при 65°С в течение 1 ч. Реакцию останавливали добавлением насыщенного хлорида аммония и реакционную смесь экстрагировали дихлорметаном (3×). Экстракты сушили над сульфатом натрия и концентрировали досуха. Остаток очищали хроматографией (элюент: градиент дихлорметан/метанол, от 100:0 до 90:10), при этом получали циклопропилзамещенный амид. Амид растворяли в смеси метанол/тетрагидрофуран/вода (90:10:20 мл) и обрабатывали гидроксидом натрия (5,8 г). Полученную смесь кипятили с обратным холодильником в течение 12 ч, охлаждали до КТ, фильтровали и подкисляли, медленно добавляя конц. хлористоводородную кислоту, до рН<2. Водный слой экстрагировали этилацетатом (2×) и сушили над сульфатом натрия. Экстракты концентрировали, при этом получали кислоту (выход 38%). Кислоту конденсировали с бициклооснованием по методике А.
Указанный способ с небольшими модификациями использовали для получения бромированных производных индазол-3-пиперидинкарбоксамидов в присутствии различных реактивов Гриньяра. Реактив Гриньяра, содержащий тиазол, является коммерческим препаратом. В другом варианте ариллитий и соответствующее производное арилцинка получали по методике, описанной в статье Reeder M.R. и др., Org. Proc. Res. Devel. 7, 696, (2003). Производное цинка и оксазола, 4-метилтиазола и 5-метилтиазола получали по указанной методике. Следующие кислоты получали по описанному способу:
6-циклопропилбензо[d]изотиазол-3-карбоновая кислота,
6-(1,3-тиазол-2-ил)-1Н-индазол-3-карбоновая кислота,
5-(1,3-тиазол-2-ил)-1Н-индазол-3-карбоновая кислота,
5-(4-метил-1,3-тиазол-2-ил)-1Н-индазол-3-карбоновая кислота,
5-(5-метил-1,3-тиазол-2-ил)-1Н-индазол-3-карбоновая кислота,
6-(4-метил-1,3-тиазол-2-ил)-1Н-индазол-3-карбоновая кислота,
6-(5-метил-1,3-тиазол-2-ил)-1Н-индазол-3-карбоновая кислота,
6-(1,3-оксазол-2-ил)-1Н-индазол-3-карбоновую кислоту.
Методика 7
Получение 7-фтор-6-метокси-1Н-индазол-3-карбоновой кислоты
В раствор этилового эфира 6-метокси-1Н-индазол-3-карбоновой кислоты (500 мг, 2,27 ммоля) в ацетонитриле (15,0 мл) добавляли бис(тетрафторборат) 1-хлорметил-4-фтор-1,4-диазонийбицикло[2.2.2]остана (1,00 г, 2,82 ммоля) и реакционную смесь выдерживали при КТ в течение 18 ч. Затем реакционную смесь распределяли между водой (50 мл) и этилацетатом (50 мл), органический слой отделяли и промывали солевым раствором (25 мл), сушили (сульфат магния) и концентрировали. Остаток очищали хроматографией (элюент: градиент гексан/этилацетат, от 95:5 до 80:20), при этом получали фторированный эфир (541 мг, 23%). Раствор эфира (124 мг, 0,520 ммоля) в этаноле (5,00 мл) разбавляли 5,0М раствором гидроксида натрия (2,00 мл) и смесь выдерживали при КТ в течение 18 ч. Полученную смесь подкисляли 6н. хлористоводородной кислотой и распределяли между водой (50 мл) и этилацетатом (50 мл). Слои разделяли и органический слой промывали солевым раствором (25 мл), сушили (сульфат магния) и концентрировали в вакууме, при этом получали кислоту (109 мг, 84%). Кислоту конденсировали с бициклооснованием по методике А.
7-Фтор-6-метокси-1Н-индазол-3-карбоновую кислоту получали по описанной методике.
Методика 8
Получение бензизоксазол-3-карбоновой кислоты из 2.5-дибромнитробензола
В суспензию гидрида натрия (3,16 г, 132 ммоля) в диметилсульфоксиде (60 мл) в течение 30 мин добавляли диэтиловый эфир малоновой кислоты (12,6 г, 79 ммолей). При этом температура реакционной смеси повышается до 60°С и образуется прозрачный раствор, затем добавляли 1,4-дибром-2-нитробензол (10 г, 36,0 ммоля) и полученный раствор выдерживали при 100°С в течение 2 ч. Затем реакционную смесь охлаждали до КТ и выливали в лед (300-400 г). Полученный твердый осадок отделяли фильтрованием и сушили, при этом получали продукт (11,0 г, 89%).
Эфир (11,0 г, 32,0 ммоля) разбавляли 2н. раствором гидроксида натрия (32 мл, 63 ммоля) и реакционную смесь выдерживали при комнатной температуре в течение 16 ч. Водный слой экстрагировали дихлорметаном (20 мл) и подкисляли. Полученный твердый осадок отделяли фильтрованием и сушили, при этом получали кислоту (7,00 г, 89%).
В раствор кислоты (7,00 г, 27,0 ммоля) в этаноле (60 мл) добавляли серную кислоту (1 мл). Реакционную смесь кипятили с обратным холодильником, выдерживали в течение 2 ч и концентрировали при пониженном давлении. Остаток распределяли между этилацетатом (250 мл) и насыщенным карбонатом натрия (50 мл), органический слой промывали насыщенным карбонатом натрия (50 мл) и солевым раствором (50 мл), органический слой сушили (сульфат натрия) и концентрировали, при этом получали эфир (8,00 г, 98%) в виде жидкости.
Этилат натрия получали при взаимодействии в атмосфере N2 с натрием (33,5 г, 1,46 моля) в этаноле.
В раствор эфира (420 г, 1,46 моля) в этаноле (3 л), помещенный в трехгорлую круглодонную колбу объемом 10 л, добавляли изоамилнитрит (225 мл) и полученную смесь нагревали до 60°С. В смесь по каплям добавляли раствор этоксида натрия, полученный из металлического натрия (33,5 г, 1,46 ммоля) в этаноле (1 л), и реакционную смесь выдерживали в течение 2 ч, охлаждали до КТ и нейтрализовали 2н. хлористоводородной кислотой. Реакционную смесь экстрагировали этилацетатом (4×2 л) и объединенные органические слои промывали водой (2×1 л), солевым раствором (2×1 л) и сушили (сульфат натрия). Остаток очищали хроматографией (элюент: градиент гексан/этилацетат, от 1:1 до 0:1), при этом получали продукт (110 г, 28%).
В раствор 6-бромбензизоксазол-3-карбоновой кислоты (20 г, 0,081 моля) в этаноле (300 мл) при 0°С в атмосфере азота добавляли 10% палладий на угле (1,5 г) и триэтиламин (7,5 г, 82,4 ммоля). Атмосферу азота удаляли в вакууме и заменяли на атмосферу водорода, реакционную смесь выдерживали в течение 1 ч. Газообразный водород удаляли в вакууме и заменяли на азот, а палладий отделяли фильтрованием через целит. Осадок на фильтре промывали этанолом (3×50 мл) и фильтраты концентрировали. Остаток растворяли в дихлорметане (200 мл) и раствор промывали водой (4×50 мл), сушили (сульфат натрия) и упаривали, при этом получали продукт в виде твердого вещества желтого цвета (13,0 г, 96%). Эфир омыляли в присутствии гидроксида натрия, при этом получали кислоту. Кислоту конденсировали с бициклооснованием по методике A. (Angell R.M., Baldwin I.R., Bamborough P., Deboeck N.M., Longstaff T., Swanson S., WO 04010995 A1.)
1,2-Бензизоксазол-3-карбоновую кислоту получали по описанному способу.
Методика 9
Получение 5-дифторметоксииндазол-3-кислоты из 3-бром-4-нитрофенола
В суспензию гидроксида натрия (29,0 ммоля) в N,N-диметилформамиде (15 мл) добавляли 3-бром-4-нитрофенол (10,0 ммоля) и суспензию выдерживали при КТ в течение 15 мин. Реакционную смесь охлаждали до 0°С и обрабатывали этиловым эфиром хлордифторуксусной кислоты (20,0 ммоля), затем нагревали при 70°С в течение 16 ч и концентрировали. Остаток разбавляли ледяной водой (200 мл) и экстрагировали этилацетатом (3×100 мл), объединенные органические слои сушили (сульфат магния) и концентрировали, при этом получали дифторметиловый эфир (выход 75%) в виде масла желтого цвета.
В суспензию гидрида натрия (328 ммолей) в диметилсульфоксиде (40 мл) при 0°С по каплям добавляли диэтиловый эфир малоновой кислоты (328 ммолей). Реакционную смесь нагревали до 60°С и выдерживали в течение 0,5 ч. Затем в смесь по каплям добавляли раствор дифторметилового эфира (149 ммолей) в диметилсульфоксиде (80 мл) и реакционную смесь нагревали при 100°С в течение 5 ч. Охлажденный раствор выливали в ледяную воду и водный слой экстрагировали дихлорметаном (3×100 мл). Объединенные органические слои сушили (сульфат магния) и концентрировали, при этом получали неочищенный диэфир (выход 112%) в виде масла. Диэфир (167 ммолей), гидроксид натрия (500 ммолей) и воду (335 мл) смешивали и нагревали при 60°С в течение 1 ч. Затем реакционную смесь охлаждали до КТ и водный слой промывали дихлорметаном (3×100 мл). Водный слой осторожно подкисляли конц. хлористоводородной кислотой до рН 1 и реакционную смесь нагревали при 60°С в течение 1 ч. Полученную суспензию охлаждали до 5°С, а полученный твердый осадок отделяли фильтрованием и сушили, при этом получали кислоту (выход 61%).
В этанол (300 мл) при 0°С по каплям добавляли ацетилхлорид (203 ммоля). Через 0,5 ч добавляли кислоту (101 ммоль) и реакционную смесь кипятили с обратным холодильником в течение 15 ч. Затем реакционную смесь концентрировали и остаток распределяли между дихлорметаном (200 мл) и насыщенным бикарбонатом натрия (100 мл). Водный слой экстрагировали дихлорметаном (2×200 мл), объединенные органические слои сушили (сульфат магния) и концентрировали, при этом получали эфир (выход 60%) в виде масла коричневого цвета.
Эфир (60,4 ммоля) растворяли в этаноле (103 мл), разбавляли водой (71 мл), затем обрабатывали хлоридом аммония (243 ммоля) и порошкообразным железом (301 ммоль). Реакционную смесь кипятили с обратным холодильником в течение 10 мин и полученную суспензию фильтровали через целит, осадок на фильтре трижды промывали этанолом. Фильтрат концентрировали, остаток суспендировали в 2н. хлористоводородной кислоте и интенсивно перемешивали в течение 0,5 ч. Водный слой промывали этилацетатом (3×50 мл) и с использованием 5М гидроксида натрия доводили рН до 9-10. Водный слой экстрагировали хлороформом (3×100 мл) и объединенные органические слои сушили (сульфат магния). В органический слой добавляли уксусный ангидрид (392 ммоля), изоамилнитрит (291 ммоль) и ацетат калия (51,0 ммоля), полученную суспензию кипятили с обратным холодильником в течение 16 ч. Раствор упаривали, остаток распределяли между насыщенным бикарбонатом натрия (50 мл) и дихлорметаном (100 мл). Затем водный слой экстрагировали дихлорметаном (2×100 мл), объединенные органические слои сушили (сульфат магния) и концентрировали, при этом получали эфир N-ацетилиндазола (выход 79%) в виде масла коричневого цвета.
Эфир (63,8 ммоля), гидроксид натрия (193 ммоля) и воду (65 мл) перемешивали и реакционную смесь выдерживали при 60°С в течение 24 ч. После охлаждения до КТ водный слой промывали дихлорметаном (3×50 мл) и подкисляли конц. хлористоводородной кислотой до рН 1. Полученный твердый осадок отделяли фильтрованием, промывали водой и дихлорметаном, сушили и при этом получали кислоту (выход 27%).
5-(Дифторметокси)-1Н-индазол-3-карбоновую кислоту получали указанным способом.
Методика 10
Получение 6-дифторметоксииндазол-3-карбоновой кислоты из 4-нитрофенола
В суспензию гидроксида натрия (485 ммолей) в N,N-диметилформамиде (150 мл) добавляли 4-нитрофенол (162 ммоля) и суспензию выдерживали при КТ в течение 15 мин. Реакционную смесь охлаждали до 0°С и обрабатывали этиловым эфиром хлордифторуксусной кислоты (329 ммолей), затем нагревали при 70°С в течение 16 ч и концентрировали. Остаток разбавляли ледяной водой (200 мл) и экстрагировали этилацетатом (3×100 мл), объединенные органические слои сушили (сульфат магния) и концентрировали, при этом получали дифторметиловый эфир (выход 59%) в виде масла желтого цвета.
Нитроэфир (149 ммолей) растворяли в этаноле (37,5 мл), разбавляли водой (25 мл), затем обрабатывали хлоридом аммония (84,7 ммоля) и порошкообразным железом (105 ммолей). Реакционную смесь кипятили с обратным холодильником в течение 30 мин и полученную суспензию фильтровали через целит, осадок на фильтре трижды промывали этанолом. Объединенные фильтраты концентрировали, остаток растворяли в воде и с использованием 5М гидроксида натрия доводили рН до 9-10. Водный слой экстрагировали этилацетатом (3×100 мл), объединенные органические слои сушили (сульфат магния) и концентрировали, при этом получали масло желтого цвета. Масло растворяли в уксусном ангидриде (23,5 ммоля), реакционную смесь выдерживали при КТ в течение 16 ч. Реакционную смесь разбавляли водой (50 мл) и нейтрализовали твердым бикарбонатом натрия. Полученный твердый осадок отделяли фильтрованием, промывали водой, сушили и при этом получали ацетамид (выход 62%) в виде твердого вещества светло-желтого цвета.
В раствор ацетамида (13,2 ммоля) в хлороформе (20 мл) добавляли уксусный ангидрид (19,6 ммоля) и реакционную смесь нагревали до температуры кипения растворителя. Затем по каплям добавляли дымящую азотную кислоту (16,0 ммоля) и реакционную смесь кипятили с обратным холодильником в течение 30 мин. Охлажденный раствор разбавляли водой (20 мл) и водный слой экстрагировали дихлорметаном (3×10 мл). Объединенные органические слои сушили (сульфат магния) и концентрировали, при этом получали нитроамид (выход 83%).
Амид (11,0 ммоля), гидроксид натрия (43,8 ммоля) и воду (10 мл) перемешивали и реакционную смесь выдерживали при 60°С в течение 1,5 ч. Реакционную смесь охлаждали до КТ, полученный твердый осадок отделяли фильтрованием, промывали водой и сушили, при этом получали анилин (выход 98%) в виде твердого вещества светло-желтого цвета.
Анилин (15,7 ммоля) перемешивали в смеси с 40% бромистоводородной кислотой (14,3 г) и водой (10 мл), реакционную смесь нагревали до 80-90°С для полного растворения анилина. Затем смесь охлаждали до 0°С и в течение 15 мин добавляли раствор нитрита натрия (23,2 ммоля) в воде (5,3 мл). Полученный раствор выдерживали при 0-5°С в течение 40 мин и фильтровали. Бромид меди (I) (18,8 ммоля) растворяли в 40% бромистоводородной кислоте (21 мл) и охлаждали до 0°С. Раствор диазосоли медленно добавляли в раствор меди и смесь выдерживали при 0-10°С в течение 30 мин. Реакционную смесь нагревали при 60°С в течение 30 мин, а затем при 100°С в течение 10 мин до полного завершения реакции. Реакционную смесь охлаждали до КТ и экстрагировали дихлорметаном (3×40 мл). Объединенные органические слои промывали 1М гидроксидом натрия, 1н. хлористоводородной кислотой и водой. Органический слой сушили (сульфат магния) и концентрировали, при этом получали нитробромид (выход 76%) в виде твердого вещества светло-желтого цвета.
В суспензию гидрида натрия (25,8 ммоля) в диметилсульфоксиде (5 мл) при 0°С по каплям добавляли диэтиловый эфир малоновой кислоты (25,7 ммоля). Реакционную смесь нагревали до 60°С и выдерживали в течение 30 мин. Затем по каплям добавляли раствор нитробромида (11,7 ммоля) в диметилсульфоксиде (7 мл) и реакционную смесь нагревали при 100°С в течение 5 ч. Охлажденный раствор выливали в ледяную воду и водный слой экстрагировали дихлорметаном (3×100 мл). Объединенные органические слои сушили (сульфат магния) и концентрировали, при этом получали неочищенный диэфир в виде масла. Диэфир (11,7 ммоля), гидроксид натрия (35 ммолей) и воду (20 мл) смешивали и нагревали при 60°С в течение 1 ч. Затем реакционную смесь охлаждали до КТ и водный слой промывали дихлорметаном (3×100 мл). Водный слой осторожно подкисляли конц. хлористоводородной кислотой до рН 1 и реакционную смесь нагревали при 60°С в течение 1 ч. Полученную суспензию охлаждали до 0°С, а полученный твердый осадок отделяли фильтрованием и сушили, при этом получали кислоту (выход 64%).
В этанол (50 мл) при 0°С по каплям добавляли ацетилхлорид (15,3 ммоля). Через 30 мин добавляли кислоту (7,69 ммоля) и реакционную смесь кипятили с обратным холодильником в течение 15 ч. Затем реакционную смесь концентрировали и остаток распределяли между дихлорметаном (20 мл) и насыщенным бикарбонатом натрия (10 мл). Водный слой экстрагировали дихлорметаном (2×20 мл), объединенные органические слои сушили (сульфат магния) и концентрировали, при этом получали эфир (выход 94%) в виде масла коричневого цвета.
В суспензию эфира (3,64 ммоля) и уксусной кислоты (7,0 мл) при 0°С добавляли уксусный ангидрид (6,0 мл), затем порциями в течение 15 мин добавляли цинковую пыль (14,6 ммоля) и смесь выдерживали при 0°С в течение 30 мин и при КТ в течение 1,5 ч, добавляли еще одну порцию цинковой пыли (6,15 ммоля) и смесь выдерживали в течение 3 ч. Суспензию фильтровали через целит и фильтрат концентрировали. Остаток распределяли между насыщенным бикарбонатом натрия (10 мл) и этилацетатом (20 мл). Затем водный слой экстрагировали этилацетатом (3×20 мл), объединенные органические слои сушили (сульфат магния) и концентрировали, при этом получали ацетамид (выход 92%) в виде масла коричневого цвета.
В раствор ацетамида (3,92 ммоля) в хлороформе (20 мл) добавляли уксусный ангидрид (13,7 ммоля), изоамилнитрит (13,7 ммоля) и ацетат калия (2,04 ммоля), полученную суспензию кипятили с обратным холодильником в течение 16 ч. Раствор упаривали и остаток распределяли между насыщенным бикарбонатом натрия (10 мл) и дихлорметаном (20 мл). Затем водный слой экстрагировали дихлорметаном (2×20 мл) и объединенные органические слои сушили (сульфат магния) и концентрировали, при этом получали эфир N-ацетилиндазола (выход 92%) в виде масла коричневого цвета.
Эфир (3,36 ммоля), гидроксид натрия (10 ммолей) и воду (5 мл) перемешивали и реакционную смесь выдерживали при 60°С в течение 24 ч. После охлаждения до КТ водный слой промывали дихлорметаном (3×30 мл) и подкисляли конц. хлористоводородной кислотой до рН 1. Полученный твердый осадок отделяли фильтрованием, промывали водой и дихлорметаном, сушили и при этом получали кислоту (выход 26%).
6-(Дифторметокси)-1Н-индазол-3-карбоновую кислоту получали указанным способом.
Получение аминов: методика 11
Получение 2-метил-2,5-диазабицикло[2.2.2]октана из диэтилового эфира 2,5-диаминогександиовой кислоты.
В раствор дигидрохлорида диэтилового эфира 2,5-диаминогександиовой кислоты (10,0 ммоля) в абсолютном этаноле (75 мл) и уксусной кислоте (10 мл) при комнатной температуре добавляли бензальдегид (21,8 ммоля). Полученную смесь нагревали при 80°С в течение 2 ч. Реакционную смесь охлаждали до комнатной температуры и небольшими порциями добавляли триацетоксиборгидрид натрия (54,2 ммоля). Полученную суспензию белого цвета выдерживали при КТ в течение 16 ч и концентрировали. Остаток разбавляли водой, охлаждали до 0°С и с помощью 1н. гидроксида натрия доводили рН до 9. Затем водный слой экстрагировали этилацетатом (3×100 мл) и объединенные органические слои промывали солевым раствором, сушили (сульфат магния) и концентрировали, при этом получали твердое вещество белого цвета (3,05 г). В раствор дибензиламина в этаноле (200 мл) добавляли метоксид натрия (25 мас.%, 23 ммоля) и реакционную смесь кипятили с обратным холодильником в течение 16 ч. Затем реакционную смесь охлаждали до КТ и концентрировали. Остаток разбавляли этилацетатом (200 мл), промывали 1н. хлористоводородной кислотой, сушили (сульфат магния) и концентрировали, при этом получали бициклолактам (выход 47%) в виде бесцветного твердого вещества.
В суспензию литийалюминий гидрида (31,6 ммоля) в тетрагидрофуране (50 мл) при перемешивании в атмосфере азота по каплям добавляли серную кислоту (15,8 ммоля). Смесь выдерживали в течение 30 мин и при 0°С по каплям добавляли супернатант в раствор бициклического лактама (1,5 ммоля) в тетрагидрофуране (50 мл). Реакционную смесь нагревали до КТ и выдерживали в течение 16 ч. Реакцию осторожно останавливали добавлением порциями твердого декагидрата сульфата натрия (2,5 г). Реакционную смесь разбавляли 2М раствором гидроксида натрия (10 мл), фильтровали через целит и фильтрат концентрировали. Остаток разбавляли 2н. хлористоводородной кислотой (100 мл) и экстрагировали этилацетатом. Водный слой подщелачивали 2М гидроксидом натрия до рН 9 и экстрагировали этилацетатом (3×50 мл). Объединенные органические слои промывали солевым раствором, сушили (сульфат магния) и концентрировали. Полученное масло светло-желтого цвета обрабатывали раствором хлористого водорода в метаноле, который получали in situ при добавлении ацетилхлорида (0,5 мл) в метанол (10 мл) при комнатной температуре в течение 10 мин. Летучие компоненты удаляли при пониженном давлении, при этом получали дигидрохлорид бициклодиамина (выход 92%) в виде пены грязно-белого цвета.
Суспензию диамина (3,00 ммоля) и 10% палладия на угле (200 мг) в метаноле (100 мл) и конц. хлористоводородной кислоты (2 мл) помещали в атмосферу водорода и выдерживали в течение 16 ч. Катализатор удаляли фильтрованием и осадок на фильтре промывали водой. Фильтрат концентрировали, при этом получали дигидрохлорид бициклодиамина (выход 88%) в виде бесцветного твердого вещества.
В раствор диамина (7,06 ммоля) в изопропаноле (100 мл), воде (35 мл) и 1М растворе гидроксида натрия (6,5 мл) при 0°С по каплям добавляли раствор ди-трет-бутилдикарбоната (6,5 ммоля) в изопропаноле (15 мл). Реакционную смесь выдерживали при 0°С в течение 1,5 ч и концентрировали до объема ~ 50 мл. Водную суспензию насыщали твердым хлоридом натрия и с помощью 2М гидроксида натрия доводили рН до 10. Водный слой экстрагировали этилацетатом (3×35 мл) и объединенные органические слои промывали солевым раствором и сушили (сульфат магния). Летучие компоненты удаляли при пониженном давлении, при этом получали неочищенный моно-защищенный диамин (выход 42%) в виде масла светло-желтого цвета.
В раствор неочищенного амина (2,97 ммоля) в тетрагидрофуране (25 мл) добавляли водный раствор формальдегида (37%, 7,43 ммоля) и уксусную кислоту (4,46 ммоля). Через 10 мин в реакционную смесь небольшими порциями добавляли твердый триацетоксиборгидрид натрия (5,94 ммоля) и реакционную смесь выдерживали в течение 16 ч. Затем реакционную смесь разбавляли 10% водным раствором бикарбоната натрия (100 мл) и экстрагировали этилацетатом (3×40 мл). Объединенные органические слои промывали солевым раствором, сушили (сульфат магния) и концентрировали, при этом получали остаток светло-желтого цвета. Остаток растворяли в диоксане (25 мл) и разбавляли конц. хлористоводородной кислотой (12,5 мл). Через 30 мин летучие компоненты удаляли и при этом получали монометилбициклооснование (выход 40%) в виде бесцветного твердого вещества. Дигидрохлорид 2-метил-2,5-диазабицикло[2.2.1]гептана получали в условиях N-метилирования и удаления карбаматзащитной группы. (Newman H., J.Heterocyclic Chem. 11, 449, (1974); Sturm P.A., Henry D.W., J.Med.Chem. 17, 481, (1974)).
Следующие основания получали указанным способом:
дигидрохлорид 2-метил-2,5-диазабицикло[2.2.2]октана,
дигидрохлорид (1S,4S)-2-метил-2,5-диазабицикло [2.2.1] гептана.
Способы синтеза
В следующих методиках (A-G) подробно описано получение замещенных производных бициклооснований.
Методика А
Конденсирование бициклооснований и карбоновых кислот с образованием производных карбоксамида
В раствор карбоновой кислоты (1 ммоль) в тетрагидрофуране (10 мл) и N,N-диметилформамида (1 мл) добавляли N,N-диизопропилэтиламин (3 ммоля) и дигидрохлорид бициклоамина (1 ммоль). Реакционную смесь выдерживали при комнатной температуре в атмосфере азота в течение 30 мин, затем добавляли HATU (1,00 ммоля). Через 18 ч реакционную смесь распределяли между насыщенным водным раствором карбоната калия и дихлорметаном/метанолом (95:5). Водный слой дважды экстрагировали дихлорметаном/метанолом (95:5), объединенные органические слои промывали солевым раствором, сушили (сульфат натрия) и концентрировали в вакууме. Остаток очищали экспресс-хроматографией на колонке с силикагелем (элюент: дихлорметан/метанол/гидроксид аммония, 90:10:1), при этом получали карбоксамид.
Следующие соединения получали по методике А:
Пример 1
Гидрохлорид 3-[(1S,4S)-2,5-диазабицикло[2.2.1]гепт-2-илкарбонил]-1H-индазола
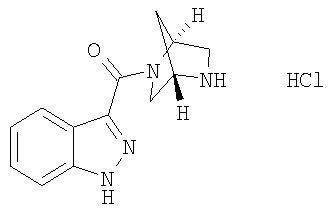
Соединение получали по методике А, выход 28%. МС-ЖХ (EI), в.у. 3,55 мин, m/z 243 (M++1).
1Н ЯМР (CD3OD): δ 8,22 (m, 1Н), 7,61 (m,1Н), 7,45 (m, 1Н), 7,27 (m, 1Н), 3,82 (m, 1Н), 3,51 (m, 2Н), 2,30 (m, 1Н), 2,07 (m, 1Н).
Пример 2
Гидрохлорид 3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-6-(1,3-тиазол-2-ил)-1Н-индазола
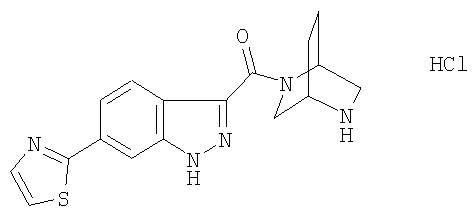
Соединение получали по методике А, выход 30%. МС-ЖХ (EI), в.у. 3,04 мин, m/z 340 (M++1).
Пример 3
Гидрохлорид 3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-1Н-индазола
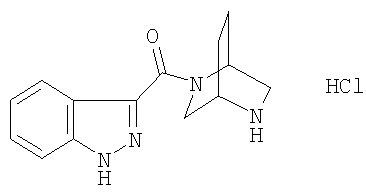
Соединение получали по методике А, выход 30%. МС-ЖХ (EI), в.у. 2,85 мин, m/z 257 (M++1).
Пример 4
Формиат 3-[(5-метил-2,5-диазабицикло[2.2.21окт-2-ил)карбонил]-1Н-индазола
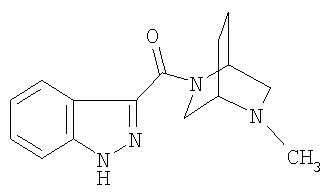
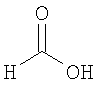
Соединение получали по методике А, выход 25%. МС-ЖХ (EI), в.у. 2,83 мин, m/z 271 (M++1).
Пример 5
Формиат 3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-6-(1,3-тиазол-2-ил)-1Н-индазола
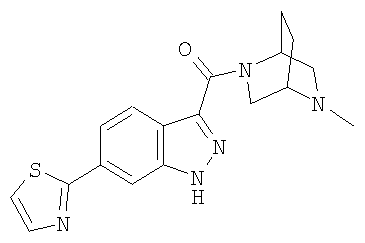
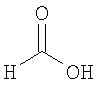
Соединение получали по методике А, выход 20%. МС-ЖХ (EI), в.у. 2,87 мин, m/z 376 (M++1).
Пример 6
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола
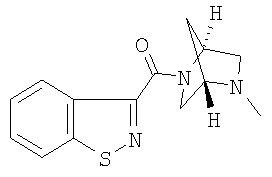
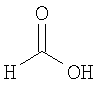
Соединение получали по методике А, выход 56%. МС-ЖХ (EI), в.у. 2,53 мин, m/z 274 (M++1).
Пример 7
3-{[(1S,4S)-5-Метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазол
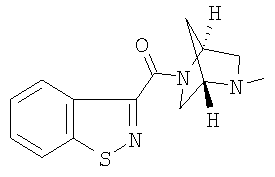
Соединение получали по методике А, выход 77%. МС-ЖХ (EI), в.у. 2,75 мин, m/z 274 (M++1).
Пример 8
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил1карбонил}-1,2-бензизоксазола
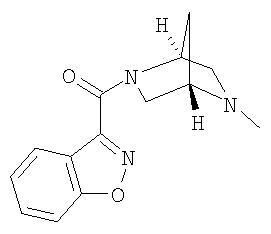
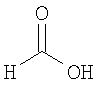
Соединение получали по методике А, выход 20%. МС-ЖХ (EI), в.у. 3,48 мин, m/z 258 (M++1).
Пример 9
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил1карбонил}-5-(1,3-тиазол-2-ил)-1Н-индазола
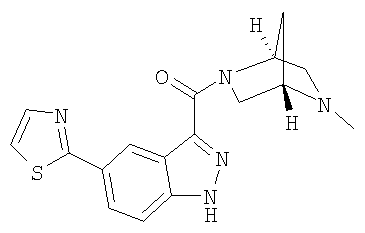
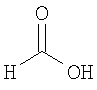
Соединение получали по методике А, выход 25%. МС-ЖХ (EI), в.у. 2,87 мин, m/z 340 (M++1).
Пример 10
Формиат 3-{[(1S',4S')-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(4-метил-1,3-тиазол-2-ил)-1Н-индазола
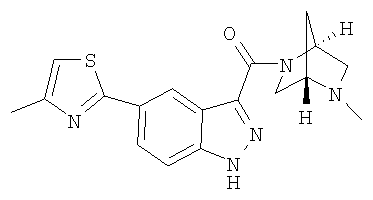
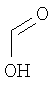
Соединение получали по методике А, выход 30%. МС-ЖХ (EI), в.у. 2,76 мин, m/z 354 (M++1).
Пример 11
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(5-метил-1,3-тиазол-2-ил)-1Н-индазола
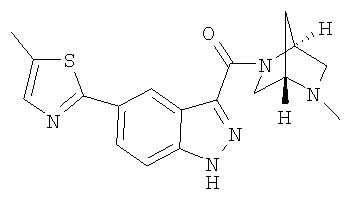
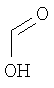
Соединение получали по методике А, выход 30%. МС-ЖХ (EI), в.у. 2,9 мин, m/z 354 (M++1).
Пример 12
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил1карбонил}-5-(тетрагидро-2Н-пиран-4-ил)-1Н-индазола
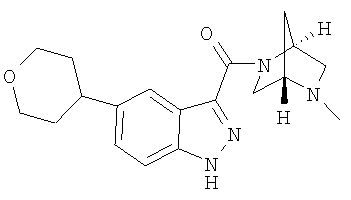
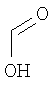
Соединение получали по методике А, выход 25%. МС-ЖХ (EI), в.у. 2,85 мин, m/z 339 (M++1).
Пример 13
Формиат 3-{[(1S,4S)-5-метил-2.5-диазабицикло[2.2.1]гепт-2-ил1карбонил}-5-(трифторметокси)-1Н-индазола
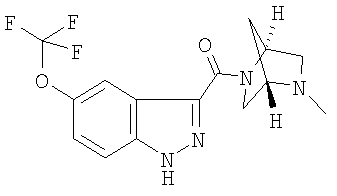
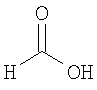
Соединение получали по методике А, выход 45%. МС-ЖХ (EI), в.у. 4,82 мин, m/z 341 (M++1).
Пример 14
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(1,3-оксазол-2-ил)-1Н-индазола
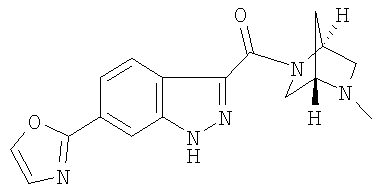
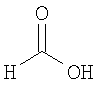
Соединение получали по методике А, выход 30%. МС-ЖХ (EI), в.у. 5,25 мин, m/z 324 (M++1).
Пример 15
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(1,3-тиазол-2-ил)-1Н-индазола
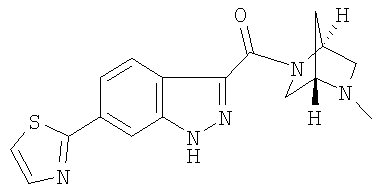
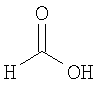
Соединение получали по методике А, выход 25%. МС-ЖХ (EI), в.у. 2,69 мин, m/z 362 (M++1).
Пример 16
Формиат 3-{[(1S,4S)-5-метил-2.5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(4-метил-1,3-тиазол-2-ил)-1Н-индазола
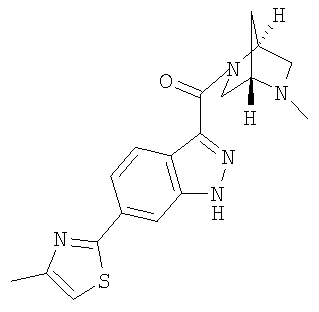
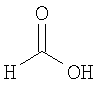
Соединение получали по методике А, выход 25%. МС-ЖХ (EI), в.у. 5,18 мин, m/z 354 (M++1).
Пример 17
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(5-метил-1,3-тиазол-2-ил)-1Н-индазола
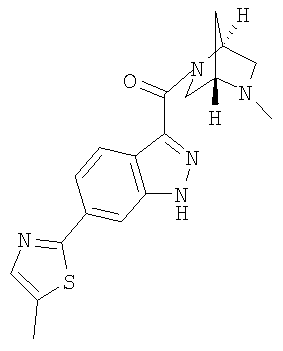
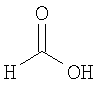
Соединение получали по методике А, выход 25%. МС-ЖХ (EI), в.у. 5,18 мин, m/z 354 (M++1).
Пример 18
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(тетрагидро-2Н-пиран-4-ил)-1Н-индазола
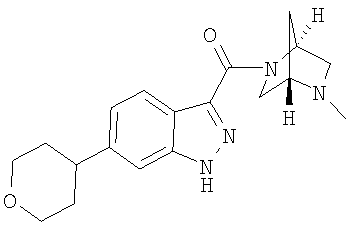
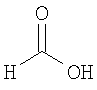
Соединение получали по методике А, выход 25%. МС-ЖХ (EI), в.у. 2,79 мин, m/z 341 (M++1).
Пример 19
Формиат 3-{[(1S,4S)-5-метил-2.5-диазабицикло[2.2.1]гепт-2-ил1]карбонил}-6-(трифторметокси)-1Н-индазола
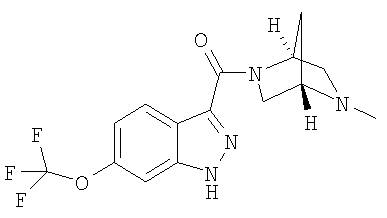
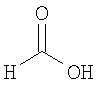
Соединение получали по методике А, выход 25%. МС-ЖХ (EI), в.у. 5,04 мин, m/z 341 (M++1).
Пример 20
Формиат 3-{[(1S,4S)-5-метил-2.5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(трифторметил)-1Н-индазола
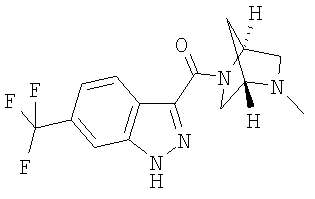
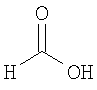
Соединение получали по методике А, выход 45%. МС-ЖХ (EI), в.у. 3,85 мин, m/z 325 (M++1).
Пример 21
Формиат 3-{[(1S,4S)-5-метил-2.5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-7-(трифторметокси)-1Н-индазола
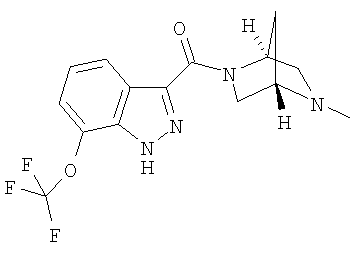
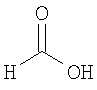
Соединение получали по методике А, выход 25%. МС-ЖХ (EI), в.у. 4,66 мин, m/z 341 (M++1).
Пример 22
Формиат 5-(3,6-дигидро-2Н-пиран-4-ил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола
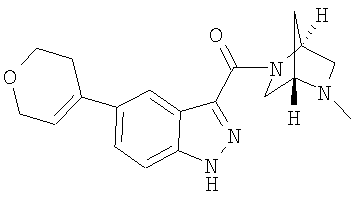
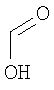
Соединение получали по методике А, выход 30%. МС-ЖХ (EI), в.у. 2,83 мин, m/z 339 (M++1).
Пример 23
Формиат 5-(дифторметокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола
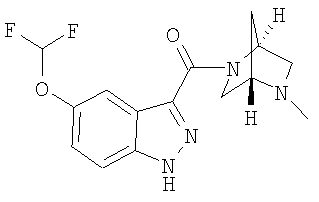
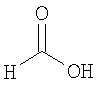
Соединение получали по методике А, выход 35%. МС-ЖХ (EI), в.у. 2,52 мин, m/z 323 (M++1).
Пример 24
Гидрохлорид 5-бром-3-[(1S,4S)-2,5-диазабицикло[2.2.1]гепт-2-илкарбонил]-1Н-индазола
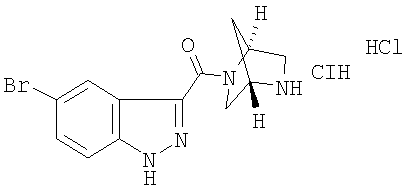
Соединение получали по методике А, выход 45%. МС-ЖХ (EI), в.у. 4,76 мин, m/z 321/323 (M++1).
Пример 25
Формиат 5-метокси-3-[(5-метил-2.5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазола
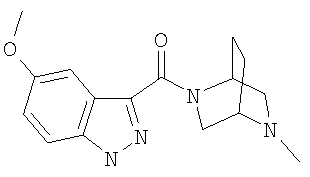
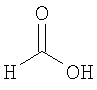
Соединение получали по методике А, выход 20%. МС-ЖХ (EI), в.у. 2,85 мин, m/z 301 (M++1).
Пример 26
Гидрохлорид 3-(2,5-диазабицикло [2.2.2]окт-2-илкарбонил)-5-метокси-1Н-индазола
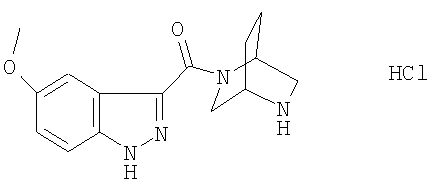
Соединение получали по методике А, выход 30%. МС-ЖХ (EI), в.у. 2,87 мин, m/z 287 (M++1).
Пример 27
Гидрохлорид 5-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола
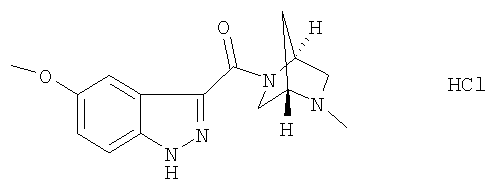
Соединение получали по методике А, выход 35%. МС-ЖХ (EI), в.у. 2,85 мин, m/z 287 (M++1).
Пример 28
Формиат 5-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола
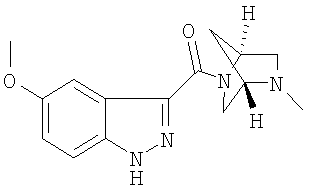
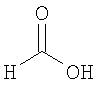
Соединение получали по методике А, выход 45%. МС-ЖХ (EI), в.у. 2,51 мин, m/z 287 (M++1).
Пример 29
Формиат 6-(3,6-дигидро-2Н-пиран-4-ил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола
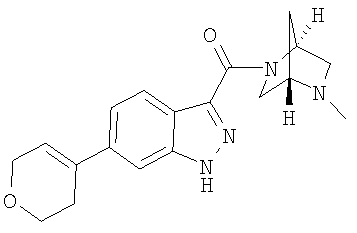
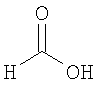
Соединение получали по методике А, выход 25%. МС-ЖХ (EI), в.у. 2,8 мин, m/z 339 (M++1).
Пример 30
Формиат 6-(дифторметокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола
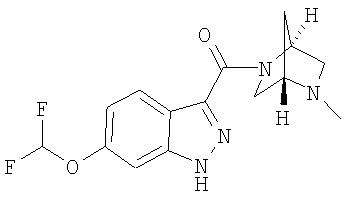
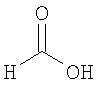
Соединение получали по методике А, выход 35%. МС-ЖХ (EI), в.у. 2,47 мин, m/z 323 (M++1).
Пример 31
Гидрохлорид 6-бром-3-[(1S,4S)-2,5-диазабидикло[2.2.1]гепт-2-илкарбонил]-1Н-индазола
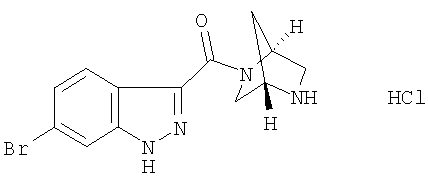
Соединение получали по методике А, выход 45%. МС-ЖХ (EI), в.у. 3,71 мин, m/z 321/323 (M++1).
Пример 32
Формиат 6-циклопропил-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил)-1,2-бензизотиазола
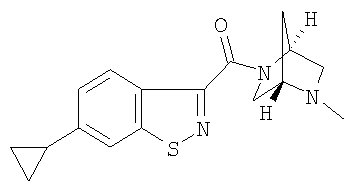
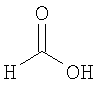
Соединение получали по методике А, выход 56%. МС-ЖХ (EI), в.у. 4,48 мин, m/z 314 (M++1).
Пример 33
Формиат 6-этокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола
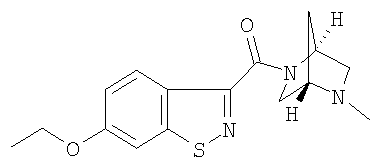
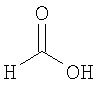
Соединение получали по методике А, выход 43%. МС-ЖХ (EI), в.у. 3,79 мин, m/z318 (M++1).
Пример 34
Гидрохлорид 3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-6-метокси-1Н-индазола
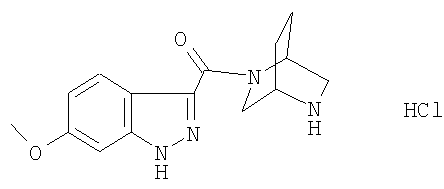
Соединение получали по методике А, выход 30%. МС-ЖХ (EI), в.у. 2,89 мин, m/z 287 (M++1).
Пример 35
Формиат 6-метокси-3-[(5-метил-2.5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазола
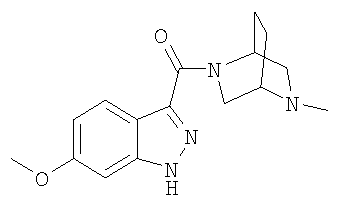
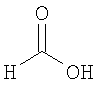
Соединение получали по методике А, выход 28%. МС-ЖХ (EI), в.у. 2,83 мин, m/z 301 (M++1).
Пример 36
Формиат 6-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола
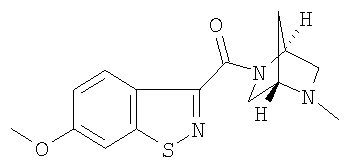
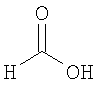
Соединение получали по методике А, выход 64%. МС-ЖХ (EI), в.у. 2,97 мин, m/z 304 (M++1).
Пример 37
6-Метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил)-1,2-бензизотиазол
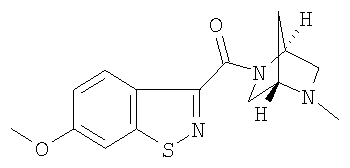
Соединение получали по методике А, выход 85%. МС-ЖХ (EI), в.у. 3,06 мин, m/z 304 (M++1).
Пример 38
Гидрохлорид 6-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло [2.2.1]гепт-2-ил]карбонил}-1Н-индазола
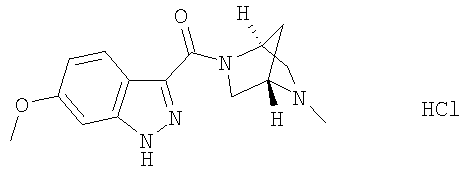
Соединение получали по методике А, выход 35%. МС-ЖХ (EI), в.у. 2,83 мин, m/z 287 (М++1).
Пример 39
Формиат 6-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола
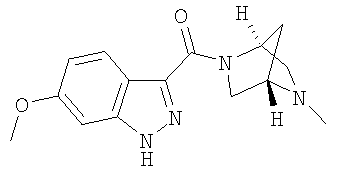
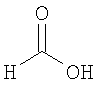
Соединение получали по методике А, выход 35%. МС-ЖХ (EI), в.у. 2,83 мин, m/z 287 (M++1).
Пример 40
Формиат 7-фтор-6-метокси-3-{[(1S,4S)-5-метил-2,5-диазабидикло[2.2.1]гепт-2-ил]карбонил}-1H-индазола
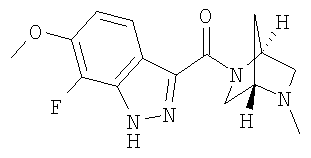
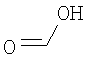
Соединение получали по методике А, выход 31%. МС-ЖХ (EI), в.у. 2,54 мин, m/z 305 (M++1).
Пример 41
Формиат 7-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола
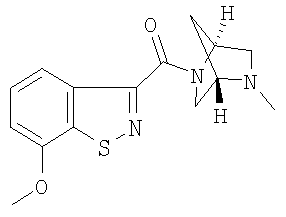
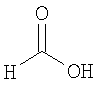
Соединение получали по методике А, выход 50%. МС-ЖХ (EI), в.у. 2,6 мин, m/z 304 (M++1).
Методика В
Конденсация бромированных и иодированных бициклокарбоксамидов и бороновых кислот с образованием арилзамещенных или гетероарилзамещенных производных
В сосуд для микроволнового реактора объемом 5 мл добавляли бромированный бициклокарбоксамид (0,3 ммоля), бороновую кислоту (0,6 ммоля), трис(дибензилиденацетон)дипалладия (0) (0,03 ммоля), тетрафторборат три-трет-бутилфосфина (0,06 ммоля) и карбонат калия (0,8 ммоля). Из сосуда удаляли воздух, заполняли аргоном и содержимое разбавляли N,N-диметилформамидом (5,0 мл). Сосуд закрывали и облучали в микроволновом реакторе при 200°С в течение 600 с. Реакционную смесь фильтровали чрез целит (промывали метанолом) и наносили на колонку 5 г SCX. Колонку промывали метанолом (50 мл) и продукт элюировали 2М аммиаком в метаноле и концентрировали. Осадок очищали хроматографией (элюент: от 1:1 до 0:1 этилацетат (этилацетат/метанол/гидроксид аммония, 70:30:1)), затем препаративной ЖХВР (элюент: градиент в течение 8 мин (0,1% муравьиная кислота)/ацетонитрил (0,1% муравьиная кислота) от 95:5 до 20:80 вода), при этом получали гетероарилзамещенный продукт.
В следующих примерах описано получение соединений по методике В:
Пример 42
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(2-тиенил)-1Н-индазола
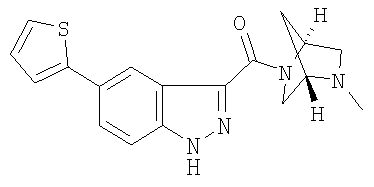
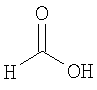
Соединение получали по методике В, выход 25%. МС-ЖХ (EI), в.у. 5,03 мин, m/z 339 (M++1).
1Н ЯМР (CD3OD): δ 8.48 (m, 2Н), 7,75 (m, 1H), 7,58 (m, 1H), 7,32 (m, 2H), 7,08 (m, 1H), 4,25 (m, 1H), 3,70 (m, 2H), 3,32 (m, 1H), 2,85 (d, 3H), 2.22 (m, 2H).
Пример 43
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]кабонил}-5-(4-метил-2-тиенил)-1Н-индазола
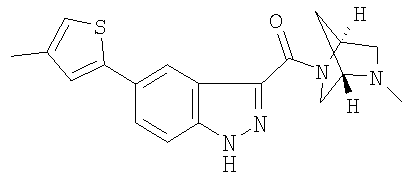
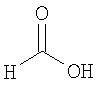
Соединение получали по методике В, выход 25%. МС-ЖХ (EI), в.у. 5,33 мин, m/z 353 (M++1).
Пример 44
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(5-метил-2-тиенил)-1Н-индазола
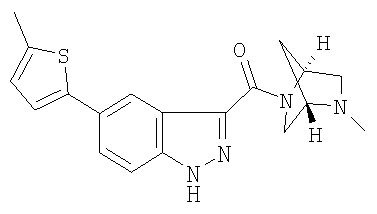
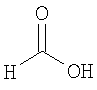
Соединение получали по методике В, выход 25%. МС-ЖХ (EI), в.у. 5,32 мин, m/z 353 (M++1).
Пример 45
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-фенил-1H-индазола
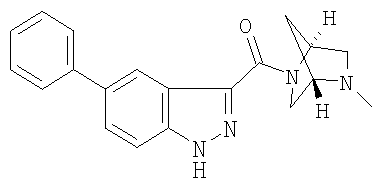
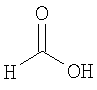
Соединение получали по методике В, выход 25%. МС-ЖХ (EI), в.у. 5,17 мин, m/z 333 (M++1).
Пример 46
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабидикло[2.2.1]гепт-2-ил]карбонил}-6-(2-тиенил)-1Н-индазола
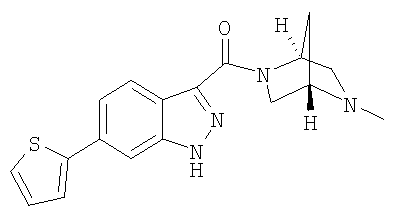
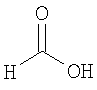
Соединение получали по методике В, выход 25%. МС-ЖХ (EI), в.у. 5,13 мин, m/z 339 (M++1).
Пример 47
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(3-тиенил)-1Н-индазола
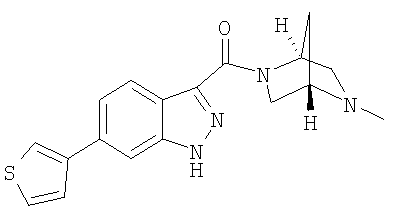
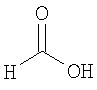
Соединение получали по методике В, выход 25%. МС-ЖХ (EI), в.у. 4,3 мин, m/z 339 (M++1).
Пример 48
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(4-метил-2-тиенил)-1Н-индазола
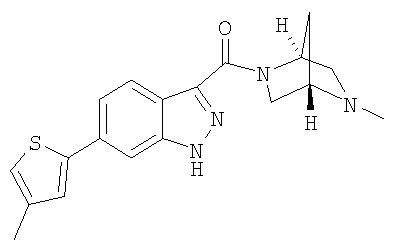
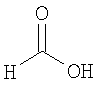
Соединение получали по методике В, выход 20%. МС-ЖХ (EI), в.у. 5,35 мин, m/z 353 (M++1).
Пример 49
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабипикло[2.2.1]гепт-2-ил]карбонил}-6-(5-метил-2-фурил)-1Н-индазола
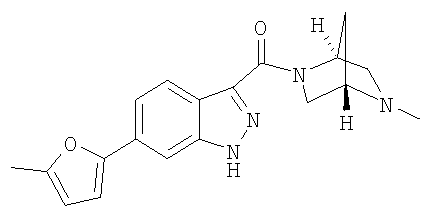
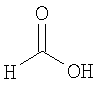
Соединение получали по методике В, выход 25%. МС-ЖХ (EI), в.у. 5,35 мин, m/z 337 (M++1).
Пример 50
Формиат 3-{[(1S,4S)-5-метил-2,5-дазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(5-метил-2-тиенил)-1Н-индазола
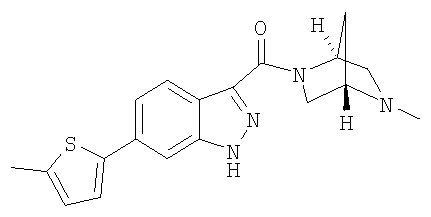
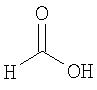
Соединение получали по методике В, выход 25%. МС-ЖХ (EI), в.у. 4,67 мин, m/z 353 (M++1).
Пример 51
Формиат 5-(2-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола
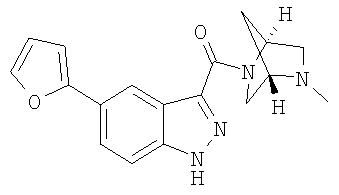
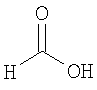
Соединение получали по методике В, выход 25%. МС-ЖХ (EI), в.у. 41 мин, m/z 323 (M++1).
Пример 52
Формиат 5-(3-фторфенил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола
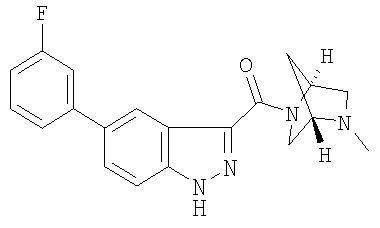
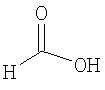
Соединение получали по методике В, выход 25%. МС-ЖХ (EI), в.у. 5,28 мин, m/z 351 (M++1).
Пример 53
Формиат 5-(4-фторфенил)-3-{[(1S,4S)-5-метил-2,5-диазабипикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола
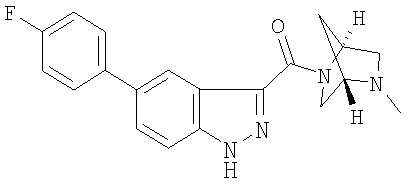
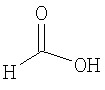
Соединение получали по методике В, выход 25%. МС-ЖХ (EI), в.у. 5,25 мин, m/z 351 (M++1).
Пример 54
Формиат 5-(4-метоксифенил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола
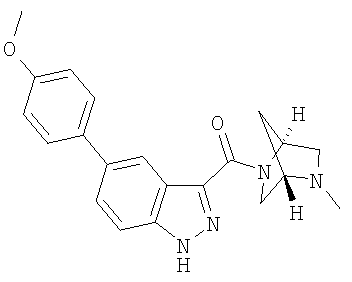
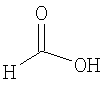
Соединение получали по методике В, выход 20%. МС-ЖХ (EI), в.у. 5,19 мин, m/z 363 (M++1).
Пример 55
Формиат 6-(2-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола
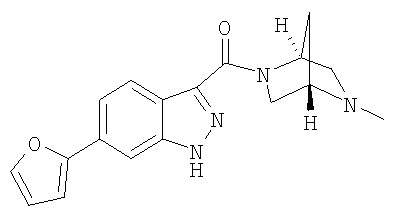
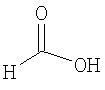
Соединение получали по методике В, выход 25%. МС-ЖХ (EI), в.у. 4,9 мин, m/z 323 (M++1).
Пример 56
Формиат 6-(3-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола
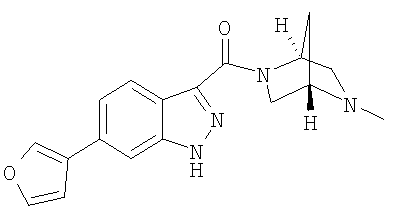
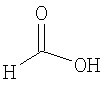
Соединение получали по методике В, выход 25%. МС-ЖХ (EI), в.у. 3,93 мин, m/z 323 (M++1).
Методика С
Восстановительная конденсация бициклокарбоксамидов и карбоксальдегидов с образованием производных третичных аминов
К суспензии гидрохлорида бициклокарбоксамида (0,4 ммоля), карбоксальдегида (1,0 ммоля), N,N-диизопропилэтиламина (1,2 ммоля) и уксусной кислоты (0,48 ммоля) добавляли триацетоксиборгидрид натрия (0,68 ммоля). Реакционную смесь выдерживали при температуре окружающей среды в течение 2 ч и выливали в воду, экстрагировали смесью дихлорметан/метанол, 95:5 (2×30 мл) и объединенные экстракты концентрировали. Остаток очищали препаративной ЖХВР (элюент: градиент в течение 8 мин вода (0,1% муравьиная кислота)/ацетонитрил (0,1% муравьиная кислота) от 95:5 до 20:80), при этом получали третичный амин.
В следующих примерах описано получение соединений по методике С:
Пример 57
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола
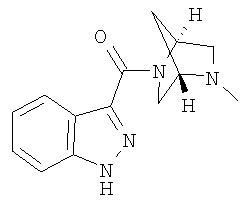
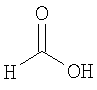
Соединение получали по методике С, выход 30%. МС-ЖХ (EI), в.у. 2,5 мин, m/z 257 (M++1).
1Н ЯМР (CD3OD): δ 8,42 (s, 1Н), 8,23 (m, 1H), 7,85 (m, 1H), 7,77 (m, 1H), 7,64 (m, 1H), 4,15 (m, 2H), 4,01 (m, 2H), 2,51 (d, 3H), 2,11 (m, 2H).
Пример 58
3-{[(1S,4S)-5-Этил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол
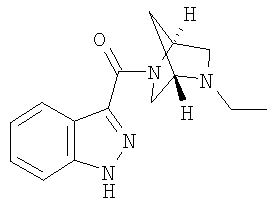
Соединение получали по методике С, выход 45%. МС-ЖХ (EI), в.у. 2,77 мин, m/z 271 (M++1).
Пример 59
N-(Циклопропилметил)-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-амин
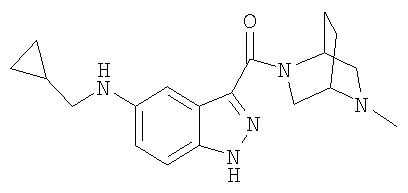
Соединение получали по методике С, выход 70%. МС-ЖХ (EI), в.у. 1,33 мин, m/z 340 (M++1).
Пример 60
N-(Циклопропилметил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-амин
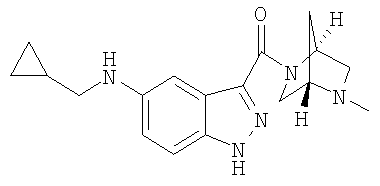
Соединение получали по методике С, выход 80%. МС-ЖХ (EI), в.у. 1,36 мин, m/z326 (M++1).
Пример 61
Формиат N,N-диметил-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-амина
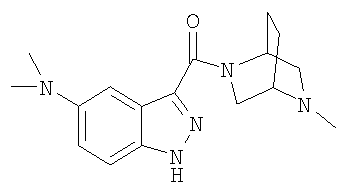
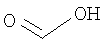
Соединение получали по методике С, выход 58%. МС-ЖХ (EI), в.у. 1,49 мин, m/z 314 (M++1).
Пример 62
Формиат N,N-диметил-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил1карбонил}-1Н-индазол-5-амина
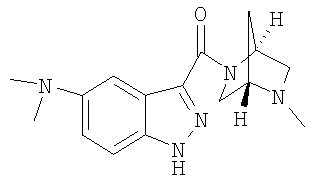
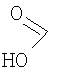
Соединение получали по методике С, выход 51%. МС-ЖХ (EI), в.у. 1,5 мин, m/z 300 (M++1).
Пример 63
Формиат N,N-диметил-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-6-амина
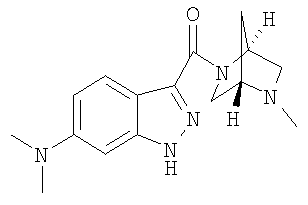
Соединение получали по методике С, выход 59%. МС-ЖХ (EI), в.у. 1,5 мин, m/z 300 (M++1).
Пример 64
5-Бром-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1H-индазол
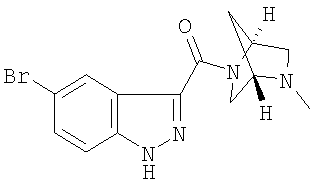
Соединение получали по методике С или А, выход 25%. МС-ЖХ (EI), в.у. 3,57 мин, m/z 335/337 (M++1).
Пример 65
Формиат 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(3-тиенил)-1Н-индазола
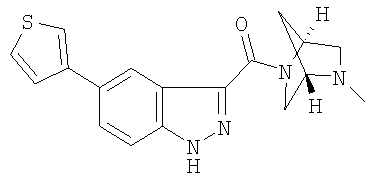
Соединение получали по методике С или В, выход 25%. МС-ЖХ (EI), в.у. 417 мин, m/z 339 (M++1).
Пример 66
Формиат 5-(3-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола
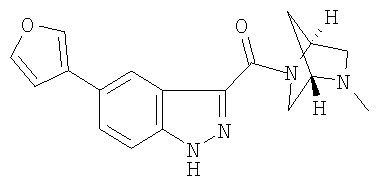
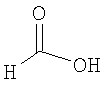
Соединение получали по методике С или В, выход 15%. МС-ЖХ (EI), в.у. 4,1 мин, m/z 323 (M++1).
Методика D
Деметилирование метоксизамещенных индазолбициклоамидов с образованием производных фенола и последующей реакцией фенола с различными алкилирующими агентами.
Метоксииндазолбициклоамид (6,98 ммоля) разбавляли дихлорметаном (60 мл) и дихлорэтаном (15 мл), раствор охлаждали до -78°С. В раствор по каплям в течение 30 мин добавляли 1,0М раствор трибромида бора в дихлорметане (35 ммолей). Реакционную смесь нагревали до комнатной температуры и выдерживали в течение 20 ч. К смеси добавляли еще одну аликвотную часть трибромида бора в дихлорметане (6 ммолей) и реакционную смесь выдерживали в течение еще 16 ч. Реакцию осторожно останавливали добавлением МеОН (30 мл) и концентрировали досуха. Остаток очищали хроматографией (элюент: дихлорметан/метанол, 90:10, затем смесь дихлорметан/метанол/гидроксид аммония, 10:10:1), при этом получали фенол (54%) в виде твердого вещества коричневого цвета. Фенол (0,734 ммоля) растворяли в N,N-диметилформамиде (10 мл) и обрабатывали карбонатом калия (1,46 ммоля) и бромистым алкилом (0,95 ммоля). Реакционную смесь выдерживали в течение 16 ч при температуре окружающей среды, фильтровали и концентрировали досуха. Остаток очищали препаративной ЖХВР (элюент: градиент в течение 8 мин вода (0,1% муравьиная кислота)/ацетонитрил (0,1% муравьиная кислота) от 95:5 до 20:80), при этом получали простой эфир.
В следующих примерах описано получение соединений по методике D:
Пример 67
5-Гидрокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол
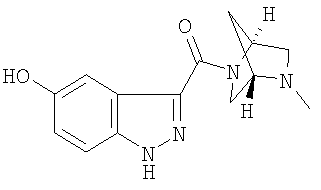
Соединение получали по методике D, выход 64%. МС-ЖХ (EI), в.у. 0,75 мин, m/z 273 (M++1).
1H ЯМР (Me2SO-d6): δ 10,76 (s, 1Н), 8,90 (s, 1H), 8,25 (m, 2Н), 7,99 (s, 1H), 7,85 (m, 1H), 4,46 (ушир., 1H), 3,62 (m, 1H), 3,38 (m, 1H), 3,20 (m, 3Н), 2,20 (m, 2Н), 1,85 (m, 2Н).
Пример 68
Формиат 5-(циклопентилокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонид}-1Н-индазола
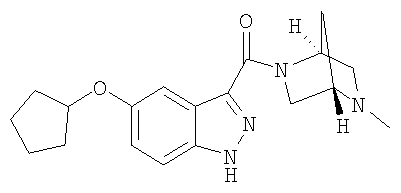

Соединение получали по методике D, выход 25%. МС-ЖХ (EI), в.у. 5,25 мин, m/z 341 (M++1).
1Н ЯМР (CD3OD) δ 8,48 (m, 2H), 7,75 (m, 1H), 7,58 (m, 1H), 7,32 (m, 2H), 7,08 (m, 1H), 4.25 (m. 1H), 3,70 (m, 2H), 3,32 (m, 1H), 2,85 (d, 3H), 2,22 (m, 2H).
Пример 69
Формиат 5-(циклопропилметокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло [2.2.1]гепт-2-ил]карбонил)-1Н-индазола
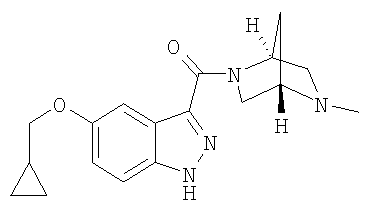
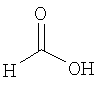
Соединение получали по методике D, выход 25%. МС-ЖХ (EI), в.у. 2,85 мин, m/z 327 (M++1).
Пример 70
Формиат 6-(циклопентилокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.11 гепт-2-ил]карбонил}-1Н-индазола
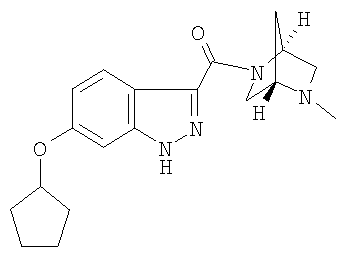
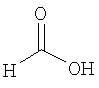
Соединение получали по методике D, выход 30%. МС-ЖХ (EI), в.у. 6,1 мин, m/z 341 (M++1).
Методика Е
Восстановление нитрозамещенных бициклоамидов с образованием производных анилина
В раствор нитрозамещенного бициклооснования (3,8 ммоля), полученого по методике А, в метаноле (100 мл) добавляли 10% палладий на угле (200 мг). Реакционную смесь помещали в атмосферу водорода (60 фунтов на кв. дюйм) и встряхивали в течение ночи. Катализатор удаляли фильтрованием через слой целита, который промывали метанолом (100 мл). Объединенные фильтраты концентрировали, при этом получали требуемый продукт.
В следующих примерах описано получение соединений по методике Е:
Пример 71
5-Амино-3-[(5-метил-2,5-диазабицкло[2.2.2]окт-2-ил)карбонил]-1Н-индазол
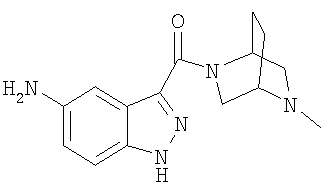
Соединение получали по методике Е, выход 92%. МС-ЖХ (EI), в.у. 1,71 мин, m/z 286 (M++1).
1Н ЯМР (CD3OD): δ 7,36 (d, J 12,0, 1H), 7,31 (s, 1H), 7,0 (d, J 12,0, 1H), 4,03 (m, 1H), 3,62 (m, 1H), 3,31 (s, 3H), 3,10 (m, 2H), 3,01 (m, 2H), 2,30-2,00 (m, 2H), 1,98-1,75 (m, 2H).
Пример 72
5-Амино-3-{[(1S,4S)-5-метил-2,5-диазабипикло[2.2.1]гепт-2-ил]карбонил}-6-(1,3-тиазол-2-ил)-1Н-индазол
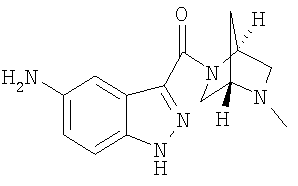
Соединение получали по методике Е, выход 74%. МС-ЖХ (EI), в.у. 1,76 мин, m/z 272 (M++1).
Методика F
Взаимодействие бициклоанилинов с хлорангидридами и ангидридами с образованием производных амида
В раствор анилина (0,460 ммоля) в пиридине (4 мл) добавляли карбонилхлорид (0,59 ммоля). Реакционную смесь выдерживали в течение 2 ч и концентрировали досуха. Полученный остаток очищали препаративной ЖХВР (элюент: градиент в течение 8 мин, вода (0,1% муравьиная кислота)/ацетонитрил (0,1% муравьиная кислота) от 95:5 до 20:80), при этом получали амид.
В следующих примерах описано получение соединений по методике F:
Пример 73
Формиат N-{3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил1-1Н-индазол-5-ил}циклопропанкарбоксамида
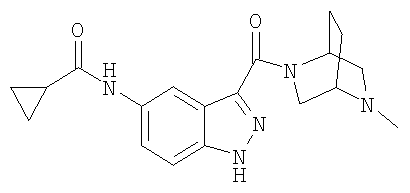
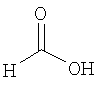
Соединение получали по методике F, выход 28%. МС-ЖХ (EI), в.у. 2,83 мин, m/z 354 (M++1).
1Н ЯМР (CD3OD): δ 8,53 (s, 1Н), 8,40 (s, 1H), 7,86 (s, 1H), 4.70 (m, 1H), 4,33 (m, 1H), 4,20 (m, 1H), 3.90 (m, 1H), 3,60-3,40 (m, 2H), 3,0 (s, 3H), 2,50-2,10 (m, 2H), 2.10-1,90 (m, 2H), 1,80 (m, 1H), 0,93 (m, 2H), 0,85 (m, 2H).
Пример 74
Формиат N-{1-(циклопропилкарбонил)-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-ил}циклопропанкарбоксамида
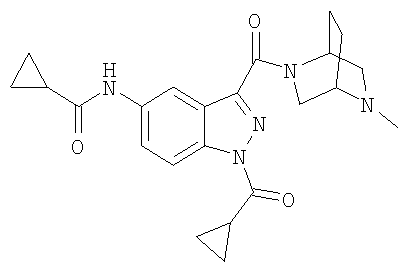
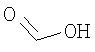
Соединение получали по методике F, выход 9,4%. МС-ЖХ (EI), в.у. 5,13 мин, m/z 422 (M++1).
Пример 75
Формиат N-(3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил)циклопропанкарбоксамида
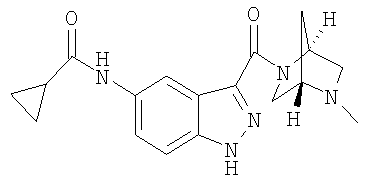
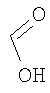
Соединение получали по методике F, выход 35%. МС-ЖХ (EI), в.у. 2,78 мин, m/z 340 (M++1).
Методика G
Реакции бициклоанилинов с изоцианатами с образованием производных мочевины
В раствор анилина (0,550 ммоля) в пиридине (4 мл) добавляли изоцианат (0,72 ммоля). Реакционную смесь выдерживали в течение 16 ч и концентрировали досуха. Остаток очищали препаративной ЖХВР (элюент: градиент в течение 8 мин, вода (0,1% муравьиная кислота)/ацетонитрил (0,1% муравьиная кислота) от 95:5 до 20:80), при этом получали мочевину.
В следующих примерах описано получение соединений по методике G:
Пример 76
Формиат N-(3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил1)-N'-пропилмочевины
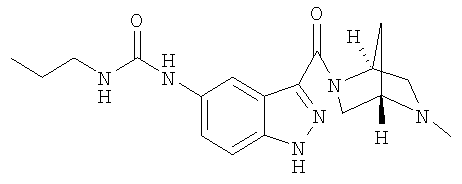
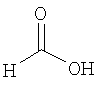
Соединение получали по методике G, выход 29%. МС-ЖХ (EI), в.у. 2,84 мин, m/z 357 (M++1).
1Н ЯМР (CD3OD): δ 8,42 (ушир., 1Н), 8,21-8,14 (m, 2H), 7,47 (m, 1H), 4,40-4,20 (m, 1H), 3,60 (m, 1H), 3,30 (s, 3H), 3,20 (m, 2H), 3,10 (t, J 6.0, 2H), 2,90 (m, 2H), 2.50-2,10 (m, 2H), 2,10-1,85 (m, 2H), 1,50 (q, J 6,0, 2H), 0,98 (t, J 6,0, 3H).
Пример 77
Формиат 3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-N-пропил-5-{[(пропиламино)карбонил]амино}-1Н-индазол-1-карбоксамида
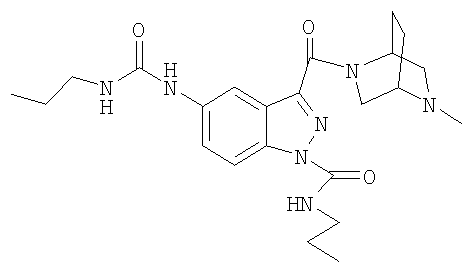
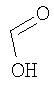
Соединение получали по методике G, выход 7,8%. МС-ЖХ (EI), в.у. 5,11 мин, m/z 456 (M++1).
Пример 78
Формиат N-(4-фторбензил)-N'-(3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил)мочевины
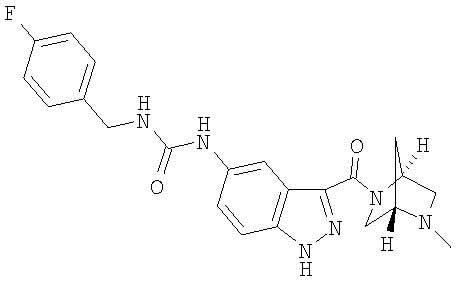
Соединение получали по методике G, выход 27%. МС-ЖХ (EI), в.у. 4,74 мин, m/z 423 (M++1).
Пример 79
Формиат N-(4-фторбензил)-5-({[(4-фторбензил)амино]карбонил}амино)-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-1-карбоксамида
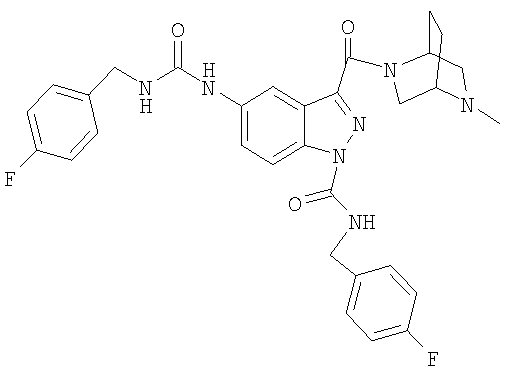
Соединение получали по методике G, выход 5,2%. МС-ЖХ (EI), в.у. 5,9 мин, m/z 5 88 (M++1).
Пример 80
Формиат N-циклопентил-N'-(3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1H-индазол-5-ил)мочевины
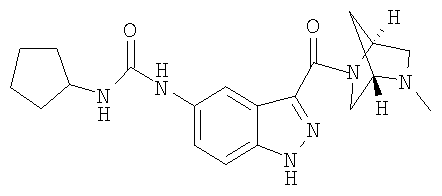
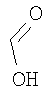
Соединение получали по методике G, выход 32%. МС-ЖХ (EI), в.у. 2,85 мин, m/z 383 (M++1).
Пример 81
Формиат N-циклопентил-5-{[(циклопентиламино)карбонил]амино}-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-1-карбоксамида
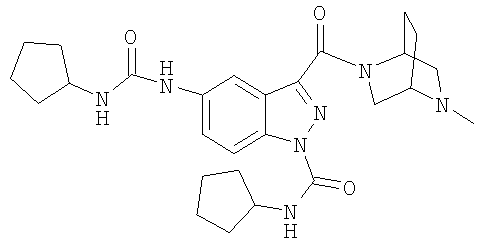
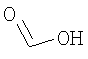
Соединение получали по методике G, выход 6,6%. МС-ЖХ (EI), в.у. 5,46 мин, m/z 508 (M++1).
Пример 82
Формиат N-(4-фторбензил)-N'-{3-[(5-метил-2,5-диазабицикло[2.2.21окт-2-ил)карбонил]-1Н-индазол-5-ил}мочевины
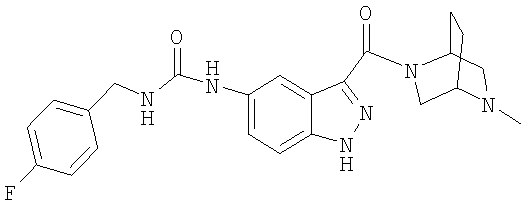
Соединение получали по методике G, выход 22%. МС-ЖХ (EI), в.у. 4,78 мин, m/z 437 (M++1).
Пример 83
Формиат N-{3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-ил}-N'-пропилмочевины
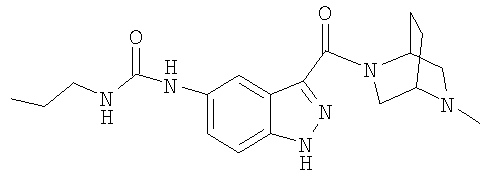
Соединение получали по методике G, выход 33%. МС-ЖХ (EI), в.у. 3,11 мин, m/z 372 (M++1).
Пример 84
Формиат N-циклопентил-N'-{3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-ил}мочевины
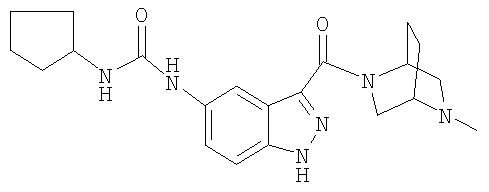
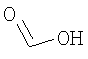
Соединение получали по методике G, выход 34%. МС-ЖХ (EI), в.у. 2,9 мин, m/z 397 (M++1).
Пример 85
Связывание [3Н] MLA
Материалы
Мозг крысы: фирмы Pel-Freez Biologicals, № по каталогу 56004-2
Таблетка смеси ингибиторов протеаз: фирмы Roche, № по каталогу 1697498
Получение мембранной фракции
Мозг крысы в 20 объемах (мас./об.) охлажденного льдом 0,32М раствора сахарозы, содержащего ингибиторы протеаз (1 таблетка на 50 мл), гомогенизировали в гомогенизаторе политрон в течение 10 с (скорость 11), затем центрифугировали в течение 10 мин при 1000 g при 4°С. Супернатант центрифугировали в течение 20 мин при 20000 g при 4°С. Осадок ресуспендировали в буферном растворе для связывания (200 мМ TRIS-HCl, 20 мМ HEPES, рН 7,5, 144 мМ NaCl, 1,5 мМ KCl, 1 мМ MgSO4, 2 мМ CaCl2, 0,1% (мас./об.) БСА) и хранили при -80°C.
Для определения насыщения 200 мкл смеси в буферном растворе для связывания, содержащем 200 мкг мембранного белка, от 0,2 до 44 нМ [3Н] MLA. Неспецифическое связывание определяли с использованием 1 мкМ MLA. Конкурнетный анализ проводили в присутствии 2 нМ [Н] MLA и исследуемых соединений в необходимом диапазоне концентраций. Исследуемую смесь выдерживали при 22°С в течение 2 ч, затем осадок собирали в приборе для сбора клеток Tomtec на фильтре GF/B, предварительно пропитанном 0,3% ПЭИ в буферном растворе для связывания. Фильтр промывали 3 раза буферным раствором для связывания и радиоактивность определяли с использованием Trilux.
Сродство к связыванию для предпочтительных соединений по настоящему изобретению составляет от 26 мкМ до 64 нМ, прежде всего от 2,5 мкМ до 64 нМ.
Условия синтеза, описанные выше в примерах, можно изменить при замене общих или конкретных реагентов и/или условий реакций по настоящему изобретению на аналогичные реагенты или условия.
Несмотря на то, что настоящее изобретение иллюстрируется на примерах получения конкретных соединений, следует понимать, что возможны изменения и модификации изобретения, не выходя за пределы объема или сущности изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНДАЗОЛЫ, БЕНЗОТИАЗОЛЫ, БЕНЗОИЗОТИАЗОЛЫ, БЕНЗОИЗОКСАЗОЛЫ, ПИРАЗОЛОПИРИДИНЫ, ИЗОТИАЗОЛОПИРИДИНЫ, ИХ ПОЛУЧЕНИЕ И ИХ ПРИМЕНЕНИЕ | 2006 |
|
RU2450003C2 |
| ПРОИЗВОДНЫЕ БИЦИКЛО[2,2,1]ГЕПТ-7-ИЛАМИНА И ИХ ПРИМЕНЕНИЯ | 2006 |
|
RU2442771C2 |
| ЛИГАНДЫ НИКОТИНОВОГО РЕЦЕПТОРА АЛЬФА-7, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2005 |
|
RU2418797C2 |
| 3-КАРБОКСАЛЬДЕГИДНЫЕ ПРОИЗВОДНЫЕ ХИНОЛИНА | 1995 |
|
RU2097379C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ ЦИКЛОПЕНТАНА | 2010 |
|
RU2572555C2 |
| 2-ОКСА-5-АЗАБИЦИКЛО[2.2.1]ГЕПТАН-3-ИЛЬНЫЕ ПРОИЗВОДНЫЕ | 2015 |
|
RU2697651C2 |
| КОНДЕНСИРОВАННОЕ ХИНОЛИНОВОЕ ПРОИЗВОДНОЕ И ЕГО ПРИМЕНЕНИЕ | 2005 |
|
RU2384571C2 |
| Способ получения замещенных диазабициклоалкилхинолон карбоновых кислот с мостиковой связью или их фармацевтически приемлемых аддитивных солей | 1986 |
|
SU1482531A3 |
| ЗАМЕЩЕННЫЕ ДИАМИНОКАРБОКСАМИДНЫЕ И ДИАМИНОКАРБОНИТРИЛЬНЫЕ ПРОИЗВОДНЫЕ ПИРИМИДИНОВ, ИХ КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ С ИХ ПОМОЩЬЮ | 2012 |
|
RU2625309C2 |
| ПРОИЗВОДНЫЕ 3-АМИНОПИРРОЛИДИНА В КАЧЕСТВЕ МОДУЛЯТОРОВ РЕЦЕПТОРОВ ХЕМОКИНОВ | 2003 |
|
RU2355679C2 |
Настоящее изобретение относится к новым соединениям формул (I) и (III), в которых радикалы и символы имеют значения, определенные в формуле изобретения, например к 1H-индазолам, 1,2-бензизоксазолам и 1,2-бензизотиазолам, Данные соединения являются лигандами рецепторов подтипа α-7 nAChR. Изобретение также относится к фармацевтической композиции, включающей указанные соединения, и к применению указанных соединений для получения лекарственных средств для лечения заболеваний, связанных с недостаточностью функции никотиновых рецепторов ацетилхолина или с их аномальной функцией, прежде всего в ткани мозга. 21 н. и 25 з.п. ф-лы.
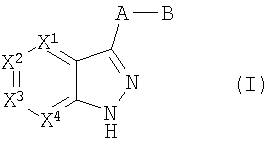
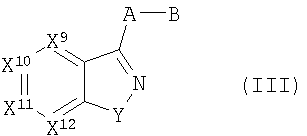
1. Соединение формул I или III:


где А означает
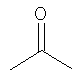 ,
,
В означает
 ;
;
Y означает О или S;
Х1-Х4 каждый независимо означает СН или CR1,
Х9-Х12 каждый независимо означает СН или CR3,
R1 и R3 каждый независимо означает Н,
C1-С6алкил, который незамещен или замещен одной или более группами:
F, Cl, Br или I,
С3-С6циклоалкил, галоген,
NR4R5, NR4CO2R5, NR4CONR4R5,
Ar,
Het или
R6O-;
R4 и R5 каждый независимо означает Н или означает фенил, фенил-С1-С4алкил,
С1-С4алкил, С3-С8циклоалкил, или С4-С8циклоалкилалкил, каждый из которых незамещен
или замещен одной или более группами: F, Cl, Br или I,
R6 означает
Н,
С1-С6алкил, который незамещен или замещен одной или более группами:
F, Cl, Br или I,
С3-С8циклоалкил, или
С4-С8циклоалкилалкил,
R7 означает Н или
С1-С4алкил,
m равно 1 или 2;
Ar означает фенильную группу, которая незамещена или замещена одной или более группами, выбранными из алкокси, содержащей от 1 до 8 атомов углерода, и галогена, или комбинации указанных групп, и
Het означает гетероциклическую группу, полностью насыщенную, частично насыщенную или полностью ненасыщенную, содержащую 5-6 атомов в цикле, в котором 1 или 2 атома в составе цикла каждый является атомом N, О или S, который является незамещенным или замещенным одной или более алкильными группами, содержащими от 1 до 8 атомов углерода, или фармацевтически приемлемая соль указанных соединений, причем, если соединение проявляет хиральность, оно может быть в форме смеси энантиомеров или смеси диастереомеров, или может быть в форме отдельного энантиомера или отдельного диастереомера.
2. Соединение по п.1, в котором R1 и R3 представляют собой NR4R5, a R4 и R5 каждый независимо означает Н, фенил или С1-С4алкил, который является незамещенным или замещенным одной или более группами F, Cl, Br или I.
3. Соединение по п.1, которое характеризуется формулой I.
4. Соединение по п.3, в котором R1 означает Н, OR, CF3, Br, незамещенный или замещенный С1-С8алкилом тиенил, незамещенный или замещенный С1-С8алкилом фурил или незамещенный или замещенный C1-С8алкоксигруппой и/или галогеном фенил.
5. Соединение по п.3, в котором R1 означает Н, OR6, NR4R5, NR4COR5, NR4CONR4R5, CF3, Br, 2-тиенил, 3-тиенил, метилтиенил, 2-фурил, 3-фурил, фенил, фторфенил, метоксифенил, тиазолил, оксазолил, тетрагидропиранил или дигидропиранил.
6. Соединение по п.1, которое характеризуется формулой III.
7. Соединение по п.1, в котором R3 означает Н, циклопропил или OR6.
8. Соединение по п.1, в котором R4 означает Н или метил.
9. Соединение по п.1, в котором R5 означает Н, метил, циклопропил, циклопентил, циклопропилметил, пропил или бензил.
10. Соединение по п.1, в котором R6 означает метил, этил, CF3, CHF2, циклопентил или циклопропилметил.
11. Соединение по п.1, в котором R7 означает Н, метил или этил.
12. Соединение по п.1, в котором m равно 1.
13. Соединение по п.1, в котором m равно 2.
14. Соединение по п.9, в котором Y означает S.
15. Соединение по п.1, в котором Het означает незамещенный или замещенный C1-С8алкилом тиенил или незамещенный или замещенный C1-С8алкилом фурил.
16. Соединение по п.1, причем упомянутое соединение выбирают из следующих соединений:
3-[(1S,4S)-2,5-диазабицикло[2.2.1]гепт-2-илкарбонил]-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(трифторметокси)-1H-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(трифторметил)-1H-индазола,
5-бром-3-[(1S,4S)-2,5-диазабицикло[2.2.1]гепт-2-илкарбонил]-1Н-индазола,
5-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
6-бром-3-[(1S,4S)-2,5-диазабицикло[2.2.1]гепт-2-илкарбонил]-1Н-индазола,
6-этокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола,
6-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола,
7-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(2-тиенил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(4-метил-2-тиенил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(5-метил-2-тиенил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-фенил-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(2-тиенил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(3-тиенил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(4-метил-2-тиенил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(5-метил-2-фурил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(5-метил-2-тиенил)-1Н-индазола,
5-(2-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-(3-фторфенил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-(4-фторфенил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-(4-метоксифенил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
6-(2-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
6-(3-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
3-{[(1S,4S)-5-этил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(3-тиенил)-1Н-индазола,
5-(3-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-бром-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола и их фармацевтически приемлемых солей, причем соединение может быть в форме смеси энантиомеров или смеси диастереомеров, или может быть в форме отдельного энантиомера или отдельного диастереомера.
17. Соединение по п.16, которое представляет собой гидрохлоридную или формиатную соль.
18. Соединение по п.16 или 17, причем упомянутое соединение выбирают из следующих соединений:
гидрохлорида 3-[(1S,4S)-2,5-диазабицикло[2.2.1]гепт-2-илкарбонил]-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(трифторметокси)-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(трифторметил)-1Н-индазола,
гидрохлорида 5-бром-3-[(1S,4S)-2,5-диазабицикло[2.2.1]гепт-2-илкарбонил]-1Н-индазола,
формиата 5-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
гидрохлорида 6-бром-3-[(1S,4S)-2,5-диазабицикло[2.2.1]гепт-2-илкарбонил]-1Н-индазола,
формиата 6-этокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола,
формиата 6-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола,
формиата 7-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(2-тиенил)-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2,2.1]гепт-2-ил]карбонил}-5-(4-метил-2-тиенил)-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(5-метил-2-тиенил)-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-фенил-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(2-тиенил)-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабипикло[2.2.1]гепт-2-ил]карбонил}-6-(3-тиенил)-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(4-метил-2-тиенил)-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(5-метил-2-фурил)-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(5-метил-2-тиенил)-1Н-индазола,
формиата 5-(2-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата 5-(3-фторфенил)-3-{[(1S,4S)-5-метил-2,5-иазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата 5-(4-фторфенил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло [2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата 5-(4-метоксифенил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата 6-(2-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата 6-(3-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата 3-{[(1S,4S)-5-этил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(3-тиенил)-1Н-индазола,
формиата 5-(3-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-бром-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
причем соединение может быть в форме смеси энантиомеров или смеси диастереомеров, или может быть в форме отдельного энантиомера или отдельного диастереомера.
19. Соединение по п.1, причем упомянутое соединение выбирают из следующих соединений:
3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-6-(1,3-тиазол-2-ил)-1Н-индазола,
3-[(1S,4S)-(2,5-диазабицикло[2.2.1]гепт-2-илкарбонил]-1Н-индазола,
3-(2,5-диазабицикло [2.2.2]окт-2-илкарбонил)-1Н-индазола,
3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазола,
3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-6-(1,3-тиазол-2-ил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(1,3-тиазол-2-ил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(2-тиенил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(3-тиенил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(4-метил-2-тиенил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(5-метил-2-тиенил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(трифторметокси)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-фенил-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(1,3-оксазол-2-ил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(1,3-тиазол-2-ил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(2-тиенил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(3-тиенил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(4-метил-1,3-тиазол-2-ил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(4-метил-2-тиенил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(5-метил-1,3-тиазол-2-ил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(5-метил-2-фурил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(5-метил-2-тиенил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(тетрагидро-2Н-пиран-4-ил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(трифторметокси)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(трифторметил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-7-(трифторметокси)-1Н-индазола,
5-(2-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-(3-фторфенил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-(3-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-(4-фторфенил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-(4-метоксифенил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-(циклопентилокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-(циклопропилметокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-амино-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазола,
5-амино-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(1,3-тиазол-2-ил)-1Н-индазола,
5-бром-3-{[(1S,4S)-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-гидрокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-метокси-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазола,
3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-5-метокси-1Н-индазола,
5-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
6-(2-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
6-(3,6-дигидро-2Н-пиран-4-ил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло [2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
6-(3-фурил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
6-(циклопентилокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
6-циклопропил-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола,
6-этокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола,
3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-6-метокси-1Н-индазола,
6-метокси-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазола,
6-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
7-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола,
N-(3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил)-N'-пропилмочевины,
N-{3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-ил}циклопропанкарбоксамида,
N-{3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-ил}-N'-пропилмочевины,
и их фармацевтически приемлемых солей,
причем соединение может быть в форме смеси энантиомеров или смеси диастереомеров, или может быть в форме отдельного энантиомера или отдельного диастереомера.
20. Соединение по п.19, которое представляет собой гидрохлоридную или формиатную соль.
21. Соединение по п.20, причем упомянутое соединение выбирают из следующих соединений:
гидрохлорида 3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-6-(1,3-тиазол-2-ил)-1Н-индазола,
гидрохлорида 3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-1Н-индазола,
формиата 3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазола,
формиата 3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-6-(1,3-тиазол-2-ил)-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(1,3-тиазол-2-ил)-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил)-6-(1,3-оксазол-2-ил)-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(1,3-тиазол-2-ил)-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(4-метил-1,3-тиазол-2-ил)-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(5-метил-1,3-тиазол-2-ил)-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(тетрагидро-2Н-пиран-4-ил)-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-6-(трифторметокси)-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-7-(трифторметокси)-1Н-индазола,
формиата 5-(циклопентилокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата 5-(циклопропилметокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата 5-метокси-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазола,
гидрохлорида 3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-5-метокси-1Н-индазола,
формиата 5-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата 6-(3,6-дигидро-2Н-пиран-4-ил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло [2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата 6-(циклопентилокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло [2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата 6-циклопропил-3-{[(1S,4S)-5-метил-2,5-диазабицикло [2.2.1]гепт-2-ил]карбонил}-1,2-бензизотиазола,
гидрохлорида 3-(2,5-диазабицикло[2.2.2]окт-2-илкарбонил)-6-метокси-1Н-индазола,
формиата 6-метокси-3-[(5-метил-2,5-диазабицикло [2.2.2]окт-2-ил)карбонил]-1H-индазола,
гидрохлорида 6-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата 6-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата N-(3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил)-N'-пропилмочевины,
формиата N-{3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-ил}циклопропанкарбоксамида,
причем соединение может быть в форме смеси энантиомеров или смеси диастереомеров, или может быть в форме отдельного энантиомера или отдельного диастереомера.
22. Соединение по п.1, причем упомянутое соединение выбирают из следующих соединений:
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизоксазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(4-метил-1,3-тиазол-2-ил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(5-метил-1,3-тиазол-2-ил)-1Н-индазола,
3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(тетрагидро-2Н-пиран-4-ил)-1Н-индазола,
5-(3,6-дигидро-2Н-пиран-4-ил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
5-(дифторметокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
6-(дифторметокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
7-фтор-6-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
N-(3-([(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил)циклопропанкарбоксамида,
N-(4-фторбензил)-N'-(3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил)мочевины,
N-(4-фторбензил)-N'-{3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-ил}мочевины,
N-(циклопропилметил)-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-амина,
N-(циклопропилметил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-амина,
N,N-диметил-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-амина,
N,N-диметил-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2,2.1]гепт-2-ил]карбонил}-1Н-индазол-5-амина,
N,N-диметил-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-6-амина,
N-циклопентил-N'-(3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил)мочевины,
N-циклопентил-N'-{3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-ил}мочевины,
и их фармацевтически приемлемых солей,
причем соединение может быть в форме смеси энантиомеров или смеси диастереомеров, или может быть в форме отдельного энантиомера или отдельного диастереомера.
23. Соединение по п.22, которое представляет собой гидрохлоридную или формиатную соль.
24. Соединение по п.23, причем упомянутое соединение выбирают из следующих соединений:
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1,2-бензизоксазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(4-метил-1,3-тиазол-2-ил)-1H-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(5-метил-1,3-тиазол-2-ил)-1Н-индазола,
формиата 3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-5-(тетрагидро-2Н-пиран-4-ил)-1Н-индазола,
формиата 5-(3,6-дигидро-2Н-пиран-4-ил)-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата 5-(дифторметокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло [2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата 6-(дифторметокси)-3-{[(1S,4S)-5-метил-2,5-диазабицикло [2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата 7-фтор-6-метокси-3-{[(1S,4S)-5-метил-2,5-диазабицикло [2.2.1]гепт-2-ил]карбонил}-1Н-индазола,
формиата N-(3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил)циклопропанкарбоксамида,
формиата N-(4-фторбензил)-N'-(3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил)мочевины,
формиата N-(4-фторбензил)-N'-{3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-ил}мочевины,
формиата N,N-диметил-3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-амина,
формиата N,N-диметил-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-амина,
формиата N,N-диметил-3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-6-амина,
формиата N-циклопентил-N'-(3-{[(1S,4S)-5-метил-2,5-диазабицикло[2.2.1]гепт-2-ил]карбонил}-1Н-индазол-5-ил)мочевины,
формиата N-циклопентил-N'-{3-[(5-метил-2,5-диазабицикло[2.2.2]окт-2-ил)карбонил]-1Н-индазол-5-ил}мочевины,
причем соединение может быть в форме смеси энантиомеров или смеси диастереомеров, или может быть в форме отдельного энантиомера или отдельного диастереомера.
25. Фармацевтическая композиция для активирования/стимулирования никотинового рецептора α-7 у пациента, включающая соединение по любому из пп.1-24 и фармацевтически приемлемый носитель.
26. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для селективного активирования/стимуляции никотиновых рецепторов α-7 у млекопитающего, причем такая активация/стимуляция проявляет лечебное действие.
27. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для лечения пациента, страдающего от психотического заболевания, нейродегенеративного заболевания, включая дисфункцию холинергической системы, и/или состояния, связанного с нарушениями памяти и/или познавательной способности.
28. Применение по п.27, в котором упомянутый пациент страдает от следующих заболеваний: шизофрения, тревожное состояние, мания, депрессия, маниакальная депрессия, болезнь Туретта, болезнь Паркинсона, болезнь Гентингтона, болезнь Альцгеймера, деменция с тельцами Леви, боковой амиотрофический склероз, нарушение памяти, потеря памяти, недостаточность познавательной способности, недостаточность внимания, гиперактивное состояние недостаточности внимания.
29. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для лечения пациента, страдающего от деменции и/или другого состояния, связанного с потерей памяти.
30. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для лечения пациента, страдающего от нарушения памяти в связи с возрастным нарушением познавательной способности средней степени, болезни Альцгеймера, шизофрении, болезни Паркинсона, болезни Гентингтона, болезни Пика, болезни Крейтцфельда-Якоба, депрессии, старения, травм головы, инсульта, гипоксии ЦНС, мозгового слабоумия, мультиинфарктной деменции, ВИЧ и сердечно-сосудистых заболеваний.
31. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для лечения и/или профилактики деменции у пациентов, страдающих болезнью Альцгеймера, посредством ингибирования связывания амилоидного бета-пептида с рецепторами nAChR.
32. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для лечения пациента с синдромами отказа от алкоголя или от отравления.
33. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для лечения пациента для обеспечения нейрозащиты от повреждений, вызванных инсультами, ишемией и глутамат-индуцированной экситотоксичностью.
34. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для лечения пациента, страдающего от никотиновой зависимости, боли, для лечения расстройства биоритмов в связи с перелетом через несколько часовых поясов, ожирения и/или диабета.
35. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для облегчения отказа от курения у пациента.
36. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для лечения пациента, страдающего от нарушения познавательной способности средней степени (MCI), сосудистой деменции (VaD), ухудшения познавательной способности, связанного с возрастом (AACD), амнезии, вызванной операциями на открытом сердце, остановкой сердца, и/или после общего наркоза, недостаточности памяти, вызванной действием введенных анестетиков, ухудшения познавательной способности, вызванного недостатком сна, синдрома хронической усталости, нарколепсии, деменции, вызванной СПИД, ухудшения познавательной способности, вызванного эпилепсией, синдрома Дауна, деменции, вызванной алкоголизмом, ухудшения памяти, вызванного приемом лекарственных средств/реагентов, деменции легионеров (синдром боксеров) и деменции у животных.
37. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для лечения потери памяти.
38. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для лечения пациента, страдающего от нарушения памяти.
39. Применение по п.38, в котором упомянутое нарушение памяти связано со сниженной активностью никотинового рецептора ацетилхолина.
40. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для лечения или профилактики заболевания или состояния, возникшего в результате дисфункции трансмиссии никотиновых рецепторов ацетилхолина у млекопитающих.
41. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для лечения или профилактики заболевания или состояния, возникшего в результате нарушения или недостаточности функции никотиновых рецепторов ацетилхолина у млекопитающих.
42. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для лечения или профилактики заболевания или состояния, возникшего в результате подавления функции трансмиссии никотиновых рецепторов ацетилхолина у млекопитающих.
43. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для лечения или профилактики заболевания или состояния, возникшего в результате потери холинергических синапсов у млекопитающих.
44. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для лечения защиты нейронов у млекопитающих от нейротоксического действия, вызванного активацией рецепторов α7nACh.
45. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для лечения или профилактики нейродегенеративного нарушения при ингибировании связывания пептидов Аβ с рецепторами α7nACh у млекопитающих.
46. Применение соединения по любому из пп.1-24 для приготовления лекарственного средства для лечения пациента, страдающего от воспалительного заболевания.
| ЕР 122119622 А2, 03.07.2002 | |||
| ГЕТЕРОЦИКЛО-ЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ АМИНОВ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ИНГИБИРОВАНИЯ ХОЛИНЭСТЕРАЗЫ, СПОСОБ ПОЛУЧЕНИЯ СОЕДИНЕНИЙ | 1992 |
|
RU2119920C1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2010-05-20—Публикация
2004-12-22—Подача