Изобретение относится к высокомолекулярным соединениям медицинского назначения, а именно к водорастворимым полимерным комплексам, содержащим лекарственное средство арбидол, общей формулы
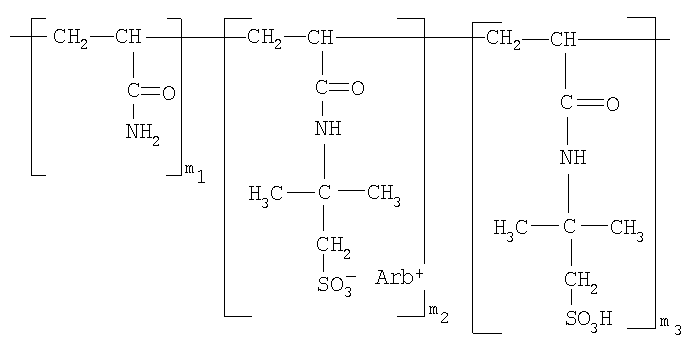
где Arb - арбидол: этиловый эфир 6-бром-4-диметил-аминометил-1-метил-5-окси-2-фенилтиометилиндолинил-3-карбоновой кислоты гидрохлорид моногидрат;
m1=100-(m2+m3), мол.%;
m2=(7,6-9,8) мол.%;
m3=(11,5-13,6) мол.%
с М.М. (19.000-31.000) Da.
Содержание Arb 26,4-32,1 мас.%.
В результате комплексообразования арбидола с полимерами, имеющими молекулярную массу 19.000-31.000 Da и состоящими из сополимеров акриламида (АА) и 2-акриламидо-2-метилпропансульфокислоты (ААМПСК), получен ряд водорастворимых производных арбидола, обладающих пониженной токсичностью по сравнению с арбидолом, повышенной биодоступностью, улучшенной фармакодинамикой, причем эти полимерные комплексы полностью сохраняют высокий уровень биологической активности арбидола, в частности противовирусной активности. Содержание арбидола в полученных водорастворимых полимерных комплексах составляет 26,4-32,1 мас.%.
Созданные водорастворимые полимерные комплексы арбидола могут найти применение в фармакологии, так как могут служить основой новых эффективных и безопасных противовирусных лекарственных средств и их лекарственных форм.
Необходимость иметь в арсенале лекарственных средств высокоэффективные противовирусные препараты широкого спектра действия в отношении вирусов гриппа А и В и других острых респираторных вирусных инфекций (ОРВИ) приводит к модификации формул найденных средств.
1. Причиной модификаций является высокая токсичность многих используемых препаратов или их недостаточная растворимость.
Широко используемыми этиотропными противовирусными препаратами являются ремантадин, ингибиторы нейраминидазы - занамивир и озельтамивир, рибавирин. Использование ремантадина ограничено отсутствием у него активности в отношении вирусов гриппа В, а также широким распространением в последние годы резистентных к нему штаммов вируса гриппа [CDC Health Alert. CCID.: www.cdc.gov/flu/han011406]. Относительно ингибиторов нейраминидазы можно отметить, что наряду с высокой стоимостью этих препаратов к их недостаткам относятся побочные эффекты в виде раздражения носоглотки при приеме занамивира и в виде тошноты и рвоты при приеме озельтамивира. Кроме того, они эффективны только в самом начале вирусной инфекции. Нередко при лечении тяжелых форм ОРВИ применяются также рибавирин и его отечественный аналог рибамидил. Из-за высокой токсичности эти препараты применяются только в условиях стационара у лиц с ослабленным иммунитетом [Киселев О.И., Деева Э.Г., Платонов В.Г., Ильенко В.И. Противовирусные препараты // «Грипп и другие ОРВИ». - СПб. - 2003. - С.96-146].
2. Одним из эффективных и технологичных способов снижения токсичности лекарственных веществ при сохранении специфической биологической активности является их комплексообразование с водорастворимыми нетоксичными ионогенными полимерами-носителями [Еропкин М.Ю., Соловский М.В., Еропкина Е.М., Шульцева Е.Л. Сравнительное исследование цитотоксического действия полимерных производных антибиотиков-аминогликозидов // Токсикол. вестник. - 2006. - №5. - С.18-22]. Полимерные препараты ремантадина (его комплекс с альгинатом натрия - альгирем и комплекс с сополимером N-винилсукцинимида с виниламидоянтарной кислотой - полирем) обладают более широким спектром противовирусного действия по сравнению с ремантадином. Немаловажным фактором является и пролонгированный эффект полимерных производных ремантадина, способствующий длительной циркуляции противовирусного компонента в эффективных терапевтических дозах [Киселев О.И., Деева Э.Г., Слита А.В., Платонов В.Г. Антивирусные препараты для лечения гриппа и ОРЗ. Дизайн препаратов на основе полимерных носителей. «Время». СПб., 2000].
3. Известен и широко применяется в качестве противовирусного средства препарат арбидол - этиловый эфир 6-бром-4-диметиламинометил-1-метил-5-окси-2-фенилтиометилиндолинил-3-карбоновой кислоты гидрохлорид моногидрат, который обладает широким спектром действия в отношении вирусов гриппа А и В и других острых респираторных вирусных инфекций (ОРВИ)
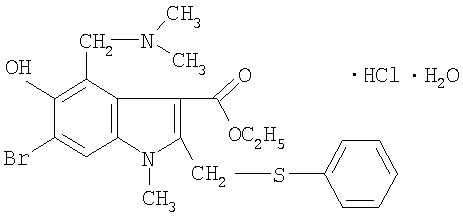
Арбидол, кроме противовирусного действия, является иммуномодулятором, индуктором интерферона и обладает антиоксидантными свойствами [Гуськова Т.А., Глушков Р.Г. Арбидол - иммуномодулятор, индуктор интерферона, антиоксидант. ЦХЛС-ВНИХФИ, М., 1999, 2001]. Вирусингибирующее действие арбидола определяется его способностью ингибировать слияние липидной оболочки вируса с мембранами эндосом, происходящее внутри клеток. Показано, что арбидол не оказывает воздействия на адсорбцию, транскрипцию и трансляцию, а также нейраминидазную активность вируса гриппа [Ленева И.А. Механизм вирусспецифического действия препарата арбидол. Автореферат докт. дисс., СПб., 2005]. В настоящее время арбидол широко распространен на отечественном фармацевтическом рынке и является одним из основных этиотропных противогриппозных препаратов.
В то же время существенный недостаток препарата состоит в том, что он практически нерастворим в воде, что уменьшает его биодоступность и ограничивает возможность создания новых лекарственных форм на его основе (растворы, аэрозоли, мази на гидрофильной основе). Кроме того, арбидол как лечебный препарат эффективен только в ранние сроки заболевания гриппом - не более 2-х суток от начала заболевания [Ленева И.А., Гуськова Т.А., Глушков Р.Г. Лекарственные средства для химиотерапии и химиопрофилактики гриппа: особенности механизма действия, эффективность и безопасность // Хим. - фарм. журнал. - 2004. - №11. - С.8-14].
При внутрижелудочном применении арбидол относится к малотоксичным препаратам [Гуськова ТА., Глушков Р.Г. Арбидол - иммуномодулятор, индуктор интерферона, антиоксидант. ЦХЛС-ВНИХФИ, М., 1999, 2001], однако при парентеральном введении на мышах и крысах его DL50 составляет 109 и 140 мг/кг соответственно, что позволяет его отнести к умеренно токсичным препаратам [Березовская И.В. Классификация химических веществ по параметрам острой токсичности при парентеральных способах введения // Хим.-фарм. ж. - 2003. - Т. 37, №3. - С.32-34]. При оценке на клеточных культурах его IC50 (среднеингибиторная концентрация, снижающая на 50% жизнеспособность клеток) составляет 40-60 мкг/мл [Ленева И.А. Механизм вирусспецифического действия препарата арбидол. Дисс. докт. биол. наук, СПб., 2005]. Кроме того, по нашим данным, при хранении препарата в течение около 6 месяцев его цитотоксичность существенно повышается (IC50 снижается до 20 мкг/мл на культуре клеток MDCK). При этом фармакологический индекс, или индекс селективности (отношение между цитотоксической концентрацией и средней вирусингибирующей концентрацией) составляет только 3,75, что является неприемлемым показателем для такого широко используемого препарата (как правило, индекс селективности по меньшей мере должен быть больше 10) [Хабриев Р.У. (ред.). Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. - М., 2005].
4. Технической задачей и положительным результатом изобретения является создание водорастворимых производных арбидола с пониженной токсичностью при сохранении широкого спектра и высокого уровня биологической активности, в частности противовирусной активности.
Указанная задача достигается за счет комплексообразования арбидола с сополимерами акриламида (АА) с 2-акриламидо-2-метилпропансульфокислотой (ААМПСК), в результате чего получают полимерный комплекс
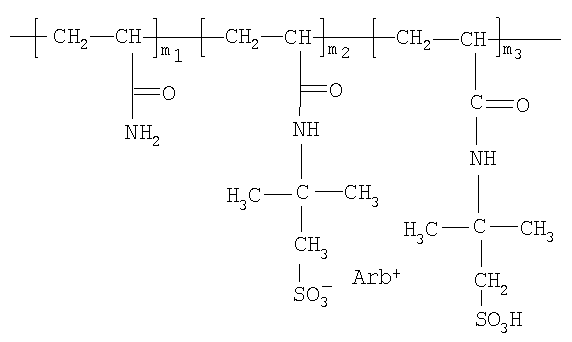
где Arb - арбидол: этиловый эфир 6-бром-4-диметил-аминометил-1-метил-5-окси-2-фенилтиометилиндолинил-3-карбоновой кислоты гидрохлорид моногидрат;
m1=100-(m2+m3), мол.%;
m2=(7,6-9,8) мол.%;
m3=(11,5-13,6) мол.%
с М.М. (19.000-31.000) Da, причем содержание в нем арбидола (26,4-32,1) мас.%.
5. Сущностью изобретения является использование для комплексообразования арбидола сополимеров АА с ААМПСК, в результате чего при строго подобранных пропорциях арбидола и сополимеров получены водорастворимые полимерные комплексы с содержанием в них арбидола от 26,4 до 32,1 мас.%, причем гидрохлорид и моногидрат в составе арбидола входят в структуру звена m2. Содержание звеньев в полимерной цепи в молярных % составляет: m1(AA)-[100-(m2+m3)], m2 (комплекс Arb с ААМПСК) - (11,5-13,6).
Небольшие по величине (19.000-31.000 Da) молярные массы полимеров (ММ) обеспечивают их полное выведение из организма по механизму почечной фильтрации, что при отсутствии у сульфосодержащих сополимеров биологической активности приводит к получению комплекса в приемлемой для организма водорастворимой форме с сохранением биологической активности арбидола как такового.
Полимерные производные арбидола и, в частности, заявляемые водорастворимые полимерные комплексы в литературе не описаны.
Выбор в качестве модификаторов свойств арбидола сополимеров АА-ААМПСК обусловлен следующими причинами:
а) Указанные сополимеры, как и все полимеры акриламида (АА), имеют высокогидрофильные полимерные цепи, хорошо растворяются в воде.
б) Сополимеры содержат сильнокислотные сульфогруппы и в водных растворах легко образуют солевую связь с первичными, вторичными и третичными аминами, а именно к аминам относится арбидол.
в) По данным литературы [М.В.Соловский, М.Ю.Еропкин, У.М.Еропкина и др. Синтез и свойства низкомолекулярных сополимеров акриламида с 2-акриламидо-2-метилсульфокислотой - потенциальных носителей биологически активных веществ // Ж. прикладной химии. - 2008, - Т. 80. - вып.10. - С.1674-1678] сополимеры АА-ААМПСК (≤ 23 мол.% сульфогрупп) нетоксичны in vitro.
6. Получение полимеров-носителей и комлексообразование с ними арбидола
Полимеры-носители - сополимеры акриламида с 2-акриламидо-2-метилпропансульфокислотой (АА-ААМПСК) получали путем гетерофазной радикальной сополимеризации со-мономеров в изопропаноле [М.В.Соловский, М.Ю.Еропкин, Е.М.Еропкина и др. Ж. прикладной химии. - 2007. - Т. 80. - Вып.10. - С.1674-1678]. Состав сополимеров АА-ААМПСК рассчитывали по данным элементного анализа на содержание серы. Молекулярные массы сополимеров АА-ААМПСК определяли вискозиметрическим методом, используя уравнение Марка-Куна-Хаувинка, известное для полиакриламида [Энциклопедия полимеров. Изд-во «Советская энциклопедия». 1972. Т. 1. - С.30].
Строение сополимеров подтверждали титрованием сульфогрупп, а также ИК-спектрами, в которых, в отличие от ИК-спектра поли-АА, наблюдаются новые характеристические полосы поглощения -SO3H групп в области 1227 см-1, 1040 см-1, 624 см-1.
Комплексообразование сополимеров АА-ААМПСК с арбидолом проводили в воде при комнатной температуре, при массовом соотношении сополимер/арбидол, равном 2,3-2,5/1. Сополимеры АА-ААМПСК растворяли в дистиллированной воде из расчета 3,0-4,0 мг/мл и к раствору прибавляли при перемешивании арбидол в сухом виде (26-30 мг). Смесь премешивали в течение 40-60 мин, при этом весь арбидол полностью переходил в раствор. Реакционную смесь фильтровали. Полимерные комплексы выделяли лиофильной сушкой. Содержание арбидола в полученных полимерных комплексах определяли методом УФ-спектроскопии. Использовали интенсивную полосу поглощения арбидола с максимумом при 320 нм (ε=13.700 моль-1·см-1). УФ-спектры снимали в смеси ДМФА + Н2О (объемное соотношение 1:9). Комплексообразование сополимеров с арбидолом схематично показано на схеме:
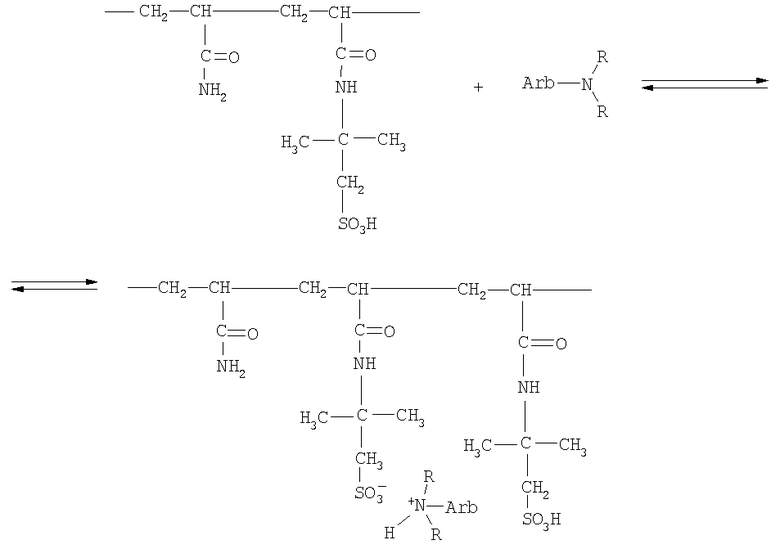
Испытания полученных комплексов осуществляли in vitro.
7. Определение противовирусной активности препаратов
Антивирусное действие синтезированных соединений и препаратов определяли в отношении эталонного штамма вируса гриппа человека A/Victoria/35/72 (H3N2). Действие арбидола и его полимерного комплекса оценивали также в отношении высокопатогенного штамма гриппа птиц, выделенного и депонированного в НИИ гриппа - А/утка/Курган/8/05 (H5N1).
Присутствие вируса в среде инкубации определяли микрометодом реакции гемагглютинации с 0,5%-ной суспензией человеческих эритроцитов I (0) группы крови. Титр вируса выражали в десятичных логарифмах в 100 мкл (lgТИД50). Противовирусную активность образцов оценивали по снижению титра вируса в опытных лунках планшетов по сравнению с контрольными (ΔlgТИД50). Среднюю вирусингибирующую концентрацию образца (ВИК50) вычисляли по цитопатической реакции клеток при воздействии на них вируса определенного титра, которую оценивали в микротетразолиевом тесте. Микротетразолиевый тест (МТТ) проводили согласно Mosmann [Mosmann Т. J Immunol Meth, 1983, v. 65 (1), p.55-63]. Клеточные культуры, выращенные в 96-луночных планшетах, инкубировали 3 ч в растворе МТТ (0,5 мг/мл) на забуференном физиологическом растворе при 37°С в СО2-инкубаторе. Образовавшиеся водонерастворимые кристаллы формазана экстрагировали 95° этанолом 30 мин и измеряли оптическую плотность образцов при длине волны 550 нм на планшетном анализаторе «Chameleon» (Hydex, Финляндия).
Степень угнетения жизнеспособности клеток в культуре коррелирует с развитием вирусной инфекции in vitro.
Противовирусную активность оценивали также в отношении вируса простого герпеса I типа HSV1/248/88 и аденовируса III типа Ad/3/et/4120 на культуре клеток А-549 (линия карциномы легкого человека). Препараты вносили по лечебно-профилактической схеме - за 30 мин до внесения в культуру суспензии вируса. Цитопатическую реакцию учитывали через 48 и 72 ч по степени деградации монослоя (микроскопическое исследование культуры), а также методом МТТ. В последнем случае для вычисления ВИК50 использовали регрессионный метод.
8. Определение цитотоксичности исследованных соединений in vitro
Токсичность арбидола («Мастерлек», М., капсульная форма), полимеров-носителей и полимерных комплексов арбидола определяли путем инкубации культур клеток MDCK с последовательными разведениями препаратов в бессывороточной среде Игла-МЕМ. Стандартное время инкубации с препаратами составляло 72 ч. Методами оценки токсичности in vitro служило восстановление клетками в культуре флуоресцентного красителя резазурина («Sigma», США) [Clothier R., Starzec G., Pradel L. et al. The prediction of human skin responses by using the combined in vitro fluorescein leakage/Alamar blue (resazurin) assay // ATLA. - 2002. - V. 30. - P.493-504] или тетразолиевого красителя МТТ - 3-(4,5-диметилтиазолил-2)2,5-дифенилтетразолий бромид («ICN Pharmaceuticals», США). Метод МТТ осуществляли, как указано выше.
Оба метода отражают интегральную активность митохондриальных дегидрогеназ и служат адекватными показателеми жизнеспособности клеток в культуре и напряженности окислительных процессов. Краситель резазурин (в англоязычной литературе - Аламар голубой) при восстановлении его митохондриальными дегидрогеназами превращается во флуоресцентный продукт резаруфин (λmах возбуждения = 530 нм, λmax эмиссии = 590 нм). Методика приспособлена к 96-луночным планшетам: измерения проводили в планшетном анализаторе «Chameleon» с соответствующими интерференционными светофильтрами для флуоресценции. Преимуществом метода является то, что измерение флуоресценции ведется непосредственно в лунках после инкубации с красителем без дополнительной экстракции, так как продукт реакции - резаруфин свободно экскретируется из клеток в среду. Клетки остаются после этого жизнеспособными, и на той же планшете после отмывки красителя можно проводить еще одно тестирование, например связывание нейтрального красного, определение содержания ДНК или белка и др. [Clothier R., Starzec G., Pradel L. et al. The prediction of human skin responses by using the combined in vitro fluorescein leakage/Alamar blue (resazurin) assay // ATLA. - 2002. - V. 30. - P.493-504].
В качестве критерия токсичности в обоих методах принимали IC50 - цитотоксическую дозу, вызывающую падение соответствующего показателя на 50% от контроля (интактные клетки), которую рассчитывали по уравнениям линейной регрессии доза-эффект. На каждую концентрацию брали не менее 4-х точек с тремя и более независимыми повторами эксперимента. Использовали два варианта представления значений концентрации - линейный и логарифмический. Математическую и статистическую обработку данных проводили в программе Excel 2000.
Сущность изобретения представлена на примерах.
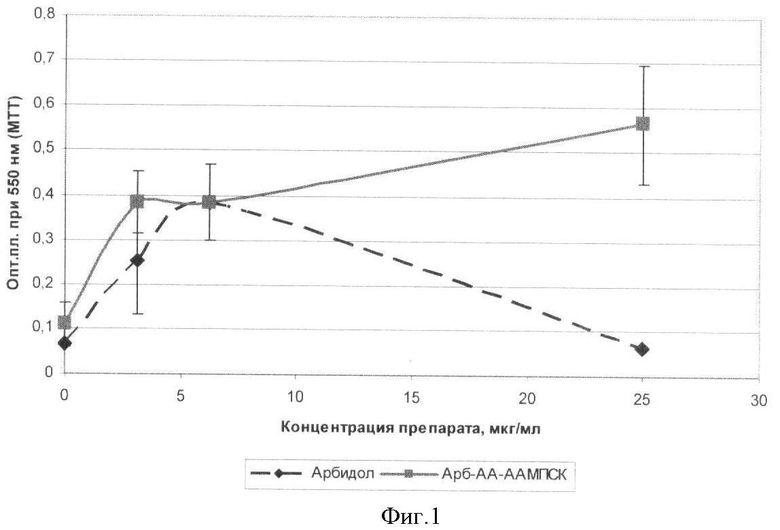
Пример 1. 68 мг сополимера АА-ААМПСК, содержащего 19,1 мол.% сульфогрупп, с ММ 19.000 Da, растворили в 20 мл дистиллированной воды. К полученному раствору при перемешивании добавили 27,2 мг сухого арбидола. Массовое соотношение сополимер/арбидол - 2,5:1. Смесь интенсивно перемешивали при комнатной температуре в течение 40 мин. При этом арбидол полностью переходил в раствор. Целевой раствор фильтровали через плотный фильтр Шота (40 пор). Фильтрат замораживали и подвергали лиофильной сушке. Получено 75,1 мг (78,8%) водорастворимого полимера, содержащего 28,1 мас.% арбидола. Состав и биологические характеристики полученного продукта приведены в табл.1-4 и на фиг.1 и 2. Из табл.1 видно, что противовирусная активность комплекса арбидола с данным носителем соизмерима с противовирусной активностью немодифицированного арбидола в отношении модельного штамма вируса гриппа A (H3N2), а его токсичность in vitro примерно в 10 раз ниже, чем у немодифицированного арбидола (соответствующее IC50 выше на порядок). По данным, представленным в табл.2, следует, что арбидол обладает в данной системе отчетливой противовирусной дозозависимой активностью (ΔlogTИД50>2,0) как в отношении модельного вируса A(H3N2), так и высокопатогенного штамма «птичьего гриппа» A(H5N1), причем активность комплекса в отношении последнего существенно выше, чем немодифицированного арбидола. Вирус А/утка/Курган/8/06 (Н5N1)выделен на клеточной культуре MDCK и переведен на куриные эмбрионы (С2/Е1). Гемагглютинирующая активность вируса: 32-128 ГАЕ/0,2 мл, инфекционная активность: 6,0 ТИД50/0,2 мл.
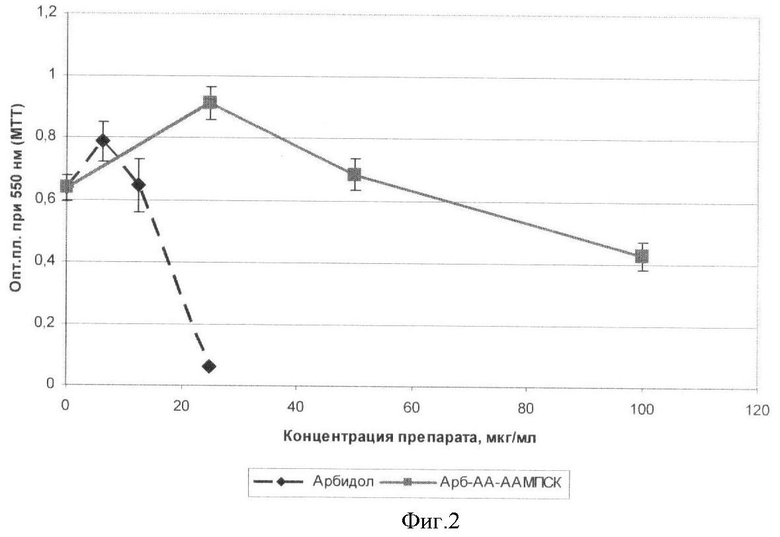
Более детальные данные о воздействии полимерно-модифицированного арбидола представлены на фиг.1 и 2. На фиг.1 представлена противовирусная активность арбидола (пуктирная линия) и комплекса Арб-АА-ААМПСК (сплошная линия) в отношении высокопатогенного гриппа птиц А/утка/Курган/8/05. По оси абсцисс -концентрация арбидола и комплекса в мкг/мл. По оси ординат - опт. пл. при 550 нм (МТТ). На фиг.2 представлена цитотоксичность арбидола (пунктирная линия) и комплекса Арб-АА-ААМПСК (сплошная линия) на культуре клеток MDCK. Обозначения те же, что на фиг.1.
ΔlogТИД50=2,0 для арбидола при концентрации его 6,25 мкг/мл. При 10 ТИД50 вирусингибирующая концентрация (BИК50) арбидола составила ВИК50=5,2 мкг/мл. Среднетоксическая концентрация арбидола in vitro в отношении клеток MDCK: IС50=19,5 мкг/мл (см. стр.2). Таким образом, фармакологический индекс (индекс селективности препарата) при 10 ТИД50 равен 3,75, что является явно неудовлетворительным показателем для такого широко используемого препарата.
В то же время для полимерно-модифицированного арбидола в эквимолярной концентрации (с учетом массового содержания в нем арбидола) при 10 ТИД50 ВИК50=12,5 мкг/мл, а токсичность IС50=190 мкг/мл. Таким образом, индекс селективности для данного препарата составил в тех же условиях 15,2, что в четыре раза лучше, чем у немодифицированного арбидола.
Отсюда можно сделать вывод, что полимерно-модифицированный арбидол не только проявляет высокую противовирусную активность в отношении высокопатогенного штамма вируса гриппа A(H5N1), выделенного на территории России, но и обладает значительно меньшей токсичностью и гораздо более высоким фармакологическим индексом по сравнению с немодифицированным арбидолом.
В табл.3 представлен противовирусный эффект арбидола и его комплекса с АА-ААМПСК (пример №1 из табл.1) в отношении вируса простого герпеса HSV1/248/88 в культуре клеток А-549. Установлен существенный противовирусный эффект арбидола и сравнимый с ним дозозависимый эффект его комплекса с АА-ААМПСК в отношении вируса простого герпеса 1 типа. Противовирусное действие сравнимо с таковым в отношении вируса гриппа человека.
В табл.4 представлен противовирусный эффект арбидола и его комплекса с АА-ААМПСК (пример №1 из табл.1) в отношении аденовируса А<3/3/эт/4/20 в культуре клеток А-549. Отмечен слабый противовирусный эффект как арбидола, так и его полимерно-модифицированного производного на аденовирусы. Концентрационной зависимости действия последнего при этом не наблюдается. Эффект действия арбидола при оценке его двумя методами совпадает, в то время как для полимерного производного он ниже при оценке по восстановлению МТТ.
Пример 2. В условиях примера 1 из 68 мг сополимера АА-ААМПСК, содержащего 22,0 мол.% сульфогрупп, с М.М. 31.000 Da и 27,2 мг арбидола (массовое соотношение сополимер/арбидол 2,5:1) получено 79,2 мг (83,2%) водорастворимого полимера, содержащего 28,6 мас.% арбидола. Состав и биологические характеристики полученного продукта приведены в табл.1.
Пример 3. В условиях примера 1 из 68 мг сополимера АА-ААМПСК, содержащего 22,8 мол.% сульфогрупп, с М.М. 28.000 Da и 27 мг арбидоола (массовое соотношение сополимер/арбидол 2,5:1) получено 79,4 мг (83,6%) водорастворимого полимера, содержащего 26,4 мас.% арбидола. Состав и биологические характеристики полученного продукта приведены в табл.1.
Пример 4. В условиях примера 1 из 68 мг сополимера АА-ААМПСК, содержащего 22,8 мол.% сульфогрупп, с М.М. 28.000 Da и 30,4 мг арбидола (массовое соотношение сополимер/арбидол 2,3:1) получено 88,3 мг (87,9%) полимера, содержащего 32,1 мас.% арбидола. Состав и биологические характеристики полученного продукта представлены в табл.1. Как видно из таблицы, противовирусная активность всех полимеров, полученных в примерах №№1-4, примерно одинакова. Соответствующий показатель (ΔlogTИД50) превышает 2,0, что свидетельствует о достаточно высокой противовирусной активности синтезированных полимерных комплексов. Противовирусная активность всех полученных в примерах №№1-4 комплексов статистически не отличается как между собой, так и от активности немодифицированного арбидола (непараметрический критерий Манна-Уитни). Токсичность in vitro всех изученных в примерах 1-4 комплексов также примерно одинакова. Наблюдается незначительное колебание цитотоксичности (статистически недостоверное) в зависимости от содержания сульфогрупп. В то же время токсичность всех синтезированных полимерных комплексов почти на порядок ниже токсичности in vitro немодифицированного арбидола, определенной нами в тех же условиях опыта (табл.1).
Пример 5 (контрольный). В условиях примера 1 из 68 мг сополимера АА-ААМПСК, содержащего 22,8 мол.% сульфогрупп, с М.М. 28.000 Da и 22,7 мг арбидола (массовое соотношение сополимер/арбидол 3,0: 1) получено 76,5 мг (84,4%) водорастворимого полимера, содержащего 24,8 мас.% арбидола. Состав и биологические характеристики полученного продукта приведены в табл.1.
Данный комплекс обладал невысокой противовирусной активностью, что соответствует самому низкому массовому содержанию в нем арбидола по сравнению с другими комплексами (примеры 1-4).
Пример 6 (контрольный). 70 мг сополимера АА-ААМПСК, содержащего 19,1 мол.% сульфогрупп с М.М. 19.000 Da, растворили в 20 мл воды. К полученному раствору добавили 36 мг арбидола (массовое соотношение сополимер/арбидол 1,95:1). При этом арбидол не растворился в растворе сополимера.
Анализ табличных данных позволяет сделать следующие выводы:
1. Поставленная изобретательская задача решена заявленными водорастворимыми полимерными комплексами арбидола с низкомолекулярными сополимерами акриламида с 2-акриламидо-2-метилпропансульфокислоты.
2. Противовирусная активность заявленных полимерных комплексов в отношении всех исследованных нами вирусов (вирус гриппа человека A (H3N2), высокопатогенный вирус гриппа птиц А (H5N1), вирус герпеса I типа (HSV1), аденовирус III типа) соизмерима с противовирусной активностью немодифицированного арбидола.
3. Токсичность in vitro заявленных комплексов примерно на порядок ниже токсичности в тех же условиях немодифицированного арбидола.
4. Фармакологический индекс (индекс селективности), рассчитанный для полимерного комплекса (пример №1) в отношении вируса гриппа А (H5N1), составил 15,2 против 3,75 для немодифицированного арбидола. Таким образом, фармакологический индекс полимерного производного в четыре раза превосходит соответствующий показатель немодифицированного арбидола.
5. Заявленные интервальные параметры определяются следующими факторами:
а) Интервал молекулярных масс сополимеров АА-ААМПСК 19.000-31.000 Da, во-первых, обеспечивает решение поставленной изобретательской задачи, а во-вторых, гарантирует полное выведение полимера-носителя из организма по механизму почечной фильтрации.
б) Заявленное содержание арбидола в комплексе (26,4-32,1) мас.% обеспечивает растворимость заявленных комплексов и их высокую противовирусную активность. При содержании арбидола в комплексе 24,8% (пример 5) комплекс характеризуется меньшей противовирусной активностью. Водорастворимый комплекс с желаемым содержанием арбидола 34% (пример 6) получить не удается.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИГИПОКСИЧЕСКОЙ И ЦИТОПРОТЕКТОРНОЙ АКТИВНОСТЯМИ, ИСПОЛЬЗУЕМОЕ ДЛЯ СНИЖЕНИЯ ТОКСИЧНОСТИ РЕМАНТАДИНА ПРИ ЛЕЧЕНИИ ГРИППОЗНОЙ ИНФЕКЦИИ | 2005 |
|
RU2302236C2 |
| ПРИМЕНЕНИЕ ФУЛЛЕРЕНОЛОВ С60(OH)18-24 И С60(OH)30-38 В КАЧЕСТВЕ ПРОТИВОВИРУСНЫХ ПРЕПАРАТОВ | 2011 |
|
RU2472496C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТИВОВИРУСНОГО ВОДОРАСТВОРИМОГО ПОЛИМЕРНОГО КОМПЛЕКСА АРБИДОЛА | 2011 |
|
RU2475255C1 |
| СУЛЬФОСОДЕРЖАЩИЕ ПОЛИМЕРЫ С СОБСТВЕННОЙ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 2016 |
|
RU2635558C2 |
| ПРИМЕНЕНИЕ 1,7,7-ТРИМЕТИЛБИЦИКЛО[2.2.1]ГЕПТАН-2-ИЛИДЕН-АМИНОЭТАНОЛА В КАЧЕСТВЕ ИНГИБИТОРА РЕПРОДУКЦИИ ВИРУСА ГРИППА | 2013 |
|
RU2530554C1 |
| ВОДОРАСТВОРИМЫЕ ПОЛИМЕРНЫЕ КОМПЛЕКСЫ АНТИБИОТИКОВ-АМИНОГЛИКОЗИДОВ | 2006 |
|
RU2335510C2 |
| Водорастворимые сульфосодержащие полимеры с собственной противовирусной активностью и способ их получения | 2023 |
|
RU2814298C1 |
| ПРОТИВОВИРУСНЫЙ ПРЕПАРАТ "ПОЛИРЕМ" | 1994 |
|
RU2071323C1 |
| Водорастворимые сополимеры винилфосфоновой кислоты | 2022 |
|
RU2788168C1 |
| Водорастворимые сополимеры оксикоричной кислоты с виниловыми сомономерами, активные против вирусов гриппа и герпеса | 2024 |
|
RU2841381C1 |
Изобретение относится к высокомолекулярным соединениям медицинского назначения. Описаны водорастворимые полимерные комплексы противовирусного средства арбидола общей формулы
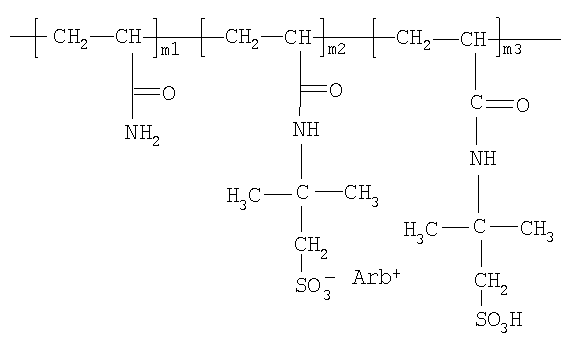
где Arb - арбидол: этиловый эфир 6-бром-4-диметил-аминометил-1-метил-5-окси-2-фенилтиометилиндолинил-3-карбоновой кислоты гидрохлорид моногидрат; m1=100-(m2+m3) мол.%; m2=(7,6-9,8) мол.%; m3=(11,5-13,6) мол.%; содержание Arb=26,4-32,1 мас.%. Созданные водорастворимые полимерные комплексы арбидола могут найти применение в фармакологии, так как могут служить основой новых эффективных и безопасных противовирусных лекарственных средств и их лекарственных форм. 4 табл., 2 ил.
Водорастворимые полимерные комплексы противовирусного средства арбидола общей формулы:
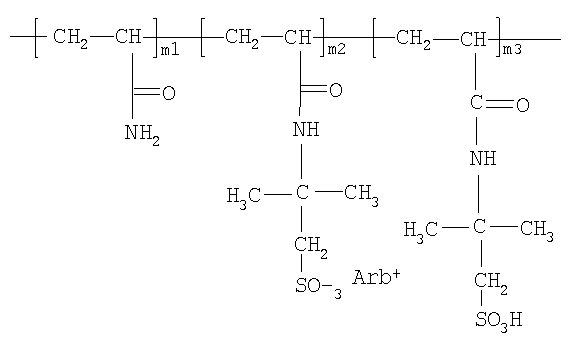
где Arb - арбидол: этиловый эфир 6-бром-4-диметил-аминометил-1-метил-5-окси-2-фенилтиометилиндолинил-3-карбоновой кислоты гидрохлорид моногидрат;
m1=100-(m2+m3) мол.%;
m2=(7,6-9,8) мол.%;
m3=(11,5-13,6) мол.%;
содержание Arb=26,4-32,1 мас.%.
| Журнал прикладной химии.-СПб.: Наука, т.80, вып.10, октябрь 2007, с.1674-1678 | |||
| ЭТИЛОВЫЙ ЭФИР 6-БРОМ-5- ГИДРОКСИ -4-ДИМЕТИЛАМИНОМЕТИЛ -1-МЕТИЛ -2-ФЕНИЛТИОМЕТИЛИНДОЛ -3-КАРБОНОВОЙ КИСЛОТЫ ГИДРОХЛОРИД МОНОГИДРАТ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ГРИППА ТИПА А И ОСТРЫХ РЕСПИРАТОРНЫХ ЗАБОЛЕВАНИЙ | 1974 |
|
RU2033156C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ АРБИДОЛА | 2003 |
|
RU2240784C1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
Авторы
Даты
2010-07-20—Публикация
2008-07-07—Подача