Область изобретения
Настоящее изобретение относится к новым хроматографическим лигандам, которые применимы для очистки биомолекул, таких как протеины. Данные лиганды применимы, например, для очистки антител и предпочтительно иммобилизованы на пористой основе, такой как частицы или мембрана. Следовательно, данное изобретение также включает хроматографическую матрицу, содержащую новые лиганды, способ ее получения и набор для очистки антител.
Предшествующий уровень техники
Иммунная система состоит из многих взаимозависимых типов клеток, которые совместно защищают организм против бактериальных, паразитических, грибковых, вирусных инфекций и от роста опухолевых клеток. Стражами иммунной системы являются макрофаги, которые постоянно перемещаются в кровотоке хозяина. При инфицировании или иммунизации макрофаги реагируют, захватывая возбудителей, помеченных чужеродными молекулами, известными как антигены. Это событие, опосредованное хелперными Т-клетками, определяет сложную цепь ответов, которая приводит к стимуляции В-клеток. Эти В-клетки, в свою очередь, продуцируют белки, называемые антителами, которые связываются с чужеродным возбудителем. Это связывание между антителом и антигеном помечает чужеродного возбудителя с целью разрушения посредством фагоцитоза или активации системы комплемента. Существует несколько разных классов антител, также известных как иммуноглобулины, такие как IgA, IgD, IgE, IgG и IgM. Они отличаются не только своей физиологической ролью, но также и своими структурами. Со структурной точки зрения были широко исследованы IgG-антитела, возможно из-за той главной роли, которую они играют в зрелом иммунном ответе. Поликлональные антитела продуцируются в соответствии со стандартными методами путем иммунизации животного подходящим антигеном. В ответ животное продуцирует антитела, которые являются поликлональными. Однако в силу многих причин желательно иметь единственный клон определенного антитела, известный как моноклональные антитела. Моноклональные антитела (mAbs) продуцируются гибридными или слитыми клетками, представляющими продукт слияния между нормальной В-клеткой, которая продуцирует только одно антитело, и аномальной миеломной опухолевой клеткой. Получаемый в результате гибрид, известный как гибридома, в настоящее время используется в стандартных методах получения антител.
Биологическую активность, которой обладают иммуноглобулины, в настоящее время используют во множестве разных применений в диагностике у человека и ветеринарной диагностике, медицинской помощи и терапевтическом секторе. Фактически в последние несколько лет моноклональные антитела и рекомбинантные конструкции антител стали самым большим классом белков, исследуемых в настоящее время в клинических испытаниях и получивших одобрение FDA (Управление по контролю за продуктами и лекарствами США) в качестве терапевтических и диагностических средств. В дополнение к системам экспрессии и стратегиям продуцирования требуются эффективные протоколы очистки для получения высокочистых антител простым и рентабельным способом.
Традиционные способы выделения иммуноглобулинов основаны на селективном обратимом осаждении белковой фракции, содержащей иммуноглобулины, в то время как другие группы белков остаются в растворе. Типичными осаждающими агентами являются этанол, полиэтиленгликоль, лиотропные соли, такие как сульфат аммония и фосфат калия, и каприловая кислота. Обычно подобные методы осаждения дают очень загрязненные продукты и в то же время являются длительными и трудоемкими. Кроме того, добавление осаждающего агента к неочищенному веществу осложняет использование супернатанта для других целей и создает проблему удаления отходов, которая становится особенно важной, когда речь идет о крупномасштабной очистке иммуноглобулинов.
Альтернативным способом выделения иммуноглобулинов является хроматография, которая включает в себя семейство близких методов разделения. Особенностью, отличающей хроматографию от большинства других физических и химических методов разделения, является то, что в контакт приводят две взаимно несмешивающиеся фазы, причем одна фаза является неподвижной, а другая - подвижной. Смесь образца, введенная в подвижную фазу, подвергается ряду взаимодействий с неподвижной и подвижной фазами, в то время как она перемещается по системе при помощи подвижной фазы. Взаимодействия основаны на различиях физических или химических свойств компонентов в образце. Эти различия определяют скорость перемещения отдельных компонентов под влиянием подвижной фазы, двигающейся через колонку, содержащую неподвижную фазу. Разделенные компоненты выходят в порядке возрастания взаимодействия с неподвижной фазой. Наименее задерживающийся компонент элюируется первым, наиболее сильно удерживаемое вещество элюируется последним. Разделение достигается, когда один компонент удерживается в степени, достаточной для того, чтобы предотвратить перекрывание с зоной соседнего растворенного вещества, когда компоненты пробы элюируются с колонки. Постоянно предпринимаются попытки создать оптимальную неподвижную фазу для каждой конкретной цели разделения. Такая неподвижная фаза обычно состоит из основы или основной матрицы, к которой присоединен лиганд, содержащий функциональные, то есть связывающие, группы. Каждый вид хроматографии обычно указывается на основании принципа взаимодействия, который она использует, например аффинная хроматография, хроматография гидрофобного взаимодействия и ионообменная хроматография.
Аффинная хроматография основана на специфических взаимодействиях между целевой биомолекулой и биоспецифическим лигандом с соответствии с принципом распознавания ключ-замок. Таким образом, мишень и лиганд составляют аффинную пару, такую как антиген/антитело, фермент/рецептор и т.д. Белковые аффинные лиганды хорошо известны, например аффинная хроматография с протеином А и протеином G, обе из которых являются широко распространенными способами выделения и очистки антител. Хорошо известно, что хроматография с протеином А обеспечивает исключительную селективность, особенно в отношении моноклональных антител и, следовательно, позволяет получить высокие степени чистоты. При использовании в комбинации с ионообменными, гидрофобными взаимодействиями, стадиями на гидроксиапатите и/или гель-фильтрации, способы, основанные на протеине А, стали предпочтительным способом очистки антител для многих биофармацевтических компаний, смотри, например, WO 8400773 и US 5151350. Однако из-за пептидных связей белков матрицы с протеином А обладают в некоторой степени чувствительностью к щелочам. Кроме того, когда матрицы с протеином А используют для очистки антител от клеточной культуральной среды, протезы, происходящие из этих клеток, могут вызывать расщепление протеина А или его пептидных фрагментов.
Ионообменная хроматография часто используется в протоколах выделения иммуноглобулинов. При ионообменной хроматографии отрицательно заряженные аминокислотные боковые цепи иммуноглобулина будут взаимодействовать с положительно заряженными лигандами хроматографической матрицы. При катионообменной хроматографии, с другой стороны, положительно заряженные аминокислотные боковые цепи иммуноглобулина взаимодействуют с отрицательно заряженными лигандами хроматографической матрицы.
Хроматография гидрофобного взаимодействия (HIC) представляет собой еще один описанный способ и используется в протоколах выделения иммуноглобулинов. Если целью является иммуноглобулиновый продукт высокой чистоты, обычно рекомендуется сочетать HIC с одной или более дополнительными стадиями. При HIC, для того чтобы иммуноглобулин эффективно связывался с НIC-матрицей, требуется добавление лиотропных солей к подвижной фазе. Связанный гемоглобин затем высвобождается из матрицы при понижении концентрации лиотропной соли. Таким образом, недостатком этого метода является необходимость добавлять лиотропную соль к необработанному веществу, так как это может вызвать проблемы и, следовательно, увеличить стоимость для крупномасштабного потребителя. Например, для необработанных веществ, таких как сыворотка, плазма и яичный желток, добавление лиотропных солей к необработанным веществам во многих случаях будет недопустимо в крупномасштабных применениях, так как соль может препятствовать любому экономически реальному применению обедненного по иммуноглобулину необработанного вещества. Дополнительной проблемой в крупномасштабных применениях будет ликвидация нескольких тысяч литров отходов.
В US 5945520 (Burton et al.) описаны хроматографические смолы смешанного режима, которые имеют гидрофобную природу при рН связывания и гидрофильный и/или электростатический характер при рН десорбции. Такая смола специально создана, чтобы связываться с целевым соединением из водного раствора, как при низкой, так и при высокой ионной силе. Это достигается с помощью выбранных ионизируемых лигандов, содержащих спейсерное плечо и по меньшей мере одну ионизируемую функциональную группу, где плотность ионизуемых лигандов на твердой матрице - основе - больше, чем более низкая из либо приблизительно 150 мкмоль/мл смолы, или 1 ммоль/г сухой массы смолы. Кроме того, гидрофобный характер смолы, содержащей указанные ионизируемые лиганды, достаточен для того, чтобы связать по меньшей мере 50% целевого соединения в водной среде при высокой и низкой ионной силе при первом рН. Иллюстративными примерами ионизируемой функциональной группы являются 4-(аминометил)пиридин, 3-(аминометил)пиридин, 2-(аминометил)пиридин, 1-(3-аминопропил)имидазол, 2-(аминометил)бензимидазол, 4-(3-аминопропил)морфолин.
Также WO 01/38228 (Belew et al.) относится к способу анионообменной адсорбции, при котором для извлечения отрицательно заряженного вещества из жидкости посредством их связывания используются тиоэфирные анионообменники. Каждый лиганд содержит положительно заряженный азот и тиоэфирную связь на расстоянии 1-7 атомов от указанного заряженного азота. Целевые вещества, такие клетки, части клеток и вещества, содержащие пептидные структуры, адсорбируются при концентрации соли около 0,25 М NaCl.
Наконец, в US 6702943 (Johansson et al.) раскрыт способ извлечения целевого вещества из жидкости путем его адсорбции на матрице, несущей множество лигандов, содержащих анионообменные группы и гидрофобные структуры. Более конкретно, лиганды содержат ароматическое кольцо вблизи положительно заряженных анионообменных групп. Целевые вещества определены как клетки, части клеток и вещества, содержащие пептидные структуры. Описанные лиганды обозначены как "высокосолевые" лиганды, благодаря их способности адсорбировать целевые вещества при высоких концентрациях соли, таких как 0,25 М NaCl.
Однако для оптимизации процесса, относящегося к очистке конкретной целевой молекулы, требуются уникальные рабочие условия, и наилучшая сепарационная матрица будет в каждом случае меняться. Например, в биотехнологической промышленности необходимо разработать конкретные процессы для очистки пептидов и белков; нуклеиновых кислот, вируса и т.д. Кроме того, при очистке антител для выбора сепарационной матрицы решающим будет тип антитела. Таким образом, все еще остается необходимость в области альтернативных сепарационных матриц обеспечить широкую возможность выбора для очистки многих новых продуктов, которые постоянно разрабатываются.
Краткое описание сущности изобретения
В одном аспекте изобретения предложен новый лиганд, который применим в отделении антител от других компонентов жидкости.
В конкретном аспекте изобретения предложен такой лиганд, который способен адсорбировать примесные белки, но не целевое антитело.
Дополнительные аспекты и преимущества данного изобретения станут понятны из подробного описания, следующего ниже.
Краткое описание графических материалов
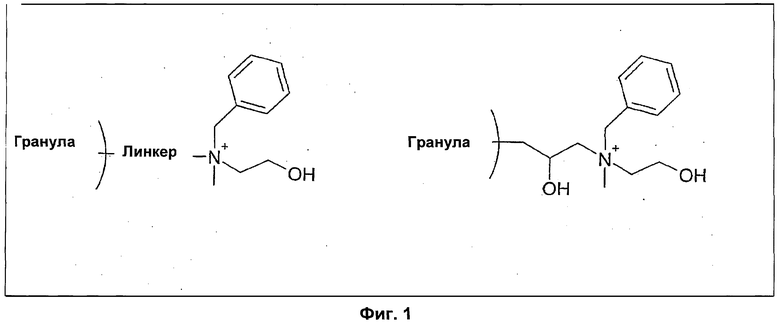
На Фиг.1 показан иллюстративный хроматографический лиганд по изобретению, а именно N-бензил-N-метилэтаноламин, соединенный с основой через свой амин.
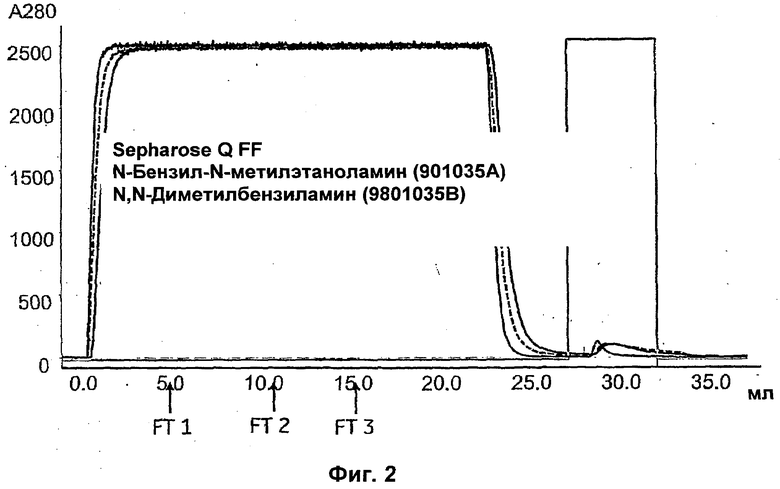
На Фиг.2 показана хроматограмма разделения моноклонального антитела на сепарационной матрице, содержащей N-бензил-N-метилэтаноламинные лиганды, иммобилизованные на Sepharose™ 6 FF и, для сравнения, сильном анионообменнике Q Sepharose™ FF, как описано ниже.
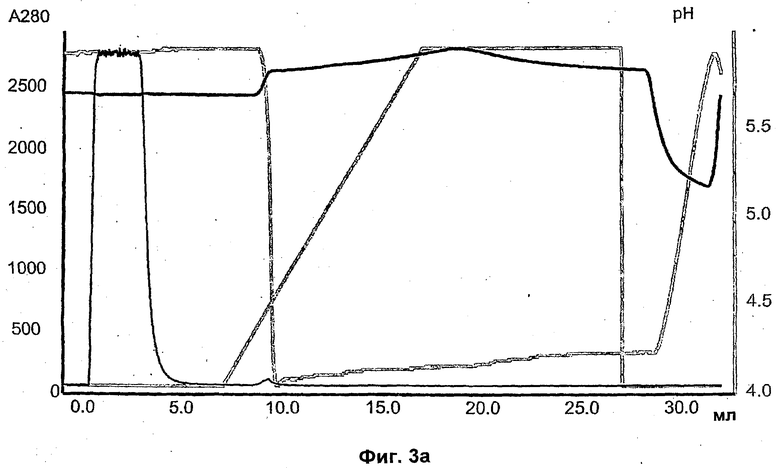
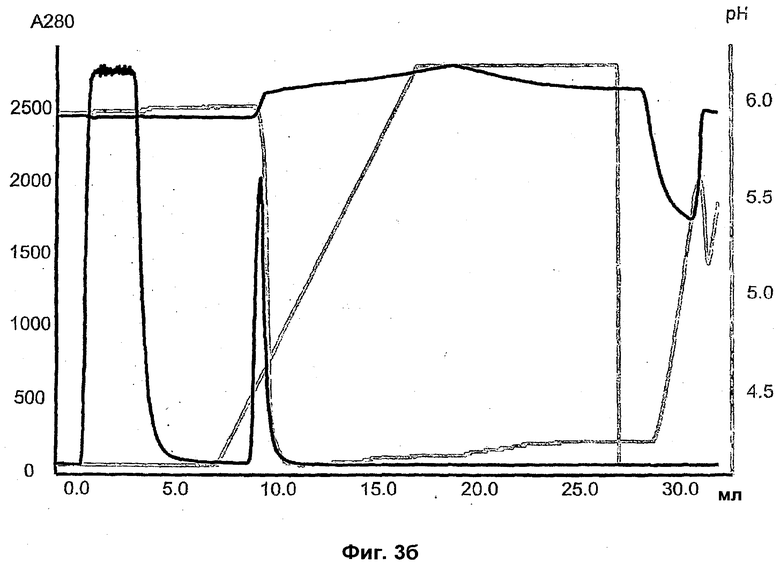
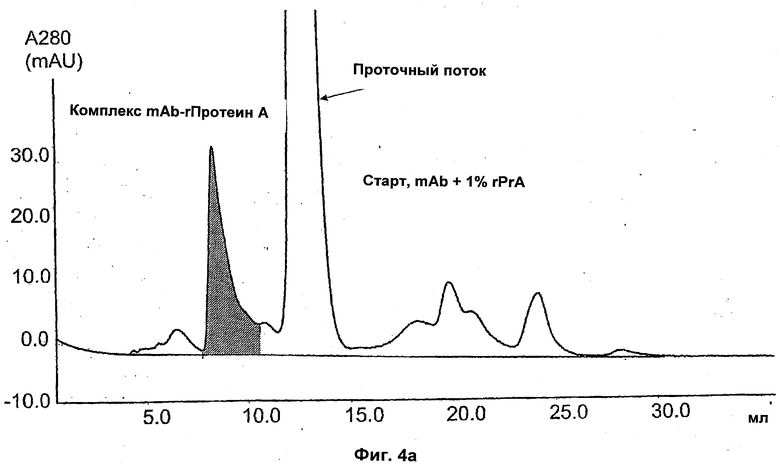
На Фиг.3а) и б) показаны результаты хроматографии, проведенной на опытных образцах лигандов со смесью mAb1-rProtein А.
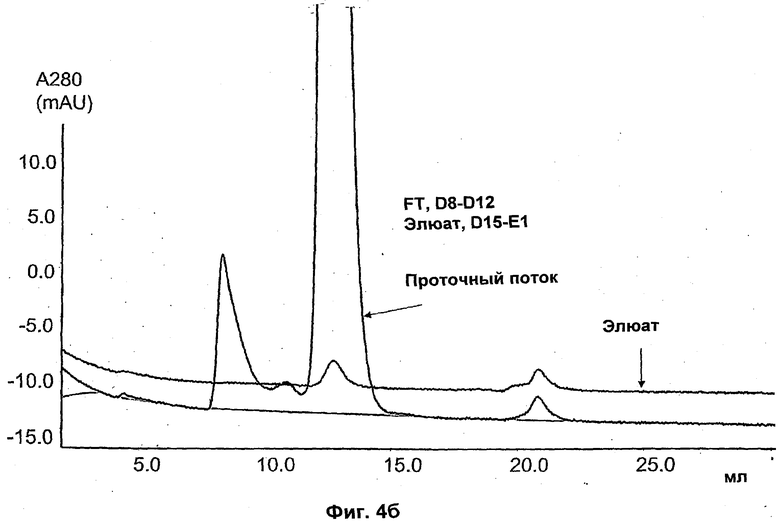
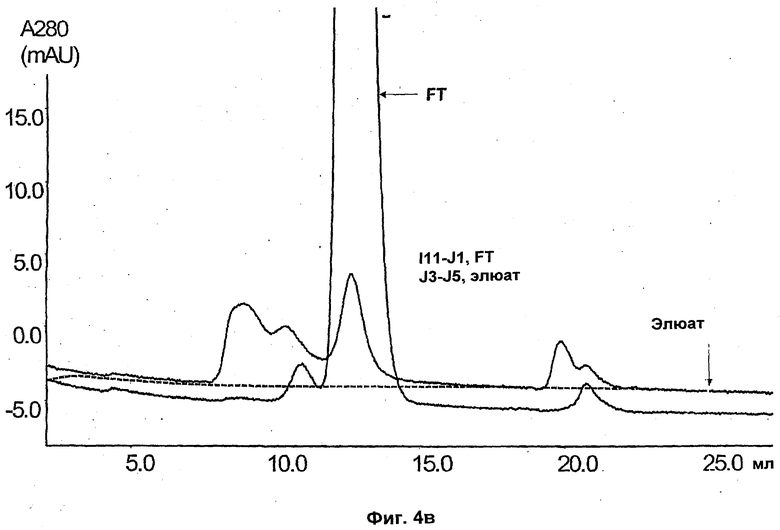
На Фиг.4а)-в) показаны результаты аналитической эксклюзионной хроматографии (SEC) пробы с mAb 1, 1%-ным rPrA и объединенных проточных и элюатных фракций с хроматографических разделений с Фиг.3.
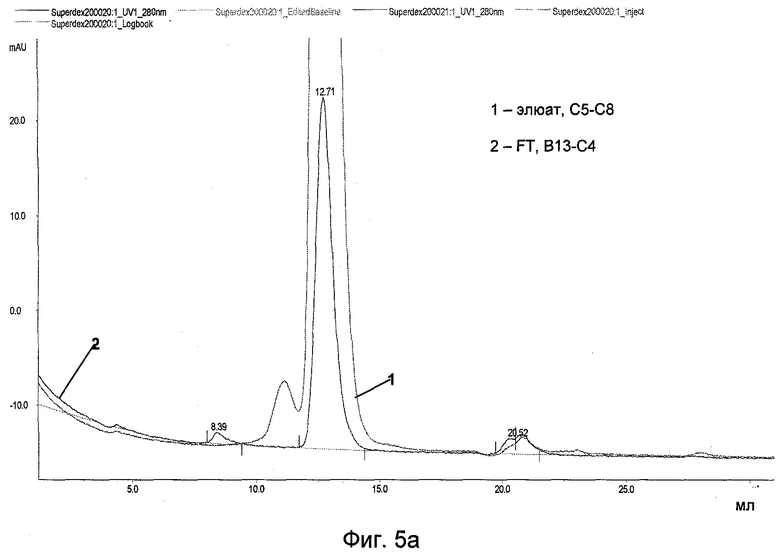
На Фиг.5а представлены результаты аналитической эксклюзионной хроматографии (SEC) для тиомикамина.
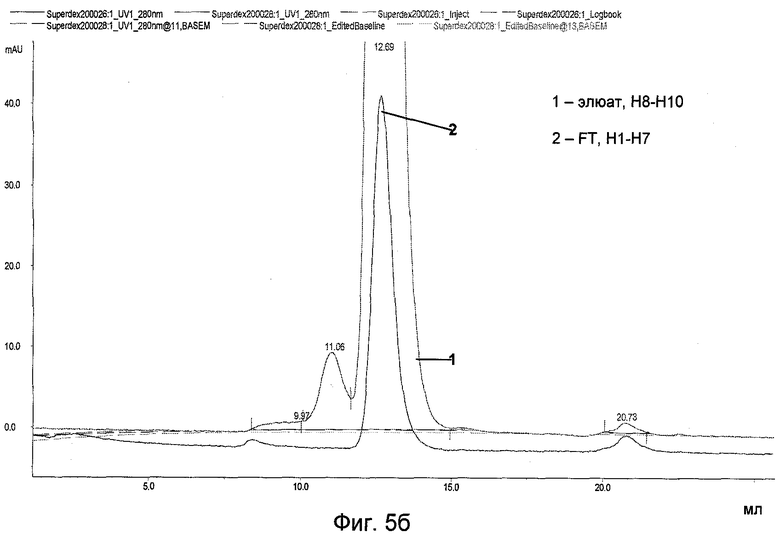
На Фиг.5б представлены результаты аналитической эксклюзионной хроматографии (SEC) для 2-аминобензимидазола.
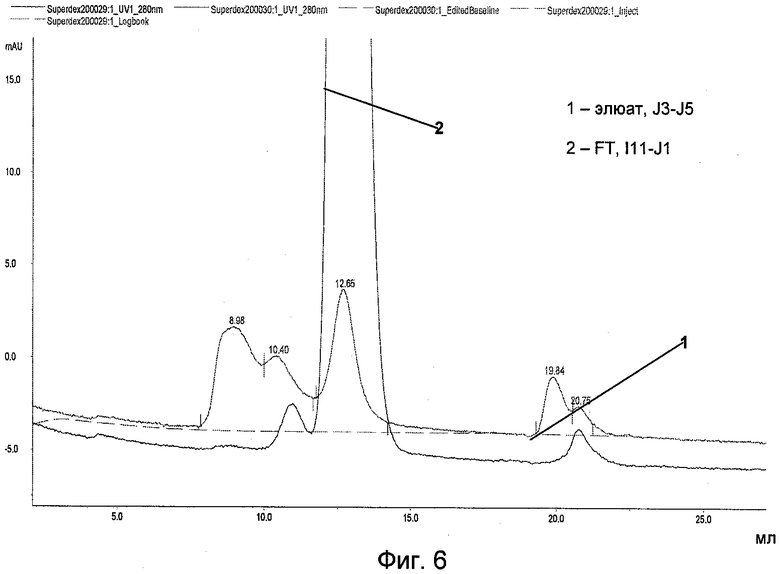
На Фиг.6 представлены результаты аналитической эксклюзионной хроматографии (SEC) для N-бензил-N-метилэтаноламина.
Определения
Термины "антитело" и "иммуноглобулин" в данной заявке используются взаимозаменяемо.
Термин "сепарационная матрица" используется здесь для обозначения материала, состоящего из основы, к которой присоединены один или более чем один лиганд, содержащий функциональные группы. Иногда для сепарационной матрицы в данной области используется термин "смола".
Термин "мультимодальная" сепарационная матрица относится к матрице, способной обеспечить по меньшей мере два разных, но совместно действующих сайта, которые взаимодействуют с соединением, которое следует связать. Например, один из этих сайтов может обеспечивать благоприятный тип заряд-зарядного взаимодействия между лигандом и интересующим веществом. Другой сайт может обеспечивать электронное акцепторно-донорное взаимодействие, и/или гидрофобные и/или гидрофильные взаимодействия. Электронные донорно-акцепторные взаимодействия включают такие взаимодействия, как водородная связь, тт-тт, катион-тт, перенос заряда, диполь-дипольного, индуцированный диполь и т.д. "Мультимодальные" сепарационные матрицы также известны как сепарационные матрицы "смешанного типа".
Термин "поверхность" означает здесь все наружные поверхности и включает в случае пористой основы наружные поверхности, а также поверхности пор.
Термин "элюент" используется в его традиционном в данной области техники значении, то есть буфер с подходящим значением рН и/или ионной силы для высвобождения одного или более компонентов с сепарационной матрицы.
Термин "стадия захвата" в контексте жидкостной хроматографии относится к начальной стадии процесса разделения. Чаще всего стадия захвата включает очистку, концентрирование, стабилизацию и значительную очистку от растворимых примесей. После стадии захвата может следовать промежуточная очистка, которая дополнительно уменьшает количества оставшихся примесей, таких как белки клеток-хозяев, ДНК, вирусы, эндотоксины, питательные вещества, компоненты клеточной культуральной среды, такие как пеногасители и антибиотики, и примеси, родственные продукту, такие как агрегаты, разновидности с неправильным фолдингом и агрегаты.
Термин "одноразовый" означает в данном описании, в контексте хроматографических колонок и других сепарационных матриц, матрицу, которая предназначена для однократного применения или для ограниченного количества применений. Одноразовые продукты преимущественно используются для удаления загрязнений, которые являются вредными даже в небольших количествах, и в этом случае удобно адсорбировать указанное загрязнение на матрицу и затем выбросить данную матрицу. Другой ситуацией, когда желательны одноразовые продукты, является стерильная обработка, когда матрица является стерильной или по меньшей мере асептической.
Термин "стадия тонкой очистки" относится, в контексте жидкостной хроматографии, к конечной стадии очистки, на которой удаляются следовые примеси с получением активного, безопасного продукта. Примеси, удаляемые на стадии тонкой очистки, часто представляют собой конформационные изомеры целевой молекулы или продукты предполагаемой утечки.
Термин "Fc-связывающий белок" означает белок, способный связываться с кристаллизуемой частью (Fc) антитела, и включает, например, протеин А и протеин G, или их любой фрагмент, или их слитый белок, который сохранил указанное свойство связывания.
Подробное описание изобретения
В первом аспекте настоящее изобретение представляет собой хроматографический лиганд, содержащий ароматический этаноламин. Лиганд в соответствии с изобретением особенно полезен в очистке антител, как более подробно будет обсуждаться ниже.
В первом воплощении настоящий лиганд определен следующей формулой:
R1-R2-N(R3)-R4-R5, где
R1 представляет собой замещенную или незамещенную ароматическую кольцевую систему, такую как фенильная группа;
R2 представляет собой углеводородную цепь, содержащую 0-4 атомов углерода;
R3 представляет собой углеводородную цепь, содержащую 1-3 атомов углерода;
R4 представляет собой углеводородную цепь, содержащую 1-5 атомов углерода; и
R5 представляет собой ОН или Н.
Как следует из вышесказанного, группа R1 соединена с амином через углеродную цепь R2, которая может не содержать атомов углерода, то есть создавать связь между R1 и амином; или содержать 1-4 атомов углерода, например 2-3 атомов углерода, которые возможно замещены. Углеродная цепь R4, соединяющая амин с R5, может содержать 1-5 атомов углерода, например 2-4 атомов углерода, которые возможно замещены. R3 амина может содержать 1-3 атомов углерода, например 2 атома углерода, которые возможно замещены.
Ароматическая кольцевая система R1 может содержать одну или более чем одну замещенную или незамещенную фенильную группу, при условии, что замещение(я) не ухудшает связывающие свойства лиганда до какой-либо существенной степени. Таким образом, R1 может содержать одно или более чем одно ароматическое кольцо, например фениленовую, бифениленовую или нафталиненовую структуру и другие ароматические кольцевые системы. Ароматические кольца могут быть гетероциклическими, то есть содержать один или более чем один атом азота, кислорода или серы, например пиридин, пиримидин, пиррол, имидазол, пиррол, имидазол, тиофен или пиран. Иллюстративные замещенные группы R1 выбраны из группы, состоящей из гидроксифенила (2-, 3- и 4-); 2-бензимидазолила; метилтиоксифенила (2-, 3- и 4-); 3-индолила; 2-гидрокси-5-нитрофенила; аминофенила (2-, 3- и 4-); 4-(2-аминоэтил)фенила; 3,4-дигидроксифенила; 4-нитрофенила; 3-трифторметилфенила; 4-имидазолила; 4-аминопиридина; 6-аминопиримидила; 2-тиенила; 2,4,5-триаминофенила; 4-аминотриазинила и 4-сульфонамидофенила.
В предпочтительном воплощении R1 представляет собой незамещенный фенил. В альтернативном воплощении R1 представляет собой фенил, замещенный одной или более группами ОН.
Кроме того, один или более из R1, R2, R3 и R4 могут быть замещены любым подходящим заместителем до тех пор, пока связывающие свойства лиганда не ухудшаются до сколько-либо существенной степени. Например, если требуется более гидрофобный лиганд, он может содержать одну или более чем одну гидрофобную группу, например группы ОН. Альтернативно, замещение может усиливать гидрофобность лиганда, и в этом случае лиганд может содержать одну или более гидрофобную группу, такую как алкил и/или фтор. Наконец, замещение можно использовать для введения одной или более дополнительных функциональных элементов, таких как заряженные элементы для усиления мультимодального характера лиганда. Кроме того, углеродные цепи R2 и R3 могут быть линейными или разветвленными до тех пор, пока разветвления не ухудшают связывающие свойства лиганда до какой-либо существенной степени.
В конкретном воплощении настоящего лиганда R2 представляет собой -СН2-. В другом воплощении R3 представляет собой -СН3. В еще одном воплощении R4 представляет собой -СН2-CH2-СН2- или -СН2-СН2-. В еще одном воплощении R1 представляет собой незамещенный фенил.
Таким образом, в предпочтительном воплощении лиганд по изобретению содержит N-бензил-N-метилэтаноламин (ВМЕА). В альтернативном воплощении лиганд представляет собой N,N-диметилбензиламин.
Лиганд по изобретению может быть легко синтезирован специалистом в данной области стандартными методами органической химии.
Еще одним аспектом данного изобретения является способ получения сепарационной матрицы, включающий иммобилизацию множества лигандов, как описано выше, на основу. Для получения матрицы, подходящей для однократного использования, особенно в области медицины или диагностики, сепарационную матрицу, изготовленную согласно изобретению, на последующей стадии также стерилизуют. Таким образом, в одном воплощении данный способ включает приготовление матрицы, как описано выше; помещение матрицы, полученной таким образом, в колонку и стерилизацию таким образом приготовленной матрицы. Специалист в данной области может легко провести стерилизацию в подходящих условиях, например путем обработки теплом; излучением или любым другим традиционно используемым способом.
Как следует из приведенной выше формулы, в его неиммобилизованном состоянии лиганд по изобретению содержит четвертичный амин, который образует подходящий инструмент для связывания его с основой, таким образом создается связанный лиганд, который содержит четвертичный амин и фенильную группу. Следовательно, считается, что при иммобилизации лиганд по изобретению является мультимодальным анионообменным лигандом, так как в дополнение к положительно заряженной четвертичной аминной группе он также содержит ароматическую кольцевую структуру, которая является гидрофобной. Способы иммобилизации лигандов на пористые или непористые поверхности хорошо известны в данной области; смотри, например, Immobilized Affinity Ligand Techniques, Hermanson et al., Greg T. Hermanson, A. Krishna Mallia and Paul K. Smith, Academic Press, INC, 1992. В одном воплощении плотность лигандов на поверхности основы находится в интервале, близком к интервалу, обычно используемому для традиционных ионообменных матриц.
В предпочтительном воплощении связывание лиганда с основой обеспечивается путем введения линкера между основой и линкером. Связывание можно проводить после любой традиционной методики ковалентного связывания, например при использовании эпихлоргидрина; эпибромгидрина; аллил-глицилового эфира; бис-эпоксидов, таких как бутандиолдиглициловый эфир; галоген-замещенные алифатические вещества, такие как дихлорпропанол; и дивинилсульфон. Эти способы хорошо известны в данной области и легко осуществимы специалистом.
В конкретном воплощении лиганд по изобретению связывают с основой через длинную линкерную молекулу, также известную как экстендер. Экстендеры хорошо известны в данной области и широко используются для пространственного увеличения расстояния между лигандом и основой. Экстендеры иногда называют щупом или гибким плечом, более подробное описание возможных химических структур можно найти, например, в US 6428707, который включен в данное описание посредством ссылки. Кратко, экстендер может находиться в форме полимера, такого как гомо- или сополимер. Гидрофобные полимерные экстендеры могут иметь синтетическое происхождение, то есть иметь синтетический скелет, или биологическое происхождение, то есть биополимер, имеющий скелет, встречающийся в природе. Типичные синтетические полимеры представляют собой поливиниловые спирты, полиакрил- и полиметакриламиды, поливиниловые эфиры и т.д. Типичные биополимеры представляют собой полисахариды, такие как крахмал, целлюлоза, декстран, агароза.
Основа может быть выполнена из органического или неорганического вещества и может быть пористой или непористой. В одном воплощении основу готовят из нативного полимера, такого как сшитое углеводное вещество, например агароза, агар, целлюлоза, декстран, хитозан, конджак, каррагинан, геллан, альгинат, пектин, крахмал и т.д. Основы из нативного полимера легко изготовить и могут быть возможно сшиты стандартными способами, такими как обратное гелеобразование в суспензии (S Hjertén: Biochem Biophys Acta 79(2), 93-398 (1964). В особенно предпочтительном воплощении основа представляет собой разновидность относительно жесткой, но пористой агарозы, которую готовят способом, усиливающим ее текучие свойства, смотри, например US 6602990 (Berg) или SE 0402322-2 (Berg et al.). В альтернативном воплощении основу готовят из синтетического полимера или сополимера, таких как сшитые синтетические полимеры, например стирол или производные стирола, дивинилбензол, акриламиды, акрилатные эфиры, метакрилатные эфиры, виниловые эфиры, виниламиды и т.д. Такие синтетические полимеры легко приготовить и можно сшить стандартными методами, смотри, например "Styrene based polymer supports developed by suspension polymerization" (R Arshady: Chimica e L"lndustria 70(9), 70-75 (1988)). Нативные или синтетические полимерные основы также имеются в продаже, например у GE Healthcare, Uppsala, Швеция, например, в форме пористых частиц. В еще одном альтернативном воплощении основу готовят из неорганического полимера, такого как силикагель. Неорганические пористые или непористые основы хорошо известны в данной области и могут быть легко приготовлены стандартными способами.
Подходящие размеры частиц сепарационной матрицы по настоящему изобретению могут находиться в диапазоне диаметров 5-500 мкм, например 10-100 мкм, например 20-80 мкм. В случае по существу сферических частиц средний размер частиц может находиться в интервале 5-1000 мкм, например 10-500. В конкретном воплощении средний размер частиц находится в интервале 10-200 мкм. Специалист в данной области может легко выбрать подходящий размер частиц и пористость в зависимости от способа, который собираются использовать. Например, для крупномасштабного процесса, по экономическим причинам может быть предпочтительным более пористая, но жесткая основа, которая позволит производить обработку больших объемов, особенно на стадии захвата. При хроматографии, на выбор будут оказывать влияние такие параметры способа, как размер и форма колонки. В способе со вспученным слоем матрица обычно содержит наполнители высокой плотности, предпочтительно наполнители из нержавеющей стали. Для других способов на природу матрицы могут влиять другие критерии.
Таким образом, вторым аспектом настоящего изобретения является сепарационная матрица, которая содержит лиганды, описанные выше, связанные с основой. Как очевидно специалисту в данной области, каждая основа обычно будет содержать множество лигандов. В конкретном воплощении основа содержит лиганд, как он описан выше, в сочетании со вторым типом лиганда, где лиганд по изобретению присутствует в количестве по меньшей мере приблизительно 30%, предпочтительно по меньшей мере приблизительно 50%, более предпочтительно по меньшей мере приблизительно 70% и наиболее предпочтительно по меньшей мере приблизительно 90% от общего количества лиганда. Такая комбинированная лигандная сепарационная матрица может быть сконструирована для конкретного случая, когда элемент дополнительных взаимодействий улучшает ее сепарационные свойства. Второй тип лиганда может содержать одну или более чем одну заряженную группу, например катионообменник, используемый для элюирования соединений посредством отталкивания заряда; гидрофобные группы; группы, способные к образованию водородной связи; аффинные группы или подобные.
В первом воплощении матрица по изобретению находится в форме частиц, например по существу сферических, вытянутых частиц или частиц неправильной формы. В конкретном воплощении сепарационная матрица является высушенной, например находится в виде сухих частиц, которые при использовании погружают в жидкость для поддерживания их первоначальной формы. В иллюстративном воплощении такая сухая сепарационная матрица состоит из сухих агарозных частиц. Однако матрица по изобретению альтернативно может принимать любую другую форму, традиционно используемую в разделении, например монолиты; фильтры или мембраны; капилляры, чипы; поверхности и т.д.
Следовательно, во втором воплощении матрица содержит мембранную структуру, такую как единственная мембрана, пакет мембран или фильтр.
Третьим аспектом изобретения является применение сепарационной матрицы, описанной выше. В первом воплощении в настоящем изобретении используется сепарационная матрица, как описано выше, в очистке белков. В предпочтительном воплощении настоящего применения белок представляет собой антитело; фрагмент антитела; или слитый белок, содержащий антитело. В другом воплощении в настоящем изобретении используют сепарационную матрицу, как описано выше, в разделении любого другого соединения, например выбранного из группы, состоящей из полипептидов; нуклеиновых кислот, например ДНК, РНК или их олигонуклеотидов, плазмид; вируса; прионов; клеток, таких как прокариотические или эукариотические клетки; липиды; углеводы; органические молекулы, такие как небольшие органические молекулы; лекарственные мишени; диагностические маркерные молекулы. Применение более подробно будет обсуждаться ниже. В еще одном воплощении в настоящем изобретении используют сепарационную матрицу, как описано выше, в качестве основы в клеточной культуре, то есть для иммобилизации клеток, которые растут на поверхностях. Как очевидно специалисту в данной области, в данной заявке термин разделение используется для очистки; выделения и извлечения соединений, а также включает идентификацию целевого соединения, например для диагностических целей.
Четвертым аспектом настоящего изобретения является способ разделения, при котором целевое соединение, такое как антитело, отделяют от одного или более других соединений в жидком образце путем приведения подвижной фазы, содержащей указанный жидкий образец, в контакт с сепарационной матрицей, как описано выше. В предпочтительном воплощении настоящий способ осуществляют, используя принципы жидкостной хроматографии, то есть путем пропускания подвижной фазы через хроматографическую колонку, содержащую сепарационную матрицу по изобретению. В еще одном альтернативном воплощении настоящий способ осуществляют, используя периодический хроматографический процесс, при котором сепарационную матрицу добавляют в сосуд, содержащий жидкий образец. В конкретном воплощении сепарационная матрица, добавляемая в периодическом процессе, содержит сухие частицы, такие как сухие частицы агарозы. В еще одном воплощении способ осуществляют, используя принципы хроматографии в вспученном слое, то есть путем добавления подвижной фазы к вспученному слою, например псевдоожиженному слою, сепарационной матрицы, которая находится в форме по существу сферических частиц, содержащих наполнитель высокой плотности.
В первом воплощении настоящего способа нежелательные соединения адсорбируют на сепарационную матрицу, в то время как нужное соединение, такое как антитела, остается в подвижной фазе неадсорбированным. Как очевидно специалисту в данной области, природа и характер адсорбированного соединения будут зависеть от происхождения жидкого образца. Примеры соединений, адсорбированных в данном воплощении, где нужные антитела не адсорбируются, являются клетки и клеточный дебрис; белки и пептиды; нуклеиновые кислоты, такие как ДНК и РНК; эндотоксины, вирусы, остатки культуральных сред и т.д. В конкретном воплощении, настоящая сепарационная матрица представлена в хроматографической колонке, а подвижная фаза проходит через эту колонку под действием гравитации и/или прокачивания, антитела получают в проточной жидкости колонки. Таким образом, преимуществом данного воплощения является то, что для него не требуется никакого элюирования продукта - антитела из колонки. Ликвидация отдельной стадии элюирования является привлекательной с точки зрения способа, так как меньшее количество стадий приведет к более быстрому протоколу очистки и, следовательно, уменьшит стоимость данного способа. Кроме того, антитела чувствительны к некоторым условиям, которые будут, например, негативно влиять на картину фолдинга; или расщеплять их, атакуя их пептидные связи. Таким образом, даже хотя условия элюирования для анионообменников в общем случае не включают никакие экстремальные химические агенты, изменение соли и/или pH может влиять на чувствительное антитело, причем данный эффект может варьироваться от вида к виду, в зависимости от р1, распределения заряда и т.д. Следовательно, еще одним преимуществом данного воплощения является то, что оно позволяет избежать добавления элюента и приложения элюирующих условий к целевым соединениям. Для получения наиболее подходящих условий для адсорбции соединений жидкий образец объединяют с подходящим буфером или другой жидкостью с получением подвижной фазы. Настоящее воплощение преимущественно осуществляют в условиях, подходящих для анионообменной хроматографии, что обычно включает адсорбцию при относительно низкой концентрации соли. Таким образом, в одном воплощении настоящего способа проводимость подвижной фазы находится в интервале 0-25, например 10-15 мС/см. В одном воплощении pH подвижной фазы составляет приблизительно 5-6. Если желательно затем высвободить адсорбированные соединения, например для повторного использования матрицы, элюирование можно провести при более высокой концентрации соли, например, используя возрастающий ингредиент соли. Для элюирования адсорбированных соединений значение pH также или альтернативно может быть сдвинутым, например представлять собой уменьшающийся градиент pH.
Во втором или альтернативном воплощении настоящего способа целевые соединения адсорбируют на матрицу, как в традиционной жидкостной хроматографии. Матрицу затем можно повторно использовать после селективного элюирования продукта. Элюирование легко осуществить, пропуская подходящий буфер через колонку. Если требуется, до или между таким(и) пропусканием(ями) можно использовать одну или более стадий промывки. В одном воплощении рабочие условия данного воплощения такие, как при традиционном ионном обмене, то есть адсорбция с использованием подвижной фазы, имеющей низкую проводимость, и элюирование с использованием буфера с высокой проводимостью, как обсуждается выше. Специалист в данной области может легко отрегулировать эти условия путем тестирования разных условий и анализа адсорбированного(ых) соединения(й) и потока. В конкретном воплощении нужными соединениями являются антитела.
Выбирая между первым и вторым воплощением из указанных выше, специалист в данной области может легко адаптировать условия для адсорбции конкретного соединения, преимущественно путем регулирования pH и/или проводимости. Например, при разделении антител разные классы антител имеют разные заряды и картины распределения зарядов, что, вместе с целью разделения, решит, является ли более предпочтительным адсорбировать антитела или позволить им пройти через колонку без адсорбции.
Антитела, разделенные в соответствии с одним воплощением данного изобретения, могут происходить из хорошо известного источника, такого как клетки, культивируемые на поверхности, или из периодической или непрерывной клеточной культуры в ферментационных резервуарах или сосудах. Таким образом, в одном воплощении жидкость представляет собой супернатант, получаемый при ферментации клеток. Примерами соединений, от которых требуется очищать антитела, являются белки, ДНК, вирусы, эндотоксины, питательные вещества, компоненты среды для культивирования клеток, такие как пеногасители и антибиотики, и родственные продукту примеси, такие как неправильно свернутые виды и агрегаты. Стадии контакта между подвижной фазой и сепарационной матрицей по настоящему изобретению, то есть стадии адсорбции, может предшествовать стадия механической фильтрации, центрифугирования и/или хроматографии. Например, если жидкий образец представляет собой ферментационный бульон, предпочтительно механически убирать клеточный дебрис, целые клетки и другие относительно крупные компоненты до стадии использования настоящей матрицы.
В одном воплощении данный способ представляет собой стадию захвата в протоколе очистки. В конкретном воплощении жидкий образец представляет собой сырую смесь, которую фильтруют перед контактом с хроматографической матрицей по изобретению. Следовательно, данное изобретение будет все еще представлять стадию захвата, даже если жидкий образец был предварительно механически очищен. Как хорошо известно, клетки-хозяева, которые продуцируют антитела, также содержат ряд других белков, традиционно известных как белки клетки-хозяина (НСР). Такие НСР включают ферменты, такие как протеазы, и другие белки, продуцируемые клетками-хозяевами. Таким образом, в одном воплощении по существу все белки клетки-хозяина из жидкого образца удаляют данным способом, например путем адсорбции на сепарационную матрицу.
В альтернативных воплощениях данный способ использует как вторую, третью или даже четвертую хроматографическую стадию в протоколе очистки, например как очистку промежуточного соединения или стадию тонкой очистки. Таким образом, в одном воплощении подвижная фаза, используемая с данной сепарационной матрицей, содержит элюат с сепарационной матрицы, содержащий антитело. В одном воплощении жидкий образец представляет собой элюат с предшествующей аффинной хроматографической матрицы. В предпочтительном воплощении сепарационная матрица, с которой получают элюат, содержит один или более чем один Fc-связывающий белковый лиганд, например лиганды-протеины А. Термин лиганды-протеины А в данном контексте включает в себя нативный, а также рекомбинантный протеин А или его функциональные фрагменты. В данном контексте термин "функциональный" фрагмент означает фрагмент, который сохранил первоначальные свойства связывания белков. Такие аффинные матрицы имеются в продаже, например MabSelect™ от GE Healthcare. Следовательно, в данном воплощении извлеченное, предпочтительно адсорбированное соединение может представлять собой одно или более, выбранное из группы, которая состоит из высвобожденного протеина А; комплексов, образованных протеином А и антителами, таких как комплексы протеин A-mAb, причем эти комплексы могут содержать ряд антител на молекулу протеина А, например 2-4 антитела в комплексе с одной молекулой протеина А; и агрегаты высвобожденного протеина А или антител. Как очевидно специалисту в данной области, в зависимости от конкретных условий, используемых на предыдущей стадии, такой как аффинная хроматография, для элюата может требоваться кондиционирование посредством соответствующих добавлений или доведений. Так, элюат объединяют с подходящим буфером или жидкостью с получением подвижной фазы.
Данный способ полезен для отделения любого моноклонального или поликлонального антитела, например антител, происходящих из хозяев-млекопитающих, например мышей, грызунов, приматов и людей, или антител, происходящих из гибридом. В одном воплощении разделенные антитела являются человеческими или гуманизированными антителами. Антитела могут быть любого класса, то есть могут быть выбраны из группы, состоящей из IgA, IgD, IgE и IgM. В одном воплощении антитела представляют собой антитела, способные связываться с протеином А, или Fc-содержащие фрагменты антител или слитые белки. В конкретном воплощении антитела представляет собой иммуноглобулины G (IgG), такие как lgG1. В одном воплощении данный способ используют для очистки антител, имеющих pI в интервале 6-9, например в интервале 7-8. В конкретном воплощении pI очищенных антител составляет приблизительно 9. В данном контексте следует понимать, что термин "антитела" также включает фрагменты антител и любой слитый белок, который содержит антитело или фрагмент антитела. Таким образом, настоящее изобретение также включает разделение фрагментов любого из указанных выше антител, а также слитых белков, содержащих такие антитела. В одном воплощении антитела представляют собой моноклональные антитела. В конкретном воплощении антитела представляют собой гуманизированные антитела.
Как следует из вышесказанного, в способе по настоящему изобретению получают по существу чистую фракцию неадсорбированных антител. В данном контексте термин "по существу чистый" означает, что по существу все соединения, не являющиеся антителами, удалены. Наиболее предпочтительно на данной сепарационной матрице удаляют по меньшей мере приблизительно 80%, например по меньшей мере 95%, то есть в интервале 95-100%, например по меньшей мере приблизительно 98%, то есть в интервале 98-100%, и предпочтительно по меньшей мере приблизительно 99%, то есть в интервале 99-100% от общего содержания примесей. Однако, как очевидно специалисту в данной области, полученная чистота будет зависеть от концентрации антитела в жидком образце, наносимом на сепарационную матрицу, а также других используемых условий. Так, в одном воплощении антитела, разделяемые согласно данному способу, представляют собой антитела терапевтического качества. Так, антитела, очищенные согласно изобретению, полезны в исследовании, а также для изготовления фармацевтических средств на основе антител, таких как лекарственные средства на основе mAb. Альтернативным применением очищенных антител является диагностическое применение. Кроме того, очищенные антитела также полезны в пищевых продуктах, например как пищевые добавки для людей. Например, бычьи антитела, очищенные согласно настоящему изобретению, полезны в пищевых продуктах.
В конкретном воплощении данного способа сепарационная матрица по настоящему изобретению представлена в виде одноразовой хроматографической колонки или одноразового фильтра. Преимущество использования одноразовых продуктов в способе очистки терапевтических соединений, таких как антитела, состоит в том, что это позволяет избежать перекрестного загрязнения между двумя разными процессами. Так, в одном воплощении данная сепарационная матрица предложена в виде стерильной хроматографической колонки или фильтра. В одном воплощении данный способ осуществляют как периодический процесс, при котором одноразовую сепарационную матрицу добавляют в сосуд, содержащий жидкость, из которой следует извлечь антитела. Целевым соединениям позволяют в течение походящего времени адсорбироваться на матрицу, после чего жидкую фазу, содержащую антитела, удаляют из сосуда. Использованную матрицу затем можно ликвидировать, без высвобождения адсорбированных соединений, что снова может быть полезным с точки зрения безопасности, так как для соединений, таких как эндотоксины и/или некоторые белки клеток-хозяев, не требуется дальнейшей обработки. В альтернативном воплощении матрица по изобретению предложена в виде одноразового продукта в хроматографической колонке, которую используют в способе, при котором адсорбируются антитела. В предпочтительном воплощении колонку и матрицу стерилизуют, что позволяет пользователю очищать продукт-антитело в асептических и даже стерильных условиях.
Во втором воплощении настоящее изобретение относится к набору для очистки антител от одного или более других компонентов в жидкости, причем набор содержит в отдельных ячейках хроматографическую колонку, заполненную сепарационной матрицей, как описано выше; один или более чем один буфер и написанные инструкции. Сепарационная матрица может быть такой, как описано выше. Указанные инструкции преимущественно подробно описывают способ, как он описан выше.
Подробное описание графических материалов.
На Фиг.1 показан образец лиганда, N-бензил-N-метилэтаноламин, иммобилизованный через атом азота на носитель в форме гранулы. Присоединенный лиганд слева показан со схематически нарисованным линкером; а справа - с иллюстративным гидрофильным линкером. В экспериментальной части опытный образец лиганда соединяли с 6%-ной агарозной матрицей Sepharose™ 6 FF (GE Healthcare, Upsala, Sweden).
На Фиг.2 приведена хроматограмма образца, содержащего 50 мг mAb 1, нанесенного на сепарационные матрицы, содержащие лиганды: N-бензил-N-метилэтаноламин, иммобилизованный на Sepharose™ 6 FF (901035A); N,N-диметилбензиламин, иммобилизованный на Sepharose™ 6 FF; и Q Sepharose™ FF в 25 мМ бис-трис, 100 мМ NaCl (~ 12 мС/см), pH 6,5. Элюирование осуществляли посредством 25 мМ бис-трис, 0,5 М NaCl, pH 6,5.
На Фиг.3а) и б) показаны результаты хроматографии, проведенной на опытных образцах с mAb1-r-Протеин А. А-буфер представлял собой 25 мМ бис-трис, 50 мМ NaCl, pH 6,0. Проводимость составляла приблизительно 7 мС/см. Для элюирования использовали Б-буфер, 0,5 М Na-ацетат, рН 4,0. Скорость потока составляла 0,5 мл/мин (150 см/ч). Образец представлял собой 10 мг mAb1, 0,10 мг rPrA в концентрации 4 мг/мл mAb1 и 1% r-ПротеинА (мас./мас.) 3а) ср. Q Sepharose™ FF и б) N-бензил-N-метилэтаноламин, 146 мкмоль/мл (901035A).
На Фиг.4а)-в) представлены результаты аналитической эксклюзионной хроматографии (SEC) образца с mAb 1, 1% PrA и объединенные проточные и элюатные фракции с хроматографических прогонов на Фиг.3. Голубая кривая представляет собой проточные фракции (FT), а красная - элюат. Более конкретно, на Фиг.4а) показан образец 4 мг/мл mAb1, 0,04 мг/мл rPrA, дающий 1% (мас./мас.); на 4б) показан FT и элюат с Фиг.3а) Q Sepharose™ FF и на 4в) показан FT и элюат с Фиг.3б) N-бензил-N-метилэтаноламин, 146 мкмоль/мл (901035А).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Данные примеры представлены исключительно для иллюстративных целей, и их не следует интерпретировать как ограничивающие каким-либо образом область изобретения, как она определена в прилагаемой формуле изобретения.
Пример 1. Получение репарационной матрицы по изобретению
Получение ВМЕА Sepharose Fast Flow (N-бензил-N-метилэтаноламинового производного сефарозы для быстрого потока)
Одно из воплощений способа получения сепарационной матрицы по изобретению показано ниже, начиная со сшитого агарозного геля (Sepharose™ 6 Fast Flow, GE Healthcare, Upsala, Sweden).
А. Введение аллильной группы на матрицу.
Sepharose 6 Fast Flow активировали аллилглицидиловым эфиром следующим образом: 100 мл Sepharose 6 Fast Flow сушили отсасыванием, смешивали с 0,3 г NaBH4, 12 г Na2SO4 и 35 мл 50%-ного водного раствора NaOH. Смесь перемешивали в течение 1 часа при 50°С. После добавления 100 мл аллилглицидилового эфира суспензию оставляли при 50°С при интенсивном перемешивании в течение еще 16 часов. После фильтрации смеси гель последовательно промывали 500 мл дистиллированной воды, 500 мл этанола, 200 мл дистиллированной воды, 200 мл 0,2 М уксусной кислоты и 500 мл дистиллированной воды.
Титрование показало степень замещения 0,22 ммоль аллила/мл геля.
Б. Активация аллил-Sepharose 6 Fast Flow посредством бромирования.
Бром добавляли к перемешиваемой суспензии 50 мл активированной аллилом Sepharose 6 Fast Flow (0,22 ммоль аллильных групп/мл высушенного геля), 1 г ацетата натрия и 15 мл дистиллированной воды, пока не получали постоянное желтое окрашивание. Затем добавляли формиат натрия, и суспензия полностью обесцвечивалась. Реакционную смесь фильтровали и гель промывали 500 мл дистиллированной воды. Активированный гель затем непосредственно был перенесен в реакционный сосуд и затем взаимодействовал с N-бензил-N-метилэтаноламином.
В. Введение групп ВМЕА (N-бензил-N-метилэтаноламина) на активированную матрицу.
Аминные группы вводили на матрицу непосредственно через атом азота аминных групп. В типичной процедуре связывание с матрицей осуществляли посредством бромирования аллильной группы и нуклеофильного замещения в щелочных условиях. 25 мл геля, активированного бромом (0,22 ммоль аллильных групп/мл высушенного геля), переносили в реакционный сосуд, содержащий раствор
N-бензил-N-метилэтаноламина (16,0 мл). Добавляли 5 мл воды и pH реакционного раствора доводили до 12,0 раствором гидроксида натрия. Реакционную смесь оставляли на 16 часов при перемешивании при 50°С. После фильтрации реакционной смеси гель последовательно промывали 3×10 мл дистиллированной воды, 3×10 мл водной 0,5 HCl и наконец 3×10 мл дистиллированной воды. Гель ВМЕА Sepharose 6 Fast Flow получали со степенью замещения 0,15 ммоль аминов/мл геля.
Пример 2: Очистка антител в потоке
Пример 2А) Диспозиция
В несвязывающих условиях образцы, содержащие приблизительно 50 мг mAb1, наносили на опытный образец 901035 А (N-бензил-N-метилэтаноламин) при приблизительно 5 и 12 мС/см. Проточные фракции (FT) собирали при 5, 10 и 15 объемах колонки (CV). Фракции пика элюирования объединяли. FT-фракции анализировали на содержание НСР и протеина А.
Чтобы подтвердить, что хроматографическая характеристика не была уникальной для одного конкретного mAb, хроматографические прогоны повторяли, используя образец, содержащий mAb2 при pH 6,0 и приблизительно 12 мС/см. Характеристику опытного образца сначала оценивали посредством аналитической SEC (эксклюзионной хроматографии). Выбранные фракции анализировали в отношении содержания НСР и протеина А. После отбора фракций с SEC выбранные фракции отправляли на анализ НСР и протеина А.
Для проверки клиренса r-Протеина А на опытном образце в mAb1 вводили 1% (мас./мас.) рекомбинантный протеин А (r-PrA). Опытный образец инъецировали с объемом образца, соответствующим 10 мг mAb1, 1% r-Протеина А, при pH 6,0 и проводимости приблизительно 7 мС/см. Приточные и элюатные фракции объединяли раздельно и анализировали посредством SEC.
Материалы/Исследуемые единицы
Колонки и гели получали от GE Healthcare, Uppsala, Sweden
Инструменты
Химические реагенты
Все химические реагенты имели аналитическое качество. Вода была отфильтрована через MilliQ.
Хроматографическая среда
Q Sepharose™ Fast Flow (FF) (GE Healthcare, Uppsala, Sweden). Лиганды сепарационных матриц являются опытными образцами, как описано в Таблице 1 ниже.
Образцы
Использовали два разных гуманизированных IgG антитела, подкласс 1, обозначенные mAb1 и mAb2 с коэффициентом экстинкции 1,46 и 1,50 соответственно. Оба антитела экспрессировали в культуре СНО (яичников китайских хомячков) и затем очищали, используя традиционную аффинную хроматография протеина А перед данными экспериментами.
Производили замену буфера на HiPrep™ Desalting колонке (GE Healthcare, Uppsala, Sweden), уравновешенной интересующим буфером, путем инъекции подходящего объема (5-15 мл) с помощью Superloop™ (GE Healthcare, Uppsala, Sweden). Скорость потока составляла 5 мл/мин, собирали фракции по 5 мл. Фракции, содержащие элюированный пик, объединяли и в параллелях определяли поглощение при 280 нм для того, чтобы рассчитать концентрацию согласно уравнению 1:

где A280 - поглощение при 280 нм;
ε (мл·мг-1·см-1) - коэффициент экстинкции для конкретного белка;
C (мг/мл) - концентрация белка;
l (см) - длина пробега.
Эксклюзионную хроматографию (SEC) осуществляли на колонке Superdex™ 200 10/300 (GE Healthcare, Uppsala, Sweden) при скорости потока 0,5 мл/мин. Буфер представлял собой PBS (фосфатный буферный солевой раствор); 10 мМ фосфата, 0,137 М NaCl, 2,7 мМ KCl, pH 7,4, приготовленный из таблеток (Sigma, P-4417).
Способ
Равновесие 2/0,1 CV 2 CV применение первый раз 0,1 CV между прогонами Инъекция образца 50 мкл
Изократическое элюирование 1,5 CV
Хроматография на опытных образцах с mAb
А-буфер представлял собой 25 мМ бис-трис, pH 6,0 или 6,5. В зависимости от нужной проводимости, приблизительно 5 или 12 мСм/см, включали 35 или 100 мМ NaCl. Элюирующий буфер (Б-буфер) представлял собой 25 мМ бис-трис, 0,5 М NaCl, pH 6,5. Скорость потока составляла 0,5 мл/мин (150 см/ч).
Хроматография на опытных образцах с mAb-r-Протеином А
А-буфер представлял собой 25 мМ бис-трис, pH 6,0. Проводимость составляла приблизительно 7 мСм/см за счет добавления 50 мМ NaCl, Б-буфер представлял собой 0,5 М Na-ацетат, pH 4,0. Скорость потока составляла 0,5 мл/мин (150 см/ч). Концентрация образца составляла 4 мг/мл mAb 1 - 0,04 мг/мл rPrA с получением 1% (мас./мас.).
CIP (очистка на месте)
После каждого хроматографического прогона опытный образец и эталонную матрицу Q Sepharose™ FF подвергали следующей СIР процедуре
Анализ протеина А
Выбранные фракции смешивали с SPA разбавителем для образца в соотношении 800 мкл SPA разбавителя образца + 200 мкл образца. После смешивания фракции нагревали на нагревательном блоке при 99°С в течение 10 минут, затем снова смешивали. Затем образцы анализировали в отношении рекомбинантного протеина А.
Анализ белков клетки-хозяина (НСР)
Образцы (минимум 600 мкл) анализировали в отношении содержания НСР. Низший предел обнаружения составляет 10 нг/мл.
Пример 2Б) mAb1-содержащий образец, очищенный на образцах - лигандах, N-бензил-N-метилэтанолмине (901035А).
Образец, содержащий 50 мг mAb1, наносили на N-бензил-N-метилэтаноламин, иммобилизованный на Sepharose™ 6 FF (901035A), приготовленной, как описано в Примере 1 выше, и на сравнительную матрицу Q Sepharose™ FF в 25 мМ бис-трис, 100 мМ NaCl (~12 мСм/см), pH 6,5. Элюирование проводили посредством 25 мМ бис-трис, 0,5 М NaCl, pH 6,5.
Хроматограммы примера 2 представлены на Фиг.2, где показан опытный образец N-бензил-N-метилэтаноламина на Sepharose™ 6 FF (901035A) по сравнению с Q Sepharose™ FF. Проточные (FT) фракции, выбранные для анализа, показаны стрелочками. Результаты НСР и клиренса протеина А, представленные в таблицах 2 и 3 ниже, показывают, что опытный образец превосходит Q Sepharose™ FF в данном отношении.
Пример 3
Очистка mAb1 в протоке из образца, содержащего mAb1 и рекомбинантный протеин А (rPrA), на опытном образце лиганда N-бензил-N-метилэтаноламина
В данном примере осуществляли хроматографию на опытных образцах образца, содержащего mAb1-r-ПротеинА. А-буфер представлял собой 25 мМ бис-трис, 50 мМ NaCl, pH 6,0. Проводимость составляла приблизительно 7 мС/см. Б-буфер представлял собой 0,5 М Na-ацетат, pH 4,0. Скорость потока составляла 0,5 мл/мин (150 см/ч). Образец представлял собой 10 мг mAb1, 0,10 мг rPrA в концентрации 4 мг/мл mAb1 и 1% r-Протеин А (мас./мас.) Результаты представлены в Таблице 3.
Наконец, осуществляли аналитическую SEC на образце с mAb1, 1% rPrA и объединенными проточными и элюатными фракциями с хроматографических прогонов на Фиг.4. Результаты представлены на Фиг.4. На Фиг.4а заштрихованный пик представляет собой комплекс mAb1-протеин А. Голубая кривая представляет собой проточные (FT) фракции, а красная представляет собой элюат.
Пример 4: Режим адсорбции
4А) Диспозиция
Для проверки селективности ВМЕА SEpharose Fast Flow (BMEA; N-бензил-N-метилэтаноламин) в адсорбционном режиме проверяли время удерживания человеческого IgG и восьми разных белков. Результаты сравнивали с имеющимся в продаже анионообменником Q Sepharose Fast Flow. Основой данного метода тестирования являлось то, что протеины инъецировали на HR5/5 колонку (содержащую ВМЕА лиганды, иммобилизованные на Sepharose™ Fast Flow), уравновешенную А-буфером (содержащим пиперазин в качестве буферного компонента). Для элюирования белков использовали градиент соли (смотри метод ниже).
Материалы/Исследуемые единицы
Колонки и Q Sepharose Fast Flow получали от GE Healthcare, Uppsala, Sweden.
HR 5/5™, номер по каталогу 18-0338-01 Объем колонки (CV=1 мл)
Инструмент
Хроматографические системы: ÄKTAExplorer™ 10
Химические реагенты и образцы
Белки, овальбумин, β-лактоглобулин, бычий сывороточный альбумин, α-лактальбумин, миоглобин, лактоферрин, рибонуклеазу А и цитохром С приобретали у Sigma, а человеческий IgG (Gammanorm) приобретали у Octapharma. Белки растворяли в А-буфере в концентрации 1-10 мг/мл. Q Sepharose Fast Flow приобретали у GE Healthcare, Uppsala, Sweden. Все химические реагенты имели аналитическую чистоту, а вода была отфильтрована через MilliQ.
Хроматография
Колонки уравновешивали А-буфером при скорости потока 0,6 мл/мин, затем наносили 100 мкл раствора образца. Одновременно анализировали только один белок. Белки элюировали при помощи линейного градиента от буфера А до буфера Б с градиентным объемом 21 объемов колонки (смотри метод ниже). Буфер А представлял собой 25 мМ пиперазин, pH 10,0, а буфер Б представлял собой 25 мМ пиперазина, 1,0 М NaCl, pH 10,0. Во время всех прогонов детектировали поглощение при 280 нм.
Метод:
Результаты
Для того чтобы зарегистрировать, взаимодействует ли ВМЕА-лиганд с иммуноглобулинами, человеческий IgG наносили на 1 мл колонку (HR 5/5), заполненную новой средой. Кроме того, также наносили белки: овальбумин, β-лактоглобулин, бычий сывороточный альбумин, α-лактальбумин, миоглобин, лактоферрин, рибонуклеазу А и цитохром С. Результаты сравнивали с временем удерживания белков, наблюдаемым для Q Sepharose Fast Flow. Q Sepharose Fast Flow является сильным анионообменником и используется в качестве эталонного анионообменника, так как имеет такую же матрицу-основу (вещество основы, размер гранул, величины пор, объем пор, процесс заполнения и т.д.) и имеет по существу такую же степень замещения (измеренную как ионообменная емкость). Как видно из Таблицы 1, ВМЕА Sepharose Fast Flow удерживала все исследуемые белки более прочно по сравнению с Q Sepharose Fast Flow. Кроме того, IgG представлял собой белок, у которого было самое длительное время удерживания на ВМЕА Sepharose Fast Flow (Таблица 1). Это указывает на значительно более сильное связывание с ВМЕА средой, чем с Q Sepharose Fast Flow. По сравнению с Q Sepharose Fast Flow, время удерживания IgG превышало 27,3 мин, когда использовали ВМЕА Sepharose Fast Flow (Таблица 1). Эти результаты ясно указывают на то, что ВМЕА Sepharose Fast Flow можно использовать для захвата и элюирования IgG селективным образом.
а) Получение репарационной мембраны
Эпокси-активация
1920 г дистиллированной воды и 198 мл NaOH 50% в течение нескольких секунд перемешивали во вращающейся колбе объемом 1000 мл с подвесной магнитной мешалкой. Затем непрерывно в течение примерно 25 минут с использованием насоса добавляли 300 мл эпихлоргидрина. Во вращающейся колбе вокруг стержня мешалки вертикально размещали сухой пласт DIN A4 мембраны Sartobind Epoxy (Sartorius-Stedim, Gottingen Germany, art. No 94EPOX06-001), завернутый в полипропиленовую сетку, и реакцию продолжали в течение 120 минут при перемешивании при 30°С. Мембранный рулон 6 раз промывали водой с временем промывания 2 минуты.
Сочетание
1810 г дистиллированной воды, 3,3 мл NaOH 50% и 180 мл N-бензил-N-метилэтаноламина перемешивали во вращающейся колбе объемом 1000 мл. Затем активированный мембранный рулон (влажный) вертикально погружали в реакционную смесь вокруг стержня мешалки и реакционную смесь оставляли на ночь при перемешивании при 50°С. Мембранный рулон один раз промывали этанолом и 6 раз водой.
Результаты
Поток воды (определенный через 25 мм перфорированный круг в фильтр-воронке в вакууме 0,7 бар (70 кПа)) составлял 1,67 дм3/мин/см2. Динамическая связывающая емкость в отношении нитрат-ионов (определенная через стопу из 5 мембранных дисков (16 мм) в колонке GE Healthcare XK 16/5) составляла 59 микромоль на мл объема мембраны и динамическая емкость (QB 10% при pH 7,4) в отношении бычьего сывороточного альбумина (BSA) составляла 3,0 мг на мл объема мембраны.
б) Удаление белка клетки-хозяина с использованием мембраны
Супернатант клеток яичников китайского хомячка (СНО), экспрессирующих моноклональные антитела, очищали на колонке с протеином А и затем фильтровали через шприцевой фильтр Sarstedt Filtropur S 0,2 микрон. Содержание антител составляло 8 мг/мл и остаточная концентрация белка клетки-хозяина составляла 400 нг/мл. После доведения pH до 6,5 и добавления NaCl с получением проводимости 7 мСм/см раствор прокачивали через пять дисков целлюлозной мембраны с лигандом N-бензил-N-метилэтаноламином, полученной, как описано выше, и упакованной в колонку GE Healthcare XK 16/5. После прохождения через мембраны концентрация белка клетки-хозяина снизилась до 160 нг/мл.
в) Стерилизация
50 г промытых сферических агарозных гранул с 104 микромоль на мл N-бензил-N-метилэтаноламина, присоединенного, как описано в примере 1, помещали во флакон объемом 500 мл. Флакон автоклавировали в автоклаве Getinge GE EC-1 с системой контроля PACS 2000 в течение 10 циклов, причем каждый цикл соответствует 17 минутам при 121,1°С при 2,5-2,7 бар (250-270 кПа). Емкость в отношении хлорид-ионов (содержание лиганда) геля перед автоклавированием составляла 104 микромоль на мл геля и после 10 циклов она составляла 96 микромоль на мл геля. Следовательно, потеря лиганда в каждом цикле была пренебрежимо малой и гель считали подходящим для стерилизации.
Сравнение с лигандами, описанными в WO 01/38227
Прототипы
Три лиганда присоединяли к сшитым агарозным гранулам Sepharose 6 Fast Flow способом, раскрытым в примере 1. Эти лиганды и полученные емкости в отношении хлорид-ионов (содержание лигандов) приведены в таблице ниже. Тиомикамин и 2-аминобензимидазол раскрыты в WO 01/38227.
Методы
Гуманизированное антитело против lgG1 с изоэлектрической точкой ≈ 9 экспрессировали в клетках СНО, частично очищали на смоле с протеином А MabSelect (GE Healthcare) и укрепляли рекомбинантным протеином А (RepliGen). Буфер заменяли на 25 мМ Bis-Tris, pH 6,0, 7 мСм/см на колонке GE Healthcare HiPrep Desalting.
Колонки GE Healthcare HR 5/5 упаковывали прототипными средами и уравновешивали 25 мМ Bis-Tris, pH 6,0, 7 мСм/см (буфером А). Наносили образец и промывали 5 объемами колонки (CV) буфера А. Колонки элюировали градиентом 0-100% буфера Б, причем буфер Б представлял собой 0,5 М Na-ацетат, pH 4,0. Образцы проточных фракций колонки (FT) и пула элюатов анализировали посредством аналитической эксклюзионной хроматографии (SEC) на колонке Superdex 200 10/300 (GE Healthcare).
Результаты
Хроматограммы SEC, представленные на Фиг.5а, 5б и Фиг.6, демонстрируют хорошую селективность N-бензил-N-метилэтаноламиновой среды. Наибольшее количество антител выделено в проточных фракциях, в то время как наибольшее количество примесей обнаружено в элюате. При использовании тиомикаминовой и аминобензимидазольной сред антитело связывается и элюируется совместно с примесями.
| название | год | авторы | номер документа |
|---|---|---|---|
| ХРОМАТОГРАФИЧЕСКИЙ ЛИГАНД | 2005 |
|
RU2541429C2 |
| СПОСОБ ОЧИСТКИ АНТИТЕЛ | 2005 |
|
RU2389552C2 |
| СПОСОБЫ И КОМПОЗИЦИИ, ВКЛЮЧАЮЩИЕ ОЧИЩЕННЫЕ РЕКОМБИНАНТНЫЕ ПОЛИПЕПТИДЫ | 2014 |
|
RU2671481C2 |
| УЛУЧШЕНИЕ АФФИННОЙ ХРОМАТОГРАФИИ ИММУНОГЛОБУЛИНОВ ПУТЕМ ПРИМЕНЕНИЯ ФЛОКУЛЯЦИИ ДО ЗАХВАТА | 2020 |
|
RU2794431C1 |
| СПОСОБЫ И КОМПОЗИЦИИ, ВКЛЮЧАЮЩИЕ ОЧИЩЕННЫЕ РЕКОМБИНАНТНЫЕ ПОЛИПЕПТИДЫ | 2014 |
|
RU2793783C1 |
| СПОСОБ ОЧИСТКИ БЕЛКА СЛИЯНИЯ | 2015 |
|
RU2698654C2 |
| СПОСОБ ОЧИСТКИ ФАКТОРА СВЕРТЫВАНИЯ КРОВИ VIII | 2009 |
|
RU2567811C2 |
| СПОСОБ ОЧИСТКИ ФАКТОРА СВЕРТЫВАНИЯ КРОВИ VIII | 2009 |
|
RU2698392C2 |
| СПОСОБ ОЧИСТКИ БЕЛКА ФАКТОРА РОСТА | 2011 |
|
RU2571926C2 |
| СПОСОБЫ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ ЭТАПОВ ОЧИСТКИ БЕЛКА, НАХОДЯЩИХСЯ НИЖЕ ПО ПОТОКУ, С ИСПОЛЬЗОВАНИЕМ МЕМБРАННОЙ ИОНООБМЕННОЙ ХРОМАТОГРАФИИ | 2012 |
|
RU2648999C2 |
Настоящее изобретение относится к хроматографическому лиганду, представляющему собой N-бензил-N-метилэтаноламин, а также к способу получения сепарационной матрицы, содержащей указанный лиганд, и хроматографической колонки для очистки антител. 5 н. и 5 з.п. ф-лы, 4 табл., 6 ил.
1. Хроматографический лиганд, представляющий собой N-бензил-N-метилэтаноламин.
2. Способ получения сепарационной матрицы, включающий иммобилизацию лиганда по п.1 на основу.
3. Способ по п.2, где лиганд иммобилизован через аминную группу.
4. Способ по п.2 или 3, где основа является пористой.
5. Сепарационная матрица, содержащая лиганд по п.1, присоединенный к основе.
6. Матрица по п.5, где основа представляет собой частицы, такие как, по существу, сферические частицы.
7. Сепарационная матрица по п.5, где основа представляет собой мембранную структуру.
8. Способ изготовления хроматографической колонки, включающий изготовление матрицы, как она определена в п.5 или 6; помещение таким образом полученной матрицы в колонку; и стерилизацию колонки, содержащей эту матрицу.
9. Одноразовая хроматографическая колонка для очистки антител, содержащая сепарационную матрицу по любому из пп.5-7.
10. Колонка по п.9, которая была подвергнута стерилизации.
| Способ получения четвертичных аммониевых оснований | 1960 |
|
SU138227A1 |
| HABTEMARIAM A; ET AL, J | |||
| Chem | |||
| Soc., Dalton | |||
| Trans., 2001, 1306-1318 | |||
| W0 2004076485 A1, 10.09.2004 | |||
| RU 2001126400/15 A, 20.06.2003 | |||
| Johansson B-L; Belew M; Eriksson S; Glad G; Lind O; Maloisel J-L; Norrman N, JOURNAL OF CHROMATOGRAPHY, 2003, 1016, 1, 35-49. | |||
Авторы
Даты
2010-08-10—Публикация
2005-10-21—Подача