Область техники, к которой относится изобретение
Настоящее изобретение относится к области молекулярной фармакологии, в частности к пептиду из интерлейкина-15 (IL-15), который ухудшает связывание IL-15 с альфа субъединицей рецептора; вследствие этого он может быть полезен для лечения заболеваний, связанных с аберрантной экспрессией IL-15 или IL-15Rα.
Предшествующий уровень техники
Цитокин, известный как IL-15, является гликопротеином массой 14-15 кДа, одновременно относящимся к двум группам как фактор активации T-клеток (Grabstein, K.H. et al., Science 1994, 264, 965; Burton, J.D. et al., Proc. Natl. Acad. Sci. USA 1994, 91, 4935). мРНК IL-15 широко экспрессируется в различных клетках и тканях, однако обнаружить белок в этих клетках или в клеточном супернатанте затруднительно вследствие сильного посттранскрипционного контроля его экспрессии на уровне трансляции и внутриклеточного транспорта (Bamford RN. et al., J. Immunol. 1998, 160: 4418-4426; Kurys G, et al., J. Biol. Chem. 2000, 275: 30653-30659). Кроме того, показано, что IL-15 может существовать в активной форме в виде мембранного белка (Musso et al., Blood 1999, Vol. 93, No 10 (May 15),: pp 3531-3539), и недавно было замечено, что он может функционировать либо как лиганд, либо как рецептор (Budalgian et al., JBC 2004, vol 279, No 40: pp 42192-42201), индуцируя через этот путь секрецию провоспалительных цитокинов. Высокий уровень экспрессии растворимого белка был связан с патогенезом аутоиммунных и воспалительных заболеваний. IL-15 был обнаружен при некоторых заболеваниях, включая болезнь Крона (Kirman I., 1996, Am. J. Gastroenterol. 91, 1789), псориаз (Ruckert R. 2000, 165: 2240-2250), лейкемию (Yamada Y. 1999, Leukemia and Lymphoma, 35(1-2): 37-45) и ревматоидный артрит (РА), (Mclnnes I.B. 1998, Immunology Today, 19, 75-79). Связывание лиганда с Т-клеточным рецептором вызывает экспрессию IL-15Rα и экспрессию некоторых антигенов активации, таких как CD69, CD25 и TNFRII. Кроме того, IL-15 является хемоаттрактантом для T лимфоцитов человеческой крови (Wilkinson 1995, J. Exp. Med. 181, 1255-1259). Все эти данные указывают на то, что IL-15, экспрессируемый антигенпредставляющими клетками, может играть важную роль в ранней активации T-клеток на участке воспаления.
Mclnnes и др., выявили отклонения экспрессии IL-15 при этом заболевании, высокую концентрацию IL-15 в синовиальной жидкости и его экспрессию в клетках синовиальной оболочки. Они предложили, что IL-15 является предшественником TNFα в цитокиновом каскаде, представляющем механизм, зависящий от клеточного контакта, в котором Т-клетки, активированные IL-15, индуцируют синтез TNFα макрофагами. Кроме того, предполагается, что IL-15 как важный фактор воздействует на миграцию Т-клеток в синовиальную жидкость (Mclnnes, 1997, NatMed, 3: 189-195).
Ziolkowska et al. сообщили, что IL-15 индуцирует экспрессию IL-17 в суставе пациентов, страдающих ревматоидным артритом, уже известно, что этот цитокин стимулирует высвобождение синовиоцитами нескольких воспалительных медиаторов, таких как IL-6, IL-8, GM-CSF и простагландин E2, что позволяет предположить о важной роли IL-15 в патогенезе ревматоидного артрита (Ziolkowska y col 2000, J Immunol, 164: 2832-2838). Рекрутинг и активация Т-клеток могут происходить вследствие локального синтеза IL-15, и подобная неспецифичная активация может приводить в результате к бесконечному воспалению. Все это позволяет предположить, что ингибирование IL-15 может иметь терапевтический потенциал для лечения этого заболевания, а также других аутоиммунных и воспалительных заболеваний.
Биологические эффекты IL-15 опосредуются через его связывание с рецептором клеточной мембраны, состоящим из трех субъединиц α, β, и γ. IL-15Rα является субъединицей, специфичной для этого цитокина, с которым она связывается с очень высокой аффинностью Kd 10-11, и может обнаруживаться в виде мембранного рецептора, или в растворимой форме (Budagian V. et al., JBC 2004, 279, 39: 40368-40375; Mortier et al., The Journal of Immunology, 2004, 173: 1681-1688).
С субъединицами β и γ также связывается IL-2, цитокин с высоким структурным сходством с IL-15. Ранее сообщалось, что Asp56 в молекуле IL-15 играет важную роль в связывании с β субъединицей рецептора, а Gln156 играет важную роль в связывании с γ субъединицей рецептора.
Мутеины ведут себя как молекулы, являющиеся антагонистами IL-15, связываясь с α субъединицей рецептора и ухудшая передачу сигнала через β и γ субъединицы. Антитела, распознающие эти аминокислоты, также действуют как антагонисты IL-15 (US 6177079, US 6168783, US 6013480, US 6001973, US 9706931, WO 9741232).
Ruchatz et al. (Ruchatz H. 1998, J. Immunol. 160: 5654-5660), создал растворимый фрагмент α субъединицы крысиного рецептора (IL-15Rα) и продемонстрировал, что введение этого фрагмента подавляет развитие коллаген-индуцированного артрита (CIA) у мышей DBA/1.
Genmab Company владеет патентом на специфичные человеческие антитела к IL-15, WO 03017935, в котором описаны 4 вида антител, из них 2 вида, 146B7 и 146H5, связываются с IL-15 в области взаимодействия на γ субъединице рецептора и подавляют IL-15-индуцированную пролиферацию клеток в линии клеток CTLL2 и PBMC (мононуклеарных клеток периферической крови), и антитела 404A8 и 404E4 не подавляют пролиферацию. Применение антитела 146B7 (Amgen) под названием AMG714 для лечения ревматоидного артрита находится на II фазе клинических испытаний.
В последнее время были идентифицированы две последовательности IL-15, связывающиеся с α субъединицей рецептора, с аминокислоты 44 по 52 и с аминокислоты 64 по 68 (Bernard et al., JBC 2004, 279 (23), 24313-24322). Они описали мутеины, которые могут действовать либо как агонисты, либо как антагонисты IL-15.
До настоящего времени не было описано какого-либо пептидного антагониста IL-15. Применение пептида короткой длины (10 aa) в качестве антагониста IL-15 имеет преимущество в селективной блокаде связывания IL-15 с α субъединицей рецептора и в опосредовании или уменьшении эффектов IL-15, проявляющихся в результате взаимодействия IL-15 с рецептором. Например, как описано в настоящем изобретении, пептид, названый Sec.No.1, имеет 10 аминокислотных областей IL-15, которые мы идентифицировали как области, взаимодействующие с α субъединицей рецептора (Фиг.1). Подобный пептид связывает слитый белок IL-15Rα-Fc в ELISA и в анализе со смолой Tentagel (Фиг.2), ингибирует IL-15-зависимую пролиферацию линии клеток CTLL-2 (Фиг.3a и 3b) и защищает от TNFα-индуцированного апоптоза (Фиг.4), этот эффект опосредуется связыванием IL-15 α цепью рецептора. Этот последний эффект позволяет применять его при заболеваниях, где необходимо подавление процесса апоптоза. Подобным образом связывание этого пептида с растворимой α цепью, как описано в настоящем изобретении, может ингибировать обратную передачу сигналов, опосредованную связанным с мембраной IL-15 (Budalgian et al., JBC 2004, vol 279, No 40: pp 42192-42201).
Подробное описание изобретения
В особенности, это изобретение относится к идентификации области IL-15, которая способна связывать субъединицу IL-15Rα. Пептид, содержащий эту область, называемый здесь Sec.No.1, химически синтезированный и способный связывать IL-15Rα-Fc (Фиг.2), подавляет IL-15-индуцированную пролиферацию CTLL2 и защищает от TNFa-индуцированной DMA фрагментации (Фиг.4).
Это изобретение также включает любые гомологичные или миметичные варианты указанного пептида, которые были получены с помощью рекомбинантного или синтетического метода, а также любую содержащую их композицию.
Аналогично, изобретение также включает применение указанного пептида, в отдельности или в комбинации с любой другой подходящей молекулой, например, противовоспалительными стероидными препаратами (кортикостероиды), препаратами, изменяющими течение заболевания (метотрексат) или другими антагонистами цитокинов, применяемыми в лечении ревматоидного артрита, и применение этого пептида для ингибирования связывания IL-15 с α субъединицей рецептора, как в растворимой, так и в связанной с мембраной формах.
Пептид в настоящем изобретении имеет линейную структуру и главным образом характеризуется своей способностью проявлять антагонизм к IL-15. С другой стороны, in vitro эффект, производимый пептидом в настоящем изобретении, демонстрируется с помощью анализа пролиферации клеток CTLL-2 и с помощью анализа ингибирования TNFa-индуцированного апоптоза.
Для выявления описанного пептида применялась технология картирования на целлюлозном фильтре, который содержит полную последовательность IL-15 в последовательных пептидах из 10 аминокислот с 5 перекрывающимися аминокислотами.
В настоящем изобретении пептид Sec.No.1 был синтезирован химически с помощью твердофазного метода, очищен с помощью HPLC, проанализирован с помощью массовой спектрометрии и, наконец, оценен в отношении его воздействия на активность IL-15.
Результаты, приведенные в настоящем изобретении, указывают на то, что идентифицированная и синтезированная область в виде пептида, состоящего из 10 аминокислот (Sec.No.1), соответствует области IL-15, взаимодействующей с α субъединицей рецептора, и поэтому препятствует связыванию IL-15 с его рецептором, ингибируя IL-15-индуцированную пролиферативную активность Т-клеток.
Пептид (Sec.No.1), содержащий аминокислоты IL-15, взаимодействующий с IL-15Rα, имитирует эффект защиты IL-15 ФНОα-индуцированного апоптоза, который опосредуется связыванием IL-15 с IL-15Rα (Bulfone-Paus et al., The FASEB Journal, 1999, September Vol. 13).
Полученные здесь результаты позволяют предположить его применение в качестве терапевтического средства в лечении вышеупомянутых заболеваний, связанных с высокой экспрессией IL-15, где оправдано применение антагонистов IL-15 и тех заболеваний, при которых необходим эффект защиты от апоптоза, а также заболеваний, связанных с высокой экспрессией растворимой IL-15Rα. Подобным образом, антитела, распознающие область, содержащуюся в Sec.No.1 IL-15, будут ингибировать связывание IL-15 с IL-15Rα и будут проявлять активность антагониста IL-15 посредством ингибирования связывания молекул с субъединицей подобного рецептора, по этой причине пептид, связанный с молекулой носителя, или химический конъюгат MAP (мультиантигенный пептид), может применяться для получения антител к антагонисту IL-15.
Цель настоящего изобретения также относится к кодированию DMA вышеупомянутого пептида. В качестве альтернативы для экспрессии пептидной последовательности может также применяться вектор, содержащий последовательность DMA, кодирующую пептид настоящего изобретения.
Описанный здесь пептид может использоваться в комбинации с другими противовоспалительными и иммуносупрессивными агентами или с другими антагонистами цитокинов, применяемыми при ревматоидном артрите, псориазе, болезни Крона и т.д. Описанный пептид может быть включен в лечебные вакцины, для оказания гуморальной реакции против IL-15.
Сущность изобретения
Настоящее изобретение заключается в идентификации последовательности IL-15 (Sec.No.1), взаимодействующей с α субъединицей рецептора. Подобная последовательность, синтезируемая в виде линейного пептида из 10 аминокислот, проявляет свойство антагониста IL-15 в отношении индукции пролиферации Т-клеток, и эффект агониста в отношении защиты от TNFa-индуцированного апоптоза.
Краткое описание чертежей
Фигура 1: картирование IL-15R на целлюлозном фильтре.
IL-15Rα-Fc распознает пептид 8, соответствующий Sec.No.1 и в меньшей степени пептид 7.
Фигура 2: Колориметрический анализ в гранулах Tentagel S.
У гранул, содержащих пептид Sec.No.1, инкубируемых с IL-15Rα-Fc (R&D) в концентрации 5 мкг/мл наблюдалось появление цвета.
2a) Инкубация смолы, содержащей a) несвязанный пептид или b) пептид Sec.No.1 с содержащейся смолой, инкубируемой с 15Rα-Fc (R&D).
2b) Инкубация смолы, содержащей пептид Sec.No.1 с IL15Rα-Fc (R&D) (a) или пептид Sec.No.1, IL15Rα-Fc (R&D) с содержащимся в избытке IL-15 (b).
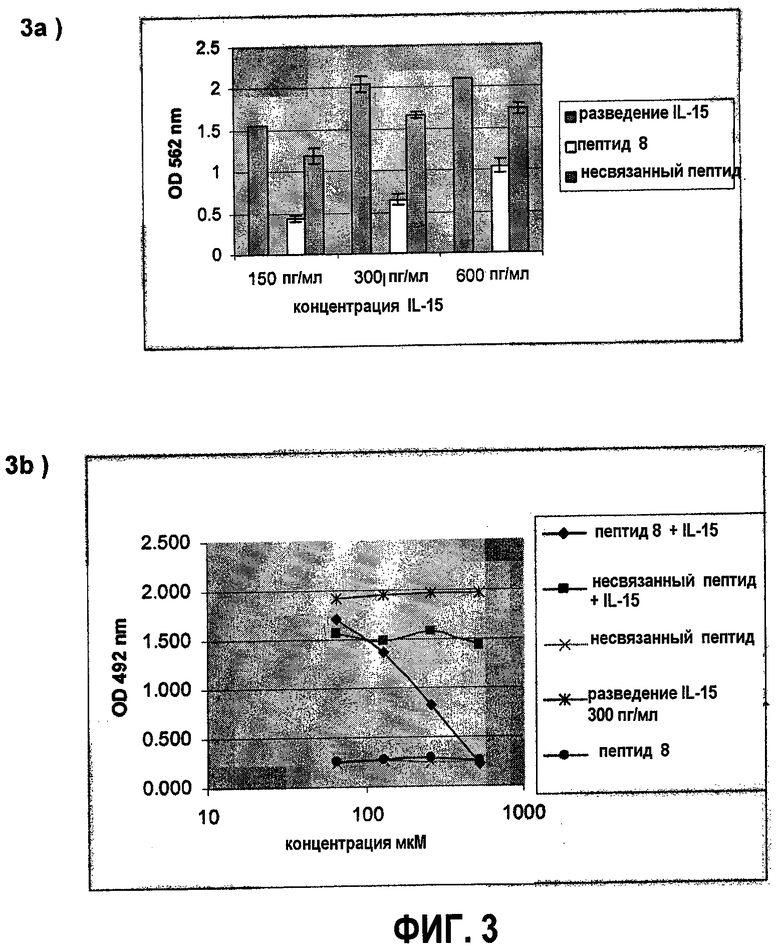
Фигура 3: анализ пролиферации CTLL-2 с человеческим IL-15 (R&D) с определенной активностью 108 Ul/мг
3a), анализ CTLL-2 при различных концентрациях IL-15α и фиксированной концентрации пептида 260 мкМ.
3b), анализ CTLL-2 при различных концентрациях пептида Sec.No.1 и фиксированной концентрации IL-15α 300 пг/мл.
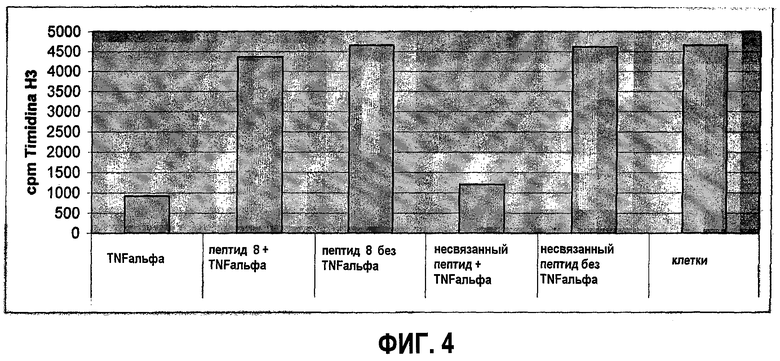
Фигура 4: анализ индукции апоптоза в линии клеток L929. Клетки инкубировались с ФНОα (100 нг/мл) в отдельности или в комбинации с пептидом Sec.No.1 (260 мкМ)
Примеры вариантов осуществления
Следующие примеры предоставлены для иллюстрации вариантов осуществления настоящего изобретения.
Пример 1: A. Идентификация области, связывающейся с IL-15Rα. Синтез на целлюлозной подложке 10-мерных пептидов, соответствующих аминокислотной последовательности IL-15
Для идентификации областей IL-15, участвующих в связывании IL-15Rα, применялся метод синтеза пептидного фрагмента, ранее описанный Frank et. al. Получение бумаги Whatman 540 осуществлялось с помощью этерифицирования первого якорного компонента, Fmoc-β-Ala-OH, используя N,N'-диизопропилкарбодиимид (DIG) и N-метилимидазол (NMI) в сухом N,N-диметилформамиде (DMF). Последовательность фрагмента на целлюлозной мембране определялась с помощью фиксации Fmoc-β-Ala-OH в предварительно отмеченных положениях, в соответствии с необходимым числом 10-мерных пептидов (22 пептида, перекрывающихся в 5 остатках, 114 аминокислот последовательности IL-15). Кроме того, несвязанный пептид из 10 аминокислот был синтезирован в фрагменте 23, а также в фрагменте 24 был фиксирован только Fmoc-β-Ala-OH, оба в качестве контроля. Для сборки всех этих молекул использовали стандартный химический метод Fmoc-/tBu. После конечного цикла синтеза, N-конца и боковые цепи всех пептидов были лишены защиты.
Связывание анти-IL-15 Abs пептидами, синтезированными на целлюлозной подложке
Лист целлюлозы был пропитан этанолом для предотвращения возможных гидрофобных взаимодействий на нем между пептидами. Этанол был замещен солевым раствором Tris-buffer (TBS) (150 мМ NaCl, 10 мМ Tris, pH 7,6) с помощью последовательного промывания. Неспецифическое связывание было блокировано с помощью инкубации мембраны в течение ночи в 10 мл блокирующего буфера IBS (5% порошкованное молоко в IBS). Лист впоследствии инкубировался в течение 3 часов с рецептором IL-15, растворенным в 10 мл буфера образца T-TBS (5% сухое молоко, 0,5% Tween-20 в IBS). Применялось разведение сыворотки 1:50. IL-15α-рецептор был подготовлен в концентрации 5 мкг/мл в том же буферном растворе. Лист целлюлозы был промыт четыре раза буфером T-TBS. Затем на 1 час в анализ IL-15α-рецептора был добавлен анти-IgG конъюгат щелочной фосфатазы (Fc специфичный) (Sigma), растворенный в буфере образца T-TBS (для античеловеческого IgG разбавление 1:25000). Лист целлюлозы был снова промыт четыре раза T-TBS, и была выполнена детекция пептидной связи с помощью инкубации мембраны с 0,5 мг/мл 5-бром,4-хлор,3-индолилфосфатом (BCIP) (Sigma) в основном буфере (100 мМ NaCl, 2 мМ MgCl2, 100 мМ Tris, pH 8,9). Позитивные фрагменты окрасились в синий/фиолетовый цвет. Окрашивание было остановлено промыванием PBS. В конце лист целлюлозы был обновлен для проведения других анализов, описанных ранее (Frank, R. (1992) Tetrahedron 48, 9217). Мы наблюдали распознавание двух пептидов, 8 и 7. В качестве контроля эксперимента мембрана инкубировалась с гуманизированным моноклональным антителом, содержащим область Fc человеческого lgG1. В этом случае мы не наблюдали распознавания на мембране какого-либо пептида.
Колориметрический анализ гранул, демонстрирующий связывание пептида с IL-15Rα. Синтез пептида Sec.No.1 на смоле NH2-7 Tentagel-S. Смола NH2-Tentagel-S (0,24 ммоль/г) была промыта несколько раз дихлорметаном (DCM) и метанолом. Затем она инкубировалась в 30% растворе трифторуксусной кислоты (TFA) в течение 10 минут; промываясь несколько раз DCM и инкубируясь в DCM с 5% содержанием диизопропилэтиламина (DIEA) в течение 1 минуты. Эта процедура вызвала активацию NH2 групп для синтеза. Затем смола была промыта DCM и инкубировалась в диметилформамиде (DMF) в течение 5 минут для синтеза пептида. Применялась обычная методика синтеза Fmoc/tBu. Реакции с образованием связи сопровождались нингидриновым тестом. После завершения анализа пептида Sec.No.1 боковые цепи аминокислот были лишены защиты и оставлены в состоянии фиксации C-концами к смоле.
Анализ на гранулах
Гранулы смолы с фиксированным пептидом несколько раз промывались солевым раствором (PBS). Неспецифичные взаимодействия были блокированы с помощью выдерживания BSA (1%) в PBS в течение 1 часа в реальном времени. Затем они инкубировались со слитым белком IL-15Rα-Fc (R&D 147-IR) в концентрации 5 мкг/мл в BSA (1%/PBS) в течение 16 часов при 4°C. После этого гранулы трижды промывались в PBS в течение 5 минут с перемешиванием, а затем инкубировались с анти-Fc IgG конъюгатом человеческой фосфатазы, разбавленном 1:25000 в BSA (1%/PBS) в течение трех часов в реальном времени. Они были тщательно промыты солевым раствором (TBS/Tween-20,1%) и инкубировались с BCIP (0,45 мг/мл) в растворе субстрата (100 мМ Tris, pH 8,9; 100 мМ NaCl; 2 мМ MgCl2) в течение приблизительно 30 минут. Они были промыты четыре раза PBS для остановки реакции. Интенсивное синее окрашивание наблюдалось только во время инкубации смолы, содержащей пептид Sec.No.1 с белком IL-15Rα-Fc, и не наблюдалось при инкубации смолы, содержащей несвязанный пептид с IL-15Rα-Fc. В этом случае хромогенный субстрат не преципитирует и не окрашивается. Подобным образом мы не наблюдали окрашивания в присутствии избытка человеческого IL-15α.
Синтез пептидов
Пептиды синтезировались согласно методу Fmoc/tBu, применяя смолу Fmoc-AM-MBHA в концентрации 0,54 ммоль/г и протоколам синтеза с механическим перемешиванием. После обработки TFA пептид был лиофилизован и тестировался с помощью HPLC-MS
Пример 2: Влияние описанных пептидов на пролиферацию линии клеток CTLL2
Линия клеток CTLL-2, зависимая от цитокинов, пролиферирует в присутствии IL-15α. IL-15 связывает молекулы, ухудшающие опосредованную рецептором передачу сигнала, подавляющие пролиферацию этой линии клеток.
Для оценки нейтрализующей способности пептида по изобретению были приготовлены его серийные разведения в 96-луночных пластинках (Costar, USA) в объеме среды RPMI (Gibco) 25 мкл, подкрепленные 10% эмбриональной бычьей сывороткой (Gibco). Предварительно промытые клетки CTLL-2 были добавлены к 5x103 клеток на ячейку и инкубировались в течение 30 мин. Затем в каждую ячейку были добавлены 300 пг IL-15а. Пластинка инкубировалась в течение 72 часов в среде с 5% CO2 и 37°C. Результаты показаны на фигуре 3b. Мы установили, что пептид, называемый Sec.No.1, ингибирует IL-15-индуцированную пролиферацию с IC50 130 мкМ. Для определения пролиферации применялось окрашивание митохондрий MTT (Cosman et al. 1984, Nature, 312: 768-771). Мы также оценили антагонистический эффект этого пептида в дозе 260 мкМ при различных концентрациях IL-15а (фигура 3a). Ингибирующий эффект пептида зависел от доз IL-15а.
Пример 3: индукция апоптоза в клетках L929
Анализ Фрагментации ДНК позволяет определить количество DMA, которое подверглось распаду, после обработки клеток TNF-альфа. ДНК клеток радиоактивно помечено с помощью выращивания клеток в присутствии 3H-тимидина так, чтобы радиоактивный 3H-тимидин был включен в ДНК. Через 24 часа клетки были обработаны Tripsin/EDTA, промыты и высеяны в концентрации 5000 клеток на лунку 96-луночной пластинки. Затем помеченные клетки инкубировались с TNFa (100 нг/мл), IL-15 (100 нг/мл), пептидами (260 мкМ) или с комбинацией TNFa с различными пептидами.
Во время этой инкубации добавленный агент (например, TNFa индуцирует клеточную смерть путем апоптоза и, следовательно, фрагментацию ДНК, тогда как ДНК необработанных клеток остается интактной). Клетки были собраны через 24 часа: во время сбора, клетки вымывались из лунок 96-луночной пластинки дважды дистиллированной водой: клетки и органеллы разрушались и освобождалась ДНК клетки. Фрагменты клетки и ДНК поступали через фильтрующую мембрану (стекловолокно). Через фильтр могут проходить только частицы менее 1,5 мкм. Так, интактная ДНК (с длиной фрагмента в миллиметровом или даже сантиметровом диапазоне) не сможет пройти через фильтр, но будет собираться на фильтрующей мембране. ДНК, которая была расщеплена/разрушена на фрагменты приблизительно 5000 bp или меньше, будет иметь достаточно мелкие размеры, чтобы проходить через поры фильтра и не будет собираться на фильтре. Мембрана фильтра была высушена и в сцинтилляционном счетчике проводился подсчет степени радиоактивности (которая соответствует количеству интактной ДНК). С помощью сравнения подсчитанной радиоактивности (единиц в минуту = cpm) клеток, которые не обрабатывались cpm, и клеток, которые обрабатывались агентом, был вычислен процент фрагментации ДНК. В результате мы обнаружили, что пептид Sec.No.1 защищен от TNF-индуцированного апоптоза.
Пример 4: получение моноклональных антител
Моноклональные антитела были получены, как описано Georges Kohler and Cesar Milstein (Nature, 256:495-497, 1975). Для индуцированных моноклональных антител, которые связывают и ингибируют активность IL-15, был использован пептид Sec.No.1, конъюгированый с KLH, или химический конъюгат, содержащий 4 молекулы этого пептида.
Мыши были подкожно иммунизированы конъюгированным пептидом, который был изготовлен для введения с помощью эмульгации со вспомогательным средством Freund's в количестве от 10 до 100 мкг, с последующими еженедельными подкожными иммунизациями пептидом в неполном вспомогательном средстве Freund's. Иммунная реакция на IL-15 была проверена с помощью ELISA. Мыши с достаточным титром анти-IL-15 иммуноглобулинов получали внутривенно стимулирующую терапию в течение 3 дней до умерщвления и удаления селезенки. Для создания гибридом, производящих моноклональные антитела к IL-15, мы применяли упомянутый протокол, опубликованный в Nature, 256:495-497, 1975. Образующиеся в результате гибридомы подвергались скринингу относительно продукции специфичных антител к IL-15 или пептиду с помощью ELISA и с помощью выявления ингибирующего активность IL-15 эффекта в анализе CTLL-2. Положительные клоны были привиты в брюшную полость сингенных мышей для развития асцита, и образующиеся в результате моноклональные антитела были очищены с помощью осаждения сульфатом аммония и аффинной хроматографии, основанной на связывании антитела с белком A от Staphylococcus aureus.
Пример 5: Оценка пептида Sec.No.1 в создании нейтрализирующих антител у обезьян Macacus irus.
По схеме иммунизации обезьян оценивались три группы, иммунизированных пептидом, конъюгированным с белком-носителем, химически-конъюгированным белком в виде тетрамера (MAP); и плацебо. Белки вводились в количествах от 100 мкг до 200 мкг на прививку, во вспомогательном средстве Freund's. Вторая иммунизация была выполнена через один месяц, а третья иммунизация была выполнена через два месяца. Через две недели после второй и третьей иммунизации были забраны образцы крови для оценки уровня антител анти-IL15 в сыворотке обезьян. Нейтрализующая способность антител, присутствующих в сыворотке обезьян, определялась с помощью анализа CTLL-2 в присутствии 300 пг IL-15.
Преимущества предложенного раствора
Пептид Sec No.1 селективно ингибирует связывание IL-15 с IL-15Ra. Пептид Sec No.1 проявляет антагонизм к эффекту IL-15-индуцированной пролиферации Т-клеток (клеток CTLL-2) и, кроме того, он является агонистом защитного от апоптоза эффекта IL-15 в клетках, чувствительных к ФНОα-индуцированному апоптозу.

| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕПТИД-АНТАГОНИСТ АКТИВНОСТИ ИНТЕРЛЕЙКИНА-15 | 2009 |
|
RU2506270C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДОСТИЖЕНИЯ ИММУННОЙ СУПРЕССИИ | 2001 |
|
RU2270691C2 |
| ВАКЦИННАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ МУТАНТНЫЙ ЧЕЛОВЕЧЕСКИЙ ИНТЕРЛЕЙКИН-15 | 2017 |
|
RU2745199C2 |
| МОДУЛЯЦИЯ IL-2- И IL-15-ОПОСРЕДОВАННЫХ Т-КЛЕТОЧНЫХ ОТВЕТОВ | 2001 |
|
RU2280255C2 |
| БИОЛОГИЧЕСКИ АКТИВИРУЕМЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА НА ОСНОВЕ ЦИТОКИНОВ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2819307C2 |
| ГЕТЕРОДИМЕРНЫЙ БЕЛОК IL-15 И ЕГО ПРИМЕНЕНИЯ | 2014 |
|
RU2689717C2 |
| РЕКОМБИНАНТНЫЙ ХИМЕРНЫЙ БЕЛОК ANTH1, КОДИРУЮЩАЯ ЕГО НУКЛЕИНОВАЯ КИСЛОТА И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2322455C2 |
| ИММУНОЦИТОКИНЫ НА ОСНОВЕ IL-15 И IL-R[альфа] ДОМЕНА SUSHI | 2012 |
|
RU2644671C2 |
| БЕЛКОВЫЙ КОМПЛЕКС ИНТЕРЛЕЙКИНА 15 И ЕГО ПРИМЕНЕНИЕ | 2015 |
|
RU2711979C2 |
| АПОПТОТИЧЕСКИЕ АНТИТЕЛА ПРОТИВ IgE | 2008 |
|
RU2500686C2 |

Изобретение относится к области молекулярной фармакологии, в частности к пептиду, являющемуся частью последовательности интерлейкина-15 (IL-15), который может ингибировать биологическую активность указанной молекулы. В изобретении показано, что при связывании с альфа субъединицей рецептора (IL-15R) пептид подавляет пролиферацию Т-клеток, индуцированную IL-15, и апоптоз, вызванный ФНО. 3 н. и 5 з.п. ф-лы, 4 ил.
1. Пептидный антагонист активности IL-15, представляющий собой аминокислотную последовательность, описанную как Sec. No. №1.
2. Пептид по п.1, характеризующийся тем, что он связывается с клеточной субъединицей IL-15Rα или с ее растворимой фракцией.
3. Пептид по п.1, характеризующийся тем, что он ингибирует IL-15Rα-зависимую биологическую активность IL-15.
4. Пептид по одному из пп.1-3, характеризующийся тем, что он получен с помощью генетической манипуляции или химического синтеза.
5. Пептид по одному из пп.1-3, характеризующийся тем, что он является активным компонентом фармацевтической композиции и способен ингибировать зависимую от клеточного рецептора IL-15Rα биологическую активность IL-15.
6. Цепь нуклеиновой кислоты, характеризующаяся тем, что она кодирует пептид по п.1, причем ее продукт способен связывать клеточный IL15Rα или его растворимую фракцию и ингибирует биологическую активность IL-15.
7. Цепь нуклеиновой кислоты по п.6, характеризующаяся тем, что будучи частью вектора экспрессии она способна ингибировать IL-15Rα-зависимую биологическую активность IL-15.
8. Вакцинная композиция, содержащая пептид по п.1, конъюгированный с белком-носителем, и способная вызывать ингибирование зависимой от клеточного IL-15Rα биологической активности IL-15.
| RU 97101868 А, 10.05.1999 | |||
| Способ изготовления керамических оснований для непроволочных электрических сопротивлений | 1954 |
|
SU102003A1 |
| WO 9741232 A1, 06.11.1997 | |||
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
Авторы
Даты
2010-08-10—Публикация
2005-09-16—Подача