Настоящее изобретение относится к способу хранения, в частности клеток человека, клеточным средам для хранения клеток, а также применению таких клеточных сред для хранения клеток, причем жизнеспособность клеток во время хранения сохраняется.
Криоконсервация представляет собой часто применяемый способ для хранения живых клеток на протяжении продолжительных периодов времени. Способы криоконсервации постоянно совершенствовались и улучшались в течение последних десятилетий. Существует также потребность в кратковременном хранении клеток, например, непосредственно после выделения из органа, перед замораживанием или после или во время оттаивания (размораживания) клеток после криоконсервации. Часто требуется, чтобы клетки после этого хранения опять сразу же вводились в организм, в частности, человеку. Это введение клеток может, например, осуществляться внутривенным введением клеток. Это введение хранящихся, в частности, посредством криоконсервации клеток в человека может быть использовано прежде всего в качестве клинического, в частности в качестве терапевтического применения. Так, например, трансплантаты печеночных клеток человека могут вводиться внутривенно для терапевтического применения. Однако процесс замораживания и процесс повторного оттаивания и предшествующее или непосредственно последующее хранение in vitro до сих пор представляет нерешенную задачу для сохранения жизнеспособности и количества живых клеток, которые должны храниться, особенно при клиническом применении.
В основе настоящего изобретения лежит техническая задача обеспечения легко приготовляемой и по возможности недорогой среды для хранения клеток животных, предпочтительно клеток человека, в частности печеночных клеток или трансплантатов печеночных клеток. Эти клетки должны предпочтительно сохраняться в связи с криоконсервацией перед замораживанием и/или после оттаивания. Поэтому в основе данного изобретения лежит также техническая задача получения среды для клеток, которая позволяет краткосрочное хранение клеток животных, предпочтительно клеток человека, особенно предпочтительно печеночных клеток или трансплантатов печеночных клеток при как можно меньшей потере жизнеспособности и количества живых клеток и за счет которой изобретение представляет альтернативу известным клеточным средам.
Для криоконсервации известны клеточные среды для хранения и повторного оттаивания (размораживания). Однако они содержат такие компоненты, как 5-20%-ная фетальная телячья сыворотка (ФТС), которые по закону не разрешены или даже не пригодны для применения, в частности для внутривенного введения людям. Поэтому в основе настоящего изобретения лежит также техническая задача обеспечения среды, которая при малой потере жизнеспособности и количества живых клеток, предпочтительно клеток человека, в частности печеночных клеток или трансплантатов печеночных клеток, делает возможным безопасное введение клеток в животное, в частности в человека.
Так, можно с успехом использовать Custodiol® в качестве клеточной среды, например, для хранения, в частности оттаявших, первоначально криоконсервированных клеток, таких как печеночные клетки; он был также разработан в качестве консервирующего раствора для трансплантации целых органов. Однако Custodiol® по закону не разрешен для внутривенного введения людям. Поэтому в основе настоящего изобретения лежит также техническая задача получения клеточной среды для кратковременного хранения клеток, в частности для криоконсервации, которая разрешена для внутривенного введения людям, и поэтому эти клетки, например, после оттаивания без дорогостоящих и уменьшающих количество живых клеток стадий промывания могут вводиться внутривенно человеку в этой клеточной среде.
Настоящее изобретение решает лежащую в его основе техническую задачу за счет способа кратковременного хранения клеток животных или человека в соответствии с патентными притязаниями. В предпочтительном способе клетки выделяют в жидкой клеточной среде, которая содержит солевой раствор, выбранный, в частности, из солевого раствора, содержащего хлорид натрия, глюконат натрия, ацетат натрия, хлорид калия, хлорид магния и цитрат натрия, и/или солевого раствора, содержащего раствор Рингера-лактат, и/или забуференного фосфатом солевого раствора и/или водного раствора высокомолекулярного сахара, в частности гидроксиэтилкрахмала, а также глюкозы, и, кроме того, сывороточный альбумин и/или плазму крови, и хранят в этой клеточной среде.
В предпочтительном варианте осуществления изобретения клетками животных являются клетки млекопитающих. Речь может идти, например, о свиных, бычьих или мышиных клетках. Особенно предпочтительно речь идет о клетках человека. Под клетками имеются в виду также суспензии клеток и трансплантаты клеток. Клетки могут быть клетками одного типа, но могут быть использованы также композиция или сокультура различных типов клеток.
Согласно данному изобретению в случае клеток животных речь идет о клетках для терапевтического применения. В следующем предпочтительном варианте осуществления в случае клеток животных речь идет о клетках для культивирования in vitro. Клетками животных могут быть, например, гепатоциты, панкреатические островки, хондроциты, хрящевые клетки, нервные клетки, кератиноциты или лимфоциты. Наиболее предпочтительно в случае подлежащих хранению в клеточной среде клеток речь идет о клетках печени, в частности гепатоцитах.
В контексте настоящего изобретения под печеночными клетками понимают смесь клеток, преимущественно состоящую из гепатоцитов. Однако они содержат также различные количественные доли лимфоцитов, эндотелиальных клеток и других непаренхиматозных групп клеток.
Оттаивание и/или хранение тромбоцитов, также называемых кровяными пластинками (Blutplattchen), исключено из настоящего изобретения. В контексте настоящего изобретения тромбоциты не входят в термин клетки животных.
В контексте настоящего изобретения под кратковременным хранением понимают хранение in vitro в среде по настоящему изобретению на протяжении до 24 ч, в частности до 10 ч, предпочтительно до 5 ч, особенно предпочтительно до 3 ч.
Под криоконсервацией имеют в виду в большинстве случаев долгосрочное хранение клеток при температуре ниже 0°С, в частности при (-20°С) - (-200°С). Замораживание происходит, как правило, при 1°С/мин.
В контексте настоящего изобретения под клеточной средой понимают также среду оттаивания или питательную среду, в частности жидкий водный раствор. Эта клеточная среда служит для хранения in vitro живых клеток при сохранении по возможности высокого количества живых клеток, следовательно, по возможности низкой смертности клеток, а также как можно более высокой жизнестойкости или жизнеспособности, которая известна специалистам также как viability.
Согласно настоящему изобретению предпочтительно компоненты применяемой по изобретению клеточной среды разрешены по закону для применения, в частности, для внутривенного применения, в организме животного, предпочтительно в организме человека. Клетки после хранения в среде по настоящему изобретению могут использоваться для клинического применения, в частности терапевтического применения, или для опытов in vitro.
В контексте настоящего изобретения под солевым раствором имеют в виду водный раствор одной или нескольких солей. Предпочтительный солевой раствор содержит хлорид натрия, глюконат натрия, ацетат натрия, хлорид калия, хлорид магния и цитрат натрия, причем эти соли растворены в воде. Используемой водой является стерильная, предпочтительно деионизированная вода для инъекции.
Предпочтительным в соответствии с настоящим изобретением солевым раствором является Composol® или соответствующий составу Composol® раствор. Composol® является водным раствором хлорида натрия, глюконата натрия, ацетата натрия, хлорида калия, хлорида магния и цитрата натрия. Он содержит 173 ммоль/л натрия, 5 ммоль/л калия, 1,5 ммоль/л магния, 98 ммоль/л хлорида, 10,9 ммоль/л цитрата, 27 ммоль/л ацетата и 23 ммоль/л глюконата, предпочтительно он состоит из них.
Поэтому согласно настоящему изобретению солевой раствор содержит 0,45-0,60 масс.%, особенно предпочтительно 0,53 масс.% хлорида натрия, 0,45-0,55 масс.%, особенно предпочтительно 0,50 масс.% глюконата натрия, 0,20-0,25 масс.%, особенно предпочтительно 0,22 масс.% ацетата натрия, 0,003-0,04 масс.%, особенно предпочтительно 0,037 масс.% хлорида калия, 0,025-0,035 масс.%, особенно предпочтительно 0,031 масс.% гексагидрата хлорида магния и 0,31-0,33 масс.%, особенно предпочтительно 0,32 масс.% цитрата натрия, предпочтительно он состоит из них. Солевой раствор имеет предпочтительно показатель рН 7,0-7,4, особенно предпочтительно 7,2.
В следующем варианте осуществления солевой раствор является смесью раствора Рингера-лактат. Обычный состав смеси раствора Рингера-лактат известен специалисту. Смесь раствора Рингера-лактат является водным раствором, содержащим хлорид натрия, хлорид калия, хлорид кальция и лактат натрия. Применяемый согласно настоящему изобретению раствор Рингера-лактат имеет показатель рН 7,0-7,4, предпочтительно 7,2.
В следующем варианте осуществления изобретения солевой раствор является солевым раствором (ЗФР), забуференным фосфатом. Обычный состав ЗФР известен специалисту. Применяемый согласно настоящему изобретению ЗФР имеет показатель рН 7,0-7,4, предпочтительно 7,2.
В следующем варианте осуществления изобретения компонентом этой среды является водный раствор по меньшей мере одного высокомолекулярного сахара. Согласно настоящему изобретению высокомолекулярными сахарами являются, например, декстран, а также растворы декстрана, такие как перфадекс, гидроксиэтилкрахмал (HES) и производные гидроксиэтилкрахмала. Согласно настоящему изобретению в качестве высокомолекулярного сахара применяют также гидроксиэтилкрахмал.
Согласно настоящему изобретению к клеточной среде в твердой форме или в виде водного раствора добавляют глюкозу.
Согласно настоящему изобретению добавляют растворенный в клеточной среде или находящийся в жидкой форме сывороточный альбумин. Сывороточный альбумин может быть, например, в виде фетальной телячьей сыворотки (ФТС), бычьего сывороточного альбумина (БСА) или человеческого сывороточного альбумина (ЧСА). Согласно настоящему изобретению предпочтительным является человеческий сывороточный альбумин, так как он одобрен для внутривенного введения человеку.
В следующем варианте осуществления сывороточный альбумин заменяют или дополняют плазмой крови. Согласно настоящему изобретению предпочтительной является человеческая, предпочтительно аутологичная плазма крови. В частности, плазму и/или ЧСА применяют в качестве криопротектора, предпочтительно отдельно или вместе с другими известными криопротекторами, в частности ДМСО.
В следующих предпочтительных вариантах осуществления изобретения применяемая согласно настоящему изобретению среда содержит по меньшей мере один дополнительный компонент, выбранный из аминокислот, гормонов, витаминов, провитаминов и антиапоптотически активных веществ.
Компоненты состава сред выбираются специалистом в зависимости от области применения в соответствии с его специальными знаниями (квалификацией), после того как он в результате ознакомления с техническим решением сможет применить его в концентрациях в соответствии с настоящим изобретением.
Способ по настоящему изобретению осуществляют предпочтительно в вышеуказанной клеточной среде с показателем рН 6,4-8, предпочтительно 7,0-7,4, в частности 7,2.
Предпочтительно клетки после оттаивания из криоконсервации промывают в клеточной среде по настоящему изобретению, отделяют от среды криоконсервации и клеточной среды настоящего изобретения и затем помещают в свежую клеточную среду настоящего изобретения. Отделение происходит предпочтительно при помощи центрифугирования.
Способ осуществляют предпочтительно при температуре 2-40°С. Клеточная среда имеет предпочтительно температуру 2-40°С. Особенно предпочтительно способ осуществляют при 4°С и/или используемая среда имеет температуру 4°С. В другом предпочтительном варианте осуществления изобретения способ осуществляют при 10°С и/или используемая среда имеет температуру 10°С. В другом особенно предпочтительном варианте осуществления изобретения способ осуществляют при 25°С и/или используемая среда имеет температуру 25°С. В другом особенно предпочтительном варианте осуществления изобретения способ осуществляют при 37оС и/или используемая среда имеет температуру 37°С.
Само собой разумеется, предметом настоящего изобретения является также специальная клеточная среда для кратковременного хранения, в частности, оттаянных после криоконсервации клеток животных или клеток человека, в частности жидкая клеточная среда, которая содержит хлорид натрия, глюконат натрия, ацетат натрия, хлорид калия, хлорид магния и цитрат натрия, а также глюкозу и, кроме того, сывороточный альбумин и/или плазму крови, и в которой указанные компоненты растворены в воде.
Предпочтительная клеточная среда состоит из хлорида натрия, глюконата натрия, ацетата натрия, хлорида калия, хлорида магния и цитрата натрия, а также глюкозы и, кроме того, сывороточного альбумина и/или плазмы крови, причем указанные компоненты растворены в воде. Особенно предпочтительная клеточная среда содержит 0,45-0,60 масс.% хлорида натрия, 0,45-0,55 масс.% глюконата натрия, 0,20-0,25 масс.% ацетата натрия, 0,003-0,04 масс.% хлорида калия, 0,025-0,035 масс.% гексагидрата хлорида магния и 0,31-0,33 масс.% цитрата натрия и, кроме того, сывороточный альбумин и/или плазму крови, причем указанные компоненты растворены в воде.
Предпочтительно эта клеточная среда содержит 0,01-0,5 масс.% глюкозы, особенно предпочтительно 0,1-0,2 масс.% глюкозы.
Согласно настоящему изобретению предпочтительно клеточная среда содержит сывороточный альбумин человека. Сывороточный альбумин человека может быть в соответствии с настоящим изобретением заменен человеческой, в частности аутологичной плазмой крови. В предпочтительном варианте осуществления изобретения среда содержит 0,5-50 масс.% сывороточного альбумина, особенно предпочтительно 3-5 масс.% сывороточного альбумина. В другом предпочтительном варианте осуществления среда содержит 0,5-50 масс.% плазмы крови, особенно предпочтительно 3-5 масс.% плазмы крови.
Клеточная среда по настоящему изобретению имеет предпочтительно показатель рН 6,4-8, предпочтительно 7,0-7,4, в частности 7,2.
Согласно изобретению предпочтительно компоненты клеточной среды по закону разрешены для применения, в частности для внутривенного применения, в организме животного, предпочтительно в организме человека.
Согласно изобретению предпочтительными являются также комбинации вариантов осуществления способа и/или клеточной среды.
Настоящее изобретение включает в себя также применение вышеуказанной клеточной среды для кратковременного хранения оттаянных после криоконсервации клеток животных, в частности в соответствии со способом, раскрытым в настоящем изобретении.
Описание фигур:
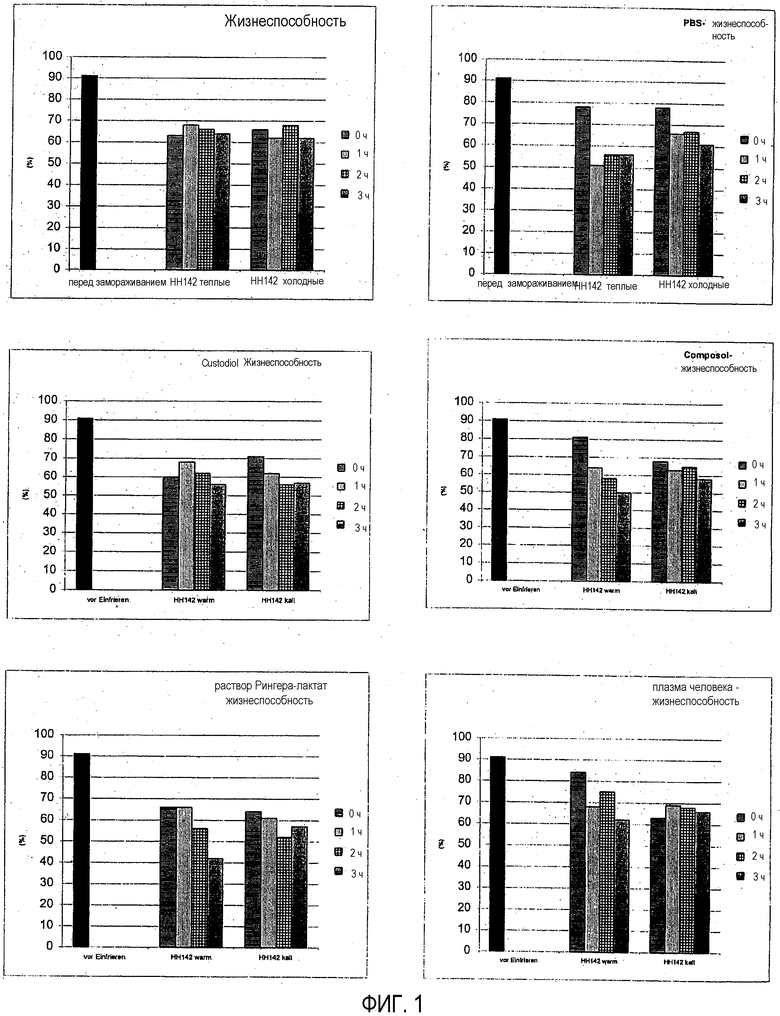
Фигура 1: Жизнеспособность сохранившихся клеток (после криоконсервации) в зависимости от времени хранения, используемой среды для хранения и температуры хранения, подпись к фигуре: “HH142”: количество отдельных препаратов клеток (загрузок), «теплые»: температура хранения 18оС, «холодные»: температура хранения 4оС, «HES»: среда 2, «ЗФР»: среда 5, «Custodiol®»: среда 1, «Composol ®»: среда 4, «Рингер-лактат»: среда 3, «плазма человека»: среда 6;
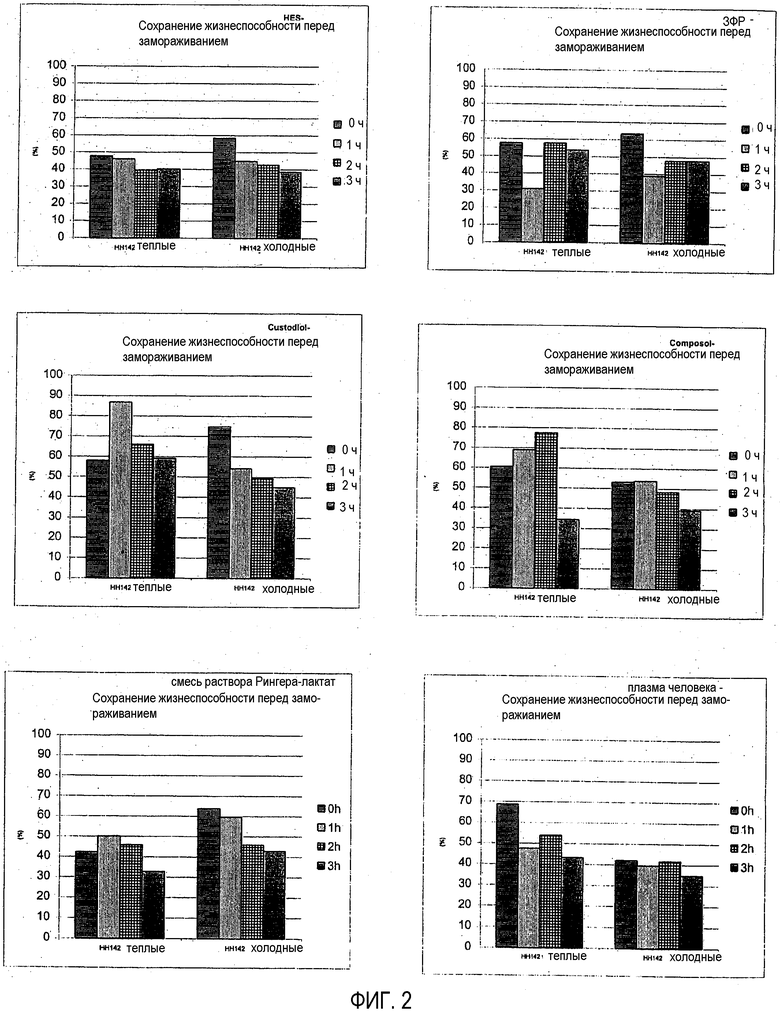
Фигура 2: Сохранение состояния сохранившихся клеток (перед криоконсервацией) в зависимости от времени хранения, используемой среды для хранения и температуры хранения, см. фигуру 1;
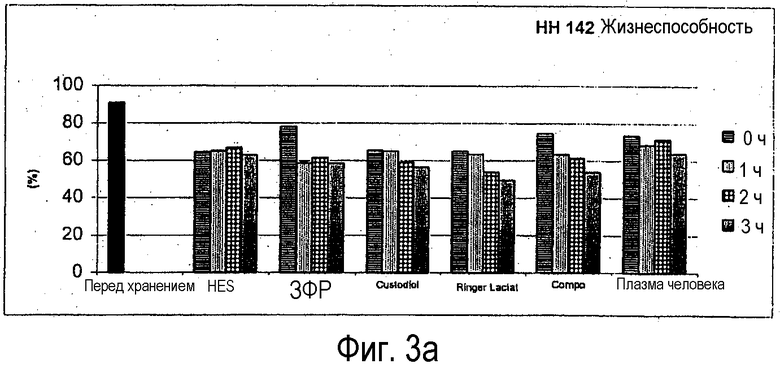
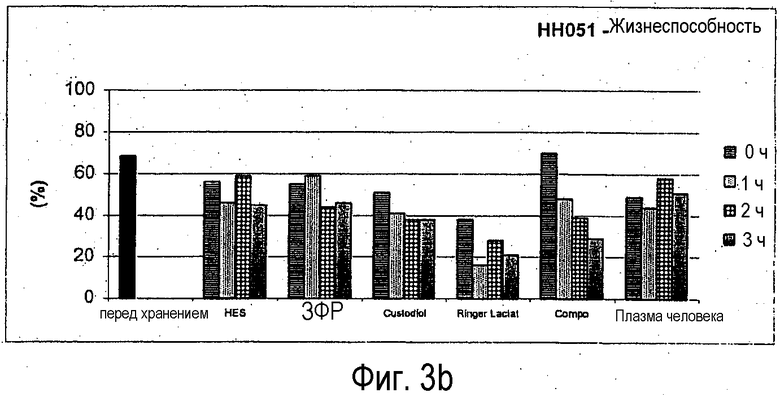
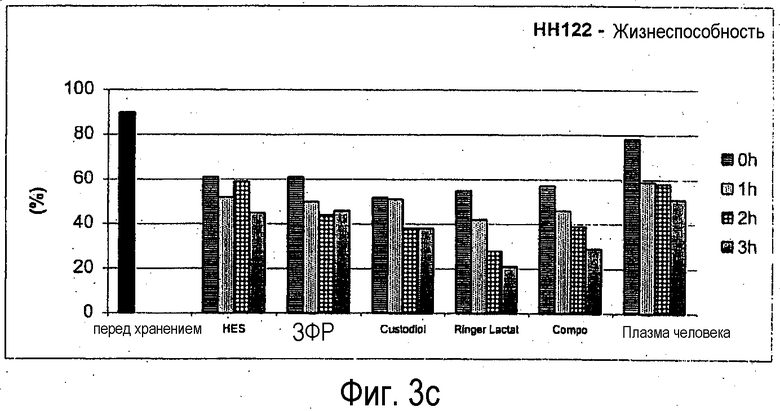
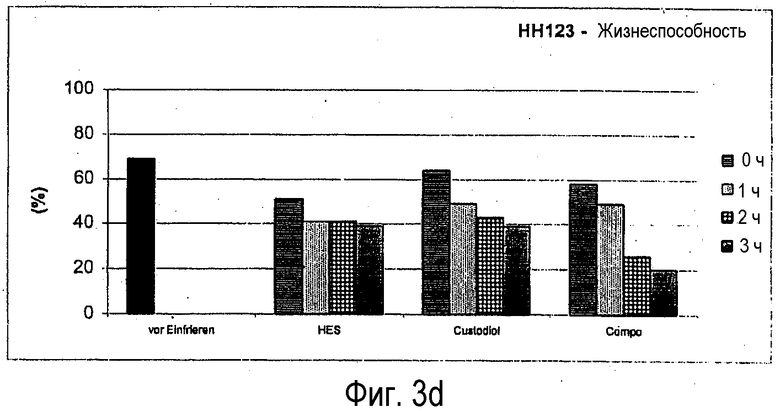
Фигура 3: Жизнеспособность сохранившихся клеток (после криоконсервации) в зависимости от времени хранения, используемой среды для хранения и температуры хранения, см. фигуру 1;
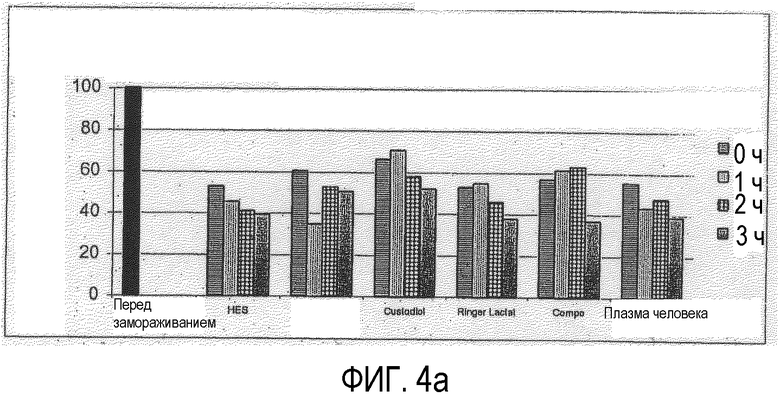
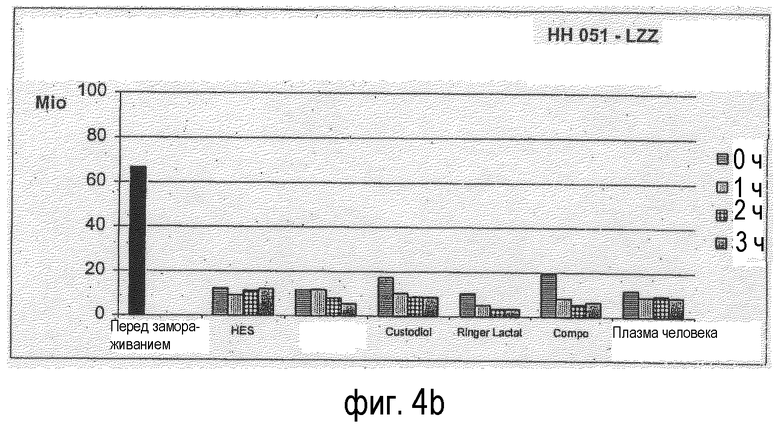
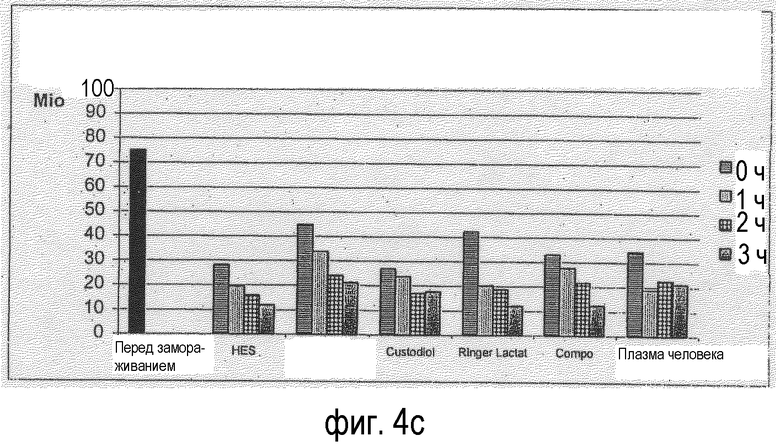
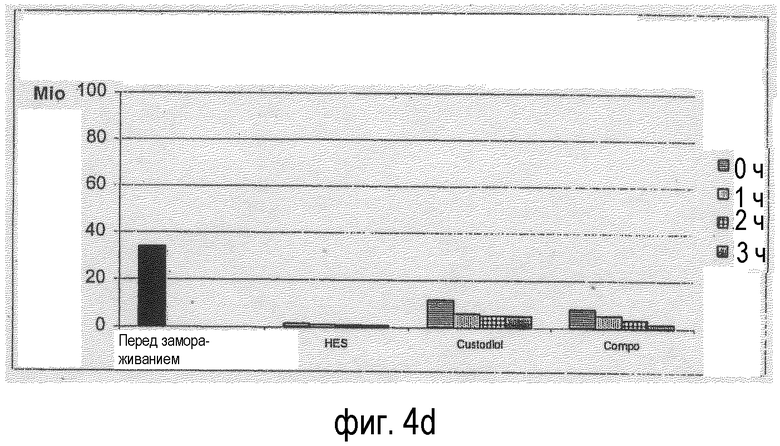
Фигура 4: Количество живых клеток (LZZ), сохранившихся (после криоконсервации) в зависимости от времени хранения и используемой среды для хранения, см. фигуру 1;
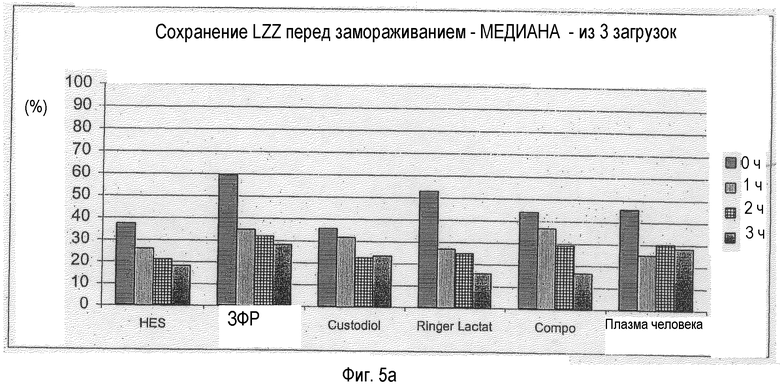
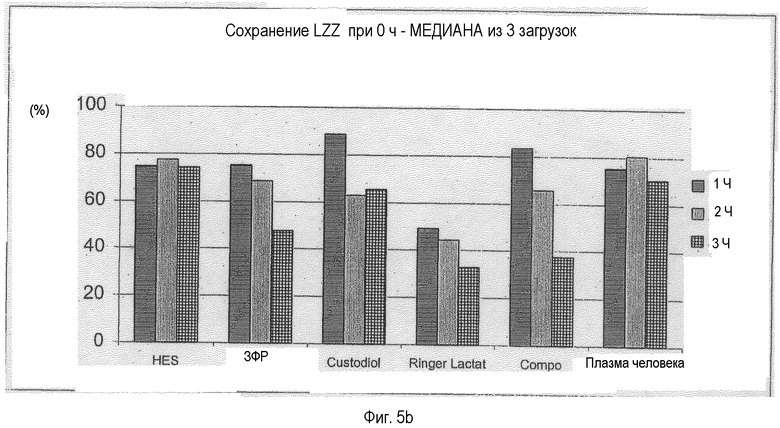
Фигура 5: Количество живых клеток (LZZ), сохранившихся (перед криоконсервацией) в зависимости от времени хранения и используемой среды для хранения, медиана из трех отдельных препаратов клеток (загрузок); см. фигуру 1:
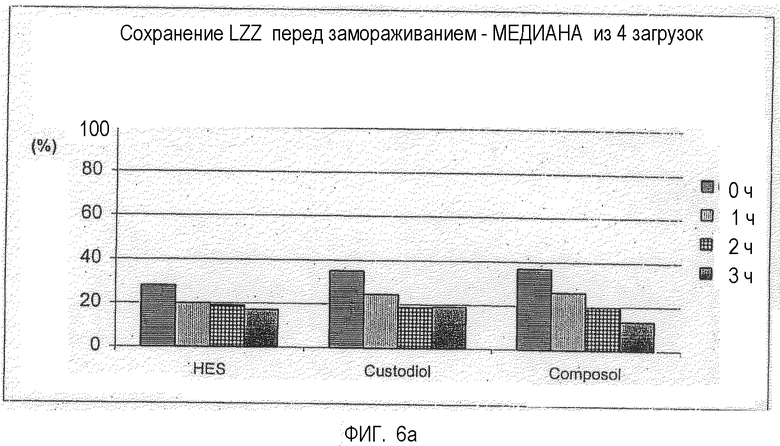
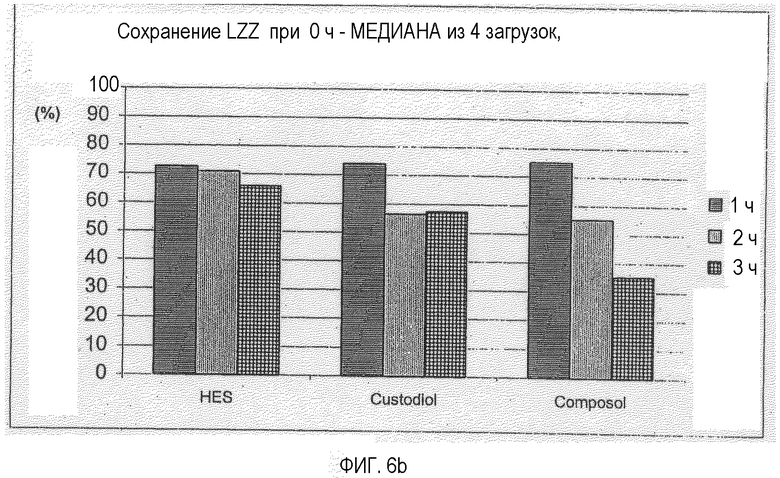
Фигура 6: Количество живых клеток (LZZ), сохранившихся (перед криоконсервацией) в зависимости от времени хранения и используемой среды для хранения, медиана из четырех отдельных препаратов клеток (загрузок); см. фигуру 1;
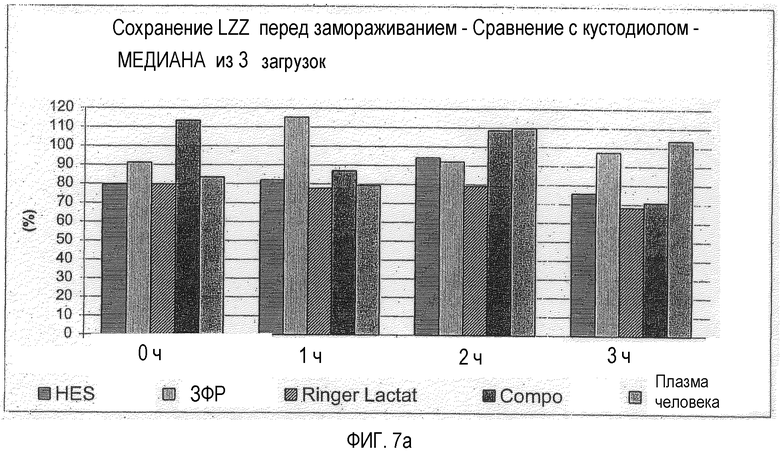
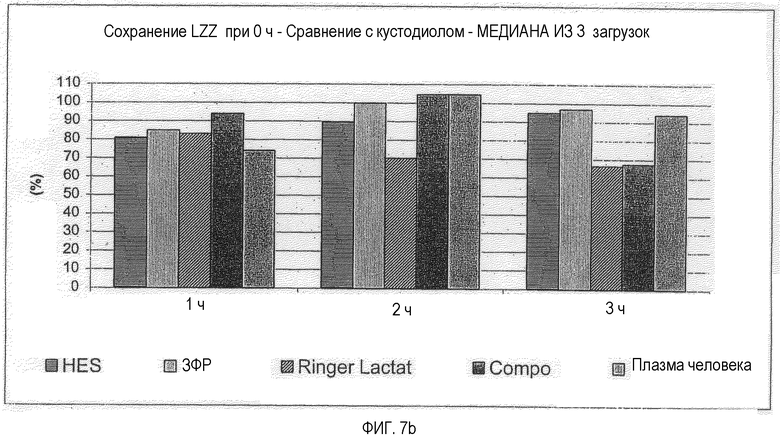
Фигура 7 А-С: Сохранения состояния, количество живых клеток (LZZ), сохранившихся (перед криоконсервацией) в зависимости от времени хранения и используемой среды для хранения, медиана из трех отдельных препаратов клеток (загрузок); фигура 7С: Сравнение с Custodiol (=100%), среднее значение из четырех периодов хранения, медиана из 3 отдельных препаратов клеток (загрузок), см. фигуру 1.
Пример
Используют криоконсервированные клетки печени из специальных криопакетов/криопробирок. Поскольку количество имеющихся в наличии криопробирок из одного отдельного препарата клеток было недостаточным для объема этого исследования, их используют только для сравнения результатов. Все рабочие стадии проводят при асептических условиях. Клеточную суспензию полностью оттаивают (размораживают) перед добавлением клеточной среды. Оттаивание криопробирок происходит во времени независимо от оттаивания пакета. Клеточную среду медленно добавляют к загруженным клеткам.
Для получения сравнимых результатов различные опыты проводятся параллельно по меньшей мере двумя, в случае необходимости тремя лицами.
Готовят следующие среды для оттаивания:
Среда 1: Custodiol® (Сравнительный пример).
Среда 2: Гидроксиэтилкрахмал (HES) + 1 г/л глюкоза + 4% ЧСА в соответствии с данным изобретением).
Среда 3: Рингер-лактат + 1 г/л глюкоза + 4% ЧСА (в соответствии с данным изобретением).
Среда 4: Composol® + 1 г/л глюкозы + 4% ЧСА (в соответствии с данным изобретением).
Среда 5: Забуференный фосфатом солевой раствор (ЗФР) + 1 г/л глюкозы + 4% ЧСА (в соответствии с данным изобретением).
Среда 6: Плазма крови человека (Сравнительный пример).
На один проход (один оттаянный пакет) требуется приблизительно по 50 мл клеточной среды. Плазму крови оттаивают на теплой (37°С) водяной бане.
В трех опытах среды поддерживают в теплой (37°С) водяной бане при постоянной температуре (= «теплые»). В 2 опытах клеточные среды охлаждают в холодильнике в течение по меньшей мере 15 мин (= «холодные»).
Готовят шесть пробирок на 50 мл с соответствующими этикетками и выдерживают их при комнатной температуре.
В «теплых» опытах центрифугируют в течение 5 мин при 18°С и 50 g, а в «холодных» опытах центрифугируют в течение 5 мин при 4°С и 50 g.
Криопакет осторожно вынимают из алюминиевой кассеты. Криосуспензию оттаивают 2-5 мин при постоянном качании, пока наблюдаются кристаллы льда. Весь процесс продолжается не более 5 мин.
Желтую крышку удаляют с пакета и перегородку протыкают прокалывающим шипом Benjamix. К Benjamix криопакета подсоединяют шприц на 60 мл и извлекают 60 мл клеточной суспензии.
По 10 мл клеточной суспензии испытывают в шести подготовленных пробирках. К ним добавляют медленно по 40 мл соответствующих клеточных сред. Весь этот процесс длится не более 5 мин.
После центрифугирования происходит рост клеток. Супернатанты отсасывают при помощи пастеровской пипетки. Осадки клеток полностью ресуспендируют осторожным качанием в 5 мл клеточной среды.
Производят подсчет клеток в отношении количества и жизнеспособности и согласно каждому подсчету клеток закладывают одну культуру клеток печени.
Для общей продолжительности хранения в течение 3 ч в каждом случае после 60 мин повторяют обе последние описанные стадии.
Используют только клетки печени с жизнеспособностью большей, чем 40%, перед криоконсервированием. Этот опыт повторяют по меньшей мере 3 раза с различными отдельными препаратами клеток (загрузками). При этом на одну загрузку оттаивают по меньшей мере 1 пакет. Для сравнения приводят результаты оттаивания криопробирок используемых загрузок.
Четыре отдельных препарата клеток (загрузок) используют в отношении влияния раствора для оттаивания. Результаты испытывают в отношении параметров жизнеспособности и количества живых клеток (LZZ) после оттаивания, а также жизнеспособности и сохранения количества живых клеток в суспензии. Температуру среды и температуру для центрифугирования устанавливают в случае трансплантатов клеток на 4°С. Опыт с загрузкой НН142 проводят один раз в «теплых» условиях и затем повторяют в «холодных» условиях (см. фигуру 1 и фигуру 2). Для дополнительного анализа берут средние величины обоих опытов и обозначают как НН142.
Отдельные результаты представлены на фигурах 3 и 4.
Для обеспечения независимого от загрузки анализа определяют параметр сохранения количества живых клеток при хранении в испытуемых растворах. Он относится к двум различным исходным пунктам. Во-первых, сохранение относится к количеству живых клеток перед замораживанием (фигура 5а). Во-вторых, сохранение относится к количеству живых клеток после промывания (час 0 в конкретной среде для хранения) (фигура 5b). Для сравнения пяти растворов рассчитывают показатели медианы для указанных параметров из трех испытанных загрузок и представляют графически на фигуре 5.
Для лучшего анализа представленных результатов выполняют следующее приближение. Параметр сохранения замороженных LZZ в случае Custodiol® брали за 100%. Для испытанных пяти исходных смесей (сравнительный пример/примеры в соответствии с данным изобретением) рассчитывают процентное отклонение этих параметров в сравнении с Custodiol® (см. фигуру 7а и фигуру 7b).
Непосредственно после промывания клеток три из этих растворов (ЗФР, Composol ® и HES) обнаруживают сравнимое (совпадение более 80%) с Custodiol® в отношении этого параметра сохранение LZZ. При этом Composol® показал даже лучшие результаты, чем Custodiol® (совпадение более 100%). В то время как после 1 ч ЗФР обнаруживал наилучшие результаты, Composol® и плазма человека после двух часов показали опять приблизительно на 10% лучшие результаты медиан, чем Custodiol®.
Для дополнительного сравнения проводят дополнительный анализ. Для каждого раствора рассчитывают среднюю величину из всех 4 временных точек (час 0-3, фигура 7с).
Независимо от временного хода этого опыта HES и Рингер-лактат показали приблизительно 20%-ную потерю LZZ в сравнении с Custodiol®, причем ЗФР, Composol® и плазма человека показали сравнимые (отклонение менее 10%) результаты в сравнении с Custodiol®.
| название | год | авторы | номер документа |
|---|---|---|---|
| Состав криоконсерванта для длительного хранения первичных кератиноцитов | 2019 |
|
RU2731065C1 |
| СПОСОБ ПОЛУЧЕНИЯ КЛЕТОК ИЗ ЗУБНОЙ ПУЛЬПЫ | 2019 |
|
RU2795621C2 |
| Способ оптимизации криоконсервации овариальной ткани для долгосрочного хранения | 2022 |
|
RU2794963C1 |
| КОМПОЗИЦИЯ И СПОСОБЫ КРИОКОНСЕРВАЦИИ КЛЕТОК HUTC | 2017 |
|
RU2748057C2 |
| ИНЪЕЦИРУЕМАЯ КОНСЕРВИРУЮЩАЯ СРЕДА ДЛЯ КОНСЕРВАЦИИ КЛЕТОК ПЛАЦЕНТАРНОЙ КРОВИ, КОСТНОГО МОЗГА И ПЕРИФЕРИЧЕСКОЙ КРОВИ | 2016 |
|
RU2727643C2 |
| КОМПОЗИЦИИ И СПОСОБЫ КРИОКОНСЕРВАЦИИ КЛЕТОК | 2021 |
|
RU2840854C1 |
| ЛЕЧЕНИЕ РАКА, КОМБИНИРУЮЩЕЕ ЛИМФОИСТОЩАЮЩЕЕ ВЕЩЕСТВО С ЦТЛ И ЦИТОКИНАМИ | 2007 |
|
RU2447900C2 |
| КОМБИНИРОВАННЫЙ КРИОПРОТЕКТОР "ДИМЕТИЛСУЛЬФОКСИД/РЕОПОЛИГЛЮКИН" ДЛЯ КРИОКОНСЕРВАЦИИ СТВОЛОВЫХ КЛЕТОК И СПОСОБ ИХ КРИОКОНСЕРВАЦИИ ДЛЯ КЛИНИЧЕСКОГО ПРИМЕНЕНИЯ | 2014 |
|
RU2563117C1 |
| УЛУЧШЕННАЯ КЛЕТОЧНАЯ КОМПОЗИЦИЯ И СПОСОБЫ ЕЕ ПОЛУЧЕНИЯ | 2009 |
|
RU2563518C2 |
| КОНЦЕНТРИРОВАННЫЙ РАСТВОР ДЛЯ ХРАНЕНИЯ В КРИОГЕННЫХ УСЛОВИЯХ (ВАРИАНТЫ), РАСТВОР ДЛЯ ХРАНЕНИЯ В КРИОГЕННЫХ УСЛОВИЯХ, СПОСОБ КРИОГЕННОГО ХРАНЕНИЯ КЛЕТОК (ВАРИАНТЫ), СПОСОБ КРИОГЕННОГО ХРАНЕНИЯ И РЕГЕНЕРАЦИИ ЖИЗНЕСПОСОБНЫХ КЛЕТОК, СПОСОБ КРИОГЕННОГО ХРАНЕНИЯ, РЕГЕНЕРАЦИИ И ТЕРАПЕВТИЧЕСКОГО ПРИМЕНЕНИЯ КЛЕТОК | 1996 |
|
RU2146088C1 |
Предложены: способ кратковременного хранения клеток гепатоцитов, в частности клеток человека клеточная среда для их хранения и применение таких клеточных сред. Изобретение отличается тем, что во время хранения жизнеспособность клеток сохраняется. 3 н. и 14 з.п. ф-лы, 7 ил.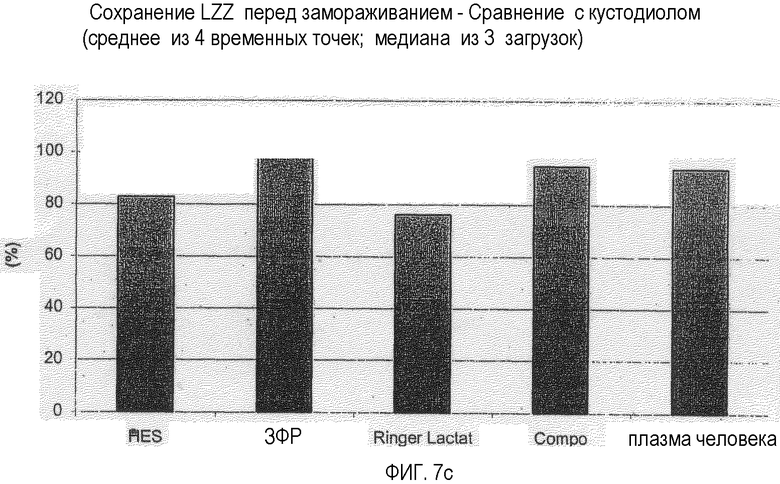
1. Способ кратковременного хранения клеток гепатоцитов, в котором эти клетки помещают в жидкую клеточную среду, содержащую
a) солевой раствор, выбранный из
солевого раствора, содержащего, в частности, хлорид натрия, глюконат натрия, ацетат натрия, хлорид калия, хлорид магния и цитрат натрия,
раствора Рингера-лактата,
забуференного фосфатом солевого раствора (ЗФР),
и/или водный раствор высокомолекулярного сахара, в частности гидроксиэтилкрахмала,
b) глюкозу и
c) сывороточный альбумин и/или плазму крови,
и хранят в этой клеточной среде.
2. Способ по п.1, в котором эти клетки являются криоконсервированными клетками, и их оттаивают (размораживают) и после оттаивания промывают в указанной клеточной среде, отделяют от клеточной среды и затем помещают в свежую клеточную среду для хранения.
3. Способ по одному из предыдущих пунктов, в котором эта клеточная среда имеет температуру 2-40°С.
4. Способ по п.1, где в случае этих клеток речь идет о клетках млекопитающих.
5. Способ по п.1, где в случае этих клеток речь идет о клетках человека.
6. Способ по п.1, где в случае этих клеток речь идет о клетках для терапевтического применения.
7. Способ по п.1, где речь идет о клетках для культивирования in vitro.
8. Применение клеточной среды по п.1, отличающееся кратковременным хранением клеток гепатоцитов, в частности, после способа по одному из пп.1-7.
9. Клеточная среда для кратковременного хранения клеток гепатоцитов, причем эта клеточная среда содержит
a) хлорид натрия, глюконат натрия, ацетат натрия, хлорид калия, хлорид магния и цитрат натрия,
b) глюкозу и
c) сывороточный альбумин и/или плазму крови,
растворенные в воде.
10. Клеточная среда по п.9, в которой сывороточный альбумин является сывороточным альбумином человека.
11. Клеточная среда по одному из пп.9 или 10, в которой плазма крови является плазмой крови человека.
12. Клеточная среда по п.9, причем эта клеточная среда содержит
0,45-0,60 мас.% хлорида натрия,
0,45-0,55 мас.% глюконата натрия,
0,20-0,25 мас.% ацетата натрия,
0,03-0,04 мас.% хлорида калия,
0,025-0,035 мас.% гексагидрата хлорида магния и
0,31-0,33 мас.% цитрата натрия.
13. Клеточная среда по п.9, причем эта клеточная среда содержит 0,01-0,5 мас.%, предпочтительно 0,1-0,2 мас.% глюкозы.
14. Клеточная среда по п.9, причем эта клеточная среда содержит 0,5-50 мас.%, предпочтительно 3-5 мас.% сывороточного альбумина.
15. Клеточная среда по п.9, причем эта клеточная среда содержит 0,5-50 мас.%, предпочтительно 3-5 мас.% плазмы крови.
16. Клеточная среда по п.9, причем эта клеточная среда имеет показатель рН 6,4-8, предпочтительно 7,0-7,4.
17. Клеточная среда по п.9, содержащая по меньшей мере один дополнительный компонент, выбранный из аминокислот, гормонов, витаминов, провитаминов и антиапоптотических активных веществ.
| Импульсная капельница | 1983 |
|
SU1149900A1 |
| KR 20010029692 A, 06.04.2001 реферат [он-лайн] [найдено 2009-10-21] | |||
| Найдено из базы данных Esp@cenet | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| JP 2002335954 А, 26.11.2002 реферат [он-лайн] [найдено 2009-10-21] | |||
| Найдено из базы данных PAJ | |||
| КОНСЕРВИРУЮЩИЙ РАСТВОР "Б-2" ДЛЯ ТРАНСПЛАНТАТОВ | 1997 |
|
RU2140152C1 |
Авторы
Даты
2010-08-20—Публикация
2006-06-30—Подача