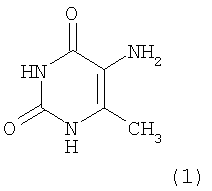
Изобретение относится к химико-фармацевтической промышленности, а именно к средству, представляющему собой 5-амино-6-метилурацилу (1) формулы:
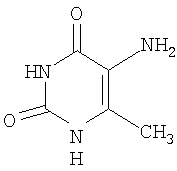
проявляющему антиоксидантную активность.
Антиоксидантная активность соединения (1) в литературе не описана. Наиболее близким аналогом по химической структуре является 5-гидрокси-6-метилурацил (оксиметилурацил):
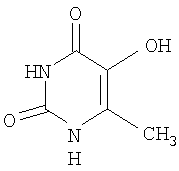
Известно, что 5-гидрокси-6-метилурацил оказывает антиоксидантное действие в модельных системах in vitro, в условиях острой гипоксии, моделируемой введением нитрита натрия, а также на моделях экспериментальных интоксикаций дихлорэтаном, смесью полихлорированных бифенилов (совтол), карбофосом, тетрахлорметаном [1-6]. Недостатком 5-гидрокси-6-метилурацила является низкая растворимость в воде и органических растворителях.
Задача, на решение которой направлено заявленное техническое решение, заключается в расширении арсенала фармакологических препаратов, обладающих низкой токсичностью и высокой антиоксидантной активностью в условиях гипоксии и при химической интоксикации, и упрощении способа получения соединения (1).
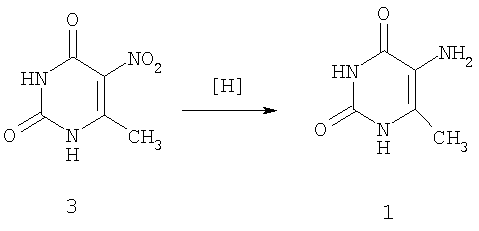
Описан способ получения соединения (1) нитрованием 6-метилурацила (2) избытком HNO3 в присутствии H2SO4 с последующим восстановлением полученного 5-нитро-6-метилурацила (3) водородом при 5 атм в присутствии никеля Ренея в дистиллированной воде [7].
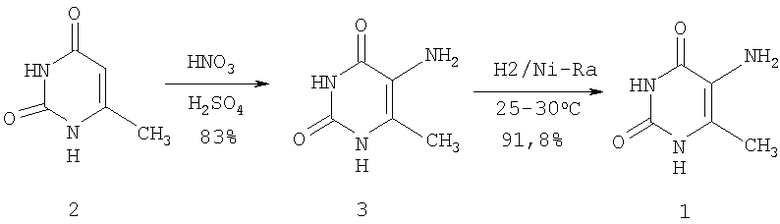
Общий выход соединения (1) по двум стадиям составляет 76,19%. Недостатком данного способа является техническая сложность проведения синтеза, заключающаяся в использовании специальной аппаратуры, газообразного водорода и высокого давления.
Известен способ получения соединения (1), заключающийся в том, что 5-нитро-6-метилурацил (3) в водной среде обрабатывают при 80-90°С Na2S2O4, затем кипятят 5 минут с углем, фильтруют и охлаждают [8]. Выход соединения (1) составляет 74,5%.
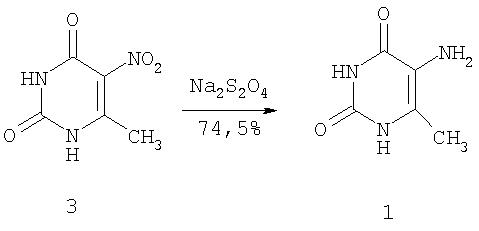
Данный способ не требует повышенного давления и специальной аппаратуры, недостатком его является низкий выход целевого продукта.
В заявленном техническом решении соединение (1) получают путем восстановления 5-нитро-6-метилурацила (3) гидразинсульфатом в присутствии никеля Ренея в этиловом спирте при температуре 70-80°С. Выход целевого продукта составляет 95%.
Токсичность соединения (1) при однократном введении в желудок определена на мышах и крысах. Соединение (1) в интервале доз от 1 до 10 г/кг не вызывает видимых признаков интоксикации и гибели животных в течение 14 суток наблюдения. В соответствии с ГОСТом 12.1.007-76 соединение (1) при введении в желудок относится к малоопасным веществам (таблица 1) [9].
При внутрибрюшинном введении мышам соединения (1) доза 2,8 г/кг вызывает 50% гибель животных, по классификации токсичности веществ соединение (1) практически нетоксично [10].
Изучение антиоксидантной активности (АОА) соединения (1) и 5-гидрокси-6-метилурацила в условиях in vitro проводили с использованием 20%-ного гомогената печени крыс в качестве субстрата перекисного окисления липидов (ПОЛ). Индукцию ПОЛ вызывали введением в 20%-ный гомогенат печени системы следующего состава: 0,5 мМ аскорбата + 6 мкМ соли Мора. Активность ПОЛ исследовали биохимическим методом по концентрации веществ, реагирующих с 2-тиобарбитуровой кислотой (ТБК-РП) (ТБК-реагирующие продукты) [11]. АОА исследуемых соединений рассчитывали по формуле [12]:
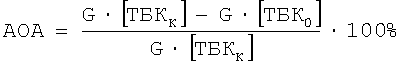
 - прирост ТБК-РП в контрольной пробе во время инкубации;
- прирост ТБК-РП в контрольной пробе во время инкубации;
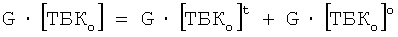 - прирост ТБК-РП в опытной пробе во время инкубации;
- прирост ТБК-РП в опытной пробе во время инкубации;
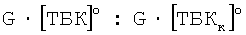 - оптическая плотность, измеренная до инкубации;
- оптическая плотность, измеренная до инкубации;
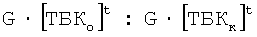 - оптическая плотность, измеренная после инкубации.
- оптическая плотность, измеренная после инкубации.
Результаты экспериментов представлены в таблице 2.
В условиях автоокисления добавление соединения (1) и 5-гидрокси-6-метилурацила в инкубационную среду в первые 3 часа эксперимента подавляло накопление ТБК-РП примерно в одинаковой степени, через 4 часа соединение (1) было менее эффективно.
АОА соединения (1) при индукции ПОЛ аскорбатом через 1 час инкубации была более выражена по сравнению с 5-гидрокси-6-метилурацилом. Через 3 часа инкубации это различие в АОА двух препаратов было максимальным и сохранялось спустя 4 часа окисления.
Таким образом, АОА соединения (1) при индуцированном ПОЛ была существенно выше, чем препарата сравнения - 5-гидрокси-6-метилурацила.
Антиоксидантная активность соединения (1) in vivo исследована на модели острой гемической гипоксии (ОГеГ) с определением содержания в органах мышей кетодиенов (КТД).
ОГеГ создавали путем подкожного введения мышам 4%-ного водного раствора нитрита натрия в дозе 100 мг/кг. Соединение (1) вводили опытным мышам однократно в брюшную полость в виде 0,25%-ных водно-твиновых растворов в дозе 100 мг/кг за 1 час до введения нитрита натрия. Контрольным животным вводили растворитель в аналогичном объеме. В качестве референтного препарата использовали 5-гидрокси-6-метилурацил, который применяли по схеме, аналогичной соединению (1) [3].
Содержание КТД в липидных экстрактах головного мозга и печени мышей определяли спектрофотометрическим методом [13, 14]. Тестирование проводили через 6 часов после введения нитрита натрия.
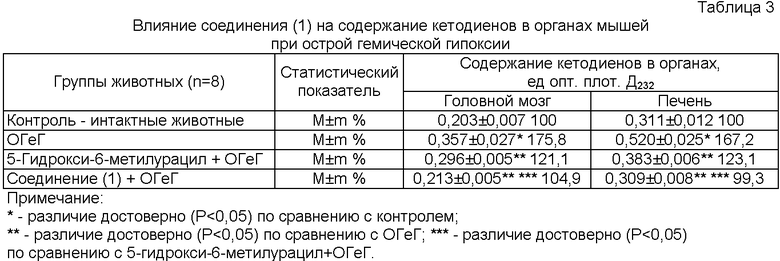
Результаты опытов представлены в таблице 3.
Введение животным нитрита натрия повышает содержание КТД в полушариях головного мозга и печени в 1,75 и 1,67 раза соответственно по сравнению с контролем, что свидетельствует о повышении активности ПОЛ в органах. В этих условиях соединение (1) и 5-гидрокси-6-метилурацил предупреждают накопление КТД, но в разной степени. 5-Гидрокси-6-метилурацил снижает повышенное гипоксией количество КТД в головном мозге на 54,7% и в печени на 44,1%. При применении соединения (1) количество КТД в органах опытных мышей практически не отличается от контроля. Выявлено статистически достоверное различие в содержание КТД в головном мозге и печени животных, получавших соединение (1) и 5-гидрокси-6-метилурацил.
Антиоксидантная активность соединения (1) исследована также на модели острого токсического гепатита, вызванного введением тетрахлорметана (ТХМ) крысам. ТХМ в виде 50%-ного раствора в оливковом масле вводили однократно в желудок в дозе 0,2 мл/кг [6]. Антиоксидантную эффективность соединения (1) (в дозе 50 мг/кг) и препарата сравнения - 5-гидрокси-6-метиолурацила (в дозе 50 мг/кг) оценивали по изменению содержания ТБК-РП в печени через 48 часов после введения крысам ТХМ. Содержание ТБК-РП продуктов в печени крыс при интоксикации ТХМ определяли по методу Стальная И.Д., Гурашвили Т.Г. [11].
Результаты проведенного эксперимента представлены в таблице 4.
Введение животным ТХМ повышает содержание ТБК-РП в печени крыс более чем в 2 раза по сравнению с контролем. Однократное введение соединения (1) и 5-гидрокси-6-метилурацила снижало количество ТБК-РП в печени отравленных крыс соответственно в 1,9 раза (Р<0,001) и 1,69 раза (Р<0,05). Соединение (1) эффективнее 5-гидрокси-6-метилурацила: различие в показателях между группами крыс 5-гидрокси-6-метилурацил + ТХМ и соединение (1) + ТХМ статистически достоверно (Р<0,05).
Таким образом, соединение (1) обладает более высокой антиоксидантной активностью и низкой токсичностью при внутрибрюшинном и внутрижелудочном введении, чем препарат сравнения - 5-гидрокси-6-метилурацил.
Сущность технического решения поясняется следующими примерами.
Пример 1. Синтез соединения (1).
В двугорлой колбе, снабженной обратным холодильником, смешивали 0,029 моль (5 г) 5-нитро-6-метилурацила, 200 мл этилового спирта и 0,087 моль (11,32 г) гидразинсульфата. Смесь нагревали до 70-80°С и небольшими порциями вносили спиртовую суспензию никеля Ренея. Начало реакции замечали по выделению азота. Каждую следующую порцию катализатора (никеля Ренея) прибавляли после того, как выделение газа уменьшалось. Ход реакции контролировали методом тонкослойной хроматографии (элюент хлороформ-метанол, 8:2). По окончании реакции добавляли остаток катализатора для полного разложения гидразинсульфата. Горячий раствор отфильтровывали от катализатора, фильтрат охлаждали. Выпавшие кристаллы отфильтровывали, перекристаллизовывали из этилового спирта. Выход соединения (1): 3,89 г (95%).
Т.пл. 253-255°С. ИК спектр, υ, см-1: 1000, 1080 (ωC=C; 1180 (=N-); 1276, 1296 (υC=O); 1624, 1648, 1712 (υC=C, υC=O, =N-C=O); 2920, 3400 (-NH2). Спектр ЯМР 1H (DMSO-d6, δ м.д.): 2.25 (с, 3H, CH3C6); 3.7 (уш. с, 2H, NH2); 10.2 (c, 1H, N1H); 10.95 (с, 1H, N3H). Спектр ЯМР 13C (DMSO-d6, δ м.д.): 13.93 (СН3С6), 117.77 (С5), 127.69 (С6); 149.40 (С2=O); 161.29 (С4=O). Масс-спектр, m/z: 140 (М-Н)-, 142 (МН)+. Найдено, %: С 43.00; Н 5.09; N 29.35. С5Н7N3O2. Вычислено, %: С 42.55; Н 4.99; N 29.77.
Пример 2. Изучение острой токсичности соединения (1).
а) Острую токсичность соединения (1) исследовали на мышах и крысах. Группе животных (n=10) однократно в желудок через зонд вводили соединение (1) в дозах 5 г/кг, 7,5 г/кг, 10 г/кг на 2%-ной крахмальной слизи. Контрольные животные получали крахмальную слизь. Наблюдения за животными вели в течение 14 суток. Отсутствие гибели животных при выше приведенных дозах свидетельствует о малой токсичности соединения (1) в соответствии с ГОСТом 12.1.007-76 [9]. Доза соединения (1), вызывающая 50% гибель: для мышей - более 10 г/кг, для крыс - более 6 г/кг.
б) Токсичность при однократном внутрибрюшинном введении соединения (1) в дозах 1,5 г/кг, 2 г/кг, 3 г/кг изучали на мышах и крысах. Статистическая группа состояла из 10 животных. Влияние соединения (1) наблюдали в течение 14 суток после введения, оценивали по смертельному эффекту и данные обрабатывали с использованием пробит-анализа. В результате исследования определена доза соединения (1), вызывающая 50% гибель: для мышей - 2,8 г/кг, для крыс - 2,3 г/кг. У препарата сравнения - 5-гидрокси-6-метилурацила доза, вызывающая 50% гибель животных: для мышей - 1,9 г/кг, для крыс - 1,7 г/кг (таблица 1).
Пример 3. Изучение антиоксидантной активности соединения (1) in vitro.
20%-ный гомогенат печени крыс подвергали спонтанному и индуцированному окислению при 37°С. Индукцию ПОЛ 0,05 мл гомогената печени крыс вызывали внесением системы, содержащей 0,5 мМ аскорбата + 6 мкМ соли Мора. Уровень активности ПОЛ в гомогенате печени крыс определяли по концентрации веществ, реагирующих с ТБК.
Исследуемые препараты - соединение (1) и 5-гидрокси-6-метилурацил - растворяли в абсолютном спирте, вносили в систему в одинаковой концентрации 100 мкМ и спектрофотометрически определяли содержание ТБК-РП.
АОА исследуемых соединений в каждой серии опытов и для каждой длительности периода окисления 1 час, 3 часа и 4 часа рассчитывали по формуле, результат выражали в процентах:
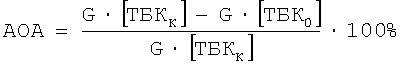
Вычисляли среднеарифметическое значение для 5 опытов (таблица 5).
Пример 4. Изучение антиоксидантной активности соединения (1) на модели острой гемической гипоксии (ОГеГ).
Для изучения АОА использованы мыши, группы из 8 животных. Модель ОГеГ создавали путем подкожного введения мышам 4%-ного водного раствора нитрита натрия в дозе 100 мг/кг [14]. Соединение (1) вводили опытным мышам однократно в брюшную полость в виде 0,25%-ных водно-твиновых растворов в дозе 100 мг/кг за 1 час до введения нитрита натрия. Контрольным животным вводили 0,25%-ный водно-твиновый раствор в аналогичном объеме. В качестве референтного препарата использовали 5-гидрокси-6-метилурацил, который применяли по схеме, аналогичной соединению (1). Антиоксидантную активность соединения (1) оценивали по содержанию КТД в органах (головном мозге, печени) мышей (таблица 3).
Пример 5. Изучение антиоксидантной активности соединения (1) на модели острого токсического гепатита.
Острый токсический гепатит у крыс вызывали однократным внутрижелудочным введением 50%-ного раствора ТХМ в оливковом масле в дозе 0,2 мл/кг. Соединение (1) (в дозе 50 мг/кг) и препарат сравнения - 5-гидрокси-6-метилурацил - (в дозе 50 мг/кг) вводили однократно в брюшную полость в виде 0,25%-ного водно-твинового раствора за 1 час до введения ТХМ. Антиоксидантную активность соединения (1) и 5-гидрокси-6-метилурацила оценивали по содержанию ТБК-РП в печени крыс через 48 часов после введения ТХМ (таблица 4).
Таким образом, соединение (1) обладает более высокой антиоксидантной активностью и низкой токсичностью при введении в желудок и внутрибрюшинно.
Литература
1. Мышкин В.А., Хайбуллина З.Г., Башкатов С.А. Влияние метилурацила и оксиметацила на свободнорадикальное окисление в модельных системах // Бюллетень экспериментальной биологии и медицины. - 1995. - №8. - С.142-144.
2. Мышкин В.А., Срубилин Д.В., Вакарица А.Ф. Эффективность и механизм действия оксиметилурацила при экспериментальной нитритной интоксикации // Здравоохранение Башкортостана. - 1997. - №3. - С.3-7.
3. Срубилин Д.В. Эффективность и механизм действия производных пиримидина при экспериментальной нитритной интоксикации // Дисс. … к.м.н. - Уфа. - 1994. - 188 с.
4. Мышкин В.А., Бакиров А.Б. Оксиметилурацил (очерки экспериментальной фармакологии). - Уфа, 2001. - 218 с.
5. Мышкин В.А., Башкатов С.А., Вакарица А.Ф. Влияние оксиметацила и атропина на свободнорадиальное окисление липидов и состояние мембран у крыс при отравлении карбофосом // Патофизиология и экспериментальная терапия. - 1993. - №2. - С.47-49.
6. Хайбуллина З.Г. Антиокислительная активность производных пиримидина и бензимидазола в биохимическом механизме их антитоксического действия //Дисс. … к.б.н. - Уфа. - 1994. - 165 с.
7. Авт. св. СССР 130044, 15.07.1960. / Адамович А.И., Витенберг А.Г. Способ получения 5-амино-4-метилурацила - (Р.Ж.Хим., 1961, 22Л223).
8. Robins R.K., Furcht F.W., Grauer A.D. and Jones J.W. Potential Purine Antagonists. II. Synthesis of Some 7- and 5,7-Substituted Pyrazolo [4,3-d]pyrimidines//Journal of the American Chemical Society. - 1956. - V.78. - P.2418-2422.
9. ГОСТ 12.1.007-76. Вредные вещества. Классификация и общие требования безопасности. Государственный комитет стандартов. - М.: 1976.
10. Измеров Н.Ф., Саноцкий И.В., Сидоров К.К. Параметры токсикометрии промышленных ядов при однократном воздействии. Справочник. - М.: Медицина, 1977. - 240 с.
11. Стальная И.Д., Гурашвили Т.Г. Метод определения малонового диальдегида с помощью тиобарбитуровой кислоты. // Современные методы в биохимии. - М. - 1977. - С.66-68.
12. Клебанов Г.И., Бабенкова И.В., Теселкин Ю.А. Оценка антиокислительной активности плазмы крови с применением желточных липопротеидов // Лаб. дело. - 1988. - №5. - С.59-61.
13. May Н.Е., Roed D.J. A kinetic assay of TPNH-dependent microsomal lipid peroxidation by changes in difference spectra. // Anal. Biochem. - 1973. - V.55. - №2. - P.331-337.
14. Tappal A.K. Lipid peroxidation damage to cell components // Fed. Proc. - V.32. - №8. - P.1870-1874.
15. Воронина Т.А. Экспериментальная характеристика противогипоксических свойств ноотропных препаратов // Фармакологическая коррекция гипоксических состояний. - М.: 1989. - С.125-132.
| название | год | авторы | номер документа |
|---|---|---|---|
| 6-МЕТИЛ-5-МОРФОЛИНОМЕТИЛ-1-(ТИЕТАН-3-ИЛ)ПИРИМИДИН-2,4(1Н,3Н)-ДИОН, ПРОЯВЛЯЮЩИЙ АНТИОКСИДАНТНУЮ АКТИВНОСТЬ | 2013 |
|
RU2539302C1 |
| СРЕДСТВО НА ОСНОВЕ ПРИРОДНЫХ ФОСФОЛИПИДОВ | 2008 |
|
RU2367443C1 |
| БИЦИКЛИЧЕСКИЕ ПИРИМИДИНЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ-АКТИВАТОРЫ АНТИОКСИДАНТНОЙ ПРОГРАММЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЦИТОПРОТЕКТОРОВ | 2014 |
|
RU2545758C1 |
| СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ ОНКОЛОГИЧЕСКОГО И НЕОНКОЛОГИЧЕСКОГО ПРОФИЛЯ И ДЛЯ КОРРЕКЦИИ НАРУШЕНИЙ ГОМЕОСТАЗА | 2001 |
|
RU2208446C2 |
| Комплексное соединение 5-гидрокси-6-метилурацила с N-ацетилцистеином, проявляющее антигипоксическую активность, и способ его получения | 2020 |
|
RU2751632C1 |
| 1,3- ДИ(3-ПИПЕРИДИНО-2-ГИДРОКСИПРОПИЛ)-6-МЕТИЛУРАЦИЛ ДЛЯ ПОВЫШЕНИЯ СОХРАННОСТИ И ПРОДУКТИВНОСТИ ПТИЦ | 2006 |
|
RU2334745C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ЭНДОТЕЛИОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2017 |
|
RU2643605C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИОКСИДАНТНОЙ, ПРОТИВОВОСПАЛИТЕЛЬНОЙ, НЕЙРОПРОТЕКТОРНОЙ, ГИПОЛИПИДЕМИЧЕСКОЙ, ГИПОХОЛЕСТЕРИНЕМИЧЕСКОЙ, ГИПОГЛИКЕМИЧЕСКОЙ, ГЕПАТОПРОТЕКТОРНОЙ, ИММУНОСУПРЕССОРНОЙ АКТИВНОСТЯМИ | 2012 |
|
RU2487884C1 |
| Комплексное соединение 5-гидрокси-6-метилурацила с аскорбиновой кислотой, проявляющее антигипоксическую активность, и способ его получения | 2016 |
|
RU2612517C1 |
| КОМПЛЕКСНОЕ СОЕДИНЕНИЕ 1,3-БИС(2-ГИДРОКСИЭТИЛ)-5-ГИДРОКСИ-6-МЕТИЛУРАЦИЛА С ФУМАРОВОЙ КИСЛОТОЙ, ПРОЯВЛЯЮЩЕЕ АНТИГИПОКСИЧЕСКУЮ АКТИВНОСТЬ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2006 |
|
RU2330025C2 |
Изобретение относится к средству, представляющему собой 5-амино-6-метилурацил формулы (1), которое обладает антиоксидантной активностью, и способу его получения. Средство может быть использовано в медицине для получения лекарственного препарата, способного тормозить процессы перекисного окисления липидов и активировать восстановительные процессы при интоксикациях химическими веществами.
Способ получения 5-амино-6-метилурацила заключается в восстановлении 5-нитро-6-метилурацила гидразинсульфатом в среде растворителя - этилового спирта при температуре 70-80°С в присутствии никеля Ренея в качестве катализатора с последующим выделением продукта. Способ позволяет повысить выход продукта. 2 н.п. ф-лы, 5 табл.
1. Средство, представляющее собой 5-амино-6-метилурацил формулы:
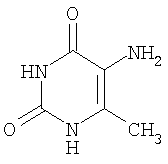
проявляющее антиоксидантную активность.
2. Способ получения 5-амино-6-метилурацила восстановлением 5-нитро-6-метилурацила в среде растворителя при повышенной температуре, с последующим выделением продукта, отличающийся тем, что в качестве восстановителя используют гидразинсульфат, в качестве растворителя - этиловый спирт и процесс ведут при температуре 70-80°С в присутствии катализатора, в качестве которого используют никель Ренея.
| Способ получения 5-амино-4-метилурацила | 1959 |
|
SU130044A1 |
| ФЕЛЬДМАН И.X | |||
| и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Mechenye Biol | |||
| Aktivn | |||
| Veshchestva | |||
| Sb | |||
| Водоотводчик | 1925 |
|
SU1962A1 |
| HAN PENG et al | |||
| Study on the catalytic reaction of methionine synthase | |||
| VII | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| Abstr | |||
| Способ закалки пил | 1915 |
|
SU140A1 |
| DE 4035599, 05.07.1992 | |||
| МИРЗОЯН | |||
Авторы
Даты
2010-09-10—Публикация
2008-04-03—Подача