Настоящее изобретение относится к производным (5Н-пиразоло[1,5-c][1,3]бензоксазин-5-ил)фенилметанона в качестве ингибиторов вирусной репликации вируса ВИЧ, способам их получения, а также фармацевтическим композициям, их применению в качестве лекарственных средств, и содержащим их диагностическим наборам. Настоящее изобретение относится также к комбинациям настоящих ингибиторов ВИЧ с другими антиретровирусными агентами. Кроме того, настоящее изобретение относится к применению указанных соединений в анализах в качестве эталонных соединений или в качестве реагентов. Соединения настоящего изобретения предназначены для предотвращения или лечения инфекции ВИЧ и для лечения СПИДа.
Число людей, живущих с ВИЧ/СПИДом, насчитывало в декабре 2004 приблизительно 40 миллионов, из которых более чем 37 миллионов являются взрослыми людьми и приблизительно 2,2 миллиона являются детьми в возрасте меньше 15 лет. Число людей, вновь инфицированных ВИЧ, только в 2004 увеличилось до 4,9 миллиона, тогда как 3,1 миллиона людей, заболевших СПИДом, в 2004 умерли. В современной химиотерапии этих людей, инфицированных ВИЧ/СПИДом, применяют ингибиторы вирусного слияния, а также ферменты обратной транскриптазы (RT) и протеазы. Ввиду появления штаммов ВИЧ, резистентных к современным ингибиторам генерации слияния, RT и протеазы, существует возрастающая потребность в разработке новых и улучшенных противовирусных средств с разными механизмами действия.
ЕР 1359147 относится к бензоксазинонам, в частности 1,4-дигидро-2Н-3,1-бензоксазин-2-онам или их стереоизомерным формам или смесям, или фармацевтически приемлемым солям, которые предназначены для применения в качестве ингибиторов обратной транскриптазы ВИЧ, содержащим их фармацевтическим композициям и диагностическим наборам, способам применения их для лечения вирусной инфекции или в качестве стандарта или реагента для анализа, способам их получения и промежуточным соединениям для их получения.
Orlov V.D. et al. (1991) описали замещенные 1,10b-дигидро-5Н-пиразоло[1,5-c]-1,3-бензоксазины, в частности (1,10b-дигидро-2-фенил-5Н-пиразоло[1,5-c]-1,3-бензоксазин-5-ил)фенилметаноны, обладающие потенциальной физиологической активностью.
ЕР 0563733 относится к применению известных 7-оксо-7Н-пиридо[1,2,3-de][1,4]бензоксазин-6-карбоновых кислот и их эфиров в качестве лекарственных средств, обладающих противовирусной активностью.
Задачей, лежащей в основе настоящего изобретения, является предоставление ингибиторов вирусной репликации вируса ВИЧ.
Настоящее изобретение относится к соединениям, имеющим формулу (I)
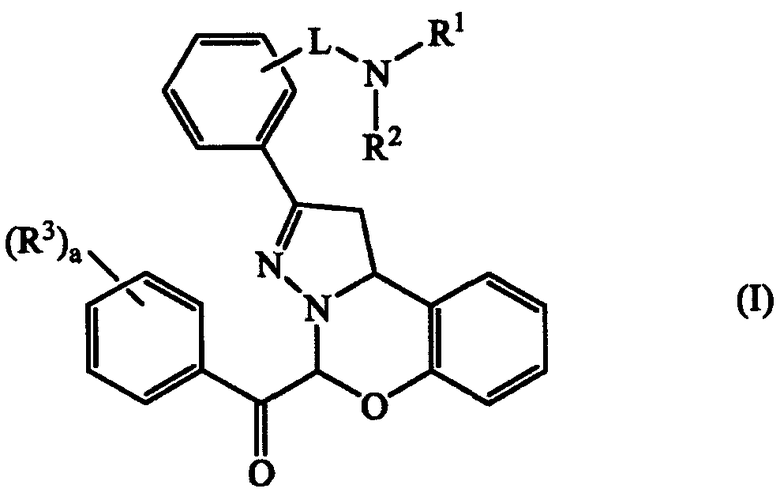
и их N-оксидам, стереоизомерным формам и солям,
где
а равно нулю, 1, 2, 3, 4 или 5;
L представляет собой С1-4алкандиил;
R1 представляет собой водород, С1-10алкил, С2-10алкенил, С2-10алкинил, С3-12циклоалкил, Het, арил или С1-10алкил, замещенный заместителем, выбранным из группы, состоящей из Het, арила, С3-10циклоалкила, аминогруппы и моно- и дизамещенной аминогруппы, где заместители аминогруппы, каждый по отдельности, выбраны из С1-10алкила, С2-10алкенила, С3-12циклоалкила, Het и арила;
R2 представляет собой водород, С1-10алкил, С2-10алкенил, С2-10алкинил, С3-12циклоалкил, Het, арил или С1-10алкил, замещенный заместителем, выбранным из группы, состоящей из Het, арила, С3-12циклоалкила, аминогруппы и моно- и дизамещенной аминогруппы, где заместители аминогруппы, каждый по отдельности, выбраны из С1-10алкила, С2-10алкенила, С3-12циклоалкила, Het и арила; или
R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют 5-12-членный насыщенный или частично насыщенный гетероцикл с одним или несколькими гетероатомами, которые, каждый по отдельности, выбраны из атома азота, кислорода или серы, и где указанный гетероцикл может быть необязательно замещен С1-10алкилом, С2-10алкенилом, С2-10алкинилом, С3-12циклоалкилом, С1-6алкилоксикарбонилом, Het, арилом или С1-10алкилом, замещенным заместителем, выбранным из группы, состоящей из Het, арила, С3-12циклоалкила, аминогруппы и моно- и дизамещенной аминогруппы, где заместители аминогруппы, каждый по отдельности, выбраны из С1-10алкила, С2-10алкенила, С3-12циклоалкила, Het и арила;
R3 представляет собой карбоксил, галоген, нитро, С1-10алкил, С3-12циклоалкил, полигалогенС1-10алкил, циано, аминогруппу, моно- или дизамещенную аминогруппу, аминокарбонил, моно- или дизамещенный аминокарбонил, С1-10алкилокси, С1-10алкилтио, С1-10алкилсульфонил, пирролидинил, пиперидинил, гомопиперидинил, морфолинил, тиоморфолинил или пиперазинил, необязательно замещенный С1-10алкилом, где заместители любой из аминогрупп, каждый по отдельности, выбраны из С1-10алкила, С2-10алкенила, С3-12циклоалкила, Het и арила;
арил представляет собой фенил, необязательно замещенный одним или несколькими заместителями, выбранными из группы, состоящей из С1-10алкила, полигалогенС1-10алкила, С1-10алкилокси, С1-10алкилтио, С1-10алкилсульфонила, нитро, циано, галогена, С3-7циклоалкила, С1-10алкилкарбонила, карбоксила, С1-10алкилоксикарбонила, аминогруппы моно- или дизамещенной аминогруппы, аминокарбонила, моно- или дизамещенного аминокарбонила, где заместители любой из аминогрупп, каждый по отдельности, выбраны из фенила, С1-10алкила, С2-10алкенила, С3-7циклоалкила, пирролидинила, пиперидинила, гомопиперидинила или пиперазинила, необязательно замещенного С1-10алкилом;
Het представляет собой 5- или 6-членный ароматический, насыщенный или частично насыщенный, моноциклический гетероцикл с одним или несколькими гетероатомами, которые, каждый по отдельности, выбраны из атома азота, кислорода или серы, и где гетероцикл может быть необязательно замещен одним или, когда возможно, более чем одним заместителем, выбранным из группы, состоящей из С1-10алкила, полигалогенС1-10алкила, С1-10алкилокси, С1-10алкилтио, С1-10алкилсульфонила, нитро, циано, галогена, С3-7циклоалкила, С1-10алкилкарбонила, карбоксила, С1-10алкилоксикарбонила, аминогруппы моно- или дизамещенной аминогруппы, аминокарбонила, моно- или дизамещенного аминокарбонила, где заместители любой из аминогрупп, каждый по отдельности, выбраны из фенила, С1-10алкила, С2-10алкенила, С3-7циклоалкила, пирролидинила, пиперидинила, гомопиперидинила или пиперазинила, необязательно замещенного С1-10алкилом.
Используемый в данном описании термин «галоген» как группа или часть группы является общим для фтора, хлора, брома или йода. Термин «полигалоген», используемый в данном описании в качестве приставки, означает радикал, замещенный одним или несколькими атомами галогена. Примеры использования термина «полигалоген» в качестве приставки к радикалу включают, например, полигалогенС1-10алкил, полигалогенС1-6алкил, полигалогенС1-4алкил и т.п. Особо представляющими интерес полигалогеналкилами являются дифторметил и трифторметил.
Термин «С1-4алкил» как группа или часть группы означает насыщенные одновалентные углеводородные радикалы с неразветвленной и разветвленной цепью, содержащие 1-4 атома углерода. Примеры таких С1-4алкильных радикалов включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил и т.п.
Термин «С1-6алкил» как группа или часть группы означает насыщенные одновалентные углеводородные радикалы с неразветвленной и разветвленной цепью, содержащие 1-6 атомов углерода. Примеры таких С1-6алкильных радикалов включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, 2-метилбутил, пентил, изоамил, гексил, 3-метилпентил и т.п.
Термин «С1-10алкил» как группа или часть группы означает насыщенные одновалентные углеводородные радикалы с неразветвленной и разветвленной цепью, содержащие 1-10 атомов углерода. Примеры таких С1-10алкильных радикалов включают примеры С1-6алкильных радикалов и гептил, октил, нонил, децил, 3-этилгептил и т.п.
Термин «С2-6алкенил» как группа или часть группы означает одновалентные углеводородные радикалы с неразветвленной и разветвленной цепью, имеющие по меньшей мере одну двойную связь и содержащие 2-6 атомов углерода. Примеры таких С2-6алкенильных радикалов включают этенил, пропенил, 1-бутенил, 2-бутенил, изобутенил, 2-метил-1-бутенил, 1-пентенил, 2-пентенил, 1-гексенил, 2-гексенил, 3-гексенил, 3-метил-2-пентенил и т.п.
Термин «С2-10алкенил» как группа или часть группы означает одновалентные углеводородные радикалы с неразветвленной и разветвленной цепью, имеющие по меньшей мере одну двойную связь и содержащие 2-10 атомов углерода. Примеры таких С2-6алкенильных радикалов включают примеры С2-6алкенила и 2-гептенил, 3-гептенил, 3-октенил, 4-октенил, 4-ноненил, 4-деценил и т.п.
Термин «С2-6алкинил» как группа или часть группы означает одновалентные углеводородные радикалы с неразветвленной и разветвленной цепью, имеющие по меньшей мере одну тройную связь и содержащие 2-6 атомов углерода. Примеры таких С2-6алкинильных радикалов включают этинил, пропинил, 1-бутинил, 2-бутинил, изобутинил, 2-метил-1-бутинил, 1-пентинил, 2-пентинил, 1-гексинил, 2-гексинил, 3-гексинил, 3-метил-2-пентинил и т.п.
Термин «С2-10алкинил» как группа или часть группы означает одновалентные углеводородные радикалы с неразветвленной и разветвленной цепью, имеющие по меньшей мере одну тройную связь и содержащие 2-10 атомов углерода. Примеры таких С2-10алкинильных радикалов включают примеры С2-6алкинила и 2-гептинил, 3-гептинил, 3-октинил, 4-октинил, 4-нонинил, 4-децинил и т.п.
Термин «С1-2алкандиил» как группа или часть группы означает двухвалентные насыщенные углеводородные радикалы с неразветвленной и разветвленной цепью, имеющие 1 или 2 атома углерода, такие как, например, метилен, этан-1,2-диил и т.п.
Термин «С1-4алкандиил» как группа или часть группы означает двухвалентные насыщенные углеводородные радикалы с неразветвленной и разветвленной цепью, имеющие 1-4 атома углерода, такие как примеры С1-2алкандиильных радикалов и пропан-1,3-диил, пропан-1,2-диил, бутан-1,4-диил и т.п.
Термин «С3-7циклоалкил» как группа или часть группы означает карбоциклические или спирокарбоциклические одновалентные углеводородные радикалы, имеющие от 3 до 7 атомов углерода в главной цепи карбоцикла или спирокарбоцикла. Примеры таких С3-7циклоалкильных радикалов включают циклопропил, циклобутил, циклопентил, циклогексил, спиро[2.4]гептанил, циклогептил и т.п.
Термин «С3-12циклоалкил» как группа или часть группы означает карбоциклические или спирокарбоциклические одновалентные углеводородные радикалы, имеющие от 3 до 12 атомов углерода в главной цепи карбоцикла или спирокарбоцикла. Примеры таких С3-12циклоалкильных радикалов включают примеры С3-7циклоалкила и циклооктил, циклононил, спиро[4.4]нонил, спиро[4.5]децил, спиро[5.5]ундецил, циклододецил, спиро[5,6]додецил и т.п.
Примеры 5- или 6-членных гетероциклов, обозначаемых Het, включают, но не ограничиваются перечисленным, пиридин, пиримидин, пиридазин, пиразин, триазин, имидазол, тиазол, оксазол, оксадиазол, тиадиазол, изотиазол, изоксазол, пиразол, фуран, тиофен, пиррол, хинолин, изохинолин, бензоксазол, изобензоксазол, бензотиазол, изобензотиазол, бензимидазол, бензотриазол, тетрагидрохинолин, тетрагидроизохинолин, пиперидин, пиперазин, морфолин, тиоморфолин, пирролидин, гомопиперидин, гомопиперазин, тетрагидрофуран и тетрагидротиенил. Каждый из обозначенных Het и указанных в качестве примеров гетероциклов может быть необязательно дополнительно замещен.
Предполагается, что используемый в данном описании термин С(=О) означает карбонильную часть и термин S(=O)2 означает сульфонильную часть. Используемый в данном описании термин «гидрокси» означает -ОН, термин «нитро» означает -NO2, термин «циано» означает -CN, термин «тио» означает -S, термин «оксо» означает =О.
Имеется в виду, что всякий раз термины «один или несколько заместителей» или «замещенный», используемые при обозначении соединений формулы (I), указывают, что один или несколько атомов водорода у атома, указанного в выражениях, использующих «один или несколько заместителей» или «замещенный», заменены с выбором из указанной групп, при условии, что не превышено нормальное число валентностей данного атома, и что замещение приводит к получению химически стабильного соединения, т.е. соединения, которое является достаточно устойчивым, чтобы выдержать выделение до необходимой степени чистоты из реакционной смеси и превращение в терапевтический агент.
Для терапевтических целей пригодными солями соединений настоящего изобретения являются соли, где противоион является фармацевтически или физиологически приемлемым. Однако соли, имеющие фармацевтически неприемлемый ион, могут также найти применение, например, при получении или очистке фармацевтически приемлемого соединения настоящего изобретения. Все соли, независимо от того, являются ли они фармацевтически приемлемыми или нет, включены в объем настоящего изобретения.
Фармацевтически приемлемые или физиологически переносимые формы кислотно-аддитивных солей, которые способны образовывать соединения настоящего изобретения, можно подходящим образом получать с использованием подходящих кислот, таких как, например, неорганические кислоты, такие как галогеноводородные кислоты, например, хлористоводородная или бромистоводородная кислота, серная, азотная, фосфорная и подобные кислоты; или органические кислоты, такие как, например, уксусная, пропановая, гидроксиуксусная, молочная, пировиноградная, щавелевая, мало новая, янтарная, малеиновая, фумаровая, яблочная, винная, лимонная, метансульфоновая, этансульфоновая, бензолсульфоновая, п-толуолсульфоновая, цикламиновая, салициловая, п-аминосалициловая, памовая и подобные кислоты.
И наоборот, указанные формы кислотно-аддитивных солей можно превратить обработкой подходящим основанием в форму свободного основания.
Соединения настоящего изобретения, содержащие кислотный протон, можно также превратить в форму нетоксичной соли металла или амино-аддитивной соли обработкой подходящими органическими или неорганическими основаниями. Подходящие формы солей оснований включают, например, аммониевые соли, четвертичные аммониевые соли, соли щелочных и щелочноземельных металлов, например, соли лития, натрия, калия, магния, кальция и т.п., соли с органическими основаниями, например, соли бензатина, N-метил-D-глюкамина, гидрабамина, и соли с аминокислотами, такими как, например, аргинин, лизин и т.п.
И наоборот, указанные формы основно-аддитивных солей можно превратить обработкой подходящей кислотой в форму свободной кислоты.
Термин «соли» включает также гидраты и формы присоединения растворителя, которые способны образовывать соединения настоящего изобретения. Примерами таких форм являются, например, гидраты, алкоголяты и т.п. Термин «соли» включает также продукты кватернизации атомов азота настоящих соединений. Основный атом азота можно кватернизировать любым агентом, известным специалисту в данной области, включающим, например, низшие алкилгалогениды, диалкилсульфаты, алкилгалогениды с длинной цепью и арилалкилгалогениды.
Имеется в виду, что формы N-оксидов настоящих соединений включают соединения, где один или несколько атомов азота окислены в так называемый N-оксид.
Настоящие соединения могут существовать также в их таутомерных формах. Предполагается, что такие формы, хотя они непосредственно не указаны в приведенной выше формуле, включены в объем настоящего изобретения.
Термин «стереохимически изомерные формы» соединений настоящего изобретения, используемый в данном описании ранее, означает все возможные соединения, составленные из тех же самых атомов, связанных той же самой последовательностью связей, но имеющие разные трехмерные структуры, которые не являются взаимообмениваемыми и которые могут иметь соединения настоящего изобретения. Если не указано или не оговорено особо, химическое определение соединения включает смесь всех возможных стереохимически изомерных форм, которые может иметь указанное соединение. Указанная смесь может содержать все диастереомеры и/или энантиомеры основной молекулярной структуры указанного соединения. Предполагается, что все стереохимически изомерные формы соединений настоящего изобретения, как в чистой форме, так и в форме смеси друг с другом, включены в объем настоящего изобретения.
Чистые стереоизомерные формы соединений и промежуточных соединений, приведенных в данном описании, определяют как изомеры, по существу не содержащие другие энантиомерные или диастереомерные формы такой же самой основной молекулярной структуры указанных соединений или промежуточных соединений. В частности, термин «стереоизомерно чистый» относится к соединениям или промежуточным соединениям, имеющим стереоизомерный избыток по меньшей мере 80% (т.е. минимум 80% одного изомера и максимум 20% других возможных изомеров) вплоть до стереоизомерного избытка 100% (т.е. 100% одного изомера и отсутствие другого), более конкретно, к соединениям или промежуточным соединениям, имеющим стереоизомерный избыток от 90% до 100%, еще более конкретно, имеющие стереоизомерный избыток от 94% до 100% и наиболее конкретно, имеющие стереоизомерный избыток от 97% до 100%. Термины «энантиомерно чистый» и «диастереомерно чистый» следует понимать аналогичным образом, но в данном случае имеющие отношение к энантиомерному избытку и диастереомерному избытку, соответственно, рассматриваемой смеси.
Чистые стереоизомерные формы соединений и промежуточных соединений данного изобретения можно получить согласно методикам, известным в данной области. Например, энантиомеры можно разделить друг от друга селективной кристаллизацией их диастереомерных солей с оптически активными кислотами. Альтернативно, энантиомеры можно разделить хроматографическими методами с использованием хиральных неподвижных фаз. Указанные чистые стереохимически изомерные формы можно также получить из соответствующих чистых стереохимически изомерных форм подходящих исходных веществ, при условии, что реакция протекает стереоспецифическим образом. Предпочтительно, если нужен определенный стереоизомер, указанное соединение можно синтезировать стереоспецифическими способами получения. В таких способах подходящим образом следует использовать энантиомерно чистые исходные вещества.
Диастереомерные рацематы соединений настоящего изобретения можно разделить на индивидуальные диастереомеры общепринятыми методами. Подходящими физическими методами разделения, которые можно использовать подходящим образом, являются, например, селективная кристаллизация и хроматография, например колоночная хроматография.
Соединения могут содержать один или несколько асимметричных центров и поэтому могут существовать в виде различных стереоизомерных форм. Абсолютную конфигурацию каждого асимметричного центра, который может присутствовать в соединениях, можно указать стереохимическими обозначениями R и S, причем эти обозначения R и S соответствуют правилам, описанным в Pure Appl. Chem. 1976, 45, 11-30.
Подразумевается также, что настоящее изобретение включает все изотопы атомов, присутствующих в настоящих соединениях. Изотопы включают такие атомы, которые представляют собой атомы, имеющие одинаковое атомное число, но разные массовые числа. В качестве общего примера, но без ограничения, изотопы водорода включают тритий и дейтерий. Изотопы углерода включают С-13 и С-14.
Имеется в виду, что всякий раз используемые в настоящем описании термины «настоящие соединения», «соединения настоящего изобретения», «соединения формулы (I)» или аналогичные термины, включают соединения формулы (I), их N-оксиды, их стереоизомерные формы, их соли или любую их подгруппу.
Представляющими интерес соединениями являются соединения формулы (I) или любая их подгруппа, где а равно нулю, 1 или 2, более конкретно, где а равно нулю или 1.
Другими представляющими интерес соединениями являются соединения формулы (I) или любая их подгруппа, где R1 представляет собой водород, С1-6алкил, С2-6алкенил, С2-6алкинил, С3-7циклоалкил, Het, арил или С1-6алкил, замещенный заместителем, выбранным из группы, состоящей из Het, арила, С3-7циклоалкила, аминогруппы и моно- и дизамещенной аминогруппы, где заместители аминогруппы, каждый по отдельности, выбраны из С1-6алкила или С3-7циклоалкила, особенно соединения, где R1 представляет собой С1-6алкил, С3-7циклоалкил, Het, арил или С1-6алкил, замещенный заместителем, выбранным из группы, состоящей из Het, арила, С3-7циклоалкила и моно- и дизамещенной аминогруппы, где заместители аминогруппы, каждый по отдельности, выбраны из С1-6алкила.
Другими представляющими интерес соединениями являются соединения формулы (I) или любая их подгруппа, где R2 представляет собой водород, С1-10алкил, С2-10алкенил, С2-10алкинил, С3-12циклоалкил или С1-10алкил, замещенный заместителем, выбранным из группы, состоящей из Het, арила, С3-7циклоалкила, аминогруппы и моно- и дизамещенной аминогруппы, где заместители аминогруппы, каждый по отдельности, выбраны из С1-6алкила; особенно соединения, где R2 представляет собой водород, С1-6алкил, С2-6алкенил или С1-6алкил, замещенный заместителем, выбранным из группы, состоящей из арилов.
Другими представляющими интерес соединениями являются соединения формулы (I) или любая их подгруппа, где R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют 5-12-членный насыщенный или частично насыщенный гетероцикл, где гетероцикл может быть необязательно замещен С1-6алкилом, С2-6алкенилом, С2-6алкинилом, С3-7циклоалкилом, С1-6алкилоксикарбонилом, Het, арилом или С1-6алкилом, замещенным заместителем, выбранным из группы, состоящей из Het, арила, С3-7циклоалкила, аминогруппы и моно- или дизамещенной аминогруппы, где заместители аминогруппы, каждый по отдельности, выбраны из С1-6алкила, С2-6алкенила, С3-7циклоалкила, Het и арила; в особенности соединения, где R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют 5-12-членный насыщенный или частично насыщенный гетероцикл, где гетероцикл может быть необязательно замещен С1-6алкилом, С1-6алкилоксикарбонилом или С1-6алкилом, замещенным арилом; более конкретно соединения, где R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют гетероцикл, выбранный из группы, состоящей из пиперазинила, гомопиперазинила, пиперидинила, гомопиперидинила, морфолинила, тиоморфолинила, пирролидинила, индолинила, 1,2,3,4-тетрагидрохинолинила, 1,2,3,4-тетрагидроизохинолинила, где гетероцикл может быть необязательно замещен С1-6алкилом, С2-6алкенилом, С2-6алкинилом, С3-7циклоалкилом, С1-6алкилоксикарбонилом, Het, арилом или С1-6алкилом, замещенным заместителем, выбранным из группы, состоящей из Het, арила, С3-7циклоалкила, аминогруппы и моно- или дизамещенной аминогруппы, где заместители аминогруппы, каждый по отдельности, выбраны из С1-6алкила, С2-6алкенила, С3-7циклоалкила, Het и арила; и еще более конкретно, соединения, где R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют гетероцикл, выбранный из группы, состоящей из пиперазинила, гомопиперазинила, пиперидинила, гомопиперидинила, морфолинила, тиоморфолинила, пирролидинила, индолинила, 1,2,3,4-тетрагидрохинолинила, 1,2,3,4-тетрагидроизохинолинила, где гетероцикл может быть необязательно замещен С1-6алкилом, С1-6алкилоксикарбонилом или С1-6алкилом, замещенным арилом.
Другими представляющими интерес соединениями являются соединения формулы (I) или любая их подгруппа, где R3 представляет собой карбоксил, галоген, нитро, С1-6алкил, С3-7циклоалкил, полигалогенС1-4алкил, циано, аминогруппу, моно- или дизамещенную аминогруппу, аминокарбонил, моно- или дизамещенный аминокарбонил, С1-6алкилокси, С1-6алкилтио, С1-6алкилсульфонил, пирролидинил, пиперидинил, гомопиперидинил, морфолинил, тиоморфолинил или пиперазинил, необязательно замещенный С1-6алкилом, где заместители любой из аминогрупп, каждый по отдельности, выбраны из С1-6алкила, С2-6алкенила, С3-7циклоалкила, Het и арила; в особенности соединения, где R3 представляет собой галоген, нитро, С1-6алкил, С3-7циклоалкил, полигалогенС1-4алкил, циано, С1-6алкилокси, С1-6алкилтио, С1-6алкилсульфонил, пиперидинил, морфолинил.
Другими представляющими интерес соединениями являются соединения формулы (I) или любая их подгруппа, где арил представляет собой фенил, необязательно замещенный одним или несколькими заместителями, выбранными из группы, состоящей из С1-6алкила, полигалогенС1-6алкила, С1-6алкилокси, С1-6алкилтио, С1-6алкилсульфонила, нитро, циано, галогена, С3-7циклоалкила, С1-6алкилкарбонила, карбоксила, С1-6алкилоксикарбонила, аминогруппы моно- или дизамещенной аминогруппы, аминокарбонила, моно- или дизамещенного аминокарбонила, где заместители любой из аминогрупп, каждый по отдельности, выбраны из фенила, С1-6алкила, С2-6алкенила, С3-7циклоалкила, пирролидинила, пиперидинила, гомопиперидинила или пиперазинила, необязательно замещенного С1-6алкилом; в особенности соединения, где арил представляет собой фенил, необязательно замещенный одним, двумя или тремя заместителями, выбранными из группы, состоящей из С1-6алкила, С1-6алкилокси, нитро, циано, галогена, аминогруппы, моно- или дизамещенной аминогруппы, где заместители любой из аминогрупп, каждый по отдельности, выбраны из С1-6алкила.
Другими представляющими интерес соединениями являются соединения формулы (I) или любая их подгруппа, где Het представляет собой 5- или 6-членный ароматический, насыщенный или частично насыщенный, моноциклический или бициклический гетероцикл с одним или несколькими гетероатомами, которые, каждый по отдельности, выбраны из атома азота, кислорода или серы, и где гетероцикл может быть необязательно замещен одним или, когда возможно, более чем одним заместителем, выбранным из группы, состоящей из С1-6алкила, полигалогенС1-6алкила, С1-6алкилокси, С1-6алкилтио, С1-6алкилсульфонила, нитро, циано, галогена, С3-7циклоалкила, С1-6алкилкарбонила, карбоксила, С1-6алкилоксикарбонила, аминогруппы моно- или дизамещенной аминогруппы, аминокарбонила, моно- или дизамещенного аминокарбонила, где заместители любой из аминогрупп, каждый по отдельности, выбраны из фенила, С1-6алкила, С2-6алкенила, С3-12циклоалкила, пирролидинила, пиперидинила, гомопиперидинила или пиперазинила, необязательно замещенного С1-6алкилом; в особенности соединения, где Het представляет собой 5- или 6-членный ароматический, насыщенный или частично насыщенный, моноциклический или бициклический гетероцикл с одним или несколькими гетероатомами, которые, каждый по отдельности, выбраны из атома азота, кислорода или серы, и где гетероцикл может быть необязательно замещен С1-6алкилом; более конкретно соединения, где Het представляет собой гетероцикл, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, пиридазинила, триазинила, пиранила, пирролила, фуранила, тиенила, оксазолила, изоксазолила, тиазолила, изотиазолила, имидазолила, тетрагидрофуранила, тетрагидротиенила, имидазолинила, диоксоланила, пирролидинила, пиперидинила, гомопиперидинила, пиперазинила, гомопиперазинила, диоксоланила, морфолинила, тиоморфолинила, где гетероцикл может быть необязательно замещен одним или, когда возможно, более чем одним заместителем, выбранным из группы, состоящей из С1-6алкила, полигалогенС1-6алкила, С1-6алкилокси, С1-6алкилтио, С1-6алкилсульфонила, нитро, циано, галогена, С3-7циклоалкила, С1-6алкилкарбонила, карбоксила, С1-6алкилоксикарбонила, аминогруппы моно- или дизамещенной аминогруппы, аминокарбонила, моно- или дизамещенного аминокарбонила, где заместители любой из аминогрупп, каждый по отдельности, выбраны из фенила, С1-6алкила, С2-6алкенила, С3-7циклоалкила, пирролидинила, пиперидинила, гомопиперидинила или пиперазинила, необязательно замещенного С1-6алкилом; еще более конкретно, соединения, где Het представляет собой гетероцикл, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, пиридазинила, триазинила, пиранила, пирролила, фуранила, тиенила, оксазолила, изоксазолила, тиазолила, изотиазолила, имидазолила, тетрагидрофуранила, тетрагидротиенила, имидазолинила, диоксоланила, пирролидинила, пиперидинила, гомопиперидинила, пиперазинила, гомопиперазинила, диоксоланила, морфолинила, тиоморфолинила, где гетероцикл может быть необязательно замещен С1-6алкилом.
Следующими, представляющими интерес соединениями являются соединения формулы (I) или любая их подгруппа, где Het представляет собой гетероцикл, выбранный из группы, состоящей из пиридинила, фуранила, тиенила, тетрагидрофуранила, пирролидинила, пиперидинила, где гетероцикл может быть необязательно замещен одним или, когда возможно, более чем одним заместителем, выбранным из группы, состоящей из С1-6алкила, полигалогенС1-6алкила, С1-6алкилокси, С1-6алкилтио, С1-6алкилсульфонила, нитро, циано, галогена, С3-7циклоалкила, С1-6алкилкарбонила, карбоксила, С1-6алкилоксикарбонила, аминогруппы моно- или дизамещенной аминогруппы, аминокарбонила, моно- или дизамещенного аминокарбонила, где заместители любой из аминогрупп, каждый по отдельности, выбраны из фенила, С1-6алкила, С2-6алкенила, С3-7циклоалкила, пирролидинила, пиперидинила, гомопиперидинила или пиперазинила, необязательно замещенного С1-6алкилом; в особенности соединения, где Het представляет собой гетероцикл, выбранный из группы, состоящей из пиридинила, фуранила, тиенила, тетрагидрофуранила, пирролидинила, пиперидинила, где гетероцикл может быть необязательно замещен С1-6алкилом.
Подходящими подгруппами соединений являются соединения формулы (I), соответствующие одному или нескольким следующим условиям:
а) а равно нулю или 1;
b) R1 представляет собой С1-10алкил, С3-12циклоалкил, Het, арил или С1-10алкил, замещенный заместителем, выбранным из группы, состоящей из Het, арила, С3-12циклоалкила и моно- или дизамещенной аминогруппы, где заместители аминогруппы, каждый по отдельности, выбраны из С1-10алкила;
с) R2 представляет собой водород, С1-10алкил, С2-10алкенил или С1-10алкил, замещенный арилом;
d) R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют 5-12-членный насыщенный или частично насыщенный гетероцикл, где указанный гетероцикл может быть необязательно замещен С1-10алкилом, С1-6алкилоксикарбонилом или С1-10алкилом, замещенным арилом;
е) L представляет собой С1-2алкандиил;
f) R3 представляет собой галоген, нитро, С1-10алкил, С3-12циклоалкил, полигалогенС1-10алкил, циано, С1-10алкилокси, С1-10алкилтио, С1-10алкилсульфонил, пиперидинил, морфолинил;
g) арил представляет собой фенил, необязательно замещенный одним или несколькими заместителями, выбранными из группы, состоящей из С1-10алкилокси, галогена, моно- или дизамещенной аминогруппы, где заместители любой из аминогрупп, каждый по отдельности, выбраны из С1-10алкила;
h) Het представляет собой 5- или 6-членный ароматический, насыщенный или частично насыщенный, моноциклический или бициклический гетероцикл с одним или несколькими гетероатомами, которые, каждый по отдельности, выбраны из атома азота, кислорода или серы, и где гетероцикл может быть необязательно замещен С1-10алкилом.
Конкретными соединениями являются соединения формулы (I) или их подгруппа, такие как представляющие интерес соединения, указанные выше, где часть -С(=О)-NR1R2 находится в параположении кольца фенила, которое связано с положением 2 структуры 1,9b-дигидро-5-окса-3,3а-диазациклопента[a]нафталина (называемой также структурой 1,10b-дигидро-5Н-пиразоло[1,5-c][1,3]бензоксазина), как показано на приведенной ниже фигуре соединением формулы (Ia)
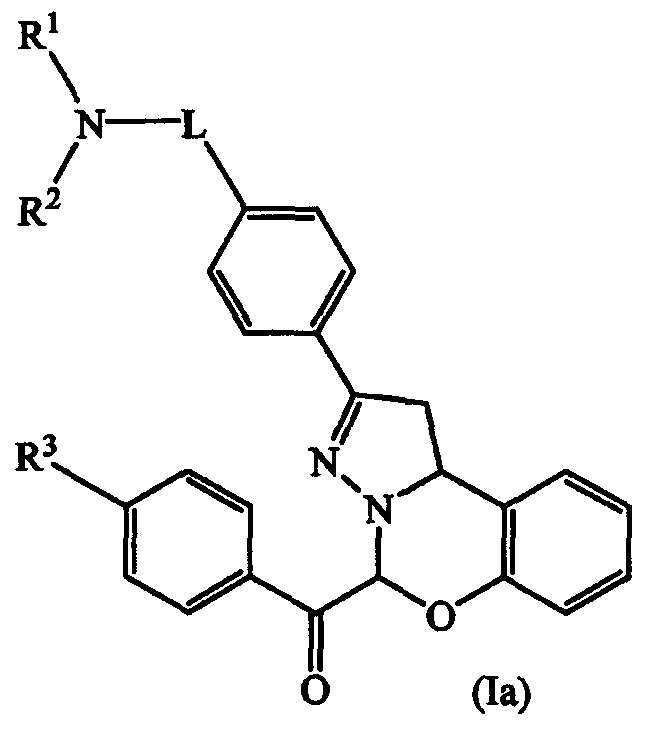
Другими конкретными соединениями являются соединения формулы (I) или любая их подгруппа, такие как представляющие интерес соединения, указанные выше, где а равно нулю или 1 и R представляет собой галоген, нитро, С1-10алкил, С3-12циклоалкил, полигалогенС1-10алкил, циано, С1-10алкилокси, С1-10алкилтио, С1-10алкилсульфонил, пиперидинил, морфолинил.
Другими конкретными соединениями являются соединения формулы (I) или (Ia) или любая их подгруппа, такие как представляющие интерес соединения, указанные выше, где R1 представляет собой С1-10алкил, С3-12циклоалкил, Het, арил или С1-10алкил, замещенный заместителем, выбранным из группы, состоящей из Het, арила, С3-12циклоалкила и моно- или дизамещенной аминогруппы, где заместители аминогруппы, каждый по отдельности, выбраны из С1-10алкила; R2 представляет собой водород, С1-10алкил, С2-10алкенил или С1-10алкил, замещенный арилом; или R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют 5-12-членный насыщенный или частично насыщенный гетероцикл, где указанный гетероцикл может быть необязательно замещен С1-10алкилом, С1-6алкилоксикарбонилом или С1-10алкилом, замещенным арилом.
Предпочтительными соединениями являются соединения формулы (I) или (Ia) или любая их подгруппа, такие как представляющие интерес и конкретные соединения, указанные выше, где
а равно нулю или 1;
R1 представляет собой С1-10алкил, С3-12циклоалкил, Het, арил или С1-10алкил, замещенный заместителем, выбранным из группы, состоящей из Het, арила, С3-12циклоалкила и моно- или дизамещенной аминогруппы, где заместители аминогруппы, каждый по отдельности, выбраны из С1-10алкила;
R2 представляет собой водород, С1-10алкил, С2-10алкенил или С1-10алкил, замещенный арилом; или
R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют 5-12-членный насыщенный или частично насыщенный гетероцикл, где указанный гетероцикл может быть необязательно замещен С1-10алкилом, С1-6алкилоксикарбонилом или С1-10алкилом, замещенным арилом;
R3 представляет собой галоген, нитро, С1-10алкил, С3-12циклоалкил, полигалогенС1-10алкил, циано, С1-10алкилокси, С1-10алкилтио, С1-10алкилсульфонил, пиперидинил, морфолинил.
Другими предпочтительными соединениями являются соединения формулы (I) или (Ia) или любая их подгруппа, такие как представляющие интерес и конкретные соединения, указанные выше, где
а равно нулю или 1;
R1 представляет собой С1-10алкил, С3-12циклоалкил, Het, арил или С1-10алкил, замещенный заместителем, выбранным из группы, состоящей из Het, арила, С3-12циклоалкила и моно- или дизамещенной аминогруппы, где заместители аминогруппы, каждый по отдельности, выбраны из С1-10алкила;
R2 представляет собой водород, С1-10алкил, С2-10алкенил или С1-10алкил, замещенный арилом; или
R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют 5-12-членный насыщенный или частично насыщенный гетероцикл, где указанный гетероцикл может быть необязательно замещен С1-10алкилом, С1-6алкилоксикарбонилом или С1-10алкилом, замещенным арилом;
R3 представляет собой галоген, нитро, С1-10алкил, С3-12циклоалкил, полигалогенС1-10алкил, циано, С1-10алкилокси, С1-10алкилтио, С1-10алкилсульфонил, пиперидинил, морфолинил;
арил представляет собой фенил, необязательно замещенный одним или несколькими заместителями, выбранными из группы, состоящей из С1-10алкилокси, галогена, моно- или дизамещенной аминогруппы, где заместители любой из аминогрупп, каждый по отдельности, выбраны из С1-10алкила;
h) Het представляет собой 5- или 6-членный ароматический, насыщенный или частично насыщенный, моноциклический или бициклический гетероцикл с одним или несколькими гетероатомами, которые, каждый по отдельности, выбраны из атома азота, кислорода или серы, и где гетероцикл может быть необязательно замещен С1-10алкилом.
Более предпочтительными соединениями являются соединения формулы (I) или (Ia) или любая их подгруппа, такие как представляющие интерес и конкретные соединения, указанные выше, где
а равно нулю или 1;
R1 представляет собой С1-6алкил, С3-7циклоалкил, Het, арил или С1-10алкил, замещенный заместителем, выбранным из группы, состоящей из Het, арила, С3-7циклоалкила и моно- или дизамещенной аминогруппы, где заместители аминогруппы, каждый по отдельности, выбраны из С1-10алкила;
R2 представляет собой водород, С1-6алкил, С2-6алкенил или С1-6алкил, замещенный заместителем, выбранным из группы, состоящей из арилов; или
R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют гетероцикл, выбранный из группы, состоящей из пиперазинила, гомопиперазинила, пиперидинила, гомопиперидинила, морфолинила, тиоморфолинила, пирролидинила, индолинила, 1,2,3,4-тетрагидрохинолинила, 1,2,3,4-тетрагидроизохинолинила, где гетероцикл может быть необязательно замещен С1-6алкилом, С1-6алкилоксикарбонилом или С1-6алкилом, замещенным арилом;
R3 представляет собой галоген, нитро, С1-6алкил, С3-7циклоалкил, полигалогенС1-4алкил, циано, С1-4алкилокси, С1-6алкилтио, С1-6алкилсульфонил, пиперидинил, морфолинил;
арил представляет собой фенил, необязательно замещенный одним, двумя или тремя заместителями, выбранными из группы, состоящей из С1-6алкила, С1-6алкилокси, нитро, циано, галогена, амино, моно- или дизамещенной аминогруппы, где заместители любой из аминогрупп, каждый по отдельности, выбраны из С1-6алкила;
Het представляет собой гетероцикл, выбранный из группы, состоящей из пиридинила, фуранила, тиенила, тетрагидрофуранила, пирролидинила, пиперидинила, где гетероцикл может быть необязательно замещен С1-6алкилом.
Другими более предпочтительными соединениями являются соединения формулы (I) или (Ia) или любая их подгруппа, такие как представляющие интерес, конкретные и предпочтительные соединения, указанные выше, где R2 представляет собой водород и R3 представляет собой циано.
Другими более предпочтительными соединениями являются соединения формулы (I) или любая их подгруппа, такие как представляющие интерес, конкретные и предпочтительные соединения, указанные выше, где а равно 1 и R3 представляет собой галоген, циано, С1-4алкил, С1-4алкилтио, морфолинил, С1-4алкилокси, нитро, С1-4алкилсульфонил, трифторметил.
Наиболее предпочтительные соединения включают
4-[2-(4-диэтиламинометилфенил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[a]нафталин-4-карбонил]бензонитрил;
4-{2-[4-(бензиламинометил)фенил]-1,9b-дигидро-5-окса-3,3а-диазациклопента[a]нафталин-4-карбонил}бензонитрил;
4-[2-(4-{[(пиридин-4-илметил)амино]метил}фенил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[a]нафталин-4-карбонил]бензонитрил;
4-[2-(4-{[(4-метоксибензил)метиламино]метил}фенил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[a]нафталин-4-карбонил]бензонитрил;
(4-трет-бутилфенил)-[2-(4-{[(4-метоксибензил)метиламино]метил}фенил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[a]нафталин-4-ил]метанон;
(4-трет-бутилфенил)-[2-(4-{[(пиридин-4-илметил)амино]метил}фенил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[a]нафталин-4-ил]метанон;
(4-трет-бутилфенил)-[2-(4-диэтиламинометилфенил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[a]нафталин-4-ил]метанон;
4-{2-[4-(2-диэтиламиноэтил)фенил]-1,9b-дигидро-5-окса-3,3а-диазациклопента[a]нафталин-4-карбонил}бензонитрил;
4-(2-{4-[(циклопентилметиламино)метил]фенил}-1,9b-дигидро-5-окса-3,3а-диазациклопента[a]нафталин-4-карбонил]бензонитрил;
4-(2-{4-[4-(4-метоксифениламино)бутил]фенил}-1,9b-дигидро-5-окса-3,3а-диазациклопента[a]нафталин-4-карбонил)бензонитрил;
(4-метансульфонилфенил)-[2-(4-{[(пиридин-4-илметил)амино]метил}фенил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[a]нафталин-4-ил]метанон;
(4-метансульфонилфенил)-[2-(4-{[(4-метоксибензил)метиламино]метил}фенил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[a]нафталин-4-ил]метанон;
[2-(4-диэтиламинометилфенил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[a]нафталин-4-ил]-(4-метансульфонилфенил)метанон
и их N-оксиды, стереоизомерные формы и соли.
Вследствие того факта, что соединения формулы (I) являются ингибиторами репликации ВИЧ, соединения формулы (I) предназначены для лечения теплокровных животных, особенно людей, инфицированных ВИЧ. Состояния, связанные с ВИЧ, которые можно предотвратить или лечить соединениями настоящего изобретения, включают СПИД, СПИД-ассоциированный комплекс (ARC), прогрессивную генерализованную лимфаденопатию (PGL), а также хронические заболевания ЦНС, вызванные ретровирусами, такие как, например, опосредуемая ВИЧ деменция и рассеянный склероз.
Соединения настоящего изобретения можно, следовательно, применять в качестве лекарственных средств. Соединения настоящего изобретения можно применять при изготовлении лекарственного средства, предназначенного для лечения состояний, связанных с инфекцией ВИЧ.
Соединения настоящего изобретения можно также применять против указанных выше состояний или в способе лечения таких состояний. Указанный способ лечения включает системное введение эффективного терапевтического количества соединения формулы (I) ВИЧ-инфицированным теплокровным животным, особенно, ВИЧ-инфицированным людям.
В одном варианте осуществления изобретение относится к применению соединений настоящего изобретения при изготовлении лекарственного средства для предотвращения передачи ВИЧ или инфекции ВИЧ или связанного с инфекцией ВИЧ заболевания теплокровных животных, особенно людей, и особенно передачи или инфекции посредством половой связи или близкого контакта между партнерами. Таким образом, изобретение относится также к способу предотвращения передачи ВИЧ или инфекции ВИЧ или связанного с инфекцией ВИЧ заболевания, включающему введение теплокровному животному, особенно человеку, эффективного для предотвращения количества соединения формулы (I), особенно для предотвращения передачи или инфекции посредством половой связи или близкого контакта между партнерами.
Благоприятные свойства настоящих соединений в отношении их способности ингибировать вирусную репликацию ВИЧ можно продемонстрировать с использованием анализа антивирусной репликации, который непосредственно измеряет продолжительную репликацию вируса ВИЧ дикого типа в МТ4-клетках посредством специфического взаимодействия ВИЧ-tat с LTR-последовательностями, связанными с GFR (MT4-LTR-EGFP-клетки). С использованием указанного выше анализа действия против вирусной репликации было обнаружено, что настоящие соединения ингибируют репликацию панели резистентных к обратной транскриптазе вирусов, резистентных к протеазе вирусов или резистентных к комбинации обратной транскриптазы и протеазы вирусов (так называемых резистентных ко множеству лекарственных средств вирусов).
Настоящие соединения испытывали в эксперименте по времени добавления. Эксперименты по времени добавления показывают, в какой точке времени испытуемое соединение ингибирует вирусную репликацию в клеточной окружающей среде. В частности, испытуемые соединения настоящего изобретения добавляли в различные интервалы времени к инфицированным ВИЧ-1 МТ4-клеткам, экспрессирующим репортерный ген ВИЧ-1-LTR-люциферазы (МТ4-LTR-Luc), или МТ4-клеткам, экспрессирующим репортерный ген ВИЧ-1-LTR-EGFP (MT4-LTR-EGFP). Первой временной точкой добавления испытуемого соединения были 30 минут после синхронизации вируса.
Настоящие соединения испытывали также в анализе вступления репортера (ERA), который измеряет ингибирование слияния клетка-клетка между клеточной линией, устойчиво экспрессирующей ВИЧ (линия клеток-эффекторов) и клеточной линией, экспрессирующей CD4 и CXCR4 (линия клеток-мишеней), снабженной LTR-EGFP, с использованием считывания данных FACS.
Анализ на токсичность, в котором пониженная экспрессия белка-репортера GFP (MT4-CMV-EGFP-клетки) служит в качестве маркера для клеточной токсичности испытуемого соединения, можно применять для измерения токсичности настоящих соединений.
В общем, соединения настоящего изобретения можно получать последовательностью синтезов, показанной на схеме 1.
Схема 1
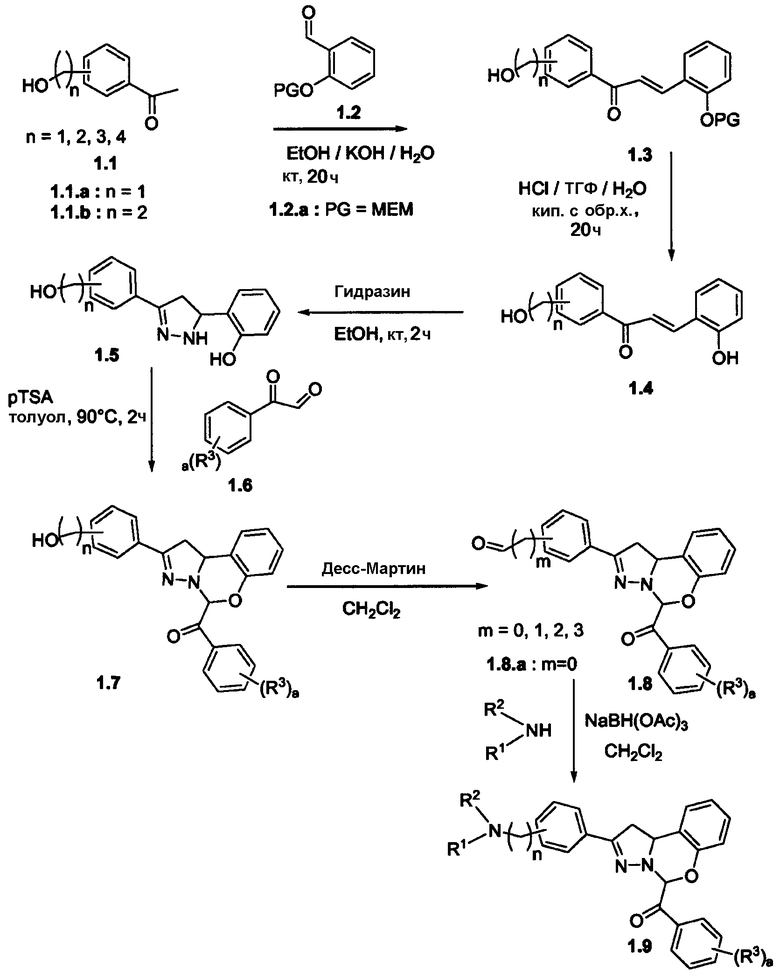
На схеме 1 промежуточные соединения формулы 1.1 может быть конденсировано с салициловым альдегидом формулы 1.2 в присутствии подходящего основания, такого как минеральное основание, подобное гидроксиду калия или гидроксиду натрия, в подходящей системе растворителей, такой как, например, смесь спирта и воды, например, смесь этанола и воды. Альтернативно, можно использовать органическое основание, такое как пирролидин, в подходящем растворителе, таком как тетрагидрофуран или дихлорметан. Имеется в виду, что символом ”PG” в промежуточном соединении 1.2 обозначена защитная группа для гидроксильной группы, такая как, например, метоксиметил, трет-бутоксиметил, тетрагидропиранил или метоксиэтоксиметил (МЕМ). Ниже, на схеме 3, показана методика реакции получения промежуточного соединения формулы 1.2, где защитной группой является МЕМ. Образовавшимся промежуточным соединением указанной выше реакции конденсации на схеме 1 является халкон формулы 1.3 (описан также в J. Med. Chem, 2000, 43, 4868-4876). У защищенного халкона формулы 1.3 можно снять защиту в кислотной среде, например, с использованием хлористоводородной кислоты в подходящем растворителе, таком как, например, тетрагидрофуран, дихлорметан или спирт, с получением таким образом промежуточного соединения формулы 1.4. Промежуточное соединение 1.4 может быть затем подвергнуто взаимодействию с гидразином в подходящем, смешиваемом с водой растворителе, таком как, например, диоксан, толуол или спирт, подобный спирту, с получением дигидропиразола формулы 1.5 (J. Ind. Chem. Soc., 1989, 66, 893-896). Соединение формулы 1.7 может быть затем получено путем сочетания дигидропиразола формулы 1.5 с подходящим глиоксалем формулы 1.6 в подходящем растворителе, таком как толуол или диоксан, и в присутствии каталитического количества кислоты, такой как паратолуолсульфоновая кислота. Промежуточное соединение 1.7 можно окислить реагентом Десс-Мартина или другим окислителем, известным в области химии, таким как условия Сверна, в подходящем растворителе, таком как дихлорметан или гексан, с получением альдегида 1.8. Требуемые амины 1.9 можно затем получить путем восстановительного аминирования альдегида 1.8 с использованием триацетоксиборогидрида натрия или цианоборогидрида натрия в подходящем растворителе, таком как дихлорметан, дихлорэтан или тетрагидрофуран (ТГФ).
Схема 2
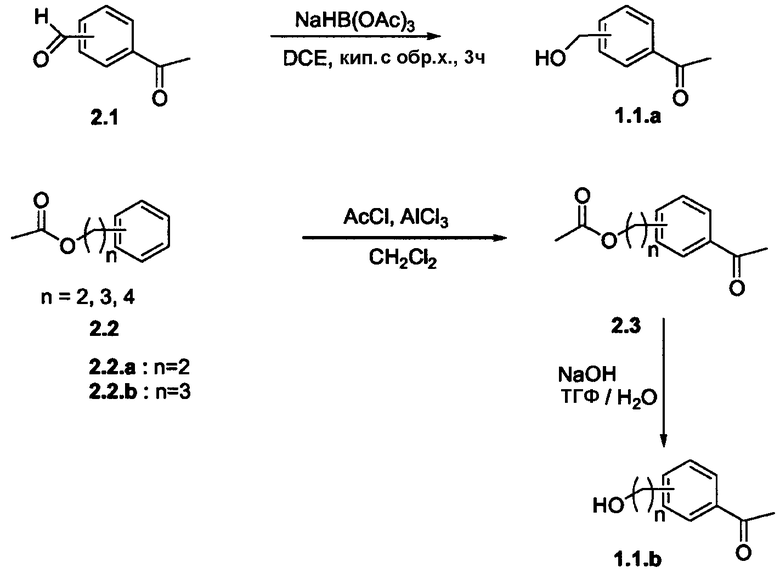
На схеме 2 соединение формулы 1.1.а, которое используют в качестве исходного вещества на схеме 1, можно получить из коммерчески доступного ацетилбензальдегида с использованием восстанавливающего агента, такого как триацетоксиборогидрид натрия, в подходящем растворителе, таком как дихлорэтан.
Кроме того, на схеме 2 соединение формулы 1.1.b может быть получено путем ацилирования по Фриделю-Крафтсу ацетата 2.2.а с использованием реагента, кислоты Льюиса, такой как хлорид алюминия или трибромид бора, в подходящем растворителе, таком как дихлорметан, простой эфир или гексан, с последующим гидролизом сложного эфира 2.3 с получением требуемого соединения 1.1.b.
Схема 3
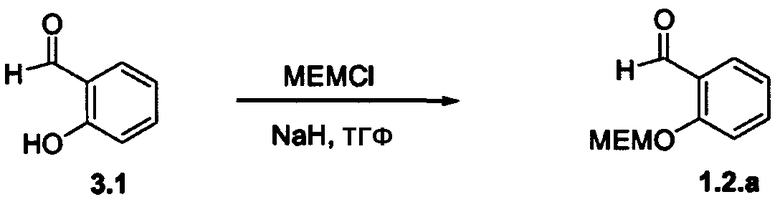
Получение промежуточного соединения формулы 1.2.а с МЕМ в качестве защитной группы может быть осуществлено взаимодействием салицилового альдегида 3.1, который является коммерчески доступным, с хлорметоксиметоксиэтаном в присутствии основания, такого как гидрид натрия или гидрид калия, и в присутствии подходящего растворителя, подобного N,N-диметилформамиду или тетрагидрофурану.
Схема 4
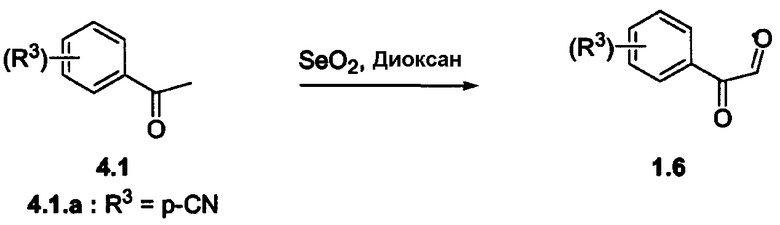
Получение глиоксаля формулы 1.6 можно осуществить, исходя из промежуточного соединения формулы 4.1, способом, описанным в J. Het. Chem. 1987, 24, 441-451, или аналогичным способом. Более конкретно, ацетильное соединение формулы 4.1 можно окислить с получением глиоксаля формулы 1.6 в растворителе, таком как диоксан, с использованием оксида селена в качестве окисляющего агента.
При получениях, описанных выше, продукты реакции можно выделить из реакционной среды и, если необходимо, далее очистить согласно методам, обычно известным в данной области, такими как, например, экстракция, кристаллизация, дистилляция, растирания и хроматография.
Соединения формулы (I), получаемые описанными выше способами, можно синтезировать в виде смеси стереоизомерных форм, в частности в форме рацемических смесей энантиомеров, которые можно отделить друг от друга по известным в данной области методам разделения. Рацемические соединения формулы (I) можно превратить в соответствующие формы диастереомерных солей взаимодействием с подходящей хиральной кислотой. Указанные формы диастереомерных солей затем разделяют, например, селективной или фракционной кристаллизацией, и энантиомеры выделяют из них щелочью. Альтернативный метод разделения энантиомерных форм соединений формулы (I) включает жидкостную хроматографию с использованием хиральной неподвижной фазы. Указанные чистые стереохимически изомерные формы можно также получить из соответствующих чистых стереохимически изомерных форм подходящих исходных веществ, при условии, что реакция протекает стереоспецифическим образом. Предпочтительно, если требуется определенный стереоизомер, указанное соединение можно синтезировать стереоспецифическими способами получения. В данных способах можно подходящим образом использовать энантиомерно чистые исходные соединения.
Соединения настоящего изобретения можно, таким образом, применять в качестве фармацевтических средств per se, в смеси друг с другом или в форме фармацевтических препаратов для животных, предпочтительно, для млекопитающих и особенно для людей.
Кроме того, настоящее изобретение относится к фармацевтическим препаратам, которые в качестве активных компонентов содержат эффективную дозу по меньшей мере одного из соединений формулы (I) в дополнение к обычным фармацевтически безвредным эксципиентам и вспомогательным веществам. Фармацевтические препараты обычно содержат 0,1-90 мас.% такого соединения. Фармацевтические препараты можно изготовить способом, известным per se специалисту в данной области. Для этой цели по меньшей мере одно соединение настоящего изобретения, вместе с одним или несколькими твердыми или жидкими фармацевтическими эксципиентами и/или вспомогательными веществами и, если необходимо, в комбинации с другими фармацевтически активными соединениями, превращают в подходящую для введения форму или дозированную форму, которую можно затем применять в качестве фармацевтического средства в медицине или ветеринарии.
Фармацевтические средства, которые содержат соединение согласно изобретению, можно вводить перорально, парентерально, например внутривенно, ректально, ингаляцией или местно, причем предпочтительное введение зависит от отдельного случая, например, определенного течения подвергаемого лечению заболевания. Предпочтительным является пероральное введение.
Специалисту в данной области известны вспомогательные вещества, которые являются подходящими для требуемого фармацевтического препарата. Помимо растворителей подходящими являются также гелеобразующие агенты, основы суппозиториев, вспомогательные вещества для получения таблеток и другие носители для соединений, антиоксиданты, диспергаторы, эмульгаторы, противовспенивающие средства, корригенты, консерванты, солюбилизаторы, агенты для достижения эффекта депо, буферные вещества или красители.
Соединения настоящего изобретения могут также найти применение при ингибировании ex vivo образцов, содержащих ВИЧ, или образцов, которые, как предполагается, подвергались действию ВИЧ. Следовательно, настоящие соединения можно применять для ингибирования ВИЧ, присутствующего в образце жидкости тела, который содержит или, как предполагается, содержит или подвергался действию ВИЧ.
Кроме того, в качестве лекарственного средства можно применять комбинацию антиретровирусного соединения и соединения настоящего изобретения. Таким образом, настоящее относится также к продукту, содержащему (а) соединение настоящего изобретения и (b) другое антиретровирусное соединение, в качестве комбинированного препарата для одновременного, раздельного или последовательного применения при лечении ретровирусных инфекций. Так, для борьбы с инфекциями ВИЧ или лечения инфекций ВИЧ или инфекции и заболевания, связанного с инфекциями ВИЧ, такого как синдром приобретенного иммунодефицита (СПИД) или СПИД-ассоциированный комплекс (ARC), соединения данного изобретения можно совместно вводить в комбинации, например, с ингибиторами связывания, такими как, например, сульфат декстрана, сурамин, полианионы, растворимый CD4, связующее вещество gp120, такое как BMS378806, соединения против CD4 Ab, такие как PRO-542 или TNX-355; ингибиторами слияния, такими как, например, Т20, Т1249, ингибиторами связывания сорецептора, такими как, например, АК-602, SCH-C, SCH-D, AMD 3100 (бицикламы), AMD-070, TAK 779, TAK 220, UK-427-857, PRO-140; ингибиторами RT, такими как, например, фоскарнет и пролекарства; нуклеозидами RTI, такими как, например, AZT, 3TC, DDC, DDI, D4T, абакавир, FTC, эмтрицитабин, DAPD, dOTC; нуклеотидами RTI, такими как, например, РМЕА, РМРА, тенофовир; NNRTI, такими как, например, невирапин, делавирдин, эфавиренц, тивирапин, ловирид, этравирин, дапивирин, рилпивирин, ТМС120, ТМС125, МКС-442, UC 781, каправирин, DPC 961, DPC963, DPC082, DPC083, каланолид А, SJ-3366, TSAO, 4”-деаминированный TSAO; ингибиторами РНКазы Н, такими как, например, SP1093V, PD126338; ингибиторами ТАТ, такими как, например, RO-5-3335, K12, K37; ингибиторами интегразы, такими как, например, L 708906, L 731988; ингибиторами протеазы, такими как, например, дарунавир, ампренавир, ритонавир, нелфинавир, саквинавир, индинавир, лопинавир, лазинавир, атазанавир, BMS 186316, DPC 681, DPC 684, типранавир, AG1776, DMP 450, L 756425, PD178390, PNU 140135; ингибиторами гликозилирования, такими как, например, кастаноспермин, деоксинойримицин.
Особо представляющими интерес являются продукты, включающие (i) соединение формулы (I) и (ii) дарунавир и усилитель, такой как ритонавир, в качестве комбинированного препарата для одновременного, раздельного или последовательного применения при лечении ретровирусных инфекций.
Особо представляющими интерес являются продукты, включающие (i) соединение формулы (I) и (ii) этравирин, в качестве комбинированного препарата для одновременного, раздельного или последовательного применения при лечении ретровирусных инфекций.
Особо представляющими интерес являются продукты, включающие (i) соединение формулы (I) и (ii) дапиварин, в качестве комбинированного препарата для одновременного, раздельного или последовательного применения при лечении ретровирусных инфекций.
Особо представляющими интерес являются продукты, включающие (i) соединение формулы (I) и (ii) рилпивирин, в качестве комбинированного препарата для одновременного, раздельного или последовательного применения при лечении ретровирусных инфекций.
Соединения настоящего изобретения можно также вводить в комбинации с иммуномодуляторами (например, бропиримином, антителом против альфа-интерферона человека, IL-2, метионинэнкефалином, интерфероном альфа и налтрексоном) или с антибиотиками (например, пентамидинизотиоратом) для уменьшения интенсивности симптомов, борьбы с инфекцией ВИЧ или устранения инфекции ВИЧ и ее симптомов.
Для получения формы для перорального введения соединения настоящего изобретения смешивают с подходящими добавками, такими как эксципиенты, стабилизаторы или инертные разбавители, и смесь превращают при помощи обычных способов в подходящие для такого введения формы, такие как таблетки, покрытые таблетки, твердые капсулы, водные, спиртовые или маслянистые растворы. Примерами подходящих инертных носителей являются аравийская камедь, оксид магния, карбонат магния, фосфат калия, лактоза, глюкоза или крахмал, особенно кукурузный крахмал. В этом случае препарат можно изготовить как в виде сухих, так и влажных гранул. Подходящими маслянистыми эксципиентами или растворителями являются растительные или животные масла, такие как подсолнечное масло или масло печени трески. Подходящими растворителями для водных или спиртовых растворов являются вода, этанол, растворы сахаров или их смеси. Полиэтиленгликоли и полипропиленгликоли являются также пригодными в качестве дополнительных вспомогательных веществ для других форм для введения.
Для подкожного или внутривенного введения активные соединения, при необходимости, вводят в раствор, суспензию или эмульсию с веществами, подходящими для этого, такими как солюбилизаторы, эмульгаторы или дополнительные вспомогательные вещества. Соединения могут быть также лиофилизованы, и полученные лиофилизаты можно применять, например, для получения препаратов для инъекции или инфузии. Подходящими растворителями являются, например, вода, физиологический солевой раствор или спирты, например, этанол, пропанол, глицерин, в дополнение также растворы сахаров, такие как растворы глюкозы или маннита, или, альтернативно, смеси различных указанных растворителей.
Подходящими фармацевтическими препаратами для введения в форме аэрозолей или спреев являются, например, растворы, суспензии или эмульсии соединений или их физиологически переносимых солей в фармацевтически приемлемом растворителе, таком как этанол или вода, или смеси таких растворителей. Если необходимо, препарат может дополнительно содержать также другие фармацевтические вспомогательные вещества, такие как поверхностно-активные вещества, эмульгаторы и стабилизаторы, а также пропеллент. Такой препарат обычно содержит активное соединение в концентрации приблизительно от 0,1 до 50%, особенно, приблизительно от 0,3 до 3 мас.%.
Для повышения растворимости и/или стабильности соединений в фармацевтических препаратах можно подходящим образом использовать α-, β- или γ-циклодекстрины или их производные. Кроме того, растворимость и/или стабильность соединений в фармацевтических композициях могут повышать сорастворители, такие как спирты. При получении водных композиций аддитивные соли рассматриваемых соединений несомненно являются более подходящими вследствие их повышенной растворимости в воде.
Подходящими циклодекстринами являются α-, β- или γ-циклодекстрины (CD) или их простые эфиры и смешанные простые эфиры, где одна или несколько гидроксигрупп звеньев ангидроглюкозы циклодекстрина замещены алкилом, особенно, метилом, этилом или изопропилом, например, произвольно метилированный β-CD; гидроксиалкил, особенно, гидроксиэтил, гидроксипропил или гидроксибутил; карбоксиалкил, особенно, карбоксиметил или карбоксиэтил; алкилкарбонил, особенно, ацетил; алкилоксикарбонилалкил или карбоксиалкилоксиалкил, особенно, карбоксиметоксипропил или карбоксиэтоксипропил; алкилкарбонилоксиалкил, особенно, 2-ацетилоксипропил. Особо заслуживающими внимания в качестве комплексообразующих агентов и/или солюбилизаторов являются β-CD, произвольно метилированный β-CD, 2,6-диметил-β-CD, 2-гидроксиэтил-β-CD, 2-гидроксиэтил-γ-CD, 2-гидроксипропил-γ-CD, и (2-карбоксиметокси)пропил-β-CD, и особенно, 2-гидроксипропил-β-CD (2-НР-β-CD).
Термин «смешанный простой эфир» означает производные циклодекстрина, где по меньшей мере две гидроксигруппы циклодекстрина превращены в простые эфиры с разными группами, такими как, например, гидроксипропил и гидроксиэтил.
Представляющий интерес способ изготовления настоящих соединений в комбинации с циклодекстрином или его производным описан в ЕР-А-721331. Хотя описанные в нем препараты содержат активные противогрибковые ингредиенты, они в равной степени представляет интерес для изготовления препаратов из соединений настоящего изобретения. Описанные в указанном патенте препараты особенно пригодны для перорального введения и включают противогрибковое средство в качестве активного ингредиента, достаточное количество циклодекстрина или его производного в качестве солюбилизатора, водную кислотную среду в качестве объемного жидкого носителя и спиртовый сорастворитель, который в значительной степени упрощает изготовление композиции. Указанные препараты можно также сделать более приятными на вкус добавлением фармацевтически приемлемых подслащивающих веществ и/или корригентов.
Другие общепринятые способы повышения растворимости соединений настоящего изобретения в фармацевтических композициях описаны в WO 94/05263, заявке РСТ № РСТ/ЕР 98/01773, ЕР-А-499299, WO 97/44014 и WO 01/22938, все из которых включены в данное описание посредством ссылок.
Более конкретно, настоящие соединения можно изготовить в составе фармацевтической композиции, содержащей терапевтически эффективное количество частиц, состоящих из твердой дисперсии, включающей (а) соединение настоящего изобретения и (b) один или несколько фармацевтически приемлемых водорастворимых полимеров.
Термин «твердая дисперсия» означает систему в твердом состоянии (в противоположность жидкому или газообразному состоянию), включающую по меньшей мере два компонента, где один компонент диспергирован более или менее равномерно по всему другому компоненту или компонентам. Когда указанная дисперсия компонентов является такой, что система химически и физически однородна или гомогенна по всей дисперсии или состоит из одной фазы, как определено в термодинамике, такую твердую дисперсию называют «твердым раствором». Твердые растворы являются предпочтительными физическими системами, поскольку компоненты в них обычно легко биодоступны в организмах, в которые их вводят.
Термин «твердая дисперсия» также включает дисперсии, которые менее гомогенны по всей дисперсии, чем твердые растворы. Такие дисперсии не являются химически и физически однородными по всей дисперсии или включают более чем одну фазу.
Водорастворимым полимером в частицах является подходящий полимер, который имеет кажущуюся вязкость 1-100 мПа при растворении в 2% водном растворе при 20°С.
Предпочтительными водорастворимыми полимерами являются гидроксипропилметилцеллюлозы или НРМС. НРМС, имеющие степень замещения метокси приблизительно от 0,8 до приблизительно 2,5 и молярное замещение гидроксипропилом приблизительно от 0,05 до приблизительно 3,0, обычно являются водорастворимыми. Степень замещения метокси относится к среднему числу присутствующих групп простого метилового эфира на звено ангидроглюкозы молекулы целлюлозы. Молярное замещение гидроксипропилом относится к среднему числу молей пропиленоксида, который реагировал с каждым звеном ангидроглюкозы молекулы целлюлозы.
Частицы, определение которым дается выше, можно получить сначала приготовлением твердой дисперсии компонентов и затем необязательно измельчением или размалыванием полученной дисперсии. Существуют различные способы получения твердых дисперсий, включающие экструзию расплава, сушку распылением и упаривание раствора.
Далее подходящим может быть изготовление настоящих соединений в форме наночастиц, которые имеют модификатор поверхности, адсорбированный на их поверхности в количестве, достаточном для поддержания эффективного среднего размера частиц меньше, чем 1000 нм. Считается, что подходящие модификаторы поверхности включают модификаторы, которые физически прилипают к поверхности антиретровирусного агента, но химически не связываются с антиретровирусным агентом.
Подходящие модификаторы поверхности можно предпочтительно выбрать из известных органических и неорганических фармацевтических эксципиентов. Такие эксципиенты включают различные полимеры, олигомеры с низкой молекулярной массой, природные продукты и поверхностно-активные вещества. Предпочтительные модификаторы поверхности включают неионогенные и анионогенные поверхностно-активные вещества.
Еще один представляющий интерес способ изготовления препаратов настоящих соединений включают способ изготовления фармацевтической композиции, при помощи которого соединения данного изобретения включают в гидрофильные полимеры и полученную смесь наносят в виде пленки-покрытия на множество маленьких гранул, получая, таким образом, композицию с хорошей биодоступностью, которую можно подходящим образом изготовить и которая является подходящей для получения фармацевтических дозированных форм для перорального введения.
Указанные гранулы включают (а) центральную, округленную или сферическую сердцевину, (b) пленку-покрытие из гидрофильного полимера и антиретровирусного агента и (с) герметично покрывающий полимерный слой.
Вещества, подходящие для применения в качестве сердцевин в гранулах, являются разнообразными, при условии, что указанные вещества являются фармацевтически приемлемыми и имеют подходящие размеры и устойчивость. Примерами таких веществ являются полимеры, неорганические вещества, органические вещества и сахариды и их производные.
Другой аспект настоящего изобретения относится к набору или контейнеру, содержащему соединение настоящего изобретения в количестве, эффективном для применения в качестве стандарта или реагента при испытании или анализе для определения способности потенциального фармацевтического средства ингибировать проникновение ВИЧ, рост ВИЧ или то и другое. Данный аспект изобретения может найти свое применение в фармацевтических исследовательских программах.
Доза настоящих соединений или их физиологически переносимых солей, которую вводят, зависит от отдельного случая и, как обычно, должна быть адаптирована к условиям отдельного случая для достижения оптимального действия. Так, она зависит, конечно, от частоты введения и от эффективности и продолжительности действия соединений, применяемых в каждом случае для терапии или профилактики, но также от природы и тяжести инфекции и симптомов и от пола, возраста, массы и индивидуальной восприимчивости подвергаемого лечению человека или животного, и от того, является ли терапия неотложной или профилактической. Обычно суточная доза соединения настоящего изобретения в случае введения пациенту с массой приблизительно 75 кг составляет от 1 мг до 5 г, предпочтительно, от 10 мг до 2 г, более предпочтительно, от 20 мг до 1 г. Дозу можно вводить в форме разовой дозы или разделенной на несколько, например, на две, три, четыре или даже больше, разовых доз.
Экспериментальная часть
Пример 1: синтез 4-[4-(4-цианобензоил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[a]нафталин-2-ил]-N,N-диэтилбензиламина 1.9.а (соединение 1)
Синтез 4-гидроксиметилбензофенона 1.1.а
К раствору 4-ацетилбензальдегида (9 г, 61 ммоль) в 1,2-дихлорэтилене (1,2-DCE) (100 мл) добавляют NaHB(OAc)3, или триацетоксиборогидрид натрия (19,3 г, 90 ммоль), и реакционную смесь кипятят с обратным холодильником в течение 7 часов. Затем смесь выливают на NH4Cl (насыщенный, водный) и экстрагируют CH2Cl2 (3×50 мл). Объединенные органические слои промывают насыщенным раствором соли, сушат (Na2SO4) и концентрируют. Продукт очищают колоночной хроматографией (этилацетат/гептан=70/30), получая 8,08 г продукта 1.1.а (выход 89%).
Синтез соединения 2.3.а
К раствору соединения 2.2.а (20 мл, 112 ммоль) в CH2Cl2 (1000 мл) добавляют алюминийхлорид (14,9 г, 112 ммоль) и смесь охлаждают до 0°С. Затем по каплям добавляют раствор ацетилхлорида (8 мл, 112 ммоль) в CH2Cl2 при поддержании температуры ниже 0°С. Затем добавляют другой эквивалент хлорида алюминия и смесь перемешивают при 0°С в течение 1,5 часа. Смесь выливают в смесь льда и воды и добавляют ~20 мл концентрированного HCl. Органический слой отделяют, промывают насыщенным раствором соли, сушат (Na2SO4) и концентрируют. Образовавшееся масло очищают колоночной хроматографией (этилацетат/гептан=1/1), получая 12,1 г 2.3.b (выход 49%).
Синтез соединения 1.1.b
Соединение 2.3.а (12,1 г, 55 ммоль) растворяют в смеси ТГФ/вода (400 мл, 1/1) и добавляют гидроксид натрия (2,3 г, 57 ммоль). Реакционную смесь перемешивают при комнатной температуре в течение 6 часов. Затем слой ТГФ отделяют и водный слой экстрагируют Et2O, или диэтиловым эфиром (2×50 мл). Объединенные органические слои промывают насыщенным раствором соли, сушат (Na2SO4) и концентрируют, получая 1.1.b в виде белого твердого вещества (9,4 г, выход 96%).
Синтез 2-(2-метоксиэтоксиметокси)бензальдегида 1.2
Промежуточное соединение 2.1 (20 ммоль) растворяют в ТГФ (150 мл). Образовавшуюся смесь охлаждают до 0°С. Добавляют гидрид натрия (30 ммоль), смесь перемешивают при комнатной температуре в течение 1 часа и добавляют хлорметоксиметоксиэтан (20 мл). Смесь перемешивают при комнатной температуре в течение 16 часов. Добавляют воду (200 мл) и смесь экстрагируют дихлорметаном. Органический слой отделяют, сушат (над MgSO4), фильтруют и растворитель выпаривают досуха. Остаток фильтруют на силикагеле с использованием дихлорметана в качестве элюента. Растворитель удаляют, получая соединение 1.2.а с выходом 95%.
Синтез 4-{3-[2-(2-метоксиэтоксиметокси)фенил]акрилоил}бензилового спирта 1.3.а
К раствору соединений 1.1.а (8 г, 53 ммоль) и 1.2.а (11,2 г, 53 ммоль) в этаноле (350 мл) добавляют KOH (5,94 г, 106 ммоль) в Н2О (5 мл). Реакционную смесь перемешивают при к.т. в течение 20 часов и затем выливают на NH4Cl (водный, насыщенный) и экстрагируют этилацетатом (EtOAc) (3×100 мл). Объединенные органические слои промывают насыщенным раствором соли, сушат (Na2SO4) и концентрируют. Продукт очищают колоночной хроматографией (этилацетат/гептан=1/1), получая 15,5 г продукта 1.3.а (выход 85%, чистота по ЖХ-МС 90%).
Синтез 4-[3-(2-гидроксифенил)акрилоил]бензилового спирта, 1.4.а
Соединение 1.3.а (15,5 г, 45 ммоль) растворяют в ТГФ (350 мл) и добавляют 1М HCl (95 мл). Реакционную смесь кипятят с обратным холодильником в течение 20 часов, с последующим выпариванием растворителя. Затем добавляют CH2Cl2 (50 мл) и органический слой экстрагируют дважды 1М NaOH (100 мл). Объединенные слои NaOH
подкисляют с использованием 1М HCl и продукт осаждают из раствора. Продукт отделяют фильтрованием и сушат в вакуумной печи, получая 9,3 г продукта 1.4.а (выход 81%).
Синтез 4-[5-(2-гидроксифенил)-4,5-дигидро-1Н-пиразол-3-ил]бензилового спирта 1.5.а
Соединение 1.4.а (9,3 г, 37 ммоль) растворяют в этаноле (EtOH) (350 мл) и одной порцией добавляют гидразин (7,3 г, 146 ммоль). Реакционную смесь перемешивают в течение 2 часов при комнатной температуре. Продукт, осажденный из раствора, отделяют фильтрованием и сушат в вакуумной печи, получая 6,2 г продукта 1.5.а (выход 63%).
Синтез 4-(2-оксоацетил)бензонитрила 1.6.а
К раствору 4-цианоацетофенона 4.1.а (6 г, 41 ммоль) в диоксане (250 мл) добавляют диоксид селена (9,1 г, 82 ммоль). Реакционную смесь кипятят с обратным холодильником в течение 20 часов, охлаждают до комнатной температуры, фильтруют и концентрируют. Остаток растворяют в CH2Cl2 и раствор снова фильтруют. Растворитель выпаривают и остаток очищают колоночной хроматографией (этилацетат/гептан=1/1), получая 5,2 г глиоксаля 1.6.а (выход 80%).
Синтез 4-[4-(4-цианобензоил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[a]нафталин-2-ил]бензилового спирта 1.7.а
Соединение 1.5.а (5,5 г, 20 ммоль) помещают в толуол (200 мл) и подвергают действию ультразвука в течение 30 минут. Затем раствор нагревают до 80°С и перемешивают при этой температуре в течение 30 минут. Затем добавляют паратолуолсульфоновую кислоту (0,19 г, 1 ммоль). Далее по каплям добавляют раствор глиоксаля 1.6.а (3,6 г, 23 ммоль) в ТГФ (20 мл) и реакционную смесь перемешивают при 80°С в течение 1,5 часа. По истечении этого времени растворитель выпаривают и продукт очищают колоночной хроматографией (CH2Cl2/МеОН=99/1), получая 5,3 г продукта 1.7.а (выход 63%). «МеОН» относится к метанолу.
Синтез 4-[4-(4-цианобензоил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[a]нафталин-2-ил]бензальдегида 1.8.а
Соединение 1.7.а (2 г, 4,9 ммоль) растворяют в CH2Cl2 (60 мл) и к реакционной смеси добавляют периодинан Десс-Мартина (14 мл, 15 мас.% в CH2Cl2, 6,83 ммоль). Реакционную смесь перемешивают в течение 4 часов при комнатной температуре. Затем добавляют NaHCO3 (водный, насыщенный) и Na2S2O3 (1 экв.) и смесь энергично перемешивают в течение 15 минут. Органический слой отделяют, промывают насыщенным раствором соли, сушат (Na2SO4) и концентрируют. Продукт очищают колоночной хроматографией (этилацетат/гептан=30/70), получая 1,22 г продукта 1.8.а (выход 61%).
Пример 2: общая методика синтеза соединений 1.9
К раствору альдегида 1.8 и соответствующего амина (1,1 экв.) в CH2Cl2 добавляют NaHB(OAc)3 (1,1-эквивалента). Реакционную смесь перемешивают при комнатной температуре в течение ночи и затем выливают на NaHCO3 (водный, насыщенный). Органический слой отделяют и водный слой экстрагируют 2 раза CH2Cl2. Объединенные органические слои промывают насыщенным раствором соли, сушат (Na2SO4) и концентрируют. Продукты очищают колоночной хроматографией с использованием смеси CH2Cl2/МеОН. Выходы составляют 20-70%.
Соединения, перечисленные в нижеследующей таблице, получают по методикам, аналогично описанным в примерах 1 или 2.
Таблица 1

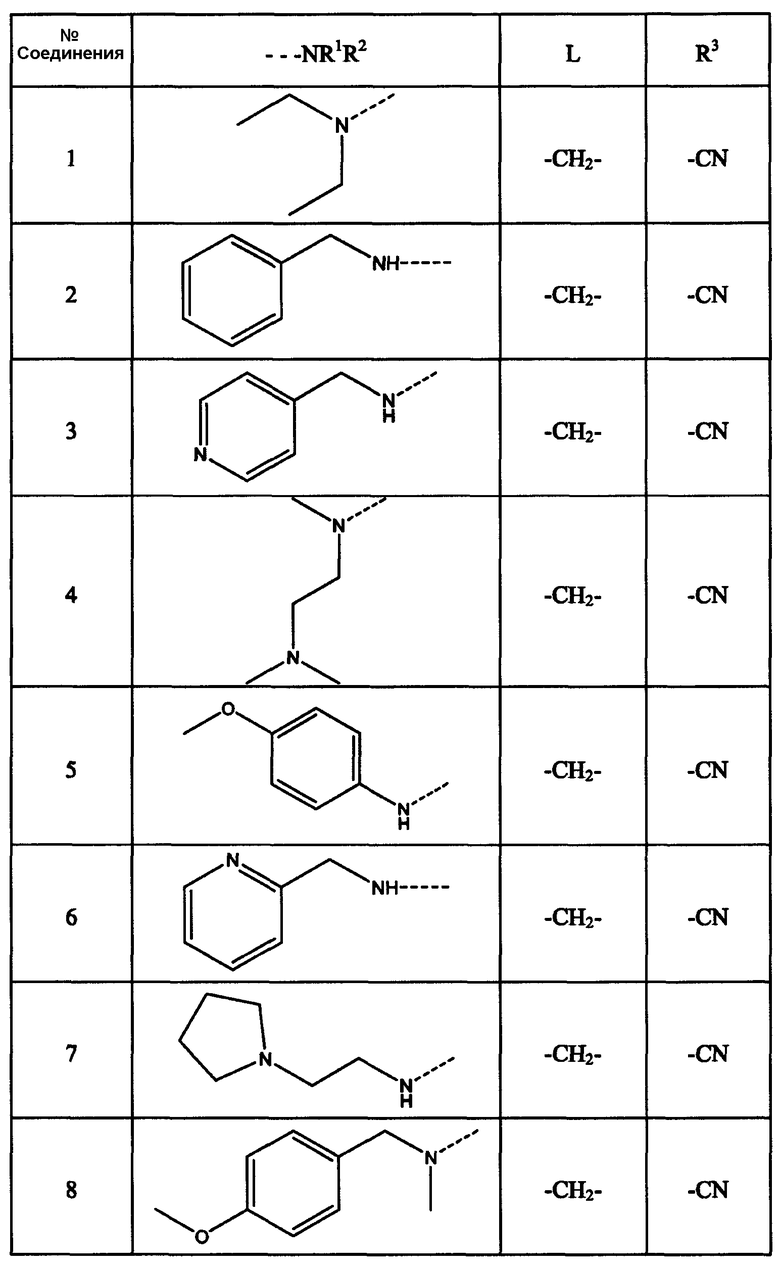
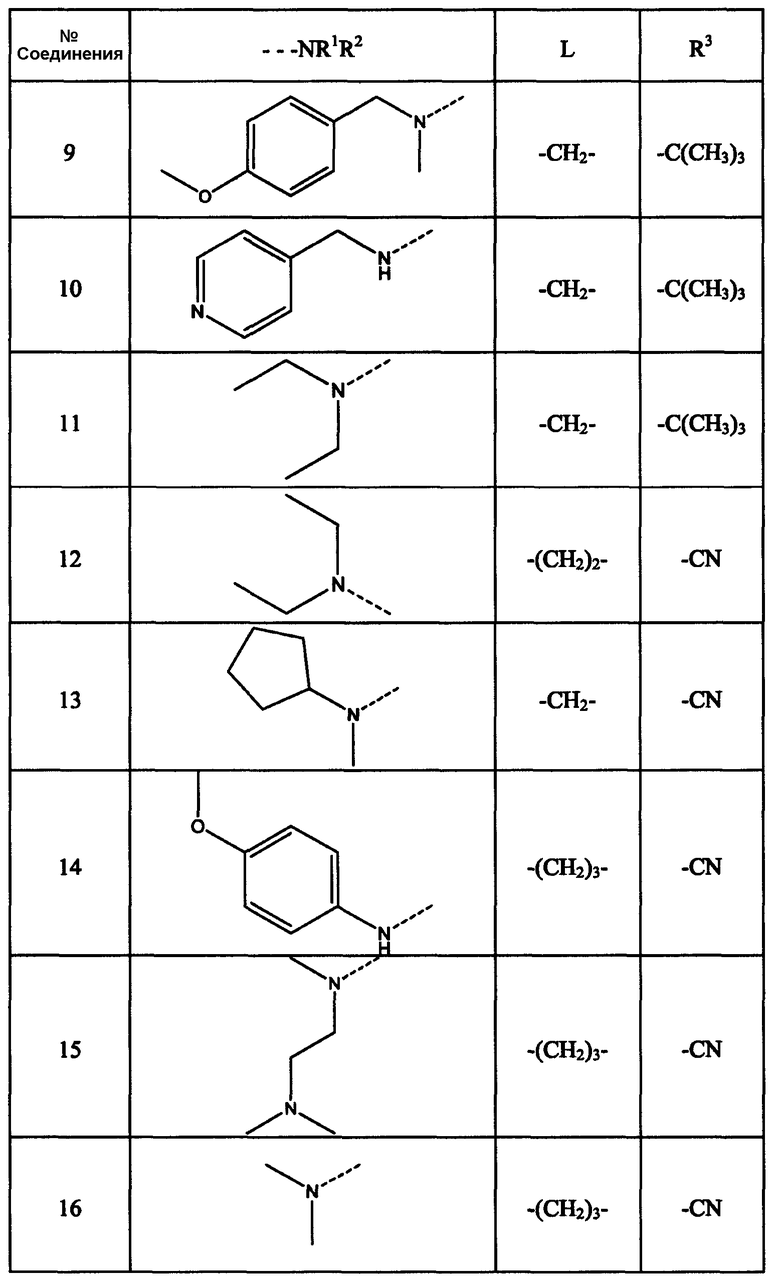
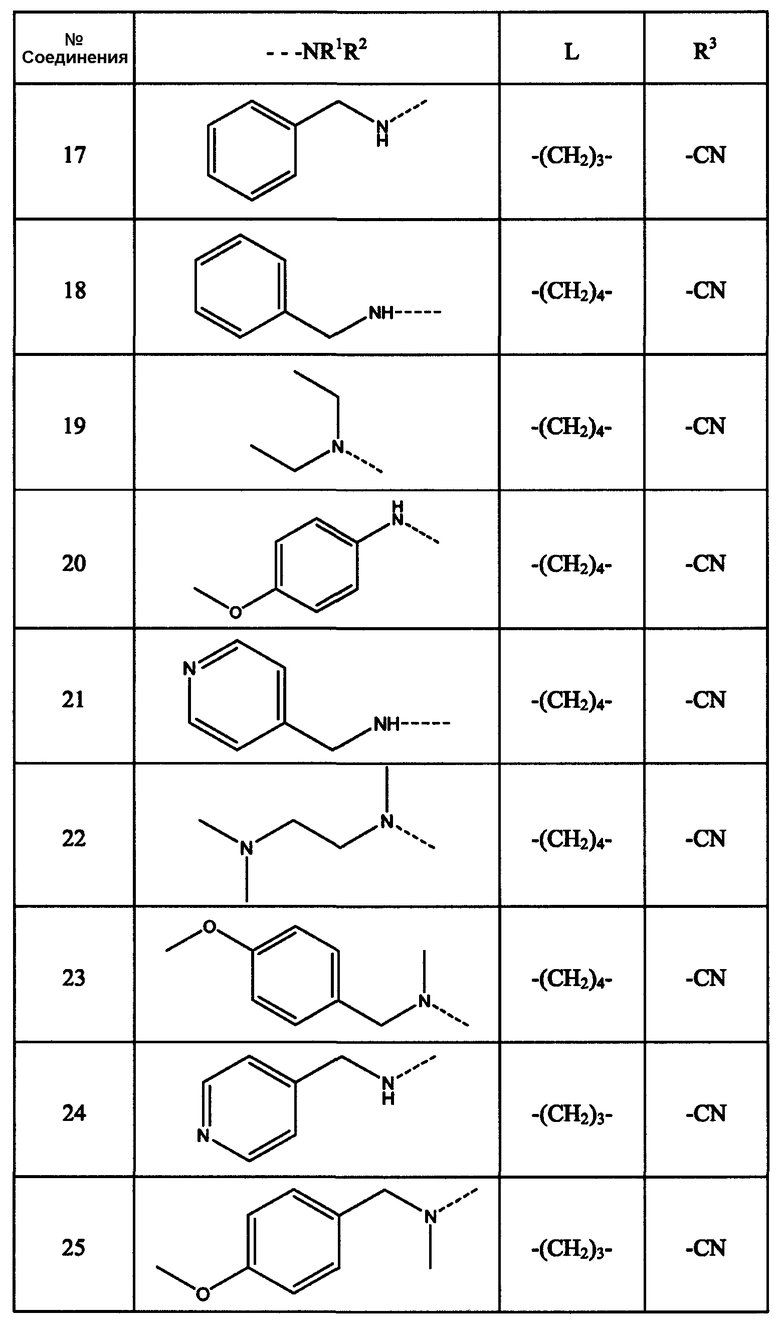
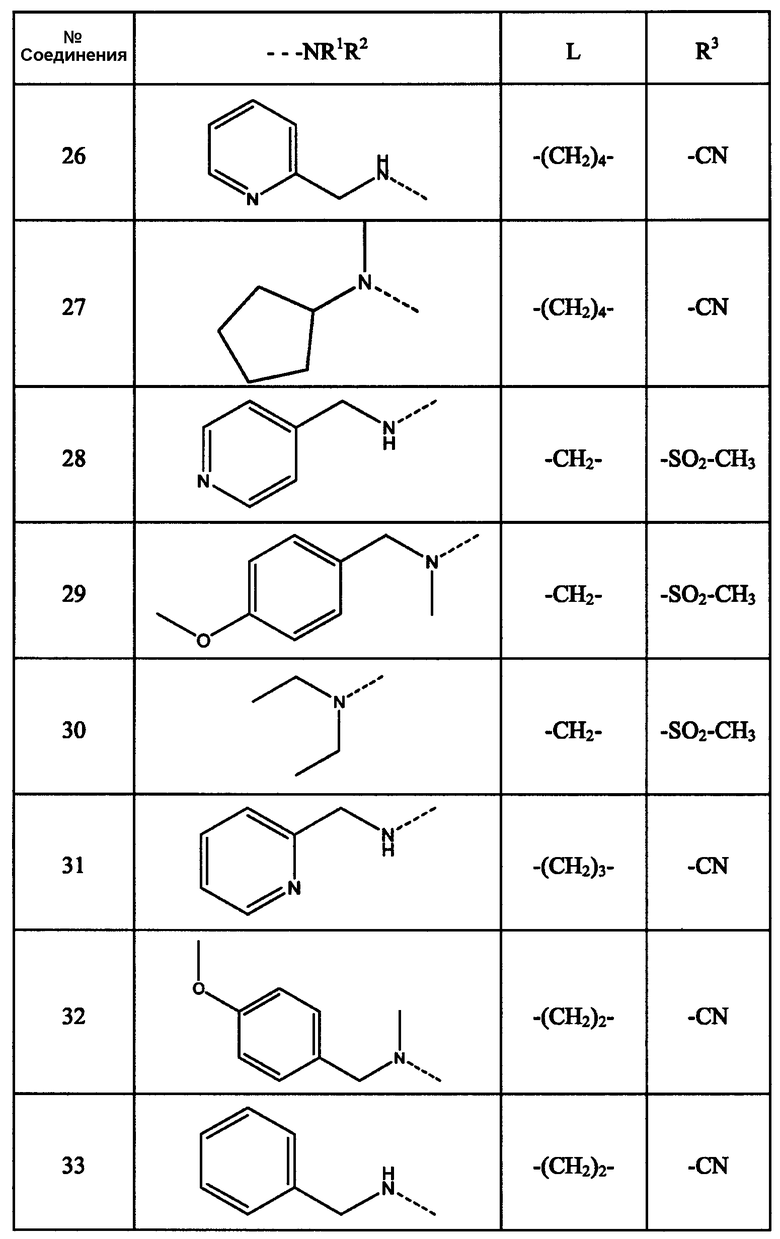
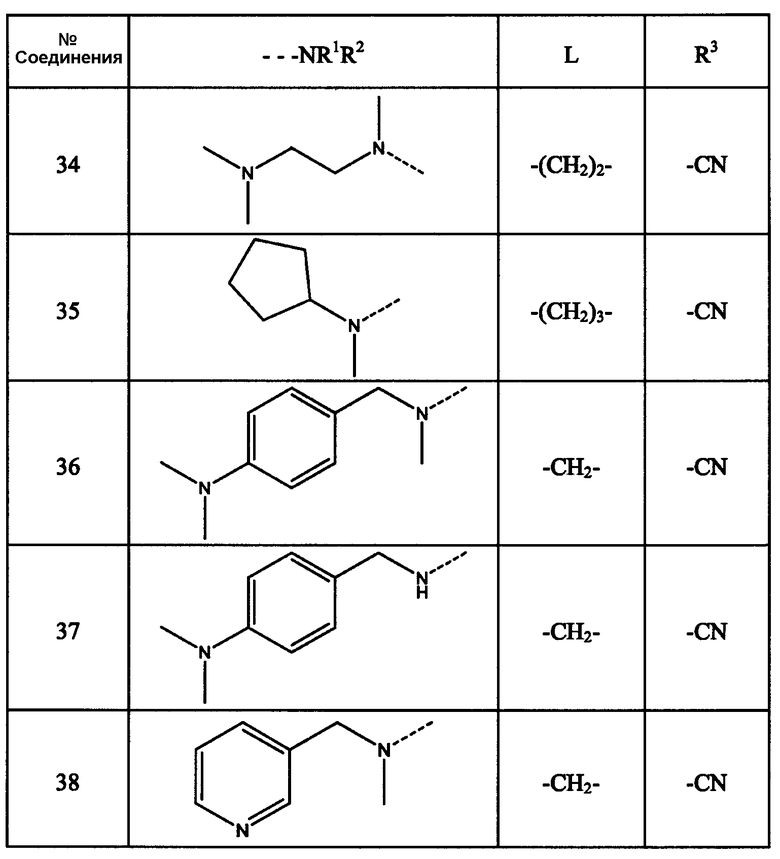
Пример 3: вирусологические свойства соединений настоящего изобретения
Соединения испытывали в клеточном анализе с использованием клеток МТ4-LTR-EGFP на противовирусную активность. Анализ показал, что указанные соединения проявляют сильную анти-ВИЧ-активность против лабораторного штамма ВИЧ дикого типа (штамм LAI ВИЧ-1) и вируса ВИЧ-1, резистентного ко многим лекарственным средствам (ВИЧ-1-MDR). Клеточный анализ проводили по следующей методике.
ВИЧ-инфицированные или ложно-инфицированные клетки МТ4-LTR-EGFP инкубировали в течение трех дней в присутствии различных концентраций ингибитора. После инфицирования GFP-репортер активируется вирусным tat-белком. В конце периода инкубации измеряли сигнал GFP. В вирусных контрольных образцах (в отсутствие любого ингибитора) получали максимальный флуоресцентный сигнал. Мониторинг ингибирующей активности соединения проводили на инфицированных вирусом клетках и выражали как ЕС50 и ЕС90. Эти величины представляют собой количество соединения, требуемого для защиты 50% и 90%, соответственно, клеток от вирусной инфекции.
Величины рЕС
50
(определены как отрицательный логарифм результата, выраженного как ЕС
50
) для испытанных соединений показаны ниже. Для некоторых соединений настоящего изобретения проводили более чем одну серию испытаний. В таком случае для определения активности класса применяли среднюю величину рЕС
50
.
Пример 4: фармацевтические композиции
Капсулы
Активный ингредиент, в случае соединения формулы (I), растворяют в органическом растворителе, таком как этанол, метанол или метиленхлорид, предпочтительно, смесь этанола и метиленхлорида. Полимеры, такие как сополимер поливинилпирролидона с винилацетатом (PVP-VA) или гидроксипропилметилцеллюлозу (НРМС), обычно мПа, растворяют в органических растворителях, таких как этанол, метанол, метиленхлорид. Подходящий полимер растворяют в этаноле. Растворы полимера и соединения смешивают и смесь затем сушат распылением. Отношение соединение/полимер выбирали от 1/1 до 1/6. Промежуточные диапазоны составляют от 1/1,5 до 1/3. Подходящим отношением является 1/6. Высушенным распылением порошком, твердая дисперсия, затем заполняют капсулы для введения. Лекарственное средство загружают в одну капсулу в количестве от 50 до 100 мг, в зависимости от размера применяемой капсулы.
Покрытые пленкой таблетки
Получение сердцевины таблетки
Смесь 100 г активного ингредиента, в случае соединения формулы (I), 570 г лактозы и 200 г крахмала хорошо смешивают и затем увлажняют раствором 5 г додецилсульфата натрия и 10 г поливинилпирролидона приблизительно в 200 мл воды. Влажную смесь порошков просеивают, сушат и снова просеивают. Затем в смесь добавляют 100 г микрокристаллической целлюлозы и 15 г гидрогенизированного растительного масла. Все компоненты хорошо смешивают и прессуют в таблетки, получая 10000 таблеток, причем каждая содержит 10 мг активного ингредиента.
Покрытие
К раствору 10 г метилцеллюлозы в 75 мл денатурированного этанола добавляют раствор 5 г этилцеллюлозы в 150 мл дихлорметана. Затем в раствор добавляют 75 мл дихлорметана и 2,5 мл 1,2,3-пропантриола. 10 г полиэтиленгликоля расплавляют и растворяют в 75 мл дихлорметана. Полученный раствор добавляют к первому, затем туда добавляют 2,5 г октадеканоата магния, 5 г поливинилпирролидона и 30 мл концентрированной суспензии красящего вещества и всю массу гомогенизируют. Сердцевины таблеток покрывают полученной таким образом смесью в устройстве для покрытия.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ 1,10b-ДИГИДРО-2-(АМИНОКАРБОНИЛФЕНИЛ)-5Н-ПИРАЗОЛО[1,5-c][1,3]БЕНЗОКСАЗИН-5-ИЛ)ФЕНИЛМЕТАНОНА В КАЧЕСТВЕ ИНГИБИТОРОВ РЕПЛИКАЦИИ ВИЧ ВИРУСА | 2005 |
|
RU2382789C2 |
| ВИЧ-ИНГИБИРУЮЩИЕ 5-КАРБО- ИЛИ ГЕТЕРОЦИКЛИЧЕСКИЕ ЗАМЕЩЕННЫЕ ПИРИМИДИНЫ | 2005 |
|
RU2403244C2 |
| ПИРИДО [2,3-d] ПИРИМИДИНЫ, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ HCV, И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2006 |
|
RU2444522C2 |
| ПРОИЗВОДНЫЕ 1, 2, 4-ТРИАЗИН-6-ОНА, ИНГИБИРУЮЩИЕ ВИЧ | 2005 |
|
RU2401833C2 |
| 5-АМИДО-ЗАМЕЩЕННЫЕ ПИРИМИДИНЫ, ИНГИБИРУЮЩИЕ ВИЧ | 2007 |
|
RU2480464C2 |
| ПРОИЗВОДНЫЕ ПИПЕРИДИНА/ПИПЕРАЗИНА | 2008 |
|
RU2478628C2 |
| ПРОИЗВОДНЫЕ ПИПЕРИДИНА/ПИПЕРАЗИНА | 2008 |
|
RU2470017C2 |
| 6,7,8,9-ЗАМЕЩЕННЫЕ 1-ФЕНИЛ-1,5-ДИГИДРОПИРИДО (3,2-b) ИНДОЛ-2-ОНЫ, ПОЛЕЗНЫЕ В КАЧЕСТВЕ АНТИИНФЕКЦИОННЫХ ФАРМАЦЕВТИЧЕСКИХ СРЕДСТВ | 2005 |
|
RU2377243C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ДИАМИНО-1,3,5-ТРИАЗИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЙ ПРОДУКТ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1997 |
|
RU2186774C2 |
| СОЕДИНЕНИЯ, ВОЗДЕЙСТВУЮЩИЕ НА ГЛЮКОКИНАЗУ | 2002 |
|
RU2329043C9 |
Настоящее изобретение относится к производным (5Н-пиразоло[1,5-с][1,3]бензоксазин-5-ил)фенилметанона, полезным в качестве ингибиторов вирусной репликации вируса ВИЧ, а также фармацевтическим композициям, их применению в качестве лекарственных средств. Соединения настоящего изобретения предназначены для предотвращения или лечения инфекции ВИЧ и для лечения СПИДа. 5 н. и 2 з.п. ф-лы, 2 табл.
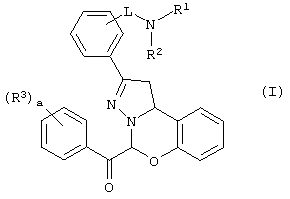
1. Соединение, имеющее формулу

его стереоизомерная форма или соль,
где а равно 1;
L представляет собой С1-4алкандиил;
R1 представляет собой С1-10алкил, С3-12циклоалкил или С1-10алкил, замещенный заместителем, выбранным из группы, состоящей из Het, арила, С3-12циклоалкила и дизамещенной аминогруппы, где заместители аминогруппы, каждый по отдельности, выбраны из С1-10алкила;
R2 представляет собой водород, С1-10алкил;
R3 представляет собой С1-10алкил, циано или С1-10алкилсульфонил;
арил представляет собой фенил, необязательно замещенный одним или несколькими заместителями, выбранными из группы, состоящей из С1-10алкилокси и дизамещенной аминогруппы;
Het представляет собой гетероцикл, выбранный из пиридинила и пирролидинила.
2. Соединение по п.1, представляющие собой
4-[2-(4-диэтиламинометилфенил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[а]нафталин-4-карбонил]бензонитрил;
4-{2-[4-(бензиламинометил)фенил]-1,9b-дигидро-5-окса-3,3а-диазациклопента[а]нафталин-4-карбонил}бензонитрил;
4-[2-(4-{[(пиридин-4-илметил)амино]метил}фенил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[а]нафталин-4-карбонил]бензонитрил;
4-[2-(4-{[(4-метоксибензил)метиламино]метил}фенил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[а]нафталин-4-карбонил]бензонитрил;
(4-трет-бутилфенил)-[2-(4-{[(4-метоксибензил)метиламино]метил}фенил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[а]нафталин-4-ил]метанон;
(4-трет-бутилфенил)-[2-(4-{[(пиридин-4-илметил)амино]метил}фенил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[а]нафталин-4-ил]метанон;
(4-трет-бутилфенил)-[2-(4-диэтиламинометилфенил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[а]нафталин-4-ил]метанон;
4-{2-[4-(2-диэтиламиноэтил)фенил]-1,9b-дигидро-5-окса-3,3а-диазациклопента[а]нафталин-4-карбонил}бензонитрил;
4-(2-{4-[(циклопентилметиламино)метил]фенил}-1,9b-дигидро-5-окса-3,3а-диазациклопента[а]нафталин-4-карбонил]бензонитрил;
4-(2-{4-[4-(4-метоксифениламино)бутил]фенил}-1,9b-дигидро-5-окса-3,3а-диазациклопента[а]нафталин-4-карбонил)бензонитрил;
(4-метансульфонилфенил)-[2-(4-{[(пиридин-4-илметил)амино]метил}фенил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[а]нафталин-4-ил]метанон;
(4-метансульфонилфенил)-[2-(4-{[(4-метоксибензил)метиламино]метил}фенил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[а]нафталин-4-ил]метанон;
[2-(4-диэтиламинометилфенил)-1,9b-дигидро-5-окса-3,3а-диазациклопента[а]нафталин-4-ил]-(4-метансульфонилфенил)метанон
или его стереоизомерную форму или соль.
3. Соединение по п.1 или 2, предназначенные для применения в качестве лекарственного средства, обладающего способностью ингибировать репликацию ВИЧ.
4. Применение соединения по п.1 или 2 при изготовлении лекарственного средства, предназначенного для лечения состояний, связанных с ВИЧ-инфекцией.
5. Применение соединения по п.1 или 2 при изготовлении лекарственного средства, предназначенного для предотвращения передачи ВИЧ или предотвращения ВИЧ-инфекции или предотвращения заболевания, связанного с ВИЧ-инфекцией.
6. Способ лечения, включающий системное введение терапевтически эффективного количества соединения по п.1 или 2 ВИЧ-инфицированным теплокровным животным, особенно, ВИЧ-инфицированным людям.
7. Фармацевтический препарат, обладающий способностью ингибировать репликацию ВИЧ, содержащий в качестве активного компонента эффективную дозу соединения по п.1 или 2 и дополнительно содержащий обычные фармацевтические нетоксичные эксципиенты и вспомогательные вещества.
| Червячный смеситель для полимерных материалов | 1986 |
|
SU1359147A1 |
| Многоканальное устройство синхронизации | 1970 |
|
SU563733A1 |
| Orlov V.D | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Chemistry of heterocyclic compounds (A translation of khimiya geterotsiklicheskikh soedinenii), New York, US, vol.27, 1991-08, p.910-914 | |||
| БЕНЗОКСАЗИНОНЫ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ ИХ ДЛЯ ИНГИБИРОВАНИЯ ОБРАТНОЙ ТРАНСКРИПЦИИ ВИЧ, ЛЕЧЕНИЯ И ПРЕДОТВРАЩЕНИЯ AIDS И ARC, СПОСОБ ИНГИБИРОВАНИЯ ВИЧ ОБРАТНОЙ ТРАНСКРИПТАЗЫ, СПОСОБ ПРЕДОТВРАЩЕНИЯ ИНФЕКЦИИ ВИЧ, ЛЕЧЕНИЯ ВИЧ И ARC, КОМБИНАЦИИ, СПОСОБ ПОЛУЧЕНИЯ (-)-6-ХЛОР-4-ЦИКЛОПРОПИЛЭТИНИЛ-4-ТРИФТОРМЕТИЛ-1,4-ДИГИДРО-2Н-3,1-БЕНЗОКСАЗ ИН-2-ОНА | 1993 |
|
RU2186775C2 |
Авторы
Даты
2011-04-20—Публикация
2006-04-11—Подача