Изобретение относится к области органической химии, к новым биологически активным веществам класса N-гетериламидов 4-арил-2,4-диоксобутановых кислот, а именно к N-(2-тиазолил)амиду 2-(2-оксо-3-индолинилиден)гидразино-4-оксо-4-фенил-2-бутеновой кислоты (1) формулы
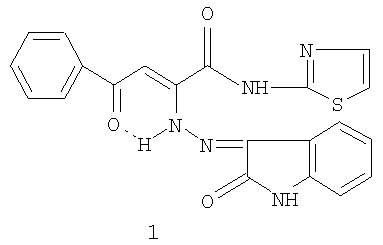
обладающему противомикробной и анальгетической активностью, что позволяет предположить его использование в медицине в качестве лекарственного противомикробного и анальгетического средства. Ближайшим аналогом по структуре и действию заявляемому соединению является N-(2-тиазолил)амид 2-гидрокси-4-оксо-4-фенил-2-бутеновой кислоты(2) [Андрейчиков Ю.С., Милютин А.В., Крылова И.В. и др. Синтез и биологическая активность гетериламидов ароилпировиноградных и 5-арилпиразол-3-карбоновых кислот// Хим.-фарм. журн. - 1990. - №7. - С.33-35] формулы
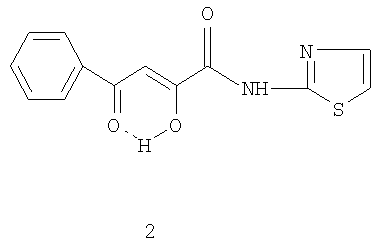
Структурный аналог 2 обладает слабой анальгетической активностью, недостаточной для практического здравоохранения. Данные по противомикробной активности структурного аналога 2 в литературе отсутствуют.
Эталонами сравнения выбраны
1) противомикробный препарат хлоргексидин [1,6-ди-(4-хлорфенилгуанидо)-гексан] (3), широко применяемый в лечебной практике и являющийся аналогом по действию [Машковский М.Д. Лекарственные средства. - 15-е изд., перераб., испр. и доп. - М.: ООО «Издательство Новая волна», 2005. - С.935-936];
2) анальгетический препарат метамизол натрия (1-фенил-2,3-диметил-4-метиламинопиразолон-5-N-метансульфонат натрия) (4), широко применяемый в лечебной практике и являющийся аналогом по действию [Машковский М.Д. Лекарственные средства. - 15-е изд., перераб., испр. и доп. - М.: ООО «Издательство Новая волна», 2005, - с.159-160]. Задачей изобретения является поиск в ряду производных N-гетериламидов 4-арил-2,4-диоксобутановых кислот веществ с выраженным противомикробным, анальгетическим действием и низкой токсичностью. Поставленная задача достигается получением N-(2-тиазолил)амида 2-(2-оксо-3-индолинилиден)гидразино-4-оксо-4-фенил-2-бутеновой кислоты (1), обладающего противомикробной и анальгетической активностью. Заявляемое соединение 1 синтезируют взаимодействием N-(2-тиазолил)амида 2-гидрокси-4-оксо-4-фенил-2-бутеновой кислоты (2) с 3-гидразоно-2-оксоиндолом при эквимолярном соотношении реагентов в среде безводного толуола при нагревании с последующим выделением целевого продукта известными методами по схеме:
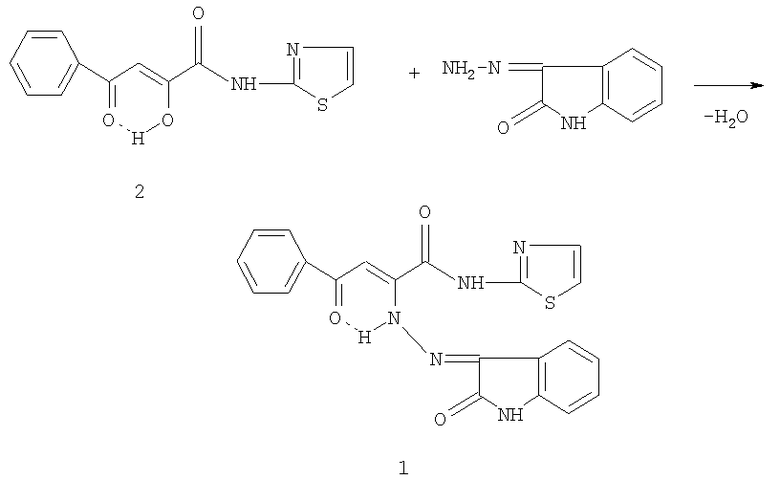
Пример получения соединения 1.
К суспензии 2,74 г (0,01 моль) N-(2-тиазолил)амида 2-гидрокси-4-оксо-4-фенил-2-бутеновой кислоты (2) в 50 мл безводного толуола прибавляют суспензию 1,61 г (0,01 моль) 3-гидразоно-2-оксоиндола в 35 мл безводного толуола и кипятят раствор 12 часов. Реакционную смесь охлаждают до комнатной температуры, выпавший осадок отфильтровывают, перекристаллизовывают из толуола и высушивают. Выход 3,59 г (86%). Т.пл. 118-120°С. Найдено, %: С 60.38; Н 3.66; N 16.75. C21H15N5O3S. Вычислено, %: С 60.42; Н 3.62; N 16.78.
ИК-спектр (Specord M80, вазелиновое масло, ν, см-1): 3360 (NHCO), 3180 (NHHt), 1685 (СОHt), 1670 (CONH), 1615, 1600 (C4=O, C=C, C=N). Спектр ЯМР 1Н (Bruker DRX 500, ДМСО-d6, ГМДС, δ, м.д.): 6.74 с (1Н, СН), 6.81-7.55 м (11Н, С6Н5, C6H4, C3H2NS), 7.99 с (NHCO), 10.57 с (NНHt), 12.98 с (NH-N=).
Заявляемое соединение 1 представляет собой желтое кристаллическое вещество, растворимое в толуоле, диоксане, ацетоне, диметилформамиде, нерастворимое в воде и гексане.
Определение бактериостатической активности проводили методом двукратных серийных разведений в жидкой питательной среде [Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ/ Фисенко В.П. (ред.). - М.: ИИА Ремедиум, 2000. - С.264-273]. Для всех исследуемых соединений были определены МПК в отношении фармакопейных штаммов: S. aureus ATCC 6538-Р и E.coli ATCC 25922. Результаты испытаний представлены в таблице. Посевы производили в мясопептонный бульон, рН 7,0, с различной концентрацией испытуемых соединений. Культуры выращивали в пробирках на скошенной агаризированной среде (мясопептонный агар). Для определения противомикробной активности использовалась 18-20-часовая культура. Для приготовления рабочей взвеси микробов производили смыв выросшей культуры изотоническим раствором натрия хлорида и устанавливали плотность микробной взвеси по стандарту мутности 5 единиц. Далее из полученной микробной взвеси (500 млн. м. т./мл) готовили рабочий раствор бактерий с концентрацией 5 млн. м. т./мл. Данную взвесь микробов вносили в количестве 0,1 мл в пробирки с серийными разведениями изучаемого препарата. Таким образом, микробная нагрузка при определении ПМА составила 250000 м. т./мл. Изучаемое соединение в количестве 0,05 г растворяли в 5 мл диметилформамида; 1 мл полученного разведения 1:100 соединяли с 4 мл мясопептонного бульона (1:500). Далее готовили ряд серийных разведений соединения с двукратно уменьшающейся концентрацией.
Учет результатов производили через 18-20 часов выдержки контрольных и опытных пробирок в термостате при температуре 37°С. Минимальную подавляющую концентрацию (МПК) устанавливали по отсутствию признаков роста на питательной среде: последняя пробирка с задержкой роста (прозрачный бульон) соответствует МПК препарата в отношении данного штамма. Бактериостатический эффект исследуемых соединений сравнивали с действием хлоргексидина.
Анальгетическая активность соединения 1 изучена на 12 белых беспородных мышах самцах массой 18-20 г по методу термического раздражения [В.В.Гацура. Методы первичных фармакологических исследований биологически активных веществ. - М.: Медицина, 1974. - С.39]. Исследуемое соединение 1 вводили в дозе 50 мг/кг перорально в виде взвеси в 2% крахмальном растворе за 30 минут до помещения животных на горячую пластинку. Показателем болевой чувствительности служила длительность пребывания мышей на пластинке до наступления оборонительного рефлекса - облизывания лапок. Контрольным животным вводили эквиобъемное количество 2% крахмального раствора. Препаратом сравнения служил метамизол натрия в дозе 50 мг/кг. Результаты обработаны статистически с помощью программы MS Excel, 2000 и представлены в таблице.
Острую токсичность (ЛД50) заявляемого соединения 1 определяли на 24 белых беспородных мышах обоего пола массой 18-22 г при пероральном пути введения в виде взвеси в 2% крахмальном растворе по экспресс-методу В.Б.Прозоровского [Прозоровский В.Б., Прозоровская М.П., Демченко В.М. Экспресс-метод определения средней эффективной дозы и ее ошибки// Фармакология и токсикология. - 1978. - №4. - С.497-502]. Установлено, что ЛД50 соединения 1 составляет 4500 мг/кг. Согласно классификации токсичности препаратов соединение 1 относится к классу практически нетоксичных веществ [Измеров И.Ф., Саноцкий И.В., Сидоров К.К. Параметры токсикометрии промышленных ядов. - М.: Медицина, 1977. - С.196-197]. Оно в 1,13 раз менее токсично, чем хлоргексидин и в 1,36 раза менее токсично, чем метамизол натрия. Как видно из таблицы, соединение 1 превышает по противомикробной активности хлоргексидин по отношению к золотистому стафилококку в 8 раз и к кишечной палочке - в 4 раза. Отношение МПК (мкг/мл) к токсичности ЛД50 (мг/кг) у соединения 1 составляет для стафилококка 0,0035 и для кишечной палочки 0,0069, в то время как у хлоргексидина эти показатели значительно уступают.
мизол
натрия
1- по сравнению с контролем; 2- по сравнению с метамизолом натрия.
В ходе проведенных исследований (см. таблицу) установлено, что соединение 1 проявляет выраженную анальгетическую активность на всех сроках наблюдения. Так, через 30 минут после введения оно действует на уровне метамизола натрия, а через 60 минут превышает по активности препарат сравнения в 1,3 раза. С учетом значений острой токсичности соединение 1 имеет определенные преимущества перед метамизолом натрия в плане его безопасности и эффективности.
Таким образом, N-(2-тиазолил)амид 2-(2-оксо-3-индолинилиден)гидразино-4-оксо-4-фенил-2-бутеновой кислоты (1) проявляет более высокую противомикробную и анальгетическую активность по сравнению со структурным аналогом и эталонами сравнения, а также является практически нетоксичным, что делает возможным использование его для создания новых лекарственных средств, обладающих противомикробной и анальгетической активностью.
Источники информации
1. Андрейчиков Ю.С., Милютин А.В., Крылова И.В. и др. Синтез и биологическая активность гетериламидов ароилпировиноградных и 5-арилпиразол-3-карбоновых кислот// Хим.-фарм. журн. - 1990. - №7. - С33-35.
2. Машковский М.Д. Лекарственные средства. - 15-е изд., перераб., испр. и доп. - М.: ООО «Издательство Новая волна», 2005. - С.159-160, 935-936.
3. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ/ Фисенко В.П. (ред.). - М.: ИИА Ремедиум. - 2000. - С.264-273.
4. В.В.Гацура. Методы первичных фармакологических исследований биологически активных веществ. - М.: Медицина, 1974. - С.39.
5. Прозоровский В.Б., Прозоровская М.П., Демченко В.М. Экспресс-метод определения средней эффективной дозы и ее ошибки// Фармакология и токсикология. - 1978. - №4. - С.497-502.
6. Измеров И.Ф., Саноцкий И.В., Сидоров К.К. Параметры токсикометрии промышленных ядов. - М.: Медицина, 1977. - С.196-197.
| название | год | авторы | номер документа |
|---|---|---|---|
| N-(2-БЕНЗОТИАЗОЛИЛ)АМИД 2-ГИДРОКСИ-4-ОКСО-4-(4-ХЛОРФЕНИЛ)-2-БУТЕНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЙ ПРОТИВОМИКРОБНОЙ И ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2396262C2 |
| N-(2-ТИАЗОЛИЛ)АМИД 3-БРОМ-2,4-ДИОКСО-4-ФЕНИЛБУТАНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЙ ПРОТИВОМИКРОБНОЙ АКТИВНОСТЬЮ | 2010 |
|
RU2459813C1 |
| БИС{3-ФЕНИЛ-1-[2-(5-МЕТИЛ-1,3,4-ТИАДИАЗОЛИЛ)]КАРБОКСАМИДО-1,3-ПРОПАНДИОНАТО}МАРГАНЕЦ, ОБЛАДАЮЩИЙ ПРОТИВОВОСПАЛИТЕЛЬНОЙ И АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2396263C2 |
| СУКЦИНАТ N-(2,4,6-ТРИМЕТИЛФЕНИЛ)АМИДА 2-(БЕТА-N, N-ДИЭТИЛАМИНОЭТИЛАМИНО)-4-ОКСО-4-(4-МЕТИЛФЕНИЛ)-2-БУТЕНОВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЙ МЕСТНОАНЕСТЕЗИРУЮЩУЮ И ПРОТИВОМИКРОБНУЮ АКТИВНОСТЬ | 2009 |
|
RU2428412C2 |
| N-ЗАМЕЩЕННЫЕ АМИДЫ 2-ГИДРОКСИ-4-ОКСО-4-(4-ХЛОРФЕНИЛ)2-БУТЕНОВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВОМИКРОБНУЮ АКТИВНОСТЬ | 2009 |
|
RU2429225C2 |
| 2-(5-ЭТИЛ-1,3,4-ТИАДИАЗОЛИЛ)АМИД 2-(4-БРОМФЕНИЛ)-4-ОКСО-4-ФЕНИЛ-2-БУТЕНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЙ АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2549572C2 |
| 2-ГИДРОКСИ-4-ОКСО-4-ФЕНИЛ-2-БУТЕНОАТ БЕНЗОТИАЗОЛИЛАММОНИЯ, ОБЛАДАЮЩИЙ ГИПОГЛИКЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2412177C2 |
| ГИДРОХЛОРИД N-(2,6-ДИМЕТИЛФЕНИЛ)АМИДА 2-(β-N,N-ДИЭТИЛАМИНОЭТИЛАМИНО)-4-ОКСО-4-(4-ЭТОКСИФЕНИЛ)-2-БУТЕНОВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЙ МЕСТНО-АНЕСТЕЗИРУЮЩУЮ АКТИВНОСТЬ | 2009 |
|
RU2412159C2 |
| 2-ГИДРОКСИ-4-ОКСО-4-(4-ХЛОРФЕНИЛ)-2-БУТЕНОАТ ТИАЗОЛИНАММОНИЯ, ОБЛАДАЮЩИЙ АНТИКОАГУЛЯНТНОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2461550C2 |
| Применение 3,4-диметил-6-(3-нитрофенил)-2-оксо-N-фенил-1,2,3,6-тетрагидропиримидин-5-карбоксамида в качестве средства, обладающего анальгетической активностью | 2022 |
|
RU2785688C1 |
Изобретение относится к N-(2-тиазолил)амиду 2-(2-оксо-3-индолинилиден)гидразино-4-оксо-4-фенил-2-бутеновой кислоты, обладающему противомикробной и анальгетической активностью, формулы
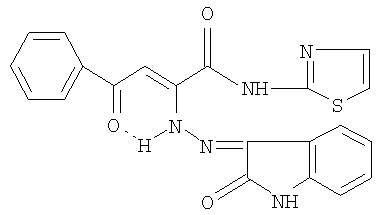
1 табл.
N-(2-Тиазолил)амид 2-(2-оксо-3-индолинилиден)гидразино-4-оксо-4-фенил-2-бутеновой кислоты формулы
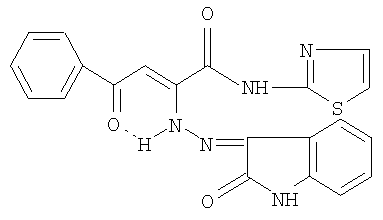
обладающий противомикробной и анальгетической активностью.
| Андрейчиков Ю.С.и др | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| ХИМИКО-ФАРМАЦЕВТИЧЕСКИЙ ЖУРНАЛ, 1990, №7, с.33-35 | |||
| WO 2004033439 A1, 22.04.2004. | |||
Авторы
Даты
2010-10-20—Публикация
2008-05-19—Подача