Изобретение относится к области ветеринарии и медицины, а именно к изучению инфекционных заболеваний, и может быть использовано для моделирования стадийности течения инфекции, прогнозирования клинического исхода и оценки схем лечения в эксперименте.
Известен способ моделирования и диагностики т.н. «конечной стадии» развития сибиреязвенной инфекции (токсического шока) у крыс линии Фишер 344 [Lincoln R.E., Walker J.S., Klein F., Rosen-Wald A.J., Jones W.J. Value of field data for extrapolation in anthrax. - Red Procceed. - 1967. - Vol.26, N5. - P.1558-1562. Ezzel J.W., Ivins B.E., Leppla S.H., Immunoelectrophoretic analysis, toxicity, and kinetics of in vitro production of the protective antigen and letal factor components of Bacillus anthracis toxin. - Infect. Immun. - 1984. - Vol.45, N3. - P.761-767. Ivins B.E., Welcos S.L. Cloning and expression of the Bacillus anthracis protective antigen in Bacillus subtilis. - Infect. Immun. - 1986. - Vol.54, N2. - P.537-542].
Способ предусматривает получение компонентов сибиреязвенного токсина в жидкой питательной среде, концентрирование, смешивание и парентеральное введение фильтрата крысам линии Фишер 344 с регистрацией симптоматики и времени их гибели. Способ имеет ряд недостатков: сложен в приготовлении препарата, применим только для изучения патогенетического действия токсина, не диагностирует инфекционно-токсический шок ввиду отсутствия этиологического фактора, а следовательно, не обеспечивает возможности определения степени генерализации (нарастания бактериемии и токсемии). Эти недостатки обусловлены чрезвычайно высокой чувствительностью крыс к токсину (для их гибели его требуется в 70 раз меньше, чем для гибели мышей, и в 170 раз меньше, чем для кроликов и обезьян) и их высокой резистентностью к заражению спорами (величина ЛД50 в 140·103 раз больше, чем у белых мышей, и в 140 раз больше, чем у кроликов и обезьян). По вышеизложенным причинам этот способ не позволяет осуществить оценку эффективности комплексных (антибактериальная + антитоксическая) схем лечения шока.
Известен способ посмертной анатомо-морфологической диагностики остропротекающей сибиреязвенной интоксикации у белых мышей, моделируемой внутрибрюшинным введением культуры спор вирулентного штамма 1СО в дозе 100-200 млн микробных клеток с регистрацией гибели животных через 12-14 часов [Патент RU №2173346. Проскурина В.А., Борисов И.В., Шиянова Е.С. Способ моделирования сибиреязвенного токсико-инфекционного шока, 2001]. Этот способ позволяет моделировать быстрое развитие сибиреязвенной инфекции у белых мышей с проявлением токсико-инфекционного шока, но обеспечивает лишь анатомо-морфологическую диагностику шока и воспроизводит условия его моделирования на биологической модели, далеко стоящей от человека по степени адекватности (подобия), что затрудняет осуществить прижизненную лабораторную диагностику степени (фазности) инфекционного процесса в организме и оценку полноты из-леченности в каждой из фаз генерализации.
Наиболее близким является способ, в котором для оценки эффективности лекарственных средств моделируется скрытая (инкубационный период), либо продромальная, или начальная (с появлением клинических признаков) стадия развития сибиреязвенной инфекции у животных [Проскурина В.А., Гребенкина М.Б., Фунтикова Т.Н. и др. Лечение сибиреязвенного токсического шока в условиях экспериментального заражения // Тезисы доклада к II Российскому Национальному конгрессу «Человек и лекарство», 10-15 апреля 1995, - М., 1995, - С.255. Инструкция по единой методике экспериментального изучения и клинических испытаний новых антибиотиков и химиопрепаратов для экстренной профилактики и лечения особо опасных инфекций. - М., 1980. Онищенко Г.Г., Васильев Н.Т., Литусов Н.В. и др. Сибирская язва: актуальные аспекты микробиологии, эпидемиологии, клиники, диагностики, лечения и профилактики. - М., 1999]. В данном способе в качестве условий моделирования и диагностических критериев стадийности используют заражение животных небольшими дозами 10-30 ЛД50, повышение температуры к 24 часам, фиксированные сроки начала лечения: 3 и 24 часа.
Однако заданные условия моделирования и диагностики фиксируют лишь начало развития инфекции, при которой общепринятые лекарственные средства являются эффективными, но не позволяют выявлять различий в эффективности антибактериальной и комбинированной схем лечения экспериментальной сибирской язвы. Кроме того, данный способ вследствие применения низких доз заражения и отсутствия объективных лабораторных критериев определения более поздних фаз развития инфекции не моделирует в заданные отрезки времени и не диагностирует токсико-инфекционный шок.
Задачей изобретения является создание условий моделирования фаз генерализации и комплекса критериев их прижизненной диагностики для изучения эффективности схем лечения поздних стадий сибирской язвы и прогнозирования клинического исхода.
Поставленная задача решается следующим образом.
Кроликам породы Шиншилла вводят подкожно суспензию спор сибиреязвенного штамма Ч-7 в дозе, соответствующей величине 500 ЛД50. Клиническое наблюдение и определение I-V фаз (стадий) генерализации осуществляют по следующим критериям: уровню бактериемии методом подсчета цепочек в мазках крови и высевом на плотную питательную среду (БК - биологическая концентрация) [Методические указания по микробиологической диагностике инфекционных заболеваний. - Горький, 1964]; уровню токсемии - методом иммуноферментного анализа содержания протективного антигена [Kobiler D., Weiss S., Levy H. et al. Protective antigen as a Correlative Marker for Anthrax // Infect. Immun. - 2006, - Vol.74, - P.5871-5876]; биохимической активности: поглотительной способности нейтрофилов и цитоморфологии клеток крови цитохимическими методами определения лизосомальных белков (ЛКТ), фагоцитарной активности нейтрофилов (ФАН) и степени деструкции нейтрофильных лейкоцитов и эритроцитов [Педиатрия. Руководство. Инфекционные заболевания / Под ред. Р.Е.Бермана, В.К.Вагана. - М., 1992].
С использованием комплекса микробиологических, цитологических и иммунологических методов детекции достигается возможность прижизненной диагностики фаз (стадий) генерализации экспериментальной сибиреязвенной инфекции и выбора наиболее эффективных схем лечения поздних стадий за счет использования более адекватной человеку биологической модели, клинико-лабораторных показателей, метода математического моделирования инфекции и прогнозирования клинического исхода у леченых и нелеченых животных.
Предложенное решение осуществляется следующим образом. Экспериментально определяют значения показателей функционального состояния организма, бактериемии, токсемии и цитоморфологии клеток крови. С учетом граничных значений показателей (таблица 1) выделяют в патологическом процессе соответствующую фазу (стадию) генерализации инфекции. Для первой - начальной фазы (стадии) характерен сравнительно невысокий уровень бактериемии: до 9·103 колониеобразующих единиц (КОЕ)·см-3, или появление одной цепочки в 10-20 полях зрения на фоне незначительного ухудшения общего функционального состояния животных и без существенного изменения цитохимических (от 1,9 до 2,4 усл. ед.) и цитоморфологических (отсутствует агрегация и дефекты в клеточной оболочке нейтрофилов и эритроцитов) показателей. Концентрация токсина в крови (по содержанию протективного антигена - ПА) составляет 0,005-0,090 мкг·см-3.
Вторая (активация патологического процесса) и третья («разгар») фазы генерализованного процесса различаются между собой в основном по концентрации возбудителя и токсина в крови. Для второй фазы развития генерализации инфекционного процесса характерны следующие диапазоны значений показателя бактериемии: 1 цепочка в 1-2 полях зрения при микроскопии и 1,0·104-4,0·104 КОЕ·см-3 по высеву, содержание токсина 0,1-0,3 мкг·см-3. В третьей фазе («разгара») имеет место существенное увеличение этих показателей: 2-4 цепочки в каждом поле зрения, 0,5·105-1,0·106 КОЕ·см-3, 1-3 мкг·см3 токсина соответственно. При этом наблюдается ухудшение функционального состояния кроликов. Величины таких показателей, как ФАН и ЛКТ, по мере утяжеления инфекционного процесса имеют тенденцию к снижению с 2,1-2,3 (II фаза) до 1,4-2,2 усл. ед. (III фаза) - для ФАН, и с 1,9-2,1 (II фаза) до 1,7-2,2 усл. ед. (III фаза) - для ЛКТ.
Следует подчеркнуть, что значение показателя ФАН, равное 1,5 усл. ед., встречающееся в III фазе в 50% случаев, является прогностически неблагоприятным признаком, поскольку эффективность антибактериального лечения резко снижается: со 100% при ФАН, равной 1,9-2,2 усл. ед., до 0-33% при ФАН, равной 1,5±0,1 усл. ед. При этом отмечается выраженная агрегация (по 3-11) эритроцитов.
На четвертой (предтерминальной или преморбидной) и пятой (терминальной) фазах генерализации концентрация возбудителя в крови составляет 2,0·106-6,0·106 КОЕ·см-3 и 7,0·106-4,0·107 соответственно или 5-17 и 18-35 цепочек в каждом поле зрения; содержание токсина в крови увеличивается до 4,0-7,0 мкг·см-3 (IV фаза) и до 8-25 мкг·см-3 и более - в V фазе. При этом для четвертой фазы характерной особенностью является выраженная агрегация эритроцитов и их деформация (более чем у 40% клеток), превышение индекса дегенерации лейкоцитов величины 50. Пятая фаза сопровождается лизисом эритроцитов и усилением дегенерации нейтрофилов. Значения цитохимических показателей резко уменьшаются - до 1,1-1,5 усл. ед. (ЛКТ) и 1,00-1,45 усл. ед. (ФАН). Более того, если на первых четырех фазах заболевания отмечается подъем температуры, то на пятой фазе генерализации обнаруживается резкое ее падение - с 40°С до 37°С.
Усиление тяжести течения сибиреязвенной инфекции при ее генерализации связано с нарастанием бактериемии и токсемии. Наличие агрегации клеток крови и их деформация на III-V фазах генерализации (т.н. «каркасы» нейтрофилов, эритроцитов, т.е. базофильных окрашенных зон клеток), как и угнетение фагоцитарной и биохимической активности лейкоцитов свидетельствует об усилении цитопатогенного действия сибиреязвенного токсина и гемолизина. Вышеуказанные изменения являются характерными признаками диссеминированного васкуляторного синдрома при инфекционно-токсическом шоке, интенсивность которого в заданных экспериментом условиях нарастает от III к V фазе.
Для прогнозирования времени начала I-V фаз (tiD) и срока гибелей (tп) кроликов в зависимости от инфицирующей дозы (D) используются следующие аппроксимирующие соотношения:
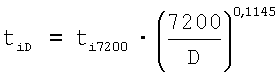 и tп=88,397·D-0,1145.
и tп=88,397·D-0,1145.
Сравнение рассчитанных и экспериментальных данных, приведенных в таблице 2, показывает, что прогнозируемые и реально получаемые характеристики близки или совпадают. Вышеуказанные соотношения наиболее удовлетворительно прогнозируют наступление времени начала I-V фаз генерализации и гибели кроликов при дозе, соответствующей величине 500 ЛД50.
Прогнозируемый уровень бактериемии (сп) рассчитывается по формулам, аппроксимирующим экспериментальные данные для инфицирующей дозы 500 ЛД50 и отрезков времени 7-25 ч и 26-29 ч соответственно.
сп=ехр(а+в·t+c·t2),
где a=5,0953, в=-0,3475, с=0,02487 при 7 ч≤t≤25 ч;
cп=ехр (-389,4259+28,0734·t-0,48494·t2), при 26 ч≤t≤29 ч.
Из данных, представленных в таблице 3, следует, что прогнозируемые уровни бактериемии для моментов времени 12, 20, 23, 26, 27, 29 ч удовлетворительно согласуются с экспериментальными данными.
Оценку эффективности новых средств и схем лечения генерализованной формы экспериментальной сибирской язвы проводят с учетом определения фаз генерализации и коэффициентов эффективности общепринятых схем лечения.
Результаты оценки эффективности двух типов схем терапии кроликов, приведенные в таблице 4, свидетельствуют о возможности использования способа определения генерализации инфекции для изучения новых лекарственных средств и выбора схем лечения, дающих максимальный терапевтический эффект на ранних или поздних стадиях заболевания.
I
II
III
IV
V
Разрушение клеточной оболочки при С от 20 до 35 и более цепочек, пойкилоцитоз, анизоцитоз
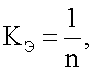 где n - количество (в долях) леченых, но погибших животных.
где n - количество (в долях) леченых, но погибших животных.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОМПЛЕКСНОЙ ПРОФИЛАКТИКИ СИБИРСКОЙ ЯЗВЫ | 2002 |
|
RU2216349C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ СИБИРЕЯЗВЕННОГО ТОКСИКО-ИНФЕКЦИОННОГО ШОКА | 1999 |
|
RU2173346C2 |
| Способ прогнозирования возможности возникновения гнойной инфекции у новорожденных | 1988 |
|
SU1649360A1 |
| СПОСОБ ВЫЯВЛЕНИЯ НАРУШЕНИЯ ФУНКЦИИ ФАГОЦИТОВ ПРИ РАЗВИТИИ РЕЦИДИВИРУЮЩИХ ИНФЕКЦИОННЫХ ПРОЦЕССОВ | 2007 |
|
RU2362997C2 |
| СРЕДСТВО ДЛЯ ИММУНОСТИМУЛЯЦИИ | 1998 |
|
RU2145500C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФАГОЦИТАРНОЙ АКТИВНОСТИ НЕЙТРОФИЛОВ ПЕРИФЕРИЧЕСКОЙ КРОВИ ЖИВЫХ ОРГАНИЗМОВ | 2003 |
|
RU2242763C1 |
| СПОСОБ МЕСТНОЙ ИММУНОТЕРАПИИ ГНОЙНЫХ РАН ЧЕЛЮСТНО-ЛИЦЕВОЙ ОБЛАСТИ | 2007 |
|
RU2361626C2 |
| СПОСОБ ДИАГНОСТИКИ СТЕПЕНИ ТЯЖЕСТИ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ ПО ПОКАЗАТЕЛЯМ ФУНКЦИОНАЛЬНОГО РЕЗЕРВА ФАГОЦИТАРНОГО ЗВЕНА СИСТЕМЫ ИММУНИТЕТА | 2023 |
|
RU2800407C1 |
| СПОСОБ СНИЖЕНИЯ РИСКА РАЗВИТИЯ ПОСЛЕРОДОВЫХ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ МАТКИ У КОРОВ | 2016 |
|
RU2634964C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ У СПОРТСМЕНОВ В СОРЕВНОВАТЕЛЬНЫЙ ПЕРИОД | 1994 |
|
RU2104541C1 |
Способ по изобретению предусматривает создание условий моделирования фаз генерализации экспериментальной сибирской язвы и комплекса критериев их прижизненной диагностики для изучения эффективности схем лечения поздних стадий сибирской язвы и прогнозирования клинического исхода. Для осуществления способа используют кроликов, которым вводят подкожно суспензию спор сибиреязвенного штамма Ч-7. Определяют фазы генерализации по результатам анализа крови: по количеству цепочек в мазках крови, концентрации живых клеток, содержанию сибиреязвенного токсина и лизосомально-катионных белков, фагоцитарной активности нейтрофилов, агломерации и деформации эритроцитов, степени дегенерации лейкоцитов. Установлены 5 фаз (стадий) генерализации сибиреязвенной инфекции, определены диапазоны значений клинико-лабораторных показателей и эффективность антибактериального лечения. Способ по изобретению может быть использован для моделирования стадийности течения инфекции, вызванной возбудителем сибирской язвы, прогнозирования клинического исхода и оценки схем лечения в эксперименте. 4 табл.
Способ прижизненной диагностики фаз генерализации экспериментальной сибирской язвы, включающий заражение лабораторных животных инфектом и диагностику функциональных систем, отличающийся тем, что в качестве лабораторных животных используют кроликов, вводят им подкожно суспензию спор сибиреязвенного штамма Ч-7 в дозе, соответствующей величине 500 ЛД50, и в процессе клинического наблюдения определяют фазы генерализации по результатам анализов крови по следующим критериям: количеству цепочек в мазках крови, концентрации живых клеток в крови при высеве на плотную питательную среду, содержанию сибиреязвенного токсина в крови, фагоцитарной активности нейтрофилов, содержанию лизосомально-катионных белков, агломерации и деформации эритроцитов, степени дегенерации лейкоцитов, причем I фазе соответствуют:
I цепочка в 10-20 полях зрения микроскопа,
от 50 до 9·103 КОЕ·см-3 при высеве,
от 0,005 до 0,090 мкг·см-3 токсина,
от 1,9 до 2,4 усл. ед. фагоцитарной активности нейтрофилов (ФАН),
от 1,9 до 2,4 усл. ед. лизосомально-катионных белков (ЛКТ),
отсутствие агломерации и деформации эритроцитов,
индекс дегенерации лейкоцитов менее 50;
II фазе соответствуют:
1 цепочка в 1-2 полях зрения микроскопа,
от 1,0·104 до 4,0·104 КОЕ·см-3 при высеве,
от 0,1 до 0,3 мкг·см-3 токсина,
от 2,1 до 2,3 усл. ед. фагоцитарной активности нейтрофилов (ФАН),
от 1,9 до 2,1 усл. ед. лизосомально-катионных белков (ЛКТ),
отсутствие агломерации и деформации эритроцитов,
индекс дегенерации лейкоцитов менее 50;
III фазе соответствуют:
от 2 до 4 цепочек в каждом поле зрения микроскопа,
от 0,5·105 до 1,0·106 КОЕ·см-3 при высеве,
от 1,0 до 3,0 мкг·см-3 токсина,
от 1,4 до 2,2 усл. ед. фагоцитарной активности нейтрофилов (ФАН),
от 1,7 до 2,2 усл. ед. лизосомально-катионных белков (ЛКТ),
наличие агломерации по 3-11 эритроцитов,
индекс дегенерации лейкоцитов менее 50;
IV фазе соответствуют:
от 5 до 17 цепочек в каждом поле зрения микроскопа,
от 2,0·106 до 6,0·106 КОЕ·см-3 при высеве,
от 4,0 до 7,0 мкг·см-3 токсина,
от 1,20 до 1,45 усл. ед. фагоцитарной активности нейтрофилов (ФАН),
от 1,2 до 1,6 усл. ед. лизосомально-катионных белков (ЛКТ), наличие агломерации и разрыхления (деформации) оболочек у менее чем 50% эритроцитов,
индекс дегенерации лейкоцитов более 50;
V фазе соответствуют:
от 18 до 35 цепочек в каждом поле зрения микроскопа,
от 7,0·106 до 40,0·106 КОЕ·см-3 при высеве,
от 8,0 до 25,0 мкг·см-3 токсина и более,
от 1,00 до 1,45 усл. ед. фагоцитарной активности нейтрофилов (ФАН),
от 1,1 до 1,5 усл. ед. лизосомально-катионных белков (ЛКТ),
наличие агломерации и деформации оболочек у более чем 50% эритроцитов, индекс дегенерации лейкоцитов более 50.
| СПОСОБ МОДЕЛИРОВАНИЯ СИБИРЕЯЗВЕННОГО ТОКСИКО-ИНФЕКЦИОННОГО ШОКА | 1999 |
|
RU2173346C2 |
| ОНИЩЕНКО Г.Г | |||
| с соавт | |||
| Сибирская язва: актуальные аспекты микробиологии, эпидемиологии, клиники, диагностики, лечения и профилактики | |||
| Металлический водоудерживающий щит висячей системы | 1922 |
|
SU1999A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕМОЛИТИЧЕСКОЙ АКТИВНОСТИ И ЕЕ ТИПА У B.ANTHRACIS | 2002 |
|
RU2238316C2 |
Авторы
Даты
2010-10-27—Публикация
2009-05-12—Подача