Область техники
Настоящее изобретение относится к биотехнологии, конкретно к способу продукции пуриновых рибонуклеозидов, таких как инозин и гуанозин, представляющих ценность в качестве сырья для синтеза 5'-инозиновой кислоты и 5-гуаниловой кисоты, соответственно. Более конкретно, настоящее изобретение относится к новому, устойчивому к ингибированию по типу обратной связи ферменту, вовлеченному в биосинтез пуринов. Более конкретно, настоящее изобретение касается новой, устойчивой к ингибированию по типу обратной связи мутантной фосфорибозилпирофосфатсинтетазы (PRPP synthetase - phosphoribosylpyrophosphate synthetase) из бактерий рода Bacillus. Данное изобретение также относится к способу продукции пуриновых рибонуклеозидов и пуриновых рибонуклеотидов путем ферментации с использованием бактериальных штаммов, содержащих устойчивый к ингибированию по типу обратной связи фермент, кодируемый мутантным геном prs.
Описание предшествующего уровня техники
Существуют известные способы ферментативной продукции пуриновых нуклеозидов с использованием ауксотрофных по аденину штаммов или таких штаммов, которым, кроме того, придана устойчивость к различным соединениям, таким как аналоги пурина и сульфагуанидин, каковые штаммы принадлежат к роду Bacillus (опубликованные патенты Японии Nos.38-23039 (1963), 54-17033 (1979), 55-2956 (1980), и 55-45199 (1980), выложенная патентная заявка Японии No.56-162998 (1981), опубликованные патенты Японии Nos.57-14160 (1982) и 57-41915 (1982) и выложенная патентная заявка Японии No.59-42895 (1984)) или к роду Brevibacterium (опубликованные патенты Японии Nos.51-5075 (1976) и 58-17592 (1972), и Agric. Biol. Chem., 42, 399 (1978)), или к роду Escherichia (международная заявка РСТ WO 9903988) и подобные им. Традиционное получение таких мутантных штаммов включает мутагенную обработку микроорганизмов, такую как УФ-облучение и обработка нитрозогуанидином (N-метил-N'-нитро-М-нитрозогуанидин), и отбор искомого штамма с использованием соответствующей селективной среды. С другой стороны, получение таких мутантных штаммов с использованием методов генной инженерии также практикуется для штаммов, принадлежащих к роду Bacillus (выложенные патентные заявки Японии Nos. 58-158197 (1983), 58-175493 (1983), 59-28470 (1984), 60-156388 (1985), 1-27477 (1989), 1-174385 (1989), 3-58787 (1991), 3-164185 (1991), 5-84067 (1993) и 5-192164 (1993), патент США 7326546 (2008)) и к роду Brevibacterium (выложенная патентная заявка Японии No.63-248394 (1988)). Продуктивность этих штаммов-продуцентов инозина может быть дополнительно улучшена путем увеличения способности к секреции инозина (патентные заявки РФ 2002101666, 2002104463 и 2002104464).
5-Фосфорибозил-α-1-пирофосфат (далее - "PRPP") и глутамин являются исходными субстратами при биосинтезе пуринов. PRPP-синтетаза [ЕС 2.7.6.1], катализирующая реакцию рибозо-5-фосфата с АТФ с образованием PRPP и АМФ, связывает пентозофосфатный путь с биосинтезом пуриновых и пиримидиновых нуклеотидов, с биосинтезом гистидина и триптофана и пиридин-нуклеотидных коферментов (Jensen K..F. In Metabolism of Nucleotides, Nucleosides and Nucleobases in Microorganisms (ed. Munch-Petersen A.), 1-25. Academic Press, London; 1983).
PRPP-синтетаза подвержена ингибированию пуринами, пиримидинами и аминокислотами по типу обратной связи. Многие пуриновые нуклеотиды ингибируют активность PRPP-синтетазы конкуретно с адениозин-5'-трифосфатом (далее, "АТР"). Однако единственный сильный нуклеотидный ингибитор - это аденозин-5'-дифосфат (ADP-adenosine-5'-diphosphate); он конкурирует с АТР и является аллостерическим ингибитором, который связывается с сайтом, отличным от активного центра (Hove-Jensen, В. et al., J. Biol. Chem. 261: 6765-6771 (1986); Amvig K. et al., Eur. J. Biochem. 192:195-200 (1990)).
Известно, что гиперурикемия человека и подагра обусловлены повышенной активностью и устойчивостью к пуриновым нуклеотидам PRPP-синтетазы (Becker M.A. et al. Arthritis Rheum, 18:6 Suppl: 687-94 (1975); Zoref E. et al., J. Clin. Invest., 56: 1093-9 (1975); Becker M.A. et al., J. Clin. Invest., 96: 2133-41 (1995)). Сверхсинтез мочевой кислоты у лиц с повышенной активностью PRPP-синтетазы является результатом повышенной продукции PRPP и последующего ускорения синтеза пуриновых нуклеотидов de novo. Показано, что повышенная активность PRPP-синтетазы является результатом нескольких мутаций в соответствующем гене, представляющих собой специфическую замену аминокислотных остатков в ферменте человека: аспарагина на гистидин в положении 51, аспарагина на серин в положении 113, лейцина на изолейцин в положении 128, аланина на валин в положении 189. Такая мутантная PRPP-синтетаза устойчива к пуриновым нуклеотидам, ингибирующим нормальный фермент по механизму, неконкурентному по отношению к АТР (Roessler. B.J. et al. J. Biol. Chem., v.268, No 35, 26476-26481 (1993); Becker, M.A. et al., J. Clin. Invest., 96: 2133-41 (1995)).
Раскрыт процесс продукции пуриновых нуклеозидов через ферментацию микроорганизма, принадлежащего к роду Escherichia и имеющего способность к продукции пуринового нуклеозида, с мутацией prs D128A (патентная заявка США 20070161090 (2007)). Кроме того, описан способ продукции L-гистидина с использованием мутантной PRPP-синтетазы, отличающейся тем, L-аминокислотный остаток, соответствующий положению 115 в PRPP-синтетазе дикого типа Escherichia coli замещен другим аминокислотным остатком (патентная заявка США 20050176033, (2005)). Кроме того, показано, что штамм Ashbya gossypii с повышенной экспрессией мутантной PRPP-синтетазы с мутацией H196Q, устойчивой к ингибированию ADP, синтезирует больше рибофлавина, чем штамм с повышенной экспрессией PRPP-синтетазы дикого типа (патент США 6878536 (2005)). Однако в настоящее время нет сообщений, описывающих мутантную PRPP-синтетазу из бактерии рода Bacillus, устойчивую к ингибированию пуриновыми нуклеотидами по типу обратной связи, и использование такой мутантной PRPP-синтетазы для улучшения продукции нуклеозида с использованием микроорганизма - продуцента пуринового нуклеозида, принадлежащего к роду Bacillus, в частности Bacillus subtilis и Bacillus amyloliquefaciens. Более того, последовательность гена prs Bacillus amyloliquefaciens К никогда ранее не была опубликована.
Описание изобретения
Целью настоящего изобретения является усовершенствование микроорганизма, предназначенного для продукции пуриновых нуклеозидов путем ферментации, и предоставление способа продукции пуриновых нуклеозидов с использованием полученных штаммов.
Эта цель была достигнута путем конструирования новой мутантной PRPP-синтетазы из Bacillus. С учетом большой степени консервативности белка PRPP-синтетазы (Eriksen Т. et al.. Nature Struct. Biol, v.7, No 4, pp.303-308 (2000)), сконструировали мутантные PRPP-синтетазы из В. subtilis и В. amyloliquefaciens с мутациями, соответствующими известным мутациям в ферменте человека. Было показано, что только некоторые мутации при введении в ген, кодирующий PRPP-синтетазу, приводят к увеличению продукции пуриновых нуклеозидов в штаммах-продуцентах пуриновых нуклеозидов. Таким образом было сделано настоящее изобретение.
Настоящее изобретение предоставляет бактерию, принадлежащую к роду Bacillus, конкретно Bacillus subtilis и Bacillus amyloliquefaciens, обладающую повышенной способностью к продукции пуриновых нуклеозидов.
Целью настоящего изобретения является предоставление мутантной бактериальной фосфорибозилпирофосфатсинтетазы (PRPP-синтетазы), отличающейся тем, что L-аминокислотный остаток, соответствующий положению 120, или 135, или 194 в последовательности PRPP-синтетазы дикого типа Bacillus subtilis, замещен остатком другой L-аминокислоты, и чувствительность фермента к ингибированию пуриновыми нуклеотидами по типу обратной связи снижена.
Также целью настоящего изобретения является предоставление описанной выше мутантной PRPP-синтетазы, отличающейся тем, что остаток аспарагина в положении 120 в последовательности PRPP-синтетазы дикого типа замещен остатком серина.
Также целью настоящего изобретения является предоставление описанной выше мутантной PRPP-синтетазы, отличающейся тем, что остаток лейцина в положении 135 в последовательности PRPP-синтетазы дикого типа замещен остатком изолейцина.
Также целью настоящего изобретения является предоставление описанной выше мутантной PRPP-синтетазы, отличающейся тем, что остаток аланина в положении 194 в последовательности PRPP-синтетазы дикого типа замещен остатком Валина.
Также целью настоящего изобретения является предоставление описанной выше мутантной PRPP-синтетазы, отличающейся тем, что PRPP-синтетазой дикого типа является PRPP-синтетаза из Bacillus subtilis или Bacillus amyloliquefaciens.
Также целью настоящего изобретения является предоставление описанной выше мутантной PRPP-синтетазы, включающей делецию, замену, вставку или добавление одной или нескольких аминокислот в одном или во множестве положений, отличных от положения 120, или 135, или 194, отличающейся тем, что ингибирование фермента пуриновыми нуклеотидами по типу обратной связи снижено.
Также целью настоящего изобретения является предоставление ДНК, кодирующую описанную выше мутантную PRPP-синтетазу.
Также целью настоящего изобретения является предоставление бактерии, содержащей описанную выше ДНК и обладающей способностью к продукции пуриновых нуклеозидов.
Также целью настоящего изобретения является предоставление указанной бактерии, отличающейся тем, что указанной бактерией является Bacillus subtilis.
Также целью настоящего изобретения является предоставление указанной бактерии, отличающейся тем, что указанной бактерией является Bacillus amyloliquefaciens.
Также целью настоящего изобретения является предоставление способа продукции пуринового нуклеозида, включающего культивирование описанной выше бактерии в питательной среде, приводящее к секреции указанного пуринового нуклеозида в указанную питательную среду, и выделение указанного пуринового нуклеозида из культуральной жидкости.
Также целью настоящего изобретения является предоставление описанного выше способа, отличающегося тем, что пуриновым нуклеозидом является инозин, ксантозин, гуанозин или аденозин.
Также целью настоящего изобретения является предоставление способа продукции пуринового нуклеотида, включающего культивирование описанной выше бактерии в питательной среде, приводящее к секреции указанного пуринового нуклеозида в указанную питательную среду, выделение указанного пуринового нуклеозида из культуральной жидкости, фосфорилирование указанного пуринового нуклеозида и выделение пуринового нуклеотида.
Также целью настоящего изобретения является предоставление описанного выше способа, отличающегося тем, что пуриновым нуклеотидом является 5'-инозиновая кислота, ксантозин-5'-фосфат, 5'-гуаниловая кислота или 5'-адениловая кислота.
PRPP-синтетаза с заменой L-аминокислотного остатка, соответствующего положению 120, или 135, или 194 в последовательности PRPP-синтетазы дикого типа Bacillus может упоминаться как "мутантная PRPP-синтетаза", ДНК, кодирующая мутантную PRPP-синтетазу, может упоминаться как "мутантный ген prs" или "мутантный ген PRPP-синтетазы", а PRPP-синтетаза без замены может упоминаться как "PRPP-синтетаза дикого типа". Термин "мутантная PRPP-синтетаза" означает, что активность фермента благодаря мутациям, приводящим к замене аминокислотных остатков в положении 120, или 135, или 194, ингибируется пуриновыми нуклеотидами, в частности ADP, в меньшей степени, чем фермент штамма дикого типа.
Далее настоящее изобретение будет подробно описано.
1. Мутантная PRPP-синтетаза и мутантный ген prs согласно настоящему изобретению.
Известно, что повышенная активность PRPP-синтетазы человека является результатом нескольких мутаций соответствующего гена, приводящих к специфической замене аминокислотных остатков в зрелом ферменте: аспарагина на гистидин в положении 51, аспарагина на серии в положении 113, лейцина на изолейцин в положении 128, аланина на валин в положение 189. Такая мутантная PRPP-синтетаза устойчива к пуриновым нуклеотидам, ингибирующим нормальный фермент по механизму, неконкурентному в отношении АТР (Becker M.A. et al., J. Clin. Invest., 96: 2133-41 (1995)). С учетом большой степени консервативности гена prs (Eriksen Т. et al. Nature Struct. Biol, v.7, No 4, pp.303-308 (2000)), сконструировали мутантные PRPP-синтетазы Bacillus с мутациями D58H, N120S, L135I или A194V, соответсвующими мутациям N51H, N113S, L128I или A189V в ферменте человека. Такие мутации неизвестны для Bacillus PRPP-синтетаз. Термин "PRPP-синтетаза из Bacillus" означает PRPP-синтетазу бактерий, принадлежащих к роду Bacillus. Предпочтительны виды В. subtilis или В. amyloliquefaciens.
Мутантную PRPP-синтетазу получали с учетом известных последовательностей путем введения мутаций в ген prs дикого типа с использованием общепринятых методов. В качестве гена prs дикого типа могут быть упомянуты ген prs из В. subtilis (нуклеотиды с 57743 по 58696 в последовательности с инвентарным номером NC_000964 в базе данных GenBank; SEQ ID NO: 1) или ген prs из В. amyloliquefaciens К (SEQ ID NO: 3). Ген pr В. subtilis расположен между ORF gcaD и ORF ctc на хромосоме штамма В. subtilis 168. Следовательно, ген prs можно получить методом ПЦР (White, T.J. et al. Trends Genet., 5, 185 (1989)) с использованием праймеров, сконструированных на основании нуклеотидной последовательности гена. Ген, кодирующий PRPP-синтетазу В. amyloliquefaciens К (SEQ ID NO: 1), можно получить сходным образом.
Мутантная PRPP-синтетаза может включать делению, замену, вставку или добавление одной или нескольких аминокислот в одном или во множестве положений, отличных от положения 120, или 135, или 194, при условии, что активность PRPP-синтетазы не нарушена. Термин "активность PRPP-синтетазы" означает активность катализа реакции образования 5-фосфорибозил-α-1-пирофосфата (PRPP) из рибозо-5-фосфата и АТР с образованием AMP. Активность PRPP-синтетазы в экстрактах и степень ингибирования фермента ADP можно измерить с использованием частично модифицированного метода К. F. Jensen et al. (Analytical Biochemistry, 98, 254-263 (1979)). Конкретно, в качестве субстрата можно использовать [α-32P]ATP и следует определять образующийся в реакции [32P]AMP.
Количество "несколько" аминокислот различается в зависимости от положения или типа аминокислотных остатков в третичной структуре белка. Это связано со следующими причинами. А именно, некоторые аминокислоты имеют высокую степень гомологии друг с другом и поэтому такие изменения не очень влияют на третичную структуру белка. Следовательно, мутантная PRPP-синтетаза настоящего изобретения может быть ферментом с гомологией не менее 30-50%, предпочтительно 50-70% по отношению к полной аминокислотной последовательности основной PRPP-синтетазы, обладающим активностью PRPP-синтетазы.
В настоящем изобретении "L-аминокислотный остаток, соответствующий положению 120, или 135, или 194” означает аминокислотный остаток, соответствующий положению 120, или 135, или 194 в аминокислотной последовательности SEQ ID NO: 2.
Для определения L-аминокислотного остатка, соответствующего мутациям N51H, N113S, L128I или A189V PRPP-синтетазы человека, необходимо выполнить выравнивание аминокислотной последовательности PRPP-синтетазы человека и аминокислотной последовательности, представляющей интерес PRPP-синтетазы из бактерии рода Bacillus, и определить в представляющей интерес бактериальной PRPP-синтетазе L-аминокислотные остатки, соответствующие номерам 51, 113, 128 или 189 в аминокислотной последовательности PRPP-синтетазы человека.
Замена, деления, вставка или добавление одного или нескольких аминокислотных остатков должны быть консервативными мутациями с тем, чтобы сохранялась активность фермента. Консервативные замены являются типичными консервативными мутациями. Примеры консервативных замен включают замену Ala на Ser или Thr, замену Arg на Gln, His или Lys, замену Asn на Glu, Gin, Lys, His или Asp, замену Asp на Asn, Glu или Gin, замену Cys на Ser или Ala, замену Gln на Asn, Glu, Lys, His, Asp или Arg, замену Glu на Asn, Gln, Lys или Asp, замену Gly на Pro, замену His на Asn, Lys, Gln, Arg или Туr, замену Ile на Leu, Met, Val или Phe, замену Leu на Ile, Met, Val или Phe, замену Lys на Asn, Glu, Gln, His или Arg, замену Met на Ile, Leu, Val или Phe, замену Phe на Trp, Tyr, Met, Ile или Leu, замену Ser на Thr или Ala, замену Thr на Ser или Ala, замену Trp на Phe или Tyr, замену Tyr на His, Phe или Trp, и замену Val на Met, Ile или Leu.
ДНК, кодирующая по существу такой же белок, как описанные выше мутантные PRPP-синтетазы, получают, например, путем модификации нуклеотидной последовательности, например, посредством метода сайт-направленного мутагенеза, таким образом, что один или несколько аминокислотных остатков в определенном сайте предполагают делецию, замену, вставку или добавление. ДНК, модифицированную, как описано выше, получают традиционными известными методами мутагенеза. Мутагенная обработка включает метод обработки ДНК, содержащей мутантный ген prs, in vitro, например, гидроксиламином, и метод обработки микроорганизма, например, бактерии с мутантным геном prs, принадлежащей к роду Bacillus, ультрафиолетовым облучением или мутагеном, таким как N-метил-N'-нитро-N-нитрозогуанидин (NTG) и азотистая кислота, используемые обычно для такой обработки. Замена, делеция, вставка или добавление нуклеотида как описано выше также включают природные мутации (мутант или вариант), обусловленные индивидуальными различиями или различиями между видами или родами бактерий, содержащих PRPP-синтетазу.
ДНК, кодирующую по существу такой же белок, как мутантная PRPP-синтетаза, можно получить путем выделения ДНК, гибридизующейся в жестких условиях с ДНК, имеющей последовательность известного гена prs, или с ее частью в качестве зонда, и кодирующей белок с активностью PRPP-синтетазы, из подвергшихся мутагенной обработке клеток с мутантной PRPP-синтетазой.
«Жесткие условия» включают такие условия, при которых специфические гибриды образуются, а неспецифические гибриды не образуются. Точно определить эти условия с использованием числовых величин трудно. Однако жесткие условия включают, например, условия, при которых ДНК с высокой степенью гомологии, например, ДНК с гомологией не менее 50%, гибридизуются друг с другом, а ДНК с более низкой гомологией не гибридизуются друг с другом.
Для оценки степени гомологии белков или ДНК можно использовать такие методы расчета как BLAST исследование, FASTA исследование и CrustalW.
BLAST (Basic Local Alignment Search Tool) - эвристический поисковый алгоритм, используемый программами blastp, blastn, blastx, megablast, tblastn и tblastx; эти программы приписывают значения показателям с использованием статистических методов Karlin, Samuel и Stephen F. Altschul ("Methods for assessing the statistical significance of molecular sequence features by using general scoring schemes". Proc. Natl. Acad. Sci. USA, 1990, 87: 2264-68; "Applications and statistics for multiple high-scoring segments in molecular sequences". Proc. Natl. Acad. Sci. USA, 1993, 90:5873-7). FASTA метод описан W.R. Pearson ("Rapid and Sensitive Sequence Comparison with FASTP and FASTA", Methods in Enzymology, 1990, 183: 63-98). Clustal W метод описан Thompson J.D., Higgins D.G. and Gibson T.J. ("CLUSTAL W: improving the sensitivity of progressive multiple sequence alignment through sequence weighting, position-specific gap penalties and weight matrix choice", Nucleic Acids Res. 1994, 22: 4673-4680).
С другой стороны, примером жестких условий являются условия, при которых ДНК гибридизуются друг с другом при концентрации соли, соответствующей обычным условиям отмывки при гибрицизации по Саузерну, т.е., 60°С, 1 × SSC, 0.1% SDS, предпочтительно 0.1 × SSC, 0.1% SDS. В качестве зонда для ДНК, кодирующей варианты и гибридизующейся с геном prs, также можно использовать часть последовательности SEQ ID NO: 1. Такой зонд можно приготовить методом ПЦР с использованием олигонуклеотидов, сконструированных на основании нуклеотидной последовательности SEQ ID NO: 1, в качестве праймеров и фрагмента ДНК, содержащего нуклеотидную последовательность SEQ ID NO: 1, в качестве матрицы. Когда в качестве зонда используют фрагмент ДНК длиной около 300 п.н., условия отмывки для гибридизации включают, например, 50°С, 2 × SSC и 0.1% SDS. Продолжительность отмывки зависит от типа мембраны, используемой для блоттинга, и, как правило, рекомендуется производителем. Например, рекомендованная продолжительность отмывки мембраны Hybond™ N+nylon (Amersham) в жестких условиях - 15 минут.
Ген, гибридизующийся в жестких условиях как описано выше, включает гены со стоп-кодоном, образовавшимся внутри кодирующей области, и кодирующие неактивный из-за мутации в активном центре белок. Однако такое затруднение легко можно устранить путем лигирования гена с коммерческим экспрессионным вектором и исследования экспрессированного белка на активность PRPP-синтетазы.
2. Бактерия настоящего изобретения
Бактерия настоящего изобретения - это бактерия-продуцент пуринового нуклеозида, содержащая ДНК, кодирующую мутантную PRPP-синтетазу согласно настоящему изобретению. Более конкретно, бактерия согласно настоящему изобретению содержит ДНК с мутантным геном prs, экспрессирующимся на хромосоме или плазмиде в бактерии, и обладает повышенной способностью к продукции пуриновых нуклеозидов.
Бактерия настоящего изобретения - это бактерия, принадлежащая к роду Bacillus.
Примеры микроорганизмов, принадлежащих к роду Bacillus, которые можно использовать в настоящем изобретении, включают Bacillus subtilis subsp. subtilis strain 168 (В.subtilis 168) или Bacillus amyloliquefaciens (В. amyloliquefaciens). В. amyloliquefaciens - довольно гетерогенные виды. Известен ряд штаммов В. amyloliquefaciens: SB, Т, Р, W, F, N, К и Н (Welker N.E., Campbell L.L., Unrelatedness of Bacillus amyloliquefaciens and Bacillus subtilis. J. Bacteriol, 94: 1124-1130, 1967). Недавно из растений выделили штаммы Bacillus, которые можно рассматривать как отдельный экотип В. amyloliquefaciens (Reva et al., Taxonomic characterization and plant colonizing abilities of some bacteria related to Bacillus amyloliquefaciens and Bacillus subtilis. FEMS Microbiol. Ecol., 48: 249-259, 2004). Определена нуклеотидная последовательность одного из штаммов, В. amyloliquefaciens FZB42 (Chen et al., Comparative analysis of the complete genome sequence of the plant growth-promoting bacterium Bacillus amyloliquefaciens FZB42. Nat. Biotechnol., 25: 1007-1014, 2007).
Примеры бактерий, принадлежащих к роду Bacillus, также включают следующие виды: Bacillus licheniformis. Bacillus pumilis. Bacillus megaterium. Bacillus brevis. Bacillus polymixa, Bacillus stearothermophilus.
Кроме уже упомянутых свойств, бактерии настоящего изобретения могут обладать другими характерными свойствами, такими как потребность в различных питательных веществах, устойчивость к антибиотику, чувствительность к антибиотику, что не выходит за рамки настоящего изобретения.
Фраза "пуриновый нуклеозид", как она используется здесь, включает инозин, ксантозин, гуанозин и аденозин, предпочтительно, инозин.
Фраза "способность к продукции пуринового нуклеозида", используемая здесь, означает способность синтезировать и накапливать пуриновый нуклеозид в питательной среде. Фраза "бактерия способна к продукции пуринового нуклеозида" означает, что бактерия, принадлежащая к роду Bacillus, способна синтезировать и накапливать в среде пурины, такие как пуриновые нуклеозиды, в количестве, большем по сравнению со штаммом В. subtilis дикого типа, таким как В. subtil is 168. Предпочтительно эта фраза означает, что микроорганизм способен синтезировать и накапливать в питательной среде не менее 10 мг/л, более предпочтительно не менее 50 мг/л инозина, ксантозина, гуанозина или/и аденозина.
Трансформация бактерии ДНК, кодирующей белок, означает введение ДНК в клетку бактерии, например, традиционными методами для введения мутации настоящего изобретения в ген, кодирующий PRPP-синтетазу. Обычно для такого введения необходимо клонирование гена в векторе, способном функционировать в бактерии, принадлежащей к роду Bacillus. Для этих целей можно использовать челночные векторы: pH Y300PLK, pMWMXl, pLF22, pKSl. Замена гена дикого типа мутантным геном происходит благодаря гомологичной рекомбинации.
Методы приготовления хромосомной ДНК, гибридизации, ПЦР, приготовления плазмидной ДНК, рестрикции и лигирования ДНК, трансформации, выбора олигонуклеотидов в качестве праймера и т.п. могут быть обычными методами, известными специалисту в данной области. Эти методы описаны, например, в Sambrook, J., Fritsch, E.F., and Maniatis, Т., "Molecular Cloning: A Laboratory Manual, Third Edition", Cold Spring Harbor Laboratory Press (2001) и т.п.
Ген, кодирующий белок PRPP-синтетазу Bacillus amyloliquefaciens К, ген prsBA, секвенирован авторами настоящего изобретения (SEQ ID NO: 3). Последовательность гена, кодирующего белок PRPP-синтетазу из Bacillus subtilis, ген prs Bacillus subtilis subsp.subtilis штамм 168, известна (нуклеотиды с 57743 по 58696 в последовательности с инвентарным номером NC_000964 в базе данных GenBank; (SEQ ID NO: 1)). Ген prs Bacillus subtilis локализован на хромосоме между генами gcaD и ctc в районе 7°. Следовательно, указанные гены prs можно получить методом ПЦР (polymerase chain reaction; refer to White, T.J. et al. Trends Genet., 5, 185 (1989)) с использованием праймеров, сконструированных на основе нуклеотидной последовательности гена. Гены, кодирующие белок PRPP-синтетазу других микроорганизмов, можно получить сходным образом (см. Пример 3).
Примеры гена prs Bacillus subtilis также включают ДНК, кодирующую белок PRPP-синтетазу с аминокислотной последовательностью, представленной в SEQ ID NO: 2, и/или белок с аминокислотной последовательностью, включающей делецию, замену, вставку или добавление одной или нескольких аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 2.
Примеры гена prs Bacillus amyloliquefaciens К также включают ДНК, кодирующую белок PRPP-синтетазу с аминокислотной последовательностью, представленной в SEQ ID NO: 4, и/или белок с аминокислотной последовательностью, включающей делецию, замену, вставку или добавление одной или нескольких аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 4.
Бактерия настоящего изобретения может быть получена путем введения вышеупомянутых ДНК в бактерию, изначально способную к продукции пуринового нуклеозида. С другой стороны, бактерия настоящего изобретения может быть получена путем придания способности к продукции пуринового нуклеозида бактерии, содержащей вышеупомянутые ДНК.
Пример родительского штамма, принадлежащего к роду Bacillus, который может быть использован в настоящем изобретении, - это штамм-продуцент инозина В, subtilis KMBS375. (KMBS375: Ppur*-Δatt ΔpurA ΔpurR ΔpupG ΔdeoD guaB24; см. Справочный пример). Другие родительские штаммы, принадлежащие к роду Bacillus, которые могут использоваться в настоящем изобретении, включают штамм В. subtilis AJ 12707 (FERM P-12951) (патентная заявка Японии JP 6113876A2), штамм В. subtilis AJ3772 (FERM Р-2555) (патентная заявка Японии JP 62014794A2), Bacillus pumilus NA-1102 (FERM BP-289), Bacillus subtilis NA-6011 (FERM BP-291), Bacillus subtilis G1136A (ATCC No. 19222) (патент США 3575809), реидентифицированный как Bacillus amyloliquefaciens AJ 1991, депонированный 3 октября 2005 г. в ВКПМ как Bacillus amyloliquefaciens G1136A (VKPM B-8994), 13 октября 2006 г. было осуществлено международное депонирование штамма, Bacillus subtilis NA-6012 (FERM BP-292) (патент США 4701413), В. pumilis Gottheil No.3218 (ATCC No. 21005) (патент США 3616206), штамм В. amyloliquefaciens AS115-7 (VKPM B-6134) (патент РФ 2003678) и подобные им. Также может использоваться штамм В. subtilis KMBS16. Этот штамм является производным известного штамма В. subtilis 168 trpC2 с мутациями, введенными в ген purR, кодирующий репрессор пурина (purR::spc), ген рurА, кодирующий сукцинил-АМФ-синтазу (рurА::erm) и ген deoD, кодирующий пуриннуклеозидфосфорилазу (deoD::kan) (патентная заявка РФ 2002103333, патент США 7326546, 2008).
Бактерия настоящего изобретения может быть дополнительно улучшена путем усиления экспрессии одного или нескольких генов, вовлеченных в биосинтез пурина. Примеры таких генов включают onepohpur из В. subtilis (Ebbole D.J. and Zalkin H.J. Biol. Chem., 262: 8274-87 (1987), Bacillus subtilis and Its Closest Relatives, Editor in Chief: A.L. Sonenshein, ASM Press, Washington D.C., 2002). Описан штамм-продуцент инозина В. subtilis с модифицированной регуляторной областью оперона риг (патент США 7326546, 2008).
3. Способ продукции нуклеозидов
Способ настоящего изобретения включает способ продукции нуклеозида, такого как инозин и/или гуанозин, включающий стадии культивирования бактерии настоящего изобретения в питательной среде для продукции и накапливания нуклеозида в среде и выделение нуклеозида из культуральной жидкости.
В настоящем изобретении культивирование бактерии, выделение нуклеозидов из культуральной жидкости и его очистка и т.п. может быть осуществлено способом, подобным традиционным способам ферментации, в которых с использованием микроорганизма получают нуклеозид. Питательная среда для продукции пуринового нуклеозида может быть обычной средой, содержащей источник углерода, источник азота, неорганические ионы, органические компоненты и другие необходимые компоненты. В качестве источника углерода можно использовать сахариды, такие как глюкоза, лактоза, галактоза, фруктоза, арабиноза, мальтоза, ксилоза, трегалоза, рибоза и гидролизаты крахмала; спирты, такие как глицерин, маннитол и сорбитол; органические кислоты, такие как глюконовая кислота, фумаровая кислота, лимонная кислота, янтарная кислота и т.п. В качестве источника азота можно использовать неорганические аммонийные соли, такие как сульфат аммония, хлорид аммония и фосфат аммония; органический азот, такой как гидролизаты соевых бобов; аммиачный газ; водный раствор аммиака и т.д. Желательно, чтобы витамины, такие как витамин B1, необходимые вещества, например, органические добавки, такие как нуклеиновые кислоты, аденин и РНК, или дрожжевой экстракт и т.п. могли присутствовать в соответствующих или даже в минимальных количествах. Кроме того, при необходимости могут быть добавлены малые количества фосфата кальция, сульфата магния, ионы железа, ионы марганца и т.п.
Выращивание осуществляется предпочтительно в аэробных условиях в течение 16-72 часов, поддерживают температуру культивирования 30-45°С, рН 5-8. рН можно регулировать с использованием неорганических или органических кислых или щелочных веществ, таких как аммиачный газ.
После выращивания твердые остатки, такие как клетки, могут быть удалены из культуральной жидкости методом центрифугирования или фильтрацией через мембрану, а затем целевой пуриновый нуклеозид может быть выделен из культуральной жидкости и очищен с использованием любой комбинации традиционных методов, таких как ионообменная хроматография и осаждение.
4. Способ продукции пуриновых нуклеотидов
Способ настоящего изобретения включает способ продукции пуриновых нуклеотидов, включающий стадии выращивания бактерии настоящего изобретения в питательной среде, приводящего к секреции бактерией пуринового нуклеозида в питательную среду, фосфорилирования полученного пуринового нуклеозида и выделения пуринового нуклеотида. Кроме того, способ настоящего изобретения включает способ продукции 5'-инозиновой кислоты, включающий стадии выращивания бактерии настоящего изобретения в питательной среде, приводящего к секреции инозина в питательную среду, фосфорилирования инозина и выделения 5'-инозиновой кислоты. Кроме того, способ настоящего изобретения включает способ продукции 5'-ксантиловой кислоты, включающий стадии выращивания бактерии настоящего изобретения в питательной среде, приводящего к секреции ксантозина в питательную среду, фосфорилирования инозина и выделения 5'-ксантиловой кислоты. Кроме того, способ настоящего изобретения включает способ продукции 5'-гуаниловой кислоты, включающий стадии выращивания бактерии настоящего изобретения в питательной среде, приводящего к секреции гуанозина в питательную среду, фосфорилирования гуанозина и выделения 5'-гуаниловой кислоты. Способ настоящего изобретения включает и способ продукции 5'-гуаниловой кислоты, включающий стадии выращивания бактерии настоящего изобретения в питательной среде, позволяющего секрецию ксантозина в питательную среду, фосфорилирования ксантозина, аминирования 5'-ксантиловой кислоты и выделения 5'-гуаниловой кислоты.
В настоящем изобретении выращивание бактерии, выделение инозина из питательной среды и очистка и т.п. могут быть осуществлены сходным образом с традиционными способами ферментации, при которых получают инозин с использованием микроорганизма. Кроме того, в настоящем изобретении стадии фосфорилирования инозина и выделения 5'-инозиновой кислоты могут быть осуществлены традиционными способами ферментации, при которых пуриновый нуклеотид, такой как 5'-инозиновая кислота, образуется из пуринового нуклеозида, такого как инозин.
Фосфорилирование пуринового нуклеозида может быть ферментативным, с использованием различных фосфатаз, нуклеозидкиназ или нуклеозидфосфотрансфераз, или химическим, с использованием фосфорилирующих агентов, таких как POCl3 и т.п. Можно использовать фосфатазу, способную катализировать С-5'-селективный перенос фосфорильной группы пирофосфата к нуклеозидам (Mihara et. al., Phosphorylation of nucleosides by the mutated acid phosphatase from Morganella morganii. Appl. Environ. Microbiol., 66: 2811-2816 (2000)), или кислую фосфатазу, использующую в качестве донора фосфорной кислоты полифосфорную кислоту (соли), фенилфосфорную кислоту (соли) или карбамилфосфорную кислоту (соли) (WO 9637603 A1), или подобные им. Также в качестве примера фосфатазы можно использовать фосфатазу, катализирующую перенос фосфорильной группы на С-2', 3' или 5' нуклеотида с использованием в качестве субстрата п-нитрофенилфосфата (Mitsugi, К., et al., Agric. Biol. Chem., 28, 586-600 (1964)), неорганического фосфата (выложенная патентная заявка Японии No. JP 42-1186) или ацетилфосфата (выложенная патентная заявка Японии No. JP 61-41555), или подобные ей. В качестве примера нуклеозидкиназы можно использовать нуклеозидкиназу, гуанозин/инозинкиназу Е. coli (Mori, H. et al. Cloning of a guanosine-inosine kinase gene of Escherichia coli and characterization of the purified gene product. J. Bacteriol. 177: 4921-4926 (1995); WO 9108286) или подобные им. В качестве примера нуклеозидфосфотрансферазы можно использовать нуклеозидфосфотрансферазу, описанную Hammer-Jespersen, К. (Nucleoside catabolism, p.203-258. In A Munch-Petesen (ed.). Metabolism of nucleotides, nucleosides, and nucleobases in microorganism. 1980, Academic Press, New York) или подобные им. Химическое фосфорилирование можно провести с использованием таких агентов как POCl3 (Yoshikawa, К. et. al. Studies of phosphorylation. III. Selective phosphorylation of unprotected nucleosides. Bull. Chem. Soc. Jpn. 42:3505-3508 (1969)) или подобных.
Аминирование 5'-ксантиловой кислоты может быть ферментативным с использованием, например, ГМФ-синтетеазы Е. coli (Fujio et. al. High level of expression of XMP aminase in Escherichia coli and its application for the industrial production of 5'-guanylic acid. Biosci. Biotech. Biochem. 1997. 61: 840-845; EP 0251489 B1).
Краткое описание рисунков
На Фигуре 1 изображено выравнивание последовательностей PRPP-синтетазы: Hum, изофермент I человека; Bs, Bacillus subtilis; BaK, Bacillus amyloliquefaciens, штамм К; BaFZB42, Bacillus amyloliquefaciens FZB42 FZB42. Аминокислоты в ферменте человека, которые заменяются другими аминокислотами для придания ферменту устойчивости к ингибированию ADP и GDP, выделены жирным шрифтом. Соответствующие аминокислоты фермента Bacillus также выделены жирным шрифтом. На Фигуре 2 изображена организация плазмиды pKSl-PRSBS.
Наилучший способ осуществления настоящего изобретения
Настоящее изобретение будет более подробно описано ниже со ссылкой на следующие не ограничивающие настоящее изобретение Примеры.
Пример 1. Клонирование гена prs дикого типа из В. subtilis и конструирование мутантных генов.
Полная нуклеотидная последовательность штамма В. subtilis 168 определена (F. Kunst, N. Ogasawara, I. Moszer, et al., The complete genome sequence of the Gram-positive bacterium Bacillus subtilis. Nature 390: 249-256 (1997)). На основании опубликованной нуклеотидной последовательности синтезировали праймеры 1 (SEQ ID NO. 5) и 2 (SEQ ID NO. 6) для амплификаци гена prs. С использованием этих праймеров и геномной ДНК B. subtilis 168 в качестве матрицы амплифицировали ген prs В. subtilis (prsBS) с прилегающими областями. Полученный фрагмент величиной 1.8 т.п.н. обрабатывали рестриктазами SalI и Ecl136I и клонировали в термочувствительном низкокопийном челночном векторе pKS, обработанном SalI и SmaI (Shatalin K.Y. and Neyfakh A.A., FEMS Microbiology Letters, 245: 315-9 (2005)), получив плазмиду pKSl-PRSBS. Затем содержащийся на этой плазмиде ген prsBS подвергли мутагенезу методом QuikChange сайт-направленного мутагенеза (Stratagene). Для этого использовали праймеры 3 (SEQ ID NO.7) и 4 (SEQ ID NO.8) для введения мутации N120S и праймеры 5 (SEQ ID NO.9) и 6 (SEQ ID NO.10) для введения мутации A194V и плазмиду pKSl-PRSBS в качестве матрицы. В результате получили плазмиды pKSl-PRSBS 120 и pKSl-PRSBS 194, содержащие prsBSN120S или prsBSA194V соответственно, и подтвердили наличие интересующих мутаций путем секвенирования.
Пример 2. Влияние мутаций prsBSN120S или prsBSA194V на продукцию инозина штаммом-продуцентом инозина В. subtilis
Плазмиды pKSl-PRSBS 120 и pKSl-PRSBS 194, содержащие prsBSN120S или prsBSA194V, методом трансформации вводили в штамм-продуцент инозина В. subtilis KMBS375, после чего prsBS штамма замещался prsBSN120S или prsBSA194V. Интеграцию мутантного гена в хромосому KMBS375 осуществляли с использованием метода, описанного для инактивации гена в В. anthracis (Shatalin and Neyfakh, FEMS Microbiology Letters, 2005) с модификациями, которые дали возможность ввести интересующие мутации (включая точечные мутации) в хромосому без селекции. Данный метод включает следующие стадии.
1) Введение полученной плазмиды методом трансформации в штамм Bacillus, отбор клонов с плазмидой при 30°С на LA (пептон 10 г/л, дрожжевой экстракт 5 г/л, NaCl 3 г/л, агар 18 г/л) с 10 мкг/мл эритромицина.
2) Выращивание трансформированного плазмидой штамма на среде LB (без эритромицина) с аэрацией при 37°С в течение ночи и рассев культуры на LB агар с 10 мкг/мл эритромицина. Около 100% устойчивых к эритромицину клеток такой ночной культуры содержат плазмиду, интегрированную в хромосому в результате единичного кроссинговера. Следовательно, полученные клоны содержат в хромосоме два аллеля интересующего гена: ген дикого типа и мутантный.
3) Выращивание отдельных клонов, содержащих интегрированную плазмиду на среде LB без эритромицина с аэрацией в течение 48 часов при 30°С. Высевали полученную культуру на чашки LA (без эритромицина) и выращивали при 34°С для получения отдельных колоний.
4) Проверка отдельных клонов на устойчивость к эритромицину; обычно 0.5-50% колоний оказываются чувствительными к эритромицину. В результате культивирования происходил второй кроссинговер и вырезание плазмиды, что приводило к тому, что на хромосоме оставался либо ген дикого типа, либо мутантный.
5) Проверка чувствительных к эритромицину клонов на наличие требуемой мутации с использованием метода ПЦР в геле. В этом методе проводят ПЦР - анализ колоний с 2 парами праймеров. 5'-концевой праймер - общий для любой пары. 3'-концевые праймеры различаются 3'-концевыми нуклеотидами. Один 3'-концевой праймер (с использованием которого будет получено максимум продукта с ДНК из колоний, образованных клетками с мутантным геном, в качестве матрицы) содержит мутантный концевой нуклеотид, а другой 3'-концевой праймер (с использованием которого будет получено максимум продукта с ДНК из колоний, образованных клетками дикого типа, в качестве матрицы) содержит концевой нуклеотид дикого типа. Кроме того, предпоследний нуклеотид обоих 3'-концевых праймеров был особенным образом изменен для дальнейшего препятствия отжига праймера на неспецифическую матрицу и таким образом для лучшего различения колоний дикого типа и мутантных.
Для отбора штаммов, содержащих prsBSN120S или prsBSA194V мутации, использовали для ПЦР в геле 5'-концевой праймер 7 (SEQ ID NO.11), 3'-концевой праймер 8 (SEQ ID NO.12) и 5'-концевой праймер 7 (SEQ ID NO. 11), 3'-концевой праймер 9 (SEQ ID NO.13) для идентификации prsBS120S, и 5'-концевой праймер 7 SEQ ID NO.11), 3'-концевой праймер 10 (EQ ID NO.14) и 5'-концевой праймер 7 (SEQ ID NO.11), 3'-концевой праймер 11 (SEQ ID NO.15) для идентификации prsBSA 194V.
Таким образом были получены производные KMBS375, содержащие мутации prsBSN120S (KMBS375 prsN120S) или prsBSA194V (KMBS375 prsA194V). После подтверждения точности замещения путем секвенирования, полученные штаммы KMBS375 prsN120S, KMBS375 prsA194V и контрольный штамм KMBS375 оценивали в пробирочных ферментациях. Для этого каждый из штаммов культивировали при 34°С в течение 18 часов в L-бульоне и 0.3 мл полученной культуры инокулировали в 3 мл ферментационной среды в пробирках 20×200 мм и культивировали на роторной качалке при 34°С в течение 72 часов.
Состав ферментационной среды (г/л):
После культивирования определяли количество накопленного в среде инозина методом ВЭЖХ.
Условия проведения ВЭЖХ:
Колонка: Luna С 18(2) 250×3 мм, 5u (Phenomenex, USA). Буфер: 2% v/v C2H5OH; 0.8% v/v триэтиламин; 0.5% v/v уксусная кислота (ледяная); рН 4.5. Температура: 30°С. Скорость протока: 0.3 мл/мин. Объем введения: 5 мкл. Детекция: UV 250 нм. Время удержания (мин):
Как видно из Таблицы 1, использование мутантного гена prs, кодирующего PRPP-синтетазу, устойчивую к ингибированию пуриновыми нуклеотидами по типу обратной связи, улучшало продуктивность по инозину штамма В. subtilis KMBS375.
Пример 3. Клонирование гена дикого типа prs В.amyloliquefaciens К и конструирование мутантных генов.
Для клонирования фрагмента ДНК, содержащего ген prs штамма В. amyloliquefaciens К (prsBA) сконструировали Праймер 12 (SEQ ID NO.16) и праймер 13 (SEQ ID NO.17) с использованием последовательностей в структурных частях генов В. subtilis gsaD и ctc, находящихся по обеим сторонам от гена prs, следуя предположению, что данные области хромосомы В. subtilis гомологичны таковым В. amyloliquefaciens. С использованием этих праймеров и геномной ДНК В. amyloliquefaciens IAM1523 (University of Tokyo, Japan) в качестве матрицы получили продукт ПЦР ожидаемого размера. Фрагмент секвенировали и обнаружили, что он содержит ген с очень высокой гомологией к гену prsBS и к гену prs растений бактерии Bacillus amyloliquefaciens FZB42, геном которой был недавно секвенирован (Fig.1).
На основании полученной последовательности области prs из В. amyloliquefaciens К сконструировали праймер 14 (SEQ ID NO.18) и праймер 15 (SEQ ID NO.19) для субклонирования гена prs с фланкирующими областями, достаточными для дальнейшей гомологичной рекомбинации.
С использованием данных праймеров и геномной ДНК В. amyloliquefaciens IAM1523 в качестве матрицы получии продукт ПЦР, который обработали рестриктазами SalI и PvuII и клонировали в вектор pKSl, обработанный рестриктазами SalI и SmaI, с образованием плазмиды pKSl-PRSBA. Затем осуществили сайт-направленный мутагенез содержащегося на этой плазмиде гена prsBa, как описано в Примере 1, с использованием плазмиды pKSl-PRSBA в качестве матрицы, праймера 16 (SEQ ID NO.20) и праймера 17 (SEQ ID NO.21); праймера 18 (SEQ ID NO.22) и праймера 19 (SEQ ID NO.23); праймера 20 (SEQ ID NO.24) и праймера 21 (SEQ ID NO.25); праймера 22 (SEQ ID NO.26) и праймера 23 (SEQ ID NO.27), соответственно, для введения мутации D58H, N120S, L135I или A194V, соответствующих мутации N51H, N113S, L128I или A189V PRPP-синтетазы человека.
Таким образом были получены плазмиды pKS1-PRSBA58, pKS1-PKSBA120, pKS1-PRSBA135 и pKS1-PRSBA194, содержащие гены prsBAD58H, prsBAN120S, prsBAL135I и prsBAA194V соответственно.
Пример 4. Влияние мутаций prsBAD58H, prsBAN120S, prsBAL135I или prsBAA194V на продукцию инозина и гуанозина штаммом-продуцентом инозина и гуанозина В. amyloliquefaciens
Полученные плазмиды pKSl-PRSBA58, pKSl-PRSBA120, pKSl-PRSBA135 и pKSl-PRSBA194 трансформировали в В. subtilis 168, получив В. subtilis 168, несущий pKSl-PRSBA58, pKSl-PRSBA120, pKSl-PRSBA135 или pKSl-PRSBA194 соответственно. Затем фаг Е40, выросший на каждом из полученных штаммов, использовали для трансдукции плазмид pKSl-PRSBA58, pKSl-PRSBA120, pKSl-PRSBA135 и pKSl-PRSBA194 в штамм-продуцент инозина и гуанозина В. amyloliquefaciens AJ 1991. Таким образом сконструировали производные В. amyloliquefaciens AJ 1991, несущие pKSl-PRSBA58, pKS1-PRSBA120, pKSl-PRSBA135 или pKSl-PRSBA194.
Интеграцию мутантных генов в хромосому АJ1991 осуществили как описано в Примере 2. Для отбора штаммов, содержащих мутации prsBAD58H, prsBAN120S, prsBAL135I или prsBAA194V, использовали 5'-концевой праймер 24 (SEQ ID NO.28), 3'-концевой праймер 25 (SEQ ID NO.29) и 3'-концевой праймер 26 (SEQ ID NO.30) для идентификации мутации prsBAD58H; 5'-концевой праймер 27 (SEQ ID NO.31), 3'-концевой праймер 28 (SEQ ID NO.32) и 3'-концевой праймер 29 (SEQ ID NO.33) для идентификации мутации prsBAN120S; 5'-концевой праймер 27 (SEQ ID NO.31), 3'-концевой праймер 30 (SEQ ID NO.34) и 3'-концевой праймер 31 (SEQ ID NO.35) для идентификации мутации prsBAL135I; 5'-концевой праймер 27 (SEQ ID NO.31), 3'-концевой праймер 32 (SEQ ID NO.36) и 3'-концевой праймер 33 (SEQ ID NO.37) для идентификации мутации prsBAA194V. Интеграцию также подтверждали путем секвенирования. Таким образом сконструировали штаммы AJ1991 prsBAD58H, AJ1991 prsBAN120S, AJ1991 prsBAL135I и AJ1991 prsBAA194V.
Штаммы AJ1991 prsBAD58H, AJ1991 prsBAN120S, AJ1991 prsBAL135I, AJ1991 prsBAA194V и контрольный штамм AJ1991 культивировали при 34°С в течение 18 часов в L-бульоне и по 0.3 мл полученных культур инокулировали в 3 мл ферментационной среды в пробирках 20×200 мм и культивировали на роторной качалке при 30°С в течение 72 часов. Результаты представлены в Таблице 2.
Состав ферментационной среды: (г/л)
Как видно из Таблицы 2, среди мутантных генов prsBA, кодирующих PRPP-синтетазу, устойчивую к ингибированию пуриновыми нуклеотидами по типу обратной связи, ген, содержащий мутацию D58H, ухудшал продуктивность по инозину и гуанозину штамма B. amyloliquefaciens, а гены, содержащие мутацию N120S, L135I или A194V, улучшали продуктивность по нуклеозидам. С другой стороны, полученные результаты показывают, что не существует строгой корреляции между устойчивостью PRPP-синтетазы к ингибированию пуриновыми нуклеотидами по типу обратной связи и продукцией пуриновых нуклеозидов. Если мутантная PRPP-синтетаза устойчива к ингибированию пуриновыми нуклеотидами по типу обратной связи, это не обязательно ведет к увеличению продукции пуриновых нуклеозидов бактерией, содержащей такую PRPP-синтетазу. Это является явным указанием на наличие изобретательского уровня у настоящего изобретения.
Справочный пример. Конструирование KMBS375
<Конструирование прототрофа В. subtilis 168 Marburg>
В. subtilis 168 Marburg (ATCC6051) является ауксотрофом по Тrр вследствие присутствия на хромосоме мутантного аллеля trpC2 (trpC; ген индол-3-глицеринфосфатсинтазы) (Albertini A.M. and A. Galizzi. 1999. The sequence of the trp operon of Bacillus subtilis 168 (trpC2) revisited. Microbiology. 145:3319-3320). Аллель trpC2, в котором три нуклеотида "att" добавлены в положении за 328-м от стартового кодона trpC2, амплифицировали в ПЦР и ввели в В. subtilis 168 Marburg как изложено далее.
(1) Амплификация аллеля trpC+ методом рекомбинантной ПЦР.
Для амплификации 5'-конца аллеля trpC+ и предшествующей ему области сконструировали ПЦР-праймеры 34 (SEQ ID NO.38) и 35 (SEQ ID NO.39) на основании информации из базы данных GenBank (Accession NO. NC 000964) и Albertini and Galizzi (Microbiology. 145:3319-3320).
ПЦР (94°C, 30 секунд; 53°С, 1 минута; 72°С, 1 минута; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)) проводили с использованием вышеописанных праймеров и хромосомной ДНК штамма В. subtilis 168 Marburg в качестве матрицы для амплификации фрагментов, содержащих область 5'-конца аллеля trpC+ и предшествующую ему область.
Для амплификации 3'-конца аллеля trpC+ и следующей за ним области сконструировали ПЦР-праймеры 36 (SEQ ID NO.40) и 37 (SEQ ID NO.41) на основании информации из базы данных GenBank (Accession NO.NC_000964) и Albertini and Galizzi (Microbiology. 145:3319-3320).
ПЦР (94°С, 30 секунд; 53°С, 1 минута; 72°С, 1 минута; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)) проводили с использованием вышеописанных праймеров и хромосомной ДНК штамма В. subtilis 168 Marburg в качестве матрицы для амплификации фрагментов, содержащих область 3'-конца аллеля trpC+ и следующую за ним область.
Для амплификации полной последовательности аллеля trpC+ методом рекомбинантной ПЦР два фрагмента ДНК, амплифицированные как описано выше, очищали с использованием MicroSpin Column S-400 (Amersham Pharmacia Biotech), надлежащее количество их смеси использовали в качестве матрицы в ПЦР (94°С, 30 секунд; 55°С, 1 минута; 72°С, 2 минуты; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)) с использованием праймеров 34 (SEQ ID NO.38) и 37 (SEQ ID NO.41), таким образом получили амплифицированный фрагмент (около 1.2 т.п.н.) аллеля trpC+.
(2) Конструирование прототрофа по trp из штамма В. subtilis 168 Marburg
Целевой фрагмент аллеля trpC+ выделили из геля после электрофореза в агарозном геле. Компетентные клетки штамма В. subtilis 168 Marburg, приготовленные как описано Dubnau and Davidoff-Abelson (Dubnau, D. and R. Davidoff-Abelson, J. Mol. Biol., 56:209-221 (1971)), трансформировали этим фрагментом ДНК и отбирали колонии, способные расти на чашках с минимальной агаризованной средой. Из этих колоний выделили хромосомную ДНК. Амплифицировали фрагменты ДНК методом ПЦР с использованием этой хромосомной ДНК в качестве матрицы и праймеров 34 (SEQ ID NO.38) и 37 (SEQ ID NO.41), затем проводили секвенирование для подтверждения вставки трех нуклеотидов в аллель trpC2 и отсутствия других мутаций, который могли появиться в результате ПЦР. Полученный таким образом рекомбинант не был ауксотрофным по Trp; этот штамм был назван KMBS275.
<Конструирование ауксотрофного по His штамма В. subtilis 168 Marburg>
Делецию в открытой рамке считывания осуществляли в гене hisC, кодирующем гистидинолфосфатаминотрансферазу (ΔhisC: деления 204 нуклеотидов 403-606) и вводили в штамм В.subtilis 168 Marburg (trpC2) как изложено далее.
(1) Амлификация ΔhisC методом рекомбинантной ПЦР
Для амплификации 5'-конца аллеля ΔhisC и предшествующей ему области сконструировали ПЦР-праймеры 38 (SEQ ID NO.42) и 39 (SEQ ID NO.43) на основании информации из базы данных GenBank (Accession NO.NC 000964). Праймер 38 содержит на 5'-конце сайт EcoRI. Праймер содержит 39 слияние, образованные при делеции в открытой рамке считывания.
ПЦР (94°С, 30 секунд; 55°С, 1 минута; 72°С, 1 минута; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)) проводили с использованием вышеописанных праймеров и хромосомной ДНК штамма В. subtilis 168 Marburg в качестве матрицы для амплификации фрагментов, содержащих область 5'-конца аллеля ΔhisC и предшествующую ему область.
Для амплификации 3'-конца аллеля ΔhisC и следующей за ним области сконструировали ПЦР-праймеры 40 (SEQ ID NO.44) и 41 (SEQ ID NO.45) на основании информации из базы данных GenBank (Accession NO.NC 000964). Праймер 40 содержит слияние, образованные при делеции в открытой рамке считывания. Праймер 41 содержит на 5'-конце сайт BamH1.
ПЦР (94°С, 30 секунд; 55°С, 1 минута; 72°С, 1 минута; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)) проводили с использованием вышеописанных праймеров и хромосомной ДНК штамма В. subtilis 168 Marburg в качестве матрицы для амплификации фрагментов, содержащих область 3'-конца аллеля AhisC и следующую за ним область.
Для амплификации полной последовательности ΔhisC методом рекомбинантной ПЦР два фрагмента ДНК, амплифицированные как описано выше, очищали с использованием MicroSpin Column S-400 (Amersham Pharmacia Biotech), надлежащее количество их смеси использовали в качестве матрицы в ПЦР с использованием праймеров 38 (SEQ ID NO.42) и 41 (SEQ ID NO.45), провели ПЦР (94°С, 30 секунды; 55°С, 1 минута; 72°С, 2 минуты; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)), таким образом получили амплифицированный фрагмент (около 1.5 т.п.н.) ΔhisC.
(2) Клонирование гена ΔhisС
Амплифицированный фрагмент обрабатывали рестриктазами EcoRI и ВаmHI (37°С, в течение ночи) и сепарировали в агарозном геле. Целевой фрагмент выделяли из геля и лигировали с интегративным вектором pJPMl хромосомы В. subtilis (Mueller, J.P., G. Bukusoglu and A. L. Sonenshein. 1992. Transcriptional regulation of Bacillus subtilis glucose starvation-inducible genes: control of gsiA by the ComP-ComA signal transduction system. J. Bacteriol. 174:4361-4373), который предварительно обрабатывали теми же ферментами (37°С, 3 часа). Отобрали плазмиду, в которую ген ΔhisC был правильно интегрирован, путем секвенирования подтвердили отсутствие мутаций, которые могли появиться в результате проведения ПЦР, плазмиду назвали рКМ186.
(3) Конструирование штамма, ауксотрофного по His, из штамма В. subtilis 168 Marburg
Компетентные клетки штамма В. subtilis 168 Marburg, приготовленные как описано выше, трансформировали плазмидой рКМ186 и отбирали колонии (рекомбинанты, образовавшиеся в результате единичного кроссинговера), способные расти на чашках с LB-агаром, содержащим 2.5 мкг/мл хлорамфеникола (Cm).
Один из полученных рекомбинантов инокулировали в 10 мл среды LB с добавлением 20 мг/л Gua (среда LB+Gua) и культивировали в течение 2 дней при 37°С. Колонии, проявляющие чувствительность к хлорамфениколу, отбирали с использованием агаризованной среды LB+Gua с/без Cm. Из полученных чувствительных к Cm колоний выделили хромосомную ДНК. Провели ПЦР таким же образом, как описано выше, с использованием праймеров 38 (SEQ ID NO.42) и 41 (SEQ ID NO.45). Идентифицировали штаммы, в которых ген hisC на хромосоме замещен разрушенным геном hisC (ΔhisC) в результате двойного рекомбинантного кроссинговера. Полученный штамм-двойной рекомбинант был назван KMBS276 (ΔhisC trpC2).
<Конструирование штамма В. subtilis KMBS375>
1. Конструирование штамма KMBS350 (ΔpurA ΔpurR ΔpupG)
Разрушенные гены pupG, purR и purA (гуанозин/инозинфосфорилаза, репрессор пуринового оперона, сукцинил-АМФ-синтетаза соответственно) последовательно вводили в рекомбинантный штамм KMBS276 (ΔhisC trpC2) - производный от штамма В. subtilis 168 Marburg, и из полученного штамма получали прототроф, как указано далее.
(1) Введение ΔpupG (делеции без нарушения рамки считывания 204 нуклеотидов (334 -537) в штамм KMBS276
(i) Амплификация ΔpupG методом рекомбинантной ПЦР
Для амплификации 5'-конца ΔpupG и предшествующей ему области сконструировали ПЦР-праймеры 42 (SEQ ID NO.46) и 43 (SEQ ID NO.47) на основании информации из базы данных GenBank (Accession NO.NC 000964). Праймер 42 содержит на 5'-конце сайт BamHI. Праймер 43 содержит слияние, образованное при делеции в отркытой рамке считывания.
ПЦР (94°С, 30 секунд; 55°С, 1 минута; 72°С, 1,5 минуты; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)) проводили с использованием вышеописанных праймеров и хромосомной ДНК штамма В. subtilis 168 Marburg в качестве матрицы для амплификации фрагментов, содержащих область 5'-конца ΔpupG и предшествующую ему область.
Для амплификации 3'-конца ΔpupG и следующей за ним области сконструировали ПЦР-праймеры 44 (SEQ ID NO.48) и 45 (SEQ ID NO.49) на основании информации из базы данных GenBank (Accession NO. NC-000964). Праймер 44 содержит слияние, образованное при делении в открытой рамке считывания. Праймер 45 содержит на 5'-конце сайт BamHI.
ПЦР (94°С, 30 секунд; 50°С, 1 минута; 72°С, 1,5 минуты; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)) проводили с использованием вышеописанных праймеров и хромосомной ДНК штамма В. subtilis 168 Marburg в качестве матрицы для амплификации фрагментов, содержащих область 3'-конца ΔpupG и следующую за ним область.
Для амплификации полной последовательности ΔpupG методом рекомбинантной ПЦР два фрагмента ДНК, амплифицированные как описано выше, очищали с использованием MicroSpin Column S-400 (Amersham Pharmacia Biotech), надлежащее количество их смеси использовали в качестве матрицы в ПЦР с использованием праймеров 42 (SEQ ID NO.46) и 45 (SEQ ID NO.49), провели ПЦР (94°С, 30 секунды; 55°С, 1 минута; 72°С, 3 минуты; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)), таким образом получили амплифицированный фрагмент (около 2 т.п.н.) ΔpupG.
(ii) Клонирование гена ΔpupG
Амплифицированный фрагмент обрабатывали рестриктазой ВаmHI (37°С, в течение ночи) и сепарировали в агарозном геле. Целевой фрагмент выделяли из геля и лигировали с интегративным вектором pJPMl хромосомы В. subtilis (J. Bacteriol. 174:4361-4373), предварительно обработанным тем же ферментом (37°С, 3 часа) с последующей обработкой фосфатазой из кишечника теленка (calf intestine phosphatase). Отбирали плазмиду, в которую ген ΔpupG был правильно интегрирован, путем секвенирования ДНК подтверждали отсутствие других мутаций, которые могли возникнуть в результате проведения ПЦР, плазмиду назвали рКМ199.
(in) Введение ΔрuрС в штамм KMBS276
Компетентные клетки штамма KMBS276, приготовленные как описано выше, трансформировали плазмидой рКМ199 и отбирали колонии (рекомбинанты, образовавшиеся в результате единичного кроссинговера), способные расти на чашках с LB-агаром, содержащим 2.5 мкг/мл Cm.
Один из полученных рекомбинантов инокулировали в 10 мл среды LB+Gua и культивировали в течение 2 дней при 37°С. Отбирали колонии, проявлявшие чувствительность к хлорамфениколу, с использованием агаризованной среды LB+Gua с/без Cm. Из клеток, полученных чувствительных к Cm колоний, выделяли хромосомную ДНК. Проводили ПЦР как описано выше с использованием праймеров 42 (SEQ ID NO.46) и 45 (SEQ ID NO.49). Идентифицировали штаммы, в которых ген pupG на хромосоме замещен разрушенным геном pupG (ΔpupG) путем двойного рекомбинантного кроссинговера. Полученный штамм двойного рекомбинанта был назван KMBS334 (ΔрuрС ΔhisC trpC2).
(2) Введение ΔpurR (делеции в открытой рамке считывания 795 нуклеотидов 31-825) в штамм KMBS334
(i) Амплификация ΔpurR методом рекомбинантной ПЦР
Для амплификации 5'-конца ΔpurR и предшествующей ему области сконструировали ПЦР-праймеры 46 (SEQ ID NO.50) и 47 (SEQ ID NO.51) на основании информации из базы данных GenBank (Accession NO.NC 000964). Праймер 46 содержит на 5'-конце сайт BamHI. Праймер 47 содержит слияние, образованное при делеции в открытой рамке считывания.
ПЦР (94°С, 30 секунд; 55°С, 1 минута; 72°С, 1,5 минуты; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)) проводили с использованием вышеописанных праймеров и хромосомной ДНК штамма В. subtilis 168 Marburg в качестве матрицы для амплификации фрагментов, содержащих область 5'-конца ΔpurR и предшествующую ему область.
Для амплификации 3'-конца ΔpurR и следующей за ним области сконструировали ПЦР-праймеры 48 (SEQ ID NO.52) и 49 (SEQ ID NO.53) на основании информации из базы данных GenBank (Accession NO.NC-000964). Праймер 48 содержит слияние, образованное при делеции в открытой рамке считывания. Праймер 49 содержит на 5°-конце сайт BamHI.
ПЦР (94°С, 30 секунд; 50°С, 1 минута; 72°С, 1,5 минуты; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)) проводили с использованием вышеописанных праймеров и хромосомной ДНК штамма В. subtilis 168 Marburg в качестве матрицы для амплификации фрагментов, содержащих область 3'-конца ΔpurR и следующую за ним область.
Для амплификации полной последовательности ΔpurR методом рекомбинантной ПЦР два фрагмента ДНК, амплифицированные как описано выше, очищали с использованием MicroSpin Column S-400 (Amersham Pharmacia Biotech), надлежащее количество их смеси использовали в качестве матрицы в ПЦР с использованием праймеров 46 (SEQ ID NO.50) и 49 (SEQ ID NO.53), провели ПЦР (94°С, 30 секунды; 55°С, 1 минута; 72°С, 3 минуты; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)), таким образом получили амплифицированный фрагмент (около 2,1 т.п.н.) ΔpurR.
(ii) Клонирование гена ΔpurR
Амплифицированный фрагмент обрабатывали рестриктазой BamHl (37°C, в течение ночи) и сепарировали в агарозном геле. Целевой фрагмент выделяли из геля и лигировали с интегративным вектором pJPMl хромосомы В. subtilis (J. Bacteriol. 174:4361-4373), предварительно обработанным тем же ферментом (37°C, 3 часа) с последующей обработкой фосфатазой из кишечника теленка. Отбирали плазмиду, в которую ген ΔpurR был правильно интегрирован, путем секвенирования ДНК подтверждали отсутствие других мутаций, которые могли возникнуть в результате проведения ПЦР, плазмиду назвали рКМ200.
(iii) Введение ΔpurR в штамм KMBS334
Компетентные клетки штамма KMBS334, приготовленные как описано выше, трансформировали плазмидой рКМ200 и отбирали колонии (рекомбинанты, образовавшиеся в результате единичного кроссинговера), способные расти на чашках с LB-агаром, содержащим 2.5 мкг/мл Cm.
Один из полученных рекомбинантов инокулировали в 10 мл среды LB+Gua и культивировали в течение 2 дней при 37°C. Отбирали колонии, проявлявшие чувствительность к хлорамфениколу, с использованием агаризованной среды LB+Gua с/без Cm. Из клеток полученных чувствительных к Cm колоний выделяли хромосомную ДНК. Проводили ПЦР как описано выше с использованием праймеров 46 (SEQ ID NO.50) и 49 (SEQ ID NO). Идентифицировали штаммы, в которых ген purR на хромосоме замещен разрушенным геном purR (Δ purR) путем двойного рекомбинантного кроссинговера. Полученный штамм двойного рекомбинанта был назван KMBS337 (ΔpurR ΔpupG ΔhisC trpC2).
(i) Амплификация ΔpurA методом рекомбинантной ПЦР
Для амплификации 5'-конца ΔpurA и предшествующей ему области сконструировали ПЦР-праймеры 50 (SEQ ID NO.54) и 51 (SEQ ID NO.55) на основании информации из базы данных GenBank (Accession NO. NC-000964). Праймер 50 содержит на 5'-конце сайт BamRl. Праймер 51 содержит слияние, образованное при делеции в открытой рамке считывания.
ПЦР (94°С, 30 секунд; 55°С, 1 минута; 72°С, 1 минута; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)) проводили с использованием вышеописанных праймеров и хромосомной ДНК штамма В. subtilis 168 Marburg в качестве матрицы для амплификации фрагментов, содержащих область 5'-конца ΔpurA и предшествующую ему область.
Для амплификации 3'-конца ΔpurA и следующей за ним области сконструировали ПЦР-праймеры 52 (SEQ ID NO.56) и 53 (SEQ ID NO.57) на основании информации из базы данных GenBank (Accession NO.NC_000964). Праймер 52 содержит слияние, образованное при делеции в открытой рамке считывания. Праймер 53 содержит на 5'-конце сайт BamHI.
ПЦР (94°С, 30 секунд; 50°С, 1 минута; 72°С, 1 минута; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)) проводили с использованием вышеописанных праймеров и хромосомной ДНК штамма В. subtilis 168 Marburg в качестве матрицы для амплификации фрагментов, содержащих область 3°-конца ΔpurA и следующую за ним область.
Для амплификации полной последовательности ΔpurA методом рекомбинантной ПЦР два фрагмента ДНК, амплифицированные как описано выше, очищали с использованием MicroSpin Column S-400 (Amersham Pharmacia Biotech), надлежащее количество их смеси использовали в качестве матрицы в ПЦР с использованием праймеров 50 (SEQ ID NO.54) и 53 (SEQ ID NO.57), провели ПЦР (94°С, 30 секунды; 55°С, 1 минута; 72°С, 2 минуты; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)), таким образом получили амплифицированный фрагмент (около 1,4 т.п.н.) ΔpurA.
(ii) Клонирование гена ΔpurA
Амплифицированный фрагмент обрабатывали рестриктазой BamHI (37°C, в течение ночи) и сепарировали в агарозном геле. Целевой фрагмент выделяли из геля и лигировали с интегративным вектором pJPMl хромосомы В. subtilis (J. Bacteriol. 174:4361-4373), предварительно обработанным тем же ферментом (37°С, 3 часа) с последующей обработкой фосфатазой из кишечника теленка. Отбирали плазмиду, в которую ген ΔpurA был правильно интегрирован, путем секвенирования ДНК подтверждали отсутствие других мутаций, которые могли возникнуть в результате проведения ПЦР, плазмиду назвали рКМ208.
(iii) Введение ΔpurA в штамм KMBS337
Компетентные клетки штамма KMBS337, приготовленные как описано выше, трансформировали плазмидой рКМ208 и отбирали колонии (рекомбинанты, образовавшиеся в результате единичного кроссинговера), способные расти на чашках с LB-агаром, содержащим 2.5 мкг/мл Cm.
Один из полученных рекомбинантов инокулировали в 10 мл среды LB+Gua и культивировали в течение 2 дней при 37°С. Отбирали колонии, проявлявшие чувствительность к хлорамфениколу, с использованием агаризованной среды LB+Gua с/без Cm. Из клеток полученных чувствительных к Cm колоний выделяли хромосомную ДНК. Проводили ПЦР как описано выше с использованием праймеров 50 (SEQ ID NO.54) и 53 (SEQ ID NO.57). Идентифицировали штаммы, в которых ген purA на хромосоме замещен разрушенным геном purA (Δ purA) путем двойного рекомбинантного кроссинговера. Полученный штамм двойного рекомбинанта был назван KMBS349 (ΔpurA ΔpurR ΔpupG ΔhisC trpC2).
(4). Введение trpC+ и hisC+ в KMBS349
Компетентные клетки штамма KMBS349, приготовленные как описано выше, трансформировали хромосомной ДНК штамма KMBS275 (см. <Конструирование прототрофа В.subtilis 168 Marburg>) и отбирали колонии, способные расти на чашках с минимальной агаризованной средой, содержащей 20 мг/л аденина (Ade).
Из полученных рекомбинантов с использованием минимальной агаризованной среды с/без Ade отобрали штаммы, ауксотрофные по аденину. Затем, с использованием ПЦР в геле (условия ПЦР, соответствующие генам pupG, purR и рur А, были описаны выше), идентифицировали штаммы, в которых три гена на хромосоме заменены разрушенными вариантами этих генов (ΔpupG, ΔpurR и ΔpurA). Полученный штамм назван KMBS350 (ΔpurA ΔpurR ΔpupG).
2. Конструирование штамма КМВ$356((ΔpurA ΔpurR ΔpupG guaB24)
Мутацию ауксотрофности по гуанину с сохранением остаточного уровня экспрессии guaB24 (такая же как guaB(A1), описанная в US 2006275874 A1) в гене guaB, кодирующем IMP-дегидрогеназу, вводили в рекомбинантный штамм KMBS349 (ΔpurA ΔpurR ΔpupG ΔhisC trpC2), производный от штамма В. subtilis 168 Marburg, и из полученного штамма получили прототроф как изложено далее.
(1). Конструирование штамма с разрушенным геном guaB из KMBS349
Компетентные клетки штамма KMBS349 (ΔpurA ΔpurR ΔpurG ΔhisC trpC2), приготовленные как описано выше, трансформировали хромосомной ДНК штамма KMBS193 (guaB::kan trpC2; US 2006275874 A1) и отбирали колонии, способные расти на чашках со средой LB с добавлением 2.5 мкг/мл канамицина (Kan).
Из полученных рекомбинантов идентифицировали штаммы, устойчивые к Каn, ауксотрофные по Gua. Полученный штамм был назван KMBS351 (guaB::kan ΔpurA ΔpurR ΔpurG MisC trpC2).
(2). Конструирование штамма с мутантным (с сохранением остаточного уровня экспрессии, тип "leaky") геном guaB из штамма KMBS349
Компетентные клетки штамма KMBS351 (guaB::kan ΔpurA ΔpurR ΔpupG ΔhisC trpC2), приготовленные как описано выше, трансформировали хромосомной ДНК штамма YMBS9 (guaB24 trpC2; компетентные клетки штамма KMBS193 трансформировали полученных методом ПЦР фрагментом ДНК области, содержащей guaB штамма, производного от В. subtilis 168 Marburg, содержащего на хромосоме мутацию guaB24, получив YMBS9) и отбирали колонии, способные расти на чашках с агаризованной минимальной агаризованной средой, содержащей 20 мг/л Ade, His и Trp.
Из полученных рекомбинантов с использованием минимальной агаризованной среды с/ без Ade+His отбирали штаммы, ауксотрофные по Ade и His. Затем с использованием метода ПЦР в геле (условия для ПЦР, соответствующие генам pupG и purr, были описаны выше) и секвенирования ДНК идентифицировали штаммы, в которых два гена на хромосоме замещены соответствующими вариантами разрушенных генов (ΔpupG и ΔpurR) и guaB::kan был правильно заменен guaB24. Полученный штамм был назван KMBS353 (guaB24 ΔpurA ΔpurR ΔpupG ΔhisC trpC2).
(3). Введение trpC+ и hisC+ в KMBS353
Компетентные клетки штамма KMBS353, приготовленные как описано выше, трансформировали хромосомной ДНК штамма KMBS350 (см.1. Конструирование KMBS350 {ΔpurA ΔpurR ΔpupG)) и отбирали колонии, способные расти на минимальной агаризованной среде, содержащей 20 мг/л Ade.
Затем с использованием секвенирования ДНК гена guaB в полученных рекомбинантах идентифицировали штаммы, в которых ген guaB дикого типа на хромосоме был заменен аллелем guaB24 с мутацией с сохранением остаточного уровня экспрессии. Полученный штамм был назван KMBS356 (guaB24 ΔpurA ΔpurR ΔpupG).
3. Конструирование штамма KMBS375(Ppur*-Δatt ΔdeoD ΔpurA ΔpurR ΔpupG)
В рекомбинантный штамм KMBS337 (ΔpurR ΔpupG ΔhisC trpC2; см.1. (2) Введение ΔpurR (делеция без сдвига рамки считывания 795 нуклеотидов 31-825) в KMBS334), производный от штамма В. subtilis 168 Marburg, последовательно вводили модифицированный промотор пуринового оперона (Ppur) и последовательность аттенюатора с делецией (Ppur*-Δatt; такая же как Ppurl-Δatt, описанная в US 2006275874 A1), разрушенный ген рurА, мутацию ауксотрофности по аденину с остаточным уровнем экспрессии guaB24 (такая же как guaB(A1), описанная в US 2006275874 A1) в гене guaB, кодирующем IMP-дегидрогеназу, и разрушенный вариант гена deoD, кодирующего пуриннуклеозидфосфорилазу, как изложено далее.
(1). Конструирование штамма с разрушенным Рриг из штамма KMBS337
Компетентные клетки штамма KMBS337 (ΔpurR ΔрuрС ΔhisC trpC2), приготовленные как описано выше, трансформировали хромосомной ДНК штамма KMBS198 (Ppur::cat trpC2; US 2006275874 A1) и отбирали колонии, способные расти на среде LB+Gua+Cm.
Штаммы, ауксотрофные по Ade и His, отбирали из полученных рекомбинантов с использованием минимальной агаризованной среды с/ без Ade+His. Затем с использованием метода ПЦР в геле (условия проведения ПЦР, соответствующие генам pupG и purR, были описаны выше) идентифицировали штаммы, в которых два гена на хромосоме заменены соответствующими вариантами разрушенных генов (ΔpupG и ΔpurR). Полученный штамм был назван KMBS340 (Ppur.cat ΔpurR ΔpupG ΔhisC trpC2).
(2). Замена Δpur::cat на Ppur*-Δatt
Компетентные клетки штамма KMBS340 (Ppur::cat ΔpurR ΔpupG ΔhisC trpC2), приготовленные как описано выше, трансформировали хромосомной ДНК штамма KMBS261 (Ppur1-Δatt purR::spc ΔpupG* trpC2; US 2006275874 A1) и отбирали колонии, спсобные расти на минимальной агаризованной среде, содержащей 20 мг/л Trp и His.
Из полученных рекомбинантов с использованием минимальной агаризованной среды с/без Ade+His отбирали штаммы, ауксотрофные по Ade и His. Затем с использованием метода ПЦР в геле (условия проведения ПЦР, соответствующие генам pupG и purR были описаны выше) и секвенирования ДНК идентифицировали штаммы, в которых два гена на хромосоме заменены соответствующими вариантами разрушенных генов (ΔpupG and ΔpurR) и Ppur*-Δatt был корректно заменен Ppur::cat. Полученный штамм был назван KMBS352 (Ppur*-Δatt ΔpurR ΔpupG ΔhisC trpC2).
(3). Введение ΔpurA (делеция в открытой рамке считывания 369 нуклеотидов с 307 по 675) в KMBS352
Компетентные клетки штамма KMBS352 (Ppur*-Δatt ΔpurR ΔpupG ΔhisC trpC2), приготовленные как описано выше, трансформировали хромосомной ДНК штамма KMBS350 [ΔpurA ΔpurR ΔpupG; см.1. Конструирование KMBS350 (ΔpurA ΔpurR ΔpupG)), и отбирали колонии, способные расти на минимальной агаризованной среде, содержащей 20 мг/л His и Ade.
Штаммы с ауксотрофностью по Ade, приобретенной в результате "конгрессии", отбирали среди полученных рекомбинантов с использованием минимальной агаризованной среды с /без Ade+His. Было обнаружено, что один из таких штаммов содержит hisC+ вместо ΔhisC. Затем с использованием метода ПЦР в геле (условия проведения ПЦР, соответствующие гену purA, были описаны выше) и секвенирования ДНК идентифицировали штаммы, в которых ген purA на хромосоме был заменен разрушенным вариантом данного гена (ΔpurA), a Ppur*-Δatt не была замещена Ppur дикого типа. Полученный штамм был назван KMBS359 (Ppur*-Δatt ΔpurA ΔpurR ΔpupG).
(4). Конструирование штамма с разрушенным геном guaB из KMBS359
Компетентные клетки штамма KMBS359 (Ppur*-Δatt ΔpurA ΔpurR ΔpupG), приготовленные как описано выше, трансформировали хромосомной ДНК штамма KMBS351 (guaB::kan ΔpurA ΔpurR ΔpupG ΔhisC trpC2; см.2. (1) Конструирование штамма с разрушенным геном guaB из KMBS349) и отбирали колонии, способные расти на чашках со средой LB+Gua с добавлением 2.5 мкг/мл Каn.
Среди полученных рекомбинантов отбирали штаммы, устойчивые к Kan, ауксотрофные по Gua. Затем с использованием метода ПЦР (условия проведения ПЦР для Ppur были описаны в заявке US 2006275874 A1) идентифицировали штаммы, в которых Ppur*-Δatt не был замещен Ppur дикого типа. Полученный штамм был назван KMBS364 (guaB::kan Ppur*-Δatt ΔpurA ΔpurR ΔpupG).
(5). Конструирование штамма с мутацией с остаточным уровнем экспрессии в гене guaB из KMBS364
Компетентные клетки штамма KMBS364 (guaB::kan Ppur*-Δatt ΔpurA ΔpurR ΔрuрС2), приготовленные как описано выше, трансформировали хромосомной ДНК штамма KMBS356 (guaB24 ΔpurA ΔpurR ΔpupG; см. 2.(3) Введение ΔtrpC+ и hisC+ в KMBS353) и отбирали колонии, способные расти на чашках с минимальной средой, содержащей 20 мг/л Ade.
Затем с использованием секвенирования ДНК идентифицировали штаммы, в которых аллель guaB::kan был правильно заменен на guaB24, a Ppur*-Δatt не был замещен Ppur дикого типа. Полученный штамм был назван KMBS365 (guaB24 Ppur*-Δatt ΔpurA ΔpurR ΔpupG).
(6). Введение ΔdeoD (делеция без сдвига рамки считывания 189 нуклеотидов 262-450) в KMBS365
(i) Амплификация ΔdeoD методом рекомбинантной ПЦР
Для амплификации 5'-конца ΔdeoD и предшествующей ему области сконструировали ПЦР-праймеры 54 (SEQ ID NO.58) и 55 (SEQ ID NO.59) на основании информации из базы данных GenBank (Accession NO. NC-000964). Праймер 54 содержит на 5'-конце сайт BamHI. Праймер 55 содержит слияние, образованное при делеции в открытой рамке считывания.
ПЦР (94°С, 30 секунд; 55°С, 1 минута; 72°С, 1,5 минуты; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)) проводили с использованием вышеописанных праймеров и хромосомной ДНК штамма В. subtilis 168 Marburg в качестве матрицы для амплификации фрагментов, содержащих область 5'-конца ΔdeoD и предшествующую ему область.
Для амплификации 3'-конца ΔdeoD и следующей за ним области сконструировали ПЦР-праймеры 56 (SEQ ID NO.60) и 57 (SEQ ID NO.61) на основании информации из базы данных GenBank (Accession NO. NC_000964). Праймер 56 содержит слияние, образованное при делеции в открытой рамке считывания. Праймер 57 содержит на 5'-конце сайт BamHI.
PCR (94°C, 30 seconds; 55°C, 1 minute; 72°C, 1 minute; 30 cycles; Gene Amp PCR System Model 9600 (Perkins Elmer)) was conducted using the above-described primers and a template of the chromosomal DNA of B. subtilis 168 Marburg strain to amplify fragments containing the 3'-end region and the downstream region of the ΔdeoD.
ПЦР (94°C, 30 секунд; 50°С, 1 минута; 72°C, 1 минута; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)) проводили с использованием вышеописанных праймеров и хромосомной ДНК штамма В. subtilis 168 Marburg в качестве матрицы для амплификации фрагментов, содержащих область 3'-конца ΔdeoD и следующую за ним область.
Для амплификации полной последовательности ΔdeoD методом рекомбинантной ПЦР два фрагмента ДНК, амплифицированные как описано выше, очищали с использованием MicroSpin Column S-400 (Amersham Pharmacia Biotech), надлежащее количество их смеси использовали в качестве матрицы в ПЦР с использованием праймеров 54 (SEQ ID NO.58) и 57 (SEQ ID NO.61), провели ПЦР (94°С, 30 секунды; 50°С, 1 минута; 72°С, 3 минуты; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)), таким образом получили амплифицированный фрагмент (около 2,0 т.п.н.) ΔdeoD.
(ii) Клонирование гена ΔdeoD
Амплифицированный фрагмент обрабатывали рестриктазой BamHI (37°C, в течение ночи) и сепарировали в агарозном геле. Целевой фрагмент выделяли из геля и лигировали с интегративным вектором pJPMl хромосомы В. subtilis (J. Bacteriol. 174:4361-4373), предварительно обработанным тем же ферментом (37°С, 3 часа) с последующей обработкой фосфатазой из кишечника теленка. Отбирали плазмиду, в которую ген ΔdeoD был правильно интегрирован, путем секвенирования ДНК подтверждали отсутствие других мутаций, которые могли возникнуть в результате проведения ПЦР, плазмиду назвали рКМ201.
(iii) Введение ΔdeoD в штамм KMBS365
Компетентные клетки штамма KMBS365, приготовленные как описано выше, трансформировали плазмидой рКМ201 и отбирали колонии (рекомбинанты, образовавшиеся в результате единичного кроссинговера), способные расти на чашках с LB-агаром, содержащим 2.5 мкг/мл Cm.
Один из полученных рекомбинантов инокулировали в 10 мл среды LB+Gua и культивировали в течение 2 дней при 37°C. Отбирали колонии, проявлявшие чувствительность к хлорамфениколу, с использованием агаризованной среды LB+Gua с/без Cm. Из клеток, полученных чувствительных к Cm колоний выделяли хромосомную ДНК. Проводили ПЦР как описано выше с использованием праймеров 54 (SEQ ID NO.58) и 57 (SEQ ID NO.61). Идентифицировали штаммы, в которых ген deoD на хромосоме замещен разрушенным геном deoD (Δ deoD) путем двойного рекомбинантного кроссинговера. Полученный штамм двойного рекомбинанта был назван KMBS375 (ΔdeoD guaB24 Ppur*-Δatt ΔpurA ΔpurR ΔpupG).
Хотя указанное изобретение описано в деталях со ссылкой на Наилучший способ осуществления изобретения, для специалиста в указанной области техники очевидно, что могут быть совершены различные изменения и произведены эквивалентные замены, и такие изменения и замены не выходят за рамки настоящего изобретения.
Каждому из упомянутых выше документов соответствует ссылка, и все цитируемые документы являются частью описания настоящего изобретения.



















| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПУРИНОВЫХ РИБОНУКЛЕОЗИДОВ И РИБОНУКЛЕОТИДОВ | 2008 |
|
RU2422510C2 |
| БЕЛОК YdhL ИЗ Bacillus amyloliquefaciens, ФРАГМЕНТ ДНК, БАКТЕРИЯ, ПРИНАДЛЕЖАЩАЯ К РОДУ Escherichia ИЛИ Bacillus, - ПРОДУЦЕНТ ПУРИНОВЫХ НУКЛЕОЗИДОВ, СПОСОБ ПОЛУЧЕНИЯ ПУРИНОВЫХ НУКЛЕОЗИДОВ И НУКЛЕОТИДОВ | 2005 |
|
RU2294962C2 |
| СПОСОБ ПРОДУКЦИИ ПУРИНОВЫХ НУКЛЕОЗИДОВ И НУКЛЕОТИДОВ МЕТОДОМ ФЕРМЕНТАЦИИ С ИСПОЛЬЗОВАНИЕМ БАКТЕРИЙ, ПРИНАДЛЕЖАЩИХ К РОДУ Escherichia ИЛИ Bacillus | 2006 |
|
RU2365622C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПУРИНОВЫХ НУКЛЕОЗИДОВ И НУКЛЕОТИДОВ, ШТАММ-ПРОДУЦЕНТ ПУРИНОВЫХ НУКЛЕОЗИДОВ (ВАРИАНТЫ) | 2002 |
|
RU2239656C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИНОЗИНА И ИНОЗИН 5'-МОНОФОСФАТА, ШТАММ БАКТЕРИИ, ПРИНАДЛЕЖАЩЕЙ К РОДУ BACILLUS - ПРОДУЦЕНТ ИНОЗИНА (ВАРИАНТЫ) | 2002 |
|
RU2260040C2 |
| СПОСОБ МИКРОБИОЛОГИЧЕСКОГО СИНТЕЗА ПУРИНОВОГО НУКЛЕОЗИДА 5'-АМИНОИМИДАЗОЛ-4-КАРБОКСАМИДРИБОЗИДА (АИКАР) И ШТАММ БАКТЕРИЙ BACILLUS SUBTILIS - ПРОДУЦЕНТ АИКАР | 2008 |
|
RU2405833C2 |
| СПОСОБ ПРОДУКЦИИ ПУРИНОВЫХ НУКЛЕОЗИДОВ МЕТОДОМ ФЕРМЕНТАЦИИ С ИСПОЛЬЗОВАНИЕМ БАКТЕРИЙ, ПРИНАДЛЕЖАЩИХ К РОДУ BACILLUS | 2005 |
|
RU2320717C2 |
| МУТАНТНАЯ ФОСФОРИБОЗИЛПИРОФОСФАТСИНТЕТАЗА, ФРАГМЕНТ ДНК, БАКТЕРИЯ РОДА ESCHERICHIA - ПРОДУЦЕНТ L-ГИСТИДИНА И СПОСОБ ПРОДУКЦИИ L-ГИСТИДИНА | 2004 |
|
RU2282660C2 |
| Новая аденилосукцинат-синтетаза и способ получения нуклеотидов пурина с ее использованием | 2018 |
|
RU2770464C1 |
| БАКТЕРИЯ Bacillus subtilis, ПРОДУЦИРУЮЩАЯ 5`-АМИНОИМИДАЗОЛ-4-КАРБОКСАМИДРИБОЗИД (АИКАР), И СПОСОБ МИКРОБИОЛОГИЧЕСКОГО СИНТЕЗА АИКАР ПУТЕМ КУЛЬТИВИРОВАНИЯ ТАКОЙ БАКТЕРИИ | 2013 |
|
RU2542387C1 |

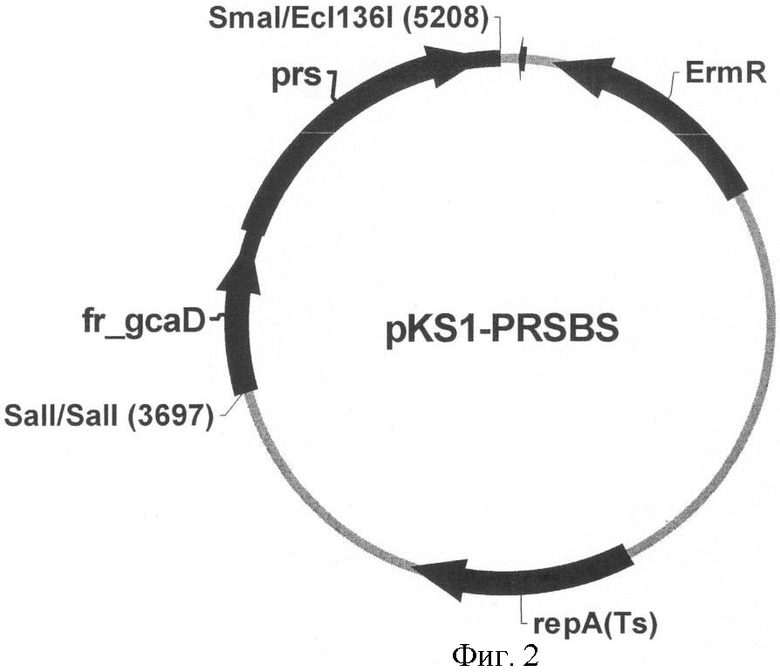
Изобретение относится к биотехнологии и представляет собой способ продукции пуриновых нуклеозидов с использованием бактерии, принадлежащей к роду Bacillus, содержащей фрагмент ДНК, кодирующий мутантную бактериальную фосфорибозилпирофосфатсинтетазу, в которой L-аминокислотный остаток, соответствующий положению 120, 135 или 194 в последовательности фосфорибозилпирофосфатсинтетазы дикого типа из Bacillus subtilis замещен остатком другой L-аминокислоты, и чувствительность указанного фермента к ингибированию пуриновыми нуклеотидами по типу обратной связи снижена. Изобретение позволяет получать пуриновые нуклеозиды с высокой степенью эффективности. 5 н. и 8 з.п. ф-лы, 2 ил., 2 табл.
1. Мутантная бактериальная фосфорибозилпирофосфатсинтетаза (PRPP-синтетаза), отличающаяся тем, что L-аминокислотный остаток, соответствующий положению 120, 135 или 194 в последовательности PRPP-синтетазы дикого типа из Bacillus subtilis, замещен остатком другой L-аминокислоты и чувствительность указанного фермента к ингибированию пуриновыми нуклеотидами по типу обратной связи снижена.
2. Мутантная PRPP-синтетаза по п.1, отличающаяся тем, что остаток аспарагина, соответствующий положению 120 в последовательности PRPP-синтетазы дикого типа из Bacillus subtilis, заменен остатком серина.
3. Мутантная PRPP-синтетаза по п.1, отличающаяся тем, что остаток лейцина, соответствующий положению 135 в последовательности PRPP-синтетазы дикого типа из Bacillus subtilis, заменен остатком изолейцина.
4. Мутантная PRPP-синтетаза по п.1, отличающаяся тем, что остаток аланина, соответствующий положению 194 в последовательности PRPP-синтетазы дикого типа из Bacillus subtilis, замещен остатком валина.
5. Мутантная PRPP-синтетаза по п.1, отличающаяся тем, что мутантной PRPP-синтетазой является фермент из Bacillus subtilis или Bacillus amyloliquefaciens.
6. Фрагмент ДНК, кодирующий мутантную PRPP-синтетазу по любому из пп.1-5.
7. Бактерия, принадлежащая к роду Bacillus, содержащая фрагмент ДНК по п.6 и обладающая способностью к продукции пуриновых нуклеозидов.
8. Бактерия по п.7, отличающаяся тем, что указанной бактерией является бактерия Bacillus subtilis.
9. Бактерия по п.7, отличающаяся тем, что указанной бактерией является бактерия Bacillus amyloliquefaciens.
10. Способ продукции пуринового нуклеозида, включающий культивирование бактерии по любому из пп.7-9 в питательной среде, приводящее к секреции указанного пуринового нуклеозида в указанную питательную среду, и выделение указанного пуринового нуклеозида из культуральной жидкости.
11. Способ продукции по п.10, отличающийся тем, что пуриновым нуклеозидом является инозин, ксантозин, гуанозин или аденозин.
12. Способ продукции пуринового нуклеотида, включающий культивирование бактерии по любому из пп.7-9 в питательной среде, приводящее к секреции указанного пуринового нуклеозида в указанную питательную среду, выделение указанного пуринового нуклеозида из культуральной жидкости, фосфорилирование указанного пуринового нуклеозида и выделение указанного пуринового нуклеотида.
13. Способ продукции пуринового нуклеотида по п.12, отличающийся тем, что пуриновым нуклеотидом является 5'-инозиновая кислота, ксантозин-5'-фосфат, 5'-гуаниловая кислота или 5'-адениловая кислота.
| МУТАНТНАЯ ФОСФОРИБОЗИЛПИРОФОСФАТСИНТЕТАЗА, ФРАГМЕНТ ДНК, БАКТЕРИЯ РОДА ESCHERICHIA - ПРОДУЦЕНТ L-ГИСТИДИНА И СПОСОБ ПРОДУКЦИИ L-ГИСТИДИНА | 2004 |
|
RU2282660C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИНОЗИНА И ИНОЗИН 5'-МОНОФОСФАТА, ШТАММ БАКТЕРИИ, ПРИНАДЛЕЖАЩЕЙ К РОДУ BACILLUS - ПРОДУЦЕНТ ИНОЗИНА (ВАРИАНТЫ) | 2002 |
|
RU2260040C2 |
| ROESSLER B.J | |||
| et | |||
| al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| J Biol Chem | |||
| Способ изготовления фанеры-переклейки | 1921 |
|
SU1993A1 |
| US 20070161090 A1, 12.07.2007. | |||
Авторы
Даты
2010-11-10—Публикация
2008-04-04—Подача