Предлагаемое изобретение относится к химии производных амидинов, в частности к способу получения N'-бензоил-N-замещенных амидинов 3-феноксибензойной кислоты или ее производных общей формулы

где 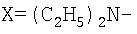 ;
;  ;
;  ;
;  ;
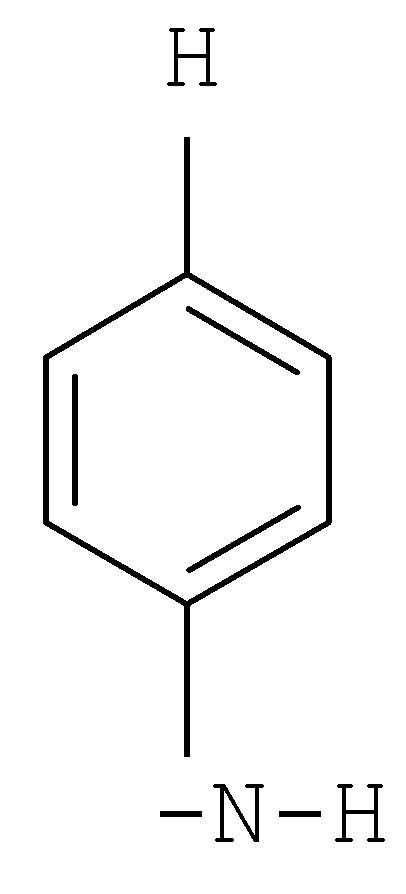
; 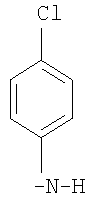 ;
;
Y - одинарная связь,
если  , то Y=
, то Y= 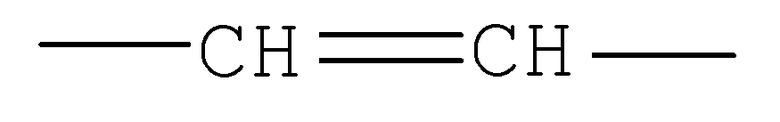 ,
,  ,
,
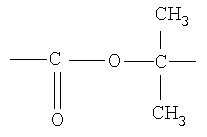
которые являются новыми по структуре 3-феноксифенилсодержащими соединениями и могут представлять собой полупродукты в синтезе вероятных биологически активных веществ. Многие соединения, содержащие дифенилоксидный фрагмент, проявляют различные виды биологической активности. Так перметрин [(3-феноксифенил)метиловый эфир 3-(2,2-дихлорэтенил)-2,2-диметилциклопропанкарбоновой кислоты, смесь цис- и транс-изомеров (3:1)] и фенотрин [2,2-диметил-3-(2-метил-1-пропенил)циклопропанкарбоновой кислоты (3-феноксифенил)метиловый эфир] используются как лекарственные препараты, обладающие противопаразитарным, противопедикулезным, инсектицидным, овоцидным фармакологическим действием. Имеются примеры использования феноксифенилацетиленов, полученных на основе 1-(2-метил-4-феноксифенил)этанона и 1-(3-феноксифенил)этанона, в качестве противотромботических, противовоспалительных, жаропонижающих агентов и анальгетиков [Химическая энциклопедия: В 5 т.: Т.5. / Ред. кол.: Кнунянц И.Л. и др. - М.: Большая Российская энцикл., 1992. - 639 с.]. В литературе сведения о методах получения соединений заявляемой структурной формулы отсутствуют.
Наиболее близким к предлагаемому изобретению является способ получения полизамащенных амидинов из имидоилбензотриазолов и аминов при микроволновом облучении. Реакции, проводимые при микроволновом облучении, с аминами были выполнены в запечатанных толстостенных трубах Пирекса или круглодонных флягах на 50 мл. Реакция, проводимая при микроволновом облучении, N-[(Е)-1-(1Н-1,2,3-бензотриазол-1-ил) этилиден]анилина и морфолина при 120°C и мощности облучения в 120 Вт в течение 10 минут дала 76%-ный выход 4-[(E)-1-метил-2-фенилэтенил] морфолина. Однако присутствие уксусной кислоты в смеси реакции привело к формированию продуктов ряда амидов ацетилированием аминов, и воды, которая была произведена, прореагировавшей с имидоилбензотриазолами, дав соответствующие амиды. Избежать этого позволило использование любого каталитического количества (20% в молях) кислоты Льюиса (AlCl3) или хлористоводородной соли аминов при 80°C и мощности облучения в 80 Вт в течение 10 мин. Используя оптимизированные условия реакции, проводимой при микроволновом облучении, было получено множество разнообразных полизамещенных амидинов с выходами 76-94%. [Alan R. Katritzky, Chunming Cai, Sandeep K. Singh. J. Org. Chem. 2006, 71(9), 3375].
Основным недостатком данного метода является применение микроволнового облучения, а следовательно, дорогостоящего оборудования, а также использование токсичных реагентов. Данный метод не приводит к получению вещества заявляемой структурной формулы.
Задачей предлагаемого изобретения является разработка технологичного малостадийного метода синтеза N'-бензоил-N-замещенных амидинов 3-феноксибензойной кислоты или ее производных, протекающего с высоким выходом.
Техническим результатом является расширение ассортимента химических соединений, в частности получение новых N'-бензоил-N-замещенных амидинов 3-феноксибензойной кислоты или ее производных, разработка метода синтеза новых N'-бензоил-N-замещенных амидинов 3-феноксибензойной кислоты или ее производных с высоким выходом.
Поставленный технический результат достигается в способе получения N'-бензоил-N-замещенных амидинов 3-феноксибензойной кислоты или ее производных общей формулы

где  ;
;  ;
;  ;
;  ;
;  ;
;
Y - одинарная связь,
если  , то Y=
, то Y=  ,
,  ,
,

путем взаимодействия N'-бензоилзамещенного этилимидата 3-феноксибензойной кислоты или ее производных кислот с аминами из ряда: диэтиламин, анилин, п-нитроанилин, п-хлоранилин, п-броманилин, в среде абсолютного бензола или хлороформа при мольных соотношениях реагентов, равных 1:1,2-1,26 соответственно, при температуре 55-76°C в течение 1-3 часов.
Сущностью метода является реакция получения N'-бензоил-N-замещенных амидинов 3-феноксибензойной кислоты или ее производных взаимодействием N'-бензоилзамещенного этилимидата 3-феноксибензойной кислоты или ее производных кислот с аминами из ряда: диэтиламин, анилин, п-нитроанилин, п-хлоранилин, п-броманилин

 ;
;  ;
;  ;
;  ;
;  ; где Y - одинарная связь,
; где Y - одинарная связь,
если  , то Y=
, то Y=  ,
,  ,
,

Способ осуществляется следующим образом.
Смесь N'-бензоилзамещенного этилимидата 3-феноксибензойной кислоты или ее производных кислот и аминов из ряда: диэтиламин, анилин, п-нитроанилин, п-хлоранилин, п-броманилин, при мольных соотношениях реагентов, равных соответственно 1:1,2-1,26 в среде абсолютного бензола или хлороформа помещают в четырехгорлый реактор, снабженный мешалкой, обратным холодильником с хлоркальциевой трубкой и термометром и при перемешивании выдерживают при температуре 55-76°C в течение 1-3 часов. После этого реакционную массу охлаждают до комнатной температуры. Из реакционной массы отгоняют растворитель при пониженном давлении. После удаления растворителя реакционная масса кристаллизуется. Выход полученного амидина после перекристаллизации из ЧХУ или после очистки с помощью колоночной хроматографии составил 55-98%.
Как показали проведенные исследования, наиболее удобным способом проведения реакции является ее осуществление в среде абсолютного бензола или хлороформа в присутствии 1,2-1,26-кратного избытка амина. Меньший избыток приводил к некоторому снижению выхода целевых продуктов за счет неполной конверсии N'-бензоилзамещенного этилимидата 3-феноксибензойной кислоты или ее производных, в случае использования в качестве второго реагента диаминов - к возможному образованию побочных продуктов дизамещения. Дальнейшее увеличение избытка амина из ряда: диэтиламин, анилин, п-нитроанилин, п-хлоранилин, п-броманилин, не влияло на выход целевых продуктов и являлось нецелесообразным.
Оптимальной температурой реакции является 55-76°C. Снижение температуры до комнатной приводит к сильному увеличению продолжительности данного взаимодействия и снижению выхода целевого продукта, в то время как ее повышение ограничено температурой кипения хлороформа и бензола.
Оптимальным временем реакции является 1-3 ч. Снижение времени реакции приводит к снижению степени превращения по исходному имидату, в то время как его повышение не влияло на выход целевых продуктов и являлось нецелесообразным. Строение синтезированных соединений подтверждено ЯМР1Н - спектроскопией и ИК-спектроскопией.
Изобретение иллюстрируется следующими примерами.
Пример 1

3-Феноксифенил-(N-бензоил-N-диэтил)амидин
В реактор помещают 4,8 г (0,014 моль) N'-бензоилзамещенного этилимидата 3-феноксибензойной кислоты в 15 мл абсолютного бензола. При перемешивании и охлаждении водяной баней по каплям прибавляют 1,23 г (0,017 моль) диэтиламина (мольное соотношение 1:1,2). Затем реакционную массу выдерживают при 55-60°C в течение 2 ч. После отгонки растворителя масса закристаллизовывается. Полученный продукт очищают перекристаллизацией из абсолютного четыреххлористого углерода. Выход 4,2 г (80% от теоретического), кристаллическое вещество белого цвета, Tпл.=127-128°C. ИК-спектр, υ, см-1: 1290-1072 (C-O-C), 1648 (C=N), 1702 (C=O), 1210 (C-N). Спектр ЯМР 1H, δ, м.д.: 6,94-7,759 м (Ar), 1,598-1,704 м (CH2), 1,179-1,219 т (CH3).
Пример 2
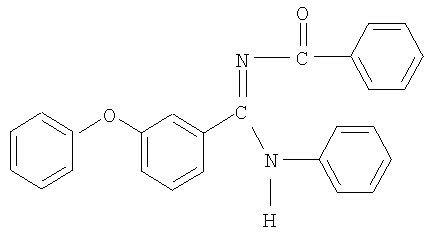
3-Феноксифенил-(N'-бензоил-N-фенил)амидин
В реактор помещают 4,8 г (0,014 моль) N'-бензоилзамещенного этилимидата 3-феноксибензойной кислоты в 15 мл абсолютного бензола. При перемешивании прибавляют 1,62 г (0,0176 моль) анилина (мольное соотношение 1:1,26). Затем реакционную массу выдерживают при 76°C в течение 3 ч. После отгонки растворителя масса закристаллизовывается. Полученный продукт очищают перекристаллизацией из абсолютного четыреххлористого углерода. Выход 4,23 г (77% от теоретического), кристаллическое вещество белого цвета, Tпл.=127-128°С.
ИК-спектр, υ, см-1: 1290-1072 (C-O-C), 1648 (C=N),1702 (C=O), 3430-3394, 1204 (N-H, C-N). Спектр ЯМР 1H, δ, м.д.: 6,895-7,756 м (Ar), 3,631 c (1H, NH).
Пример 3.

3-Феноксифенил-(N'-бензоил-N-4-нитрофенил)амидин
В реактор помещают 1 г (0,0029 моль) N'-бензоилзамещенного этилимидата 3-феноксибензойной кислоты в 20 мл абсолютного хлороформа. При перемешивании прибавляют 0,48 г (0,00348 моль) п-нитроанилина (мольное соотношение 1:1,2). Затем реакционную массу выдерживают при 60-65°C в течение 1-1,5 ч. После отгонки растворителя масса закристаллизовывается. Полученный продукт очищают перекристаллизацией из абсолютного четыреххлористого углерода. Выход 0,8 г (63% от теоретического), кристаллическое вещество светло-желтого цвета, Tпл.=96-100°C.
ИК-спектр, υ, см-1: 1290-1072 (C-O-C), 1650-1600 (C=N), 1700-1670 (С=О), 1360-1000 (C-N), 3430-3394 (N-H), 1548-1344 (NO2).
Спектр ЯМР 1H, δ, м.д.: 4,1 c (1H, NH), 6,727-7,911 м (Ar).
Пример 4
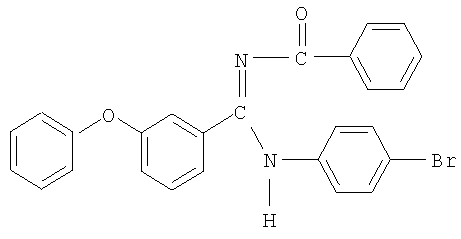
3-Феноксифенил-(N'-бензоил-N-4-бромфенил)амидин
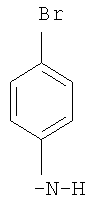
В реактор помещают 1 г (0,0029 моль) N'-бензоилзамещенного этилимидата 3-феноксибензойной кислоты в 30 мл абсолютного хлороформа. При перемешивании прибавляют 0,6 г (0,00348 моль) п-броманилина (мольное соотношение 1:1,2). Затем реакционную массу выдерживают при 60-65°C в течение 1-1,5 ч. После отгонки растворителя масса закристаллизовывается. Полученный продукт очищают перекристаллизацией из абсолютного четыреххлористого углерода. Выход 0,86 г (59% от теоретического), кристаллическое вещество белого цвета, Tпл.=l16-119°C.
ИК-спектр, υ, см-1: 1290-1072 (C-O-C), 1650-1600 (C=N), 1700-1670 (C=O), 1360-1000 (C-N), 3430-3394 (N-H).
Спектр ЯМР 1H, δ, м.д.: 6,895-7,756 м (Ar), 4,1 c (1H, NH).
Пример 5

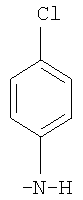
3-Феноксифенил-(N'-бензоил-N-4-хлорфенил)амидин
В реактор помещают 1 г (0,0029 моль) N'-бензоилзамещенного этилимидата 3-феноксибензойной кислоты в 15 мл абсолютного хлороформа. При перемешивании прибавляют 0,44 г (0,00348 моль) п-броманилина (мольное соотношение 1:1,2). Затем реакционную массу выдерживают при 60-65°C в течение 1-1,5 ч. После отгонки растворителя масса закристаллизовывается. Полученный продукт очищают перекристаллизацией из абсолютного четыреххлористого углерода. Выход 0,68 г (55% от теоретического), кристаллическое вещество белого цвета, Tпл.=75-80°C.
ИК-спектр, υ, см-1: 1290-1072 (C-O-C), 1650-1600 (С=N), 1700-1670 (C=O), 1360-1000 (C-N), 3430-3394 (N-H).
Спектр ЯМР 1H, δ, м.д.: 6,727-7,911 м (Ar), 4,1 c (1H, NH).
Пример 6

3-(3-Феноксифенил)-2-пропенил-(N'-бензоил-N-4-бромфенил)амидин
В реактор помещают 4,8 г (0,014 моль) N'-бензоилзамещенного этилимидата 3-(3-феноксифенил)-2-пропеновой кислоты в абсолютном бензоле. При перемешивании и охлаждении водяной баней прибавляют 1,23 г (0,017 моль) п-броманилина. Затем реакционную массу выдерживают при 55-60°C в течение 2 ч. После очистки с помощью колоночной хроматографии выход N'-бензоилзамещенного амидина 3-(3-феноксифенил)-2-пропеновой кислоты составил 98%. T.кип. 252-254°C/4 мм рт.ст.
ИК-спектр, υ, см-1: 3320-3450 (C-N, N-H); 1740 (N-H); 1695 (C=O); 1678 (C=N); 1240-1070 (C-O-C).
Спектр ЯМР 1H, δ, м.д.: 6,839-7,657 м (9Н, C6H5OC6H4), 3,55 с (1H, NH), 75,44-7,46 д (1H, Ar-CH), 5,62-5,67 д (1H, CH-CN).
Пример 7

3-(3-Феноксифенил)-2-бутенил-(N'-бензоил-N-4-бромфенил)амидин
В реактор помещают 5 г (0,014 моль) N'-бензоилзамещенного этилимидата 3-(3-феноксифенил)-2-бутеновой кислоты в абсолютном бензоле. При перемешивании и охлаждении водяной баней прибавляют 1,23 г (0,017 моль) п-броманилина. Затем реакционную массу выдерживают при 55-60°C в течение 2 ч. После очистки с помощью колоночной хроматографии выход N'-бензоилзамещенного амидина 3-(3-феноксифенил)-2-бутеновой кислоты составил 97%. Т.кип. 260-262°C/4 мм рт.ст.
ИК-спектр, υ, см-1: 3350-3500 (C-N, N-H); 1755 (N-H); 1708 (C=O); 1672 (C=N); 970-1126 (C-O-C).
Спектр ЯМР 1H, δ, м.д.: 6,622-7,657 м (9H, C6H5OC6H4), 7,442-7,467 c (1H, CH-CN), 3,55 с (1H, NH), 2,22-2,35 c (3H, CH3).
Пример 8

2-Метил-2-(3-феноксибензоат)пропил-(N'-бензоил-N-4-бромфенил)амидин
В реактор помещают 5,6 г (0,014 моль) N'-бензоилзамещенного этилимидата 2-метил-2-(3-феноксибензоат)пропионовой кислоты в абсолютном бензоле. При перемешивании и охлаждении водяной баней прибавляют 1,23 г (0,017 моль) п-броманилина. Затем реакционную массу выдерживают при 55-60°C в течение 2 ч. После очистки с помощью колоночной хроматографии выход N'-бензоилзамещенного амидина 2-метил-2-(3-феноксибензоат)пропионовой кислоты составил 95%. T.кип. 258-260°C/4 мм рт.ст.
ИК-спектр, υ, см-1: 1654 (C=N); 2938 (ν CH); 1287 (δ CH3); 1732 (C=O).
Спектр ЯМР 1H, δ, м.д.: 1,8 c (6H, CH3), 6,9-7,8 м (C6H5OC6H4), 3,45 c (1H, NH).
Выводы
Предлагаемый способ позволяет получить N'-бензоил-N-замещенные амидины 3-феноксибензойной кислоты или ее производных в одну стадию с хорошими выходами. К его достоинствам можно отнести препаративную простоту синтеза и легкость выделения целевых продуктов с высокой степенью чистоты. Структура синтезированных соединений подтверждена ИК-, ЯМР 1H-спектроскопией.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ N, N-ДИАЛКИЛ, N'-АЦИЛ-(АЦИЛДИАЛКОКСИФОСФОРИЛ)ЭТАНАМИДИНОВ | 2008 |
|
RU2374258C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-ФЕНОКСИФЕНИЛМЕТОКСИПРОПИОНИТРИЛА | 2009 |
|
RU2412161C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-4-НИТРОФЕНИЛБЕНЗАМИДИНА | 2012 |
|
RU2480452C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-N-ФЕНИЛАМИНО-2-ЦИАНОАДАМАНТАНА ИЛИ ЕГО ПРОИЗВОДНЫХ | 2007 |
|
RU2344124C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-МЕТИЛ-2-(3-ФЕНОКСИБЕНЗОАТ)ПРОПИОНИТРИЛА | 2009 |
|
RU2398762C1 |
| СПОСОБ ПОЛУЧЕНИЯ 10-АРИЛ-7,8,12,13-ТЕТРАОКСА-10-АЗАСПИРО[5.7]ТРИДЕКАНОВ | 2014 |
|
RU2584950C1 |
| Способ получения производных N-фениладамантан-1-карбоксамида | 2016 |
|
RU2626237C1 |
| Замещенные N-адамантиланилины, проявляющие психостимулирующую и антикаталептическую активность | 1980 |
|
SU860446A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(3-ФЕНОКСИФЕНИЛ)БУТАН-1,3-ДИОНА | 2013 |
|
RU2529029C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЕННЫХ (2-ТРИМЕТИЛСИЛИЛ-2-ДИАЛКОКСИФОСФОРИЛ)АЦЕТАМИДИНОВ | 2010 |
|
RU2427583C1 |
Изобретение относится к способу получения N'-бензоил-N-замещенных амидинов 3-феноксибензойной кислоты или ее производных общей формулы
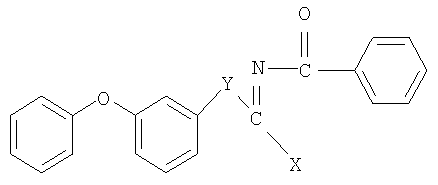
где  ;
;  ;
;  ;
;  ;
;  ; Y - одинарная связь,
; Y - одинарная связь,
если  то Y=
то Y=  ,
, 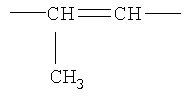 ,
,
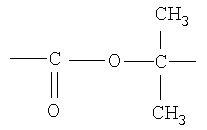
заключающемуся во взаимодействии N'-бензоилзамещенного этилимидата 3-феноксибензойной кислоты или ее производных с аминами из ряда: диэтиламин, анилин, п-нитроанилин, п-хлоранилин, п-броманилин, в среде абсолютного бензола или хлороформа при мольных соотношениях, равных 1:1,2-1,26, при температуре 55-76°С в течение 1-3 часов. Техническим результатом является получение новых N'-бензоил-N'-замещенных амидинов 3-феноксибензойной кислоты или ее производных с высоким выходом.
Способ получения N'-бензоил-N-замещенных амидинов 3-феноксибензойной кислоты или ее производных общей формулы

 ;
;  ;
;  ;
;  ;
;  ; где Y - одинарная связь
; где Y - одинарная связь
Если 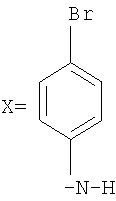 ; то Y=
; то Y=  ,
, 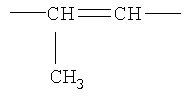 ,
,

заключающийся во взаимодействии N'-бензоилзамещенного этилимидата 3-феноксибензойной кислоты или ее производных с аминами из ряда: диэтиламин, анилин, п-нитроанилин, п-хлоранилин, п-броманилин в среде абсолютного бензола или хлороформа при мольных соотношениях реагентов, равных соответственно 1:1,2-1,26, при температуре 55-76°С в течение 1-3 ч.
| Попов Ю.В | |||
| и др | |||
| Синтез и реакции гидрохлоридов имидатов м-феноксибензойной кислоты | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Katritzky A.R | |||
| Efficient microwave access to polysubstituted amidines from imidobenzotriazoles | |||
| J | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
Авторы
Даты
2011-01-10—Публикация
2009-06-16—Подача