3 Предлагаются новые биологически активные соединения замещенные М-адамантиланилина. проявляющие психостимулирующую и антикаталептическую активность. Известны различные производные адамантана, обладающие психостимулирующей активностью, например амид 4-кетоадамантанкарбоновой кислоты, имеющей ярко выраженную имМуностимулирующу активность с одновременным повышение) физической работоспособности. Кроме того, известен Ы-(2-адамантил)анилин, который наряду с психостимулирующими свойствами имеет значительную токсичность. В медицинской практике используют как психомоторный стимулятор фенамин, а также мидантан, обладающий антикаталептическим действием. Целью изобретения является расширег ние арсенала средств воздействия на живой организм, повышающих физическую работоспособность, проявляющих антикатзлептическую активность и обладающих низкой токсичностью. Поставленная цель достигается новыми замещенными N-адамантиланилина общей формулы Ч -НН-О-йц : где - Н; R -CHa(1); Ri«R2 R3 R5-H;R4-OH(2); Ri-R2 R3 R5 - Н; R4-OCH3(3); Ri R3 R4 R5-H;R2-CI(4); Ri R2-R4 R5 - Hr Rs-CI(5); Ri R2 R3 R5-K;R4-CI(6); - H; R4-Br(, Ri R2 R4-R5-H;R3-N02(8); Ri R2 R3 R5-H;R4-N03(9); R2 R3-R4 R5-H,-Ri-OH(lO); R2-R3 R5-H; Ri-OH; R4-F(11); R2-R3 R5-H; Ri-CI; R4-F(12). обладающими психостимулирующей и антикаталептической активностью. Предлагаемые соединения и их хлористоводородные соли представляют собой белые или окрашенные кристаллические вещества, растворимые в спирте или воДе. Их получают известным способом - взаимодействием со ответствующего кетона с муравьиной кислотой и амином или с муравьинокислой солью амина при нагревании. В предложенном случае взаимодейстВИЮ подвергают смесь 1 моль адамантзноиа, 2 моль ароматического амина и 2 моль муравьиной кислоты при кипячении в течение 6-10 ч при температуре 130-180°С, а аатем в течение 1-2 ч с избытком соляной кислоты. Непрореагировавший адамантанон экстрагируют эфиром или бензолом, кислый водный слой насыщают бикарбонатом натрия и экстрагируют эфиром или бензолом. Экстракт сушат сернокислым магнием, растворитель отгоняют и получают целевой продукт в виде основания. Следует отметить, что при выделении именно К|-(2-адамантил)-п-броманилина после окончания нагревания ведут подкисленив охлажденной реакционной массы строго расчетным количеством соляной кислоты и оадок целевого продукта (в виде основания отфильтровывают (не вошедший в реакцию п-броманилин, взятый в избытке, остается в растворе в виде соли). П р и м е р 1. Получение М-(2-адамантил)п-нитроанилина. Смесь 5.5 г (0,04 моль) п-нитроанилина и 1.85 г (0.04 моль) 99%-ной муравьиной кислоты нагревают до 100°С и при этой температуре прибавляют 3 г (0.02 моль) адамантанона. Реакционную смесь кипятят 10 ч при температуре 150-160°С, охлаждают, добавляют 16 мл разбавленной соляной кислоты и кипятят 2 ч. Кислый раствор экстрагируют эфиром, водный слой насыщают бикарбонатом натрия и экстрагируют эфиром основание амина. Экстракт сушат сернокислым магнием, растворитель отгоняют и получают 4,1 г целевого продукта (кристаллы желтого цвета), выход 76%. т.пл.180-181.5°С (из этанола). Найдено. %: С 71.00; Н 7.47; N10.36. Cl6H2QN202 Вычислено.%: 070.56; Н 7.40; N 10,28. П р и м е р 2. Получение Ы-(2-адамантил)п-анизидина. К нагретой до 100°С смеси 9.85 г (0.08 моль) п-анизидина и 3.68 г (0.08 моль) 99%-ной муравьиной кислоты прибавляют 6 г (0,04 моль) адамантанона и кипятят 10ч при.температуре бани 150-160°С. К охлажденной реакционной массе прибавляют 35 мл разбавленной соляной кислоты, кипятят 2 ч, охлаждают, осадок отфильтровывают и получают 6.5 г хлоргидрата Ы-(2-адамантил)-п-анизидина. выход 56%. т.пл. 247-248°С (из этанола). Найдено.%: СП2.87. Ci7H23NO.HCt, Вычислено,%: С 12.41, Хлоргидрат растворяют в воде, насыщают бикарбонатом натрия и экстрагируют эфиром основание амина, т.пл. 106-.107°С (60%-ный этанол). Найдено, %: С80.00; Н 8,93; N 5,71. C17H23NO-HCI Вычислено,%: С 79.33: Н 9.01; N 5,44. П р и м е р 3. Получение f f лдлмантил)г п-нитроанилина.
К нагретой до 100°С смеси 5,5 г (0,04 моль) п-нитроанилина и 1,85 г (0,04 моль) муравьиной кислоты прибавляют 3 г (0,02 моль)1адамантднона и кипятят 10 ч при температуре 150-160°С. К охлажденной массе прибавляют 18 мл разбавленной (1:1) соляной кислоты, кипятят 2 ч, из охлажденного раствора экстрагируют эфиром непрореагировавший кетон. Водный слой насыщают бикарбонатом натрия и экстрагирук т эфиром, экстракт сушат сернокислым магнием, растворитель отгоняют и получают 4 г основания (кристаллы оранжевого цвета), выход 74%, т.пл. 92-93°С (из этанола),
Найдено,%: С 70,41,- Н 7,27: N 10.40,
Cl6H20N202
Вычислено,%: С 70,56: Н 7,40: N 10,28.
П р и м е р 4. Получение Ы-(1-окси-4-адамантил)анилина.
Смесь 3 г (0,018 моль) 1-окси-4-адамантанона, 4,5 г (0,036 моль) форманилида и 1,1 г (0,024 моль) муравьиной кислоты кипятят 12 ч при температуре бани , добавляют 10 мл 10%-ной соляной кислоты и кипятят 1ч..
Реакционную смесь охлаждают и экстрагируют бензолом непрореагировавший кетон. Водный слой насыщают бикарбонатом натрия и экстрагируют хлороформом, хлороформный экстракт сушат сернокислым магнпем, растворитель упаривают и получают 2,6 г (59%) целевого амина, т,пл. , 188-189 С (из этанола).
Найдено,%: С 78,84: Н 8,52: N5,75.
C16H21NO
Вычислено,%: С 78,97: Н 8.70: N 5,76.
Хлоргидрат плавится при 237-238 С (из этанола)..
Найден6,%: С112,17.
Ci6H2iNO-HGI
Вычислено,%: С1 12,66.
П р и м е р 5. Получение Ы-(1-окси-4-адамантил)-п-фторанилина.
К нагретой до 100°С смеси 4 г (0,036 моль) п-фторанилина и 1,72 г (0,036 моль) 99%-ной муравьиной кислоты прибавляют в течение 15 мин 3 г(0,018 моль) 1-ркси-4-адамантанона и кипятят смесь 15 ч при температуре 150-160 С. После охлаждения к реакционной массе прибавляют 10 мл 10%-ной соляной кислоты и кипятят 2 ч. Непрореагировавший кетон экстрагируют бензолом (3x50 мл). Кислый водный раствор насыщают бикарбонатом натрия и экстрагируют хлороформом (8x30 .мл). Экстракт сушат сульфатом магния и обрабатывают углем. Хлороформ отгоняют в вакууме и получают 2.8 г (75%) основания амина т.пл.98-107°С (смесь стереоизомеров, из этанола).
Найдено,%: N5,60.
Ci6H2oNO
Вычислено, %; N5,36.
Хлоргидрат плавится при 221-223 С (из ацетона).
Найдено, %: СП 1,25.
Ci6H2oNO-Ha
Вычислено,%: С111,90.
Приме р 6, Получение N-{2-aдaмaнтил)п-хлоранилина.
Кнагретойдо ЮО Ссмео 10,02 гСО,08 моль) п-хлоранилина и 3,68 г (0,08 моль) 99%-ной муравьиной кислоты прибавляют в течение 20 м|47( 6 г (0,04 моль) адамантанона и кипятят смесь 6 ч при температуре 150-160 С.
После охлаждения к реакционной массе прибавляют 15 мл 15%-ной соляной кислоты, кипятят 2 ч, исходный кетон экстрагируют эфиром (3x50). Водный кислый раствор насыщают бикарбонатом натрия и экстрагирует эфиром (4x80). Эфирный экстракт сушат сульфатом магния. Эфир отгоняют в вакууме и получают 7,28 г (70%) основания амина, т.пл.82-83 С (из спирта).
Найдено,%: С113,29.
Ci6H2oNCI
Вычислено,%: С113,54.
П р и м е р 7. Получение N-(2-aдaмaнтил)п-хлоранилина.
Смесь 10,02 г(0,08 моль) п-хлоранилина и 3,68 г (0, моль) 99%-ной муравьиной кислоты нагревают до 100°С, при этой температуре прибавляют 6 г(0,04 моль) адамантанона и кипятят 6 ч при температуре 150-ТбО С. После охлаждения к реакционной массе прибавляют 15 мл 10%гной соляной кислоты и кипятят 2 ч. Выпавший после охлаждения осадок отф 1льтровывают и промывают два раза эфиром. Выход хлоргидрата 8,1 г (77,8%), т.пл.195-196 С (из абсолютного этанола).
Найдено,%:С123,32.
Ci6H2oNCr-HCI
Вычислено,%: С123,77.
П р и м е р 8, Получение N-(2-aдaмaнтил)п-броманилйна.
К смеси 13,7 г(0,08 моль) п-броманилина и 3,68 г (0,08 моль) 99%-ной муравьиной кислоты прибавляют 6 г (0,04 моль) адамантанона и кипятят 6 ч при температуре 150160°С. К охлажденной реакционной смеси прибавляют 15 мл 15%-ной соляной кислоты, кипятят 0,5 ч,.охлаждают и отфильтровывают 9,6 г основания N-{2-aAaмантил)-п-броманилина, выход 80%, т.пл. 100-102°С (абсолютный этанол).
Найдено,%: С 62,91: И 6,51: N 4,65; Вг 26,11.
Ci6H2oBrN 786044 Вычислено.%; С 62.75; Н 6,58: N4.57; 8г 26,09. . П р и м е р 9. Получение М-(1-хлор-4-адамантил}-п-фторанилина. Смесь 2,38 г(0.021 моль)п-фторанилине5 «м 1,05 г (0,02 моль) 99%-ной муравьиной кислоты нагревают До 100°С. при этой температуре прибавляют2 г 1-хлор-4-адамантаиона и кипятят 10 ч при температуре 150-160 С. После охлаждения к реакцион-10 ной массе прибавляют 10 мл 15%-нйй соляной кислоты, кипятят 2 ч. осадок отфильтровывают, два раза промывают зфиром. Осадок растворяют в воде, раствор иасыщают бикарбонатом натрия и экстраги-15 руют эфиром, Эфирный экстракт сушат сульфатом магния, эфир отгоняют и получают 2.4 г (80%) основания амина; t.ri}iii83S5°C (из этанола). Найдено.%; N 5.23.- F 7.14; О 15.53. .20 CieHigClNF Вычислено,%: N 5,25; F 6.91; CI12.71. Хлоргидрат плавится при 221 222С (из абсолютного этанола). НайденоД:С111,18.25 Ct9Hi9CI Вычислено,%: С111,22. П р им ер 10. Получение М-{2-адамантил -п-яминофендла.. Смесь 4,36 г (0.04 мрль)п-аминофенола30 и2 г(0,04 моль)99%-мой муравьиной кислоты нагревают до 1рО°С. при этой температуре прибавляют 3 г (0,02 моль) адамантанона и кипятят 6 ч при температуре 150-160°С. После охлаждения к реакционной смеси35 прибавляют 15 мл 1-5%-ной соляной кислоты, кипятят 1,5 ч. охлаждают, выпавший осадок отфильтровывают, промывают эфиром W получают4г(80%)хлоргИдратаМ-{2-адамантил)-п-ам1/1нофенола. После кристаллизации40 из этанола т.разл.275°С. 1- йдено.%: СИЗ,03. C16H22CINO Вычислено.%: СМ2,67. П р и м 8 р 11. Получение М-(2-адаман-45 тил)-о-хлоранилина. К горячему раствору 3.7 г (0,03 моль) о-хлоранилйна в 2.5 мл 99%-иой муравьиной кислоты прибавляют 3 г (0.02 моль) адамантанона и кипятят при температуре50 150°С в течение 5 ч. К охлажденной реакционной массе добавляют 10 мл 15%-ного раствора соляной кислоты, кипятят 1 ч, экстрагируют эфиром непрореагировавший адамантанон, водный слой насыщают би-55 карбонатом натрия и экстрагируют эфиром основание амина. Экстракт сушат сернокислым магнием, растворитель отгоняют и получают 3.2 г целевого продукта, выход 62%, т.пл.114-115 С (абсолютный этанол). 68 Найдено.%: Ct13,55. Ci6H2oCIN. Вычислено,%: С1 13.64. П р и м е р 12. Получение М-(2-адамантил)-п-толуидина. Смесь 4,3 г (0,04 моль) п-толуидина. 2 мл муравьиной кисльты и 3 г (0,02 моль) адамантано а кипятятх4 ч при температуре 130-150 С. К раствору добавляют концентрированную соляную кислоту, кипятят 1 ч и экстрагируют эфиром непрореагировавший адамантанон. Кислый слой разбавляют ЕОДОй и отфильтровывают выпавшую солянокислую соль М-(2-адамантил1-п-толуид,ина, выходб г(90%).т.пл.254-258С(вода). Найдено.%: СМ2,76, CnHzaN.HCI Вычислено,%: С 12,80. Солянокислую соль суспендируют в воде, подщелачивают щелочью и экстрагируют эфиром основание амина, т.пл.48-49°С. Найдено.%: С 84,48; Н 9,82. Ci7H23N Изучение указанных соединений показывает, что они проявляют свойства, обесаечивающие увеличение уровня физической работоспособности, усиление двигательной активности и снятие трифтазиновой каталепсии. Наиболее сильным положительным влиянием на уровень физической работоспособности обладают соединения адамантиланилина, содержащие галоид, (соединения 4, 5, 6 и 7). Все заявляеЙ1,1е соединения по данному типу действия активнее известного фенамина и имеют значите.яьно большую широту терапевтического действия, чем фенамин. Эти соединения обладают также выра енной антикаталептической активностью (по тесту трифтазиновой каталепсии), в 9-19 раз превосходящей активность мидантана (прототипа), и в 2-30 раз меньшей тОксичностью. Наиболее активным из заявляемых соединений является (2-адамантил)-п-броманилин (бромантан). Бромактан обладает выраженной психостимулирующей активностью, что проявляется в повышении уровня физической работоспособности, оптимизации оперант Ой деятельности, снятия психрдепримирующих эффектов транквилизаторов, Это соединение в 83 раза менее токсич Ог чемфенамин. По елияник на уровень физической работоспособности это соедииение превосходит фенамин 84 раза. Так, максимальное увеличение длительности плавания мышей при введении фенамина составляет 54% по сравнению с исходным
9«6044610
уровнем, а после введения бромантанаского раствора), полученными в тот же день. 210%. Разрешенный для клинических испы- Исследуемые соединения вводили анутританий препарат адапрамин, являюи(1 йсябрюшинно за 60 мин до плавания. Нераствопроизводным адамантана, увеличивает дли- римые в воде вещества вводили в виде тельность плавания мышей на 51% (макси- 5 суспензии в твине-80. Вещества вводили в
мально).дозах 1,5,10и25мг/кг,
Следует отметить, что положительноеДругим тестом, характеризующим псивлияние фенамина, а также другого исполь- хостимулИрующие зффекты заявляемых соезуемого в настоящее время психостимулято- динений, являлся уровеньспонтанной
ра-сиднокарба - на сложную оперантнуюТО двигательной активности (ориентировочная
деятельность крыс проявляется в дозах, нереакция) при помещении животных в актодающих прироста физической работоспо- метр на 15 мин.
собности. Фенамин и сиднокарб в дозах,, Спонтанную двигательную активность
оказывающих положительное влияние ндизучади на приборе ДАЭР-20 всегда в одно
уровень физической работоспособности, от-15 и то же время дня. Результаты опытных
рицательно влияют на качество оперантнойгрупп сравнивали с контролем, который стадеятельности крыс.вился ежедневно. Исследуемые вещества
Бромантан обладает способностью опвводили знутрибрюшинно за 60 мин до опытимизировать сложную оперативную дея-та в дозз 10 мл/кг. Эффектзаявляемых сое тельность животных в щироком диапазоне20 дйкений по двум указанным тестам доз, в том числе и в дозах, оказывающихсравнивали с действием известного психоположительное влияние на уровень физиче-моторного стимулятора фенамина, ской работоспособности.
Указанное свойство выгодно отличает, Противоп ркинсоническЬе действие
заявляемый бромантан от фенамина и сид-25 оценивали на крысах по антикаталептиченокарба, так как приего применении можноской активности заявляемых соединений на
получи1-ь- одновременно стимуляци(6 физи-модели трифтазиноврй каталепс ии 02 мг/кг
ческой и психической работоспособности.внутрибрюшинно) с оценкой выраженности.
Заявляемый бромантан оказывает ояти-каталепсии в баллах по метрдике Morpufgo.
мальное корректорное действие на психодеп-30 Заявляемые соединения вводили внутриримирующие эффекты различныхбрюшинно вдозах5и Юмг/кгзаЗОмин до
транквилизаторов (бензодиазелина, триокса-введения нейролептика: Уровень каталепзина, мепробамата, оксибутирата натрия) посии (способность животного .удерживать
, тесту расстройств оперантной деятельности.придан ную ему неудобную позу с опорой на
Восстановление нарушенной после вве-35 ступеньки разной высоты) оценивали через
дения указанных транквилизаторов операн-бОмин после введения трифтазина. Больший
твой деятельности с помощью фенамина илиуровень каталепсии соответствует большему
сиднокарба происходит частично или с про-числу баллов, выставленных данной группе
явлением отрицательного действия исполь-животных. Результаты, полученные в опыт
зованных психостимуляторов на отдельные40 ных группах, сравнивали с контролем (введ&показатели зтой деятельностиние трифтазина и физиологического
Кроме того, бромантан обладает способ-раствора). .
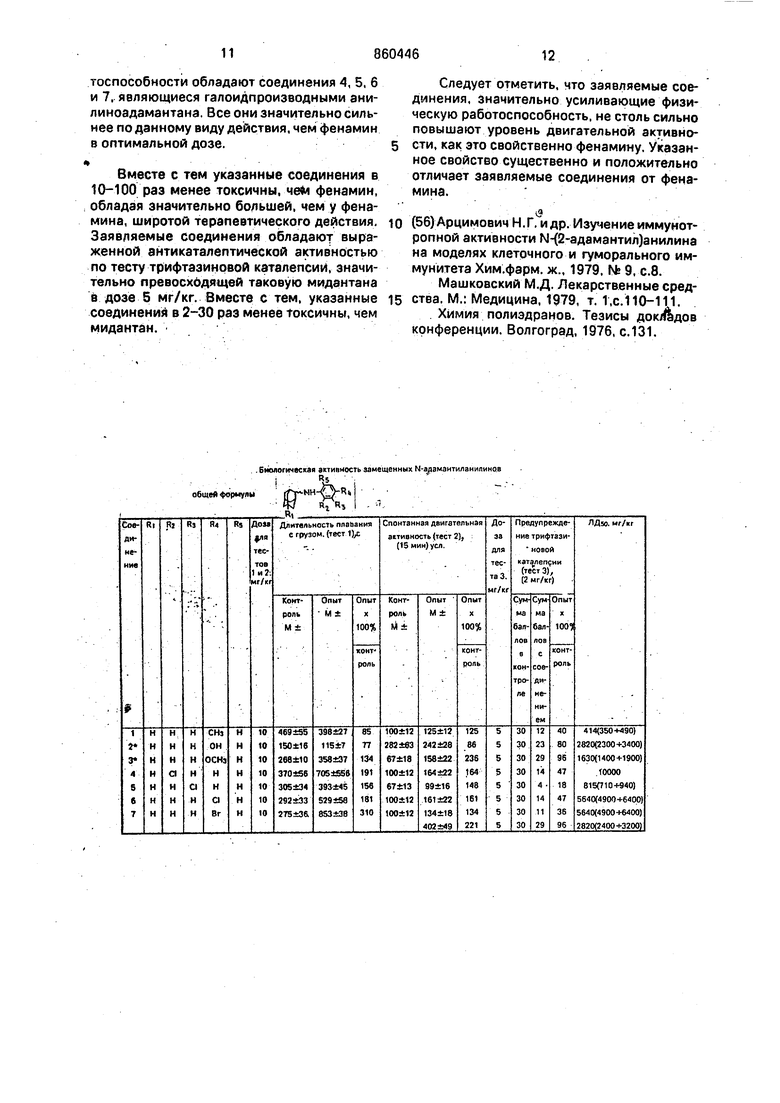
ностью снимать вызванную трифтазином иДля сравнения йслользовали один из нагалоперидолом каталепсию. По зтому видуиболее активных противопаркинсонических действия он превосходит используемый на45 П|эепаратов-мидантан, являющийся гидропрактике противопаркинсонический препа-хлоридом 1-аминоадамантана. рат мидантан в 2,5 раза. , Кроме; того, иссл$/|овали острую суточДля оценки влияни заявляемых соедй : ; ную то сичНбсть.заявляемых соединений нений на уровень физической работоспособ- зкспресс-методом. Полученные результаты ности использовали тест плавания мышей сSO по биологической активности для некоторых грузом в 10% от веса тела до полного изучавшихся доз заявляемых соединений ления (погружение на дно). Животные плава представлены втабяице. Из данныхтаблицы ли в термостатируемой ванне (температуреследует, что заявляемые соединения обладаводы 27°С). Показателем уровня физическойют выражен ной биологической активностью, работоспособности являлось время с МО-55 проявляющейся длЯбольшинсгва из них в мента помещения животного в воду до егоувеличении уровня физической работоспопогружения на дно. Для оценки эффекта со-собности, усилении двигVтeльнoй активединения брали группы из 20 мышей. Опыт-ности или снятии трифтазиновой ные данные сравнивали с .даннымикаталепсии. Наиболее сильным положительконтрольной группы (введение физиологиче-ным влиянием на уровень физической работоспособности обладают соединения 4, 5, 6 и 7, являющиеся галоиДпроизводными анилиноадамантана. Все они значительно сильнее поданному виду действия, чем фенамин в оптимальной дозе.
. ,
Вместе с тем указанные соединения в 10-100 раз менее токсичны, че411 фенамин, обладая значительно большей, чем у фенамина, широтой терапевтического действия, Заявляемые соединения обладают выраженной антикаталептической активностью по тесту трифтазиновой каталепсии, значительно превосхддящей таковую мидантана в дозе 5 мг/кг. Вместе с тем, указанные соединения в 2-30 раз менее токсичны, чем мидантан.
Следует отметить, что заявляемые соединения, значительно усиливающие физическую работоспособность, не столь сильно повышают уровень двигательной активности, как зто свойственно фенамину. Указанное свойство существенно и положительно отличает заявляемые соединения от фенамина.
9
(56) Арцимович Н, Г. и др. Изучение иммунотропной активности N-{2-aдaмaнтил)aнилинa на моделях клеточного и гуморального иммунитета Хим.фарм. ж., 1979, № 9, с.8.
Машковский М.Д. Лекарственные средства, М,: Медицина, 1979, т. 1,с.110-111,
Химия полиэдранов. Тезисы конференции. Волгоград, 1976, с.131.




| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ N-АДАМАНТИЛАНИЛИНЫ, ПРОЯВЛЯЮЩИЕ ПСИХОСТИМУЛИРУЮЩУЮ И АНТИКАТАЛЕПТИЧЕСКУЮ АКТИВНОСТЬ | 1981 |
|
SU1018361A1 |
| ОКСИПРОИЗВОДНЫЕ ДИ-(АДАМАНТИЛ)АМИНА, ОБЛАДАЮЩИЕ АНТИКАТАЛЕПТИЧЕСКОЙ АКТИВНОСТЬЮ | 1978 |
|
SU731714A1 |
| Хлоргидрат N-(2-адамантил)-N-фторанилина, обладающий иммуностимулирующей активностью и повышающий физическую работоспособность | 1979 |
|
SU782313A1 |
| Гидрохлорид 4-адамантоиламино-3-0-адамантоил-6-метил-2-этил-пиридин, обладающий психостимулирующей активностью, повышающий физическую работоспособность и имеющий антикаталептическую активность | 1982 |
|
SU1055105A1 |
| Производные 2-аминоадамантана, проявляющие антикаталептическую активность | 1974 |
|
SU580864A1 |
| Производные 1-оксиадамантана, проявляющие антикаталептическую активность | 1974 |
|
SU535085A1 |
| СПОСОБ ПОЛУЧЕНИЯ N-(4-БРОМФЕНИЛ)-N-(2-АДАМАНТИЛ)АМИНА | 1988 |
|
RU1601978C |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛОАЛКИЛАМИНОВ | 2010 |
|
RU2425828C1 |
| ГИДРОХЛОРИД АДАМАНТ-2-ИЛАМИНОЭТИЛОВОГО ЭФИРА П-ХЛОРФЕНОКСИУКСУСНОЙ КИСЛОТЫ, ОБЛАДАЮЩИЙ ТЕРМОПРОТЕКТОРНОЙ И ПСИХОСТИМУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 1990 |
|
SU1771186A1 |
| Гидрохлориды 8-замещенных 2,3,3 @ ,4,5,6-гексагидро-1Н-пиразино-/3,2,1- @ ,к/-карбазолов, обладающие психотропным действием | 1981 |
|
SU1694582A1 |

. Биологическая активяость замещенных Ы-адэмантилаиилинав 1 RS
-R
NHобщейяТ
Соединение испытимли е «ие пориетомморойной соли.
1фодолхекие TaiJanuji
Авторы
Даты
1993-11-30—Публикация
1980-04-21—Подача