Изобретение относится к фармацевтической промышленности и может быть использовано при получении полимикроэлементных лекарственных препаратов.
Широко известны поливитаминно-микроэлементные препараты («Квадевит», «Компливит», «Витрум», «Центрум» и другие), приготовленные на основе сульфатов переходных металлов - железа, цинка, марганца, кобальта, меди и др. Однако степень усвоения железа, а также меди, кобальта и других многовалентных металлов из их ионных соединений относительно низка: обычно она составляет 3-7% (изредка и в условиях особой диеты - до 15-17%), что обусловлено прежде всего необратимым связыванием этих ионов в исключительно прочные нерастворимые комплексы некоторыми специфическими компонентами пищи - фитином, полифенольными соединениями, оксалатами, определенными белками бобовых и т.д. Другой важной причиной низкой биологической доступности металлов из простых ионогенных соединений является взаимное конкурентное подавление абсорбции различных ионов в желудочно-кишечном тракте (ЖКТ): так, типичные для пищевых продуктов концентрации ионов кальция в 2,5-4 раза уменьшают биодоступность ионов железа, наличие ионов цинка препятствует усвоению ионов меди и т.д.
Кроме того, в тонком кишечнике ионы железа, в свою очередь, осаждают фосфат-ион с образованием нерастворимого фосфата железа: общеизвестна опасность развития рахита детей в условиях избыточного потребления железа (что связано обычно со спецификой водоснабжения населения данной местности). Ионы двухвалентного железа количественно связывают сероводород, являющийся одним из основных медиаторов перистальтики кишечника, - следствием может являться серия трудно диагностируемых кишечных расстройств и дисбактериозов. Ионы железа образуют прочное нерастворимое соединение с селенит-ионом, препятствуя его усвоению. Ионные соединения железа при пероральном применении резко ухудшают цвет зубной эмали: если в животноводстве этот фактор и не кажется чересчур значимым, то в витаминно-микроэлементных композициях медицинского назначения присутствие свободных ионов Fe(II) или Fe(III) все же крайне нежелательно. Ионы железа и меди резко обостряют протекание заболеваний, связанных с эрозией слизистых оболочек ЖКТ.
Особенно существенна проблема химической несовместимости йодид-ионов с ионами меди (II) и железа (III). В ходе совместного хранения в составе премикса йодид-ионы окисляются ионами железа (III) до свободного йода и теряются за счет высокой летучести последнего. Двухвалентная медь (и в ходе хранения, и в ЖКТ) переводит йодид-ион в абсолютно пассивный в биологическом отношении йодид одновалентной меди: а поскольку мольное отношение Cu/I в премиксах весьма велико, то в типичных условиях можно ожидать полного или почти полного отсутствия усвояемого йода в пищевых добавках (не говоря уж о вынужденной - по этой причине - практике огромной передозировки йодидов, что весьма нежелательно с точки зрения стабильности гормонального статуса животных или человека).
Ионы металлов переменной валентности катализируют окисление и окислительную полимеризацию ненасыщенных органических соединений кислородом воздуха, что отражается прежде всего на сохранности витаминов в премиксе или витаминно-микроэлементной композиции. Если полиненасыщенные жирные кислоты («витамин F») еще можно вводить в рацион помимо премикса, то жирорастворимые витамины (A, D, Е) являются традиционными его компонентами: ионы переходных металлов, входящих в состав этой поливитаминно-полимикроэлементной композиции, резко уменьшают допустимые сроки хранения продукта (что выражается в «прогоркании» масел и падении аналитически определяемых концентраций жирорастворимых витаминов, а также витамина С).
Следует отметить, что в наиболее современные полимикроэлементные препараты западного производства переходные металлы вводят не в виде простых неорганических солей, а в виде хелатов - аминоатов, т.е. комплексов с аминокислотами (медь, железо), или глюконатов (марганец, цинк). Например, известен способ получения такого микроэлементного препарата, включающий получение раствора аминокислоты, добавление в него оксидов меди и цинка и карбоната марганца, добавление в раствор гидроксида натрия, получение фильтрата, добавление в фильтрат сульфата железа, перемешивание, добавление иодида калия, и/или селенита натрия, и/или хлорида кобальта, высушивание смеси распылением с получением аминокислотного хелатного премикса (см. CN 101248839, опуб. 27.08.2008).
Однако данный прием лишь отчасти смягчает остроту проблемы, поскольку степень усвоения металлов в этом случае повышается с 3-7% только до 15-20%, конкурентное взаимное ингибирование абсорбции ионов в ЖКТ не устраняется, а скорость окисления йодид-иона ионом меди, хотя и уменьшается многократно, остается все же заметной.
Известен способ получения микроэлементных препаратов путем взаимодействия щелочного водного раствора динатриевой или дикалиевой соли этилендиамин-N,N'-диянтарной кислоты с рассчитанным количеством растворов солей переходных металлов - железа (III), меди (II), марганца (II), кобальта (II) и цинка (II) (см. патенты РФ №2097045, 27.11.97, №2277800, 20.06.2006). При синтезе препарата используют натриевую или калиевую щелочь. В качестве солей микроэлементов используют, как правило, их хлоридные или сернокислые соли. В полученных препаратах металлы присутствуют также в виде ионных соединений (частично диссоциированных комплексов), и им присущи - хотя и в заметно меньшей степени - указанные выше недостатки. Кроме того, молекулы комплексона, освобождающегося в ходе биологического усвоения комплексоната металла, не подвергаются сколько-нибудь заметной ферментативной трансформации в организмах млекопитающих (обнаруживаются в моче в интактном виде) и способны образовать в плазме крови исключительно прочные комплексы с иными поливалентными ионами, изменяя их равновесные концентрации: известно, например, что в развитых странах использование комплексоната железа и ЭДТА (этилендиаминтетрауксусной кислоты) в качестве источника железа для людей не разрешено именно в связи с потенциальной опасностью вмешательства освобождающегося комплексона в естественный биологический обмен ионов цинка и других микроэлементов.
В случае использования микроэлементных препаратов, полученных известными ранее способами, биологически необходимые переходные металлы вводятся в рацион в виде минеральных ионизируемых соединений. Применение неионогенной формы соединений переходных металлов позволило бы устранить или сгладить перечисленные проблемы.
Наиболее близким к предложенному является способ получения железосодержащего лекарственного средства на основе неионогенного соединения, включающий смешивание растворимой соли железа (III) с низкомолекулярным декстраном или декстрином, нейтрализацию полученной смеси до начала образования осадка гидроокиси железа (III), подщелачивание до рН 10,5-11,5 при перемешивании и нагреве, повторную нейтрализацию раствора, его фильтрование и выделение железосодержащего комплекса путем ультрафильтрации на мембранах с пределом эксклюзии 10 кДа или более (RU 2198665 С1, опуб. 20.02.2003).
Задачей изобретения является создание способа получения высокоэффективного полимикроэлементного препарата с более высокой степенью усвоения железа.
Техническим результатом изобретения является обеспечение получения железосодержащего препарата, содержащего дополнительно микроэлементы, обеспечивающего лучшие результаты лечения железодефицитных состояний, а также в большей степени способствующего устойчивости иммунной системы.
Технический результат достигается предлагаемым способом.
Предлагаемый способ получения микроэлементного лекарственного средства заключается в том, что смесь водорастворимой соли железа (III) и одной или более водорастворимых солей, содержащих другие микроэлементы, с низкомолекулярным декстрином, нейтрализуют в водном растворе при перемешивании до начала образования осадка гидроксида железа (III), подщелачивают ее до рН 9-11, нагревают смесь до полного растворения осадка, нейтрализуют раствор кислотой, очищают и концентрируют полученный коллоидный раствор железо-декстринового комплекса с депонированными в полимерной ковалентной решетке оксида железа (III) атомами микроэлементов.
При этом обессоливание и концентрирование полученного комплекса осуществляют ультрафильтрацией его коллоидного раствора на мембранах с пределом эксклюзии не менее 10 кДа.
В качестве одной или более водорастворимых солей, содержащих другие микроэлементы, используют соль или соли из ряда: селенит (IV) и соли переходных металлов кобальта (II), меди (II), цинка (II), марганца (II).
При этом в результате получают неионогенную форму препарата в виде коллоидной полимерной окиси (сильно дегидратированной гидроокиси) железа с депонированными в ее решетке микроэлементами.
Сущность изобретения состоит в получении устойчивых железо-декстриновых комплексов, в которых часть ионов железа, образующих кристаллическую решетку полимерной (сильно дегидратированной) гидроокиси Fe(III), замещена ионами гетероэлементов (кобальт, медь, цинк, марганец, селен и др.), а стабильность водных коллоидных растворов полученных комплексов обусловлена химической иммобилизацией низкомолекулярных декстринов на поверхностях субмикрочастиц модифицированной гетероэлементами полимерной гидроокиси железа (III). Получаемые растворы характеризуются низкой вязкостью, высокой стабильностью при хранении, их применение обеспечивает значительное повышение степеней биологического усвоения указанных микроэлементов.
В связи с отсутствием в РФ к началу XXI века собственных парентеральных противоанемических препаратов для животных (при строгой обязательности их применении молочным поросятам) авторами была разработана сравнительно простая и дешевая технология синтеза и глубокой очистки коллоидных железо-декстрановых частиц с использованием современных мембранных технологий и запатентован способ, принятый в качестве ближайшего аналога (RU 2198665).
В ходе разработки условий синтеза неорганических оксидно-гидроксидных «ядер» для железо-декстрановых наночастиц была обнаружена принципиальная возможность замены весьма значительной доли атомов железа в полимерной оксидной решетке атомами иных поливалентных элементов - меди, кобальта, цинка, селена и т.д.: при соблюдении соответствующих технологических процедур такая замена не приводит к заметному уменьшению стабильности и ухудшению реологических свойств препарата. Данный факт послужил основой для разработки опытной серии препаратов с повышенным содержанием селена, меди и кобальта. Особо отметим, что и атомы перечисленных гетероэлементов присутствуют в растворе в неионном состоянии, будучи включенными в качестве структурных элементов в ковалентную решетку кристаллической окиси (сильно обезвоженной гидроокиси) трехвалентного железа: они не демонстрируют химических реакций, типичных для ионов данных элементов, и не могут быть отделены от наночастиц методами диализа и ультрафильтрации.
Экспериментально показано, что введение даже незначительных концентраций микроэлементов (Сu, Со, Se) в железо-оксидную матрицу коллоидных частиц железо-декстрина резко повышает терапевтический противоанемический эффект препарата. Таким образом, депонирование атомов микроэлементов в ковалентной решетке окиси железа представляется приемом оригинальным и весьма перспективным.
В предлагаемом способе для синтеза модифицированных микроэлементами наночастиц гидроокиси железа (с молекулярными массами от 100 КДа до 350 КДа, в зависимости от условий проведения процесса) используются наиболее простые неорганические соли металлов, эффективность биологического усвоения минеральных компонентов наночастиц исключительно высока, и в результате биоконверсии частиц в кровь попадают только простейшие неорганические ионы (в принципе не являющиеся ксенобиотиками); в то же время высокая нагрузка наночастицы гетероэлементами позволяет без особого труда и риска однократно ввести животному или человеку 3-4-недельную норму потребления данного микроэлемента.
Способ получения микроэлементного лекарственного средства приведен ниже.
Концентрированный раствор декстрина, содержащий хлориды Fe (III), Со (II), Cu (II), Zn (II), Mn (II) и селенит натрия (состав и пропорции для каждой группы животных или человека установлены согласно отработанным рекомендациям), нейтрализуют при перемешивании концентрированным раствором соды до начала образования осадка, подщелачивают смесь раствором едкого натра до рН 9-11, нагревают ее до температуры растворения осадка, полученный красно-бурый раствор подкисляют концентрированной НСl до рН 5,8-6,5. Концентрирование и обессоливание коллоидного раствора проводят ультрафильтрацией на мембранах с пределом эксклюзии более 10 кДа.
Ниже приведены примеры выполнения синтезов по данному способу.
ПРИМЕР 1.
СИНТЕЗ ЖЕЛЕЗО-ДЕКСТРИНОВОГО КОЛЛОИДА, ОБОГАЩЕННОГО МАРГАНЦЕМ
К 220 мл раствора, содержащего 40 г гексагидрата хлорного железа, 1,5 г тетрагидрата хлористого марганца прибавили при перемешивании 100 мл 25%-ного водного раствора декстрина, затем медленно прибавляли при комнатной температуре и перемешивании 120 мл 18%-ного водного раствора безводного карбоната натрия до получения густой смеси. Затем полученный раствор подщелачивали 40%-ным раствором едкого натра до рН 11,2 и нагревали 1 час при 95-97°С (происходит полное растворение осадка и образование гомогенного красно-бурого раствора). Раствор охлаждали, подкисляли 20%-ной соляной кислотой до рН 6,5, фильтровали сквозь бумагу и подвергали ультрафильтрации на волоконных мембранах с пределом эксклюзии 100 КДа: раствор обессоливали до остаточной концентрации NaCl, равной 8 мг/мл, и концентрировали до содержания железа около 72-80 мг/мл.
Полученный коллоидный препарат в количестве 110 мл стабилен при хранении, характеризуется невысокой относительной вязкостью (вязкость относительно воды - 2,5) и не окисляет йодид-ион в концентрированном растворе KI в течение 2 часов.
После минерализации аликвоты препарата кипячением с 2N HCl методом атомно-абсорбционной спектрофотометрии определены концентрации железа и марганца, равные соответственно 75 мг/мл и 3,9 мг/мл, отношение [Fe]/[Mn]=19,2.
ПРИМЕР 2.
СИНТЕЗ ЖЕЛЕЗО-ДЕКСТРИНОВОГО КОЛЛОИДА, ОБОГАЩЕННОГО ЦИНКОМ
К 220 мл водного раствора, содержащего 40 г гексагидрата хлорного железа, 4,2 г безводного хлористого цинка, прибавили при перемешивании 100 мл раствора, содержащего 30 г декстрина. Затем прибавляли при перемешивании 130 мл 18%-ного раствора безводного карбоната натрия до получения густой бурой смеси. Подщелочили смесь 40%-ным раствором едкого натра до рН 9,8, нагревали при перемешивании при 95-98°С в течение 1 часа. Гомогенный раствор фильтровали, подкисляли 6 N соляной кислотой до рН 6,7 и очищали ультрафильтрацией на волоконном мембранном фильтре с пределом эксклюзии 100 Кда. Раствор обессоливали до остаточной концентрации NaCl, равной 10 мг/мл, и концентрировали до содержания железа, близкого к 50 мг/мл. После минерализации аликвоты образца кипящей соляной кислотой методом атомно-абсорбционной спектрофотометрии определены концентрации металлов в коллоидном растворе: [Fe]=52 мг/мл, [Zn]=12,4 мг/мл, отношение [Fe]/[Zn]=4,2.
ПРИМЕР 3.
СИНТЕЗ ЖЕЛЕЗО-ДЕКСТРИНОВОГО КОЛЛОИДА, ОБОГАЩЕННОГО МЕДЬЮ, КОБАЛЬТОМ И СЕЛЕНОМ
К 220 мл водного раствора, содержащего 40 г гексагидрата хлорного железа, 1,80 г дигидрата хлорной меди, 0,51 г гексагидрата хлористого кобальта, 17,0 мг гидроселенита натрия прибавили при перемешивании 100 мл раствора, содержащего 30 г декстрина. Затем прибавляли при перемешивании 140 мл 18%-ного раствора безводного карбоната натрия до образования густой бурой смеси. Затем подщелачивали образец до рН 10,2, нагревали до 95-98°С, перемешивали при этой температуре в течение 1 часа. Раствор охлаждали, подкисляли 6N соляной кислотой до рН 6,5, фильтровали сквозь бумагу и подвергали ультрафильтрации на волоконных мембранах с пределом эксклюзии 100 кДа. Обессоливание раствора проведено до остаточной концентрации NaCl, равной 10 мг/мл, его концентрирование - до содержания железа, равного 50 мг/мл. После минерализации образца указанным выше методом проведено аналитическое определение содержания минеральных компонентов смеси: отношение концентраций [Fe]:[Cu]:[Co]:[Se]=100:7,9:1,7:0,1.
Было проведено исследование сравнительной эффективности железосодержащих препаратов, полученных способом по патенту РФ 2198665 и предложенным способом.
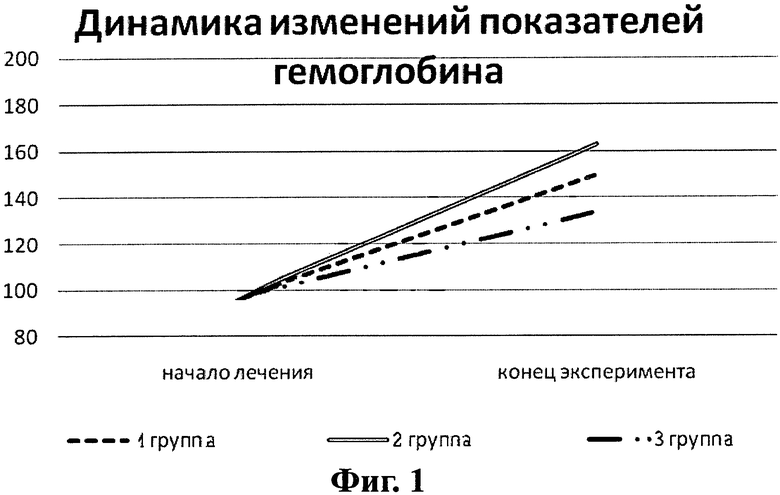
На фиг.1 показана динамика изменений показателей гемоглобина у подопытных животных.
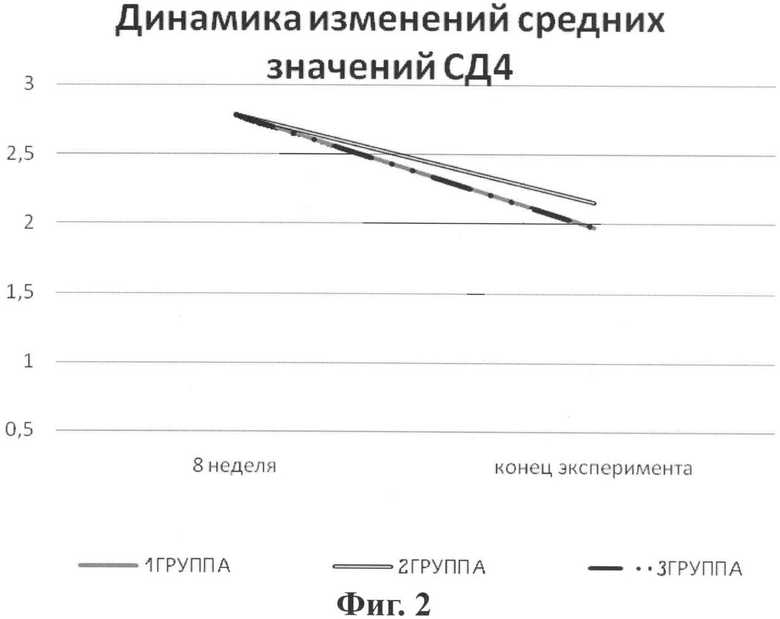
На фиг.2 - динамика изменений средних показателей клеточного иммунитета (СД4) в процессе лечения подопытных животных.
Для определения сравнительной эффективности железосодержащих препаратов были сформированы 3 рандомизированные группы крыс в количестве 18 животных.
Используя известные методы анемизации в условиях острого эксперимента, удалось за 6 недель достичь анемии средней тяжести у подопытных животных.
Для проведения коррекции анемии использовались инъекционные железосодержащие препараты «Био-железо кормовое с микроэлементами» (полученное предложенным способом) (содержит микроэлементы: Fe(III) - 50 мг/мл, Со - 0,2 мг/мл, Cu - 0,1 мг/мл, Se - 0,07 мг/мл) и «Био-железо кормовое» (полученное способом по патенту 2198665) (содержит Fe(III) - 50 мг/мл), синтезированные ООО "А-БИО" (Россия). Синтез коллоидов проведен из следующего сырья: кристаллогидрата хлорного железа реактивной чистоты (Красноперекопский завод, Украина) и полисахаридов - декстрина «Куросан» (ФРГ).
При проведении эксперимента распределили подопытных животных на 3 группы следующим образом.
ПЕРВАЯ группа крыс получала железополимерный препарат «Био-железо кормовое» в дозе 0,25 мл/100 г 1 раз в неделю, 2 недели.
ВТОРАЯ группа крыс получала железополимерный препарат «Био-железо кормовое с микроэлементами» в дозе 0,25 мл/100 г 1 раз в неделю, на протяжении 2 недель.
ТРЕТЬЯ группа крыс была контрольной, животные этой группы лечения не получали.
При анализе динамики показателей красной крови у подопытных крыс в процессе лечения позитивная тенденция наблюдалась в большинстве групп по сравнению с контрольной. Ярче всего динамику изменений красной крови в процессе лечения подопытных животных можно отобразить в виде диаграммы изменений показателей гемоглобина, которая значительно отличалась в группах на фоне лечения (см. фиг.1).
Препарат «Био-железо кормовое с микроэлементами» (2 группа) проявляет стимулирующее действие на показатели гемоглобина, как и препарат «Био-железо кормовое» (без микроэлементов - 1 группа), однако эффективность второго в конце лечения оказалась достоверно более высокой в сравнении с конечными результатами в группе 1.
Данный факт может быть объяснен наличием в полимерном комплексе «Био-железо кормовое с микроэлементами» кроме железа еще ряда микроэлементов, которые могли проявить синергическое стимулирующее действие на гемопоэз.
Анализ динамики изменений показателей клеточного иммунитета в процессе лечения приведен на диаграмме (см. фиг.2). Как видно, во всех группах подопытных животных на протяжении лечения наблюдалось статистически достоверное снижение показателей СД4 в сравнении с подъемом Т-хелперов, отмеченным на 4-6 неделе анемизации.
Лишь с помощью препарата «Био-железо кормовое с микроэлементами» нам удалось до определенной степени притормозить прогрессирующее снижение СД4, причем препарат оказывал стабилизирующее влияние на количество Т-хелперов.
Выводы:
1. Применение в пероральной форме полимальтозных (декстриновых) соединений полимерной гидроокиси железа с микроэлементами Со, Cu, Se, включенными в решетку железо-декстринового полимера, обеспечивает достоверно лучшие результаты лечения железодефицитных состояний в сравнении с тем же соединением полимерной гидроокиси железа без микроэлементов.
2. Также преимущество полимера с микроэлементами наблюдалось при снижении клеточного иммунитета в процессе лечения. Полимер с микроэлементами в большей степени способствует устойчивости иммунной системы, оказывая стабилизирующее влияние на количество Т-хелперов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Биологически активная добавка к пище, содержащая неионные формы йода и селена | 2021 |
|
RU2765999C1 |
| МИКРОЭЛЕМЕНТНЫЙ ПРЕПАРАТ ПРОЛОНГИРОВАННОГО ДЕЙСТВИЯ ДЛЯ ЖИВОТНЫХ | 2021 |
|
RU2771240C1 |
| ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЖЕЛЕЗОДЕФИЦИТНЫХ СОСТОЯНИЙ У ЖИВОТНЫХ | 2010 |
|
RU2455999C2 |
| ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЖЕЛЕЗОДЕФИЦИТНЫХ СОСТОЯНИЙ У ЖИВОТНЫХ | 2003 |
|
RU2257213C2 |
| ПРОТИВОАНЕМИЧЕСКИЙ И РОСТОСТИМУЛИРУЮЩИЙ ПРЕПАРАТ ДЛЯ ЖИВОТНЫХ | 2003 |
|
RU2263504C2 |
| ПРОТИВОАНЕМИЧЕСКИЙ И РОСТОСТИМУЛИРУЮЩИЙ ПРЕПАРАТ ДЛЯ ЖИВОТНЫХ | 2003 |
|
RU2234317C1 |
| ПРОТИВОАНЕМИЧЕСКИЙ И РОСТОСТИМУЛИРУЮЩИЙ ПРЕПАРАТ | 2004 |
|
RU2252020C1 |
| МИКРОЭЛЕМЕНТНЫЙ ПРЕПАРАТ ДЛЯ ЖИВОТНЫХ | 2016 |
|
RU2640908C2 |
| Способ получения высокоусвояемого элементосбалансированного поликомпонентного препарата на основе коллоидных хелатных комплексов эссенциальных микроэлементов цинка, марганца, железа, меди и кобальта | 2021 |
|
RU2778509C1 |
| МИКРОЭЛЕМЕНТНЫЙ ПРЕПАРАТ ДЛЯ ЖИВОТНЫХ | 2005 |
|
RU2277800C1 |
Изобретение относится к способу получения микроэлементного лекарственного средства на основе железо-декстринового комплекса. Способ включает следующие стадии: смесь водорастворимой соли железа (III) и одной или более водорастворимых солей, содержащих другие микроэлементы, например кобальт, медь, цинк, марганец и селенит, с низкомолекулярным декстрином нейтрализуют до начала образования осадка гидроксида железа (III), подщелачивают ее до рН 9-11, нагревают смесь до полного растворения осадка и нейтрализуют раствор кислотой. Затем ультрафильтрацией на мембранах очищают полученный коллоидный раствор железо-декстринового комплекса с депонированными в полимерной ковалентной решетке оксида железа (III) атомами микроэлементов и концентрируют его. Способ позволяет получать высокоэффективный полимикроэлементный препарат с высокой степенью усвоения железа, что обеспечивает лучшие результаты лечения железодефицитных состояний и способствует устойчивости иммунной системы. 2 з.п. ф-лы, 2 ил.
1. Способ получения микроэлементного лекарственного средства, заключающийся в том, что смесь водорастворимой соли железа (III) и одной или более водорастворимых солей, содержащих другие микроэлементы, с низкомолекулярным декстрином, нейтрализуют в водном растворе при перемешивании до начала образования осадка гидроксида железа (III), подщелачивают ее до рН 9-11, нагревают смесь до полного растворения осадка, нейтрализуют раствор кислотой, очищают и концентрируют полученный коллоидный раствор железодекстринового комплекса с депонированными в полимерной ковалентной решетке оксида железа (III) атомами микроэлементов.
2. Способ по п.1, отличающийся тем, что очищение полученного комплекса осуществляют ультрафильтрацией на мембранах с пределом эксклюзии не менее 10 кДа.
3. Способ по п.1, отличающийся тем, что в качестве одной или более водорастворимых солей, содержащих другие микроэлементы, используют соль или соли из ряда: селенит (IV) и соли переходных металлов кобальта (II), меди (II), цинка (II), марганца (II).
| 2001 |
|
RU2198665C | |
| Приспособление для подачи гильз в гильзовых машинах к раскручивающему прибору | 1925 |
|
SU5336A1 |
| «Новая жизнь Суиферрофита - Суиферровит А» | |||
| Журнал «Био», №4 (91), апрель 2008, с.22-24 | |||
| ПРЕПАРАТ ДЛЯ ПРОФИЛАКТИКИ АЛИМЕНТАРНОЙ АНЕМИИ ПОРОСЯТ | 1991 |
|
SU1797196A1 |
| СПОСОБ ПОВТОРНОЙ ПОДАЧИ ЛЕНТЫ В МАШИНЕ ДЛЯ УПАКОВКИ И БАНДАЖИРОВАНИЯ И МАШИНА ДЛЯ УПАКОВКИ И БАНДАЖИРОВАНИЯ С МЕХАНИЗМОМ ПОВТОРНОЙ ПОДАЧИ | 2003 |
|
RU2257312C2 |
Авторы
Даты
2011-01-20—Публикация
2009-05-07—Подача