ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к азот-содержащим гетероциклическим производным, которые полезны в качестве медикаментов и лекарственных средств, содержащих их в качестве активного ингредиента.
В виде более подробного пояснения настоящего изобретения, последнее относится к
(1) соединению, представленному формулой (I)
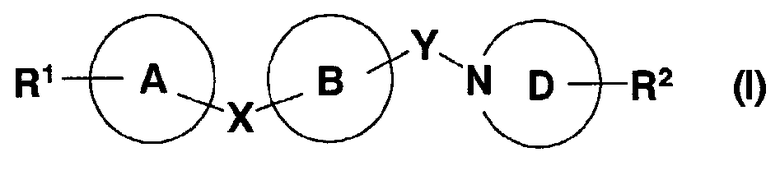
(в которой все символы имеют те же значения, что описаны здесь далее), его солям, N-оксидам или сольватам, или их пролекарствам,
(2) лечению и/или профилактике связанных с CCR5 заболеваний с помощью соединений, представленных формулой (I), его солей, N-оксидов или сольватов, или их пролекарств на их основе в качестве активного ингредиента, и к
(3) способу их получения.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Хемокин известен как эндогенный основный белок, обладающий лейкоцитхемотактическими и активирующими способностями и сильными гепарин-связывающими способностями. В настоящее время считается, что хемокин связан не только с борьбой с инфильтрацией специфических лейкоцитов во время воспалений и иммунных ответных реакций, но также с развитием и возвратом лимфоцитов при физиологических состояниях и миграцией клеток предшественника гемоцита и соматических клеток.
C дифференциацией, пролиферацией и гибелью клеток гемоцитов борются с помощью разных типов цитокина. В живом теле воспаления встречаются топически, а дифференциация, созревание и т.п. лимфоцитов осуществляются в некоторых конкретно определенных участках. А именно, различные необходимые клетки мигрируют в конкретные участки и накапливаются в них, вызывая ряд воспалений и иммунных ответных реакций. Соответственно, миграция клеток в дополнение к дифференциации, пролиферации и гибели клеток представляет также обязательное явление.
Миграция гемоцитов в живом теле начинается прежде всего на стадии развития сдвигом гематопоэза, начинающегося в AGM области, в перманентный гематопоэз в костном мозге через фетальную печень. Далее, клетки предшественники Т клеток и дендритные клетки тимуса мигрируют из фетальной печени в костный мозг, а затем в тимусную железу и цитодифференциируются в окружающей среде тимуса. Т клетка, которая получила селекцию клона, мигрирует во вторичные лимфоидные ткани и принимает участие в иммунной ответной реакции на периферии. Клетка Лангерганса кожи, активируемая и дифференцируемая захватом антигена, мигрирует в область Т клеток местного лимфатического узла и активирует там безыскусственные Т клетки в качестве дендритных клеток. Запоминающая Т клетка выполняет свой возврат снова в лимфатический узел через лимфатические и кровеносные сосуды. Клетки В, Т клетки в кишечном эпителии, γδ Т клетки, NKT клетки и дендритные клетки также мигрируют из костного мозга без прохождения через тимусную железу и дифференциируются, принимая участие в иммунной ответной реакции.
Хемокин серьезно принимает участие в миграции таких разных клеток. Рецепторы хемокина значительно связаны с борьбой с воспалением и иммунными ответными реакциями через механизм, по которому они экспрессируются в некоторые определенные периоды в разнообразных специфических клетках, а эффекторные клетки накапливаются в области, в которой продуцируется хемокин.
Например, в исследовании на моделях животных, таких как CCR5-пораженные мыши, сообщается о предположении, что CCR5 как рецептор хемокина играет значительную роль в отторжении при трансплантации органов или аутоиммунном заболевании, и др. (Transplantation, Vol.72(7), 1199-1205 (2001); Diabetes, Vol.51(8), 2489-2495 (2002); Journal of Virology, Vol.77(1), 191-198 (2003); Journal of Immunology Vol.164(12), 6303-6312 (2000)). Сообщается также о проведенном сравнении риска развития нескольких заболеваний и длительности выживания трансплантата и др. между человеком с неактивным CCR и человеком с CCR дикого типа (см. The Lancet, Vol.357, 1758-1761 (2001); Arthritis & Rheumatism, Vol.42(5), 989-992 (1999); The Lancet, Vol.354, 1264-1265 (1999); European Journal of Immunogenetics, Vol.29(6) 525-528 (2002)). Предполагается, что CCR5 связан с несколькими заболеваниями, но в публикациях нет никаких ссылок на действия лекарств, которые антагонизируют CCR в данных сообщениях.
В настоящее время предоставляется иммуносуппрессивное лечение заболеваний в области трансплантации. А именно, ингибитор кальциневрина, такой как циклоспорин или такролимус (FK506), используется главным образом с различными типами иммуносуппрессантных агентов, например TOR (мишень рапамицина) ингибитор, такой как сиролимус (рапамицин), неспецифический антифлогистический агент, такой как кортикостероиды, антипролиферативное лекарство, такое как азатиоприн, микофенолят мофетил, и др. Но он часто вызывает хроническое отторжение или тяжелые побочные эффекты, поэтому желателен полезный новый иммуносуппрессантный агент, который продлевает длительность выживания пересаженного трансплантата и снижает побочные эффекты по сравнению с существующими лекарствами.
Противовоспалительное лекарство или лекарство, которое модулирует иммунную функцию, такое как нестероидное противовоспалительное лекарство (NSAIDы), которые обладают ингибиторной активностью против циклооксигеназы (COX), модифицирующие болезнь противовоспалительные лекарства (DMARDы), стероиды, и др., используются для лечения аутоиммунного заболевания или аллергических заболеваний. Чем более эффективно лекарство, тем более сильным является побочное действие, вызываемое им, и полагают, что лечение данными лекарствами не является основным средством лечения заболевания, а является лишь симптоматическим лечением.
В то же самое время, синдром приобретенного иммунодефицита (называемый здесь далее как “СПИД”), который вызывается вирусом иммунодефицита человека (называемым здесь далее “ВИЧ”), является одним из заболеваний, поиск методов лечения от которых в последние годы наиболее актуален. Когда заражение ВИЧ завершается в CD4-положительной клетке, которая является главной клеткой мишени, ВИЧ повторяет свою пролиферацию в теле пациента и раньше или позднее полностью разрушает Т клетку, которая получает нагрузку иммунологической функции. Во время данного процесса иммунологическая функция постепенно снижается, вызывая лихорадку, диарею, увеличение лимфатических узлов и аналогичные различные состояния иммунодефицита, которые склонны вызывать осложнения с пневмонией, возбудителями которой являются пневмоциты, и аналогичными различными оппортунистическими инфекциями. Такие состояния являются началом или атакой СПИДа, и хорошо известно, что они вызывают и усугубляют саркому Капоши и аналогичные злокачественные опухоли.
В качестве последних профилактических и/или терапевтических методов от СПИДа были сделаны попытки, например, (1) ингибировать рост ВИЧ путем введения ингибитора обратной транскриптазы или ингибитора протеазы и (2) предотвратить или облегчить оппортунистические инфекции путем введения лекарства, обладающего иммунопотенциирующей активностью.
Вспомогательные Т клетки, которые получают заряд или нагрузку центральной иммунной системы, главным образом инфицируются ВИЧ. С 1985 г. известно, что ВИЧ использует мембранный белок CD4, экспрессирующий в инфекции на мембране Т клеток (Cell, 52, 631 (1985)). CD4 молекула состоит из 433 остатков аминокислот, и его экспрессия может встречаться в макрофагах, некоторых В клетках, сосудистых эндотелиальных клетках, клетках Лангерганса в кожных тканях, дендритных клетках в лимфоидных тканях, клетках глии центральной нервной системы и аналогичных, в дополнение к зрелым вспомогательным Т клеткам. Однако, поскольку было обнаружено, что заражение ВИЧ не завершается одной CD4 молекулой, было высказано предположение о возможности присутствия факторов иных, чем CD4 молекула, которые связаны с заражением клеток ВИЧ.
CCR5, который является рецептором RANTES, MIP-1α и MIP-1β, также используется во время заражения тропическим (R5) ВИЧ макрофага (Science, 272, 1955 (1996)).
Соответственно, вещества, которые могут конкурировать с CCR5 в отношении ВИЧ или которые могут связываться с ВИЧ вирусом, вызывая таким образом вирус, неспособный связываться с CCR5, могли бы стать ингибиторами ВИЧ заражения.
Сообщается также о возможности того, что CCR5 используется при заражении Респираторным Синцитиальным Вирусом (называемым здесь далее “RSV”).
Сообщается, что CCR5 экспрессируются в артериосклеротических бляшках, поэтому считается, что модуляторы рецептора хемокина полезны также при лечении сердечнососудистых заболеваний.
На основе изложенного выше, считается, что рецепторы хемокина (например, RANTES, MIP-1α, MIP-1β, и др.), особенно CCR5 серьезно связаны с воспалением, иммунологическими заболеваниями, инфекционными заболеваниями (заражением ВИЧ, заражением RSV, и др.) и сердечнососудистыми заболеваниями. Например, считается, что они связаны с различными воспалительными заболеваниями (астмой, нефритом, нефропатией, гепатитом, артритом, ревматоидным артритом, ринитом, конъюнктивитом, воспалительным заболеванием кишечника, таким как язвенный колит и др.), иммунологическими заболеваниями (аутоиммунными болезнями, отторжением при трансплантации органа (отторжением трансплантата твердого органа, отторжением трансплантата панкреатических островковых клеток при лечении диабета, болезнью трансплантат-против-хозяина и др.), иммуноподавлением, псориазом, рассеянным склерозом и др.), инфекционными заболеваниями (заражением вирусом иммунодефицита человека, синдромом приобретенного иммунодефицита, RSV заражением и др.), аллергическими заболеваниями (атопическим дерматитом, крапивницей, аллергическим бронхолегочным аспергиллезом, аллергическим эозинофильным гастроэнтеритом и др.), сердечнососудистыми заболеваниями (артериосклерозом, ишемическим реперфузионным повреждением и др.), синдромом острого респираторного дистресса, шоком, сопровождающим бактериальную инфекцию, сахарным диабетом, метастазом раковой опухоли и аналогичными.
Сообщается, что производные аминопиперидина, представленные формулой (Z)
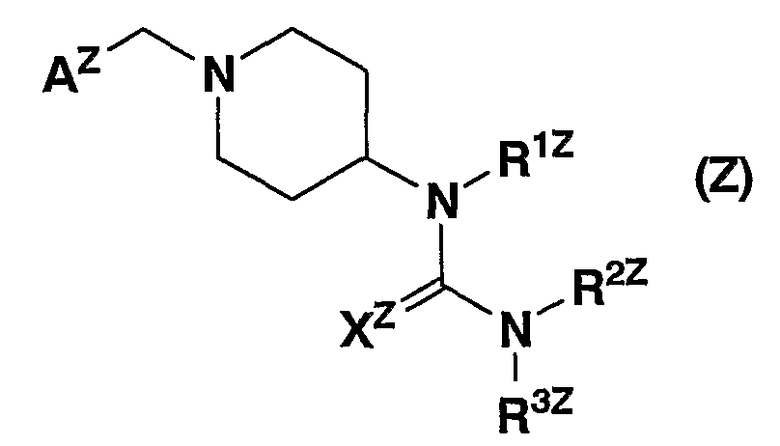
(в которой R1Z представляет атом водорода или C1-12 алкил, R2Z и R3Z представляют каждый независимо атом водорода или C1-12 алкил, XZ представляет атом азота или атом кислорода, AZ представляет
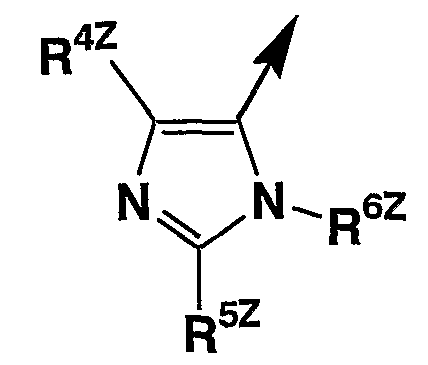 или
или 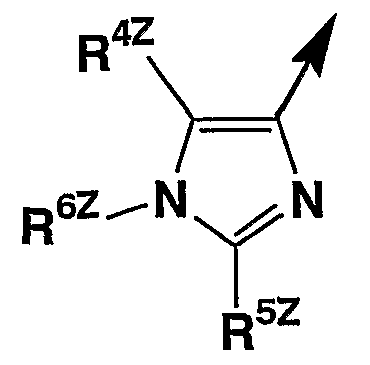
(в которой R4Z представляет атом водорода, C1-12 алкил, С3-8 циклоалкил, арил, замещенный арил, арил-C(=O)- или арил-CH(OH)-, R5Z представляет водород, C1-12 алкил, C1-4 алкокси, галоген или COR, R6Z представляет водород, С1-12 алкил или замещенный С1-4 алкил, при условии, что определение каждого символа выбрано частично), являются полезными в качестве ингибиторов рецепторов хемокина (см. описание WO02/079186).
Описывается, что сульфонокислотные соединения, представленные формулой (W)
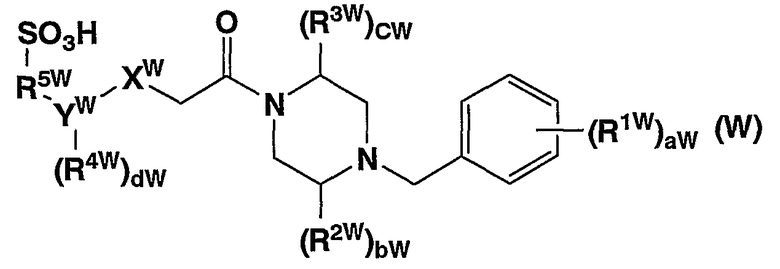
(в которой XW представляет -O-, -S-, -CH2- или -NR6-, YW представляет С6-10 арил или С2-9 гетероарил, R1W выбран из группы, состоящей из: H-, HO-, галогена-, С1-8 алкила-, необязательно замещенного 1-3 атомами фтора, и др., R2W и R3W выбраны из группы, состоящей из: Н-, оксо, С1-8 алкила-, необязательно замещенного 1-3 атомами фтора, и др., R4W выбран из группы, состоящей из: Н-, НО-, галогена-, NC-, и др., R5W представляет С1-8 алкил, aW представляет 0-5, bW представляет 0-2, cW представляет 0-2, и dW представляет 0-4, при условии, что определение каждого символа выбрано частично), их фармакологически приемлемые соли и их пролекарства являются селективными антагонистами CCR1 (см. описание WO02/102787).
Кроме того, 1-(4-пиридил)-пиперазиновые производные описываются как CCR5 антагонисты (см. описание патента США 6391865).
С другой стороны, сообщается, что производные триазаспиро[5.5]ундекана, их четвертичные аммониевые соли и их N-оксиды, или их фармакологически приемлемые соли регулируют действие рецептора хемокин/хемокин, поэтому они используются для профилактики и/или лечения различных воспалительных заболеваний, астмы, атопического дерматита, крапивницы, аллергических заболеваний (аллергического бронхолегочного аспергиллеза или аллергического эозинофильного гастроэнтерита и др.), нефрита, нефропатии, гепатита, артрита, ревматоидного артрита, псориаза, ринита, конъюнктивита, ишемического реперфузионного расстройства, рассеянного склероза, язвенного колита, синдрома острого респираторного дистресса, цитотоксического шока, диабета, аутоиммунного заболевания, реакций отторжения трансплантированного органа, иммуносупрессии, метастазы рака и синдрома приобретенного иммунодефицита (см. описание WO01/40227).
Описывается, что соединения, представленные формулой (М)
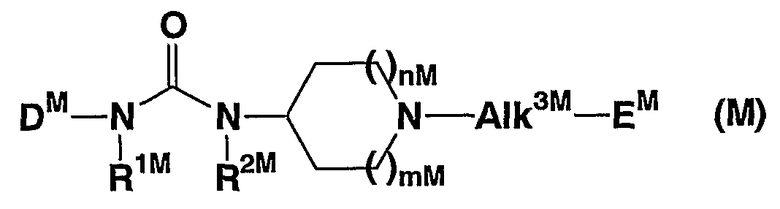
(в которой mM и nM, которые являются одинаковыми или различными, каждый представляет ноль или целое число 1 или 2, Alk3M представляет ковалентную связь или прямую или разветвленную С1-6 алкиленовую цепь, R1M и R2M, которые являются одинаковыми или различными, каждый представляет атом водорода или прямую или разветвленную С1-6 алкильную группу, DM представляет необязательно замещенную ароматическую или гетероароматическую кольцевую группу, ЕМ представляет необязательно замещенную С7-10 циклоалкильную, С7-10 циклоалкенильную или С7-10 полициклоалифатическую группу), являются модуляторами CXCR3 (см. описание WO03/070242).
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Соединение, которое обладает антагонистической активностью против CCR5, является полезным в профилактике и/или лечении CCR5-связанных заболеваний. Следовательно, желательно, чтобы были разработаны безопасные CCR5 антагонисты.
Чтобы найти соединение, которое конкретно связывает хемокиновый рецептор, особенно CCR5, и обладает антагонистической активностью против него, настоящие изобретатели провели интенсивные исследования и нашли в результате, что данные цели могут быть достигнуты соединением, представленным формулой (I), и таким образом было выполнено настоящее изобретение.
Настоящее изобретение относится к следующему:
1. соединение, представленное формулой (I)
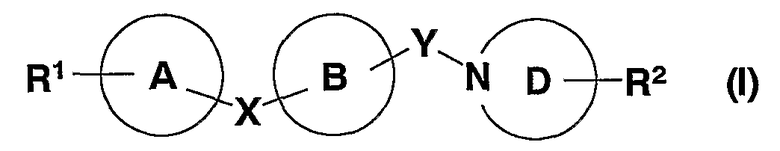
в которой R1 представляет (1) -N(R1A)SO2-R1B, (2) -SO2NR1CR1D, (3) -COOR1E, (4) -OR1F, (5) -S(O)mR1G, (6) -CONR1HR1J, (7) -NR1KCOR1L, или (8) циано, где m представляет 0, 1 или 2; R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L каждый независимо представляет атом водорода, углеводородную группу, которая может иметь заместитель(заместители), или 3-15-членную гетероциклическую группу, которая может иметь заместитель(заместители) и в которой R1C и R1D или R1H и R1J могут образовывать азот-содержащую гетероциклическую группу, которая может иметь заместитель(заместители) вместе с атомом азота, с которым они связаны;
Х и Y представляет каждый независимо связь или спейсер, содержащий 1 - 3 атома, в качестве основной цепи;
кольцо А и кольцо В, которые являются одинаковыми или различными, каждый представляет 3-15-членную карбоциклическую группу или гетероциклическую группу, которая может иметь заместитель(заместители);
кольцо D представляет 3-15-членную азот-содержащую гетероциклическую группу, которая может иметь заместитель(заместители);
R2 представляет (1) атом водорода, (2) углеводородную группу, которая может иметь заместитель(заместители), (3) циано группу, (4) гидрокси группу, которая может быть защищена, (5) амино группу, которая может иметь заместитель(заместители), (6) оксо группу, (7) 3-15-членную гетероциклическую группу, которая может иметь заместитель(заместители), или (8) =N-OR6, где R6 представляет атом водорода или С1-4 алкил,
его соль, его N-оксид или его сольват, или его пролекарство;
2. соединение согласно описанному выше п.1, в котором X и Y каждый независимо представляет связь или двухвалентную группу, включающую в себя сочетание одного или двух звеньев, выбранных из (1) -CR7R8-, (2) -NR9-, (3) -CO-, (4) -O-, (5) -S-, (6) -SO-, (7) -SO2- и (8) -C(=N-OR10)-, где R7 и R8 каждый независимо представляет атом водорода, С1-4 алкил, -OR11 или фенил; R9 представляет атом водорода, С1-4 алкил, или фенил; R10 и R11 каждый независимо представляет атом водорода или С1-4 алкил;
3. соединение согласно описанному выше п.2, в котором Х представляет связь, -О- или -СН2-;
4. соединение согласно описанному выше п.2, в котором Y представляет С1-2 алкилен;
5. соединение согласно описанному выше п.1, в котором кольцо D представляет 5-10-членную азот-содержащую гетероциклическую группу, которая может иметь заместитель(заместители);
6. соединение согласно описанному выше п.5, в котором кольцо D представляет тропановое, пирролидиновое, пиперидиновое или азепановое кольцо, которое может иметь заместитель(заместители);
7. соединение согласно описанному выше п.6, в котором кольцо D представляет пиперидиновое кольцо, которое может иметь заместитель(заместители);
8. соединение согласно описанному выше п.1, в котором кольцо А и кольцо В, которые являются одинаковыми или различными, каждое представляет 5- или 6-членную ароматическую кольцевую группу, которая может иметь заместитель(заместители);
9. соединение согласно описанному выше п.1, в котором R2 представляет группу формулы
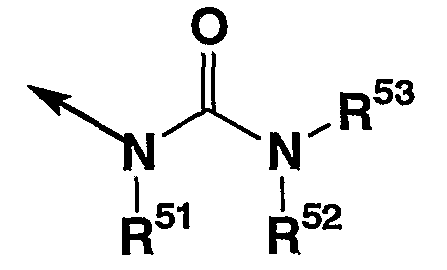
в которой стрелка указывает положение связи с кольцом D, R51, R52 и R53 каждый независимо представляет (1) атом водорода, (2) углеводородную группу, которая может иметь заместитель(заместители), (3) 3-15-членную гетероциклическую группу, которая может иметь заместитель(заместители), (4) С1-4 алкокси группу, которая может иметь заместитель(заместители), (5) фенокси группу, которая может иметь заместитель(заместители), или (6) бензилокси группу, которая может иметь заместитель(заместители);
10. соединение согласно описанному выше п.1, в котором R2 представляет группу формулы
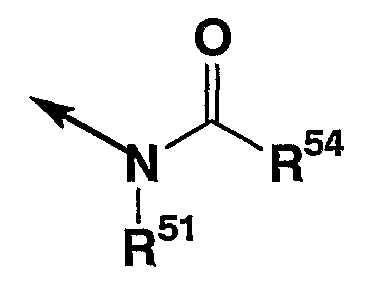
в которой стрелка указывает положение связи с кольцом D, R51 и R54 каждый независимо представляет (1) атом водорода, (2) углеводородную группу, которая может иметь заместитель(заместители), (3) 3-15-членную гетероциклическую группу, которая может иметь заместитель(заместители), (4) С1-4 алкокси группу, которая может иметь заместитель(заместители), (5) фенокси группу, которая может иметь заместитель(заместители), или (6) бензилокси группу, которая может иметь заместитель(заместители);
11. соединение согласно описанному выше п.1, которое представлено формулой (Ib)
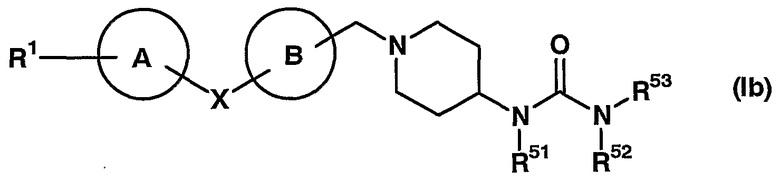
в которой все символы имеют те же значения, как описаны в пп.1 и 9;
12. соединение согласно описанному выше п.9, в котором углеводородная группа, которая может иметь заместитель(заместители), или 3-15-членная гетероциклическая группа, которая может иметь заместитель(заместители), представленная символом R51, представляет ароматическую кольцевую группу, которая может иметь заместитель(заместители);
13. соединение согласно описанному выше п.12, в котором ароматическая кольцевая группа, которая может иметь заместитель(заместители), представляет бензольное, пиррольное, имидазольное, триазольное, тетразольное, пиразольное, пиридиновое, пиразиновое, пиримидиновое, пиридазиновое, оксазольное, изоксазольное, тиазольное, изотиазольное, фуразановое, оксадиазольное или тиадиазольное кольцо;
14. соединение согласно описанному выше п.12, которое представлено формулой (Ie), (If), (Ig) или (Ih)
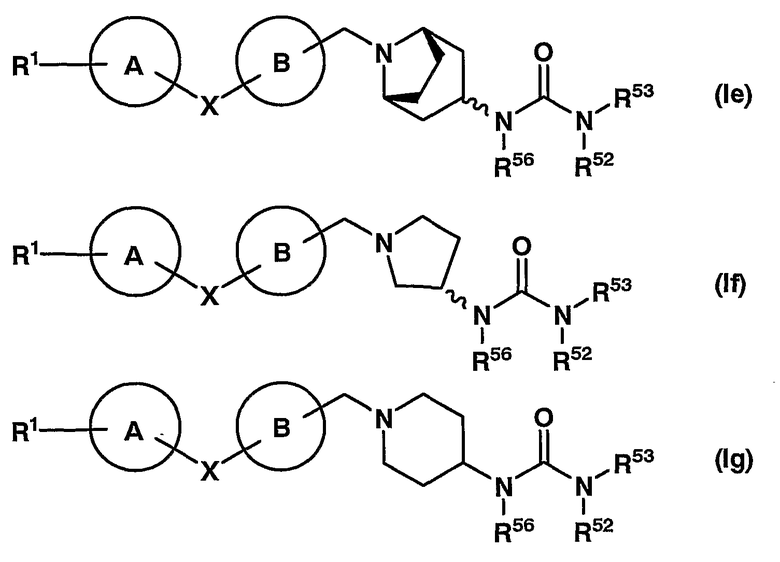
или
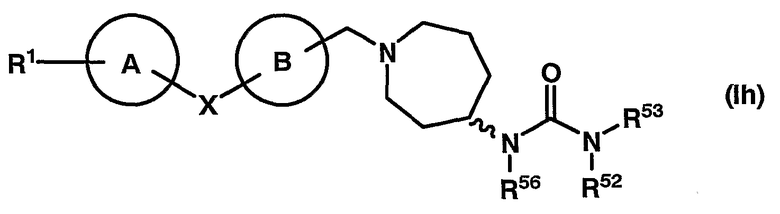
где символ _ представляет β-конфигурацию и символ _ представляет α-конфигурацию, β-конфигурацию или их смесь; R56 представляет ароматическую кольцевую группу, которая может иметь заместитель(и); другие символы имеют те же значения как описано в пп.1 и 9 выше;
15. соединение согласно описанному выше п.1, где углеводородной группой, которая может иметь заместитель(и), представленной R51 является С1-15 алкил;
16. соединение согласно описанному выше п.15, которое выбрано из группы состоящей из:
(1) 5-({[бутил(1-{4-[4-(метилсульфонил)фенокси]бензил}-4-пиперидинил)амино]карбонил}амино)-2,4-дифторбензамида,
(2) 5-[({бутил[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида,
(3) 5-({[бутил(1-{[6-(4-{[(2-метоксиэтил)амино]карбонил}фенокси)-3-пиридинил]метил}-4-пиперидинил)амино]карбонил}амино)-2,4-дифторбензамида,
(4) 5-{[(бутил{1-[(6-{4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида,
(5) 5-{[(бутил{1-[(6-{2-метил-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2-хлор-4-фторбензамида,
(6) 2-(5-{[(бутил{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторфенил)ацетамида,
(7) 5-[({бутил[1-(4-{4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифтор-N-метилбензамида,
(8) 5-{[(бутил{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида, и
(9) 5-[({бутил[1-(4-{4-[(метиламино)сульфонил]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида;
17. соединение согласно описанному выше п.12, где ароматической кольцевой группой представленной R51 является моно- карбоциклическая группа или моно- гетероциклическая группа которые обладают ароматичностью;
18. соединение согласно описанному выше п.17, которое выбрано из группы, состоящей из:
(1) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-3-метоксифенил)метансульфонамида,
(2) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида,
(3) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(3-тиенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида,
(4) N-[4-({5-[(4-{3-тиенил[(3-тиениламино)карбонил]амино}-1-пиперидинил)метил]-2-пиридинил}окси)фенил]метансульфонамида,
(5) 2-фтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамида,
(6) N-{4-[4-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-3,5-диметил-1H-пиразол-1-ил]фенил}метансульфонамида,
(7) 4-[4-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-3,5-диметил-1H-пиразол-1-ил]-N-[2-(4-морфолинил)этил]бензолсульфонамида,
(8) N-(4-{[5-({4-[{[(2,4-дифторфенил)амино]карбонил}(3-тиенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида,
(9) 2-хлор-N-метил-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамида,
(10) N-(4-{[5-({4-[({[4-хлор-3-(4-морфолинилкарбонил)фенил]амино}карбонил)(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида,
(11) 2-фтор-5-{[((3-фторфенил){1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}бензамида,
(12) N-(3-фторфенил)-N'-(6-метил-3-пиридинил)-N-[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]мочевины,
(13) 2-[4-({4-[[({4-фтор-3-[(метилсульфонил)амино]фенил}амино)карбонил](фенил)амино]-1-пиперидинил}метил)фенокси]-5-[(метилсульфонил)амино]бензамида,
(14) 2-фтор-N-метил-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамида,
(15) 2-фтор-N-метил-5-({[[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил](фенил)амино]карбонил}амино)бензамида,
(16) 2-[4-({4-[({[3-(ацетиламино)-4-фторфенил]амино}карбонил)(фенил)амино]-1-пиперидинил}метил)фенокси]-5-[(метилсульфонил)амино]бензамида,
(17) N-(4-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида,
(18) N-[2-фтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)фенил]ацетамида,
(19) N-{4-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]фенил}метансульфонамида, и
(20) N'-(4-фторфенил)-N-[1-({6-[4-(метилсульфонил)фенокси]пиридин-3-ил}метил)пиперидин-4-ил]-N-фенилмочевины;
19. соединение, согласно описанному выше п.11, которое выбрано из группы, состоящей из:
(1) 2-фтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамида,
(2) N-(4-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида,
(3) N-[2-фтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)фенил]ацетамида, и
(4) N-{4-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]фенил}метансульфонамида,
20. соединение, согласно описанному выше п.11, которое выбрано из группы, состоящей из:
(1) 5-[({бутил[1-(4-{2-метил-4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида,
(2) N-(4-{[5-({4-[{[(2,4-дифторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-3-метоксифенил)метансульфонамида,
(3) N-(4-{[5-({4-[{[(4-метилфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида,
(4) N-(4-{[5-({4-[{[(4-хлорфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида, и
(5) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)ацетамида;
21. соединение согласно описанному выше п.1, которое выбрано из группы, состоящей из:
(1) 2-фтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамида,
(2) дигидрохлорида N-(4-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида,
(3) гидрохлорида N-[2-фтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)фенил]ацетамида,
(4) дигидрохлорида N-{4-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]}метил}-2-пиридинил)окси]фенил}метансульфонамида,
(5) гидрохлорида 5-[({бутил[1-(4-{2-метил-4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида,
(6) гидрохлорида N-(4-{[5-({4-[{[(2,4-дифторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-3-метоксифенил)метансульфонамида,
(7) N-(4-{[5-({4-[{[(4-метилфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида,
(8) N-(4-{[5-({4-[{[(4-хлорфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида, и
(9) гидрохлорида N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)ацетамида;
22. фармацевтическая композиция, которая включает соединение согласно описанному выше п.1, его соль, его N-оксид, его сольват или его пролекарство;
23. фармацевтическая композиция согласно описанному выше п.22, которая является антагонистом рецептора хемокина;
24. фармацевтическая композиция согласно описанному выше п.23, которая является антагонистом CCR5;
25. фармацевтическая композиция согласно описанному выше п.24, которая является агентом для лечения и/или профилактики(предотвращения) заболеваний, имеющих отношение к CCR5;
26. фармацевтическая композиция согласно описанному выше п.25, где заболеванием, имеющим отношение к CCR5, являются инфекционные заболевания, иммунологические заболевания, воспалительные заболевания и/или кардиоваскулярные заболевания;
27. фармацевтическая композиция согласно описанному выше п.26, где заболеванием, имеющим отношение к CCR5, является инфицирование вирусом иммунодефицита человека, синдром приобретенного иммунодефицита, инфицирование Респираторным Синцитиальным Вирусом, отторжение органов при трансплантации, рассеянный склероз, воспалительное заболевание кишечника, и/или астма;
28. фармацевтическая композиция согласно описанному выше п.26, где иммунологическим заболеванием является отторжение при трансплантации органов;
29. фармацевтическая композиция согласно описанному выше п.22, которая является агентом для профилактики и/или лечения инфекционных заболеваний, иммунологических заболеваний, воспалительных заболеваний и/или кардиоваскулярных заболеваний;
30. медикамент (лекарство), включающий сочетание соединения, представленного формулой (I) согласно описанному выше п.1, его соли, его N-оксида, его сольвата или его пролекарства, и одного или более агента(ов), выбранных из ингибитора обратной транскриптазы, ингибитора протеазы, ингибитора интегразы, антагониста CCR2, антагониста CCR3, антагониста CCR4, антагониста CCR5, антагониста CXCR3, антагониста CXCR4, ингибитора слияния, антитела против поверхностного антигена ВИЧ, и вакцины ВИЧ;
31. медикамент (лекарство), включающий сочетание соединения, представленного формулой (I) согласно описанному выше п.1, его соли, его N-оксида, его сольвата или его пролекарства, и одного или более агента(ов), выбранных из иммуносупрессивного(иммуноподавляющего) агента, нестероидного противовоспалительного лекарства, модифицирующего заболевание противоревматического лекарства, стероидов, противовоспалительных ферментных препаратов, хондрозащитных агентов, ингибитора Т-клеток, ингибитора TNFα, ингибитора синтазы простагландина, ингибитора IL-1, ингибитора IL-6, агониста гамма интерферона, простагландинов, ингибитора фосфодиэстеразы, и ингибитора металлопротеиназы;
32. способ профилактики или лечения заболеваний, имеющих отношение к CCR5 у млекопитающих, который включает назначение млекопитающим эффективного количества соединения, представленного формулой (I) согласно описанному выше п.1, его соли, его N-оксида, его сольвата или его пролекарства;
33. применение соединения, представленного формулой (I) согласно описанному выше п.1, его соли, его N-оксида, его сольвата или его пролекарства для производства агента для профилактики и/или лечения заболеваний, имеющих отношение к CCR5;
34. фармацевтическая композиция согласно описанному выше п.22, которая является ингибитором клеточной миграции; и
35. способ получения соединения, представленного формулой (I) согласно описанному выше п.1, его соли, его N-оксида или сольвата или его пролекарства.
Обозначение “углеводородная группа” в словосочетании “углеводородная группа, которая может иметь заместитель(лей)” представлена R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L, включает, например, (а) С1-15 алкил, такой как метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил, гексил, гептил, октил, нонил, децил, ундецил, додецил, тридецил, тетрадецил, пентадецил и т.д.; (b) С3-8 циклоалкил, такой как циклопропил, циклобутил, циклопентил, циклогексил и т.д.; (с) С2-10 алкенил, такой как винил, аллил, 2-метилаллил, 2-бутенил, 3-бутенил, 3-октенил и т.д.; (d) С2-10 алкинил, такой как этинил, 2-пропинил, 3-гексинил и т.д.; (е) С3-10 циклоалкенил, такой как циклопропенил, циклопентенил, циклогексенил и т.д.; (f) С6-14 арил, такой как фенил, нафтил и т.д.; (g) С7-16 аралкил, такой как бензил, фенилэтил и т.д.; (h) (С3-8 циклоалкил)-(С1-4 алкил), такой как циклогексилметил, циклогексилэтил, циклогексилпропил, 1-метил-1-циклогексилметил, циклопропилэтил и т.д.
Обозначение “3-15-членный гетероцикл” в словосочетании “3-15-членная гетероциклическая группа, которая может иметь заместитель(и)” представленное R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L, включает, “3-15-членный ненасыщенный гетероцикл” или “3-15-членный насыщенный гетероцикл”.
“3-15-членный ненасыщенный гетероцикл” включает, например, пиррол, имидазол, триазол, тетразол, пиразол, пиридин, пиразин, пиримидин, пиридазин, азепин, диазепин, фуран, пиран, оксепин, тиофен, тиопиран, тиепин, оксазол, изоксазол, тиазол, изотиазол, фуразан, оксадиазол, оксазин, оксадиазин, оксазепин, оксадиазепин, тиадиазол, тиазин, тиадиазин, тиазепин, тиадиазепин, индол, изоиндол, индолизин, бензофуран, изобензофуран, бензотиофен, изобензотиофен, дитианафталин, индазол, хинолин, изохинолин, хинолизин, пурин, фталазин, птеридин, нафтиридин, хиноксалин, хиназолин, циннолин, бензоксазол, бензотиазол, бензимидазол, хромен, бензоксепин, бензоксазепин, бензоксадиазепин, бензотиепин, бензотиазепин, бензотиадиазепин, бензазепин, бензодиазепин, бензофуразан, бензотиадиазол, бензотриазол, карбазол, бета-карболин, акридин, феназин, дибензофуран, ксантен, дибензотиофен, фенотиазин, феноксазин, феноксатиин, тиантрен, фенантридин, фенантролин, перимидин, пирролин, имидазолин, триазолин, тетразолин, пиразолин, дигидропиридин, тетрагидропиридин, дигидропиразин, тетрагидропиразин, дигидропиримидин, тетрагидропиримидин, дигидропиридазин, тетрагидропиридазин, дигидроазепин, тетрагидроазепин, дигидродиазепин, тетрагидродиазепин, дигидрофуран, дигидропиран, дигидрооксепин, тетрагидрооксепин, дигидротиофен, дигидротиопиран, дигидротиепин, тетрагидротиепин, дигидрооксазол, дигидроизоксазол, дигидротиазол, дигидроизотиазол, дигидрофуразан, дигидрооксадиазол, дигидрооксазин, дигидрооксадиазин, дигидрооксазепин, тетрагидрооксазепин, дигидрооксадиазепин, тетрагидрооксадиазепин, дигидротиадиазол, дигидротиазин, дигидротиадиазин, дигидротиазепин, тетрагидротиазепин, дигидротиадиазепин, тетрагидротиадиазепин, индолин, изоиндолин, дигидробензофуран, дигидроизобензофуран, дигидробензотиофен, дигидроизобензотиофен, дигидроиндазол, дигидрохинолин, тетрагидрохинолин, дигидроизохинолин, тетрагидроизохинолин, дигидрофталазин, тетрагидрофталазин, дигидронафтиридин, тетрагидронафтиридин, дигидрохиноксалин, тетрагидрохиноксалин, дигидрохиназолин, тетрагидрохиназолин, дигидроциннолин, тетрагидроциннолин, бензоксатиан, дигидробензоксазин, дигидробензотиазин, пиразиноморфолин, дигидробензоксазол, дигидробензотиазол, дигидробензимидазол, дигидробензазепин, тетрагидробензазепин, дигидробензодиазепин, тетрагидробензодиазепин, бензодиоксепан, дигидробензоксазепин, тетрагидробензоксазепин, дигидрокарбазол, тетрагидрокарбазол, дигидроакридин, тетрагидроакридин, дигидродибензофуран, дигидродибензотиофен, тетрагидродибензофуран, тетрагидродибензотиофен, диоксаиндан, бензодиоксан, хроман, бензодитиолан, бензодитиан и т.д.
“3-15-членный насыщенный гетероцикл” включает, например, азиридин, азетидин, азокан, пирролидин, имидазолидин, триазолидин, тетразолидин, пиразолидин, пиперидин, пиперазин, пергидропиримидин, пергидропиридазин, азепан (пергидроазепин), пергидродиазепин, оксиран, оксетан, тетрагидрофуран, тетрагидропиран, пергидрооксепин, тииран, тиэтан, тетрагидротиофен, тетрагидротиопиран, пергидротиепин, тетрагидрооксазол (оксазолидин), тетрагидроизоксазол (изоксазолидин), тетрагидротиазол (тиазолидин), тетрагидроизотиазол (изотиазолидин), тетрагидрофуразан, тетрагидрооксадиазол (оксадиазолидин), тетрагидрооксазин, тетрагидрооксадиазин, пергидрооксазепин, пергидрооксадиазепин, тетрагидротиадиазол (тиадиазолидин), тетрагидротиазин, тетрагидротиадиазин, пергидротиазепин, пергидротиадиазепин, морфолин, тиоморфолин, оксатиан, пергидробензофуран, пергидроизобензофуран, пергидробензотиофен, пергидроизобензотиофен, пергидроиндазол, пергидрохинолин, пергидроизохинолин, пергидрофталазин, пергидронафтиридин, пергидрохиноксалин, пергидрохиназолин, пергидроциннолин, пергидробензоксазол, пергидробензотиазол, пергидробензимидазол, пергидрокарбазол, пергидроакридин, пергидродибензофуран, пергидродибензотиофен, диоксолан, диоксан, дитиолан, дитиан,
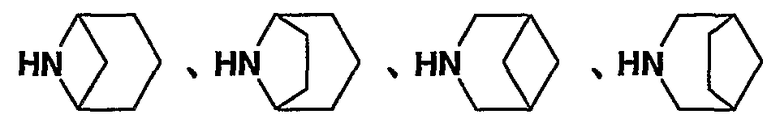 или
или 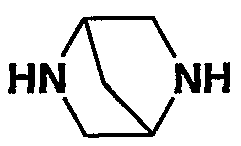 и т.д.
и т.д.
“Заместители” в словосочетании “углеводородная группа, которая может иметь заместитель(и)” или 3-15-членная гетероциклическая группа, представленные R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L, включают, например, (1) нитро, (2) гидрокси группу, (3) оксо, (4) тиоксо, (5) циано, (6) карбамоил, (7) аминокарбонил, замещенный С1-8 углеводородом, замещенным одним или двумя заместителем(лями), выбранными из (а) гидроксила, (b) амино, (c) С1-4 алкокси, (d) моно- или дизамещенного амино замещенного С1-8 углеводородной группой, и т.д., (e) карбоксила, (f) С1-6 алкокси-карбонила и т.д. (например, N-метиламинокарбонила, N-этиламинокарбонила, N-пропиламинокарбонила, N-бутиламинокарбонила, N-циклогексилметиламинокарбонила, N-N-диметиламинокарбонила, N-бутил-N-циклогексилметиламинокарбонила, N-циклогексиламинокарбонила, фениламинокарбонила, N-(2-метоксиэтил)аминокарбонила, N-(2-гидроксиэтил)аминокарбонила, N-(2-аминоэтил)аминокарбонила, N-[2-(N',N'-диметиламино)этил]аминокарбонила, N-(2-карбоксиэтил)аминокарбонила, N-(2-метоксикарбонилэтил)аминокарбонила, и т.д.) (8) карбокси, (9) С1-6 алкоксикарбонил, такой как метоксикарбонил, этоксикарбонил, пропоксикарбонил, изопропоксикарбонил, бутоксикарбонил, изобутоксикарбонил, трет-бутоксикарбонил, и т.д. (10) сульфо, (11) галоген такой, как фтор, хлор, бром или йод, (12) С1-6 алкокси, который может быть замещен галогеном (например метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси, трет-бутокси, дифторметокси или трифторэтокси), (13) фенокси, (14) галогенфенокси такой, как о-, м- или п-хлорфенокси или о-, м- или п-бромфенокси и т.д., (15) С1-6 алкилтио такой, как метилтио, этилтио, пропилтио, изопропилтио, бутилтио, трет-бутилтио, и т.д., (16) фенилтио, (17) С1-6 алкилсульфинил такой, как метилсульфинил, этилсульфинил, пропилсульфинил, бутилсульфинил и т.д. (18) С1-6 алкилсульфонил такой, как метилсульфонил или этилсульфонил, пропилсульфонил, бутилсульфонил и т.д., (19) амино, (20) С1-6 низший ациламино такой, как ацетиламино или пропиониламино и т.д., (21) моно- или дизамещенный амино замещенный углеводородной группой (“углеводородная группа” имеет те же значения, что и “углеводородная группа”, указанная выше, и может быть замещена оксо, амино который может быть замещен необязательным заместителем (например, углеводородом), карбамоилом, галогеном или гидрокси группой и т.д.) (например метиламино, этиламино, пропиламино, изопропиламино, бутиламино, диметиламино, диэтиламино, циклогексиламино, 1-карбамоил-2-циклогексилэтиламино, N-бутил-N-циклогексилметиламино или фениламино и т.д.), (22) С1-8 алканоил такой как формил или ацетил, пропионил, бутирил, изобутирил, циклогексилкарбонил, и т.д., (23) С6-10 арил-С1-4 низший ацил такой как бензоил, бензилкарбонил, (24) 3-15-членную гетероциклическую группу, которая включает 1-4 гетероатома, выбранные из кислорода, серы и азота кроме атома углерода, и необязательно имеет 1-4 заместителя, выбранные из (а) галогена, такого как бром, хлор или фтор, (b) углеводорода, необязательно замещенного оксо или гидрокси группой и т.д., (“углеводородная группа” имеет те же значения как вышеуказанная “углеводородная группа”) такого как метил, этил, пропил, изопропил, бензил, циклогексил, циклогексилметил или циклогексилэтил и т.д., (c) галогенфенокси, такого как о-, м- или п-хлорфенокси, или о-, м- или п-бромфенокси и т.д. и (d) оксо и т.д., такого как тиенил, фурил, пиразолил, тетрагидропиранил, тиазолил, изотиазолил, оксазолил, изоксазолил, имидазолил, триазолил, тетразолил, пиридил, пиромидинил, пиридазинил, хинолил, изохинолил, индолил, азиридинил, азетидинил, пирролидинил, пирролинил, пирролил, имидазолидинил, пиперидино, морфолино, дигидропиридил, N-метилпиперазинил, N-этилпиперазинил и т.д., (25) С1-10 галогеналкил, такой как дифторметил, трифторметил, трифторэтил, хлорметил, дихлорметил или трихлорэтил и т.д., (26) гидроксиимино, (27) алкилоксиимино, такой как метилоксиимино или этилоксиимино и т.д., (28) алкилсульфониламино, такой как метилсульфониламино, этилсульфониламино или бензилсульфониламино и т.д., или (29) арилсульфониламино, такой как фенилсульфониламино или п-толуолсульфониламино и т.д., (30) циклический аминокарбонил, такой как 1-азиридинилкарбонил, 1-азетидинилкарбонил, 1-пирролидинилкарбонил, 1-пиперидинилкарбонил, N-метилпиперазинилкарбонил, морфолинокарбонил и т.д., (31) С1-8 углеводородную группу, замещенную одним или двумя заместителями, выбранными из (а) гидрокси, (b) амино, (c) С1-4 алкокси, (d) моно- или дизамещенного амино замещенного С1-8 углеводородной группой, и т.д., (е) аминокарбонила замещенного С1-8 углеводородной группой и т.д., которая может иметь заместитель(и) (Эти заместители выбраны из, например, (а) гидрокси, (b) амино, (c) С1-4 алкокси, (d) моно- или дизамещенного амино замещенного С1-8 углеводородной группой и т.д., (е) карбокси, (f) С1-6 алкокси-карбонила, и могут иметь 1 или 2 группы.) такие как гидроксиметил, гидроксиэтил, аминометил, метоксиметил, N,N-диметиламинометил, карбамоилметил, N-метиламинокарбонилметил, N,N-диметиламинокарбонилметил и т.д., (32) (С1-4 алкокси)-(С1-4 алкил) группу, такую как метоксиэтил и т.д., (33) С1-8 алканоилокси группу, такую как формилокси, ацетилокси, пропионилокси, бутирилокси, изобутирилокси или циклогексилкарбонилокси и т.д., или бензоилокси группу, (34) амидино группу, (35) имино группу, (36) С1-8 алканоиламидную группу, такую как формамид, ацетамид, трифторацетамид, пропиониламид, бутириламид, изобутириламид, циклогексилкарбониламино и т.д., (37) бензамидную группу, (38) карбамоиламино группу, (39) N-С1-4 алкилкарбамоиламино группу, такую как N-метилкарбамоиламино, N-этилкарбамоиламино, N-пропилкарбамоиламино, N-изопропилкарбамоиламино, N-бутилкарбамоиламино и т.д., (40) N,N-ди-С1-4 алкилкарбамоиламино группу, такую как N,N-диметилкарбамоиламино, N,N-диэтилкарбамоиламино, N,N-дипропилкарбамоиламино, N,N-дибутилкарбамоиламино и т.д., (41) С1-3 алкилендиокси группу, такую как метилендиокси или этилендиокси и т.д., (42) -В(ОН)2, (43) эпокси группу, (44) меркапто группу, (45) сульфино группу, (46) фосфоно группу, (47) сульфамоильную группу, (48) С1-6 моноалкилсульфамоил, такой как N-метилсульфамоил, N-этилсульфамоил, N-пропилсульфамоил, N-изопропилсульфамоил или N-бутилсульфамоил и т.д., (49) ди-С1-4 алкилсульфамоильную группу, такую как N,N-диметилсульфамоил, N,N-диэтилсульфамоил, N,N-дипропилсульфамоил или N,N-дибутилсульфамоил и т.д., (50) фенилсульфинилную группу, (51) фенилсульфонильную группу, (52) азидную группу, или (53) углеводородную группу (Данная “углеводородная группа” имеет те же значения что и вышеописанная “углеводородная группа”, например, метил, этил, пропил, изопропил, винил, этинил, циклогексенил, фенил, нафтил, бензил, циклогексил, циклогексилметил, циклогексилэтил, и т.д.). “Углеводородная группа, которая может иметь заместитель(и)” или “3-15-членная гетероциклическая группа, которая может иметь заместитель(и)”, могут иметь 1-10 заместителей, выбранных из пунктов выше (1)-(53). Когда число заместителей 2 или больше, каждый из заместителей может быть одинаковым или разным.
“Азот-содержащая гетероциклическая группа” в словосочетании “азот-содержащая гетероциклическая группа, которая может иметь заместитель(и)”, образованная R1C и R1D или R1H и R1J, вместе с атомом азота, к которому они присоединены, включает, например, азиридин, азетидин, пирролин, пирролидин, имидазолин, имидазолидин, дигидропиридин, тетрагидропиридин, пиперидин, дигидропиразин, тетрагидропиразин, пиперазин, пергидропиримидин, пергидропиридазин, тетрагидроазепин, азепан (пергидроазепин), тетрагидродиазепин, пергидродиазепин, тетрагидрооксазол (оксазолидин), тетрагидротиазол (тиазолидин), тетрагидрооксазин, пергидрооксазепин, тетрагидротиазин, пергидротиазепин, морфолин, тиоморфолиновое кольцо, и т.д.
“Заместители” в словосочетании “азот-содержащая гетероциклическая группа, которая может иметь заместитель(и)”, образованная R1C и R1D или R1H и R1J, вместе с атомом азота, к которому они присоединены, включает те же значения, что и “заместитель” в словосочетании “углеводородная группа, которая может иметь заместитель(и)”, или “3-15-членная гетероциклическая группа, которая может иметь заместитель(и)”, имеет то же значение, что и “углеводородная группа, которая может иметь заместитель(и)”, представленная R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L.
“Спейсер содержащий 1-3 атома в виде главной цепи”, представленный X и Y означает промежуток, образуемый 1-3 непрерывными атомами главной цепи. В данном случае, “количество атомов в виде главной цепи” должно быть рассчитано таким образом, чтобы число атомов в виде главной цепи становилось минимальным. “Спейсер, имеющий от 1 до 3 атомов в виде главной цепи”, включает, например, бивалентную группу, включающую 1-3 группы, выбранные из -CR7R8-, -NR9-, -CO-, -O-, -SO-, -SO2- и -С(=N-OR10)- (где R7 и R8 каждый независимо представляет атом водорода, С1-4 алкил, -OR11 или фенил, R9 представляет атом водорода, С1-4 алкил или фенил, R10 R11 каждый независимо представляет атом водорода, С1-4 алкил). В случае, когда “С1-4 алкил” представлен R7 R10, он включает, например, метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил и т.д. Конкретно, “Спейсер, имеющий 1 - 3 атома в виде главной цепи”, включает, например, -CR7R8-, -NR9-, -CO-, -O-, -S-, -С(=N-OR10)-, -NR9CO-, -CONR9-, -NR9COCR7R8- или -CONR9CR7R8- (где R7 -R10 имеют те же значения, что описаны выше).
“С1-2 алкилен”, представленный, Y представляет метилен или этилен.
“3-15-членная карбоциклическая группа” в “3-15-членной карбоциклической группе или гетероциклической, которая может иметь заместитель(и)”, представленная кольцом А и кольцом В, включает, например, “3-15-членный циклический углеводород” и т.д. “Циклический углеводород” в словосочетании “3-15-членный циклический углеводород” включает, например, “ненасыщенный циклический углеводород” или “насыщенный циклический углеводород”. “Насыщенный циклический углеводород” включает, например, циклоалкан, такой как циклопропан, циклобутан, циклопентан, циклогексан, циклогептан, циклооктан, циклононан, циклодекан, циклоундекан, циклододекан, циклотридекан, циклотетрадекан или циклопентадекан и т.д.; пергидропентален; пергидроазулен; пергидроинден; пергидронафталин; пергидрогептален; спиро[4.4]нонан; спиро[4.5]декан; спиро[5.5]ундекан; бицикло[2.2.1]гептан; бицикло[3.1.1]гептан; бицикло[2.2.2]октан; адамантан; норадамантан и т.д. “Ненасыщенный циклический углеводород” включает, например циклоалкен, такой как циклопентен, циклогексен, циклогептен, циклооктен, циклопентадиен, циклогексадиен, циклогептадиен или циклооктадиен и т.д.; бензол; пентален; азулен; инден; нафталин; дигидронафталин; тетрагидронафталин; гептален; бифенилен; ас-индацен; с-индацен; аценафтен; аценафтилен; флуорен; фенален; фенантрен; антрацен; бицикло[2.2.1]гепт-2-ен; бицикло[3.1.1]гепт-2-ен; бицикло[2.2.2]окт-2-ен и т.д.
“3-15-членная гетероциклическая группа” в словосочетании “3-15-членная карбоциклическая группа или гетероциклическая группа, которая может иметь заместитель(и)”, представленная кольцом А и кольцом В, имеет те же значения, как и описанная выше “3-15-членная гетероциклическая группа” в словосочетании “3-15-членная гетероциклическая группа, которая может иметь заместитель(и)”, представленная R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L.
“Заместители” в словосочетании “3-15-членная карбоциклическая группа или гетероциклическая группа, которая может иметь заместитель(и)”, представленные кольцом А и кольцом В, имеют те же значения, что и “заместители” в словосочетании “углеводородная группа, которая может иметь заместитель(и)” или “3-15-членная гетероциклическая группа, которая может иметь заместитель(и)”, представленные R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L. 1-10 заместители могут иметь место везде, где возможно. Когда число заместителей два или более, каждый из заместителей может быть одинаковым или разным.
“5-6-членная ароматическая кольцевая группа” в словосочетании “5-6-членная ароматическая кольцевая группа, которая может иметь заместитель(и)”, представленная кольцом А и кольцом В, включает, например, бензол, пиррол, имидазол, триазол, тетразол, пиразол, пиридин, пиразин, пиримидин, пиридазин, триазин, фуран, тиофен, оксазол, изоксазол, тиазол, изотиазол, фуразан, оксадиазол или тиадиазольное кольцо и т.д.
“Заместители” в словосочетании “5-6-членная ароматическая кольцевая группа, которая может иметь заместитель(и)”, представленные кольцом А и кольцом В, имеют те же значения, что и “заместители” в словосочетании “углеводородная группа, которая может иметь заместитель(и)”, или “3-15-членная гетероциклическая группа, которая может иметь заместитель(и)”, представленные R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L. 1 - 10 заместителей могут иметь место везде, где возможно. Когда число заместителей два или более, каждый из заместителей может быть одинаковым или разным.
“Азот-содержащая гетероциклическая группа” в словосочетании “3-15-членная азот-содержащая гетероциклическая группа, которая может иметь заместитель(и)”, представленная кольцом D, относится к гетероциклу, который может содержать, в дополнение к, по крайней мере, одному атому азота, помимо атома углерода, 1-3 гетеро атома, выбранных из атомов азота, кислорода или серы. “3-15-членный азот-содержащий гетероцикл” включает “3-15-членный азот-содержащий ненасыщенный гетероцикл” и “3-15-членный азот-содержащий насыщенный гетероцикл”.
“3-15-членная азот-содержащая ненасыщенная гетероциклическая группа” включает, например, пиррол, имидазол, триазол, тетразол, пиразол, индол, изоиндол, индазол, пурин, бензимидазол, бензоазепин, бензодиазепин, бензотриазол, карбазол, β-карболин, фенотиазин, феноксазин, перимидин, пирролин, имидазолин, триазолин, тетразолин, пиразолин, дигидропиридин, тетрагидропиридин, дигидропиразин, тетрагидропиразин, дигидропиримидин, тетрагидропиримидин, дигидропиридазин, тетрагидропиридазин, дигидроазепин, тетрагидроазепин, дигидродиазепин, тетрагидродиазепин, дигидрооксазол, дигидроизоксазол, дигидротиазол, дигидроизотиазол, дигидрофуразан, дигидрооксадиазол, дигидрооксазин, дигидрооксадиазин, дигидрооксазепин, тетрагидрооксазепин, дигидрооксадиазепин, тетрагидрооксадиазепин, дигидротиадиазол, дигидротиазин, дигидротиадиазин, дигидротиазепин, дигидротиадиазепин, тетрагидротиадиазепин, индолин, изоиндолин, дигидроиндазол, дигидрохинолин, тетрагидрохинолин, дигидроизохинолин, тетрагидроизохинолин, дигидрофталазин, тетрагидрофталазин, дигидронафтиридин, тетрагидронафтиридин, дигидрохиноксалин, тетрагидрохиноксалин, дигидрохиназолин, тетрагидрохиназолин, дигидроциннолин, тетрагидроциннолин, дигидробензоксазин, дигидробензотиазин, пиразиноморфолин, дигидробензоксазол, дигидробензотиазол, дигидробензимидазол, дигидробензоазепин, тетрагидробензоазепин, дигидробензодиазепин, тетрагидробензодиазепин, дигидробензооксазепин, тетрагидробензооксазепин, дигидрокарбазол, тетрагидрокарбазол, дигидроакридин, тетрагидроакридин; или 3-15-членная азот-содержащая насыщенная гетероциклическая группа, включает, например, азиридин, азетидин, азокан, пирролидин, имидазолидин, триазолидин, тетразолидин, пиразолидин, пиперидин, пиперазин, пергидропиримидин, пергидропиридазин, азепан (пергидроазепин), пергидродиазепин, тетрагидрооксазол (оксазолидин), тетрагидроизоксазол (изоксазолидин), тетрагидротиазол (тиазолидин), тетрагидроизотиазол (изотиазолидин), тетрагидрофуразан, тетрагидрооксадиазол (оксадиазолидин), тетрагидрооксазин, тетрагидрооксадиазин, пергидрооксазепин, пергидрооксадиазепин, тетрагидротиадиазол, (тиадиазолидин), тетрагидротиазин, тетрагидротиадиазин, тетрагидротиазепин, пергидротиазепин, пергидротиадиазепин, морфолин, тиоморфолин, пергидроиндазол, пергидрохинолин, пергидроизохинолин, пергидрофталазин, пергидронафтиридин, пергидрохиноксалин, пергидрохиназолин, пергидроциннолин, пергидробензоксазол, пергидробензотиазол, пергидробензимидазол, пергидрокарбазол, пергидроакридин,  или
или  и т.д.
и т.д.
“Заместители” в словосочетании “3-15-членная азот-содержащая гетероциклическая группа, которая может иметь заместитель(и)”, представленные кольцом D, имеют те же значения, что и “заместители” в словосочетании “углеводородная группа, которая может иметь заместитель(и)”, или “3-15-членная гетероциклическая группа, которая может иметь заместитель(и)”, представленные R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L. 1-10 заместителей могут иметь место везде, где возможно. Когда число заместителей два или более, каждый из заместителей может быть одинаковым или разным.
“5-10-членная азот-содержащая гетероциклическая группа” в словосочетании “5-10-членная азот-содержащая гетероциклическая группа, которая может иметь заместитель(и)”, представленная кольцом D, относится к “5-10-членной азот-содержащей гетероциклической группе”, вышеописанной “3-15-членной азот-содержащей гетероциклической группе”, представленной кольцом D. Примеры включают пирролидин, пиперидин, пиперазин, азепан или тропан и.т.д.
“Заместители” в словосочетании “5-10-членная азот-содержащая гетероциклическая группа, которая может иметь заместитель(и)”, представленные кольцом D, имеют те же значения, что и “заместители” в словосочетании “углеводородная группа, которая может иметь заместитель(и)”, или “3-15-членная гетероциклическая группа, которая может иметь заместитель(и)”, представленная R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L. 1-10 заместителей могут иметь место везде, где возможно. Когда число заместителей два или более, каждый из заместителей может быть одинаковым или разным.
“Гидрокси группа, которая может быть защищенной”, представленная R2, является “гидрокси группой”, которая может быть защищена “защитной группой”. “Защитная группа” гидрокси группы включает, например, (1) С1-6 алкильную группу (например, метил, этил, пропил, изопропил, бутил, трет-бутил, и т.д.), которая может иметь 1-4 заместителя выбранные из (а) атома галогена такого, как хлор, бром или фтор и т.д.; (b) C6-10 арила такого, как фенил или нафтил и т.д.; (c) С7-12 аралкильной группы такой, как бензил или фенилэтил и т.д.; и (d) нитро группы и т.д., (2) С6-10 арил (например, фенил или нафтил и т.д.), который может иметь 1-4 заместителя выбранные из (а) атома галогена такого, как хлор, бром или фтор и т.д.; (b) С1-6 алкильной группы такой, как метил, этил или пропил и т.д.; (с) C6-10 арила такого, как фенил или нафтил и т.д.; (d) С7-12 аралкильной группы такой, как бензил или фенилэтил и т.д.; и (е) нитро группы и т.д., (3) С7-12 аралкильную группу (например, бензил, фенилэтил или нафтилметил и т.д.), которая может иметь 1-4 заместителя, выбранные из (а) атома галогена такого, как хлор, бром или фтор и т.д.; (b) С1-6 алкильной группы такой, как метил, этил или пропил и т.д.; (с) C6-10 арила такого, как фенил или нафтил и т.д.; (d) С7-12 аралкильной группы такой, как бензил или фенилэтил и т.д.; и (е) нитро группы и т.д., (4) формил, (5) С1-6 алкилкарбонильную группу (например, ацетил или пропионил и т.д.), которая может иметь 1-4 заместителя, выбранные из (а) атома галогена такого, как хлор, бром или фтор и т.д.; (b) С1-6 алкильной группы такой, как метил, этил или пропил и т.д.; (с) C6-10 арила такого, как фенил или нафтил и т.д.; (d) С7-12 аралкильной группы такой, как бензил или фенилэтил и т.д.; и (е) нитро группы и т.д., (6) С6-10 арилоксикарбонильную группу (например, фенилоксикарбонил или нафтилоксикарбонил и т.д.), которая может иметь 1-4 заместителя, выбранные из (а) атома галогена такого, как хлор, бром или фтор и т.д.; (b) С1-6 алкильной группы такой, как метил, этил или пропил и т.д.; (с) C6-10 арила такого, как фенил или нафтил и т.д.; (d) С7-12 аралкильной группы такой, как бензил или фенилэтил и т.д.; и (е) нитро группы и т.д., (7) С6-10 арилкарбонильную группу (например, бензоил или нафтилкарбонил и т.д.), которая может иметь 1-4 заместителя, выбранные из (а) атома галогена такого, как хлор, бром или фтор и т.д.; (b) С1-6 алкильной группы такой, как метил, этил или пропил и т.д.; (с) C6-10 арила такого, как фенил или нафтил и т.д.; (d) С7-12 аралкильной группы такой, как бензил или фенилэтил и т.д.; и (е) нитро группы и т.д., (8) С7-12 аралкилкарбонильную группу (например, бензилкарбонил или фенэтилкарбонил и т.д.), которая может иметь 1-4 заместителя, выбранные из (а) атома галогена такого, как хлор, бром или фтор и т.д.; (b) С1-6 алкильной группы такой, как метил, этил или пропил и т.д.; (с) C6-10 арила такого, как фенил или нафтил и т.д.; (d) С7-12 аралкильной группы такой, как бензил или фенилэтил и т.д.; и (е) нитро группы и т.д., (9) пиранила или фуранила, которые могут иметь 1-4 заместителя, выбранные из (а) атома галогена такого, как хлор, бром или фтор и т.д.; (b) С1-6 алкильной группы такой, как метил, этил или н-пропил и т.д.; (с) C6-10 арила такого, как фенил или нафтил и т.д.; (d) С7-12 аралкильной группы такой, как бензил или фенилэтил и т.д.; и (е) нитро группы и т.д., или (10) три-С1-4 алкилсилил такой, как триметилсилил или триэтилсилил и т.д.
Термин “заместители” в словосочетании “амино группа, которая может иметь заместитель(и)”, представленный R2, включает углеводородную группу, которая может иметь заместитель(и), -SO2R201 или =NR202 (в которых R201 и R202 представляют углеводородную группу, которая может иметь заместитель(и)). “Углеводородная группа, которая может иметь заместитель(и)”, имеет те же значения, что и “углеводородная группа, которая может иметь заместитель(и)”, представленная R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L. 1 или 2 заместителя, которых имеет амино группа, могут иметь место везде, где возможно. Когда число заместителей два или более, каждый из заместителей может быть одинаковым или разным. “Амино группой, которая может иметь заместитель(и)”, представленной R2, является
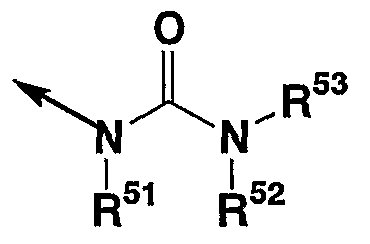 или
или 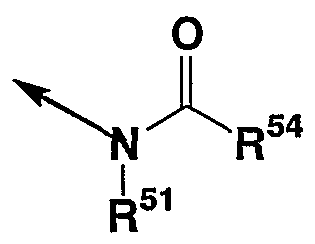
(в которых стрелка представляет место присоединения к кольцу D, и R51, R52, R53 и R54 каждый независимо представляют атом водорода, углеводородную группу, которая может иметь заместитель(и), 3-15-членную гетероциклическую группу, которая может иметь заместитель(и), С1-4 алкокси группу, которая может иметь заместитель(и), фенокси, который может иметь заместитель(и), или бензилокси, который может иметь заместитель(и)). “Углеводородная группа, которая может иметь заместитель(и)” и “3-15-членная гетероциклическая группа, которая может иметь заместитель(и)”, имеют те же значения, что и “углеводородная группа, которая может иметь заместитель(и)”, и “3-15-членная гетероциклическая группа, которая может иметь заместитель(и)”, представленные R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L соответственно. “С1-4 алкокси группа” в “С1-4 алкокси группе, которая может иметь заместитель(и)”, включает, например, метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси или трет-бутокси и т.д. “Заместители” в словосочетаниях “С1-4 алкокси группа, которая может иметь заместитель(и)”, “фенокси группа, которая может иметь заместитель(и)” и “бензилокси группа, которая может иметь заместитель(и)”, включают, например, “заместители” в словосочетании “углеводородная группа, которая может иметь заместитель(и)”, представленные R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L, и т.д.
“Углеводородная группа, которая может иметь заместитель(и)”, представленная R2, имеет те же значения, что и “углеводородная группа, которая может иметь заместитель(и)”, представленная R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L. 1 - 10 заместителей, которых имеет углеводородная группа, могут иметь место везде, где возможно. Когда число заместителей два или более, каждый из заместителей может быть одинаковым или разным. “Углеводородная группа, которая может иметь заместитель(и)”, представленная R2, представляет
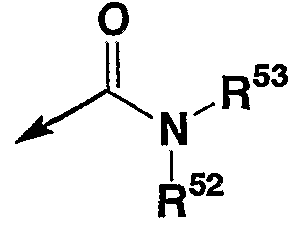
(в которой стрелка представляет место присоединения к кольцу D, и R52 и R53 имеют те же значения, что описаны выше).
“3-15-членная гетероциклическая группа, которая может иметь заместитель(и)”, представленная R2, имеет те же значения, что и “3-15-членная гетероциклическая группа, которая может иметь заместитель(и)”, представленная R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L.
С1-4 алкил, представленный R6, включает, например, метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, и т.д.
“Углеводородная группа, которая может иметь заместитель(и)”, представленная R51, имеет те же значения, что и “углеводородная группа, которая может иметь заместитель(и)”, представленная R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L.
“С1-15 алкил”, представленный R51, имеет те же значения, что и “С1-15 алкил” в качестве “углеводородной группы”, в словосочетании “углеводородная группа, которая может иметь заместитель(и)”, представленной R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L.
“Ароматическая кольцевая группа” в словосочетании “ароматическая кольцевая группа, которая может иметь заместитель(и)”, представленная R51, относится к “моно-, би- или трициклической карбоциклической группе или гетероциклической группе, которая обладает ароматичностью” “углеводородной группы” в словосочетаниях “углеводородная группа, которая может иметь заместитель(и)”, и “3-15-членная гетероциклическая группа, которая может иметь заместитель(и)”, представленная R51. “Моно- би, или трициклическая карбоциклическая группа, которая обладает ароматичностью”, включает, например бензол, азулен, нафталин, фенантрен, антраценовое кольцо, и т.д. “Моно- би, или трициклическая гетероциклическая группа, которая обладает ароматичностью” включает, например, пиррол, имидазол, триазол, тетразол, пиразол, пиридин, пиразин, пиримидин, пиридазин, фуран, тиофен, оксазол, изоксазол, тиазол, изотиазол, фуразан, оксадиазол, тиадиазол, индол, изоиндол, бензофуран, изобензофуран, бензотиофен, изобензотиофен, индазол, хинолин, изохинолин, пурин, фталазин, птеридин, нафтиридин, хиноксалин, хиназолин, циннолин, бензоксазол, бензотиазол, бензимидазол, бнзофуразан, бензотиадиазол, бензотриазол, карбазол, бета-карболин, акридин, феназин, дибензофуран, дибензотиофен, фенантридин, фенантролин, перимидиновое кольцо и т.д.
“Заместители” в словосочетании “ароматическая кольцевая группа, которая может иметь заместитель(и)”, представленные R51, имеют те же значения, что и “заместители” в словосочетании “углеводородная группа, которая может иметь заместитель(и)”, или “3-15-членная гетероциклическая группа, которая может иметь заместитель(и)”, представленные R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L. 1 - 10 заместители могут иметь место везде, где возможно. Когда число заместителей два или более, каждый из заместителей может быть одинаковым или разным.
“Моно- карбоциклическая группа или моно- гетероциклическая группа, которые обладают ароматичностью”, представленные R51, относятся к моноциклической группе вышеописанной “ароматической кольцевой группы”, представленной R51. Примеры включают бензол, пиррол, имидазол, тиазол, тетразол, пиразол, пиридин, пиразин, пиримидин, пиридазин, оксазол, изоксазол, тиазол, изотиазол, фуразан, оксадиазол или тиадиазольное кольцо и т.д.
“Ароматическая кольцевая группа, которая может иметь заместитель(и)”, представленная R56, имеет те же значения, что и вышеописанная “ароматическая кольцевая группа, которая может иметь заместитель(и)”, представленная R51.
Если особо не упоминается иное, в настоящее изобретение включены все изомеры. Например алкил, алкенил, алкинил, алкокси, алкилтио, алкилен, алкенилен и алкинилен включают прямую цепь и разветвленную. Более того, в настоящее изобретение включены все изомеры, образованные вследствие двойной связи, кольца и конденсированного кольца (E-, Z-, цис- и транс-формы), изомеры, образованные вследствие присутствия асимметричных атома(ов) углерода и т.д. (R-, S-, α- и β-конфигурация, энантиомер и диастереомер), оптически активные субстанции, имеющие вращение плоскости поляризации (D-, L-, d- и l-формы), полярное соединение хроматографического отделения (более полярное соединение или менее полярное соединение), равновесные соединения, вращательные изомеры, их смесь в любой пропорции и рацемическая смесь.
Согласно настоящему изобретению, символ _представляет β-конфигурацию, а символ _ представляет α-конфигурацию, β-конфигурацию или их смесь. Нет никаких особых ограничений касательно соотношения α-конфигурации и β-конфигурации в смеси.
Соли:
Соль соединения формулы (I) охватывает все из солей, которые являются нетоксичными или фармацевтически приемлемыми солями. Что касается фармацевтически приемлемых солей, предпочитаются соли, которые являются низко токсичными и растворимыми в воде. Примерами соответствующих солей соединения формулы (I) являются соли со щелочными металлами (такими, как калий, натрий и литий), соли со щелочно-земельными металлами (такими как кальций и магний), аммониевые соли (такие как тетраметиламмониевая соль и тетрабутиламмониевая соль), соли с органическими аминами (такими как триэтиламин, метиламин, диметиламин, циклопентиламин, бензиламин, фенэтиламин, пиперидин, моноэтаноламин, диэтаноламин, трис(гидроксиметил)метиламин, лизин, аргинин и N-метил-D-глюкамин) и аддитивные соли кислот [такие как соли с неорганическими кислотами (например, гидрохлорид, гидробромид, гидроиодид, сульфат, фосфат и нитрат) и соли с органическими кислотами (например, ацетат, трифторацетат, лактат, тартрат, оксалат, фумарат, малеат, бензоат, цитрат, метансульфонат, этансульфонат, бензолсульфонат, толуолсульфонат, изотионат, глюкуронат и глюконат), и др.]. Соль соединения настоящего изобретения включает также сольваты, а также сольваты с упомянутыми выше солями щелочных (щелочно-земельных) металлов, аммониевыми солями, солями органических аминов и кислотно-аддитивными солями. Сольват является предпочтительно низкотоксичным и водорастворимым. Примерами соответствующих сольватов являются сольваты с водой и со спиртовым растворителем (таким, как этанол). Соединения настоящего изобретения превращаются в низкотоксичные соли или фармацевтически приемлемые соли с помощью известных методов.
Кроме того, соль включает четвертичную аммониевую соль. Четвертичная аммониевая соль соединения, представленного формулой (I), представляет соединение, в котором азот соединений, представленных формулой (I), кватернизован R0 (R0 представляет С1-8 алкил или С1-8 алкил, замещенный фенилом).
Соль включает также N-оксид. Соединение настоящего изобретения может быть превращено в N-оксид с помощью известных методов. N- оксид представляет соединение, в котором азот соединения, представленного формулой (I), окислен.
Пролекарства:
Пролекарство соединения формулы (I) обозначает соединение, которое превращается в соединение формулы (I) с помощью реакции с ферментой, желудочной кислотой или аналогичными в живом организме. Например, что касается пролекарств соединения формулы (I), когда соединение формулы (I) имеет амино группу, соединения, в которых амино группа, например, ацилируется, алкилируется или фосфорилируется (например, соединения, в которых амино группа соединения формулы (I) эйкозаноилируется, аланилируется, пентиламинокарбонилируется, (5-метил-2-оксо-1,3-диоксолен-4-ил)метоксикарбонилируется, тетрагидрофуранилируется, пирролидилметилируется, пивалоилоксиметилируется, ацетоксиметилируется, трет-бутилируется, и пр.); когда соединение формулы (I) имеет гидроксильную группу, соединения, в которых гидроксильная группа, например, ацилируется, алкилируется, фосфорилируется или борируется (например, соединения, в которых гидроксильная группа соединения формулы (I) ацетилируется, пальмитоилируется, пропаноилируется, пивалоилируется, сукцинилируется, фумарилируется, аланилируется или диметиламинометилкарбонилируется); и карбоксильная группа соединения формулы (I), например, сложноэтерифицируется или амидируется (например, соединения, в которых карбоксильная группа соединения формулы (I) превращается в этиловый эфир, фениловый эфир, фенилэтиловый эфир, карбоксиметиловый эфир, диметиламинометиловый эфир, пивалоилоксиметиловый эфир, этоксикарбонилоксиэтиловый эфир, фталидиловый эфир, (5-метил-2-оксо-1,3-диоксолен-4-ил)метиловый эфир, циклогексилоксикарбонилэтиловый эфир или метиламид). Данные соединения могут быть получены с помощью метода, известного самого по себе. Пролекарство соединения формулы (I) может быть или гидратом, или не гидратом. Пролекарством соединения формулы (I) может быть также соединение, которое превращается в соединение формулы (I) в физиологических условиях, как описано в “Iyakuhin no kaihatsu, Vol.7 (Bunshi-sekkei), стр. 163-198 (Hirokawa-Shoten), 1990”. Соединение формулы (I) может быть также мечено радиоизотопом (таким, как 3H, 14C, 35S, 125I и др.).
В настоящем изобретении предпочтительными являются все определения, представленные символами R1, X, Y, кольцом А, кольцом В, кольцом D и символом R2 в формуле (I). Все символы в каждой предпочтительно группе, перечисленной ниже, имеют те же самые значения, что описаны выше.
Предпочтительным в качестве R1 является, например, -N(R1A)SO2-R1B, -SO2NR1CR1D, -S(О)mR1G, -CONR1HR1J, -NR1KCOR1L и др., и более предпочтительным является, например, -N(R1A)SO2-R1B, -SO2NR1CR1D, -S(О)mR1G, -CONR1HR1J и др. Предпочтительными в качестве R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L является, например, атом водорода или углеводородная группа, которая может иметь заместитель(и), и др. Более предпочтительным в качестве R1 является, например, -NHSO2CH3, -NHSO2CH2CH3, -SO2NHCH3, -SO2CH3, -CONHCH2CH2OCH3 и др.
Предпочтительным в качестве Х является, например, связь, -CR7R8-, -NR9-, -CO-, -O-, -S-, -SO-, -SO2- или -C(=N-OR10)- и др. Более предпочтительно Х представляет связь, -О- или -СН2- и др.
Предпочтительным в качестве Y является, например, метилен, этилен или пропилен и др. Более предпочтительно Y представляет метилен, этилен. Наиболее предпочтительно Y представляет метилен.
Предпочтительно, кольцо А или кольцо В представляет, например, “5-10-членную карбоциклическую группу или гетероциклическую группу” (это относится к 5-10-членной карбоциклической группе или гетероциклической группе описанной выше 3-15-членной карбоциклической группы или гетероциклической группы) и др. Более предпочтительно им является, например, “5-10-членная ненасыщенная карбоциклическая группа или гетероциклическая группа” (это относится к 5-10-членной ненасыщенной карбоциклической группе или гетероциклической группе описанной выше 3-15-членной карбоциклической группы или гетероциклической группы) и др. Более предпочтительным является, например 5- или 6-членное ароматическое кольцо, такое как бензольное, пиррольное, имидазольное, триазольное, тетразольное, пиразольное, пиридиновое, пиразиновое, пиримидиновое, пиридазиновое, триазиновое, фурановое, тиофеновое, оксазольное, изоксазольное, тиазольное, изотиазольное, фуразановое, оксадиазольное или тиадиазольное кольцо и др. Наиболее предпочитается, например, бензольное или пиридиновое кольцо и др. Предпочтительно, заместитель кольца А или кольца В представляет, например, углеводородную группу, алкокси, атом галогена, карбокси, алканоиламид и др., и более предпочтительной является, например, углеводородная группа, алкокси, атом галогена и др., и наиболее предпочтительным является, например, атом хлора, метил или метокси и др.
Предпочтительно кольцо D представляет, например, “5-10-членную азот-содержащую гетероциклическую группу” (это относится к 5-10-членной азот-содержащей гетероциклической группе описанной выше 3-15-членной азот-содержащей гетероциклической группы) и др., и более предпочтительно представляет тропановое, пирролидиновое, пиперидиновое, азепановое или пиперазиновое кольцо и др., и наиболее предпочитается, например, пиперидиновое кольцо. Предпочтительно, кольцо D не имеет заместителя или замещено углеводородной группой, моно-С1-4 алкиламино группой или ди-С1-4 алкиламино группой и др. Наиболее предпочтительно кольцо D не имеет заместителя.
В качестве R2 предпочтительной является, например, углеводородная группа, которая может иметь заместитель(заместители), или амино группа, которая может иметь заместитель(заместители), и др. Предпочтительной в качестве “заместителей” является “углеводородная группа, которая может иметь заместитель(заместители)”. Конкретно более предпочтительной в качестве R2 является, например, группа
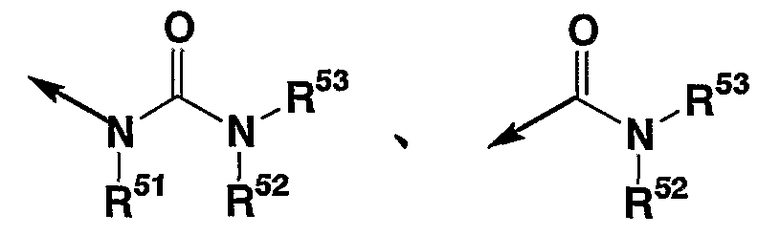 или
или 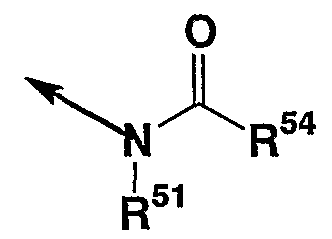
(в которой стрелка указывает положение связи с кольцом D, каждый из R51, R52, R53 и R54 независимо имеет значения, описанные выше), и др. Предпочтительно R51, R52, R53 или R54 представляет, например, атом водорода, углеводородную группу, которая может иметь заместитель(заместители), или 3-15-членную гетероциклическую группу, которая может иметь заместитель(заместители) и др. Кроме того, предпочитается соединение, в котором любой среди R52 и R53 представляет атом водорода. Более предпочтительной в качестве R2 является, например, группа
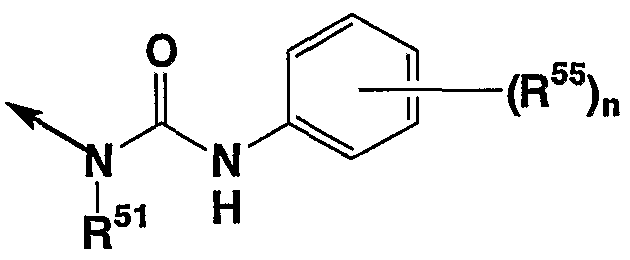 или
или 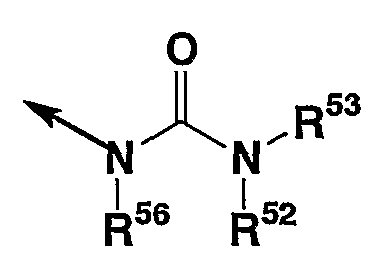
(R55 имеет те же значения, что “заместители” в “углеводородной группе, которая может иметь заместитель(заместители)”, представленной символами R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L, n представляет 0-5, а другие символы имеют те же значения, что описаны выше), и др. Предпочтительной в качестве R51 является, например, углеводородная группа, которая может иметь заместитель(заместители), и др., и более предпочтительной является, например, С1-15 алкил, который может иметь заместитель(заместители), С6-14 арил, который может иметь заместитель(заместители), или R56, и др., и наиболее предпочитается, например, бутил или фенил, который может иметь заместитель(заместители), и др. Предпочтительным в качестве заместителя является метил, метокси, трифторметил, атом фтора и др., и более предпочтительным является метил или атом фтора. Предпочтительным в качестве R55 является, например, атом галогена, карбамоил или аминокарбонил, замещенный С1-8 углеводородной группой, и др., и более предпочитается, например, атом фтора, атом хлора, карбамоил, N-метиламинокарбонил, и др. В качестве n предпочитается 1-3.
Предпочтительной в качестве R56 является моно-карбоциклическая группа или моно-гетероциклическая группа, которая обладает ароматичностью, которая может иметь заместитель(заместители), и более предпочтительным является бензольное, пиррольное, имидазольное, триазольное, тетразольное, пиразольное, пиридиновое, пиразиновое, пиримидиновое, пиридазиновое, оксазольное, изоксазольное, тиазольное, изотиазольное, фуразановое, оксадиазольное или тиадиазольное кольцо, которое может иметь заместитель(заместители), и наиболее предпочтительным является бензольное кольцо, которое может иметь заместитель(заместители). В качестве заместителя предпочитается метил, метокси, трифторметил, атом фтора, и др., и более предпочтительным является метил или атом фтора.
В настоящем изобретении предпочтительным является соединение, представленное формулой (I), включающее сочетание описанной выше предпочитаемой группы и кольца.
Например, предпочтительными также являются соединение, в котором кольцом D является пиперидин, и Y представляет метиленовую группу, т.е. соединение, представленное формулой (Ia)
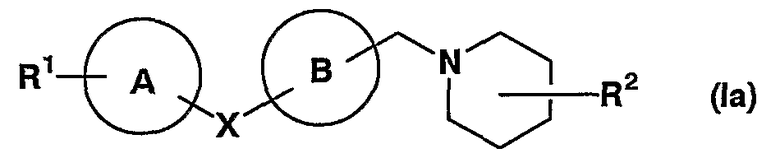
(в которой все символы имеют значения, описанные выше); соединение, в котором кольцом D является пиперидин, и Y представляет метиленовую группу, R2 представляет
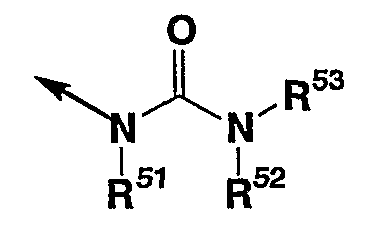
(в которой все символы имеют значения, описанные выше), т.е. соединение, представленное формулой (Ib)
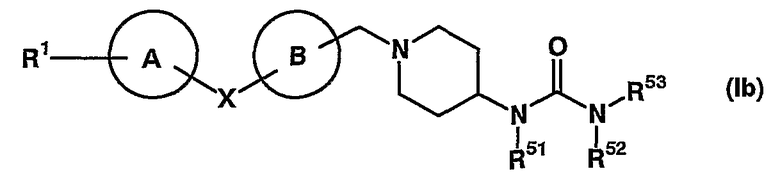
(в которой все символы имеют значения, описанные выше); соединение, в котором X представляет -O-, Y представляет метиленовую группу, кольцо А и кольцо В каждое независимо представляет бензол, который может иметь заместитель(заместители), кольцо D представляет пиперидин, R2 представляет
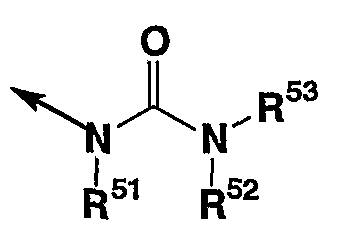
(в которой все символы имеют значения, описанные выше), т.е. соединение, представленное формулой (Ic)
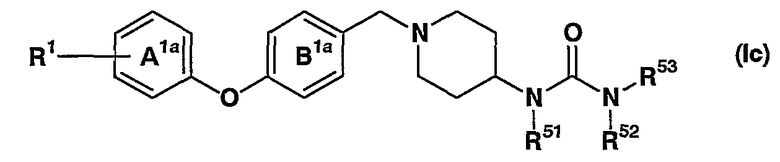
(в которой кольцо А1а и кольцо В1а каждое независимо представляет бензол, который может иметь заместитель(заместители) и другие символы имеют значения как описано выше); соединением, в котором Х представляет -О-, Y представляет метиленовую группу, кольцо А и кольцо В каждое независимо представляет бензол, который может иметь заместитель(и), кольцо D представляет пиперидин, R2 представляет
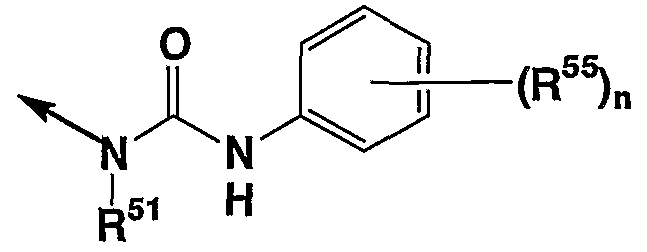
(в которой все символы имеют значения, описанные выше), т.е. соединение, представленное формулой (Id)
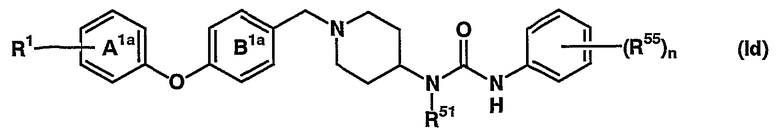
(в которой все символы имеют значения, описанные выше); соединение, в котором кольцом D является тропановое кольцо, и Y представляет метиленовую группу, R2 представляет
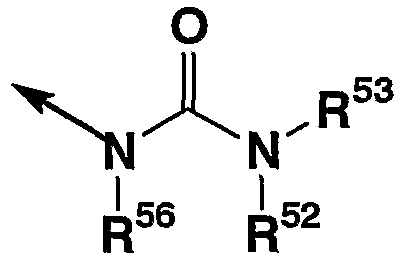
(в которой все символы имеют значения, описанные выше), т.е. соединение, представленное формулой (Ie)
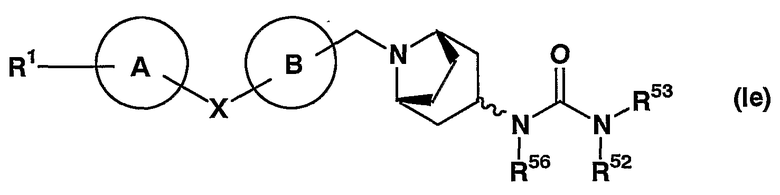
(в которой все символы имеют значения, описанные выше); соединение, в котором кольцо D представляет пирролидиновое кольцо и Y представляет метиленовую группу, R2 представляет
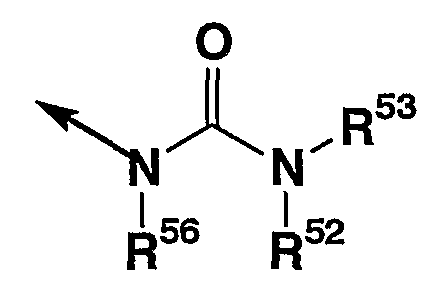
(в которой все символы имеют значения, описанные выше), т.е. соединение, представленное формулой (If)
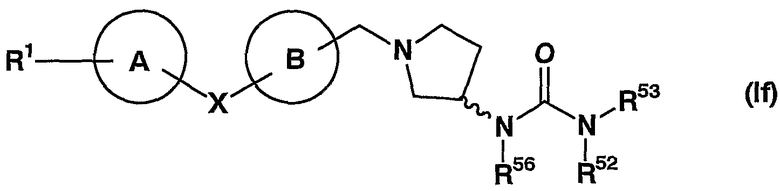
(в которой все символы имеют значения, описанные выше); соединение, в котором кольцо D представляет пиперидин и Y представляет метиленовую группу, R2 представляет
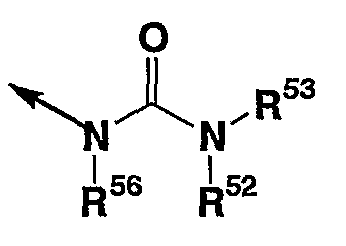
(в которой все символы имеют значения, описанные выше), т.е. соединение, представленное формулой (Ig)
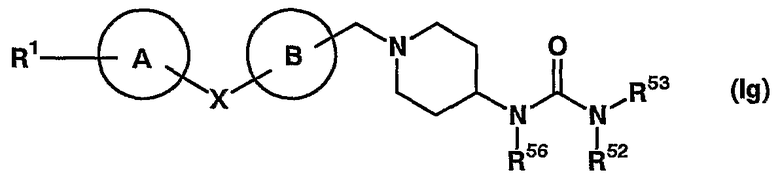
(в которой все символы имеют значения, описанные выше); соединение, в котором кольцо D представляет азепановое кольцо и Y представляет метиленовую группу, R2 представляет
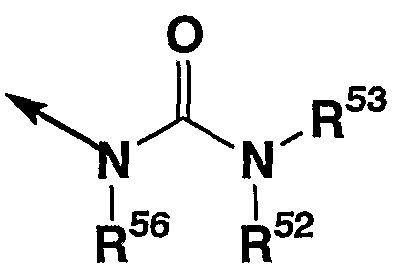
(где все символы имеют те же значения, что и описанные выше), т.е., соединение представленное формулой (Ih)
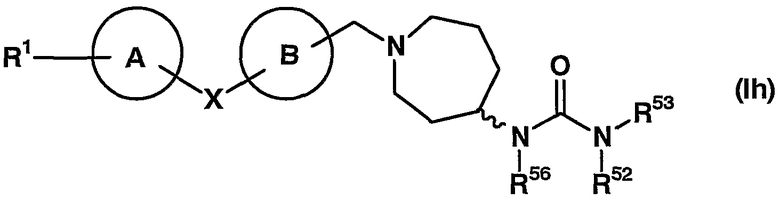
(где все символы имеют те же значения, что и описанные выше), его соли, его N-оксиды, его сольваты и его пролекарства.
Предпочтительными являются соединения в Примерах, их соли, их N-оксиды, их сольваты и их пролекарства. Более предпочтительными являются
(1) 5-({[бутил(1-{4-[4-(метилсульфонил)фенокси]бензил}-4-пиперидинил)амино]карбонил}амино)-2,4-дифторбензамид,
(2) 5-[({бутил[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамид,
(3) 5-({[бутил(1-{[6-(4-{[(2-метоксиэтил)амино]карбонил}фенокси)-3-пиридинил]метил}-4-пиперидинил)амино]карбонил}амино)-2,4-дифторбензамид,
(4) 5-{[(бутил{1-[(6-{4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамид,
(5) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-3-метоксифенил)метансульфонамид,
(6) 5-{[(бутил{1-[(6-{2-метил-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2-хлор-4-фторбензамид,
(7) 2-(5-{[(бутил{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторфенил)ацетамид,
(8) 5-[({бутил[1-(4-{4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифтор-N-метилбензамид,
(9) 5-{[(бутил{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамид,
(10) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(11) 5-[({бутил[1-(4-{4-[(метиламино)сульфонил]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамид,
(12) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(3-тиенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(13) N-[4-({5-[(4-{3-тиенил[(3-тиениламино)карбонил]амино}-1-пиперидинил)метил]-2-пиридинил}окси)фенил]метансульфонамид,
(14) 2-фтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамид,
(15) N-{4-[4-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-3,5-диметил-1H-пиразол-1-ил]фенил}метансульфонамид,
(16) 4-[4-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-3,5-диметил-1H-пиразол-1-ил]-N-[2-(4-морфолинил)этил]бензолсульфонамид,
(17) N-(4-{[5-({4-[{[(2,4-дифторфенил)амино]карбонил}(3-тиенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(18) 2-хлор-N-метил-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамид,
(19) N-(4-{[5-({4-[({[4-хлор-3-(4-морфолинилкарбонил)фенил]амино}карбонил)(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(20) 2-фтор-5-{[((3-фторфенил){1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}бензамид,
(21) N-(3-фторфенил)-N'-(6-метил-3-пиридинил)-N-[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]мочевина,
(22) 2-[4-({4-[[({4-фтор-3-[(метилсульфонил)амино]фенил}амино)карбонил](фенил)амино]-1-пиперидинил}метил)фенокси]-5-[(метилсульфонил)амино]бензамид,
(23) 2-фтор-N-метил-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамид,
(24) 2-фтор-N-метил-5-({[[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил](фенил)амино]карбонил}амино)бензамид,
(25) 2-[4-({4-[({[3-(ацетиламино)-4-фторфенил]амино}карбонил)(фенил)амино]-1-пиперидинил}метил)фенокси]-5-[(метилсульфонил)амино]бензамид,
(26) N'-(4-фторфенил)-N-[1-({6-[4-(метилсульфонил)фенокси]пиридин-3-ил}метил)пиперидин-4-ил]-N-фенилмочевина,
(27) N-(4-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(28) N-[2-фтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)фенил]ацетамид,
(29) N-{4-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]фенил}метансульфонамид,
(30) 5-[({бутил[1-(4-{2-метил-4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамид,
(31) N-(4-{[5-({4-[{[(2,4-дифторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-3-метоксифенил)метансульфонамид,
(32) N-(4-{[5-({4-[{[(4-метилфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(33) N-(4-{[5-({4-[{[(4-хлорфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(34) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)ацетамид,
их соли, их N-оксиды, их сольваты и их пролекарства и т.д.
Более предпочтительными являются
2-фтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамид,
N-(4-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
N-[2-фтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)фенил]ацетамид,
N-{4-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]фенил}метансульфонамид,
5-[({бутил[1-(4-{2-метил-4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамид,
N-(4-{[5-({4-[{[(2,4-дифторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-3-метоксифенил)метансульфонамид,
N-(4-{[5-({4-[{[(4-метилфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
N-(4-{[5-({4-[{[(4-хлорфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)ацетамид,
их соли, их N-оксиды, их сольваты и их пролекарства и т.д.
В настоящем изобретении так же предпочтительными являются
(1) N-{4-[(5-{[4-((3-метилфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]фенил}метансульфонамид,
(2) N-(2-фтор-5-{[((3-метилфенил){1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}фенил)ацетамид,
(3) N-(2-фтор-5-{[((3-фторфенил){1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}фенил)ацетамид,
(4) N-(2-фтор-5-{[((3-фторфенил){1-[(6-{2-метил-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}фенил)ацетамид,
(5) N-[5-({[{1-[(6-{2-хлор-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(3-фторфенил)амино]карбонил}амино)-2-фторфенил]ацетамид,
(6) N-{4-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]-3-метилфенил}метансульфонамид,
(7) N-{3-хлор-4-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]фенил}метансульфонамид,
(8) 2-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]-5-[(метилсульфонил)амино]бензамид,
(9) 2-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]-N-метил-5-[(метилсульфонил)амино]бензамид,
(10) N-[4-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-3-(метилсульфонил)фенил]метансульфонамид,
(11) N-{2-[(5-{[4-((3-метилфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]-5-[(метилсульфонил)амино]фенил}ацетамид,
(12) N-(4-{[5-({4-[[[(4-фторфенил)амино](имино)метил](фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(13) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонотиоил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(14) 2-фтор-N-метил-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-3-азетидинил}(фенил)амино]карбонил}амино)бензамид,
(15) N-(4-{[5-({(3R)-3-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пирролидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(16) N-[2-фтор-5-({[{(3S)-1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-3-пирролидинил}(фенил)амино]карбонил}амино)фенил]ацетамид,
(17) N-(4-{[5-({(4R)-4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-азепанил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(18) N-(4-{[5-({(4S)-4-[{[(4-хлорфенил)амино]карбонил}(фенил)амино]-1-азепанил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(19) 2-фтор-5-({[(1-{[6-({4-[(метилсульфонил)амино]фенил}сульфонил)-3-пиридинил]метил}-4-пиперидинил)(фенил)амино]карбонил}амино)бензамид,
(20) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]метил}фенил)метансульфонамид,
(21) 2-{[5-({4-[{[(4-хлорфенил)амино]карбонил}(3-фторфенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-5-[(метилсульфонил)амино]бензамид,
(22) N-(3-метилфенил)-N'-(6-метил-3-пиридинил)-N-[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]мочевина,
(23) N-[1-({6-[4-(этилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]-N-(3-фторфенил)-N'-(6-метил-3-пиридинил)мочевина,
(24) N-(3-фторфенил)-N-[1-({6-[4-(изопропилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]-N'-(6-метил-3-пиридинил)мочевина,
(25) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]метил}фенил)этансульфонамид,
(26) 2-фтор-5-{[((3-фторфенил){1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-3-азетидинил}амино)карбонил]амино}бензамид,
(27) N-(4-{[5-({4-[{[(6-этил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(28) N-{4-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-6-метил-2-пиридинил)окси]фенил}метансульфонамид,
(29) N-[2-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]-5-(метилсульфонил)фенил]ацетамид,
(30) N-(4-{[5-({4-[{[(6-этил-3-пиридинил)амино]карбонил}(3-фторфенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(31) N-{2-{[5-({4-[{[(4-хлорфенил)амино]карбонил}(3-фторфенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-5-[(метилсульфонил)амино]фенил}ацетамид,
(32) N-{2-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)метил]-5-[(метилсульфонил)амино]фенил}ацетамид,
(33) N-[4-(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)фенил]метансульфонамид,
(34) 2-фтор-5-({[{1-[(2-метил-6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамид,
(35) N-{4-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)сульфонил]фенил}метансульфонамид,
(36) N-(4-{[5-({4-[{[(4-хлорфенил)амино]карбонил}(3-метилфенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(37) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(3-метилфенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(38) 2-фтор-5-({[{1-[(2-метил-6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(3-метилфенил)амино]карбонил}амино)бензамид,
(39) N-этил-2-фтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамид,
(40) 2-фтор-N-метил-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонотиоил}амино)бензамид,
(41) 2-фтор-5-{[((3-фторфенил){(3S)-1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-3-пирролидинил}амино)карбонил]амино}-N-метилбензамид,
(42) N-[5-({[{(4S)-1-[(6-{4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-азепанил}(фенил)амино]карбонил}амино)-2-фторфенил]ацетамид,
(43) 2-{[5-({4-[({[3-(ацетиламино)-4-фторфенил]амино}карбонил)(3-фторфенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-N-метил-5-[(метилсульфонил)амино]бензамид,
(44) N-[5-({[{1-[(6-{2-хлор-4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(3-фторфенил)амино]карбонил}амино)-2-фторфенил]ацетамид,
(45) 5-({[{(3R)-1-[(6-{4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-3-пирролидинил}(фенил)амино]карбонил}амино)-2-фторбензамид,
(46) N-(3-хлор-4-{[5-({4-[{[(4-хлорфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(47) 5-({[{1-[(6-{2-(аминокарбонил)-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(3-фторфенил)амино]карбонил}амино)-2-фтор-N-метилбензамид,
(48) 2-фтор-N-метил-5-({[{1-[(6-{2-метил-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамид,
(49) N-(4-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]сульфонил}фенил)метансульфонамид,
(50) 2-фтор-N-метил-5-{[((3-метилфенил){1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}бензамид,
(51) 2-фтор-5-{[((3-метилфенил){1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}бензамид,
(52) 2-фтор-5-{[((3-фторфенил){1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-N-метилбензамид,
(53) N-(3-метил-4-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(54) N-(3-хлор-4-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(55) N-(4-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)этансульфонамид,
(56) N-(4-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиразинил]окси}фенил)метансульфонамид,
(57) N-(4-{[5-({(3S)-3-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пирролидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(58) N-(4-{[5-({(4S)-4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-азепанил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(59) N-(4-{[5-({(3R)-3-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пирролидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид,
(60) 2-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-5-[(метилсульфонил)амино]бензамид,
(61) 2-{[5-({4-[({[3-(ацетиламино)-4-фторфенил]амино}карбонил)(3-фторфенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-5-[(метилсульфонил)амино]бензамид,
(62) 2-{[5-({4-[{[(4-хлорфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-5-[(метилсульфонил)амино]бензамид,
(63) N-[4-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]-3-(метилсульфонил)фенил]метансульфонамид,
(64) N-(4-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]метил}фенил)метансульфонамид,
(65) N-{4-[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]фенил}метансульфонамид,
(66) N-{4-[(5-{[4-((3-метилфенил){[(6-метил-3-пиридинил)-амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]-фенил}метансульфонамид,
(67) N-[5-({[{1-[(6-{4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(3-фторфенил)амино]карбонил}амино)-2-фторфенил]ацетамид,
(68) 2-фтор-5-({[{1-[(6-{2-метил-4-[(метилсульфонил)амино]-фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамид,
(69) N-[5-({[{1-[(6-{4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)-2-фторбензамид, и
(70) N-{4-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)-амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]-фенил}этансульфонамид, их соли, их N-оксиды, их сольваты и их пролекарства.
Процессы получения соединения настоящего изобретения:
Соединение настоящего изобретения, представленное формулой (I), может быть получено методами, которые должным образом улучшают и сочетают известные методы, таких как методы, описанные ниже, методы, описанные в Примерах, или методы, описанные в Comprehensive Organic Transformations: А Guide to Functional Group Preparations, 2nd Edition (Richard C. Larock, John Willey & Sons Inc, 1999). В каждом способе, описанном ниже, исходный материал может использоваться в виде его соли. Пример соли включает соль соединения формулы (I), описанной выше.
Среди соединений, представленных формулой (I), соединение, в котором спейсер является смежным с кольцом D и представляет -CH2-, -CO- или -SO2-, может быть получено с помощью алкилирования, амидирования или сульфонамидирования соединением, представленным формулой (1)
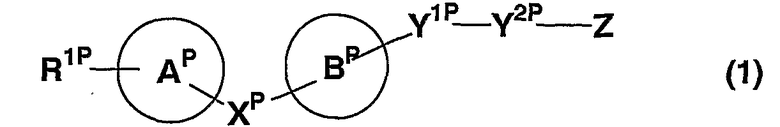
(в которой Z представляет гидрокси группу или уходящую группу (например, атом галогена п-толуолсульфонилокси группу, метансульфонилокси группу, трифторметансульфонилокси группу и др.), Y1P представляет связь или спейсер, содержащий 1 или 2 атома в качестве главной цепи, Y2P представляет -CH2-, -CO- или -SO2-, и R1P, XP, кольцо AP и кольцо BP имеют те же значения, что и R1, X, кольцо А и кольцо В, соответственно, при условии, что карбокси группа, гидрокси, амино или меркапто группа в R1P, XP, Y1P, Y2P, кольце AP и кольце BP могут быть защищены, если необходимо. Другие символы имеют те же значения, что описаны выше) и соединением, представленным формулой (2)
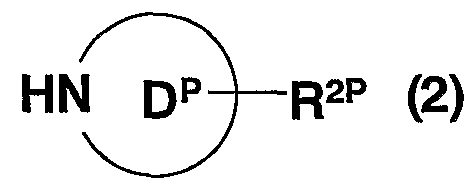
(которой R2P и кольцо DP имеют те же значения, что и R2 и D соответственно. При условии, что карбокси группа, гидрокси, амино или меркапто группа в R2P или кольце DP могут быть защищены, если необходимо), если необходимо, с последующим удалением защитной группы.
Алкилирование хорошо известно. Например, оно может осуществляться в органическом растворителе (например, диметилформамиде, диметилсульфоксиде), в присутствии щелочи (например, карбоната калия, карбоната натрия, триэтиламина и пр.) и в присутствии или отсутствии иодида натрия или иодида калия примерно при 0-150°С.
Амидирование является известным. Например, оно включает способ
(1) через ацилгалогенид,
(2) через смешанный ангидрид кислоты,
(3) с использованием конденсирующего агента.
Данные способы поясняются следующим образом.
(1) Способ через ацилгалогенид может осуществляться, например, с помощью реакции карбоновой кислоты с ацилгалогенидом (например, оксалилхлоридом или тионилхлоридом) в органическом растворителе (например, хлороформе, дихлорметане, диэтиловом эфире или тетрагидрофуране) или без растворителя при температуре примерно от -20°С до температуры кипения с обратным холодильником. А затем полученное ацилгалогенидное производное может подвергаться реакции с амином в органическом растворителе (например, хлороформе, дихлорметане, диэтиловом эфире или тетрагидрофуране) в присутствии основания (например, пиридина, триэтиламина, диметиланилина, диметиламинопиридина или диизопропилэтиламина и пр.) примерно при 0-40°С. В качестве альтернативы, полученное ацилгалогенидное производное может подвергаться реакции с амином в органическом растворителе (например, диоксане, тетрагидрофуране) с использованием щелочного водного раствора (например, бикарбоната натрия, гидроокиси натрия) примерно при -78-40°С.
(2) Способ через смешанный ангидрид кислоты может осуществляться, например, с помощью реакции карбоновой кислоты с ацилгалогенидом (например, пивалоилхлоридом, п-толуолсульфонилхлоридом или метансульфонилхлоридом) или производным кислоты (например, этилхлорформиатом или изобутилхлорформиатом) в органическом растворителе (например, хлороформе, дихлорметане, диэтиловом эфире или тетрагидрофуране) или без растворителя, в присутствии основания (например, пиридина, триэтиламина, диметиланилина, диметиламинопиридина или диизопропилэтиламина) примерно при 0-40°С. А затем полученное смешанное кислотноангидридное производное может подвергаться реакции с амином в органическом растворителе (например, хлороформе, метиленхлориде, диэтиловом эфире или тетрагидрофуране) примерно при 0-40°С.
(3) Способ с использованием конденсирующего агента может осуществляться, например, с помощью реакции карбоновой кислоты с амином в органическом растворителе (например, хлороформе, дихлорметане, диметилформамиде, диэтиловом эфире или тетрагидрофуране) или без растворителя, в присутствии или отсутствии основания (например, пиридина, триэтиламина, диметиланилина или диметиламинопиридина), с использованием конденсирующего агента (например, 1,3-дициклогексилкарбодиимида (DCC), 1-этил-3-[3-(диметиламино)пропил]карбодиимида (EDC), 1,1'-карбодиимидазола (CDI), 2-хлор-1-метилпиридинийиодида или циклического ангидрида 1-пропанфосфоновой кислоты (PPA)), в присутствии или отсутствии 1-гидроксибензотиазола (HOBt), примерно при 0-40°С.
Реакция, описанная в (1), (2) и (3), может осуществляться в атмосфере инертного газа (например, аргона, азота) для избегания воды для того, чтобы получить предпочтительный результат.
Сульфонамидирование хорошо известно. Например, оно может осуществляться, с помощью реакции сульфоновой кислоты с ацилгалогенидом (например, оксалилхлоридом или тионилхлоридом, пентахлоридом фосфора или трихлоридом фосфора) в органическом растворителе (например, хлороформе, дихлорметане, дихлорэтане, диэтиловом эфире, тетрагидрофуране или трет-бутилметиловом эфире) или без растворителя при температуре примерно от -20°С до температуры кипения. А затем полученное сульфонилгалогенидное производное может подвергаться реакции с амином в органическом растворителе (например, хлороформе, дихлорметане, диэтиловом эфире или тетрагидрофуране) в присутствии основания (например, диизопропилэтиламина, пиридина, триэтиламина, диметиланилина или диметиламинопиридина или и пр.) примерно при 0-40°С.
Удаление защитной группы является известным и может осуществляться следующим способом.
Карбонил-защитная группа включает, например, метил, этил, аллил, трет-бутил, трихлорэтил, бензил (Bn) или фенацил и пр.
Защитная группа гидрокси группы включает, например, метил, тритил, метоксиметил (MOM), 1-этоксиэтил (EE), метоксиэтоксиметил (MEM), 2-тетрагидропиранил (THP), триметилсилил (TMS), триэтилсилил (TES), трет-бутилдиметилсилил (TBDMS), трет-бутилдифенилсилил (TBDPS), ацетил (Ac), пивалоил, бензоил, бензил (Bn), п-метоксибензил, аллилоксикарбонил (Alloc) и 2,2,2-трихлорэтоксикарбонил (Troc) и др.
Защитная группа амино группы включает такую, как бензилоксикарбонил, трет-бутоксикарбонил, аллилоксикарбонил (Alloc), 1-метил-1-(4-бифенил)этоксикарбонил (Bpoc), трифторацетил, 9-флуоренилметоксикарбонил (Fmoc), бензил (Bn), п-метоксибензил, бензилоксиметил (BOM) или 2-(триметилсилил)этоксиметил (SEM) и др.
Защитная группа меркапто группы включает, например, бензил, метоксибензил, метоксиметил (MOM), 2-тетрагидропиранил (THP), дифенилметил и ацетил (Ac) и др.
Что касается защитных групп для карбоксила, гидроксила, амино и меркапто, в отношении указанных выше групп нет никаких особых ограничений до тех пор, пока ею является группа, которая способна легко и селективно отщепляться. Например, реакция снятия защиты может осуществляться по способу, упомянутому в “T. W. Greene, Protective Groups in Organic Synthesis, John Willey & Sons Inc, 1999”.
Реакция удаления защитной группы для карбоксила, гидроксила, амино и меркапто является известной и ее примерами являются следующие.
(1) реакция снятия защиты с помощью гидролиза щелочью;
(2) реакция снятия защиты в кислых условиях;
(3) реакция снятия защиты с помощью гидрогенолиза;
(4) реакция снятия защиты силила;
(5) реакция снятия защиты с использованием металла; и
(6) реакция снятия защиты с использованием металлического комплекса.
Данные способы будут конкретно проиллюстрированы следующим образом.
(1) Реакция снятия защиты с использованием щелочи осуществляется, например, примерно при 0-40°С с использованием гидроксида щелочного металла (такого как гидроокись натрия, гидроокись калия и гидроокись лития), гидроокиси щелочно-земельного металла (такой как гидроокись бария и гидроокись кальция), карбоната (такого как карбонат натрия и карбонат калия), водного раствора их или смеси их в органическом растворителе (например, метаноле, тетрагидрофуране и диоксане и др.)
(2) Реакция снятия защиты в кислых условиях осуществляется, например, примерно при 0-100°С в органической кислоте (например, уксусной кислоте, трифторуксусной, метансульфоновой или п-толуолсульфоновой кислоте), неорганической кислоте (например, соляной и серной кислоте) или в их смеси (такой как бромистый водород/уксусная кислота) в органическом растворителе (таком как дихлорметан, хлороформ, диоксан, этилацетат и анизол и др.).
(3) Реакция снятия защиты с помощью гидрогенолиза осуществляется, например, примерно при 0-200°С в атмосфере водорода при обычном давлении или высоком давлении или в присутствии формиата аммония в присутствии катализатора (такого как палладий-уголь, палладиевая чернь, гидроокись палладия, окись платины и никель Ренея) в растворителе [таком как растворитель типа простого эфира (такой как тетрагидрофуран, диоксан, диметоксиэтан и диэтиловый эфир), растворитель спиртового типа (такой как метанол и этанол), бензольного типа (такой как бензол и толуол), типа кетона (такой как ацетон и метилэтилкетон), нитрильного типа (такой как ацетонитрил), типа амида (такой как диметилформамид), вода, этилацетат, уксусная кислота или смешанный растворитель, включающий два или более их].
(4) Реакция депротекции или снятия защиты силила осуществляется, например, примерно при 0-40°С с использованием фторида тетрабутиламмония в органическом растворителе, смешиваемом с водой (таком как тетрагидрофуран и ацетонитрил и др.).
(5) Реакция снятия защиты с использованием металла осуществляется, например, примерно при 0-40°С с или без ультразвукового излучения в присутствии порошкообразного цинка в кислотном растворителе (таком как уксусная кислота, буфер с рН 4,2-7,2 и смешанный раствор раствора его с органическим растворителем, таким как тетрагидрофуран).
(6) Реакция снятия защиты с использованием комплекса металла осуществляется, например, примерно при 0-40°С с использованием металлического комплекса [такого как тетракистрифенилфосфинпалладий (0), дихлорид бис(трифенилфосфин)палладия (II), ацетат палладия (II) и хлорид трис(трифенилфосфин)родия (I)] в присутствии или отсутствии фосфинового агента (такого как трифенилфосфин) в присутствии улавливающего реагента (такого как трибутилоловогидрид, триэтилсилан, димедон, морфолин, диэтиламин и пирролидин), органической кислоты (такой как уксусная кислота, муравьиная кислота и 2-этилкапроновая кислота) и/или соли органической кислоты (такой как 2-этилгексаноат натрия и 2-этилгексаноат калия) в органическом растворителе (таком как дихлорметан, диметилфорамид, тетрагидрофуран, этилацетат, ацетонитрил, диоксан и этанол), воде или смешанном растворителе из указанных.
Помимо изложенного выше, снятие защиты может также проводиться, например, в соответствии со способами, описанными в T. W. Greene, Protective Groups in Organic Synthesis, Willey, New York, 1999.
Специалисты в данной области техники могут легко понять, что целевое соединение настоящего изобретения может быть легко получено с использованием соответствующих реакций из реакций снятия защиты.
Среди соединений настоящего изобретения, представленных формулой (I), соединение, в котором R2 представляет амино группу, которая может иметь заместитель(заместители), т.е. соединение, представленное формулой (I-a)
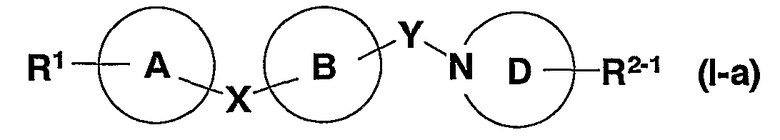
(в которой R2-1 представляет амино группу, которая может иметь заместитель(заместители), а другие символы имеют значения, описанные выше), может получаться с помощью восстановительного аминирования соединения, представленного формулой (3)
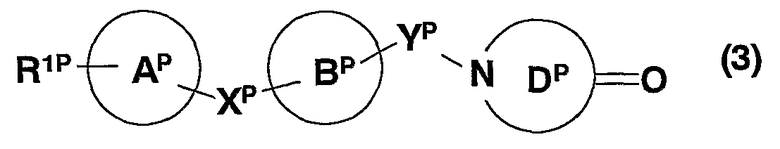
(в которой все другие символы имеют значения, описанные выше), и соединения, представленного формулой (4)
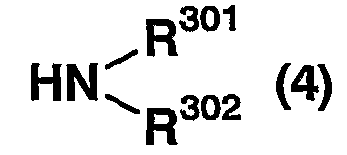
(в которой R301 и R302, которые являются одинаковыми или различными, каждый представляет атом водорода или имеют те же значения, что и “заместители” описанной выше “амино группа, которая может иметь заместитель(заместители)”, а другие символы имеют значения, описанные выше, при условии, что карбокси, гидрокси, амино или меркапто группа в R301 и R302 могут быть, если необходимо, защищены), с последующим, если необходимо, удалением защитной группы.
Восстановительное аминирование хорошо известно. Например, оно может осуществляться с помощью восстанавливающего агента (например, триацетоксиборгидрида натрия или цианоборгидрида натрия) примерно при 0-40°С в органическом растворителе (например, дихлорэтане, дихлорметане или диметилформамиде) в присутствии или отсутствии третичного амина (например, триэтиламина или диизопропилэтиламина), в присутствии или отсутствии уксусной кислоты.
Удаление защитной группы может осуществляться с помощью описанного выше способа.
Среди соединений настоящего изобретения, представленных формулой (I), соединение, в котором R2 представляет
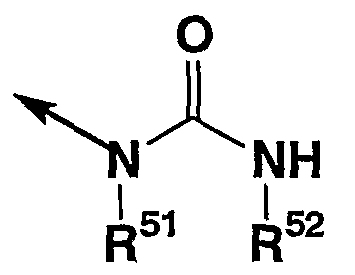
(в которой все символы имеют значения, описанные выше), т.е. соединение, представленное формулой (I-d)
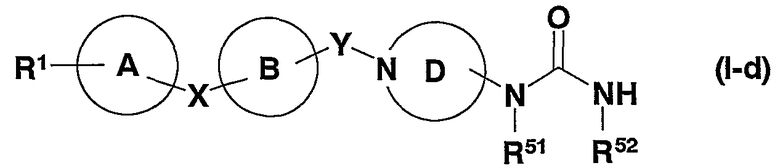
(в которой все символы имеют значения, описанные выше), может быть получено с помощью представленной ниже реакции с использованием соединения, представленного формулой (5)
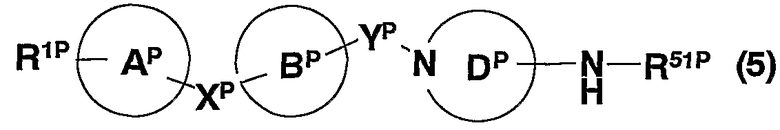
(в которой R51P имеет те же значения, что и R51, а другие символы имеют значения, описанные выше, при условии, что карбокси, гидрокси, амино или меркапто группа в R51P, если необходимо, может быть защищена) и соединения, представленного формулой (6)

(в которой R52P имеет те же значения, что и R52, а другие символы имеют значения, описанные выше, при условии, что карбокси, гидрокси, амино или меркапто группа в R52P, если необходимо, может быть защищена), если необходимо с последующим удалением защитной группы.
Реакция является хорошо известной. Например, она может осуществляться в органическом растворителе (например, N,N-диметилформамиде, толуоле или тетрагидрофуране) с помощью основания (например, пиридина, триэтиламина, диметиланилина, диметиламинопиридина или диизопропилэтиламина) примерно при 20-120°С.
Удаление защитной группы может осуществляться с помощью описанного выше способа.
Кроме того, соединение, представленное формулой (I-d), может получаться с помощью реакции образования мочевины с использованием соединения, представленного формулой (5), и соединения, представленного формулой (7)
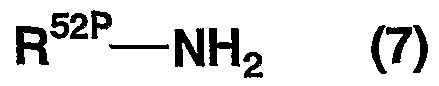
(в которой символ имеет значения, описанные выше), если необходимо с последующим удалением защитной группы.
Реакция является хорошо известной. Например, она может осуществляться в органическом растворителе (например, тетрагидрофуране или N,N-диметилформамиде) в присутствии трифосгена с помощью основания (например, триэтиламина) примерно при 0-40°С. Кроме того, она может осуществляться в органическом растворителе (например, дихлорметане или N,N-диметилформамиде) в присутствии 1,1'-карбонилбис-1Н-имидазола (CDI) с помощью основания (например, триэтиламина или N-метилморфолина) или без основания примерно при 0-80°С.
Удаление защитной группы может осуществляться с помощью описанного выше способа.
Среди соединений настоящего изобретения, представленных формулой (I), соединение, в котором Y представляет метилен, т.е. соединение, представленное формулой (Ie)
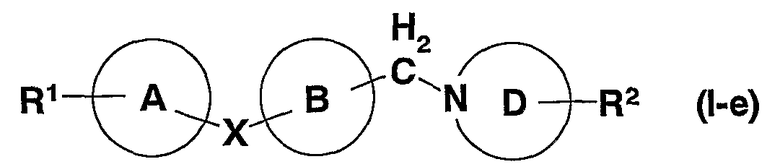
(в которой все символы имеют значения, описанные выше), может получаться с помощью восстановительного аминирования соединения, представленного формулой (8)
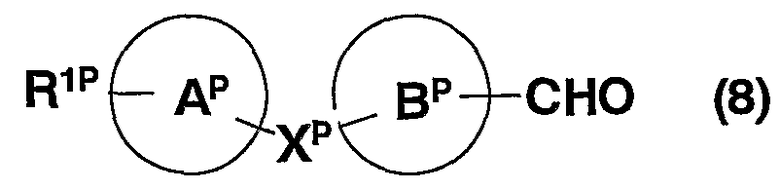
(в которой все символы имеют значения, описанные выше), и соединения, представленного формулой (2), с последующим, если необходимо, удалением защитной группы.
Восстановительное аминирование и удаление защитной группы может осуществляться с помощью описанного выше способа.
Среди соединений, представленных формулой (I), соединение, в котором, по крайней мере, один атом азота представляет четвертичную аммониевую соль, т.е. соединения формулы (I-2)
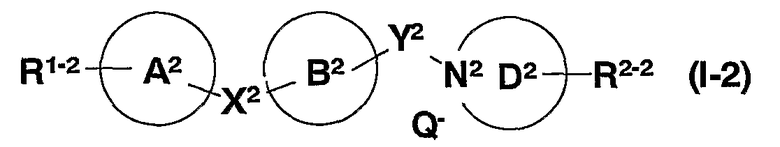
(в которой R1-2, R2-2, X2, Y2, кольцо A2, кольцо B2 и кольцо D2 имеют те же значения, что и R1, R2, X, Y, кольцо A, кольцо B и кольцо D, соответственно, и N2 представляет атом азота, при условии, что, по крайней мере, один атом азота представляет четвертичную аммониевую соль, а Q- представляет ион галогена), могут быть получены с помощью реакции соединения формулы(I) с соединениями формулы (9)

(в которой R0 представляет С1-8 алкил или С1-8 алкил, замещенный фенилом, и Q представляет галоген).
Данная реакция хорошо известна и может осуществляться, например, в органическом растворителе (ацетоне, диметилформамиде или метилэтилкетоне и пр.) примерно при 0-40°С.
Среди соединений формулы (I) соединение, в котором, по крайней мере, один азот представляет N-оксид, т.е. соединение формулы (I-3)
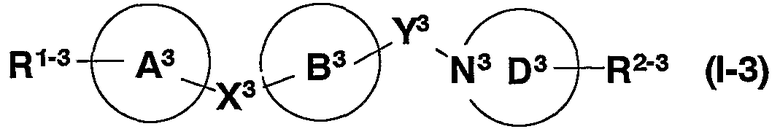
(в которой R1-3, R2-3, X3, Y3, кольцо A3, кольцо B3 и кольцо D3 имеют те же значения, что и R1, R2, X, Y, кольцо A, кольцо B и кольцо D, соответственно, и N3 представляет атом азота, при условии, что, по крайней мере, один атом азота представляет N-оксид), могут быть получены с помощью окисления соединения формулы (I).
Окисление является хорошо известным и может осуществляться, например, в подходящем органическом растворителе (например, дихлорметане, хлороформе, бензоле, гексане или трет-бутиловом спирте) в присутствии избыточного окисляющего агента (перекиси водорода, периодата натрия, ацилнитрита, пербората натрия, перокси кислоты (например, 3-хлорпербензойной кислоты или перуксусной кислоты и др.), ОКСОНА (наименование брэнда, ОКСОН является сокращенным названием для пероксимоносульфата калия), перманганата калия или хромовой кислоты и др.) примерно при 20-60°С.
Соединение настоящего изобретения может быть получено с помощью данных реакций или частично модифицированных реакций.
Другие исходные соединения или соединения, используемые в качестве реагентов, являются известными и могут легко получаться с помощью сочетания известных способов, например, способов, описанных в Comprehensive Organic Transformations: А Guide to Functional Group Preparations, 2nd Edition (Richard C. Larock, John Willey & Sons Inc, 1999) или Elmer J. Rauckman et al., J. Org. Chem., vol.41, No.3, 1976, стр. 564-565 и др.
В каждой реакции, приведенной в описании, реакции с нагреванием, как это очевидно специалистам в данной области техники, могут осуществляться с водяной баней, масляной баней, песочной баней и микроволновым излучением.
В каждой реакции в описании может использоваться твердофазный реагент, который осажден на полимере (например, полистироле, полиакриламиде, полипропилене или полиэтиленгликоле и др.).
В каждой реакции в описании полученные продукты могут очищаться с помощью общепринятых приемов. Например, очистка может осуществляться с помощью перегонки при атмосферном или пониженном давлении, высокоэффективной жидкостной хроматографии с сикагелем или силикатом магния, тонкослойной хроматографии, ионно-обменных смол, поглощающих или акцепторных смол, колоночной хроматографии, промывки или кристаллизации. Очистка может проводиться после каждой реакции или после нескольких реакций.
В реакции с использованием полистирольной смолы, приведенной в описании, полученные продукты могут очищаться с помощью общепринятых приемов. Например, очистка может осуществляться путем споласкивания их растворителем (диметилформамидом, дихлорметаном, метанолом, тетрагидрофураном, толуолом, смесью уксусная кислота/толуол, и др.) более одного раза.
Токсичность:
Токсичность соединения, представленного формулой (I), его соли, N-оксида или сольвата, или его пролекарства (называемых здесь далее “соединение настоящего изобретения”) является очень низкой и поэтому оно может считаться безопасным для фармацевтического использования.
Применение для фармацевтических целей:
Соединение настоящего изобретения имеет хорошую растворимость и абсорбируемость. Соединение настоящего изобретения имеет слабую ингибирующую активность против ферментов, метаболизирующих лекарственное средство. Данные характериститки представляют физические, химические и фармацевтические свойства, предъявляемые лекарственным средствам, и соединения настоящего изобретения обладают надлежащими условиями по отношенил к превосходным лекарственным средствам [см. (The Merck Manual of Diagnosis and Therapy (17th Ed.), Merck & Co.)].
То, что соединение настоящего изобретения полезно в качестве лекарственного средства, можно оценить с помощью различных экспериментальных методов, описанных ниже, методов, описанных в биологических примерах, и должным образом усовершенствованных способов. С помощью известных методов можно также легко оценить, что соединение настоящего изобретения обладает хорошими фармакокинетическими свойствами, такими как продолжительность периода полураспада сыворотки, стабильность в желудочно-кишечном тракте, абсорбция пероральных препаратов, биодоступность и др., например, по способу, описанному в “Yakubutsu bioavailability (Hyouka to kaizen no kagaku), July 6, 1998, Gendaiiryou-sha” и др.
(I) Эксперимент по оценке ингибирующей активности соединения настоящего изобретения против ферментов, метаболизирующих лекарственное средство.
(i) Ингибирующая активность против CYP2C9 человека
Ингибирующая активность соединения настоящего изобретения против CYP2C9 человека можно оценить по методу Sato et al. (Yakubutsudotai (Xenobio. Metabol. And Dispos.), 16(2), 115-126 (2001)), который усовершенствован с отношении точности анализа и/или чувствительности анализа.
(ii) Ингибирующая активность против CYP3A4 человека
Ингибирующая активность соединения настоящего изобретения против CYP3A4 человека можно оценить с помощью усовершенствованного метода, описанного в Drug Metabolism and Disposition, Vol.28(12), 1440-1448 (2000).
Например, приготавливают реакционный раствор, состоящий из фосфатнокалиевого буфера (рН 7,4) (конечная концентрация: 200 мМ), гексагидрата хлорида магния (конечная концентрация: 5 мМ), субстрата (7-бензилоксихинолина (7-BQ), конечная концентрация 40 мкМ) и микросомы экспрессионной системы (Daiichikagakuyakuhin, конечная концентрация: 0,25 мг/мл. 100 мкл реакционного раствора распределяют на 96-луночной планшете и добаляют 50 мкл водного раствора, содержащего испытуемое соединение и 0,8% ацетонитрила, для осуществления 10-минутного предварительного инкубирования при 37°С. Для инициирования реакции добавляют 50 мкл восстановленного никотинамидадениндинуклеотидфосфата (NADPH, 4 мМ). Интенсивности флуоресценции каждой лунки измеряют в момент, когда добавляют NADPH, и после инкубирования в течение 30 минут. Измеряют длину волны возбуждения при 409 нм и эмиссионную длину волны при 530 нм хинолинола, который является метаболитом субстрата. Степень ингибирования (%) испытуемого соединения вычисляют с помощью следующей вычислительной формулы с получением показателя IC50 (ИК50).
Степень ингибирования (%) = [1-{(измеренная величина с добавлением испытуемого соединения)-(холостой показатель)/(контрольный показатель-холостой показатель}}]x100.
(II) Эксперимент по оценке токсичности
(i) Испытание на острую токсичность на крысах
Испытуемое соединение вводят шестинедельной крысе Crj:CD (SD) в виде разовой внутривенной дозы или разового перорального введения. Токсичность можно оценить по контрасту с показателем, когда испытуемое соединение не добавлялось. Основная оценка токсичности может быть проведена путем, например, наблюдения состояния совершаемых поступков или локомоторной активности и пр.
(ii) Оценка активности соединения настоящего изобретения против hERG I Kr тока
Согласно сообщению Zou et al. (Biophys. J., Vol.74, 230-241 (1998)), с использованием HEK293 клеток сверхэкспрессируемого гена спецефических калиевых каналов сердца человека (human ether-a-go-go-related gene (hERG)), с помощью регистрации фиксации потенциала измеряют максимальный количественный ход hERG I Kr тока, индуцируемого деполяризационным импульсом с последующим реполяризационным импульсом. Степень изменения (степень ингибирования) вычисляют сравнением максимального количественного хода между периодом до добавления испытуемого соединения и спустя 10 минут после. Влияние испытуемого соединения на hERG I Kr ток можно оценить по степени ингибирования.
Соединения настоящего изобретения обладают антагонистической активностью против рецептора хемокина, особенно CCR5, у животных, включая человека, особенно у человека, поэтому они полезны при профилактике и/или лечении связанных с CCR5 заболеваний, например, разнообразных воспалительных заболеваний (астмы, нефрита, нефропатии, гепатита, артрита, ревматоидного артрита, ринита, конъюнктивита, воспалительного заболевания кишечника, такого как язвеный колит и др.), иммунологических заболеваний (аутоиммунной болезни, отторжения при трансплантации органов (отторжения трансплантата твердого органа, отторжения трансплантата панкреатических островковых клеток при лечении диабета, GVHD (заболевание трансплантат-против-хозяина), и пр.), иммуносупрессии, псориаза, рассеянного склероза, и др.), инфекционных заболеваний (заражения вирусом иммунодефицита человека, синдрома приобретенного иммунодефицита, RSV заражения, и др.), аллергических заболеваний (атопического дерматита, крапивницы, аллергического бронхолегочного аспергиллеза, аллергического эозинофильного гастроэнтерита, и др.), сердечнососудистых заболеваний (артериосклероза, ишемического реперфузионного повреждения и др.), синдрома острого респираторного дистресса, шока, сопровождающего бактериальную инфекцию, диабета, метастазы раковой опухоли и так далее.
Соединения настоящего изобретения обладают ингибирующей активностью против миграции клеток у животных, включая человека, особенно у человека, поэтому они полезны при профилактике и/или лечении разнообразных воспалительных заболеваний (астмы, нефрита, нефропатии, гепатита, артрита, ревматоидного артрита, ринита, коньюктивита, воспалительного заболевания кишечника, такого как язвеный колит и др.), иммунологических заболеваний (аутоиммунных болезней, отторжения при трансплантации органов (отторжения трансплантата твердого органа, отторжения трансплантата панкреатических островковых клеток при лечении диабета, GVHD и пр.), иммуносупрессии, псориаза, рассеянного склероза и др.), инфекционных заболеваний (заражения вирусом иммунодефицита человека, синдрома приобретенного иммунодефицита, RSV заражения и др.), аллергических заболеваний (атопического дерматита, крапивницы, аллергического бронхолегочного аспергиллеза, аллергического эозинофильного гастроэнтерита и др.), сердечнососудистых заболеваний (артериосклероза, ишемического реперфузионного повреждения и др.), синдрома острого респираторного дистресса, шока, сопровождающего бактериальную инфекцию, диабета, метастазы раковой опухоли и так далее.
Для описанной выше цели соединения настоящего изобретения могут обычно вводиться системно или локально, обычно с помощью перорального или парентерального введения.
Вводимые дозы определяются в зависимости, например, от возраста, веса тела, симптомов, желаемого терапевтического эффекта, способа введения и длительности лечения. У взрослых людей дозы на человека составляют обычно от 1 мг до 1000 мг с помощью перорального введения до нескольких раз в день и от 1 мг до 100 мг с помощью парентерального введения (предпочтительно внутривенного введения) до нескольцих раз в день или непрерывного введения от 1 до 24 часов в день в вену.
Как упоминалось выше, используемые дозы зависят от различных факторов. Поэтому, есть случаи, в которых могут использоваться дозы более низкие, или более высокие, чем указанные выше интервалы.
Соединения настоящего изобретения могут вводиться, например, в форме твердого препарата для перорального введения, в жидких формах для перорального введения, в виде инъекций, линиментов (лекарственных форм для наружного применения) или медицинских свечей для парентерального введения.
Твердые формы для перорального введения включают прессованные таблетки, пиллюли, капсулы, диспергируемые порошки и гранулы. Капсулы включают твердые и мягкие капсулы.
В таких твердых формах одно или более активных соединений могут быть смешаны с наполнителями (такими как лактоза, маннит, глюкоза, микрокристаллическая целлюлоза или крахмал), связующими (такими как гидроксипропилцеллюлоза, поливинилпирролидон или алюминат метасиликата магния), дезинтегрирующими или разрыхляющими агентами (такими как кальцийгликолят целлюлозы), смазочными агентами (такими как стеарат магния), стабилизирующими агентами и адьювантами растворов (такими как глютаминовая кислота или аспарагиновая кислота), и приготавливаются они в соответствии с методами, хорошо известными в обычной фармацевтической практике. Твердые формы могут при желании покрываться агентами покрытий (такими как сахар, желатин, гидроксипропилцеллюлоза или фталат гидроксипропилметилцеллюлозы), или покрываться двумя или более пленками. И, кроме того, покрытие может включать содержимое внутри капсул из абсорбируемых материалов, таких как желатин.
Жидкие формы для перорального введения включают фармацевтически приемлемые растворы, суспензии, эмульсии, сиропы и эликсиры. В таких формах одно или более активных соединений могут растворяться, суспендироваться или эмульгироваться в разбавителях, обычно используемых в данной области техники (таких как очищенная вода, этанол или их смесь). Помимо этого, такие жидкие формы могут также включать некоторые добавки, такие как смачивающие агенты, суспендирующие агенты, эмульгирующие, подслащивающие, вкусовые агенты, отдушки, консервирующие или буферирующие агенты.
Инъекционные препараты для парентерального введения включают стерильные водные препараты, суспензии, эмульсии и твердые формы, которые растворяются или суспендируются в растворителях для инъекции непосредственно перед использованием. В инъекционных препаратах одно или более активных соединений могут растворяться, суспендироваться или эмульгироваться в растворителях. Растворители могут включать дистиллированную воду для инъекций, физиологический раствор, растительное масло, пропиленгликоль, полиэтиленгликоль, спирт, такой как этанол, или их смеси. Инъекционные препараты могут включать некоторые добавки, такие как стабилизирующие агенты, адьюванты растворов (такие как глютаминовая кислота, аспарагиновая кислота или ПОЛИСОРБАТ80 (зарегистрированная торговая марка)), суспендирующие, эмульгирующие, успокаивающие агенты, буферирующие агенты, консерванты. На конечной стадии они могут стерилизоваться или могут приготавливаться стерильными методами. Они могут также производиться в виде стерильных твердых форм, таких как высушенные замораживанием продукты, которые могут непосредственно перед использованием растворяться в стерильной воде или некоторых других стерильных разбавителях для инъекций.
Другие формы для парентерального введения включают жидкости для наружного использования, мази и внутрикожные линименты, ингаляции, спреи, медицинские свечи и вагинальные суппозитории, которые включают одно или более активных соединений, и могут приготавливаться по способам, известным самим по себе.
Спреи могут включать дополнительные вещества иные, чем разбавители, используемые обычно, стабилизаторы, такие как бисульфит натрия, и буферы, способные придавать изотоничность, например, изотонические буферы, такие как хлорид натрия, цитрат натрия или лимонная кислота.
Соединения настоящего изобретения могут использоваться вместе с другими лекарственными препаратами, например, профилактическими и/или лечебными агентами от ВИЧ инфекций (в частности, агентами для профилактики и/или лечения СПИДа, или агентами против отторжения органов при трансплантации и/или для лечения аутоиммунных заболеваний. В данном случае лекарство, как таковое, может смешиваться с фармакологически приемлемым эксципиентом, связующим, дезинтегрирующим агентом, смазкой, стабилизатором, солюбилизатором, разбавителем и др. или отдельно или одновременно с изготовлением фармацевтического препарата и может вводиться или перорально, или парентерально в виде фармацевтической композиции для профилактики и/или лечения ВИЧ инфекций, отторжения органов при тансплантации и/или аутоиммунных заболеваний.
Соединения настоящего изобретения обладают активностью ингибирования заражения ВИЧ, который приобрел устойчивость к другим агентам для профилактики и/или лечения ВИЧ инфекции в частности агентам для профилактики и/или лечения СПИДа. Поэтому они могут также использоваться для ВИЧ-инфицированных пациентов, для которых другие агенты для профилактики и/или лечения ВИЧ инфекции больше не эффективны. В этом случае, хотя соединение настоящего изобретения может использоваться одно, оно может также использоваться вместе с агентами для профилактики и/или лечения ВИЧ инфекции, когда ВИЧ инфицирующий штамм приобрел устойчивость, или с другими лекарственными средствами.
Настоящее изобретение охватывает сочетание соединений настоящего изобретения с лекарственными средствами, которые не ингибируют ВИЧ инфекцию, с помощью чего профилактическое и/или лечебное действие на ВИЧ инфекцию усиливается по сравнению с одиночным препаратом.
Примерами других агентов для профилактики и/или лечения ВИЧ инфекции, используемых для сочетания с соединениями настоящего изобретения, являются ингибитор обратной транскриптазы, ингибитор протеазы, антагонист хемокина (такой как CCR2 антагонист, CCR3 антагонист, CCR4 антагонист, CCR5 антагонист, CXCR3 антагонист и CXCR4 антагонист), ингибитор интегразы, ингибитор слияния, антитело к антигену поверхности ВИЧ и вакцина от ВИЧ.
Ингибиторами обратной транскриптазы являются в частности (1) ингибиторы нуклеозид/нуклеотид обратной транскриптазы: зидовудин (наименование брэнда: Ретровир), диданозин (наименование брэнда: Видекс), зальцитабин (наименование брэнда: HIVID), ставудин (наименование брэнда: Zerit), ламивудин (наименование брэнда: Эпивир), абакавир (наименование брэнда: Ziagen), адефовир, адефовирдипивоксил, эмтрицитабин (наименование брэнда: Coviracil) или РМРА (наименование брэнда: Tenofovir) и др. и (2) ингибиторы ненуклеозид обратной транскриптазы: невирапин (наименование брэнда: Вирамун), делавирдин (наименование брэнда: Рескриптор), эфавиренц (наименование брэнда: Sustiva, Stocklin) или каправирин (AG1549) и др.
Ингибиторами протеазы являются, в частности, индинавир (наименование брэнда: Crixivan), ритонавир (наименование брэнда: Norvir), нельфинавир (наименование брэнда: Viracept), саквинавир (наименование брэнда: Invirase, Fortovase), ампренавир (наименование брэнда: Agenerase), лопинавир (наименование брэнда: Kaletra) или типранавир и др.
В качестве антагонистов хемокина в сочетание включают внутренний лиганд хемокинового рецептора, его производные, его не-пептидные низкомолекулярные соединения или антитела рецептора хемокина.
Примерами внутреннего лиганда рецептора хемокина являются, в частности, MIP-1α, MIP-1β, RANTES, SDF-1α, SDF-1β, MCP-1, MCP-2, MCP-4, Эотаксин и MDC и др.
Производными внутреннего лиганда являются, в частности, AOP-RANTES, Met-SDF-1α, Met-SDF-1β и др.
Рецепторами антител хемокина являются, в частности, Pro-140 и др.
CCR2 Антагонисты описаны, в частности, в описаниях WO99/07351, WO99/40913, WO00/46195, WO00/46196, WO00/46197, WO00/46198, WO00/46199, WO00/69432 или WO00/69815 или в Bioorg. Med. Chem. Lett., 10, 1803(2000) и др.
Антагонисты CCR3 описаны, например, в описаниях DE19837386, WO99/55324, WO99/55330, WO00/04003, WO00/27800, WO00/27835, WO00/27843, WO00/29377, WO00/31032, WO00/31033, WO00/34278, WO00/35449, WO00/35451, WO00/35452, WO00/35453, WO00/35454, WO00/35876, WO00/35877, WO00/41685, WO00/51607, WO00/51608, WO00/51609, WO00/51610, WO00/53172, WO00/53600, WO00/58305, WO00/59497, WO00/59498, WO00/59502, WO00/59503, WO00/62814, WO00/73327 или WO01/09088 и др.
Антагонистами CCR5 являются, например, TAK-779, SCH-351125 (SCH-C), SCH-417690(SCH-D), UK-427857, GW873140 (ONO-4128), TAK-220 и др. Кроме того, сочетание включает в себя соединения, описанные, например в описаниях WO99/17773, WO99/32100, WO00/06085, WO00/06146, WO00/10965, WO00/06153, WO00/21916, WO00/37455, EP1013276, WO00/38680, WO00/39125, WO00/40239, WO00/42045, WO00/53175, WO00/42852, WO00/66551, WO0/66558, WO00/66559, WO00/66141, WO00/68203, JP2000309598, WO00/51607, WO00/51608, WO00/51609, WO00/51610, WO00/56729, WO00/59497, WO00/59498, WO00/59502, WO00/59503, WO00/76933, WO98/25605, WO99/04794, WO99/38514, Bioorg. Med. Chem. Lett., 11, 2663 (2003), Curr. Med. Chem. Anti-Infective Agents, 4, 133 (2005), Current Opinion in Pharmacology, 4, 447 (2004), или Current Opinion in Investigational Drugs, 5, 851 (2004) и др.
Антагонисты CXCR3 описаны, например, в описании WO01/16114, WO02/083143, WO02/085862, US6469002, или WO03/101970 и др.
Антагонистами CXCR4 являются, например, AMD-3100, AMD-070, T-22, KRH-1120, KRH-1636, KRH-2731 или соединения, описанные в описании WO00/66112 и др.
Ингибиторами интегразы являются Эквисетин, Темакрацин, PL-2500, V-165, NSC-618929, L-870810, L-708906 аналог, S-1360, или 1838 и др.
Ингибиторами слияния являются, в частности, T-20 (Пентасульфид) и T-1249 и др.
Примеры агентов сочетаний, приведенные выше, предназначены для иллюстрации настоящего изобретения, но никак не ограничивают их.
Типичные примеры обычных дозировочных уровней в клинических испытаниях ингибиторов обратной транскриптазы или ингибиторов протеазы, приведенные ниже, предназначены для иллюстрации настоящего изобретения, но не для ограничения изобретения ими.
300 мг таблетка, 300 мг на дозу, дважды в день;
Примерами других агентов для профилактики и/или лечения отторжения органов при транплантации, используемых в сочетании или комбинации соединений настоящего изобретения, являются иммуносупрессанты.
Примеры иммуносупрессантов включают такролимус (FK506), циклоспорин, сиролимус (рапамицин), кортикостероиды, азатиоприн, микофенолят мофетил, FTY-720, циклофосфамид, клеточно-поверхностные лигандные антитела, и др.
Примеры клеточно-поверхностных лигандных антител включают Атгам, Тимоглобулин, Симулект, Занапакс или Ортоклон и др.
Примерами других агентов для профилактики и/или лечения аутоиммунных заболеваний, используемых в сочетаниях с соединениями настоящего изобретения, являются нестероидные противовоспалительные лекарственные средства, модифицирующие заболевание противоревматические лекарственные средства (DMARDs, медленно действующие противоревматические лекарственные средства), стероиды, иммуносуппресантные агенты, противовоспалительные ферментные препараты, хондрозащитные агенты, ингибиторы Т-клеток, ингибитор TNFα (фактора некроза опухоли) (включают белковые препараты, такие как анти- TNFα антитела), ингибитор простагландинсинтазы, IL-1 ингибитор, IL-6 ингибитор (включает белковый препарат, такой как антитело анти-IL-6 рецептора), гамма-агонисты интерферона, простагландины, ингибитор фосфодиэстеразы, ингибитор металлопротеиназы и др.
Примеры нестероидного противовоспалительного лекарственного средства включают сасапирин, салицилат натрия, аспирин, аспириндиалюминатная форма препарата, дифлунизал, индометацин, супрофен, уфенамат, диметилизопропилазулен, буфексамак, фелбинак, диклофенак, толметин-натрий, Клинорил, фенбуфен, напметон, проглуметацин, индометацин-фарнезил, ацеметацин, проглуметацинмалеат, амфенак-натрий, мофезолак, этодолак, ибупрофен, ибупрофен-пиконол, напроксен, флурбипрофен, флурбипрофен-аксетил, кетопрофен, фенопрофен-кальций, тиапрофенен, оксапроцин, пранопрофен, локсопрофен-натрий, алюминопрофен, залтопрофен, мефенамовую кислоту, мефенамат алюминия, толфенамовую кислоту, флоктофенин, кетофенилбутазон, оксифенбутазон, пироксикам, теноксикам, анпироксикам, напагель крем, эпиризол, гидрохлорид тиарамида, гидрохлорид тиноридина, эморфазон, сульпирин, Мигренин, Саридон, Седес G, Ампило N, Сорбон, пириновые системные антипиретики, ацетаминофен, фенацетин, мезилат диметотиазина, симетридную форму, или антипириновые системные антипиретики и др.
Примеры модифицирующего болезнь противоревматического лекарства (DMARDs, медленно действующие противоревматические лекарства) включают, например, золото-тиоглюкозу, ауротиомалат-натрий, ауранофин, актарит, D-пеницилламиновые препараты, лобензарит-динатрий, буцилламин, гидроксихлорохин, салазосульфапиридин, метотрексат, или лефлуномид, и др.
Примеры стероидов для наружного применения включают пропионат клобетазола, ацетат дифлоразона, флуоцинонид, фуранкарбоксилат монометазона, дипропионат бетамезона, бутиропропионат бетамезона, валерат бетамезона, дифлупреднат, будезонид, валерат дифлукортолона, амцинонид, халцинонид, дексаметазон, пропионат дексаметазона, валерат диксаметазона, ацетат дексаметазона, ацетат гидрокортизона, бутират гидрокортизона, ацетопропионат гидрокортизона, пропионат депродона, валероацетат преднизолона, ацетонид флуоцинолона, дипропионат беклометазона, ацетонид триамцинонида, пивалат флуметазона, преднизолон, пропионат беклометазона и флудроксикортид и др.
Примеры стероидов для внутреннего применения или инъекции включают ацетат кортизона, гидрокортизон, натрийфосфат гидрокортизона, натрийсукцинат гидрокортизона, ацетат флудрокортизона, преднизолон, ацетат преднизолона, натрийсукцинат преднизолона, бутилацетат преднизолона, натрийфосфат преднизолона, ацетат галопредона, метилпреднизолон, ацетат метилпреднизолона, натрийсукцинат метилпреднизолона, триамицинолон, ацетат триамицинолона, ацетонид триамицинолона, дексаметазон, ацетат дексаметазона, натрийфосфат дексаметазона, пальмитат дексаметазона, ацетат параметазона и бетаметазон и др.
Примеры стероидов в качестве ингаляционного средства включают беклометазонпропионат, пропионат флутиказона, будезонид, флунизолид, триамицинолон, ST-126P, циклезонид, паломитионат дексаметазона, фуранкарбоксилат монометазона, сульфонат прастерона, дефлазакорт, сулептанат метилпреднизолона и натрийсукцинат метилпреднизолона и др.
Примеры противовоспалительных ферментных препаратов включают, например, хлорид лизозима, бромелаин, проназу, серрапептазу или стрептокиназа-стрептодорназа и др.
Примеры хондрозащитных агентов включают, например, гиалуронат натрия, глюкозамин, сульфат хондроитина и полисульфат глюкозамингликана и др.
Примеры ингибитора TNFα (включая белковый препарат, такой как анти-TNFα антитело) включают, например, инфликсимаб, адалимумаб или этанерцепт и др.
Примеры ингибиторов простагландинсинтазы включают, например, салазосульфапиридин, месалазин, ольсалазин, 4-аминосалициловую кислоту, JTE-522, ауранофин, капрофен, дифенпирамид, флуноксапрофен, флурбипрофен, индометацин, кетопрофен, лорноксикам, локсопрофен, Мелоксикам, оксапроцин, парсальмид, пипроксен, пироксикам, пироксикамбетадекс, циннамат пироксикама, индометацинат тропина, зальтопрофен и пранопрофен и др.
Примеры IL-1 ингибитора (включая белковый препарат, такой как антагонист IL-1 рецептора человека) включают, например, анакинру и др.
Примеры IL-6 ингибитора (включая белковый препарат, такой как антитело анти-IL-6 рецептора) включают, например, MRA и др.
Примеры простагландинов (называемых далее сокращенно “PG”) включают агонист PG рецептора и антагонист PG рецептора и др. Примеры PG рецептора включают PGE рецептор (EP1, EP2, EP3 и EP4), PGD рецептор, (DP, CRTH2), PGF рецептор (FP), PGI рецептор (IP) или TX рецептор (TP)и др.
Примеры ингибитора фосфодиэстеразы включают, например, ролипрам, циломиласт (торговая марка: Арифло), Bay 19-8004, NIK-616, рофлумиласт (BY-217), ципамфиллин (BGL-61063), атизолам (CP-80633), SCH-351591, YM-976, V-11294A, PD-168787, D-4396, IC-485, или ONO-6126 в качестве ингибитора PDE-4, и др.
Примерами других агентов для профилактики и/или лечения других аллергических заболеваний, например, астмы, используемых в сочетании с соединениями настоящего изобретения, являются стероиды, β2 адренорецептор стимулирующий агент, антагонист рецептора лейкотриена, ингибитор тромбоксансинтетазы, антагонист тромбоксан А2 рецептора, медиатор, высвобождающий ингибитор, антигистамины, производные ксантина, антихолинергический агент, ингибитор цитокина, простагландины, форсколин, ингибитор фосфодиэстеразы, ингибитор эластазы, ингибитор металлопротеиназы, отхаркивающий агент и антибиотик.
Примеры β2 адренорецептор стимулирующего агента включают гидробромид фенотерола, сульфат сальбутамола, сульфат тербуталина, фумарат формотерола, ксинафоат сальметерола, сульфат изопротенола, сульфат орципреналина, сульфат хлорпреналина, эпинефрин, гидрохлорид триметохинола, сульфат гексопреналинмезила, гидрохлорид прокатерола, гидрохлорид тулобетерола, тулобетерол, гидрохлорид пирбутерола, гидрохлорид кленбутерола, гидрохлорид мабутерола, гидрохлорид ритодрина, бамбутерол, гидрохлорид допексамина, тартрат мерадрина, AR-C68397, левосальбутамол, R,R-формотерол, KUR-1246, KUL-7211, AR-C89855 и S-1319 и др.
Примеры антагонистов рецептора лейкотриена включают пранлукастгидрат, монтелукаст, зафирлукаст, сератродаст, MCC-847, KCA-757, CS-615, YM-158, L-740515, CP-195494, LM-1484, RS-635, A-93178, S-36496, BIIL-284 и ONO-4057 и др.
Примеры ингибитора тромбоксансинтетазы включают гидрохлорид озагреля и имитродастнатрий и др.
Примеры антагониста тромбоксан А2 рецептора включают сератродаст, раматробан, кальцийдигидрат домитробана и KT-2-962 и др.
Примеры медиатор высвобождающего ингибитора включают траниласт, кромогликат натрия, анлексанокс, репиринаст, ибудиласт, тазаноласт и пемилоласткалий и др.
Примеры антигистаминов включают фурат кетотифена, меквитацин, гидрохлорид ацеластина, оксатомид, терфенадин, фумарат эмедастина, гидрохлорид эпинастина, астемизол, эбастин, гидрохлорид цетиризина, бепотастин, фексофенадин, лолатадин, дезлолатадин, гидрохлорид олопатадина, TAK-427, ZCR-2060, NIP-530, фуроат мометазона, мизоластин, BP-294, андоласт, ауранофин и акрибастин и др.
Примеры ксантиновых производных включают аминофиллин, теофилин, доксофиллин, ципамфиллин и дипрофиллин и др.
Примеры антихолинергического агента включают бромид ипратропия, бромид окситропия, бромид флутропия, темиверин, бромид тиотропия и реватропат (UK-112166) и др.
Примеры ингибитора цитокина включают тозилат суплатаста (торговая марка: IPD) и др.
Примеры ингибиторов эластазы включают ONO-5046, ONO-6818, MR-889, PBI-1101, EPI-HNE-4, R-665, ZD-0892, ZD-8321, GW-311616, AE-3763 и др.
Примеры отхаркивающего средства включают нашатырный спирт, бикарбонат натрия, гидрохлорид бромгексина, карбоцистеин, амброксолгидрохлорид, гидрохлорид амброксола длительного или непрерывного высвобождения, гидрохлорид метилцистеина, ацетилцистеин, гидрохлорид L-этилцистеина и тилоксапол и др.
Примеры антибиотиков включают цефуроксимнатрий, тригидрат меропенема, сульфат нетильмицина, сульфат сизомицина, цефтибутен, PA-1806, IB-367, тобрамицин, PA-1420, доксорубицин, сульфат астромицина, или гидрохлорид цефетаметпивоксила и др.
Примеры антибиотиков как ингаляционного средства включают PA-1806, IB-367, тобрамицин, PA-1420, доксорубицин, сульфат астромицина, или гидрохлорид цефетаметпивоксила и др.
Другие фармацевтические средства, которые добавляют и/или усиливают профилактическое и/или лечебное действие соединения настоящего изобретения, не ограничиваются примерами, приведенными выше. Что касается других фармацевтических средств, которые добавляют и/или усиливают профилактическое и/или лечебное действие соединения настоящего изобретения, охватываются не только те средства, которые уже найдены до настоящего времени, но также и те, которые будет обнаружены в будущем на основе упомянутого выше механизма.
Номенклатура соединений настоящего изобретения описывается ниже.
Все соединения, описанные в настоящем описании, были названы с использованием ACD/наименование (зарегистрированная торговая марка, Advanced Chemistry Development Inc.) или ACD/наименование Batch (зарегистрированная торговая марка, Advanced Chemistry Development Inc.), или названы в соответствии с системой номенклатуры IUPAC. Например, соединение, представленное формулой
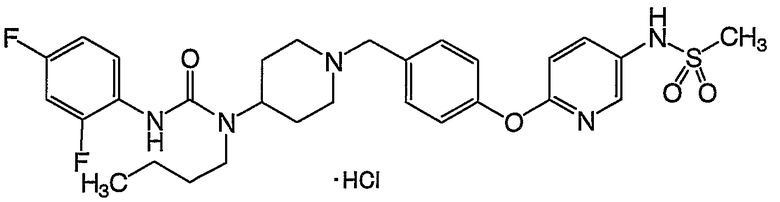
названо гидрохлорид N-[6-(4-{[4-(бутил{[(2,4-дифторфенил)амино]карбонил}амино)-1-пиперидинил]метил}фенокси)-3-пиридинил]метансульфонамида.
В настоящем описании “гидрохлорид (или дигидрохлорид)” означает или гидрохлорид или дигидрохлорид, и таким образом он не означает смесь гидрохлорида и дигидрохлорида. В настоящем описании “дигидрохлорид (или тригидрохлорид)” означает или дигидрохлорид, или тригидрохлорид, и таким образом он не означает смесь дигидрохлорида и тригидрохлорида. “·HCl или 2HCl” в структуре, описанной в настоящем описании, означает или HCl, или 2HCl, и таким образом он не охватывает смесь HCl и 2HCl. “·2HCl или 3HCl” в структуре, описанной в настоящем описании, означает или 2HCl, или 3HCl, и таким образом он не охватывает смесь 2HCl и 3HCl.
ЭФФЕКТ ИЗОБРЕТЕНИЯ
Соединения настоящего изобретения, представленные формулой (I), обладают антагонистической активностью против рецептора хемокина, особенно CCR5, поэтому они полезны в профилактике и/или лечении CCR5-связанных заболеваний.
Тот факт, что соединение настоящего изобретения проявляет CCR5 антагонизм, демонстрируется, например, следующим экспериментом. Общая операция основывается на основных методах генной инженерии приготовления высоко экспрессирующих ген клеток и используются обычные методы. В способе анализа настоящего изобретения по оценке соединения настоящего изобретения улучшается также точность измерения и/или чуствительность измерения, как описано ниже. Подробные эксперементальные методы показаны ниже.
(I) Испытание по ингибированию связывания RANTES и CCR5
Выделение CCR5 гена человека
Приготавливается плацентарная кДНК человека с использованием кДНК амплификационного комплекта Marathon (Clontech). PCR праймеры hCCR5Xbal-F1:
5'-AGCTAGTCTAGATCCGTTCCCCTACAAGAAACTCTCC-3' (SEQ ID NO:1) и hCCR5Xbal-R1:
5'-AGCTAGTCTAGAGTGCACAACTCTGACTGGGTCACCA-3' (SEQ ID NO:2) обзначаются на основе последовательности ГенБанка U54994.
Используя человеческую плацентарную кДНК в качестве шаблона и используя Ex Taq (Takara), осуществляют реакцию PCR (2 минуты при 95°С → (30 секунд при 95°С, 45 секунд при 60°С, 1 минута при 72°С) х 35 раз). Амплифицированный таким образом PCR продукт подвергают 1% агарозному гель-электрофорезу, очищают с использованием QIAquick гель-экстракционного комплекта (QUIAGEN), а затем ферментативно гидролизуют с ферментом рестрикции XbaI. Гидролизованные фрагменты лигируют с вектором экспрессии PEF-BOS-bsr с использованием ДНК комплекта лигирования Ver. 2 (Takara) и трансформируют в Escherichia coli DH5α. Путем приготовления получающейся плазмиды pEF-BOS-bsr/hCCR5 поверяют ее ДНК последовательность.
(2) Культивирование СНО клеток
CHO-dhfr(-) выращивают с использованием Ham's F-12 (содержащей плодную бычью сыворотку (10%), пенициллин (50 Ед/мл) и стрептомицин (50 мг/мл)). С помощью добавления в указанную выше среду бластицидина (5 мг/мл) выращивают также трансдуцированные клетки.
(3) Трансдукция в CHO клетки
Плазмида PEF-BOS-bsr/hCCR5 трансдуцируется в CHO-dhfr(-) клетку с использованием DMRIE-C реагента (Gibco BRL). Через 48 часов среда замещается средой, содержащей 5 мг/мл бластицидина для осуществления отбора, устанавливая таким образом стабильно сверхэксперссирующие клетки.
(4) Испытание ингибирования связывания хемокина (RANTES, MIP-1α и MIP-1β) с CCR5 (активность хемокина вызывать переменное увеличение Са ионов).
Созданные таким образом стабильные CHO клетки, сверхэкспрессирующие CCR5 человека (CCR5/CHO клетки), суспендируют в среде Ham's F-12, содержащей FBS (10%), и высевают с плотностью 3,0×106 клеток/лунку на 96-луночной планшете. Спустя один день, после культивирования при 37°С супернатант культуры отбрасывают, и среду Ham's F-12 (содержащую Fura-2AM (5 мкМ), Пробенецид (2,5 мМ) и HEPES (20 мМ; рН 7,4)) распределяют частями по 80 мкл/лунку для осуществления 1-часовой инкубации при 37°С в условиях затенения. После промывки дважды раствором 1x Hanks/HEPES (20 мМ; рН 7,4) тот же самый раствор распределяют частями по 100 мкл/лунку. Каждое из испытуемых соединений добавляют к CCR5/CHO клеток с включенным таким образом Fura-2AM и через 3 минуты после этого добавляют туда рекомбинантный человеческий CCR5 лиганд (RANTES, MIP-1α или MIP-1β) (Pepro Tach), разбавленный раствором 1x Hanks/HEPES (20 мМ; рН 7,4), до конечной концентрации (Rantes: 10 нМ;; MIP-1α: 30 нМ; MIP-1β: 30 нМ). Временное увеличение концентрации внутриклеточного Са2+, индуцированное CCR5 лигандом человека, измеряют с использованием Са2+ детектора для 96-луночного использования (Hamamatsu Photonics), и степень ингибирования (%) испытуемого соединения вычисляют с помощью следующей формулы:
Степень ингибирования = (Ec - Ea)/Ec x 100
Ec: измеренная величина временного увеличения Са2+ с помощью CCR5 лиганда
Ea: измеренная величина временного увеличения Са2+ с помощью CCR5 лиганда с добавлением испытуемого соединения.
(II) Испытание миграции человеческих CCR5 экспрессирующих клеток (hCCR5-Ba/F3 клетку):
(1) Создание человеческих CCR5 экспрессирующих клеток
(1-A) Выделение CCR5 гена человека
Выделение осуществляют в соответствии с методикой изоляции CCR5 гена человека, как описано в приведенном выше способе (I)-(1).
(1-B) Выращивание Ba/F3 клеток
Ba/F3 клетки культивируют статически с использованием среды RMMI-1640 (Gibco BRL), содержащей антибиотики (Антибиотик-Антимикотик) (конечная концентрация: пенициллин G натрий (100 Ед./мл), сульфат стрептомицина (100 мкг/мл), амфотерицин В (0,25 мкг/мл) (Gibco BRL), плодная бычья сыворотка (FBS) (10%), 2-меркаптоэтанол (55 мкМ), мышиный интерлейкин-3 (IL-3) (5 нг/мл) (Pepro Tech, Inc.) в диоксидуглеродном инкубаторе (температура: 37°С, концентрация СО2: 5%, влажность: 95%). Стабильные гиперэкспрессионные клетки экзогенного гена выращивают в описанной выше среде, к которой добавляют бластицидин (Kaken Pharmaceutical) с получением конечной концентрации 10 мкг/мл.
(1-C) Трансформация в Ba/F3 клетки
Плазмиду для экспресии CCR5 человека (pEF-BOS-bsr/hCCR5) гидролизуют с помощью AatII для перевода в линейную форму. Переведенная в линейную форму плазмида очищается с помощью QIA комплекса быстрой PCR очистки (QIAGEN) и вводится в Ba/F3 клетки с помощью электропорации (Gene Pulser (BIO RAD), 960 мкF/250V). Клетки высевают на 96-луночную планшету для культивирования при плотности 1000, 100, 10 клеток/100 мкл/лунку и выращивают в течение 48 часов. Затем туда добавляют бластицидин для получения конечной концентрации 10 мкг/мл с последующим клонированиеми бластицидин-устойчивой линии клеток, создавая тем самым сверхэкспрессирующий стабильный клон трансфицированный экзогенный ген (hCCR5-Ba/F3 клетки).
(1-D) Анализ экспрессии CCR5
Уровень экспрессии CCR5 человека в клоне, полученном по способу, описанному выше (1-С), определяют с помощью FAC Sort (торговое наименование, Becton, Dickinson) с помощью детектирования клеток с флуоресценцией изотиоцианат (FITC)-меченых античеловеческих CCR5 антител (BD Pharmingen) и анализируют. В данной связи в качестве контрольного антитела изотипа используют FITC-меченый мышиный IgG2aκ (BD Pharmingen).
(2) Испытание миграции клеток
Проверяют влияние испытуемых соединений на миграционную способность CCR5 экспрессирующих Ba/F3 клеток человека против RANTES, MIP-1α или MIP-1β. Сначала добавляют соответственно 0,3 мл 0 или 3 нМ хемокин (RANTES, MIP-1α или MIP-1β)-содержащей среды в нижнее простанство Chemo T x 96 луночной планшеты (Neuro Probe). Затем устанавливают фильтр (размер пор: 5 мкм) и добавляют раствор смеси (1×105 клеток/лунку) испытуемого соединения и приготовленных заранее CCR5-Bs/F3 клеток при 65 мкл. Добавляемое испытуемое соединение получают разбавлением его 0,1% ДМСО-содержащей средой для получения конечной концентрации на фильтре 0, 0,01, 0,03, 0,1 или 0,3 мкМ. Данные клетки выращивают в СО2 инкубаторе (37°С, 5% СО2, относительная влажность: 95%) в течение 3 часов, а затем удаляют среду и немигрировавшие клетки на фильтре. Кроме того, удаляют фильтр, центрифугируют микропланшету (1500 об. в мин, 10 минут, комн. темп.) и с помощью декантации удаляют супернатант. Клетки на микропланшете суспендируются в 100 мкл фосфатного буфера (PBS), и 1/10 часть его дополнительно разбавляется 90 мкл PBS, передвигают на белую планшету для анализа флуоресценции и используют в качестве аналитического образца для количества мигрировавших клеток (конечный: 100 мкл/лунку).
Затем Titer-Glo реагент клеток (торговое наименование, Promega), который получают предварительно при комнатной температуре, добавляют к указанному выше аналитическому образцу на количество мигрировавших клеток (100 мкл/лунку), и последующим осторожным смешиванием (300 об. в мин, 2 минуты с KA-SCHUTTLER MTS4) для лизирования клеток, смесь инкубируют при комнатной температуре в течение 10 минут и измеряют флуоресценцию с помощью wallac ARVO SX 1420 MULTILABEL COUNTER (торговое наименование, Perkin Elmer) (детекция с помощью подсчет/секунду).
Количество мигрировавших клеток (количество естественно падающих клеток) при концентрации хемокина 0 нмоль/л используется в качестве основы, и вычисляется ингибирующая степень испытуемого соединения против 0,1% ДМСО контрольной группы.
Степень ингибирования миграции (%) испытуемого соединения вычисляется с помощью следующего уравнения:
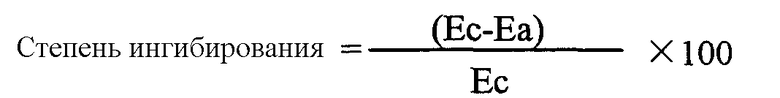
Ec: (величина флуоресценции, измеренная при добавлении 0,1% ДМСО)-(измеренная величина флуоресценции естественно падающих клеток)
Ea: (величина флуоресценции, измеренная при добавлении испытуемого соединения)-(измеренная величина флуоресценции естественно падающих клеток).
НАИЛУЧШИЙ СПОСОБ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Следующие примеры получения, биологические примеры и примеры готовых форм предназначены для иллюстрации настоящего изобретения, но не для ограничения ими.
При хроматографических разделениях и ТСХ, растворители в скобках показывают элюирующие и проявляющие растворители, а соотношения используемых растворителей даны по объему.
ЯМР представляет измеренную величину 1Н ЯМР. Растворители в скобках в данных ЯМР показывают растворители, используемые для измерения.
Пример получения
Пример 1
N-[6-(4-формилфенокси)пиридин-3-ил]метансульфонамид
{4-[(5-нитропиридин-2-ил)окси]фенил}метанол подвергали восстановлению нитро группы с использованием цинка и уксусной кислоты, полученное соединение подвергали реакции с метансульфонилхлоридом в пиридине и полученное соединение подвергали окислению с использованием двуокиси марганца, с получением указанного в заголовке соединения, имеющего следующие физические данные.
ТСХ: Rf 0,67 (дихлорметан: метанол = 9: 1);
ЯМР (CDCl3): δ 3,04, 6,56, 7,05, 7,29, 7,80, 7,94, 8,08, 9,99.
Пример 2
Гидрохлорид N-бутил-N'-(2,4-дифторфенил)-N-пиперидин-4-илмочевины
К раствору трет-бутил 4-(бутиламино)пиперидин-1-карбоксилата (1 г) в диметилацетамиде (13 мл) добавляли триэтиламин (1,6 мл) и 2,4 дифторфенилизоцианат (907 мг). Реакционную смесь перемешивали в течение 5 минут при комнатной температуре. К реакционной смеси добавляли насыщенный водный раствор кислого углекислого натрия и экстрагировали этилацетатом. Экстракт промывали водой и солевым раствором, сушили безводным сульфатом натрия и концентрировали. К раствору полученного соединения (1,28 г) в этилацетате (2 мл) добавляли 4 н. хлористый водород в растворе этилацетата (10 мл). Реакционную смесь перемешивали в течение 20 минут при комнатной температуре и концентрировали. Полученный остаток промывали трет-бутилметиловым эфиром, сушили, с получением указанного в заголовке соединения, имеющего следующие физические данные.
ТСХ:Rf 0,52 (дихлорметан: метанол: уксусная кислота= 5:1:0,1);
ЯМР (CD3OD): δ 0,99, 1,34-1,47, 1,60-1,71, 1,95-2,01, 2,08-2,22, 3,03-3,13, 3,27-3,34, 3,44-3,50, 4,13, 7,00, 7,37, 8,01.
Пример 3
Гидрохлорид (или дигидрохлорид) N-[6-(4-{[4-(бутил{[2,4-дифторфенил)амино]карбонил}амино)-1-пиперидинил]метил}фенокси)-3-пиридинил]метансульфонамида
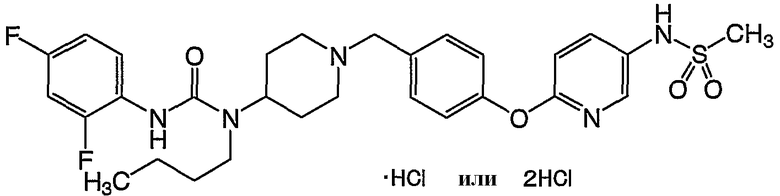
К раствору соединения, полученного в Примере 1 (95 мг), и соединения, полученного в Примере 2 (80 мг) в диметилформамиде (1,5 мл), добавляли уксусную кислоту (0,15 мл) и триацетоксиборгидрид натрия (116 мг). Реакционную смесь перемешивали в течение 18 часов при комнатной температуре. Реакционную смесь дополняли насыщенным водным раствором кислого углекислого натрия и экстрагировали этилацетатом. Экстракт сушили безводным сульфатом натрия и концентрировали. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат: метанол = 10:1). К раствору полученного соединения добавляли 4 н. хлористый водород в растворе этилацетата. Реакционную смесь концентрировали, с получением указанного в заголовке соединения (115 мг), имеющего следующие физические данные.
ТСХ:Rf 0,44 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,35-1,48, 1,58-1,70, 1,95-2,08, 2,18-2,34, 3,00, 3,08-3,20, 3,25-3,34, 3,57-3,65, 4,19, 4,34, 6,89-7,03, 7,09, 7,25, 7,38, 7,60, 7,85, 8,06.
Пример 3(1)-3(107)
С помощью процедуры, аналогичной описанной в Примере 3, с использованием соответствующих аминовых соединений и соответствующих альдегидных соединений, с получением следующих соединений по настоящему изобретению.
Пример 3(1)
Гидрохлорид (или дигидрохлорид) N-{4-[(6-{[4-(бутил{[(2,4-дифторфенил)амино]карбонил}амино)-1-пиперидинил]метил}-3-пиридинил)окси]фенил}метансульфонамида
ТСХ:Rf 0,30 (хлороформ: метанол =10:1);
ЯМР (CD3OD): δ 0,99, 1,30-1,50, 1,60-1,80, 1,90-2,10, 2,20-2,40, 2,97, 3,20-3,40, 3,60-3,70, 4,20, 4,47, 6,92-7,02, 7,09-7,12, 7,31-7,40, 7,47-7,58, 8,45.
Пример 3(2)
Гидрохлорид N-{4-[4-({4-[{[(2-гидроксибутил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)фенокси]фенил}метансульфонамида
ТСХ:Rf 0,41 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,89, 1,20-1,42, 1,55-1,70, 2,05-2,17, 2,95, 3,08-3,28, 3,37-3,50, 4,21, 4,51, 7,00, 7,02, 7,21-7,30, 7,41, 7,44-7,55.
Пример 3(3)
Дигидрохлорид N-{4-[4-({4-[бутил({[1-(2-гидроксиэтил)-1H-пиразол-4-ил]амино}карбонил)амино]-1-пиперидинил}метил)фенокси]фенил}метансульфонамида
ТСХ:Rf 0,40 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,31-1,42, 1,50-1,72, 1,91-2,01, 2,15-2,31, 2,95, 3,10-3,32, 3,51-3,60, 3,87, 4,23, 4,30, 4,35, 7,03, 7,06, 7,29, 7,53, 7,98, 8,12.
Пример 3(4)
Гидрохлорид 5-[({бутил[1-(4-{4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифтор-N-метилбензамида
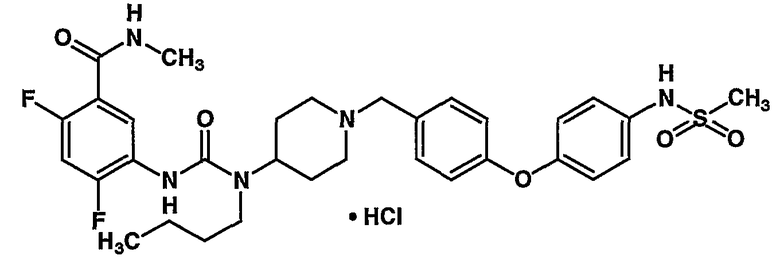
ТСХ:Rf 0,90 (хлороформ: метанол= 4:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,50, 1,60-1,70, 1,90-2,10, 2,10-2,30, 2,91, 2,95, 3,00-3,20, 3,20-3,40, 3,50-3,60, 4,15, 4,29, 7,02-7,09, 7,12, 7,29, 7,50, 7,78.
Пример 3(5)
Гидрохлорид N-{4-[4-({4-[{[(транс-4-гидроксициклогексил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)фенокси]фенил}метансульфонамида
ТСХ:Rf 0,46 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,00-1,18, 1,21-1,37, 1,55-1,68, 1,71-1,89, 2,04-2,15, 2,95, 3,04-3,18, 3,38-3,54, 4,21, 4,60, 6,98-7,07, 7,18-7,23, 7,28, 7,41, 7,45-7,53.
Пример 3(6)
Гидрохлорид N-[4-(4-{[4-(3-бутенил{[(2-гидроксибутил)амино]карбонил}амино)-1-пиперидинил]метил}фенокси)фенил]метансульфонамида
ТСХ:Rf 0,51 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,95, 1,30-1,58, 1,90-2,00, 2,07-2,24, 2,28-2,38, 2,95, 3,02-3,35, 3,50-3,60, 4,12, 4,28, 5,05, 5,11, 5,81, 7,03, 7,06, 7,29, 7,50.
Пример 3(7)
Гидрохлорид N-бутил-N'-(2,4-дифторфенил)-N-(1-{4-[4-(4-морфолинилсульфонил)фенокси]бензил}-4-пиперидинил)мочевины
ТСХ:Rf 0,60 (дихлорметан: метанол= 20:1);
ЯМР (CD3OD): δ 0,99, 1,39-1,43, 1,60-1,70, 2,00-2,05, 2,16-2,30, 2,94-2,97, 3,06-3,28, 3,29-3,36, 3,52-3,61, 3,69-3,72, 4,13, 4,23, 6,90-7,03, 7,20, 7,23, 7,37, 7,58, 7,78.
Пример 3(8)
Гидрохлорид N-бутил-2-(2,4-дифторфенил)-N-[1-(4-{4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]ацетамида
ТСХ:Rf 0,41 (хлороформ: метанол= 10:1);
ЯМР (d6-DMSO): δ 0,92, 1,20-1,40, 1,40-1,60, 1,70-1,90, 2,20-2,40, 2,90-3,10, 2,97, 3,15-3,30, 3,30-3,50, 3,71, 4,05-4,30, 6,94-7,09, 7,12-7,25, 7,57, 9,34, 10,50.
Пример 3(9)
Дигидрохлорид (или тригидрохлорид) N-{4-[(5{[4-(бутил{[(1-метил-1H-пиразол-4-ил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]фенил}метансульфонамида
ТСХ:Rf 0,16 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,96, 1,30-1,45, 1,50-1,65, 1,90-2,05, 2,20-2,35, 2,98, 3,10-3,40, 3,50-3,70, 4,00, 4,20, 4,36, 7,09-7,16, 7,32, 7,95, 8,06, 8,08, 8,31.
Пример 3(10)
Гидрохлорид N-(4-{4-[(4-{{[(4-фторфенил)амино]карбонил}[4-(метилсульфанил)фенил]амино}-1-пиперидинил)метил]фенокси}фенил)метансульфонамида
ТСХ:Rf 0,67 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,60-1,79, 2,10-2,20, 2,51, 2,95, 3,08-3,20, 3,42-3,55, 4,22, 4,64, 6,95, 7,02, 7,03, 7,15-7,31, 7,39, 7,42.
Пример 3(11)
Гидрохлорид N-(4-{4-[(4-{{[(4-фторфенил)амино]карбонил}[3-(метилсульфанил)фенил]амино}-1-пиперидинил)метил]фенокси}фенил)метансульфонамида
ТСХ:Rf 0,67 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,62-1,80, 2,12-2,20, 2,51, 2,95, 3,04-3,22, 3,42-3,57, 4,22, 4,64, 6,89-7,10, 7,17-7,32, 7,34-7,49.
Пример 3(12)
Гидрохлорид N-бутил-2,4-дифтор-N-[1-(4-{4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]бензамида
ТСХ:Rf 0,41 (хлороформ: метанол= 10:1);
ЯМР (d6-DMSO): δ 0,70-0,90, 1,10-1,30, 1,40-1,60, 1,75-1,90, 2,30-2,55, 2,80-3,05, 2,96, 3,10-3,45, 4,00, 4,17, 7,00, 7,01-7,04, 7,12, 7,19-7,30, 7,42, 7,57, 9,35.
Пример 3(13)
Гидрохлорид N-(4-{4-[(4-{{[(4-фторфенил)амино]карбонил}[4-(метилсульфинил)фенил]амино}-1-пиперидинил)метил]фенокси}фенил)метансульфонамида
ТСХ:Rf 0,47 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,67-1,83, 2,14-2,23, 2,84, 2,95, 3,10-3,21, 3,46-3,55, 4,23, 4,67, 6,96, 7,00, 7,02, 7,23, 7,28, 7,43, 7,54, 7,84.
Пример 3(14)
Гидрохлорид N-(4-{4-[(4-{{[(4-фторфенил)амино]карбонил}[3-(метилсульфинил)фенил]амино}-1-пиперидинил)метил]фенокси}фенил)метансульфонамида
ТСХ:Rf 0,47 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,62-1,80, 2,14-2,25, 2,86, 2,95, 3,08-3,21, 3,47-3,55, 4,23, 4,66, 6,96, 7,01, 7,02, 7,20-7,30, 7,42, 7,51, 7,66, 7,70-7,80.
Пример 3(15)
Гидрохлорид N-(4-{4-[(4-{{[(4-фторфенил)амино]карбонил}[4-(метилсульфонил)фенил]амино}-1-пиперидинил)метил]фенокси}фенил)метансульфонамида
ТСХ:Rf 0,54 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,70-1,88, 2,14-2,23, 2,95, 3,10-3,20, 3,16, 3,46-3,55, 4,23, 4,64, 6,96, 7,01, 7,02, 7,24, 7,28, 7,43, 7,57, 8,08.
Пример 3(16)
Гидрохлорид N-(4-{4-[(4-{{[(4-фторфенил)амино]карбонил}[3-(метилсульфонил)фенил]амино}-1-пиперидинил)метил]фенокси}фенил)метансульфонамида
ТСХ:Rf 0,54 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,64-1,80, 2,17-2,28, 2,95, 3,10-3,21, 3,19, 3,45-3,55, 4,23, 4,67, 6,96, 7,01, 7,02, 7,24, 7,28, 7,42, 7,66, 7,78, 7,89, 8,05.
Пример 3(17)
Гидрохлорид N-[4-(4-{[4-(бутил{[(2,4-дифторфенил)амино]карбонил}амино)-1-пиперидинил]метил}фенокси)-3-метоксифенил]метансульфонамида
ТСХ:Rf 0,50 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,50, 1,60-1,70, 1,90-2,10, 2,15-2,30, 2,99, 3,05-3,20, 3,20-3,40, 3,50-3,60, 3,74, 4,15, 4,25, 6,85-6,95, 6,99, 7,03, 7,38, 7,43.
Пример 3(18)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида
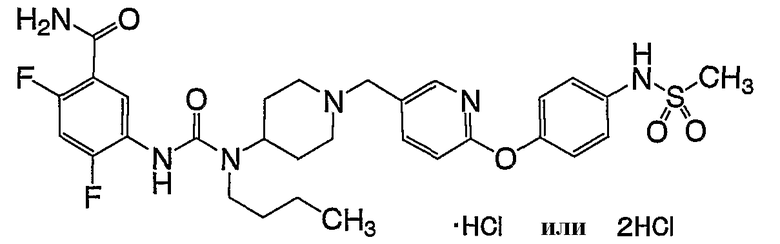
ТСХ:Rf 0,41 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,98, 1,30-1,45, 1,55-1,70, 1,95-2,10, 2,15-2,35, 2,98, 3,05-3,20, 3,25-3,35, 3,50-3,65, 4,15, 4,34, 7,09-7,18, 7,33, 7,86, 8,03, 8,28.
Пример 3(19)
Дигидрохлорид 5-{[(бутил{1-[(5-{4-[(метилсульфонил)амино]фенокси}-2-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида
ТСХ:Rf 0,36 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,99, 1,30-1,50, 1,60-1,70, 1,90-2,10, 2,20-2,40, 2,96, 3,20-3,40, 3,60-3,70, 4,20, 4,45, 7,10, 7,15, 7,33, 7,44-7,50, 7,87, 8,44.
Пример 3(20)
Гидрохлорид 5-[({бутил[1-(4-{2-метокси-4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида
ТСХ:Rf 0,34 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,50, 1,55-1,70, 1,90-2,10, 2,10-2,30, 2,99, 3,05-3,20, 3,20-3,40, 3,50-3,60, 3,74, 4,15, 4,25, 6,87, 6,92, 7,03, 7,14, 7,42, 7,85.
Пример 3(21)
Гидрохлорид 5-[({бутил[1-(4-{2-хлор-4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида
ТСХ:Rf 0,33 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,50, 1,55-1,70, 1,90-2,10, 2,10-2,30, 3,01, 3,10-3,20, 3,25-3,35, 3,50-3,60, 4,15, 4,28, 6,99, 7,13, 7,14, 7,24, 7,43, 7,50, 7,85.
Пример 3(22)
Гидрохлорид 4-(4-{[4-(бутил{[(2,4-дифторфенил)амино]карбонил}амино)-1-пиперидинил]метил}фенокси)-N-(2-гидроксиэтил)бензолсульфонамида
ТСХ:Rf 0,69 (дихлорметан: метанол= 10:1);
ЯМР (CD3OD): δ 0,98, 1,36-1,43, 1,59-1,70, 1,98-2,03, 2,18-2,30, 2,96, 3,09-3,30, 3,54, 3,54-3,61, 4,16, 4,33, 6,90-7,03, 7,16, 7,20, 7,37, 7,59, 7,86.
Пример 3(23)
Дигидрохлорид 4-(4-{[4-(бутил{[(2,4-дифторфенил)амино]карбонил}амино)-1-пиперидинил]метил}фенокси)-N-[2-(диметиламино)этил]бензолсульфонамида
ТСХ:Rf 0,56 (дихлорметан: метанол= 2:1);
ЯМР (CD3OD): δ 0,98, 1,33-1,46, 1,59-1,70, 1,96-2,00, 2,20-2,35, 2,93, 3,05-3,12, 3,17-3,30, 3,52-3,56, 4,18, 4,30, 6,89-7,03, 7,19, 7,37, 7,61, 7,90.
Пример 3(24)
Гидрохлорид N-{4-[4-({4-[{[(2,4-дифторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)фенокси]фенил}метансульфонамида
ТСХ:Rf 0,76 (этил ацетат: метанол= 10:1);
ЯМР (CD3OD): δ 1,60-1,80, 2,10-2,30, 2,95, 3,05-3,20, 3,40-3,55, 4,21, 4,65, 6,85-6,96, 6,99-7,04, 7,28, 7,35-7,40, 7,41, 7,51-7,58.
Пример 3(25)
Гидрохлорид 4-(4-{[4-(бутил{[(2,4-дифторфенил)амино]карбонил}амино)-1-пиперидинил]метил}фенокси)-N-метилбензолсульфонамида
ТСХ:Rf 0,63 (этил ацетат: метанол= 10:1);
ЯМР (CD3OD): δ 0,98, 1,36-1,46, 1,59-1,70, 1,99-2,04, 2,17-2,30, 2,53, 3,07-3,17, 3,24-3,35, 3,57-3,61, 4,15, 4,33, 6,89-7,03, 7,16, 7,20, 7,36, 7,57, 7,83.
Пример 3(26)
Гидрохлорид 4-(4-{[4-(бутил{[(2,4-дифторфенил)амино]карбонил}амино)-1-пиперидинил]метил}фенокси)-N,N-диметилбензолсульфонамида
ТСХ:Rf 0,67 (этил ацетат: метанол= 10:1);
ЯМР (CD3OD): δ 0,98, 1,34-1,46, 1,60-1,70, 1,99-2,03, 2,19-2,30, 2,68, 3,09-3,17, 3,25-3,36, 3,57-3,61, 4,16, 4,33, 6,89-7,03, 7,18, 7,21, 7,36, 7,59, 7,78.
Пример 3(27)
Гидрохлорид 4-(4-{[4-(бутил{[(2,4-дифторфенил)амино]карбонил}амино)-1-пиперидинил]метил}фенокси)-N-(2-метоксиэтил)бензолсульфонамида
ТСХ:Rf 0,60 (этил ацетат: метанол= 10:1);
ЯМР (CD3OD): δ 0,98, 1,34-1,46, 1,60-1,70, 1,99-2,03, 2,19-2,30, 3,03, 3,09-3,17, 3,26, 3,26-3,30, 3,36, 3,56-3,61, 4,16, 4,33, 6,89-7,03, 7,14, 7,19, 7,37, 7,57, 7,85.
Пример 3(28)
Гидрохлорид 4-(4-{[4-(бутил{[(2,4-дифторфенил)амино]карбонил}амино)-1-пиперидинил]метил}фенокси)-N-тетрагидро-2H-пиран-4-илбензолсульфонамида
ТСХ:Rf 0,57 (этил ацетат: метанол= 10:1);
ЯМР (CD3OD): δ 0,98, 1,36-1,53, 1,63-1,68, 2,01-2,04, 2,21-2,25, 3,07-3,37, 3,57-3,61, 3,81-3,85, 4,14, 4,33, 4,80, 6,89-7,03, 7,14, 7,19, 7,36, 7,57, 7,87.
Пример 3(29)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
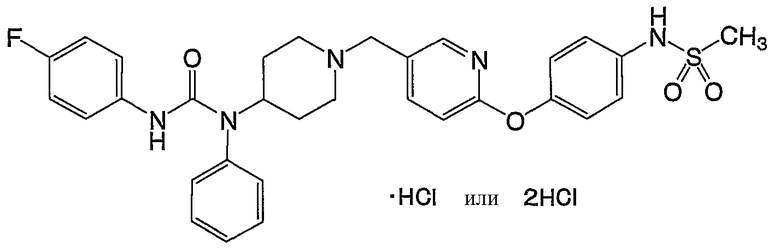
ТСХ:Rf 0,53 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,60-1,80, 2,12-2,23, 2,97, 3,11-3,24, 3,48-3,58, 4,27, 4,67, 6,95, 7,06, 7,11, 7,21, 7,28-7,35, 7,48-7,60, 7,90, 8,18.
Пример 3(30)
Гидрохлорид N-[5-(4-{[4-(бутил{[(2,4-дифторфенил)амино]карбонил}амино)-1-пиперидинил]метил}фенокси)-2-пиридинил]метансульфонамида
ТСХ:Rf 0,53 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,34-1,44, 1,58-1,68, 1,96-2,05, 2,15-2,31, 3,03-3,18, 3,28, 3,25-3,33, 3,52-3,60, 4,17, 4,30, 6,88-7,04, 7,12, 7,14, 7,37, 7,51-7,60, 8,10.
Пример 3(31)
Гидрохлорид 5-({[бутил(1-{4-[4-(4-морфолинилсульфонил)фенокси]бензил}-4-пиперидинил)амино]карбонил}амино)-2,4-дифторбензамида
ТСХ:Rf 0,48 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,98, 1,30-1,50, 1,60-1,70, 1,90-2,10, 2,20-2,35, 2,96, 3,00-3,20, 3,20-3,40, 3,50-3,60, 3,71, 4,10, 4,33, 7,11-7,24, 7,59, 7,78, 7,87.
Пример 3(32)
Гидрохлорид 5-[({бутил[1-(4-{4-[(тетрагидро-2H-пиран-4-иламино)сульфонил]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида
ТСХ:Rf 0,40 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,98, 1,30-1,50, 1,60-1,70, 1,90-2,10, 2,20-2,30, 3,10-3,20, 3,20-3,40, 3,50-3,70, 3,80-3,90, 4,15, 4,33, 7,11-7,21, 7,60, 7,87, 7,88.
Пример 3(33)
Гидрохлорид 5-[({бутил[1-(4-{2,6-диметил-4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида
ТСХ:Rf 0,34 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,50, 1,60-1,70, 1,90-2,10, 2,08, 2,20-2,30, 2,99, 3,00-3,20, 3,20-3,40, 3,50-3,60, 4,15, 4,26, 6,86, 7,04, 7,14, 7,45, 7,85.
Пример 3(34)
Гидрохлорид 5-[({бутил[1-(4-{4-[метил(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида
ТСХ:Rf 0,40 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,98, 1,30-1,50, 1,60-1,70, 1,90-2,10, 2,15-2,30, 2,99, 3,00-3,20, 3,20-3,40, 3,30, 3,50-3,60, 4,15, 4,30, 7,05-7,18, 7,45, 7,52, 7,86.
Пример 3(35)
Гидрохлорид 5-[({бутил[1-(4-{4-[(метилсульфонил)амино]бензил}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида
ТСХ:Rf 0,33 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,50, 1,60-1,70, 1,90-2,10, 2,15-2,30, 2,91, 3,00-3,20, 3,20-3,40, 3,50-3,60, 3,98, 4,15, 4,27, 7,10-7,20, 7,34, 7,44, 7,85.
Пример 3(36)
Дигидрохлорид 5-{[(бутил{1-[(3,5-диметил-1-{4-[(метилсульфонил)амино]фенил}-1H-пиразол-4-ил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида
ТСХ:Rf 0,20 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,34-1,47, 1,60-1,72, 1,98-2,10, 2,27-2,50, 2,39, 2,43, 3,04, 3,12-3,40, 3,65-3,75, 4,24, 4,29, 7,15, 7,43, 7,49, 7,87.
Пример 3(37)
Гидрохлорид 5-({[(1-{4-[4-(аминосульфонил)фенокси]бензил}-4-пиперидинил)(бутил)амино]карбонил}амино)-2,4-дифторбензамида
ТСХ:Rf 0,33 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,35-1,47, 1,58-1,70, 1,97-2,08, 2,18-2,32, 3,08-3,20, 3,23-3,35, 3,52-3,63, 4,16, 4,33, 7,10-7,24, 7,58, 7,64, 7,90.
Пример 3(38)
Гидрохлорид 5-[({бутил[1-(4-{4-[(метиламино)сульфонил]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида
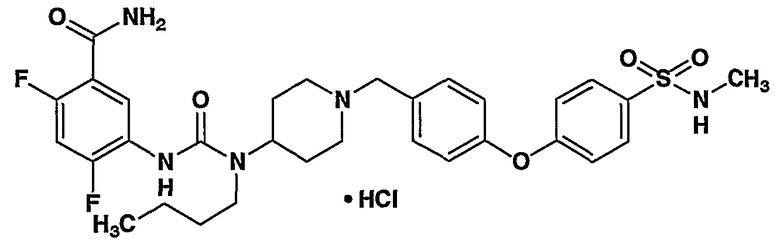
ТСХ:Rf 0,47 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,32-1,47, 1,60-1,71, 1,98-2,10, 2,20-2,36, 2,53, 3,08-3,20, 3,26-3,35, 3,52-3,64, 4,18, 4,33, 7,14, 7,16, 7,19, 7,60, 7,83, 7,86.
Пример 3(39)
Гидрохлорид 5-[({бутил[1-(4-{4-[(диметиламино)сульфонил]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида
ТСХ:Rf 0,55 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,32-1,49, 1,59-1,72, 1,97-2,09, 2,19-2,38, 2,68, 3,08-3,21, 3,23-3,35, 3,58-3,64, 4,16, 4,34, 7,14, 7,19, 7,21, 7,60, 7,79, 7,86.
Пример 3(40)
Гидрохлорид N-[4-(4-{[4-(бутил{[2,4-дифторфенил)амино]карбонил}амино)-1-пиперидинил]метил}фенокси)-3-метилфенил]метансульфонамида
ТСХ:Rf 0,39 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,50, 1,55-1,70, 1,90-2,10, 2,10-2,30, 2,16, 2,96, 3,00-3,20, 3,20-3,40, 3,50-3,60, 4,15, 4,27, 6,91-6,99, 7,13, 7,20, 7,36, 7,46.
Пример 3(41)
Гидрохлорид 5-[({бутил[1-(4-{2-метил-4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида
Белый аморфный порошок;
ТСХ:Rf 0,28 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,98, 1,30-1,50, 1,55-1,70, 1,90-2,10, 2,10-2,30, 2,16, 2,96, 3,00-3,20, 3,20-3,40, 3,50-3,60, 4,10, 4,26, 6,91-6,97, 7,11-7,20, 7,46, 7,86.
Пример 3(42)
Гидрохлорид 4-[4-({4-[({[5-(аминокарбонил)-2,4-дифторфенил]амино}карбонил)(бутил)амино]-1-пиперидинил}метил)фенокси]бензойной кислоты
ТСХ:Rf 0,49 (дихлорметан: метанол= 5:1);
ЯМР (CD3OD): δ 0,98, 1,35-1,45, 1,60-1,70, 1,98-2,03, 2,20-2,30, 3,10-3,34, 3,56-3,60, 4,16, 4,33, 7,07, 7,14, 7,18, 7,57, 7,86, 8,04.
Пример 3(43)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{2-хлор-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида
ТСХ:Rf 0,33 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,50, 1,55-1,70, 1,90-2,10, 2,20-2,40, 3,02, 3,10-3,25, 3,25-3,40, 3,50-3,60, 4,20, 4,35, 7,10-7,26, 7,43, 7,86, 8,09, 8,26.
Пример 3(44)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{2-метокси-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида
ТСХ:Rf 0,49 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,33-1,47, 1,58-1,71, 1,97-2,08, 2,20-2,38, 3,01, 3,07-3,21, 3,25-3,35, 3,55-3,65, 3,72, 4,18, 4,35, 6,90, 7,04-7,19, 7,86, 8,08, 8,29.
Пример 3(45)
Гидрохлорид 5-({[бутил(1-{4-[4-(метилсульфонил)фенокси]бензил}-4-пиперидинил)амино]карбонил}амино)-2,4-дифторбензамида
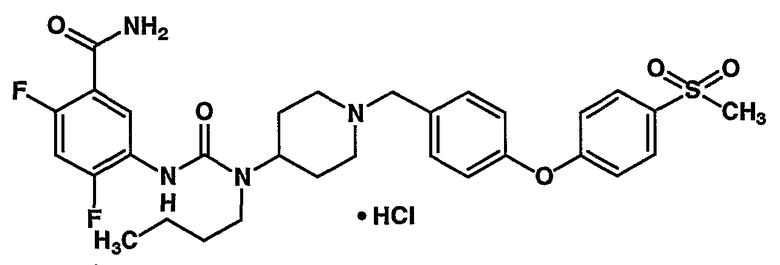
ТСХ:Rf 0,50 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,35-1,48, 1,59-1,70, 1,98-2,08, 2,19-2,34, 3,12, 3,08-3,21, 3,25-3,35, 3,55-3,64, 4,16, 4,34, 7,14, 7,21, 7,22, 7,61, 7,86, 7,95.
Пример 3(46)
Гидрохлорид 4-[4-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)фенокси]бензойной кислоты
ТСХ:Rf 0,49 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,67-1,80, 2,12-2,22, 3,12-3,24, 3,48-3,55, 4,26, 4,68, 6,95, 7,05, 7,14, 7,22, 7,33, 7,47-7,60, 8,03.
Пример 3(47)
Гидрохлорид 4-[4-({4-[({[5-аминокарбонил)-2,4-дифторфенил]амино}карбонил)(бутил)амино]-1-пиперидинил}метил)фенокси]-3-метоксибензойной кислоты
ТСХ:Rf 0,66 (хлороформ: метанол= 3:1);
ЯМР (CD3OD): δ 0,98, 1,30-1,50, 1,60-1,70, 1,90-2,10, 2,10-2,35, 3,05-3,20, 3,25-3,35, 3,50-3,60, 3,82, 4,10, 4,28, 6,98, 7,09, 7,15, 7,47, 7,77, 7,75, 7,86.
Пример 3(48)
Гидрохлорид 4-[4-({4-[({[5-(аминокарбонил)-2,4-дифторфенил]амино}карбонил)(бутил)амино]-1-пиперидинил}метил)фенокси]-3-хлорбензойной кислоты
ТСХ:Rf 0,65 (хлороформ: метанол= 3:1);
ЯМР (CD3OD): δ 0,98, 1,30-1,50, 1,60-1,70, 1,90-2,10, 2,20-2,35, 3,05-3,20, 3,25-3,35, 3,50-3,60, 4,10, 4,33, 7,10-7,17, 7,57, 7,86, 7,95, 8,14.
Пример 3(49)
Гидрохлорид 4-[4-({4-[({[5-(аминокарбонил)-2,4-дифторфенил]амино}карбонил)(бутил)амино]-1-пиперидинил}метил)фенокси]-3-нитробензойной кислоты
ТСХ:Rf 0,51 (хлороформ: метанол= 3:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,50, 1,60-1,70, 1,90-2,10, 2,20-2,35, 3,00-3,15, 3,20-3,35, 3,50-3,60, 4,15, 4,29, 7,10-7,20, 7,58, 7,86, 8,20, 8,56.
Пример 3(50)
Гидрохлорид 5-[({бутил[1-(4-{3-метокси-4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида
ТСХ:Rf 0,42 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,32-1,47, 1,58-1,70, 1,97-2,08, 2,17-2,31, 2,91, 3,06-3,20, 3,24-3,35, 3,51-3,63, 3,86, 4,13, 4,29, 6,57, 6,81, 7,10, 7,14, 7,36, 7,51, 7,86.
Пример 3(51)
Гидрохлорид 5-[({бутил[1-(4-{3-хлор-4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида
ТСХ:Rf 0,44 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,32-1,48, 1,60-1,72, 1,98-2,08, 2,12-2,31, 3,00, 3,08-3,20, 3,24-3,35, 3,52-3,62, 4,15, 4,31, 7,00, 7,10-7,20, 7,51-7,59, 7,86.
Пример 3(52)
Гидрохлорид (или дигидрохлорид) 5-({[бутил(1-{[6-(4-метоксифенокси)-3-пиридинил]метил}-4-пиперидинил)амино]карбонил}амино)-2,4-дифторбензамида
ТСХ:Rf 0,39 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,50, 1,60-1,70, 1,90-2,10, 2,20-2,35, 3,05-3,20, 3,20-3,35, 3,50-3,65, 3,81, 4,20, 4,34, 6,97-7,20, 7,86, 8,05, 8,31.
Пример 3(53)
Гидрохлорид (или дигидрохлорид) 4-{[5-({4-[({[5-(аминокарбонил)-2,4-дифторфенил]амино}карбонил)(бутил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}бензойной кислоты
ТСХ:Rf 0,63 (хлороформ: метанол= 3:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,45, 1,55-1,70, 1,85-2,00, 2,05-2,20, 2,65-2,85, 3,20-3,40, 4,05, 4,10, 7,09-7,21, 7,89, 7,97, 8,07, 8,23.
Пример 3(54)
Гидрохлорид N-(4-{4-[(4-{фенил[(тетрагидро-2H-пиран-4-иламино)карбонил]амино}-1-пиперидинил)метил]фенокси}фенил)метансульфонамида
ТСХ:Rf 0,46 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,24-1,40, 1,55-1,75, 2,05-2,15, 2,95, 3,04-3,18, 3,34-3,50, 3,68-3,84, 4,21, 4,60, 6,98-7,04, 7,22, 7,28, 7,41, 7,45-7,56.
Пример 3(55)
Дигидрохлорид 5-{[(бутил{1-[(5-{4-[(метилсульфонил)амино]фенокси}-2-пиразинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида
ТСХ:Rf 0,40 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,99, 1,34-1,48, 1,59-1,72, 1,98-2,08, 2,21-2,38, 2,97, 3,17-3,38, 3,62-3,71, 4,18, 4,46, 7,14, 7,18, 7,33, 7,67, 8,24, 8,54.
Пример 3(56)
Гидрохлорид 5-[4-({4-[({[5-(аминокарбонил)-2,4-дифторфенил]амино}карбонил)(бутил)амино]-1-пиперидинил}метил)фенокси]-2-[(метилсульфонил)амино]бензойной кислоты
ТСХ:Rf 0,48 (дихлорметан: метанол= 5:1);
ЯМР (CD3OD): δ 0,96, 1,28-1,47, 1,59-1,71, 1,95-2,06, 2,18-2,37, 3,02, 3,00-3,20, 3,24-3,35, 3,50-3,61, 4,15, 4,30, 7,08, 7,14, 7,25, 7,51, 7,67-7,72, 7,86.
Пример 3(57)
Гидрохлорид 2-[4-({4-[({[5-(аминокарбонил)-2,4-дифторфенил]амино}карбонил)(бутил)амино]-1-пиперидинил}метил)фенокси]-5-[(метилсульфонил)амино]бензойной кислоты
ТСХ:Rf 0,35 (дихлорметан: метанол= 5:1);
ЯМР (CD3OD): δ 0,98, 1,31-1,48, 1,54-1,71, 1,94-2,04, 2,12-2,36, 3,00, 3,00-3,18, 3,20-3,35, 3,51-3,61, 4,15, 4,27, 6,98, 7,08, 7,14, 7,41-7,52, 7,82, 7,84.
Пример 3(58)
Гидрохлорид N-[4-(4-{[4-(бутил{[(3,4-дицианофенил)амино]карбонил}амино)-1-пиперидинил]метил}фенокси)фенил]метансульфонамида
ТСХ:Rf 0,41 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,96, 1,31-1,42, 1,52-1,64, 1,98-2,07, 2,21-2,39, 2,95, 3,04-3,21, 3,28-3,35, 3,52-3,61, 4,19, 4,30, 7,03, 7,06, 7,29, 7,52, 7,79-7,89, 8,11.
Пример 3(59)
Гидрохлорид N-[4-(4-{[4-(бутил{[(4-циано-2,5-дифторфенил)амино]карбонил}амино)-1-пиперидинил]метил}фенокси)фенил]метансульфонамида
ТСХ:Rf 0,50 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,35-1,46, 1,55-1,68, 1,95-2,06, 2,19-2,37, 2,95, 3,08-3,21, 3,24-3,38, 3,52-3,61, 4,18, 4,29, 7,03, 7,06, 7,29, 7,50, 7,60, 7,87.
Пример 3(60)
Гидрохлорид (или дигидрохлорид) 5-({[бутил(1-{[6-(4-цианофенокси)-3-пиридинил]метил}-4-пиперидинил)амино]карбонил}амино)-2,4-дифторбензамида
ТСХ:Rf 0,54 (дихлорметан: метанол= 10:1);
ЯМР (CD3OD): δ 0,98, 1,36-1,43, 1,59-1,67, 2,00-2,04, 2,21-2,32, 2,99-3,18, 3,26-3,30, 3,56-3,63, 4,14, 4,36, 7,14, 7,21, 7,33, 7,80, 7,86, 8,06, 8,29.
Пример 3(61)
Гидрохлорид 3-({[[1-(4-{4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил](фенил)амино]карбонил}амино)бензамида
ТСХ:Rf 0,33 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,63-1,80, 2,14-2,23, 2,95, 3,10-3,22, 3,47-3,55, 4,23, 4,69, 7,01, 7,03, 7,25-7,37, 7,40-7,60, 7,72.
Пример 3(62)
Гидрохлорид 4-[({бутил[1-(4-{4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]бензамида
ТСХ:Rf 0,33 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,50, 1,50-1,70, 1,95-2,10, 2,10-2,30, 2,95, 3,00-3,20, 3,20-3,40, 3,50-3,60, 4,20, 4,30, 7,02-7,08, 7,29, 7,47-7,52, 7,80.
Пример 3(63)
Гидрохлорид N-{4-[4-({4-[бутил({[2,4-дифтор-5-(4-морфолинилкарбонил)фенил]амино}карбонил)амино]-1-пиперидинил}метил)фенокси]фенил}метансульфонамида
ТСХ:Rf 0,38 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,98, 1,30-1,50, 1,60-1,70, 1,95-2,05, 2,10-2,30, 2,95, 3,00-3,20, 3,20-3,50, 3,50-3,70, 3,70-3,80, 4,10, 4,29, 7,02-7,08, 7,15, 7,29, 7,46, 7,49.
Пример 3(64)
Гидрохлорид 5-[({бутил[1-(4-{4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифтор-N-(2-метоксиэтил)бензамида
ТСХ:Rf 0,44 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,98, 1,30-1,50, 1,60-1,75, 1,90-2,10, 2,15-2,35, 2,95, 3,00-3,20, 3,20-3,40, 3,50-3,60, 3,55, 4,13, 4,28, 7,02-7,08, 7,13, 7,29, 7,49, 7,78.
Пример 3(65)
Гидрохлорид 5-[({бутил[1-(4-{4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифтор-N,N-диметилбензамида
ТСХ:Rf 0,46 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,98, 1,30-1,50, 1,60-1,80, 1,90-2,10, 2,20-2,30, 2,95, 2,97, 3,05-3,20, 3,10, 3,25-3,35, 3,50-3,60, 4,15, 4,29, 7,02-7,08, 7,14, 7,29, 7,43, 7,50.
Пример 3(66)
Гидрохлорид 5-[({бутил[1-(4-{4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифтор-N-(2-гидроксиэтил)бензамида
ТСХ:Rf 0,38 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,98, 1,30-1,50, 1,60-1,70, 1,90-2,10, 2,10-2,30, 2,95, 3,05-3,20, 3,20-3,40, 3,50, 3,50-3,60, 3,67, 4,15, 4,27, 7,02-7,07, 7,13, 7,29, 7,50, 7,81.
Пример 3(67)
Дигидрохлорид (или тригидрохлорид) N-{4-[(5-{[4-(бутил{[(1-метил-1H-пиразол-4-ил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]-3-хлорфенил}метансульфонамида
ТСХ:Rf 0,57 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,96, 1,30-1,45, 1,50-1,65, 1,90-2,10, 2,20-2,40, 3,02, 3,10-3,50, 3,50-3,65, 4,08, 4,25, 4,37, 7,16, 7,24-7,26, 7,43, 8,12, 8,16, 8,23, 8,28.
Пример 3(68)
Дигидрохлорид (или тригидрохлорид) N-{4-[(5-{[4-(бутил{[(1-метил-1H-пиразол-4-ил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]-3,5-диметилфенил}метансульфонамида
ТСХ:Rf 0,56 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,96, 1,30-1,50, 1,50-1,65, 1,90-2,05, 2,08, 2,20-2,40, 2,98, 3,10-3,40, 3,55-3,65, 4,06, 4,25, 4,37, 7,05, 7,08, 8,13, 8,16, 8,20, 8,33.
Пример 3(69)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{2-метил-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида
ТСХ:Rf 0,43 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,32-1,45, 1,58-1,70, 1,95-2,07, 2,14, 2,20-2,40, 2,98, 3,08-3,21, 3,24-3,37, 3,55-3,64, 4,20, 4,36, 7,02-7,25, 7,86, 8,14, 8,34.
Пример 3(70)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{2,6-диметил-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида
ТСХ:Rf 0,44 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,32-1,45, 1,58-1,70, 1,95-2,08, 2,08, 2,21-2,39, 2,98, 3,08-3,21, 3,24-3,35, 3,55-3,65, 4,20, 4,36, 7,05, 7,08, 7,14, 7,86, 8,14, 8,33.
Пример 3(71)
Гидрохлорид 5-[({2-бутинил[1-(4-{4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида
ТСХ:Rf 0,52 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,82, 2,01-2,12, 2,12-2,31, 2,95, 3,08-3,19, 3,52-3,61, 4,10, 4,29, 4,32, 7,03, 7,06, 7,15, 7,29, 7,51, 7,96.
Пример 3(72)
Гидрохлорид 2,4-дифтор-5-({[[1-(4-{4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил](пропил)амино]карбонил}амино)бензамида
ТСХ:Rf 0,51 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,62-1,75, 1,98-2,08, 2,18-2,30, 2,95, 3,02-3,18, 3,21-3,33, 3,52-3,60, 4,14, 4,28, 7,03, 7,06, 7,14, 7,29, 7,50, 7,85.
Пример 3(73)
Гидрохлорид N-{4-[4-({4-[бутил({[2,4-дифтор-5-(гидроксиметил)фенил]амино}карбонил)амино]-1-пиперидинил}метил)фенокси]фенил}метансульфонамида
ТСХ:Rf 0,80 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,98, 1,30-1,50, 1,60-1,75, 1,90-2,10, 2,20-2,35, 2,96, 3,05-3,20, 3,20-3,40, 3,50-3,65, 4,20, 4,29, 4,60, 6,97, 7,03, 7,06, 7,29, 7,46, 7,52.
Пример 3(74)
Гидрохлорид (или дигидрохлорид) 2,4-дифтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(пентил)амино]карбонил}амино)бензамида
ТСХ:Rf 0,52 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,93, 1,28-1,45, 1,60-1,71, 1,97-2,08, 2,20-2,38, 2,98, 3,08-3,22, 3,25-3,35, 3,55-3,64, 4,18, 4,35, 7,09-7,20, 7,33, 7,86, 8,08, 8,31.
Пример 3(75)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида
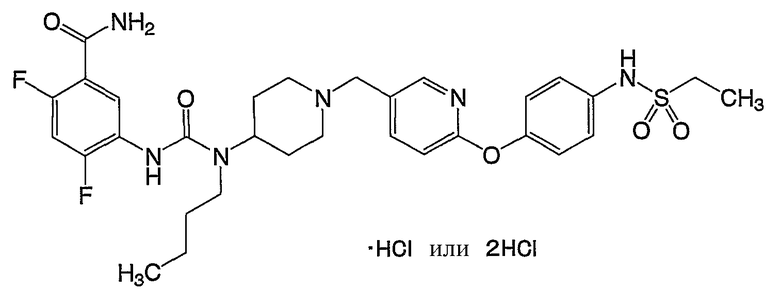
ТСХ:Rf 0,48 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,32, 1,28-1,45, 1,57-1,70, 1,95-2,08, 2,21-2,38, 3,11, 3,08-3,21, 3,25-3,35, 3,52-3,64, 4,18, 4,35, 7,07-7,17, 7,33, 7,86, 8,08, 8,31.
Пример 3(76)
Дигидрохлорид (или тригидрохлорид) N-(4-{[5-({4-[{[(1-метил-1-H-пиразол-4-ил)амино]карбонил}(пентил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,50 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,92, 1,28-1,42, 1,52-1,64, 1,92-2,04, 2,20-2,38, 2,98, 3,10-3,29, 3,52-3,64, 4,04, 4,24, 4,37, 7,11, 7,16, 7,34, 8,05, 8,12, 8,14, 8,34.
Пример 3(77)
Дигидрохлорид (или тригидрохлорид) N-{4-[(5-{[4-(бутил{[(1-этил-1H-пиразол-4-ил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]фенил}метансульфонамида
ТСХ:Rf 0,50 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,28-1,42, 1,52, 1,50-1,64, 1,90-2,02, 2,20-2,38, 2,98, 3,04-3,29, 3,51-3,64, 4,24, 4,30-4,44, 7,13, 7,16, 7,34, 8,05-8,16, 8,21, 8,34.
Пример 3(78)
Гидрохлорид (или дигидрохлорид) 5-[({бутил[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида
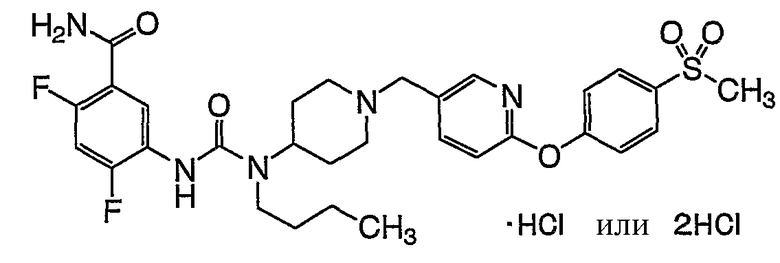
ТСХ:Rf 0,48 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,98, 1,30-1,50, 1,55-1,70, 2,00-2,10, 2,20-2,40, 3,05-3,20, 3,15, 3,25-3,40, 3,50-3,70, 4,20, 4,36, 7,14, 7,22, 7,40, 7,86, 8,01, 8,07, 8,29.
Пример 3(79)
Гидрохлорид (или дигидрохлорид) 2,4-дифтор-5-({[[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил](пентил)амино]карбонил}амино)бензамида
ТСХ:Rf 0,44 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,94, 1,30-1,45, 1,60-1,75, 2,00-2,10, 2,15-2,40, 3,00-3,20, 3,15, 3,20-3,40, 3,50-3,70, 4,15, 4,35, 7,14, 7,22, 7,39, 7,86, 8,01, 8,05, 8,29.
Пример 3(80)
Гидрохлорид (или дигидрохлорид) 2,4-дифтор-5-({[{1-[(6-{2-метил-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(пентил)амино]карбонил}амино)бензамида
ТСХ:Rf 0,46 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,93, 1,30-1,45, 1,60-1,75, 1,95-2,10, 2,13, 2,15-2,30, 2,98, 3,10-3,40, 3,55-3,65, 4,15, 4,34, 7,01-7,21, 7,86, 8,04, 8,26.
Пример 3(81)
Гидрохлорид (или дигидрохлорид) 5-({[{1-[(6-{2,6-диметил-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(пентил)амино]карбонил}амино)-2,4-дифторбензамида
ТСХ:Rf 0,50 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,93, 1,30-1,45, 1,60-1,70, 2,00-2,10, 2,06, 2,15-2,30, 2,99, 3,00-3,40, 3,50-3,70, 4,10, 4,32, 7,03, 7,08, 7,14, 7,86, 7,98, 8,20.
Пример 3(82)
Гидрохлорид (или дигидрохлорид) 5-({[{1-[(6-{4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(пентил)амино]карбонил}амино)-2,4-дифторбензамида
ТСХ:Rf 0,46 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,93, 1,30-1,45, 1,33, 1,60-1,70, 2,00-2,10, 2,20-2,40, 3,00-3,40, 3,11, 3,50-3,70, 4,15, 4,34, 7,08-7,17, 7,32, 7,86, 8,03, 8,28.
Пример 3(83)
Гидрохлорид (или дигидрохлорид) 5-({[{1-[(6-{2-хлор-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(пентил)амино]карбонил}амино)-2,4-дифторбензамида
ТСХ:Rf 0,45 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,93, 1,30-1,50, 1,60-1,75, 2,00-2,10, 2,15-2,25, 3,02, 3,05-3,35, 3,50-3,70, 4,10, 4,33, 7,14-7,28, 7,42, 7,86, 8,00, 8,20.
Пример 3(84)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-3-метоксифенил)метансульфонамида
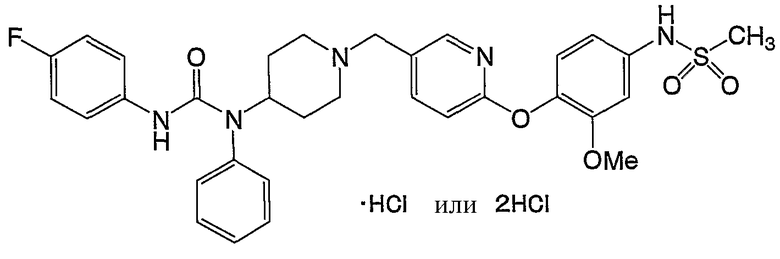
ТСХ:Rf 0,45 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,64-1,82, 2,11-2,21, 3,00, 3,10-3,24, 3,48-3,57, 3,71, 4,31, 4,67, 6,87-7,00, 7,02-7,09, 7,12, 7,20, 7,32, 7,45-7,59, 8,03, 8,26.
Пример 3(85)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[{[(2,4-дифторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-3-метоксифенил)метансульфонамида
Аморфный порошок;
ТСХ:Rf 0,45 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,67-1,82, 2,11-2,24, 3,00, 3,12-3,24, 3,50-3,57, 3,71, 4,30, 4,67, 6,84-6,97, 7,01-7,08, 7,11, 7,35, 7,48-7,61, 8,02, 8,24.
Пример 3(86)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{2-метил-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2-хлор-4-фторбензамида
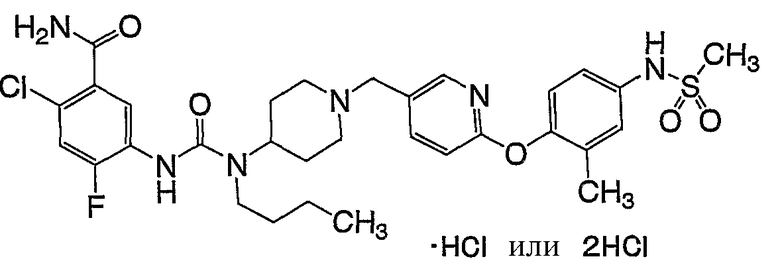
ТСХ:Rf 0,40 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,50, 1,55-1,70, 1,90-2,10, 2,12, 2,20-2,40, 2,97, 3,00-3,20, 3,25-3,35, 3,50-3,70, 4,20, 4,33, 7,00-7,21, 7,32, 7,66, 8,01, 8,24.
Пример 3(87)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2-хлор-4-фторбензамида
ТСХ:Rf 0,40 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,98, 1,33, 1,35-1,50, 1,60-1,70, 1,95-2,10, 2,20-2,40, 3,10, 3,10-3,20, 3,20-3,40, 3,50-3,65, 4,15, 4,33, 7,08-7,12, 7,30-7,34, 7,65, 7,99, 8,24.
Пример 3(88)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{4-[(этилсульфонил)амино]-2-метилфенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида
ТСХ:Rf 0,62 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,33, 1,28-1,45, 1,59-1,70, 1,97-2,08, 2,12, 2,18-2,34, 3,11, 3,06-3,20, 3,25-3,35, 3,52-3,63, 4,12, 4,33, 7,00, 7,07, 7,13, 7,15, 7,20, 7,86, 8,01, 8,24.
Пример 3(89)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{2-метил-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифтор-N-метилбензамида
ТСХ:Rf 0,53 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,47, 1,58-1,70, 1,95-2,07, 2,13, 2,20-2,37, 2,91, 2,98, 3,04-3,21, 3,22-3,35, 3,52-3,64, 4,18, 4,34, 7,01-7,24, 7,79, 8,06, 8,27.
Пример 3(90)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифтор-N-метилбензамида
ТСХ:Rf 0,53 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,33, 1,30-1,47, 1,59-1,70, 1,98-2,05, 2,20-2,38, 2,91, 3,11, 3,07-3,21, 3,22-3,35, 3,52-3,64, 4,18, 4,35, 7,08-7,16, 7,32, 7,79, 8,06, 8,29.
Пример 3(91)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{2-хлор-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифтор-N-метилбензамида
ТСХ:Rf 0,53 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,32-1,45, 1,58-1,70, 1,97-2,05, 2,20-2,37, 2,91, 3,02, 3,04-3,21, 3,22-3,35, 3,51-3,62, 4,18, 4,34, 7,06-7,29, 7,42, 7,79, 8,06, 8,23.
Пример 3(92)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{2-метокси-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифтор-N-метилбензамида
ТСХ:Rf 0,52 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,32-1,45, 1,58-1,70, 1,95-2,05, 2,19-2,37, 2,91, 3,00, 3,04-3,21, 3,22-3,35, 3,54-3,62, 3,72, 4,18, 4,34, 6,90, 7,04-7,17, 7,79, 8,06, 8,27.
Пример 3(93)
Гидрохлорид (или дигидрохлорид) 2-(5-{[(бутил{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторфенил)ацетамида
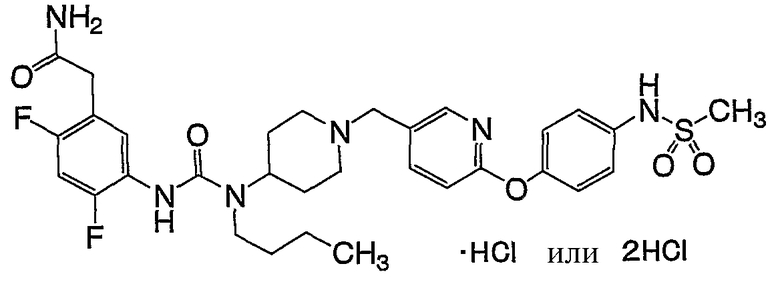
ТСХ:Rf 0,42 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,50, 1,50-1,70, 1,95-2,10, 2,15-2,30, 2,97, 3,05-3,20, 3,20-3,40, 3,50-3,60, 3,53, 4,10, 4,33, 7,00, 7,08-7,14, 7,30-7,34, 7,97, 8,24.
Пример 3(94)
Гидрохлорид (или дигидрохлорид) 2-[2,4-дифтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(пентил)амино]карбонил}амино)фенил]ацетамида
ТСХ:Rf 0,43 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,93, 1,30-1,50, 1,55-1,75, 1,90-2,10, 2,15-2,35, 2,97, 3,10-3,20, 3,20-3,40, 3,50-3,60, 3,53, 4,15, 4,33, 7,00, 7,08-7,14, 7,30-7,34, 7,99, 8,25.
Пример 3(95)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифтор-N-метилбензамида
ТСХ:Rf 0,41 (хлороформ: метанол=7:1);
ЯМР (CD3OD): δ 0,98, 1,35-1,50, 1,65-1,80, 1,95-2,10, 2,20-2,35, 2,91, 2,97, 3,05-3,20, 3,20-3,40, 3,55-3,70, 4,10, 4,34, 7,08-7,16, 7,32, 7,80, 8,00, 8,24.
Пример 3(96)
Гидрохлорид (или дигидрохлорид) 2,4-дифтор-N-метил-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(пентил)амино]карбонил}амино)бензамида
ТСХ:Rf 0,43 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,93, 1,30-1,50, 1,60-1,75, 1,95-2,10, 2,20-2,40, 2,91, 2,97, 3,05-3,20, 3,20-3,40, 3,50-3,70, 4,15, 4,34, 7,08-7,16, 7,32, 7,79, 8,00, 8,24.
Пример 3(97)
Гидрохлорид (или дигидрохлорид) 5-({[{1-[(6-{4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(пентил)амино]карбонил}амино)-2,4-дифтор-N-метилбензамида
ТСХ:Rf 0,45 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,93, 1,33, 1,30-1,45, 1,60-1,70, 1,90-2,10, 2,15-2,30, 2,91, 3,05-3,20, 3,10, 3,20-3,40, 3,50-3,60, 4,10, 4,33, 7,07-7,16, 7,32, 7,79, 7,97, 8,24.
Пример 3(98)
Гидрохлорид (или дигидрохлорид) 2,4-дифтор-N-метил-5-({[{1-[(6-{2-метил-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(пентил)амино]карбонил}амино)бензамида
ТСХ:Rf 0,45 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,93, 1,30-1,40, 1,60-1,70, 1,95-2,05, 2,13, 2,20-2,40, 2,91, 2,98, 3,05-3,20, 3,20-3,40, 3,55-3,65, 4,15, 4,34, 7,11-7,21, 7,79, 8,04, 8,26.
Пример 3(99)
Дигидрохлорид N-[4-(4-{[4-(бутил{[(1,5-диметил-1H-пиразол-4-ил)амино]карбонил}амино)-1-пиперидинил]метил}фенокси)фенил]метансульфонамида
ТСХ:Rf 0,84 (хлороформ: метанол= 4:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,50, 1,60-1,80, 1,90-2,10, 2,10-2,30, 2,27, 2,95, 3,00-3,20, 3,20-3,40, 3,50-3,60, 3,92, 4,20, 4,29, 7,02-7,08, 7,31, 7,51, 7,84.
Пример 3(100)
Дигидрохлорид 4-(4-{[4-(бутил{[(2,4-дифторфенил)амино]карбонил}амино)-1-пиперидинил]метил}фенокси)-N-[2-(диметиламино)этил]бензолсульфонамида
ТСХ:Rf 0,40 (дихлорметан: метанол= 5:1);
ЯМР (CD3OD): δ 0,98, 1,36-1,43, 1,60-1,70, 1,98-2,02, 2,20-2,35, 2,94, 3,10-3,34, 3,56-3,60, 4,21, 4,34, 6,90-7,01, 7,18-7,21, 7,36, 7,62, 7,89.
Пример 3(101)
Гидрохлорид 5-{[(бутил{1-[(6-{4-[(метилсульфонил)амино]фенокси}-1-оксид-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида
ТСХ:Rf 0,54 (хлороформ: метанол= 4:1);
ЯМР (CD3OD): δ 0,99, 1,30-1,50, 1,55-1,70, 1,95-2,15, 2,20-2,40, 3,01, 3,10-3,40, 3,55-3,70, 4,15, 4,39, 7,12-7,21, 7,25, 7,40, 7,81, 7,87, 8,70.
Пример 3(102)
Дигидрохлорид 5-{[(бутил[1-(4-{4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-N-[2-(диметиламино)этил]-2,4-дифторбензамида
ТСХ:Rf 0,17 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 0,98, 1,30-1,50, 1,60-1,80, 1,90-2,10, 2,20-2,40, 2,95, 2,98, 3,00-3,20, 3,20-3,40, 3,50-3,80, 4,20, 4,29, 7,02-7,08, 7,17, 7,29, 7,52, 7,91.
Пример 3(103)
Гидрохлорид (или дигидрохлорид) 5-{[(бензил{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида
ТСХ:Rf 0,51 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,97-2,06, 2,07-2,22, 2,97, 3,04-3,18, 3,47-3,58, 4,30, 4,37, 4,66, 7,04-7,17, 7,21-7,45, 7,89, 8,00, 8,24.
Пример 3(104)
Гидрохлорид метил 4-[4-({4-[({[5-(аминокарбонил)-2,4-дифторфенил]амино}карбонил)(бутил)амино]-1-пиперидинил}метил)фенокси]-3-метоксибензоата
ТСХ:Rf 0,58 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,32-1,44, 1,58-1,70, 1,95-2,04, 2,12-2,30, 3,08-3,18, 3,22-3,35, 3,51-3,61, 3,82, 3,91, 4,14, 4,28, 6,99, 7,09, 7,14, 7,47, 7,67, 7,73, 7,85.
Пример 3(105)
Гидрохлорид (или дигидрохлорид) 2,4-дифтор-5-{[(гексил{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}бензамида
ТСХ:Rf 0,47 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,91, 1,30-1,50, 1,60-1,70, 2,00-2,10, 2,20-2,35, 2,97, 3,00-3,20, 3,20-3,40, 3,50-3,70, 4,10, 4,33, 7,08-7,18, 7,32, 7,86, 7,98, 8,24.
Пример 3(106)
Гидрохлорид метил N-[4-(4-{[4-(бутил{[(2,4-дифторфенил)амино]карбонил}амино)пиперидин-1-ил]метил}фенокси)фенил]-N-(метилсульфонил)глицината
ТСХ:Rf 0,46 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,96, 1,27-1,44, 1,55-1,90, 2,10-2,20, 2,95-3,07, 3,08, 3,21-3,34, 3,53, 3,74, 4,05, 4,46, 6,85-7,04, 7,03-7,45, 7,47.
Пример 3(107)
Гидрохлорид метил N-{4-[4-({4-[({[5-(аминокарбонил)-2,4-дифторфенил]амино}карбонил)(бутил)амино]пиперидин-1-ил}метил)фенокси]фенил}-N-(метилсульфонил)глицината
ТСХ:Rf 0,52 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,32-1,42, 1,58-1,68, 1,70-1,97, 2,12-2,28, 2,99-3,12, 3,08, 3,20-3,35, 3,57, 3,74, 4,02, 4,46, 6,92-7,04, 7,16, 7,36, 7,47, 8,54.
Пример 4
гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{4-[(метиламино)карбонил]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида
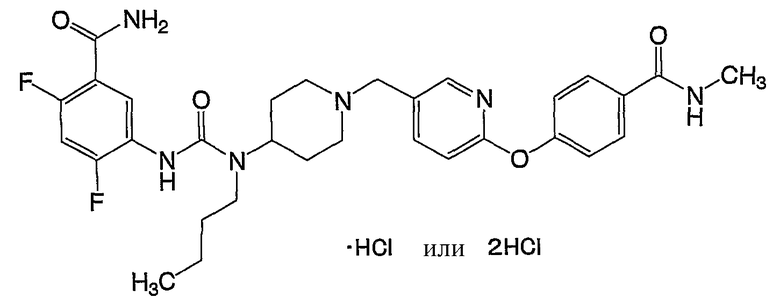
К раствору соединения, полученного в Примере 3(53) (132 мг) в диметилформамиде (1 мл), добавляли 1-гидроксибензотриазол (46 мг), гидрохлорид 1-этил-3-[3-(диметиламино)пропил]карбодиимида (65 мг) и раствор 33% метиламина в метаноле (32 мкл). Реакционную смесь перемешивали в течение 2,5 часов при комнатной температуре. К смеси добавляли насыщенный водный раствор гидрокарбоната натрия и все экстрагировали этилацетатом. Экстракт сушили безводным сульфатом натрия и концентрировали. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат: метанол = 5:1). К раствору полученного соединения в этилацетате добавляли 4 н. хлористый водород в растворе этилацетата. Реакционную смесь концентрировали, с получением указанного в заголовке соединения (73 мг), имеющего следующие физические данные.
ТСХ:Rf 0,48 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,32-1,45, 1,58-1,70, 1,95-2,08, 2,25-2,40, 2,92, 3,10-3,22, 3,27-3,38, 3,58-3,64, 4,24, 4,37, 7,13, 7,15, 7,24, 7,86, 7,90, 8,12, 8,33.
Примеры 4(1) - 4(9)
С помощью процедуры, аналогичной описанной в Примере 4, с использованием соответствующих аминовых соединений вместо метиламина и соединения, полученного в Примере 3(53), или соединения, полученного в Примере 3(47), с получением следующих соединений по настоящему изобретению.
Пример 4(1)
Гидрохлорид (или дигидрохлорид) 5-({[[1-({6-[4-(аминокарбонил)фенокси]-3-пиридинил}метил)-4-пиперидинил](бутил)амино]карбонил}амино)-2,4-дифторбензамида
ТСХ:Rf 0,47 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,35-1,48, 1,59-1,70, 1,95-2,08, 2,19-2,38, 3,06-3,22, 3,24-3,35, 3,55-3,65, 4,18, 4,36, 7,14, 7,16, 7,23, 7,86, 7,96, 8,05, 8,30.
Пример 4(2)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{4-[(диметиламино)карбонил]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида
ТСХ:Rf 0,50 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,34-1,45, 1,58-1,70, 1,95-2,08, 2,20-2,40, 3,02-3,22, 3,24-3,35, 3,52-3,65, 4,19, 4,36, 7,14, 7,16, 7,25, 7,52, 7,86, 8,09, 8,30.
Пример 4(3)
Гидрохлорид (или дигидрохлорид) 5-[({бутил[1-({6-[4-(4-морфолинилкарбонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида
ТСХ:Rf 0,50 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,32-1,47, 1,59-1,70, 1,95-2,08, 2,20-2,39, 3,10-3,20, 3,25-3,35, 3,45-3,82, 4,18, 4,36, 7,14, 7,16, 7,25, 7,52, 7,86, 8,08, 8,30.
Пример 4(4)
Гидрохлорид (или дигидрохлорид) 5-({[бутил(1-{[6-(4-{[(2-метоксиэтил)амино]карбонил}фенокси)-3-пиридинил]метил}-4-пиперидинил)амино]карбонил}амино)-2,4-дифторбензамида
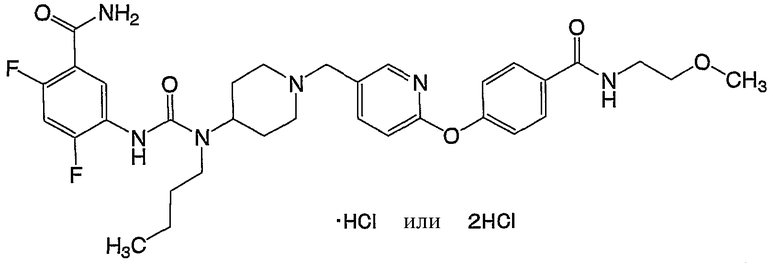
ТСХ:Rf 0,50 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,35-1,47, 1,60-1,70, 1,95-2,08, 2,20-2,38, 3,08-3,21, 3,25-3,40, 3,57, 3,51-3,64, 4,16, 4,36, 7,14, 7,16, 7,23, 7,86, 7,90, 8,05, 8,30.
Пример 4(5)
Дигидрохлорид (или тригидрохлорид) 5-[({бутил[1-({6-[4-({[2-(диметиламино)этил]амино}карбонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида
ТСХ:Rf 0,35 (дихлорметан: метанол= 5:1);
ЯМР (CD3OD): δ 0,97, 1,35-1,45, 1,59-1,70, 1,94-2,05, 2,23-2,40, 2,99, 3,10-3,22, 3,22-3,35, 3,40, 3,55-3,65, 3,78, 4,22, 4,37, 7,14, 7,17, 7,27, 7,86, 7,99, 8,13, 8,34.
Пример 4(6)
Гидрохлорид (или дигидрохлорид) 5-({[бутил(1-{[6-(4-{[(2-метоксиэтил)амино]карбонил}-2,6-диметилфенокси)-3-пиридинил]метил}-4-пиперидинил)амино]карбонил}амино)-2,4-дифторбензамида
ТСХ:Rf 0,51 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,34-1,46, 1,57-1,68, 1,98-2,08, 2,13, 2,18-2,35, 3,08-3,21, 3,22-3,40, 3,56, 3,51-3,64, 4,17, 4,33, 7,11, 7,14, 7,62, 7,86, 8,06, 8,22.
Пример 4(7)
Гидрохлорид 5-({[(1-{4-[4-(аминокарбонил)-2-метоксифенокси]бензил}-4-пиперидинил)(бутил)амино]карбонил}амино)-2,4-дифторбензамида
ТСХ:Rf 0,41 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,32-1,47, 1,58-1,70, 1,97-2,05, 2,12-2,31, 3,04-3,18, 3,22-3,35, 3,51-3,60, 3,82, 4,15, 4,27, 6,97, 7,09, 7,14, 7,47, 7,53, 7,65, 7,85.
Пример 4(8)
Гидрохлорид 5-{[(бутил{1-[4-(2-метокси-4-{[(2-метоксиэтил)амино]карбонил}фенокси)бензил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида
ТСХ:Rf 0,53 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,32-1,47, 1,58-1,70, 1,95-2,04, 2,12-2,30, 3,04-3,18, 3,22-3,35, 3,50-3,61, 3,57, 3,82, 4,14, 4,27, 6,97, 7,09, 7,14, 7,45, 7,47, 7,61, 7,85.
Пример 4(9)
Гидрохлорид 5-({[бутил(1-{4-[2-метокси-4-(4-морфолинилкарбонил)фенокси]бензил}-4-пиперидинил)амино]карбонил}амино)-2,4-дифторбензамида
ТСХ:Rf 0,52 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,32-1,44, 1,58-1,70, 1,95-2,04, 2,12-2,30, 3,04-3,17, 3,22-3,35, 3,47-3,81, 3,79, 4,14, 4,27, 6,97, 7,05, 7,12, 7,14, 7,20, 7,45, 7,85.
Пример 5
Гидрохлорид [[4-(4-{[4-(бутил{[(2,4-дифторфенил)амино]карбонил}амино)-1-пиперидинил]метил}фенокси)фенил](метилсульфонил)амино]уксусной кислоты
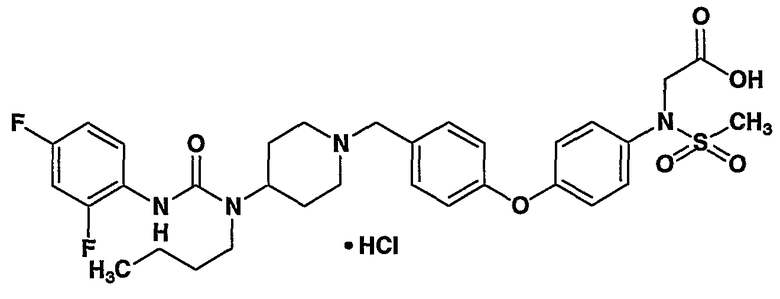
К раствору соединения, полученного в Примере 3(106) (80 мг) в метаноле (1 мл), добавляли 2 н. водный раствор гидроксида натрия (0,5 мл). Реакционную смесь перемешивалиь в течение 2,5 часов при комнатной температуре. К реакционной смеси на ледяной бане добавляли 1 н. соляную кислоту, пока рН раствора не становилось ниже 5, затем смесь экстрагировали этилацетатом. Экстракт сушили безводным сульфатом натрия, концентрировали. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле (дихлорметан: метанол = 9:1). К раствору полученного соединения в этилацетате добавляли 4 н. хлористый водород в растворе этилацетата. Реакционную смесь концентрировали, с получением указанного в заголовке соединения (64 мг), имеющего следующие физические данные.
ТСХ:Rf 0,45 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,32-1,45, 1,57-1,70, 1,92-2,05, 2,12-2,31, 3,09, 3,06-3,20, 3,22-3,35, 3,51-3,61, 4,17, 4,30, 4,43, 6,88-7,05, 7,06, 7,12, 7,36, 7,51-7,58.
Пример 5(1)
Гидрохлорид [{4-[4-({4-[({[5-(аминокарбонил)-2,4-дифторфенил]амино}карбонил)(бутил)амино]-1-пиперидинил}метил)фенокси]фенил}(метилсульфонил)амино]уксусной кислоты
С помощью процедуры, аналогичной описанной в Примере 5, с использованием соединения, полученного в Примере 3(107), получали следующее указанное в заголовке соединение.
ТСХ:Rf 0,17 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,42, 1,57-1,70, 1,90-2,02, 2,11-2,30, 2,95-3,10, 3,10, 3,23-3,40, 3,41-3,52, 4,16, 4,21, 4,30, 7,01, 7,06, 7,13, 7,48, 7,57, 7,86.
Примеры 6(1) - 6(20)
С помощью процедуры, аналогичной описанной в Примере 3, с использованием соответствующего альдегидного соединения вместо соединения, полученного в Примере 1, и соответствующего аминового соединения вместо соединения, полученного в Примере 2, с получением следующих соединений по настоящему изобретению.
Пример 6(1)
Гидрохлорид (или дигидрохлорид) 2-(5-{[(бутил{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторфенил)ацетамида
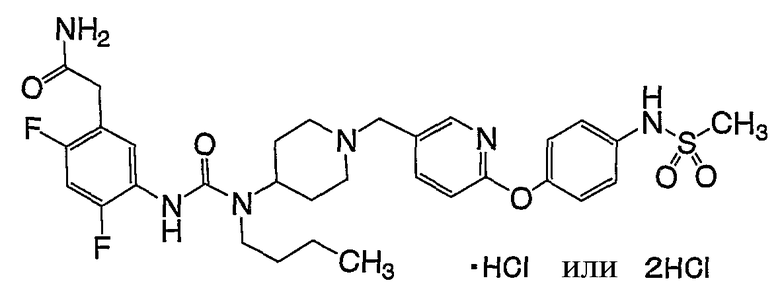
ТСХ:Rf 0,42 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,50, 1,50-1,70, 1,95-2,10, 2,15-2,30, 2,97, 3,05-3,20, 3,20-3,40, 3,50-3,60, 3,53, 4,10, 4,33, 7,00, 7,08-7,14, 7,30-7,34, 7,97, 8,24.
Пример 6(2)
Гидрохлорид (или дигидрохлорид) 2-[2,4-дифтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(пентил)амино]карбонил}амино)фенил]ацетамида
ТСХ:Rf 0,43 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,93, 1,30-1,50, 1,55-1,75, 1,90-2,10, 2,15-2,35, 2,97, 3,10-3,20, 3,20-3,40, 3,50-3,60, 3,53, 4,15, 4,33, 7,00, 7,08-7,14, 7,30-7,34, 7,99, 8,25.
Пример 6(3)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифтор-N-метилбензамида
ТСХ:Rf 0,41 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,98, 1,35-1,50, 1,65-1,80, 1,95-2,10, 2,20-2,35, 2,91, 2,97, 3,05-3,20, 3,20-3,40, 3,55-3,70, 4,10, 4,34, 7,08-7,16, 7,32, 7,80, 8,00, 8,24.
Пример 6(4)
Гидрохлорид (или дигидрохлорид) 2,4-дифтор-N-метил-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(пентил)амино]карбонил}амино)бензамида
ТСХ:Rf 0,43 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,93, 1,30-1,50, 1,60-1,75, 1,95-2,10, 2,20-2,40, 2,91, 2,97, 3,05-3,20, 3,20-3,40, 3,50-3,70, 4,15, 4,34, 7,08-7,16, 7,32, 7,79, 8,00, 8,24.
Пример 6(5)
Гидрохлорид (или дигидрохлорид) 5-({[{1-[(6-{4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(пентил)амино]карбонил}амино)-2,4-дифтор-N-метилбензамида
ТСХ:Rf 0,45 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,93, 1,33, 1,30-1,45, 1,60-1,70, 1,90-2,10, 2,15-2,30, 2,91, 3,05-3,20, 3,10, 3,20-3,40, 3,50-3,60, 4,10, 4,33, 7,07-7,16, 7,32, 7,79, 7,97, 8,24.
Пример 6(6)
Гидрохлорид (или дигидрохлорид) 2,4-дифтор-N-метил-5-({[{1-[(6-{2-метил-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(пентил)амино]карбонил}амино)бензамида
ТСХ:Rf 0,45 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,93, 1,30-1,40, 1,60-1,70, 1,95-2,05, 2,13, 2,20-2,40, 2,91, 2,98, 3,05-3,20, 3,20-3,40, 3,55-3,65, 4,15, 4,34, 7,11-7,21, 7,79, 8,04, 8,26.
Пример 6(7)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{2-хлор-4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида
ТСХ:Rf 0,46 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,33, 1,30-1,47, 1,59-1,70, 1,95-2,08, 2,20-2,37, 3,15, 3,05-3,20, 3,22-3,35, 3,52-3,62, 4,18, 4,34, 7,10-7,28, 7,41, 7,86, 8,05, 8,24.
Пример 6(8)
Гидрохлорид 5-({[(1-{4-[4-(аминокарбонил)фенокси]бензил}-4-пиперидинил)(бутил)амино]карбонил}амино)-2,4-дифторбензамида
ТСХ:Rf 0,40 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,32-1,49, 1,59-1,70, 1,95-2,09, 2,19-2,38, 3,08-3,20, 3,27-3,35, 3,51-3,65, 4,18, 4,32, 7,07, 7,08, 7,16, 7,57, 7,86, 7,91.
Пример 6(9)
Гидрохлорид 5-({[бутил(1-{4-[4-(4-морфолинилкарбонил)фенокси]бензил}-4-пиперидинил)амино]карбонил}амино)-2,4-дифторбензамида
ТСХ:Rf 0,45 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,31-1,47, 1,60-1,70, 1,98-2,07, 2,15-2,30, 3,04-3,20, 3,25-3,35, 3,50-3,80, 4,13, 4,31, 7,08-7,18, 7,48, 7,54, 7,86.
Пример 6(10)
Гидрохлорид 2-{5-[({бутил[1-(4-{4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторфенил}ацетамида
ТСХ:Rf 0,42 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,98, 1,30-1,50, 1,60-1,75, 1,95-2,10, 2,10-2,30, 2,95, 3,05-3,40, 3,53, 3,55-3,65, 4,15, 4,28, 7,00-7,08, 7,28, 7,29, 7,49.
Пример 6(11)
Гидрохлорид (или дигидрохлорид) 2-{5-[({бутил[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторфенил}ацетамида
ТСХ:Rf 0,44 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,98, 1,30-1,50, 1,60-1,70, 1,90-2,10, 2,15-2,30, 3,05-3,40, 3,15, 3,53, 3,55-3,65, 4,15, 4,36, 7,00, 7,23, 7,33, 7,40, 8,01, 8,04, 8,29.
Пример 6(12)
Гидрохлорид (или дигидрохлорид) 2-{5-[({бутил[1-({6-[2-хлор-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторфенил}ацетамида
ТСХ:Rf 0,42 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,98, 1,30-1,50, 1,60-1,70, 1,95-2,10, 2,15-2,35, 3,00-3,40, 3,30, 3,53, 3,55-3,65, 4,15, 4,37, 7,00, 7,25, 7,33, 7,35, 7,53, 8,06, 8,16, 8,31.
Пример 6(13)
Гидрохлорид (или дигидрохлорид) 2-[5-({[{1-[(6-{4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(пентил)амино]карбонил}амино)-2,4-дифторфенил}ацетамида
ТСХ:Rf 0,33 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,93, 1,30-1,50, 1,33, 1,60-1,70, 1,90-2,10, 2,15-2,35, 3,00-3,40, 3,10, 3,53, 3,55-3,65, 4,10, 4,33, 7,00, 7,07-7,13, 7,32, 7,33, 7,97, 8,24.
Пример 6(14)
Гидрохлорид (или дигидрохлорид) 2-[2,4-дифтор-5-({[{1-[(6-{2-метил-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(пентил)амино]карбонил}амино)фенил]ацетамида
ТСХ:Rf 0,45 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,93, 1,30-1,50, 1,60-1,70, 1,90-2,10, 2,12, 2,20-2,40, 2,97, 3,00-3,40, 3,53, 3,55-3,65, 4,15, 4,33, 6,96-7,21, 7,33, 8,01, 8,24.
Пример 6(15)
Гидрохлорид (или дигидрохлорид) 2-[2,4-дифтор-5-({[[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил](пентил)амино]карбонил}амино)фенил]ацетамида
ТСХ:Rf 0,39 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,93, 1,30-1,50, 1,60-1,70, 1,90-2,10, 2,10-2,30, 3,00-3,40, 3,15, 3,53, 3,55-3,65, 4,15, 4,36, 7,00, 7,22, 7,33, 7,40, 8,01, 8,04, 8,29.
Пример 6(16)
Гидрохлорид (или дигидрохлорид) 2-[5-({[[1-({6-[2-хлор-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил](пентил)амино]карбонил}амино)-2,4-дифторфенил]ацетамида
ТСХ:Rf 0,44 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,94, 1,30-1,50, 1,60-1,70, 1,90-2,10, 2,10-2,30, 3,00-3,40, 3,30, 3,53, 3,55-3,65, 4,10, 4,35, 7,00, 7,25, 7,33, 7,37, 7,52, 8,05, 8,16, 8,31.
Пример 6(17)
Гидрохлорид (или дигидрохлорид) N'-(4-фторфенил)-N-[1-({6-[4-(метилсульфонил)фенокси]пиридин-3-ил}метил)пиперидин-4-ил]-N-фенилмочевины
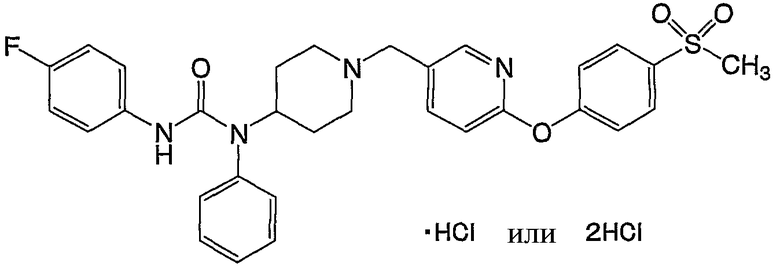
ТСХ:Rf 0,54 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,62-1,80, 2,14-2,03, 3,14, 3,12-3,25, 3,48-3,58, 4,30, 4,67, 6,95, 7,16-7,25, 7,30-7,40, 7,46-7,58, 7,96, 8,00, 8,22.
Пример 6(18)
Гидрохлорид (или дигидрохлорид) N-[1-({6-[2-хлор-4-(метилсульфонил)фенокси]пиридин-3-ил}метил)пиперидин-4-ил]-N'-(4-фторфенил)-N-фенилмочевины
ТСХ:Rf 0,54 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,62-1,80, 2,15-2,23, 3,12-3,28, 3,31, 3,49-3,59, 4,30, 4,68, 6,95, 7,10, 7,18-7,25, 7,30-7,40, 7,49-7,58, 7,98, 8,15, 8,24.
Пример 6(19)
Гидрохлорид (или дигидрохлорид) N-[1-({6-[2-хлор-4-(метилсульфонил)фенокси]пиридин-3-ил}метил)пиперидин-4-ил]-N'-(2,4-дифторфенил)-N-фенилмочевины
ТСХ:Rf 0,54 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,62-1,80, 2,15-2,25, 3,10-3,30, 3,31, 3,50-3,60, 4,31, 4,68, 6,84-6,96, 7,21, 7,30-7,39, 7,48-7,60, 7,98, 8,15, 8,24.
Пример 6(20)
Гидрохлорид (или дигидрохлорид) 5-({[бутил(1-{[6-(4-{[(2-метоксиэтил)амино]карбонил}-2-метилфенокси)пиридин-3-ил]метил}-пиперидин-4-ил)амино]карбонил}амино)-2,4-дифторбензамида
ТСХ:Rf 0,52 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,97, 1,32-1,47, 1,60-1,70, 1,97-2,04, 2,21, 2,20-2,37, 3,10-3,20, 3,21-3,40, 3,57, 3,50-3,62, 4,18, 4,34, 7,10-7,20, 7,72, 7,80, 7,86, 8,06, 8,26.
Примеры 7(1) - 7(121)
С помощью процедуры, аналогичной описанной в Примере 3, с использованием соответствующего альдегидного соединения вместо соединения, полученного в Примере 1, и соответствующего аминового соединения вместо соединения, полученного в Примере 2, и при необходимости преобразовывали в свободное основание, с получением следующих соединений по настоящему изобретению.
Пример 7(1)
Гидрохлорид (или дигидрохлорид) 5-({[[1-({6-[2,6-диметил-4-(метилсульфонил)фенокси]-3-пиридинил}-метил)-4-пиперидинил](пентил)амино]карбонил}амино)-2,4-дифторбензамида
ТСХ:Rf 0,42 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,93, 1,30-1,50, 1,60-1,80, 1,95-2,10, 2,17, 2,20-2,35, 3,00-3,40, 3,14, 3,50-3,70, 4,15, 4,33, 7,14, 7,21, 7,74, 7,86, 8,07, 8,18.
Пример 7(2)
Гидрохлорид (или дигидрохлорид) 5-({[[1-({6-[2-хлор-4-(метилсульфонил)фенокси]-3-пиридинил}-метил)-4-пиперидинил](пентил)амино]карбонил}амино)-2,4-дифторбензамида
ТСХ:Rf 0,48 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,93, 1,30-1,50, 1,60-1,80, 1,95-2,10, 2,20-2,40, 3,10-3,40, 3,30, 3,50-3,70, 4,15, 4,37, 7,14, 7,25, 7,35, 7,53, 7,86, 8,10, 8,16, 8,32.
Пример 7(3)
Гидрохлорид (или дигидрохлорид) 5-[({бутил[1-({6-[2-хлор-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]амино}карбонил)амино]-2-фторбензамида
ТСХ:Rf 0,35 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,50, 1,60-1,80, 1,95-2,10, 2,20-2,40, 3,10-3,40, 3,30, 3,50-3,70, 4,15, 4,36, 7,14, 7,25, 7,35, 7,50, 7,53, 7,78, 8,07, 8,16, 8,32.
Пример 7(4)
Гидрохлорид (или дигидрохлорид) 5-[({бутил[1-({6-[2-метил-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]амино}карбонил)амино]-2-фторбензамида
ТСХ:Rf 0,36 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,97, 1,30-1,50, 1,55-1,70, 1,90-2,10, 2,20-2,40, 2,26, 3,00-3,40, 3,14, 3,50-3,70, 4,20, 4,35, 7,11-7,30, 7,53, 7,76-7,85, 7,92, 8,07, 8,24.
Пример 7(5)
Гидрохлорид (или дигидрохлорид) 2,4-дифтор-5-{[гексил{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}бензамида
ТСХ:Rf 0,37 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,98, 1,30-1,50, 1,60-1,70, 1,90-2,05, 2,20-2,35, 2,97, 3,00-3,35, 3,50-3,70, 4,20, 4,34, 7,08-7,17, 7,32, 7,86, 8,02, 8,24.
Пример 7(6)
Гидрохлорид (или дигидрохлорид) 2,4-дифтор-5-{[((2-метилбензил){1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}бензамида
ТСХ:Rf 0,53 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,98-2,20, 2,36, 2,97, 3,04-3,18, 3,48-3,57, 4,30, 4,43, 4,57, 7,04-7,33, 7,85, 7,98, 8,23.
Пример 7(7)
Гидрохлорид (или дигидрохлорид) 2,4-дифтор-5-({[[1-({6-[2-метил-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил](пентил)амино]карбонил}амино)бензамида
ТСХ:Rf 0,38 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,94, 1,30-1,50, 1,60-1,80, 1,90-2,10, 2,26, 2,20-2,40, 3,05-3,40, 3,14, 3,50-3,70, 4,15, 4,33, 7,11-7,29, 7,81-7,89, 7,92, 8,03, 8,23.
Пример 7(8)
Гидрохлорид (или дигидрохлорид) 2,4-дифтор-5-{[({1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}бензамида
ТСХ:Rf 0,37 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,65-1,80, 2,20-2,30, 2,98, 3,08-3,21, 3,50-3,60, 3,83, 4,34, 7,07-7,19, 7,33, 8,02, 8,27, 8,38.
Пример 7(9)
Гидрохлорид (или дигидрохлорид) N'-(4-фторфенил)-N-[1-({6-[2-метокси-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]-N-фенилмочевины
ТСХ:Rf 0,55 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,64-1,80, 2,12-2,22, 3,17, 3,10-3,25, 3,48-3,58, 3,79, 4,27, 4,67, 6,95, 7,12, 7,22, 7,30-7,38, 7,45-7,64, 7,93, 8,12.
Пример 7(10)
Гидрохлорид (или дигидрохлорид) N'-(2,4-дифторфенил)-N-[1-({6-[2-метил-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]-N-фенилмочевины
ТСХ:Rf 0,56 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,65-1,80, 2,15-2,28, 2,24, 3,13, 3,12-3,24, 3,50-3,58, 4,29, 4,68, 6,85-6,98, 7,17, 7,26, 7,34-7,38, 7,48-7,60, 7,81, 7,91, 7,98, 8,17.
Пример 7(11)
Гидрохлорид (или дигидрохлорид) N'-(2,4-дифторфенил)-N-[1-({6-[2,6-диметил-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]-N-фенилмочевины
ТСХ:Rf 0,56 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,62-1,80, 2,15, 2,12-2,23, 3,13, 3,10-3,24, 3,50-3,58, 4,27, 4,68, 6,85-6,98, 7,18, 7,33-7,37, 7,50-7,60, 7,73, 7,96, 8,11.
Пример 7(12)
Гидрохлорид (или дигидрохлорид) N'-(2,4-дифторфенил)-N-[1-({6-[2-метокси-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]-N-фенилмочевины
ТСХ:Rf 0,55 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,64-1,80, 2,15-2,24, 3,17, 3,12-3,25, 3,48-3,58, 3,79, 4,28, 4,68, 6,85-6,98, 7,12, 7,33-7,37, 7,50-7,60, 7,95, 8,13.
Пример 7(13)
Гидрохлорид (или дигидрохлорид) 2,4-дифтор-5-[({гексил[1-({6-[2-метокси-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]амино}карбонил)амино]бензамида
ТСХ:Rf 0,35 (хлороформ: метанол= 7:1);
ЯМР (CD3OD): δ 0,91, 1,25-1,45, 1,60-1,75, 1,90-2,10, 2,20-2,40, 3,05-3,40, 3,14, 3,50-3,70, 3,81, 4,15, 4,35, 7,14, 7,15, 7,38, 7,60-7,65, 7,86, 8,09, 8,24.
Пример 7(14)
Гидрохлорид (или дигидрохлорид) N'-(4-фторфенил)-N-[1-({6-[2-метил-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]-N-фенилмочевины
ТСХ:Rf 0,75 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,63-1,80, 2,12-2,23, 2,24, 3,13, 3,10-3,25, 3,48-3,57, 4,29, 4,67, 6,95, 7,15-7,35, 7,47-7,60, 7,81, 7,91, 7,97, 8,17.
Пример 7(15)
Гидрохлорид (или дигидрохлорид) N-[1-({6-[2,6-диметил-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]-N'-(4-фторфенил)-N-фенилмочевины
ТСХ:Rf 0,75 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,64-1,80, 2,15, 2,10-2,23, 3,13, 3,10-3,25, 3,48-3,58, 4,27, 4,67, 6,95, 7,15-7,25, 7,30-7,35, 7,48-7,60, 7,73, 7,97, 8,11.
Пример 7(16)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(2-метил-6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида
ТСХ:Rf 0,56 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,32-1,45, 1,58-1,70, 1,95-2,05, 2,24-2,40, 2,67, 2,99, 3,20-3,35, 3,60-3,69, 4,28, 4,43, 6,95, 7,14, 7,22, 7,37, 7,87, 8,20.
Пример 7(17)
Гидрохлорид (или дигидрохлорид) 4-хлор-2-фтор-5-({[[1-({6-[2-метил-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил](пентил)амино]карбонил}амино)бензамида
ТСХ:Rf 0,55 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,94, 1,30-1,50, 1,67-1,80, 1,98-2,06, 2,26, 2,19-2,38, 3,10-3,20, 3,14, 3,25-3,35, 3,55-3,65, 4,20, 4,34, 7,21, 7,28, 7,41, 7,83, 7,90-7,99, 8,06, 8,24.
Пример 7(18)
Гидрохлорид (или дигидрохлорид) 4-хлор-5-({[[1-({6-[2,6-диметил-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил](пентил)амино]карбонил}амино)-2-фторбензамида
ТСХ:Rf 0,55 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,94, 1,30-1,47, 1,65-1,80, 1,98-2,08, 2,17, 2,15-2,35, 3,08-3,20, 3,13, 3,25-3,35, 3,55-3,65, 4,19, 4,33, 7,21, 7,41, 7,74, 7,97, 8,06, 8,18.
Пример 7(19)
Гидрохлорид (или дигидрохлорид) 5-{[(бутил{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-4-хлор-2-фторбензамида
ТСХ:Rf 0,54 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,35-1,48, 1,62-1,75, 1,98-2,08, 2,19-2,38, 2,97, 3,08-3,20, 3,25-3,35, 3,55-3,63, 4,17, 4,34, 7,09, 7,13, 7,32, 7,42, 7,94, 8,02, 8,27.
Пример 7(20)
Гидрохлорид (или дигидрохлорид) 5-[({бутил[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]амино}карбонил)амино]-4-хлор-2-фторбензамида
ТСХ:Rf 0,54 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,99, 1,38-1,50, 1,64-1,75, 1,98-2,07, 2,20-2,38, 3,15, 3,08-3,20, 3,25-3,35, 3,58-3,65, 4,18, 4,36, 7,22, 7,40, 7,41, 7,94, 8,02, 8,07, 8,30.
Пример 7(21)
Гидрохлорид (или дигидрохлорид) 5-[({бутил[1-({6-[2-хлор-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]амино}карбонил)амино]-4-хлор-2-фторбензамида
ТСХ:Rf 0,55 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,99, 1,38-1,45, 1,64-1,75, 1,98-2,07, 2,20-2,38, 3,08-3,22, 3,25-3,35, 3,31, 3,58-3,65, 4,18, 4,37, 7,25, 7,36, 7,41, 7,53, 7,94, 8,09, 8,16, 8,32.
Пример 7(22)
Гидрохлорид (или дигидрохлорид) 5-[({бутил[1-({6-[2,6-диметил-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]амино}карбонил)амино]-4-хлор-2-фторбензамида
ТСХ:Rf 0,56 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,98, 1,35-1,48, 1,62-1,75, 1,97-2,08, 2,17, 2,19-2,38, 3,08-3,21, 3,14, 3,25-3,35, 3,52-3,65, 4,19, 4,33, 7,21, 7,41, 7,73, 7,94, 8,07, 8,18.
Пример 7(23)
Дигидрохлорид N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиразинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,50 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,70-1,84, 2,14-2,23, 2,97, 3,20-3,35, 3,55-3,65, 4,40, 4,68, 6,95, 7,17, 7,22, 7,29-7,38, 7,48-7,60, 8,19, 8,48.
Пример 7(24)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[[(циклогексиламино)карбонил](фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,51 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 0,93-1,15, 1,20-1,38, 1,49-1,80, 2,08-2,18, 2,97, 3,10-3,21, 3,47-3,58, 4,28, 4,62, 7,07, 7,12, 7,18-7,25, 7,33, 7,42-7,55, 7,98, 8,23.
Пример 7(25)
Гидрохлорид (или дигидрохлорид) N-[4-({5-[(4-{фенил[(3-тиениламино)карбонил]амино}-1-пиперидинил)метил]-2-пиридинил}окси)фенил]метансульфонамида
ТСХ:Rf 0,50 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,64-1,80, 2,12-2,20, 2,98, 3,12-3,26, 3,50-3,59, 4,32, 4,68, 6,91, 7,10, 7,04-7,20, 7,27-7,37, 7,48-7,60, 8,07, 8,31.
Пример 7(26)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[(анилинкарбонил)(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,56 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,62-1,80, 2,15-2,24, 2,97, 3,12-3,23, 3,49-3,57, 4,27, 4,68, 6,97-7,14, 7,18-7,22, 7,28-7,38, 7,48-7,60, 7,89, 8,17.
Пример 7(27)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[[(бензиламино)карбонил](фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,55 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,60-1,78, 2,08-2,18, 2,97, 3,08-3,21, 3,48-3,55, 4,25, 4,29, 4,64, 7,08, 7,10-7,27, 7,32, 7,40-7,58, 8,01, 8,27.
Пример 7(28)
Гидрохлорид (или дигидрохлорид) N-{4-[(5-{[4-(фенил{[(2-фенилэтил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]фенил}метансульфонамида
ТСХ:Rf 0,55 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,57-1,73, 2,04-2,13, 2,67, 2,98, 3,10-3,22, 3,27-3,35, 3,48-3,55, 4,31, 4,60, 7,04-7,25, 7,34, 7,40-7,47, 8,06, 8,31.
Пример 7(29)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(3-тиенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
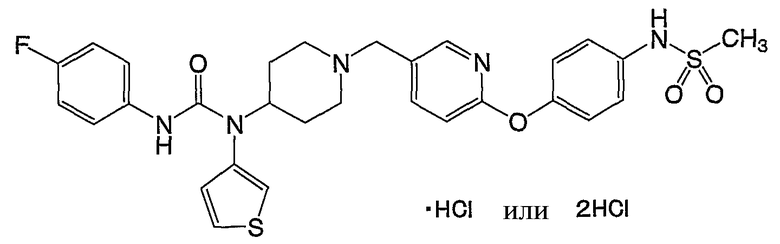
ТСХ:Rf 0,30 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,60-1,80, 2,10-2,20, 2,97, 3,10-3,25, 3,50-3,60, 4,29, 4,65, 6,93-7,13, 7,22-7,33, 7,53, 7,61, 7,94, 8,21.
Пример 7(30)
Гидрохлорид (или дигидрохлорид) N-[4-({5-[(4-{3-тиенил[(3-тиениламино)карбонил]амино}-1-пиперидинил)метил]-2-пиридинил}окси)фенил]метансульфонамида
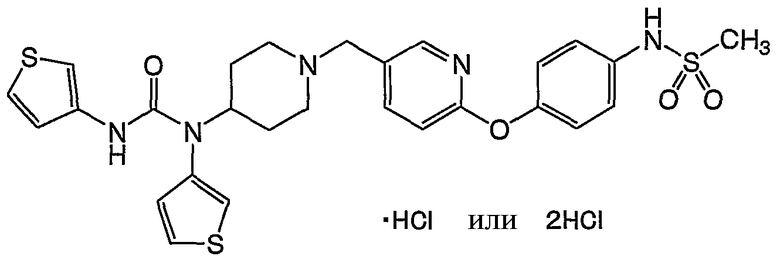
ТСХ:Rf 0,55 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,62-1,78, 2,11-2,20, 2,97, 3,12-3,25, 3,48-3,58, 4,28, 4,67, 6,95, 7,00, 7,06, 7,11, 7,17-7,23, 7,31, 7,49, 7,60, 7,90, 8,18.
Пример 7(31)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[{[(3-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,56 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,62-1,80, 2,12-2,24, 2,97, 3,12-3,25, 3,48-3,58, 4,27, 4,68, 6,72, 6,93, 7,03-7,35, 7,48-7,60, 7,89, 8,17.
Пример 7(32)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[{[(2-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,56 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,63-1,80, 2,18-2,25, 2,97, 3,12-3,25, 3,48-3,58, 4,28, 4,69, 6,98-7,15, 7,31, 7,35-7,40, 7,50-7,62, 7,73, 7,90, 8,17.
Пример 7(33)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[{[(4-метоксифенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,48 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,62-1,80, 2,13-2,21, 2,97, 3,12-3,25, 3,48-3,57, 3,73, 4,27, 4,67, 6,79, 7,05, 7,09, 7,10, 7,28-7,35, 7,47-7,58, 7,90, 8,17.
Пример 7(34)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[{[(3-метоксифенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,48 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,62-1,80, 2,13-2,25, 2,97, 3,12-3,25, 3,48-3,57, 3,72, 4,28, 4,67, 6,58, 6,73, 6,94, 7,04-7,15, 7,29-7,35, 7,49-7,60, 7,90, 8,18.
Пример 7(35)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[{[(2-метоксифенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,48 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,62-1,80, 2,15-2,27, 2,97, 3,12-3,25, 3,50-3,60, 3,55, 4,29, 4,71, 6,80-6,97, 7,05, 7,11, 7,31, 7,37, 7,51-7,64, 7,91, 7,95, 8,18.
Пример 7(36)
N-(4-{[5-({4-[{[(4-метилфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид
Аморфный порошок;
ТСХ:Rf 0,48 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,34-1,50, 1,80-1,91, 2,10-2,20, 2,23, 2,83-2,98, 2,95, 3,44, 4,43, 6,88, 6,98-7,10, 7,28, 7,45-7,57, 7,73, 7,98.
Пример 7(37)
N-(4-{[5-({4-[{[(3-метилфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид
ТСХ:Rf 0,48 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,35-1,50, 1,80-1,91, 2,08-2,20, 2,24, 2,84-2,98, 2,94, 3,44, 4,43, 6,80, 6,87, 6,97-7,12, 7,26-7,34, 7,44-7,58, 7,73, 7,98.
Пример 7(38)
N-(4-{[5-({4-[{[(2-метилфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид
ТСХ:Rf 0,48 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,38-1,54, 1,84-1,96, 1,91, 2,10-2,20, 2,85-2,98, 2,95, 3,44, 4,43, 6,88, 6,97, 7,02-7,14, 7,28, 7,35, 7,42-7,60, 7,73, 7,98.
Пример 7(39)
N-(4-{[5-({4-[{[(4-хлорфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид
Белый аморфный порошок;
ТСХ:Rf 0,52 (дихлорметан: метанол= 9:1);
ЯМР (CDCl3): δ 1,32-1,48, 1,80-1,89, 2,08-2,20, 2,82-2,90, 3,01, 3,40, 4,53, 5,83, 6,43, 6,85, 7,08-7,28, 7,44-7,55, 7,61, 8,00.
Пример 7(40)
N-(4-{[5-({4-[{[(3-хлорфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид
ТСХ:Rf 0,52 (дихлорметан: метанол= 9:1);
ЯМР (CDCl3): δ 1,32-1,50, 1,80-1,90, 2,08-2,20, 2,82-2,90, 3,01, 3,41, 4,53, 5,85, 6,52, 6,85, 6,94, 7,02-7,15, 7,19-7,28, 7,35, 7,44-7,55, 7,61, 8,01.
Пример 7(41)
N-(4-{[5-({4-[{[(2-хлорфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид
ТСХ:Rf 0,52 (дихлорметан: метанол= 9:1);
ЯМР (CDCl3): δ 1,38-1,53, 1,82-1,90, 2,08-2,20, 2,83-2,92, 3,01, 3,41, 4,53, 6,47, 6,59, 6,85, 6,87, 7,12, 7,18, 7,22-7,28, 7,42-7,55, 7,61, 8,01, 8,27.
Пример 7(42)
N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(1-метил-1H-пиразол-4-ил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид
ТСХ:Rf 0,40 (дихлорметан: метанол= 9:1);
ЯМР (CDCl3): δ 1,30-1,48, 1,70-1,80, 2,08-2,19, 2,81-2,90, 3,01, 3,41, 3,96, 4,46, 6,26, 6,35, 6,85, 6,92, 7,11, 7,18-7,28, 7,37, 7,61, 8,01.
Пример 7(43)
2-фтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамид
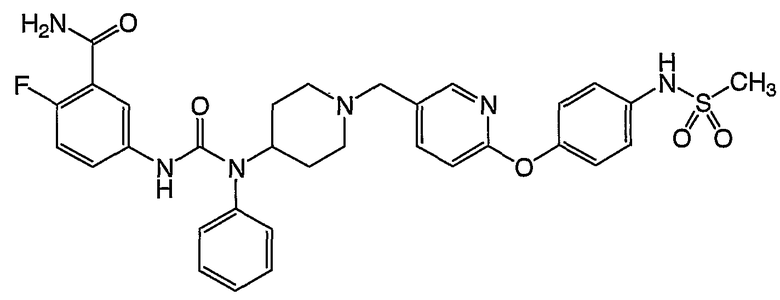
Свободное основание;
Белый аморфный порошок;
ТСХ:Rf 0,45 (дихлорметан: метанол= 9:1);
ЯМР (CDCl3): δ 1,32-1,48, 1,80-1,90, 2,08-2,20, 2,81-2,92, 3,00, 3,40, 4,55, 5,86, 5,97, 6,62-6,77, 6,85, 7,06, 7,11, 7,18-7,30, 7,34, 7,45-7,55, 7,61, 8,00, 8,04.
Гидрохлорид (или дигидрохлорид);
Белый аморфный порошок;
ТСХ:Rf 0,45 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,62-1,81, 2,12-2,23, 2,97, 3,12-3,35, 3,47-3,58, 4,29, 4,67, 7,07-7,16, 7,29-7,36, 7,43, 7,48-7,58, 7,68, 7,95, 8,22.
Пример 7(44)
4-фтор-N-{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}-N-фенилбензамид
ТСХ:Rf 0,58 (хлороформ: метанол= 7:1);
ЯМР (CDCl3): δ 1,50-1,70, 1,85-1,95, 2,10-2,30, 2,85-2,95, 2,98, 3,41, 4,72, 6,75-6,84, 6,95-6,98, 7,07, 7,19-7,25, 7,59, 7,99.
Пример 7(45)
N-[4-({5-[(4-{фенил[3-пиридиниламино)карбонил]амино}-1-пиперидинил)метил]-2-пиридинил}окси)фенил]метансульфонамид
ТСХ:Rf 0,40 (дихлорметан: метанол= 9:1);
ЯМР (CDCl3): δ 1,34-1,50, 1,80-1,90, 2,10-2,20, 2,80-2,90, 3,00, 3,40, 4,54, 5,87, 6,83, 7,09, 7,18, 7,20-7,28, 7,45-7,55, 7,59, 7,91, 7,99, 8,16, 8,20.
Пример 7(46)
N-(4-{[5-({4-[(аминокарбонил)(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид
ТСХ:Rf 0,38 (дихлорметан: метанол= 9:1);
ЯМР (CDCl3): δ 1,30-1,44, 1,76-1,85, 2,08-2,18, 2,80-2,88, 3,01, 3,39, 4,20, 4,48, 6,83, 6,90, 7,11, 7,13-7,18, 7,22-7,28, 7,35-7,45, 7,59, 7,98.
Пример 7(47)
N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(4-метоксифенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид
ТСХ:Rf 0,43 (дихлорметан: метанол= 9:1);
ЯМР (CDCl3): δ 1,31-1,49, 1,77-1,86, 2,09-2,18, 2,81-2,90, 3,01, 3,40, 3,86, 4,50, 5,85, 6,38, 6,84, 6,89, 6,96, 7,08-7,25, 7,60, 7,99.
Пример 7(48)
N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(3-метоксифенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид
ТСХ:Rf 0,43 (дихлорметан: метанол= 9:1);
ЯМР (CDCl3): δ 1,37-1,51, 1,80-1,89, 2,08-2,18, 2,81-2,90, 3,01, 3,40, 3,83, 4,51, 5,87, 6,38, 6,73, 6,80, 6,84, 6,90, 6,98, 7,08-7,26, 7,37, 7,60, 8,00.
Пример 7(49)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({3-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-8-азабицикло[3.2.1]окт-8-ил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,29 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,90-2,05, 2,20-2,30, 2,35-2,50, 2,60-2,75, 2,97, 3,85-3,95, 4,16, 4,55, 6,92-6,98, 7,06-7,14, 7,19-7,24, 7,29-7,33, 7,36-7,40, 7,48-7,58, 8,01, 8,25.
Пример 7(50)
Гидрохлорид (или дигидрохлорид) 4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}бензойной кислоты
ТСХ:Rf 0,39 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,65-1,80, 2,10-2,25, 3,10-3,30, 3,50-3,60, 4,30, 4,65, 6,92-6,98, 7,13, 7,19-7,24, 7,31-7,34, 7,49-7,55, 7,96, 8,08, 8,25.
Пример 7(51)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[{[(2,4-дифторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,63 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,65-1,80, 2,10-2,30, 2,98, 3,10-3,30, 3,50-3,60, 4,31, 4,70, 6,88-6,92, 7,09, 7,15, 7,32-7,34, 7,33, 7,51-7,58, 8,04, 8,29.
Пример 7(52)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[{[(3-фтор-4-метоксифенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,50 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,65-1,82, 2,12-2,22, 2,98, 3,12-3,28, 3,48-3,58, 3,79, 4,32, 4,67, 6,84-6,96, 7,09, 7,13-7,22, 7,28-7,38, 7,45-7,58, 8,05, 8,30.
Пример 7(53)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[{[(3-хлор-4-метоксифенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,50 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,68-1,82, 2,12-2,22, 2,98, 3,12-3,28, 3,48-3,58, 3,81, 4,32, 4,68, 6,92, 7,06, 7,09, 7,16, 7,30-7,38, 7,45-7,58, 8,05, 8,30.
Пример 7(54)
Дигидрохлорид (или тригидрохлорид) N-(4-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
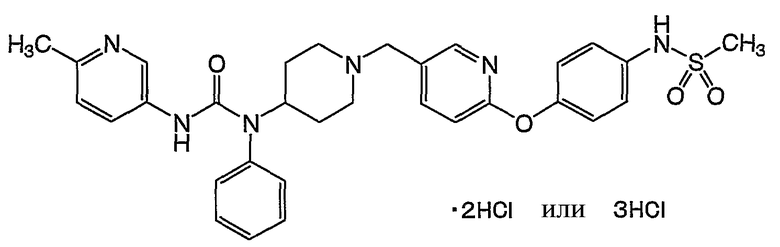
Аморфный порошок;
ТСХ:Rf 0,48 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,68-1,85, 2,12-2,25, 2,68, 2,97, 3,15-3,28, 3,50-3,60, 4,31, 4,71, 7,07, 7,13, 7,29-7,38, 7,50-7,62, 7,73, 8,01, 8,25, 8,31, 8,97.
Пример 7(55)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)ацетамида
Аморфный порошок;
ТСХ:Rf 0,23 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,60-1,80, 2,10-2,25, 3,10-3,25, 3,50-3,60, 3,55, 4,28, 4,70, 6,95, 7,04-7,10, 7,19-7,24, 7,31-7,38, 7,49-7,55, 7,93, 8,21.
Пример 7(56)
Дигидрохлорид N-{4-[4-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-3,5-диметил-1H-пиразол-1-ил]фенил}метансульфонамида
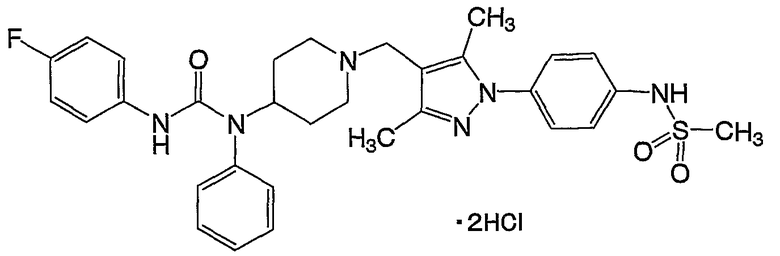
ТСХ:Rf 0,21 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,70-1,85, 2,10-2,25, 2,31, 2,33, 3,03, 3,20-3,35, 3,55-3,65, 4,20, 4,70, 6,96, 7,21-7,25, 7,33-7,41, 7,50-7,56.
Пример 7(57)
Тригидрохлорид 4-[4-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-3,5-диметил-1H-пиразол-1-ил]-N-[2-(4-морфолинил)этил]бензолсульфонамида
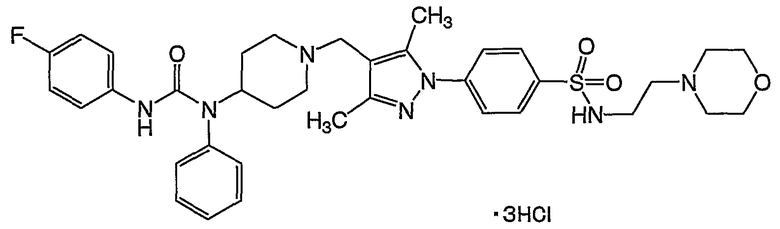
ТСХ:Rf 0,20 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,70-1,85, 2,10-2,25, 2,34, 2,41, 3,20-3,40, 3,50-3,65, 3,80-3,95, 4,00-4,15, 4,21, 4,70, 6,96, 7,20-7,25, 7,35, 7,45-7,56, 7,75, 8,05.
Пример 7(58)
Гидрохлорид (или дигидрохлорид) N-{4-[(5-{[4-((3,5-диметил-4-изоксазолил){[(4-фторфенил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]фенил}метансульфонамида
ТСХ:Rf 0,53 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,68-1,88, 2,09-2,23, 2,20, 2,40, 2,97, 3,12-3,25, 3,50-3,60, 4,32, 4,60, 6,99, 7,09, 7,13, 7,25-7,35, 8,01, 8,25.
Пример 7(59)
Дигидрохлорид (или тригидрохлорид) N-{4-[(5-{[4-(1,3-бензотиазол-6-ил{[(4-фторфенил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]фенил}метансульфонамида
ТСХ:Rf 0,49 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,68-1,85, 2,19-2,28, 2,97, 3,12-3,25, 3,50-3,60, 4,30, 4,71, 6,94, 7,07, 7,13, 7,23, 7,32, 7,51, 8,00, 8,15, 8,20, 8,25, 9,46.
Пример 7(60)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[{[(3,4-дифторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,51 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,64-1,81, 2,12-2,22, 2,97, 3,12-3,25, 3,48-3,58, 4,29, 4,68, 6,93, 7,02-7,15, 7,28-7,35, 7,38, 7,45-7,58, 7,95, 8,21.
Пример 7(61)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[[(2,3-дигидро-1,4-бензодиоксин-6-иламино)карбонил](фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,51 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,63-1,80, 2,12-2,22, 2,97, 3,11-3,25, 3,48-3,55, 4,17, 4,29, 4,68, 6,56, 6,66, 6,81, 7,07, 7,12, 7,27-7,35, 7,45-7,58, 7,96, 8,22.
Пример 7(62)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[{[(2,4-дифторфенил)амино]карбонил}(3-тиенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
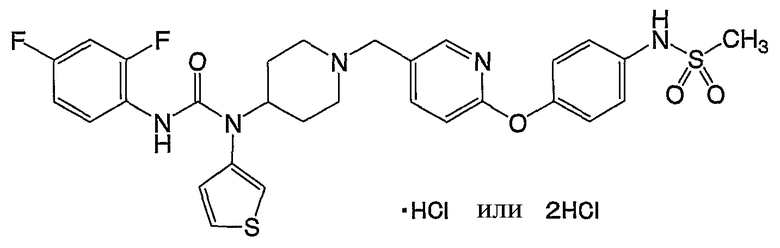
ТСХ:Rf 0,52 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,63-1,80, 2,12-2,22, 2,97, 3,12-3,25, 3,48-3,58, 4,28, 4,68, 6,85-6,98, 7,03-7,08, 7,11, 7,31, 7,53-7,60, 7,64, 7,89, 8,18.
Пример 7(63)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[{[(3,4-дифторфенил)амино]карбонил}(3-тиенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,52 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,62-1,80, 2,10-2,20, 2,97, 3,12-3,25, 3,48-3,58, 4,28, 4,68, 6,94-7,16, 7,31, 7,40, 7,51, 7,61, 7,90, 8,18.
Пример 7(64)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(2-метоксифенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,52 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,61-1,83, 2,15-2,25, 2,97, 3,10-3,22, 3,48-3,56, 3,84, 4,28, 4,58, 6,95, 7,05-7,29, 7,32, 7,46, 7,97, 8,23.
Пример 7(65)
Гидрохлорид (или дигидрохлорид) N-{4-[(5-{[4-((4-фторфенил){[(4-фторфенил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]фенил}метансульфонамида
ТСХ:Rf 0,52 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,60-1,78, 2,12-2,21, 2,97, 3,10-3,25, 3,48-3,58, 4,28, 4,65, 6,95, 7,05, 7,09, 7,19-7,37, 7,90, 8,17.
Пример 7(66)
Гидрохлорид (или дигидрохлорид) N-{4-[(5-{[4-((3-фторфенил){[(4-фторфенил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]фенил}метансульфонамида
ТСХ:Rf 0,52 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,65-1,85, 2,12-2,25, 2,97, 3,12-3,25, 3,48-3,58, 4,28, 4,65, 6,95, 7,04-7,20, 7,22-7,33, 7,30, 7,53, 7,90, 8,17.
Пример 7(67)
Гидрохлорид (или дигидрохлорид) N'-(4-хлорфенил)-N-[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]-N-фенилмочевины
ТСХ:Rf 0,26 (этил ацетат);
ЯМР (CD3OD): δ 1,60-1,80, 2,10-2,30, 3,10-3,30, 3,14, 3,50-3,60, 4,30, 4,65, 7,17-7,23, 7,31-7,39, 7,52-7,55, 7,90-8,02, 8,21.
Пример 7(68)
Гидрохлорид (или дигидрохлорид) N'-(4-фторфенил)-N-[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]-N-(3-тиенил)мочевины
ТСХ:Rf 0,29 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,60-1,80, 2,05-2,20, 3,14, 3,15-3,25, 3,50-3,60, 4,29, 4,65, 6,97, 7,04, 7,18-7,27, 7,38, 7,52, 7,61, 7,96-8,02, 8,23.
Пример 7(69)
Гидрохлорид (или дигидрохлорид) 2-хлор-N-метил-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамида
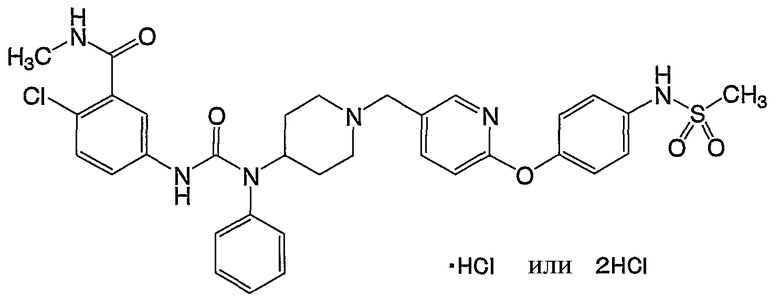
ТСХ:Rf 0,50 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,65-1,81, 2,12-2,22, 2,86, 2,97, 3,12-3,25, 3,49-3,58, 4,29, 4,67, 7,07, 7,13, 7,25-7,35, 7,43, 7,46-7,60, 7,96, 8,22.
Пример 7(70)
Гидрохлорид (или дигидрохлорид) 2-хлор-N,N-диметил-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамида
ТСХ:Rf 0,50 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,65-1,81, 2,12-2,22, 2,86, 2,97, 3,08, 3,12-3,25, 3,49-3,58, 4,30, 4,67, 7,08, 7,14, 7,27-7,36, 7,48-7,60, 7,99, 8,25.
Пример 7(71)
N-(4-{[5-({4-[{[(4-хлор-3-нитрофенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид
ТСХ:Rf 0,39 (хлороформ: метанол= 7:1);
ЯМР (CDCl3): δ 1,40-1,60, 1,80-1,90, 2,10-2,20, 2,80-2,90, 2,99, 3,46, 4,51, 4,64, 6,08, 6,84, 7,09, 7,21-7,27, 7,31-7,41, 7,51-7,54, 7,61, 7,89, 8,01.
Пример 7(72)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[({[4-(метилсульфонил)фенил]амино}карбонил)(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,52 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,65-1,85, 2,10-2,30, 2,97, 3,05, 3,10-3,30, 3,50-3,60, 4,29, 4,70, 7,06, 7,11, 7,30-7,35, 7,32, 7,51-7,58, 7,77, 7,94, 8,20.
Пример 7(73)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[({[3-(метилсульфонил)фенил]амино}карбонил)(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,49 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,65-1,85, 2,10-2,25, 2,98, 3,07, 3,10-3,30, 3,50-3,60, 4,31, 4,70, 7,08, 7,15, 7,31-7,36, 7,44-7,59, 8,02, 8,02, 8,26.
Пример 7(74)
Гидрохлорид 2-хлор-5-({[[1-(4-{4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил](фенил)амино]карбонил}амино)бензамида
ТСХ:Rf 0,43 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,62-1,79, 2,12-2,22, 2,95, 3,10-3,22, 3,45-3,55, 4,22, 4,67, 7,01, 7,02, 7,25-7,34, 7,41, 7,46-7,58.
Пример 7(75)
Гидрохлорид (или дигидрохлорид) N-(4-{[5-({4-[({[4-хлор-3-(4-морфолинилкарбонил)фенил]амино}карбонил)(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
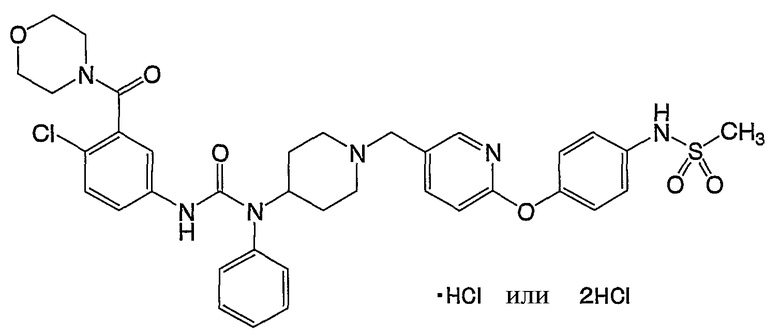
ТСХ:Rf 0,43 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,65-1,82, 2,12-2,22, 2,98, 3,14-3,35, 3,49-3,80, 4,31, 4,67, 7,08, 7,14, 7,28-7,37, 7,45-7,59, 8,02, 8,27.
Пример 7(76)
Гидрохлорид (или дигидрохлорид) 2-хлор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензойной кислоты
ТСХ:Rf 0,48 (дихлорметан: метанол= 5:1);
ЯМР (CD3OD): δ 1,64-1,82, 2,12-2,25, 2,97, 3,12-3,24, 3,47-3,60, 4,29, 4,67, 7,06, 7,11, 7,28-7,36, 7,41, 7,45-7,60, 7,82, 7,94, 8,20.
Пример 7(77)
N'-(4-хлор-3-нитрофенил)-N-[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]-N-фенилмочевины
ТСХ:Rf 0,50 (этил ацетат);
ЯМР (CDCl3): δ 1,35-1,55, 1,80-1,90, 2,10-2,25, 2,90-3,00, 3,06, 3,44, 4,50, 6,04, 6,93, 7,20-7,39, 7,31-7,41, 7,50-7,53, 7,67, 7,92-8,05.
Пример 7(78)
Гидрохлорид 2-[4-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)фенокси]-5-[(метилсульфонил)амино]бензамида
ТСХ:Rf 0,53 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,62-1,79, 2,12-2,21, 2,99, 3,08-3,22, 3,43-3,57, 4,23, 4,67, 6,95, 7,01, 7,06, 7,22, 7,29-7,35, 7,32-7,59, 7,70.
Пример 7(79)
Гидрохлорид (или дигидрохлорид) 2-фтор-5-({[[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил](фенил)амино]карбонил}амино)бензамида
ТСХ:Rf 0,45 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,64-1,81, 2,13-2,25, 3,14, 3,10-3,25, 3,50-3,58, 4,31, 4,67, 7,08, 7,19, 7,30-7,58, 7,69, 7,95-8,04, 8,23.
Пример 7(80)
Гидрохлорид (или дигидрохлорид) 2-фтор-5-{[((3-фторфенил){1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}бензамида
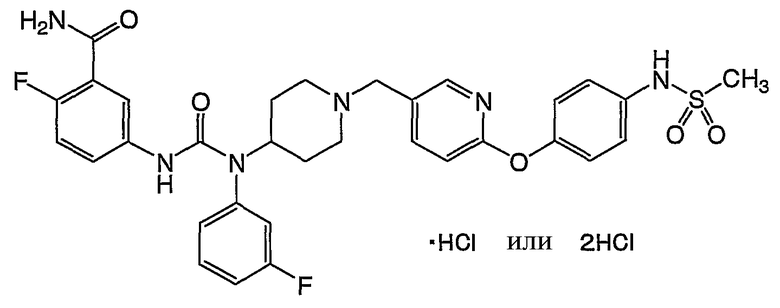
ТСХ:Rf 0,49 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,68-1,85, 2,14-2,23, 2,97, 3,12-3,25, 3,50-3,58, 4,30, 4,65, 7,04-7,19, 7,25, 7,31, 7,46, 7,51, 7,70, 7,92, 8,23.
Пример 7(81)
Гидрохлорид (или дигидрохлорид) 2-фтор-5-[({(3-фторфенил)[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]амино}карбонил)амино]бензамида
ТСХ:Rf 0,52 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,68-1,87, 2,15-2,25, 3,14, 3,12-3,25, 3,50-3,58, 4,31, 4,67, 7,09, 7,12-7,20, 7,25, 7,37, 7,46, 7,54, 7,71, 7,90-8,04, 8,23.
Пример 7(82)
Гидрохлорид (или дигидрохлорид) 2-фтор-5-[({(3-фторфенил)[1-({6-[2-метокси-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]амино}карбонил)амино]бензамида
ТСХ:Rf 0,52 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,67-1,85, 2,15-2,25, 3,17, 3,12-3,25, 3,48-3,58, 3,80, 4,28, 4,65, 7,04-7,19, 7,25, 7,35, 7,46, 7,50-7,65, 7,71, 7,95, 8,13.
Пример 7(83)
Гидрохлорид (или дигидрохлорид) N-[2-фтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)фенил]ацетамида
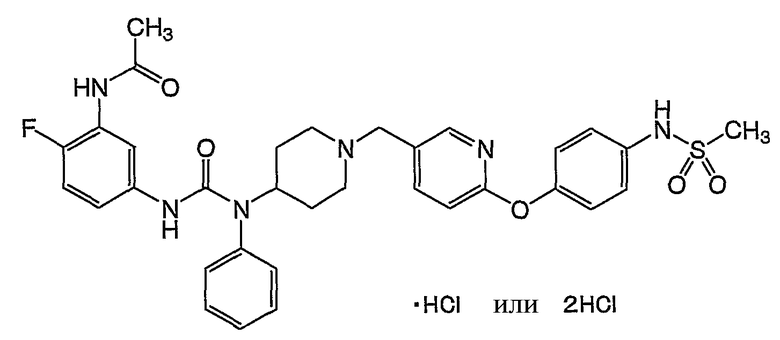
Белый аморфный порошок;
ТСХ:Rf 0,36 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,60-1,80, 2,10-2,30, 2,12, 2,97, 3,10-3,25, 3,45-3,55, 4,27, 4,65, 7,00-7,12, 7,30-7,33, 7,49-7,55, 7,78, 7,90, 8,18.
Пример 7(84)
Гидрохлорид (или дигидрохлорид) N-[2-фтор-5-({[{1-[(6-{2-метокси-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)фенил]ацетамида
ТСХ:Rf 0,31 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,60-1,80, 2,10-2,30, 2,12, 2,99, 3,10-3,25, 3,45-3,55, 3,69, 4,26, 4,65, 6,87, 6,98-7,08, 7,06, 7,31-7,34, 7,49-7,55, 7,78, 7,86, 8,11.
Пример 7(85)
Гидрохлорид (или дигидрохлорид) N-[2-фтор-5-({[[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил](фенил)амино]карбонил}амино)фенил]ацетамида
ТСХ:Rf 0,53 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,60-1,80, 2,10-2,30, 2,12, 3,10-3,25, 3,14, 3,45-3,55, 4,30, 4,65, 7,00-7,05, 7,19, 7,31-7,39, 7,50-7,55, 7,90, 7,94-8,02, 8,11.
Пример 7(86)
Гидрохлорид (или дигидрохлорид) N-[2-фтор-5-({[[1-({6-[2-метокси-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил](фенил)амино]карбонил}амино)фенил]ацетамида
ТСХ:Rf 0,52 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,60-1,80, 2,10-2,30, 2,12, 3,10-3,25, 3,17, 3,45-3,55, 3,79, 4,26, 4,66, 7,00-7,11, 7,19, 7,31-7,36, 7,49-7,63, 7,78, 7,78, 8,11.
Пример 7(87)
Гидрохлорид (или дигидрохлорид) 2-фтор-5-{[((3-фторфенил){1-[(6-{2-метокси-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}бензамида
ТСХ:Rf 0,44 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,69-1,85, 2,12-2,25, 3,00, 3,12-3,25, 3,48-3,58, 3,70, 4,28, 4,65, 6,87, 6,99-7,19, 7,25, 7,46, 7,54, 7,71, 7,93, 8,17.
Пример 7(88)
Гидрохлорид (или дигидрохлорид) 2-фтор-5-({[{1-[(6-{2-метокси-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамида
ТСХ:Rf 0,44 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,64-1,81, 2,12-2,24, 3,00, 3,12-3,25, 3,48-3,58, 3,70, 4,28, 4,67, 6,87, 7,00-7,12, 7,29-7,35, 7,42, 7,47-7,58, 7,68, 7,94, 8,18.
Пример 7(89)
Гидрохлорид (или дигидрохлорид) 2-фтор-5-({[[1-({6-[2-метокси-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил](фенил)амино]карбонил}амино)бензамида
ТСХ:Rf 0,44 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,64-1,80, 2,12-2,22, 3,17, 3,12-3,25, 3,48-3,58, 3,79, 4,28, 4,67, 7,04-7,14, 7,29-7,38, 7,43, 7,48-7,64, 7,68, 7,94, 8,13.
Пример 7(90)
Дигидрохлорид (или тригидрохлорид) N-{4-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]фенил}метансульфонамида
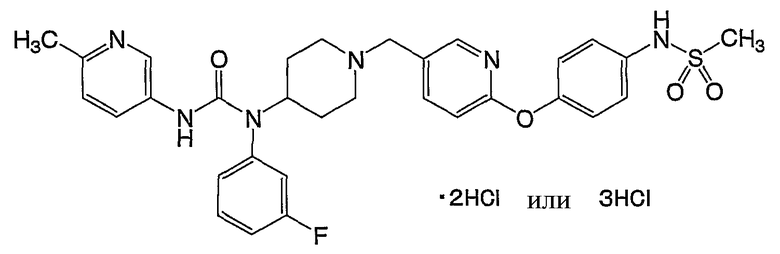
Белый аморфный порошок;
ТСХ:Rf 0,49 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,70-1,90, 2,12-2,25, 2,68, 2,97, 3,12-3,35, 3,48-3,60, 4,33, 4,70, 7,08, 7,12-7,23, 7,25-7,35, 7,55, 7,73, 8,05, 8,23-8,34, 8,96.
Пример 7(91)
Дигидрохлорид (или тригидрохлорид) N-(3-фторфенил)-N'-(6-метил-3-пиридинил)-N-[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]мочевины
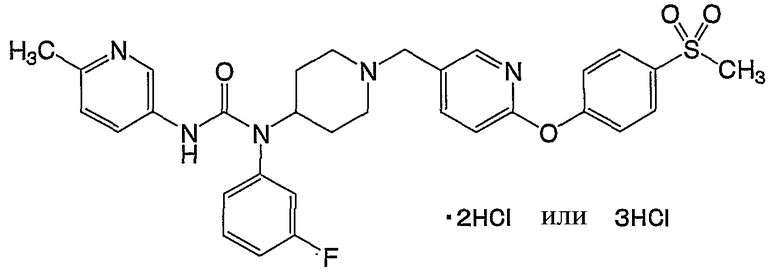
ТСХ:Rf 0,50 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,70-1,90, 2,12-2,25, 2,68, 3,14, 3,12-3,35, 3,48-3,60, 4,33, 4,70, 7,12-7,21, 7,29, 7,38, 7,56, 7,73, 8,00, 8,03, 8,22-8,36, 8,96.
Пример 7(92)
Дигидрохлорид (или тригидрохлорид) N-(3-фторфенил)-N-[1-({6-[2-метокси-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]-N'-(6-метил-3-пиридинил)мочевины
ТСХ:Rf 0,50 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,70-1,90, 2,12-2,25, 2,68, 3,17, 3,12-3,35, 3,48-3,60, 3,80, 4,30, 4,70, 7,12, 7,15-7,23, 7,29, 7,35, 7,51-7,64, 7,73, 7,99, 8,15, 8,31, 8,96.
Пример 7(93)
Гидрохлорид (или дигидрохлорид) N-[2-фтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)фенил]метансульфонамида
ТСХ:Rf 0,33 (этил ацетат: метанол= 10:1);
ЯМР (CD3OD): δ 1,60-1,80, 2,10-2,30, 2,97, 2,97, 3,10-3,25, 3,40-3,60, 4,27, 4,65, 7,03-7,11, 7,29-7,33, 7,44-7,54, 7,87, 8,16.
Пример 7(94)
Гидрохлорид (или дигидрохлорид) N-[2-фтор-5-({[[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил](фенил)амино]карбонил}амино)фенил]метансульфонамида
ТСХ:Rf 0,41 (этил ацетат: метанол= 10:1);
ЯМР (CD3OD): δ 1,60-1,80, 2,10-2,30, 2,97, 3,14, 3,15-3,25, 3,45-3,55, 4,30, 4,62, 7,03-7,06, 7,18, 7,31-7,39, 7,44-7,54, 7,95-8,02, 8,22.
Пример 7(95)
Гидрохлорид (или дигидрохлорид) N-[2-фтор-5-({[[1-({6-[2-метокси-4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил](фенил)амино]карбонил}амино)фенил]метансульфонамида
ТСХ:Rf 0,39 (этил ацетат: метанол= 10:1);
ЯМР (CD3OD): δ 1,60-1,80, 2,10-2,25, 2,97, 3,10-3,25, 3,17, 3,45-3,55, 3,79, 4,26, 4,65, 7,03-7,06, 7,12, 7,31-7,36, 7,45-7,63, 7,91, 8,10.
Пример 7(96)
Гидрохлорид 2-[4-({4-[[({4-фтор-3-[(метилсульфонил)амино]фенил}амино)карбонил](фенил)амино]-1-пиперидинил}метил)фенокси]-5-[(метилсульфонил)амино]бензамида
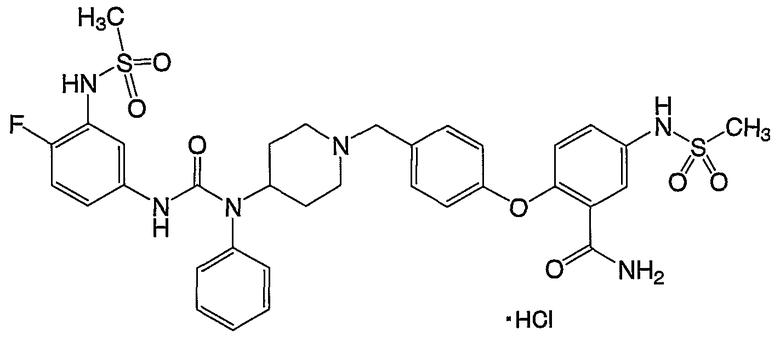
ТСХ:Rf 0,20 (этил ацетат: метанол= 10:1);
ЯМР (CD3OD): δ 1,60-1,80, 2,10-2,30, 2,97, 2,99, 3,10-3,20, 3,45-3,55, 4,23, 4,65, 6,99-7,04, 7,31-7,55, 7,69.
Пример 7(97)
Гидрохлорид (или дигидрохлорид) 2-фтор-N-метил-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамида
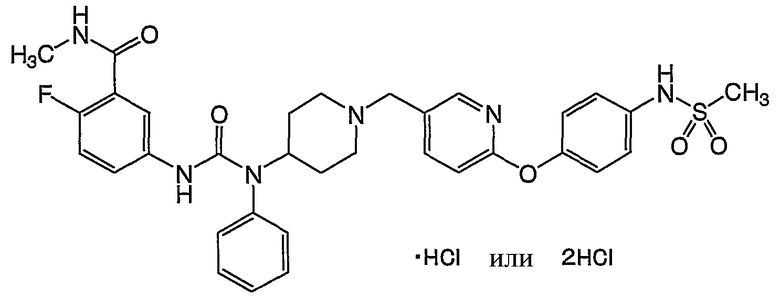
ТСХ:Rf 0,50 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,65-1,81, 2,12-2,23, 2,89, 2,97, 3,12-3,25, 3,48-3,58, 4,29, 4,67, 7,01-7,15, 7,27-7,35, 7,40, 7,47-7,57, 7,61, 7,95, 8,21.
Пример 7(98)
Гидрохлорид (или дигидрохлорид) 2-фтор-N-метил-5-({[[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил](фенил)амино]карбонил}амино)бензамида
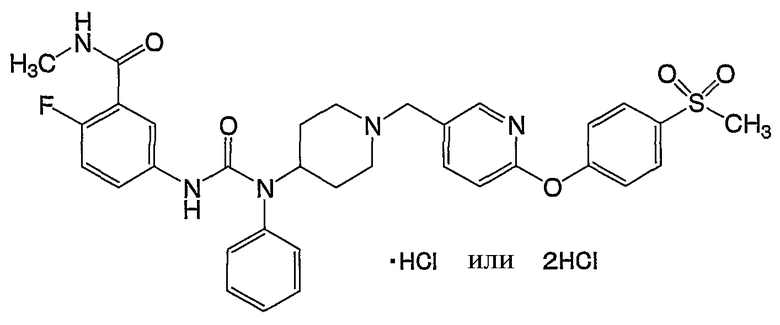
ТСХ:Rf 0,50 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,65-1,81, 2,12-2,23, 2,89, 3,14, 3,12-3,25, 3,48-3,59, 4,30, 4,67, 7,06, 7,18, 7,30-7,43, 7,47-7,57, 7,61, 7,94-8,05, 8,22.
Пример 7(99)
Дигидрохлорид (или тригидрохлорид) N'-(6-метил-3-пиридинил)-N-[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]-N-фенилмочевины
ТСХ:Rf 0,49 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,70-1,87, 2,12-2,24, 2,68, 3,14, 3,17-3,35, 3,50-3,60, 4,33, 4,71, 7,18, 7,32-7,36, 7,38, 7,42-7,59, 7,72, 8,00, 8,05, 8,27, 8,30, 8,96.
Пример 7(100)
Гидрохлорид 2-[4-({4-[({[3-(ацетиламино)-4-фторфенил]амино}карбонил)(фенил)амино]-1-пиперидинил}метил)фенокси]-5-[(метилсульфонил)амино]бензамида
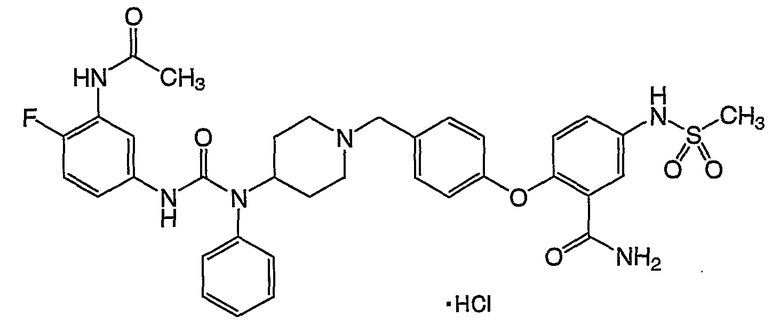
ТСХ:Rf 0,43 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,61-1,80, 2,12, 2,05-2,22, 2,99, 3,05-3,21, 3,45-3,55, 4,23, 4,67, 6,97-7,08, 7,28-7,35, 7,35-7,58, 7,69, 7,77.
Пример 7(101)
Дигидрохлорид (или тригидрохлорид) N-(3-метил-4-([5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,48 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,68-1,85, 2,11, 2,12-2,23, 2,67, 2,97, 3,12-3,28, 3,50-3,60, 4,30, 4,71, 7,02, 7,04, 7,15, 7,20, 7,31-7,38, 7,49-7,60, 7,73, 8,00, 8,17, 8,22, 8,31, 8,96.
Пример 7(102)
Дигидрохлорид (или тригидрохлорид) N-(3-хлор-4-([5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,48 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,65-1,85, 2,12-2,25, 2,67, 3,01, 3,15-3,28, 3,48-3,58, 4,30, 4,72, 7,12, 7,19-7,28, 7,31-7,37, 7,41, 7,48-7,60, 7,74, 7,98, 8,17, 8,30, 8,97.
Пример 7(103)
Дигидрохлорид (или тригидрохлорид) N-(4-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)этансульфонамида
ТСХ:Rf 0,48 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,32, 1,70-1,85, 2,15-2,25, 2,68, 3,11, 3,15-3,28, 3,50-3,60, 4,33, 4,71, 7,08, 7,14, 7,30-7,38, 7,50-7,60, 7,73, 8,07, 8,28-8,35, 8,96.
Пример 7(104)
Дигидрохлорид (или тригидрохлорид) N-{4-[(5-{[4-((3-метилфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]фенил}метансульфонамида
ТСХ:Rf 0,48 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,68-1,87, 2,12-2,23, 2,41, 2,68, 2,97, 3,13-3,28, 3,50-3,60, 4,31, 4,71, 7,05-7,18, 7,29-7,37, 7,43, 7,73, 8,01, 8,13, 8,26, 8,31, 8,96.
Пример 7(105)
Гидрохлорид (или дигидрохлорид) 2-фтор-5-{[((3-метилфенил){1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}бензамида
ТСХ:Rf 0,46 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,65-1,81, 2,12-2,24, 2,40, 2,97, 3,13-3,28, 3,48-3,58, 4,29, 4,67, 7,04-7,17, 7,28-7,35, 7,37-7,47, 7,68, 7,95, 8,21.
Пример 7(106)
Гидрохлорид (или дигидрохлорид) 2-фтор-N-метил-5-{[((3-метилфенил){1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}бензамида
ТСХ:Rf 0,49 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,65-1,81, 2,12-2,22, 2,40, 2,89, 2,97, 3,12-3,26, 3,48-3,58, 4,30, 4,67, 7,02-7,18, 7,28-7,35, 7,36-7,44, 7,61, 7,99, 8,25.
Пример 7(107)
Гидрохлорид (или дигидрохлорид) N-(2-фтор-5-{[((3-метилфенил){1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}фенил)ацетамида
ТСХ:Rf 0,45 (этил ацетат: метанол= 10:1);
ЯМР (CD3OD): δ 1,60-1,80, 2,10-2,25, 2,12, 2,40, 2,97, 3,10-3,30, 3,50-3,60, 4,27, 4,65, 7,00-7,15, 7,30, 7,31, 7,42, 7,78, 7,90, 8,17.
Пример 7(108)
Гидрохлорид (или дигидрохлорид) N-(2-фтор-5-{[((3-фторфенил){1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}фенил)ацетамида
ТСХ:Rf 0,46 (этил ацетат: метанол= 10:1);
ЯМР (CD3OD): δ 1,60-1,80, 2,10-2,25, 2,13, 2,97, 3,10-3,30, 3,50-3,60, 4,28, 4,65, 6,98-7,17, 7,29, 7,31, 7,54, 7,82, 7,94, 8,20.
Пример 7(109)
Тригидрохлорид N-(4-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиразинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,49 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,71-1,88, 2,15-2,26, 2,68, 2,97, 3,22-3,35, 3,58-3,68, 4,42, 4,75, 7,17, 7,29-7,38, 7,52-7,62, 7,73, 8,17, 8,20, 8,31, 8,48, 8,97.
Пример 7(110)
Гидрохлорид (или дигидрохлорид) 2-фтор-5-{[((3-фторфенил){1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-N-метилбензамида
ТСХ:Rf 0,45 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,70-1,85, 2,15-2,23, 2,89, 2,97, 3,12-3,25, 3,50-3,58, 4,30, 4,65, 7,03-7,19, 7,25, 7,32, 7,42, 7,54, 7,65, 7,99, 8,25.
Пример 7(111)
Дигидрохлорид (или тригидрохлорид) N-(4-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-азепанил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,42 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,70-2,50, 2,67, 2,98, 3,18-3,35, 3,40-3,62, 4,37, 4,50, 7,10, 7,16, 7,30-7,40, 7,48-7,60, 7,72, 8,12, 8,29, 8,33, 8,96.
Пример 7(112)
Дигидрохлорид (или тригидрохлорид) N-(4-{[5-({(3R)-3-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пирролидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,48 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 2,40, 2,65, 2,69, 2,98, 3,41-3,65, 3,80-3,98, 4,30-4,72, 7,08-7,20, 7,28-7,62, 7,74, 8,14, 8,32, 8,39, 8,51, 8,97.
Пример 7(113)
Дигидрохлорид (или тригидрохлорид) N-(4-{[5-({(3S)-3-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пирролидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
ТСХ:Rf 0,48 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 2,40, 2,65, 2,69, 2,98, 3,41-3,65, 3,80-3,98, 4,30-4,72, 7,08-7,20, 7,28-7,62, 7,74, 8,14, 8,32, 8,39, 8,51, 8,97.
Пример 7(114)
Гидрохлорид (или дигидрохлорид) N-(2-фтор-5-{[((3-фторфенил){1-[(6-{2-метил-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}фенил)ацетамида
ТСХ:Rf 0,29 (этил ацетат: метанол= 10:1);
ЯМР (CD3OD): δ 1,65-1,90, 2,00-2,20, 2,11, 2,12, 2,97, 3,10-3,30, 3,50-3,60, 4,27, 4,63, 6,98-7,06, 7,13-7,27, 7,53, 7,81, 7,94, 8,17.
Пример 7(115)
Гидрохлорид (или дигидрохлорид) N-[5-({[{1-[(6-{4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(3-фторфенил)амино]карбонил}амино)-2-фторфенил]ацетамида
ТСХ:Rf 0,24 (этил ацетат: метанол= 10:1);
ЯМР (CD3OD): δ 1,32, 1,60-1,80, 2,10-2,30, 2,12, 3,08, 3,10-3,25, 3,50-3,60, 4,29, 4,70, 7,00-7,16, 7,25, 7,31, 7,54, 7,81, 7,95, 8,22.
Пример 7(116)
Гидрохлорид (или дигидрохлорид) 2-фтор-5-({[{1-[(6-{2-метил-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамида
ТСХ:Rf 0,48 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,68-1,82, 2,12, 2,09-2,22, 2,98, 3,12-3,25, 3,48-3,59, 4,31, 4,68, 7,01-7,23, 7,30-7,37, 7,43, 7,47-7,58, 7,68, 8,03, 8,27.
Пример 7(117)
Гидрохлорид (или дигидрохлорид) 5-({[{1-[(6-{4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)-2-фторбензамида
ТСХ:Rf 0,48 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,32, 1,65-1,82, 2,12-2,22, 3,10, 3,10-3,25, 3,49-3,58, 4,31, 4,68, 7,05-7,10, 7,13, 7,29-7,36, 7,43, 7,47-7,58, 7,68, 8,02, 8,28.
Пример 7(118)
Дигидрохлорид (или тригидрохлорид) N-{4-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]фенил}этансульфонамида
ТСХ:Rf 0,46 (дихлорметан: метанол= 9:1);
ЯМР (CD3OD): δ 1,32, 1,72-1,90, 2,12-2,25, 2,68, 3,11, 3,18-3,30, 3,50-3,60, 4,34, 4,70, 7,07-7,23, 7,29, 7,33, 7,56, 7,74, 8,10, 8,29-8,38, 8,97.
Пример 7(119)
Дигидрохлорид (или тригидрохлорид) 2-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-5-[(метилсульфонил)амино]бензамида
ТСХ:Rf 0,69 (хлороформ: метанол= 5:1);
ЯМР (CD3OD): δ 1,70-1,90, 2,10-2,30, 2,68, 2,93, 3,20-3,40, 3,50-3,60, 4,41, 4,70, 7,04, 7,33-7,43, 7,50-7,60, 7,73, 7,96, 8,17, 8,27, 8,30, 8,54, 8,96.
Пример 7(120)
Дигидрохлорид (или тригидрохлорид) 2-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]-5-[(метилсульфонил)амино]бензамида
ТСХ:Rf 0,59 (хлороформ: метанол= 5:1);
ЯМР (CD3OD): δ 1,70-1,90, 2,10-2,30, 2,68, 2,93, 3,20-3,40, 3,50-3,70, 4,41, 4,70, 7,03, 7,15-7,20, 7,30, 7,41, 7,56, 7,74, 7,96, 8,25-8,35, 8,39, 8,54, 8,97.
Пример 7(121)
Гидрохлорид (или дигидрохлорид) 2-{[5-({4-[({[3-(ацетиламино)-4-фторфенил]амино}карбонил)(3-фторфенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-5-[(метилсульфонил)амино]бензамида
ТСХ:Rf 0,56 (хлороформ: метанол= 5:1);
ЯМР (CD3OD): δ 1,70-1,90, 2,10-2,30, 2,12, 2,93, 3,20-3,40, 3,50-3,70, 4,37, 4,65, 6,99-7,10, 7,03, 7,15-7,20, 7,25, 7,40, 7,54, 7,82, 7,96, 8,15, 8,28, 8,49.
Пример 8
Гидрохлорид (или дигидрохлорид) 4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-N-(2-метоксиэтил)бензамида
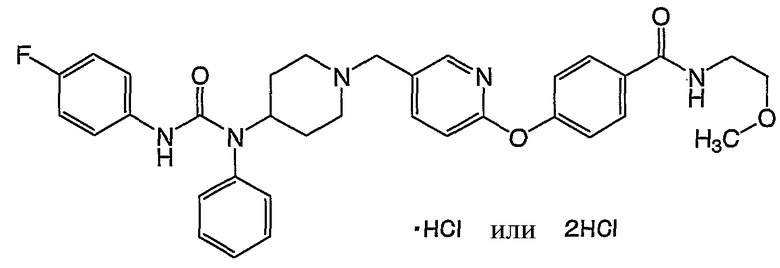
К раствору соединения, полученного в Примере 7(50) (80 мг) в N,N-диметилформамиде (3 мл), добавляли гексафторфосфат О-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония (84 мг), диизопропилэтиламин (38 мкл) и 1-метоксиэтиламин (19 мкл) и смесь перемешивали в течение ночи. К реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия и смесь экстрагировали этилацетатом. Органический слой сушили безводным сульфатом натрия, концентрировали. Полученный остаток обрабатывали 4 н. хлористым водородом в растворе этилацетата, с получением указанного в заголовке соединения(65 мг), имеющего следующие физические данные.
ТСХ:Rf 0,49 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,65-1,80, 2,10-2,25, 3,10-3,30, 3,30-3,40, 3,50-3,60, 3,56, 4,29, 4,70, 6,92-6,98, 7,11, 7,19-7,24, 7,31-7,34, 7,52-7,55, 7,89, 7,90, 8,20.
Пример 8(1)
Гидрохлорид (или дигидрохлорид) N'-(4-фторфенил)-N-[1-({6-[4-(4-морфолинилкарбонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]-N-фенилмочевины
С помощью процедуры, аналогичной описанной в Примере 8, с использованием морфолина вместо 1-метоксиэтиламина, получали следующее указанное в заголовке соединение, имеющее следующие физические данные.
ТСХ:Rf 0,51 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,65-1,80, 2,10-2,25, 3,10-3,25, 3,40-3,55, 3,55-3,80, 4,26, 4,65, 6,92-6,95, 7,11, 7,19-7,23, 7,32-7,34, 7,49-7,55, 7,94, 8,18.
Пример 9
Дигидрохлорид (или тригидрохлорид) N-(4-{[5-({4-[{[(3-амино-4-хлорфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида
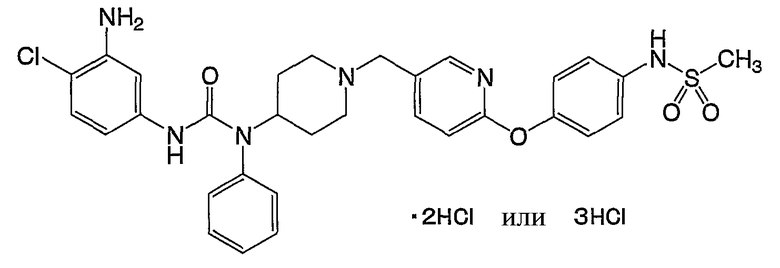
К раствору соединения, полученного в Примере 7(71) (720 мг) в уксусной кислоте (10 мл) и воде (10 мл), добавляли железный порошок (244 мг) и смесь перемешивали в течение 2 часов при 40°С. Реакционную смесь фильтровали через Целит (зарегистрированный товарный знак). После того, как фильтрат нейтрализовали 1 н. водным раствором гидроксида натрия, его экстрагировали этилацетатом. Органический слой промывали водой и солевым раствором, сушили безводным сульфатом натрия и концентрировали. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле (дихлорметан: метанол = 20:1). Данное свободное основание обрабатывали 4 н. хлористым водородом в растворе этилацетата, с получением указанного в заголовке соединения (420 мг), имеющего следующие физические данные.
ТСХ:Rf 0,48 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,65-1,80, 2,10-2,30, 2,97, 3,10-3,25, 3,50-3,60, 4,28, 4,70, 7,05, 7,10, 7,15, 7,29-7,32, 7,30, 7,37, 7,50-7,55, 7,72, 7,90, 8,17.
Пример 10
Гидрохлорид (или дигидрохлорид) N-[2-хлор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)фенил]метансульфонамида
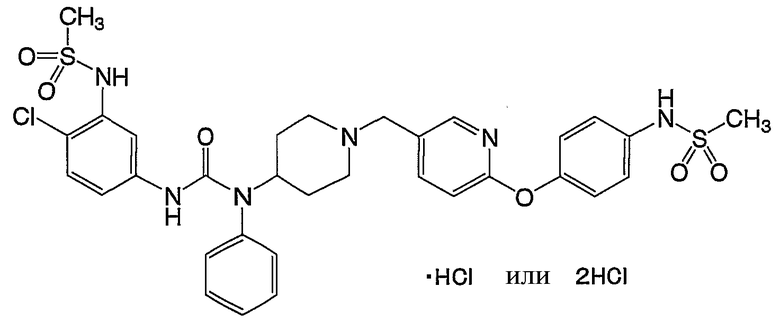
К смеси соединения свободного основания, полученного в Примере 9 (160 мг), и триэтиламина (36 мкл) в тетрагидрофуране (5 мл) добавляли метансульфонилхлорид (20 мкл) и смесь перемешивали в течение ночи при комнатной температуре. Реакционную смесь экстрагировали этилацетатом, сушили безводным сульфатом натрия и концентрировали. Полученный остаток растворяли в тетрагидрофуране (10 мл) и к данному раствору добавляли фтористый тетрабутиламмоний (146 мкл). Смесь перемешивали в течение 3 часов при 60°С. К смеси добавляли воду и экстрагировали этилацетатом. Органический слой промывали водой и солевым раствором, сушили безводным сульфатом натрия и концентрировали. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле (дихлорметан: метанол = 20:1). Полученное соединение обрабатывали 4 н. хлористым водородом в растворе этилацетата, с получением указанного в заголовке соединения (35 мг), имеющего следующие физические данные.
ТСХ:Rf 0,48 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,65-1,80, 2,10-2,25, 2,97, 2,97, 3,10-3,25, 3,50-3,60, 4,29, 4,70, 7,06, 7,10-7,15, 7,28-7,34, 7,52-7,58, 7,94, 8,21.
Пример 11
Гидрохлорид (или дигидрохлорид) N-[2-хлор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)фенил]ацетамида
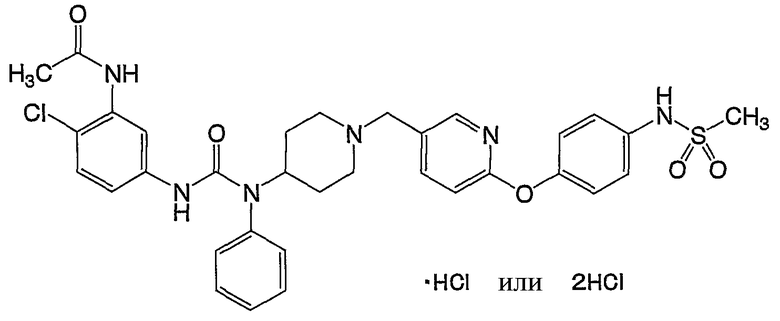
К раствору соединения свободного основания, полученного в Примере 9 (160 мг) в пиридине (4 мл), добавляли ангидрид уксусной кислоты (72,4 мкл) и смесь перемешивали в течение ночи при комнатной температуре. Реакционную смесь экстрагировали этилацетатом, сушили безводным сульфатом натрия и концентрировали. К раствору полученного остатка, в метаноле (4 мл), добавляли 28% метоксид натрия в растворе метанола (506 мкл) и все перемешивали в течение 30 минут при комнатной температуре. Реакционную смесь концентрировали, добавляли воду и смесь экстрагировали этилацетатом. Органический слой промывали водой и солевым раствором, сушили безводным сульфатом натрия и концентрировали. Полученный остаток обрабатывали 4 н. хлористым водородом в растворе этилацетата, с получением указанного в заголовке соединения (64 мг), имеющего следующие физические данные.
ТСХ:Rf 0,40 (хлороформ: метанол= 10:1);
ЯМР (CD3OD): δ 1,65-1,80, 2,13, 2,15-2,25, 2,97, 3,10-3,35, 3,50-3,60, 4,30, 4,65, 7,07, 7,12-7,16, 7,25-7,34, 7,49-7,51, 7,68, 7,99, 8,25.
Пример 12
Гидрохлорид (или дигидрохлорид) N-[2-хлор-5-({[[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил](фенил)амино]карбонил}амино)фенил]ацетамида
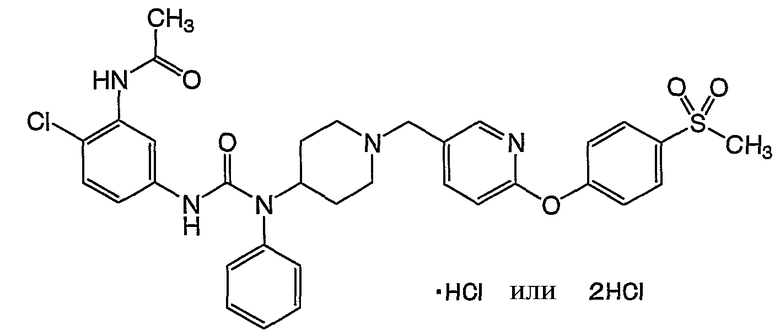
К раствору аминового соединения, полученного с помощью восстановления, процедура которого описана в Примере 9, с использованием соединения, полученного в Примере 7(77) (160 мг) и 1,8-диазабицикло[5.4.0]ундец-7-ена (34 мкл) в тетрагидрофуране (5 мл), добавляли ангидрид уксусной кислоты (63 мкл) и смесь нагревали с обратным холодильником в течение 4 часов. Реакционную смесь выливали в воду и экстрагировали этилацетатом. Органический слой промывали водой и солевым раствором, сушили над безводным сульфатом натрия и концентрировали. К раствору полученного остатка в метаноле (4 мл) добавляли 28% метилат натрия в растворе метанола (447 мкл), перемешивали в течение 30 минут при комнатной температуре. Реакционную смесь концентрировали, добавляли воду и смесь экстрагировали этилацетатом. Органический слой промывали водой и солевым раствором, сушили над безводным сульфатом натрия и концентрировали. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат:метанол = 20:1). Полученное соединение обрабатывали 4 н. хлористым водородом в растворе этилацетата, с получением указанного в заголовке соединения (89 мг), имеющего следующие физические данные.
ТСХ: Rf 0,56 (этилацетат: метанол = 10:1);
ЯМР (CD3OD): δ 1,60-1,80, 2,10-2,25, 2,14, 3,14, 3,15-3,30, 3,50-3,60, 4,30, 4,70, 7,15-7,39, 7,51-7,55, 7,68, 7,96, 8,00, 8,22.
БИОЛОГИЧЕСКИЕ ПРИМЕРЫ
С помощью следующего эксперимента доказывается, что соединение настоящего изобретения, представленное формулой (I), обладает антагонистической активностью против рецептора хемокина, особенно CCR5, и ингибирующей активностью против клеточной миграции, а также проявляют надлежащие условия, чтобы быть очень полезным медикаментом.
Биологический Пример 1
Испытание на антагонистическую активность против CCR5
С помощью процедуры, например, описанной в JP-A-2004-256531, можно доказать, что соединение настоящего изобретения обладает антагонистической активностью против CCR5.
Биологический Пример 2
Испытание клеточной миграции
С помощью следующего экспермента, например, было доказано, что соединение настоящего изобретения обладает ингибирующей активностью против клеточной миграции.
Получение РВМС (моноядерных клеток периферической крови)
Венозная кровь человека (50 мл), собранная с использованием шприца с гепарин-натрием (конечная концентрация: 10 Ед./мл, инъекция гепарин-натрия 1000 Ед./мл, Shimizu Pharmaceutical Co., Ltd.), хранилась в 50 мл конической трубке, изготовленной из полипропилена. В трубку Lymphoprep (HYCOMED PHARMA, Cat.No 1019818) добавлялось 16,5 мл DPBS (-) (GIBCO, Cat.No. 14190-136) и образец крови, покачивалось несколько раз, затем центрифугировалось при 3000 об. в мин в течение 10 минут при комнатной температуре. Около 7 мл PBMC фазы (центральная фаза) собиралось в 50 мл коническую трубку, изготовленную из полипропилена, с использованием пипетки Пастера, и добавлялся DPBS (-) до конечной концентрации (50 мл), затем центрифугировался при 1200 об. в мин в течение 10 минут при комнатной температуре. После удаления супернатанта остаток повторно растворялся в 50 мл DPBS (-). Суспензия клеток центрифугировалась при 1500 об/мин в течение 3 минут при комнатной температуре. Супернатант удалялся, затем туда добавлялось 3 мл гемолизного буфера (0,8% NH4Cl, 0,1% KHCO3, 1 ммоль/л EDTA) для достаточного суспендирования, а затем оставлялось на 2 минуты при комнатной температуре. К суспензии добавлялось 30 мл DPBS (-) PBMC, центрифугировалось при 1500 об/мин в течение 3 минут при комнатной температуре. Супернатант удалялся, давая РВМС.
Культура PBMC человека
После того как 24-луночная планшета с нанесенными на нее античеловеческими CD3 атителами OKT3 (Janssen Pharmaceutical K.K., 1 мкг/мл) хранилась на протяжении ночи при 4°С, она блокировалась культуральной средой (RPMI 1640 (GIBCO, Cat.No. 11875-085), 10% FBS (GIBCO, Cat.No. 112318-028), 1% PSF (GIBCO, Cat.No. 15240-096)) через 30 минут при 37°С. Полученная культура человеческой PBMC высевалась на планшету с нанесенными на нее OKT3 (2×106 клеток/лунку), выращивалась в течение нескольких дней при 37°С. РВМС собиралась и высевалась на планшету, не покрытую клетками ОКТ3 (2×106 клеток/лунку), в присутствии человеческого IL2 (5 нг/мл), затем культивировалась. РВМС субкультивировалась каждые два или три дня.
Анализ экспрессии CCR5 человека с использованием FACS
После того как 10 мкл FITC меченых античеловеческих CCR5 антител (2D7) (BD Pharmingen, Cat.No 555992) и PE меченых античеловечских CD45RO антител (BD Pharmingen, Cat.No 347967) добавлялись к PBMC человека, культивируемой в 1×106 клеток, смесь затенялась на 15 минут или оставлялась на 30 минут на льду, затем туда добавляли DPBS (GIBCO) и промывали. Клетки суспендировали в 500 мкл DPBS, а затем с использованием FACS измеряли интенсивности флуоресценции.
Эксперимент клеточной миграции in vitro
50 мкл 5 х 105 клеток суспензии PBMC человека (культуральная среда) и 50 мкл раствора испытуемого соединения (0-2 мкмоль/л: двойная концентрация конечной концентрации) добавлялись в верхнюю лунку транс-лунки, а в нижнюю лунку добавлялись 300 мкл 60 нмоль/л человеческого MIP-1β (Pepro tech, Cat.No. 300-09) и 300 мкл двойной концентрации раствора испытуемого соединения. Получалось, что концентрация ДМСО в верхней лунке была 0,01%. Раствор инкубировался 1,5 часа в атмосфере газа двуокиси углерода (37°С, 5% СО2, степень влажности: 95%). После того как растворитель в верхней лунке тщательно аспирировался, туда добавляли 100 мкл 20 мкмоль/л EDTA/DPBS (-) и инкубировали 30 минут при 4°С, затем центрифугировали при 1500 об/мин в течение 5 минут. 100 мкл раствора переносили на белую 96-луночную планшету для флуоресценции, из нижней лунки отмеряли с помощью пипетки некоторое количество клеток с использованием Celltiter Glo (Promega) (измерение АТР), степень ингибирования клеточной миграции вычислялась с помощью следующей формулы. Величина IC50 вычислялась по степени ингибирования клеточной миграции в каждой концентрации. Величина представлена средней величиной (n=3).
В результате соединения настоящего изобретения показали ингибирующую активность против индуцируемой MIP-1β-человека клеточной миграции культивируемых PBMC человека в виде величины IC50 0,01 мкМ или менее. Например, соединение, полученное в примере 7(29), показало величину IC50 0,0012 мкМ.
Степень ингибирования клеточной миграции = (Ea - Ec)/(Eb - Ec) × 100
Биологический Пример 3: Испытание стабильности на микросомах печени обезьяны
С помощью следующих экспериментов было продемонстрировано, например, что соединения настоящего изобретения имеют метаболическую стабильность.
К раствору 100 ммоль/л фосфатного буфера (рН 7,4, он был получен из 100 ммоль/л водного раствора вторичного кислого дикалийфосфата и 100 ммоль/л водного раствора вторичного кислого монокалийфосфата) добавлялись микросомы печени обезьяны (конечная концентрация: 1 мг/мл) и испытуемое соединение (конечная концентрация: 5 мкмоль/л), и раствор смеси предварительно инкубировали в течение 5 минут. К раствору смеси добавлялась NADPH генерирующая система (13 ммоль/л β-NADP+ (конечная концентрация: 1,3 ммоль/л), 33 ммоль/л G-6-P (конечная концентрация: 3,3 ммоль/л), 10 Ед./мл G-6-P DH (из дрожжей) (конечная концентрация: 0,4 Ед./мл) и 33 ммоль/л раствора хлорида магния (конечная концентрация: 3,3 ммоль/л). Пока смесь инкубировалась при 37°С, спустя 0 и 30 минут от начала отбиралось 100 мкл реакционного раствора и добавлялось к ацетонитрилу (2 мл) для прекращения реакции (n=2). После того как туда добавлялся раствор внутреннего стандарта, раствор смеси перемешивался, а затем центрифугировался при 3000 об/мин в течение 5 минут. 100 мкл получающегося в результате супернатанта смешивалось со 100 мкл подвижной фазы А, а затем анализировалось с помощью LC/MS/MS.
Условия LC/MS/MS для анализа показаны ниже.
Условия LC:
Состав подвижных фаз и скорость потока:
Условия MS/MS:
Измерительное оборудование: API3000 (AB/MDS SCIEX)
Способ ионизации: Ионизация с электрораспылением (ESI, положительная)
Для каждого образца выбирался соответствующий контролирующий ион. Например, для соединения, полученного в Примере 7(83), выбирались 647,5 (m/z) в качестве исходного или основного иона и 277,0 (m/z) в качестве дочернего иона.
Остаточная степень неметаболита (%) испытуемого соединения в микросомах печени обезьяны вычислялась с помощью следующей формулы.
Остаточная степень неметаболита (%)
=(концентрация испытуемого соединения через 30 минут)
/(концентрация испытуемого соединения через 0 минут) × 100.
В результате было доказано, что соединения настоящего изобретения являются метаболически стабильными в микросомах печени. Например, остаточная степень неметаболита соединения, полученного в Примере 7(83), составляла 88%.
Биологический Пример 4
Фармакокинетическое испытание на крови обезьяны
С помощью следующих экспериментов, например, было продемонстрировано, что соединения настоящего изобретения обладают хорошими свойствами фармакокинетики в крови.
Каждое из испытуемых соединений взвешивалось и растворялось в Солтоле (Товарный знак; BASF Takeda Vitamins Ltd.)/ пропиленгликоль = 7/3, нагретом до 50°С, с получением его 5 мг/мл раствора. Взвешивалось равное количество каждого из 5 образцов, смешивалось, а затем разбавлялось дистиллированной водой для инъекций в пять раз с получением раствора для перорального введения. Раствор для перорального введения (1 мг/кг) вводился насильно внутрижелудочно обезьянам cynomolgus (самцы, Hamri Co., Ltd) с помощью зонда (n=3). Введение производилось в состоянии голода, но животные имеют свободный доступ к воде для питья. Из поверхностной краниальной вены отбирались образцы крови 1 мл каждого с использованием гепаринизированного шприца, через 5, 15, 30 минут, 1, 2, 4, 6, 8 и 24 часа после введения. Собранные образцы хранились во льду, центрифугировались при 3000 об/мин в течение 15 минут с получением плазмы. Плазма хранилась при-20°С. Образец плазмы, хранившийся при -20°С, растворялся, затем к 100 мкл получающегося раствора добавлялись раствор внутреннего стандарта и ацетонитрил (2 мл), перемешивались, центрифугировались при 3000 об/мин в течение 10 минут. Получающийся супернатант сушили с использованием центрифужного концентратора. Остаток повторно растворялся в 100 мкл подвижной фазы А, а затем 40 мкл получающегося раствора анализировалось с помощью LC/MS/MS.
Условия LC/MS/MS для анализа показаны ниже.
Условия LC:
Измерительное оборудование: Waters 2790 (Waters)
Колонка: YMC-Pack MB-ODS 5 мкм (2,1 ммID × 50мм))( YMC)
Температура колонки: комнатная температура
Скорость потока: 200 мкл/минуту
Подвижная фаза: 20 ммоль/л водный раствор ацетата аммония/ацетонитрила (1/1, V/V)
Условия MS/MS:
Измерительное оборудование: QUATTRO Ultima (Micromass)
Способ ионизации: ES+
Напряжение капилляров: 3,20 кВ
Температура источника: 150°С
Температура десольватации: 250°С
Умножитель: 650В.
Для каждого образца выбирался соответствующий контролирующий ион. Например, для соединения, полученного в Примере 6(17), выбирались 575,64 (m/z) в качестве исходного иона и 262,07 (m/z) в качестве дочернего иона, а для соединения, полученного в Примере 7(54), выбирались, соответственно, 587,20 (m/z) в качестве исходного иона и 227,12 (m/z) в качестве дочернего иона.
Переход концентрации плазмы испытуемого соединения у обезьян анализировался с помощью непространственного аналитического способа с использованием WinNonlin 4.0.1 (Pharsight) и вычислялся AUC.
В результате было доказано, что соединения настоящего изобретения обладают хорошими свойствами фармакокинетики в крови. Например, AUC соединения, полученного в Примерах 6(17) и 7(54), были, соответственно, 226 нг.ч/мл и 1150 нг.ч/мл.
Биологический Пример 5
Измерение биодоступности (BA):
С помощью следующих экспериментов, например, было продемонстрировано, что соединения настоящего изобретения обладают хорошей абсорбцией пероральных препаратов.
Испытуемое соединение взвешивалось и растворялось в 30% HP-β-CD (товарный знак; Mitsubishi Corporation) для получения 1 мг/мл раствора для внутривенного введения. Испытуемое соединение взвешивалось и растворялось в Солтоле (Товарный знак; BASF Takeda Vitamins Ltd.)/ пропиленгликоль = 7/3, нагретом до 50°С, с получением его 5 мг/мл раствора. Взвешивалось равное количество каждого из 5 образцов, смешивалось, а затем разбавлялось дистиллированной водой для инъекций в пять раз с получением раствора для перорального введения. Раствор для внутривенного введения (1 мг/кг) вводился обезьянам cynomolgus (самцы, Hamri Co., Ltd) через поверхностную краниальную вену в виде одной внутривенной дозы (n=3). Раствор для перорального введения (3 мг/кг) вводился насильно внутрижелудочно обезьянам cynomolgus (самцы, Hamri Co., Ltd) с помощью зонда (n=3). Введение производилось в состоянии голода, но животные имеют свободный доступ к воде для питья. Из поверхностной краниальной вены отбирались образцы крови 1 мл каждого с использованием гепаринизированного шприца, через 5, 15, 30 минут, 1, 2, 4, 6, 8 и 24 часа после введения. Собранные образцы хранились во льду, центрифугировались при 3000 об/мин в течение 15 минут с получением плазмы. Плазма хранилась при-20°С. Образец плазмы, хранившийся при -20°С, растворялся, затем к 100 мкл получающегося раствора добавлялись раствор внутреннего стандарта и ацетонитрил (2 мл), перемешивались, центрифугировались при 3000 об/мин в течение 10 минут. Остаток повторно растворялся в 100 мкл подвижной фазы А, а затем 40 мкл получающегося раствора анализировалось с помощью LC/MS/MS.
Условия LC/MS/MS для анализа показаны ниже.
Условия LC:
Измерительное оборудование: Waters 2790 (Waters)
Колонка: YMC-Pack MB-ODS 5 мкм (2,1 ммID × 50мм)(YMC)
Температура колонки: комнатная температура
Скорость потока: 200 мкл/минуту
Подвижная фаза: 20 ммоль/л водный раствор ацетата аммония/ацетонитрила (1/1)
Условия MS/MS:
Измерительное оборудование: QUATTRO Ultima (Micromass)
Способ ионизации: ES+
Напряжение капилляров: 3,20 кВ
Температура источника: 150°С
Температура десольватации: 250°С
Умножитель: 650В.
Для каждого образца выбирался соответствующий контролирующий ион. Например, для соединения, полученного в Примере 6(17), выбирались 575,64 (m/z) в качестве исходного иона и 262,07 (m/z) в качестве дочернего иона (диффузорный ток: 35 В, коллизионный ток: 34 эВ).
Переход концентрации плазмы испытуемого соединения у обезьян анализировался с помощью непространственного аналитического способа с использованием WinNonlin 4.0.1 (Pharsight) и вычислялся AUC.
ВА вычислялся с помощью следующей формулы.
ВА (%) = (AUCp.o./Дозар.o.)/(AUCi.v./Дозаi.v.)×100
AUCp.o.: AUC, когда испытуемое соединение вводится перорально
Дозар.o.: количество соединения, вводимого перорально
AUCi.v.: AUC, когда испытуемое соединение вводится внутривенно.
Дозаi.v.: количество соединения, вводимого внутривенно
В результате было доказано, что соединения настоящего изобретения обладают хорошей абсорбцией в пероральных препаратах. Например, ВА соединения, полученного в Примере 6(17), составляет 42%.
Биологический Пример 6
Модель ренальной аллотрансплантации на обезьянах cynomolgus для оценки иммуносуппрессивного эффекта соединения настоящего изобретения:
Обезьяны cynomolgus (вес тела: 3-4,5 мг), которые были АВО-совместимыми, главный комплекс гистосовместимости (МНС)-иной, более конкретно, сочетания донор (самец) с отсутствием выборки MLR -рецепиент (любого пола) подвергались билатеральной нефроэктомии с последующей имплантацией аллогенной почки от выбранного животного донора. Ежедневно вводилось испытуемое вещество (соединение настоящего изобретения и/или иммуноподавляющий агент), начиная с дня-1 (день до транплантации) до тех пор, пока не был определен день до отторжения. Эффективность оценивалась с помощью сравнения длительности выживания трансплантированной почки.
Соединение настоящего изобретения вводилось в сочетании с субтерапевтическим иммуноподавляющим агентом, имеющимся на рынке (Циклоспорин, сиролимус, и/или такролимус). Эффективность демонстрировалась путем сравнения со случаем введения одного иммуноподавляющего агента.
Соединение настоящего изобретения вводилось, например, через рот (РО), дважды в день при уровне дозы 3, 10 или 30 мг/кг.
Например, присутствие отторжения подозревали в том случае, если уровни креатинина в сыворотке повышались. В частности, отторжение трансплантированной почки определялось как увеличение уровней креатинина в сыворотке до 8 мг/дл.
В результате соединение настоящего изобретения показало иммуноподавляющий эффект на модели ренальной аллотрансплантации на обезьянах cynomolgus.
Примеры готовых форм препаратов
Пример готовой формы 1
Гидрохлорид N'-(4-фторфенил)-N-[1-({6-[4-(метилсульфонил)-фенокси]пиридин-3-ил}метил)пиперидин-4-ил]-N-фенилмочевины (10 г), кальциевая карбоксиметилцеллюлоза (дезинтегрирующий агент, 2,0 г), стеарат магния (смазочный агент, 1,0 г) и микрокристаллическая целлюлоза (87 г) смешиваются общепринятым образом, штампуются для получения 1000 таблеток, каждая из которых содержит 10 мг активного ингредиента.
Пример готовой формы 2
Гидрохлорид N'-(4-фторфенил)-N-[1-({6-[4-(метилсульфонил)-фенокси]пиридин-3-ил}метил)пиперидин-4-ил]-N-фенилмочевины (10 г), маннит (200 г) и дистиллированная вода (5 л) смешиваются обычным образом. Затем раствор фильтровался через пыленепроницаемый фильтр, а затем 5 мл аликвоты загружались в ампулы, которые автоклавировались, давая 1000 ампул, каждая из которых содержит 10 мг активного ингредиента.
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ
Соединения настоящего изобретения, представленные формулой (I), обладают антагонистической активностью против рецептора хемокина, особенно CCR5, поэтому они полезны в профилактике и/или лечении связанных с CCR5 заболеваний, например, разнообразных воспалительных заболеваний (астмы, нефрита, нефропатии, гепатита, артрита, ревматоидного артрита, ринита, коньюнктивита, воспалительного заболевания кишечника, такого как язвеный колит и др.), иммунологических заболеваний (аутоиммунных болезней, отторжения трансплантированного органа (отторжения трансплантата твердого органа, отторжения трансплантата панкреатических островковых клеток при лечении диабета, заболевания трансплантат-против-хозяина и др.), иммуноподавления, псориаза, рассеянного склероза и др.), инфекционных заболеваний (заражении вирусом иммунодефицита человека, синдрома приобретенного иммунодефицита, RSV заражения и др.), аллергических заболеваний (атопического дерматита, крапивницы, аллергического бронхолегочного аспергиллеза, аллергического эозинофильного гастроэнтерита и др.), сердечнососудистых заболеваний (артериосклероза, ишемического реперфузионного повреждения и др.), синдрома острого респираторного дистресса, шока, вызываемого бактериальной инфекцией, диабета, метастазов раковой опухоли и т.д. Поэтому антагонист хемокинового рецептора, особенно антагонист CCR5, полезен в качестве медикамента.


| название | год | авторы | номер документа |
|---|---|---|---|
| АЗОТСОДЕРЖАЩИЕ ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ И ЛЕКАРСТВЕННЫЕ СРЕДСТВА, СОДЕРЖАЩИЕ ИХ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2004 |
|
RU2366655C2 |
| ФЕНИЛЬНОЕ ПРОИЗВОДНОЕ | 2012 |
|
RU2619105C2 |
| НОВОЕ ПРОИЗВОДНОЕ ПИРИДИНА И ПРОИЗВОДНОЕ ПИРИМИДИНА (3) | 2006 |
|
RU2362771C1 |
| ПРОИЗВОДНЫЕ ДИАМИНОПИРИМИДИНА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2587981C2 |
| ПРОИЗВОДНОЕ ФЕНИЛА | 2014 |
|
RU2639875C2 |
| ПРОИЗВОДНЫЕ ДИАМИНОПИРИМИДИНА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2587493C2 |
| ПРОИЗВОДНЫЕ ПИРИДИНА В КАЧЕСТВЕ ИНГИБИТОРОВ ДИПЕПТИДИЛПЕПТИДАЗЫ IV | 2004 |
|
RU2353617C2 |
| ПРОИЗВОДНЫЕ 1,5-НАФТИРИДИНА И ИНГИБИТОРЫ MELK, СОДЕРЖАЩИЕ ИХ | 2012 |
|
RU2645339C1 |
| ПРОИЗВОДНЫЕ ТИЕНО[2,3-с]ХИНОЛИНА-4-ОНА, ПОЛЕЗНЫЕ ПРИ ЛЕЧЕНИИ РВК-ЗАВИСИМОГО ЗАБОЛЕВАНИЯ | 2011 |
|
RU2574398C2 |
| Соединение на основе оксазолидина и содержащий его селективный агонист андрогенового рецептора | 2015 |
|
RU2702001C2 |
Изобретение относится к соединению, представленному формулой (Ib) 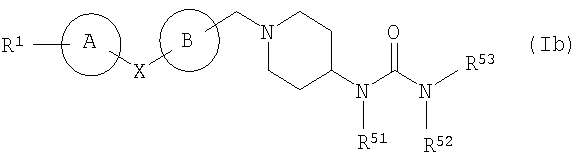 в которой R1 представляет (1) -N(R1A)SO2-R1B, (2) -SO2NR1CR1D, (3) -COOR1E, (4) -OR1F, (5) -S(O)mR1G, (6) -CONR1HR1J, (7) -NR1KCOR1L, или (8) циано, где m представляет 0, 1 или 2; Х представляет собой связь или спейсер, содержащий 1-3 атома, в качестве основной цепи; R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L каждый независимо представляет собой (1) атом водорода, (2) С1-8алкильную группу, которая может иметь заместитель(заместители), выбранные из группы, состоящей из [1] гидрокси группы, [2] карбокси группы, [3] С1-6алкокси группы, которая может быть замещена галогеном, и [4] моно- или дизамещенного аминозамещенного С1-8 алкильной группой или (3) тетрагидропиран, пиперазин, пиперидин, азетидин, пирролидин или морфолин, каждый из которых может иметь заместитель (заместители), выбранные из группы, состоящей из гидрокси, галогена, С1-8алканоила и C1-10галогеналкила, и где R1C и R1D или R1H и R1J вместе с атомом азота, к которому они присоединены, могут образовывать пиперазин, пиперидин, азетидин, пирролидин или морфолин, каждый из которых может иметь заместитель (заместители), выбранные из группы, состоящей из гидрокси, галогена, С1-8алканоила и C1-10галогеналкила; кольцо А представляет собой бензольное кольцо или пиридиновое кольцо, каждое из которых может иметь заместитель (заместители), выбранные из группы, состоящей из С1-8алкила, нитро, C1-6алкокси и галогена; кольцо В представляет собой бензольное кольцо, пиридиновое кольцо или пиразиновое кольцо, каждое из которых может иметь заместитель (заместители), выбранные из группы, состоящей из С1-8алкила; R51 представляет собой (1) С1-8алкил, С2-8алкенил или С2-8алкинил, каждый из которых может иметь заместитель (заместители) бензола или (2) бензол, пиразол, пиридин, изоксазол, тиофен, бензотиазол, каждый из которых может иметь заместитель (заместители), выбранные из группы, состоящей из С1-4алкокила, C1-6алкокси, C1-6алкилтио, С1-6алкилсульфинила, C1-6алкилсульфоинила и галогена; R52 представляет собой атом водорода; R53 представляет собой (1) С1-8алкил, С2-8алкенил или С2-8алкинил, каждый из которых может иметь заместитель (заместители) бензола или (3) бензол, пиразол, пиридин, тиофен, бензодиоксан, циклогексан или тетрагидропиран, каждый из которых может иметь заместитель(заместители), выбранные из группы, состоящей из [1] гидрокси группы, [2] циано, [3] карбомоила, [4] аминокарбонила, замещенного одним или двумя заместителями выбранными из (а) гидрокси группы, (b) амино, (с) С1-4алкокси, (d) моно или дизамещенного амина, замещенного С1-8углеводородной группой, (е) карбоксила и (f) C1-6алкоксикарбонила, [5] карбокси, [6] галогена, [7] C1-6алкокси, [8] С1-6алкилсульфонила, [9] амино, [10] C1-6ациламино, [11] алкил-сульфониламино, [12] циклического аминокарбонила и [13] С1-8углеводородная группа, замещенная 1 или 2 заместителями, выбранными из (а) гидрокси, (b) амино, (с) С1-4алкокси, (d) моно или дизамещенного амина, замещенного С1-8углеводородной группой, и (е) аминокарбонила, замещенного С1-8углеводородной группой; к его соли, его N-оксиду, его сольвату. А также к фармацевтической композиции на основе этого соединения, обладающей антагонистической активностью в отношении CCR5, к применению соединения формулы (Ib) для производства агента для профилактики или лечения заболеваний, связанных с CCR5. Технический результат: получены и описаны новые соединения, которые имеют антагонистическую активность против CCR5, поэтому они полезны в предотвращении или профилактике и/или лечении связанных с CCR5 заболеваний, например разнообразных воспалительных заболеваний, иммунологических заболеваний и т.д. 4 н. и 3 з.п. ф-лы, 1 табл.
в которой R1 представляет (1) -N(R1A)SO2-R1B, (2) -SO2NR1CR1D, (3) -COOR1E, (4) -OR1F, (5) -S(O)mR1G, (6) -CONR1HR1J, (7) -NR1KCOR1L, или (8) циано, где m представляет 0, 1 или 2; Х представляет собой связь или спейсер, содержащий 1-3 атома, в качестве основной цепи; R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L каждый независимо представляет собой (1) атом водорода, (2) С1-8алкильную группу, которая может иметь заместитель(заместители), выбранные из группы, состоящей из [1] гидрокси группы, [2] карбокси группы, [3] С1-6алкокси группы, которая может быть замещена галогеном, и [4] моно- или дизамещенного аминозамещенного С1-8 алкильной группой или (3) тетрагидропиран, пиперазин, пиперидин, азетидин, пирролидин или морфолин, каждый из которых может иметь заместитель (заместители), выбранные из группы, состоящей из гидрокси, галогена, С1-8алканоила и C1-10галогеналкила, и где R1C и R1D или R1H и R1J вместе с атомом азота, к которому они присоединены, могут образовывать пиперазин, пиперидин, азетидин, пирролидин или морфолин, каждый из которых может иметь заместитель (заместители), выбранные из группы, состоящей из гидрокси, галогена, С1-8алканоила и C1-10галогеналкила; кольцо А представляет собой бензольное кольцо или пиридиновое кольцо, каждое из которых может иметь заместитель (заместители), выбранные из группы, состоящей из С1-8алкила, нитро, C1-6алкокси и галогена; кольцо В представляет собой бензольное кольцо, пиридиновое кольцо или пиразиновое кольцо, каждое из которых может иметь заместитель (заместители), выбранные из группы, состоящей из С1-8алкила; R51 представляет собой (1) С1-8алкил, С2-8алкенил или С2-8алкинил, каждый из которых может иметь заместитель (заместители) бензола или (2) бензол, пиразол, пиридин, изоксазол, тиофен, бензотиазол, каждый из которых может иметь заместитель (заместители), выбранные из группы, состоящей из С1-4алкокила, C1-6алкокси, C1-6алкилтио, С1-6алкилсульфинила, C1-6алкилсульфоинила и галогена; R52 представляет собой атом водорода; R53 представляет собой (1) С1-8алкил, С2-8алкенил или С2-8алкинил, каждый из которых может иметь заместитель (заместители) бензола или (3) бензол, пиразол, пиридин, тиофен, бензодиоксан, циклогексан или тетрагидропиран, каждый из которых может иметь заместитель(заместители), выбранные из группы, состоящей из [1] гидрокси группы, [2] циано, [3] карбомоила, [4] аминокарбонила, замещенного одним или двумя заместителями выбранными из (а) гидрокси группы, (b) амино, (с) С1-4алкокси, (d) моно или дизамещенного амина, замещенного С1-8углеводородной группой, (е) карбоксила и (f) C1-6алкоксикарбонила, [5] карбокси, [6] галогена, [7] C1-6алкокси, [8] С1-6алкилсульфонила, [9] амино, [10] C1-6ациламино, [11] алкил-сульфониламино, [12] циклического аминокарбонила и [13] С1-8углеводородная группа, замещенная 1 или 2 заместителями, выбранными из (а) гидрокси, (b) амино, (с) С1-4алкокси, (d) моно или дизамещенного амина, замещенного С1-8углеводородной группой, и (е) аминокарбонила, замещенного С1-8углеводородной группой; к его соли, его N-оксиду, его сольвату. А также к фармацевтической композиции на основе этого соединения, обладающей антагонистической активностью в отношении CCR5, к применению соединения формулы (Ib) для производства агента для профилактики или лечения заболеваний, связанных с CCR5. Технический результат: получены и описаны новые соединения, которые имеют антагонистическую активность против CCR5, поэтому они полезны в предотвращении или профилактике и/или лечении связанных с CCR5 заболеваний, например разнообразных воспалительных заболеваний, иммунологических заболеваний и т.д. 4 н. и 3 з.п. ф-лы, 1 табл.
1. Соединение, представленное формулой (Ib)
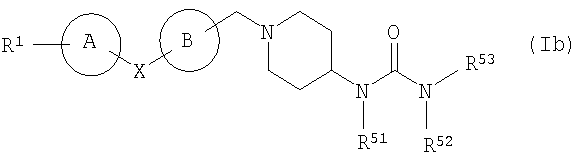
в которой R1 представляет (1) -N(R1A)SO2-R1B, (2) -SO2NR1CR1D, (3) -COOR1E, (4) -OR1F, (5) -S(O)mR1G (6) -CONR1HR1J, (7) -NR1KCOR1L, или (8) циано, где m представляет 0, 1 или 2;
Х представляет собой связь или спейсер, содержащий 1-3 атома, в качестве основной цепи;
R1A, R1B, R1C, R1D, R1E, R1F, R1G, R1H, R1J, R1K и R1L каждый независимо представляет собой (1) атом водорода, (2) С1-8алкильную группу, которая может иметь заместитель(заместители), выбранные из группы, состоящей из [1] гидрокси группы, [2] карбокси группы, [3] С1-6алкокси группы, которая может быть замещена галогеном и [4] моно- или дизамещенного амино замещенного С1-8алкильной группой или (3) тетрагидропиран, пиперазин, пиперидин, азетидин, пирролидин или морфолин, каждый из которых может иметь заместитель (заместители) выбранные из группы, состоящей из гидрокси, галогена, С1-8алканоила и С1-10галогеналкила, и
где R1C и R1D, или R1H и R1J вместе с атомом азота, к которому они присоединены, могут образовывать пиперазин, пиперидин, азетидин, пирролидин или морфолин, каждый из которых может иметь заместитель (заместители), выбранные из группы, состоящей из гидрокси, галогена, С1-8алканоила и C1-10галогеналкила;
кольцо А представляет собой бензольное кольцо или пиридиновое кольцо, каждое из которых может иметь заместитель (заместители), выбранные из группы, состоящей из С1-8алкила, нитро, C1-6алкокси и галогена;
кольцо В представляет собой бензольное кольцо, пиридиновое кольцо или пиразиновое кольцо, каждое из которых может иметь заместитель (заместители), выбранные из группы, состоящей из С1-8алкила;
R51 представляет собой (1) С1-8алкил, С2-8алкенил или С2-8алкинил, каждый из которых может иметь заместитель (заместители) бензола или (2) бензол, пиразол, пиридин, изоксазол, тиофен, бензотиазол, каждый из которых может иметь заместитель (заместители), выбранные из группы, состоящей из С1-4алкокила, C1-6алкокси, C1-6алкилтио, С1-6алкилсульфинила, C1-6алкилсульфоинила и галогена;
R52 представляет собой атом водорода;
R53 представляет собой (1) водород, (2) С1-8алкил, С2-8алкенил или С2-8алкинил, каждый из которых может иметь заместитель (заместители) бензола или (3) бензол, пиразол, пиридин, тиофен, бензодиоксан, циклогексан или тетрагидропиран, каждый из которых может иметь заместитель(заместители), выбранные из группы, состоящей из [1] гидрокси группы, [2] циано, [3] карбомоила, [4] аминокарбонила, замещенного одним или двумя заместителями, выбранными из (а) гидроксигруппы, (b) амино, (с) С1-4алкокси, (d) моно или дизамещенного амина, замещенного С1-8углеводородной группой, (е) карбоксила и (f) C1-6алкоксикарбонила, [5] карбокси, [6] галогена, [7] C1-6алкокси, [8] С1-6алкилсульфонила, [9] амино, [10] C1-6ациламино, [11] алкилсульфониламино, [12] циклического аминокарбонила и [13] С1-8углеводородная группа, замещенная 1 или 2 заместителями, выбранными из (а) гидрокси, (b) амино, (с) С1-4алкокси, (d) моно или дизамещенного амина, замещенного С1-8углеводородной группой и (е) аминокарбонила, замещенного С1-8углеводородной группой;
его соль, его N-оксид, его сольват.
2. Соединение по п.1, выбранное из
(1) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил} метил)-2-пиридинил]окси}фенил)метансульфонамида;
(2) 5-[({бутил[1-(4-{2-метил-4-[(метилсульфонил)амино]фенокси}бензил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида;
(3) 5-{[(бутил{1-[(6-{2-метил-4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида;
(4) 5-{[(бутил{1-[(6-{4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида;
(5) 5-[({бутил[1-({6-[4-(метилсульфонил)фенокси]-3-пиридинил}метил)-4-пиперидинил]амино}карбонил)амино]-2,4-дифторбензамида;
(6) 5-({[{1-[(6-{4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(пентил)амино]карбонил}амино)-2,4-дифторбензамида;
(7) N-(4-{[5-({4-[{[(2,4-дифторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}-3-метоксифенил)метансульфонамида;
(8) 5-{[(бутил{1-[(6-{4-[(этилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифтор-N-метилбензамида;
(9) N'-(4-фторфенил)-N-[1-({6-[4-(метилсульфонил)фенокси]пиридин-3-ил}метил)пиперидин-4-ил]-N-фенилмочевины;
(10) 5-{[(бутил{1-[(2-метил-6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида;
(11) N-(4-{[5-({4-[{[(4-метилфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид;
(12) N-(4-{[5-({4-[{[(4-хлорфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамид;
(13) 2-фтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)бензамид;
(14) Н-(4-{[5-({4-[{[(2,4-дифторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида;
(15) N-(4-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида;
(16) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)ацетамида;
(17) N-(4-{[5-({4-[{[(4-фторфенил)амино]карбонил}(2-метоксифенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)метансульфонамида;
(18) N-{4-[(5-{[4-((3-фторфенил){[(4-фторфенил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]фенил}метансульфонамида;
(19) N-[2-фтор-5-({[{1-[(6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-пиперидинил}(фенил)амино]карбонил}амино)фенил]ацетамида;
(20) N-{4-[(5-{[4-((3-фторфенил){[(6-метил-3-пиридинил)амино]карбонил}амино)-1-пиперидинил]метил}-2-пиридинил)окси]фенил}метансульфонамида;
(21) N-(4-{[5-({4-[{[(6-метил-3-пиридинил)амино]карбонил}(фенил)амино]-1-пиперидинил}метил)-2-пиридинил]окси}фенил)этансульфонамида.
3. Соединение по п.1, в котором R1 представляет
[А] (1) -N(R1A)SO2-R1B, (2) -SO2NR1CR1D, (6) -CONR1HR1J, (7) -NR1KCOR1L-, где R1A, R1B, R1C, R1D, R1H, R1J, R1K и R1L каждый независимо представляет (1) атом водорода, (2) С1-8алкильную группу, которая может иметь заместитель(заместители), выбранные из группы состоящей из [1] гидрокси группы, [2] карбокси группы, [3] 1-6алкокси группы, которая может быть замещена галогеном и [4] моно- или дизамещенного амино замещенного С1-8 алкилом или (3) тетрагидропиран, пиперазин, пиперидин, азетидин, пирролидин или морфолин, каждый из которых может иметь заместитель(заместители) выбранные из группы состоящей из гидрокси, галогена, С1-8алканоила и C1-10галогеналкила,
при условии что по меньшей мере один из R1A и R1B, R1C и R1D или R1H и R1J представляют собой тетрагидропиран, пиперазин, пиперидин, азетидин, пирролидин или морфолин, каждый из которых может иметь заместитель(заместители) выбранные из группы, состоящей из гидрокси, галогена, С1-8алканоила и C1-10галогеналкила;
[B] (2) -SO2NR1CR1D или (6) -CONR1HR1J, где R1C и R1D, или R1H и R1J вместе с атомом азота, к которому они присоединены, могут образовывать пиперазин, пиперидин, азетидин, пирролидин или морфолин, каждый из которых может иметь заместитель(заместители), выбранные из группы, состоящей из гидрокси, галогена, С1-8алканоила и C1-10галогеналкила;
[C] (3) -COOR1E, (4) -OR1F или (5) -S(O)mR1g, где m представляет 0, 1 или 2;
R1E, R1F и R1G независимо представляют собой тетрагидропиран, пиперазин, пиперидин, азетидин, пирролидин или морфолин, каждый из которых может иметь заместитель(заместители), выбранные из группы, состоящей из гидрокси, галогена, С1-8алканоила и C1-10галогеналкила;
[D] (5) -S(O)mR1g, где m равно 0; R1G независимо представляет собой С1-8алкил, который может иметь заместитель(заместители), выбранные из группы, состоящей из [1] гидрокси, [2] карбоксигруппы, [3] С1-6алкоксигруппы, которая может быть замещена галогеном и [4] моно- или дизамещенного аминозамещенного С1-8 алкильной группой или [Е] (8) циано.
4. Фармацевтическая композиция, обладающая антагонистической активностью в отношении CCR5, включающая соединение, заявленное в п.1, его соль, его N-оксид или его сольват.
5. Применение соединения, заявленного в п.1, его соли, его N-оксида или его сольвата для производства агента для профилактики и/или лечения заболеваний, связанных с CCR5.
6. Соединение 5-{[(бутил{1-[(2-метил-6-{4-[(метилсульфонил)амино]фенокси}-3-пиридинил)метил]-4-
пиперидинил}амино)карбонил]амино}-2,4-дифторбензамид, его соль, N-оксид или сольват, или его пролекарство.
7. Соединение по п.6, соль которого представляет гидрохлорид 5-{[(бутил{1-[(2-метил-6-{4-[(метилсульфонил)амино]-фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида или
дигидрохлорид 5-{[(бутил(1-[(2-метил-6-{4-[(метилсульфонил)амино]-фенокси}-3-пиридинил)метил]-4-пиперидинил}амино)карбонил]амино}-2,4-дифторбензамида.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| ПРОИЗВОДНЫЕ ФЕНОКСИ- ИЛИ ФЕНОКСИАЛКИЛПИПЕРИДИНА И АНТИВИРУСНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1993 |
|
RU2125565C1 |
Авторы
Даты
2011-01-20—Публикация
2005-09-12—Подача