Изобретение относится к химии аминокислот и пептидов, принадлежащих классу алифатических диэфиров дипептидов.
Катионные амфифилы являются перспективной основой для разработки систем генного переноса в экспериментах in vitro. Они способны самостоятельно формировать в водной среде бислойные агрегаты, неиммуногенны и биодеградируемы.
Известен медиатор трансфекции - 1,2-диолеоил-3-триметиламмонийпропан (DOTAP), в котором гидрофобные цепи присоединены к полярной компоненте биодеградируемой сложноэфирной связью:
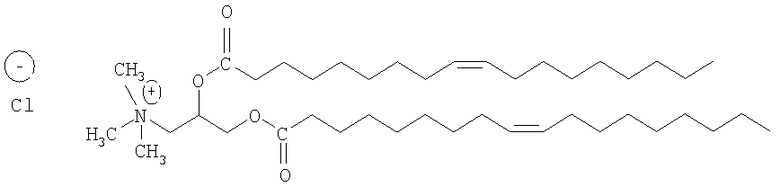
DOTAP широко применяется для доставки в клетки генетического материала, в основном в смеси с нейтральными липидами. Недостатком указанного соединения является его достаточно высокая цитотоксичность и низкая эффективность.
Наиболее близким к заявленному техническим решением является 2,3-диолеилокси-N-[2(сперминкарбоксамидо)этил]-N,N-диметил-1-пропиламоний трифторацетат «Lipofectamine 2000»).
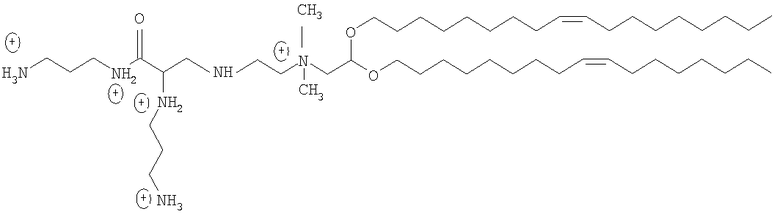
В настоящее время этот коммерческий препарат широко применяется для трансфекции in vitro, проявляет высокую эффективность в отношении линий клеток 293, СНО, COS-7, HeLa, Vero, PC 12 и многих других как в бессывороточной среде, так и в присутствии сыворотки. Разработан универсальный протокол применения «Lipofectamine», который может быть использован для решения различных задач: доставки в клетки олигонуклеотидов, малой интерферирующей РНК, а также плазмидных конструктов, кодирующих биосинтез специальных белков.
Однако «Lipofectamine» обладает заметной токсичностью и малоэффективен для некоторых типов клеток, например лейкоцитов. Кроме того, недостатком препарата является сложность его детектирования в клетке, что является необходимым условием для изучения механизма преодоления плазматических мембран и локализации внутри клетки. Это не позволяет определить, на каком этапе процесса трансфекции происходит снижение эффективности.
Техническим результатом предлагаемого изобретения является создание катионного липодипептида, 1-гексадецил-5-(1-пиренбутинил)-N-(L-орнитил)-L-глутамат бисхлорида, содержащего стабильную флуоресцентную метку на основе пирена.
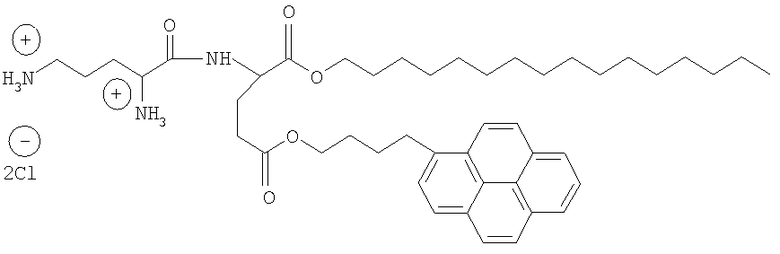
Пирен является одним из наиболее часто используемых в клеточной биологии флуорофоров при изучении транспорта или метаболизма липидов. Его отличительными характеристиками являются длительное время существования в возбужденном состоянии и гидрофобность, благодаря которой он не оказывает заметного влияния на конформацию липидных молекул [Р.Somerharju, Chemistry and Physics of Lipids, 2002, 116, 57-74]. Кроме того, отличительной особенностью медиатора трансфекции на основе дипептида является высокая трансфекционная активность на опухолевых, неопухолевых, а также труднотрансфицируемых линиях клеток, которая сопоставима или превышает эффективность коммерческих агентов, низкая токсичность и высокая аффинность по отношению к нуклеиновым кислотам.
Для достижения указанного технического результата разработана схема получения соединения, состоящая из следующих стадий: получение эфира L-глутаминовой кислоты - гидрофобного блока амфифила, защита и активация L-орнитина - гидрофильного блока, удаление защитных групп и введение флуоресцентной метки.
Реализация данного изобретения подтверждается примером.
К раствору N-оксисукцинимидного эфира Вос2-L-орнитина 0.1 г (0.175 ммоль) в 4 мл THF и при перемешивании порциями добавляли 0.072 г (0.193 ммоль) 1-гексадецил-5-третбутил-L-глутамата (2). Смесь выдерживали при комнатной температуре 5 ч, растворитель отгоняли в вакууме. Продукт выделяли препаративной ТСХ в системе толуол-хлороформ-метилэтилкетон 10:6:3. Выход 0.06 г (33.3%). Выход 0.107 г (52%), Rf 0.60 (толуол-хлороформ-метилэтилкетон 10:6:3), [α]D 20+10° (с 0.1, С2Н5ОН).
Полученный защищенный дипептид 0.1 г (0.23 ммоль) растворяли в 3 мл хлороформа, добавляли 0.3 мл безводной СF3СООН. Раствор перемешивали при комнатной температуре 12 ч. Кислоту отгоняли в вакууме. Продукт выделяли тонкослойной хроматографией на силикагеле в системе хлороформ-метанол-вода 7:3:1. Выход 0.098 г (99%), Rf 0.1 (Б), [α]D 20+25° (с 0.1, C2H5OH). Масс-спектр [M]+ 486.41.
Введение флуоресцентной метки осуществляли следующим способом.
К 0.055 г (0.092 ммоль) 5-гексадецил-N-(L-орнитил)-L-глутамата добавляли 26 мкл (0.37 ммоль) тионилхлорида и каплю ДМФА. Нагревали в течение 2 ч при 50°С, после чего отгоняли тионилхлорид и ДМФА в вакууме. Полученное аморфное вещество растворяли в 3 мл хлороформа, добавляли раствор 0.025 г (0.092 ммоль) 1-пиренбутанола в хлороформе, реакционную массу перемешивали в течение суток при комнатной температуре. Растворитель отгоняли в вакууме. Продукт выделяли препаративной тонкослойной хроматографией на силикагеле в системе хлороформ-метанол 9:1. Выход 0.03 г (38%), Rf 0.3 (хлороформ-метанол, 9:1).
1Н-ЯМР-спектр (СDСl3, δ, м. д.): 0.8 (3 Н, т, СН3), 1.22 (24 Н, с, 12 CH2), 1.6 (4 Н, м, 2βСН2), 1.75 (2 Н, м, CH2), 2.14 (2 Н, м, СH2), 2.6 (2 Н, м, CH2CH2), 2.7 (2 Н, т, CH2СОО), 3.9 (2 Н, м, αСН2), 4.2-4.5 (2 Н, м, 2СН), 7.6 (5Н, м, СН=), 8.7 (4 Н, с, NH3 +).
Масс-спектр [М]+ 742.81.
УФ (хлороформ, макс., нм): 270,280.8, 338, 353.
Спектр флуоресценции (λехс=355, макс., нм): 381, 399.
Полученный нами флуоресцентный липодипептид не уступает по своим биологическим параметрам коммерческому агенту «Lipofectamine». При этом эффективность изобретения может быть охарактеризована приведенными ниже данными.
В результате исследования тропности липосом к клеткам линии COS-7 с помощью флуоресцентной микроскопии было показано, что через 35 минут после инкубации наблюдается флуоресценция клеток по периметру, что свидетельствует о связывании липосом с клетками, а через 60-80 мин происходит накопление флуоресцентной метки в цитоплазме в виде дискретных образований и по периметру ядра.
На опухолевых клетках (НЕР) синтезированное соединение проявило эффективность трансфекции 83%, специальный реагент для данного типа клеток (HEP-G2 transfection reagent) в тех же условиях проявил меньшую активность (77%). В экспериментах с неопухолевыми клетками (СНО) эффективность трансфекции была сопоставима с контрольным образцом (69% и 71% соответственно). Полученный медиатор трансфекции проявил достаточно высокий уровень активности (49%) по отношению к лейкоцитам крысы - клеткам, которые относятся к плохо трансфицируемым линиям клеток и эффективность для них на большинстве коммерческих препаратов не превышает 35%. Синтезированное соединение проявило токсичность по отношению к клеткам HeLa и НЕР в 10 раз меньшую, по сравнению с аналогом «Lipofectamine».
Продемонстрированная высокая эффективность трансфекции для 1-гексадецил-5-(1-пиренбутинил)-N-(L-орнитил)-L-глутамат бисхлорида позволит использовать его в биохимических исследованиях, направленных на получение специальных белков для целей молекулярной биологии, цитологии и медицины. Благодаря наличию устойчивой флуоресцентной метки в структуре синтезированного соединения становится возможным изучение локализации меченых липосом и времени протекания процесса трансфекции.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛИПОТЕТРАПЕПТИДЫ НА ОСНОВЕ ДИЭФИРОВ L-ГЛУТАМИНОВОЙ КИСЛОТЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2013 |
|
RU2533554C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИПОДИПЕПТИДОВ | 2011 |
|
RU2463307C1 |
| ДОСТАВКА НУКЛЕИНОВЫХ КИСЛОТ | 1995 |
|
RU2160278C2 |
| ЛИПОТРИПЕПТИДЫ НА ОСНОВЕ ДИЭФИРОВ L-ГЛУТАМИНОВОЙ КИСЛОТЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2014 |
|
RU2575851C1 |
| ФОЛАТ-ПОЛИЭТИЛЕНГЛИКОЛЬ-ДИГЕКСАДЕЦИЛ-L-ГЛУТАМАТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2011 |
|
RU2472796C1 |
| rac-N-[2,3-ДИ(ТЕТРАДЕЦИЛОКСИ)ПРОП-1-ИЛ]ПИРИДИНИЙ БРОМИД В КАЧЕСТВЕ АГЕНТА ДЛЯ ДОСТАВКИ НУКЛЕИНОВЫХ КИСЛОТ В КЛЕТКИ МЛЕКОПИТАЮЩИХ | 2009 |
|
RU2405772C1 |
| Незаряженный липид, композиция на его основе с поликатионным амфифилом и нейтральным фосфолипидом и способ ее получения для доставки нуклеиновых кислот in vitro | 2020 |
|
RU2747559C1 |
| Способ получения амфифильных блок-сополимеров N,N-диметиламиноэтилметакрилата для доставки нуклеиновых кислот в живые клетки | 2014 |
|
RU2617059C2 |
| МОДИФИЦИРОВАННАЯ ЛИПИДОМ ДВУХЦЕПОЧЕЧНАЯ РНК, ОБЛАДАЮЩАЯ ЭФФЕКТОМ РНК-ИНТЕРФЕРЕНЦИИ | 2008 |
|
RU2489167C2 |
| Пептиды для внутриклеточной доставки нуклеиновых кислот | 2020 |
|
RU2771605C2 |
Изобретение относится к липодипептиду, представляющему собой 1-гексадецил-5-(1-пиренбутил)-N-(L-орнитил)-L-глутамат бисхлорид, который проявляет способность доставлять нуклеиновые кислоты в клетки и содержит в своей структуре стабильную флуоресцентную метку в виде пирена. Полученное соединение по сравнению с «Lipofectamine» проявило меньшую в 10 раз токсичность по отношению к клеткам HeLa и НЕР. Синтезированное соединение проявило более высокую эффективность трансфекции на опухолевых (HeLa, НЕР, COS-7) и неопухолевых линиях клеток (СНО, лейкоциты крысы), чем специально разработанные коммерческие агенты трансфекции для клеток НЕР и СНО. Благодаря наличию устойчивой флуоресцентной метки в структуре синтезированного соединения существенно расширяется область применения таких веществ и становится возможным изучение локализации меченых липосом и времени протекания процесса трансфекции.
1-гексадецил-5-(1-пиренбутил)-N-(L-орнитил)-L-глутамат бисхлорид
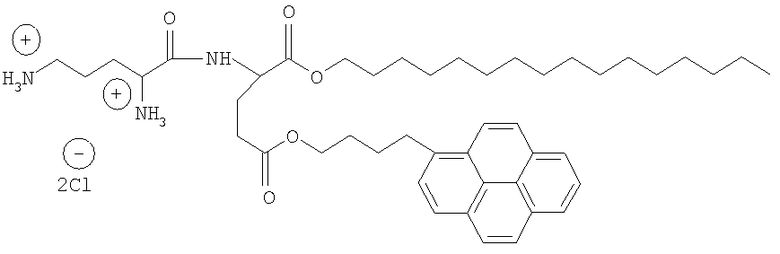
как медиатор трансфекции.
| КАТИОННЫЕ ДИМЕРНЫЕ АМФИФИЛЫ В КАЧЕСТВЕ АГЕНТОВ ТРАНСФЕКЦИИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2002 |
|
RU2233834C2 |
| WO 9700241 A1, 03.01.1997 | |||
| Себякин Ю.Л | |||
| и др | |||
| рН-ЧУВСТВИТЕЛЬНЫЕ КАТИОННЫЕ ЛИПОПЕПТИДЫ ДЛЯ СОЗДАНИЯ ТРАНСПОРТНЫХ СИСТЕМ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ | |||
| БИООРГАНИЧЕСКАЯ ХИМИЯ, 2006, Т.32, №5, С.453-458. | |||
Авторы
Даты
2011-01-20—Публикация
2009-03-04—Подача