ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новым вариантам ИЛ-21, где указанные варианты полезны для терапии.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Пептиды ИЛ-21 были впервые раскрыты в WO 00/53761 как SEQ ID No:2. Пропептид представляет собой пептид из 161 аминокислотного остатка. Для удобства эта последовательность повторена в настоящей заявке как SEQ ID No:1. Первоначально считали, что зрелый пептид представляет собой пептид, состоящий из аминокислот №33-162 последовательности SEQ ID No:1; однако затем (WO 2004/112703) предположили, что зрелый пептид представляет собой в действительности аминокислоты №30-162, что представлено как SEQ ID No:11 с дополнительным N-концевым метионином в настоящей заявке.
ИЛ-21 представляет собой цитокин. Цитокины в целом стимулируют пролиферацию, дифференциацию и/или активацию клеток гемопоэтической линии или принимают участие в механизмах иммунного и воспалительного ответа организма. Интерлейкины представляют собой семейство цитокинов, которые опосредуют иммунологические ответы посредством продуцирования различных цитокинов, и они осуществляют адаптивный иммунитет к антигенам. Зрелые Т клетки могут быть активированы, например, антигеном или другим стимулом, на продуцирование, например, цитокинов, молекул биохимической передачи сигнала или рецепторов, которые далее влияют на судьбу популяции Т клеток.
Цитокины, продуцируемые Т клеткой, классифицированы на тип 1 и тип 2 (Kelso, A. Immun. Cell Biol. 76: 300-317, 1998). Цитокины типа 1 включают ИЛ-2, ИФН-γ, LT-α, и они вовлечены в воспалительные ответы, иммунитет к вирусам, иммунитет к внутриклеточным паразитам и отторжение аллотрансплантата. Цитокины типа 2 включают ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-10 и ИЛ-13, и они вовлечены в гуморальные ответы, иммунитет к гельминтам и аллергический ответ. Общие цитокины между типом 1 и 2 включают ИЛ-3, GM-CSF и TNF-α. Имеются некоторые данные, позволяющие предположить, что популяции Т клеток, продуцирующие тип 1 и тип 2, преимущественно мигрируют в различные типы воспаленной ткани.
Зрелые Т клетки могут быть активированы, например, антигеном или другим стимулом, на продуцирование, например, цитокинов, молекул биохимической передачи сигнала или рецепторов, которые далее влияют на судьбу популяции Т клеток.
В клетки могут быть активированы посредством рецепторов на их клеточной поверхности, включая рецептор В клеток и другие вспомогательные молекулы для осуществления вспомогательных клеточных функций, таких как продуцирование цитокинов и антител.
Естественные клетки-киллеры (NK) имеют общую клетку-предшественника с Т клетками и В клетками и играют роль в иммунном контроле. МК-клетки, которые включают вплоть до 15% лимфоцитов крови, не экспрессируют рецепторы антигенов и, следовательно, не используют распознавание ГКС (главным комплексом гистосовместимости) как потребность для связывания с клеткой-мишенью. МК-клетки вовлечены в распознавание и уничтожение некоторых опухолевых клеток и клеток, инфицированных вирусами. Считают, что in vivo NK-клетки требуют активации, однако показано, что in vitro МК-клетки уничтожают некоторые типы опухолевых клеток посредством активации, зависимой от лиганда KIR.
Несмотря на эффективность, проявляемую ИЛ-21 при лечении различных заболеваний, остается необходимость в вариантах ИЛ-21 с улучшенными или альтернативными свойствами, такими как активность, избирательность, стабильность и время циркуляции или период биологической полужизни, для удовлетворения медицинских нужд.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Авторы настоящего изобретения неожиданно сделали открытие, что активность ИЛ-21 в высокой степени сохраняется или даже улучшается, когда аминокислоты в области 66-98 делегированы и/или заменены. В настоящем контексте нумерация аминокислот соответствует зрелому 133-аминокислотному пептиду (аминокислоты №30-162 пропептида, SEQ ID No:1). Данная последовательность приведена как SEQ ID No:11, включая дополнительный N-концевой метионин, с получением 134-аминокислотного пептида. SEQ ID No:2 представляет собой аминокислоты №30-162 пропептида, SEQ ID No:1, без дополнительного N-концевого метионина с получением 133-аминокислотного пептида. Соответственно, в одном воплощении изобретение относится к пептиду, содержащему
а) первую последовательность, полученную в результате делеции и/или замены одной или более чем одной аминокислоты в области, состоящей из а.к. с аминокислоты №65 до аминокислоты №96 последовательности SEQ ID No:2;
или
б) последовательность, полученную в результате консервативной замены вплоть до 10 аминокислот в указанной первой последовательности.
В одном воплощении в изобретении предложено применение пептида по настоящему изобретению в терапии.
В одном воплощении изобретение относится к фармацевтической композиции, содержащей пептид по настоящему изобретению.
В одном воплощении в изобретении предложен терапевтический способ, при котором вводят терапевтически эффективное количество пептида по настоящему изобретению пациенту, нуждающемуся в этом.
В одном воплощении изобретение относится к применению пептида по настоящему изобретению при изготовлении лекарственного средства.
В одном воплощении изобретение относится к нуклеиново-кислотной конструкции, кодирующей пептид по настоящему изобретению; к векторам, содержащим указанные конструкции; и к клеткам-хозяевам, содержащим указанные векторы.
В одном воплощении изобретение относится к специфичным антителам против пептида по настоящему изобретению.
ГРАФИЧЕСКИЕ МАТЕРИАЛЫ
Фиг.1. Baf3/hIL-21R/Stat-Luc анализ вариантов ИЛ-21
Надосадочная жидкость из клеток HEK293-FS, трансфицированных указанными конструкциями ИЛ-21, была проанализирована в анализе гена-репортера BAf3-hIL-21R/Stat-Luc. Содержание белка оценивали с помощью ЭЛАЙЗА (твердофазного иммуноферментного анализа).
■ ИЛ-21 дикого типа; ▲ делеционный мутант ИЛ-21 [А83-R86] (SEQ ID No: 3); и ∆ вариант ИЛ-21, в котором последовательность [К77-Т92] заменена (SEQ ID No: 7).
Фиг.2. Кривые доза-ответ для hIL-WT и ChimIL-21/4
Очищенные белки были проанализированы в анализе гена-репортера с использованием клеток Ваf3/hИЛ-21Rа. Кривые представляют собой суммирование независимых экспериментов (n=4), где все проведены в трех повторах. Активность выражена в виде процента максимального ответа. Представлены полученные значения ЕС50±S.E.M. Chim-IL21 представляет собой ИЛ-21 sub[K77-Т92].
ОПРЕДЕЛЕНИЯ
В настоящем контексте единственное число предназначено для обозначения одного или более чем одного.
В настоящем контексте термин "пептид" предназначен для обозначения двух или более чем двух аминокислот, которые связаны пептидной связью. Указанные кислоты могут быть кодируемыми или некодируемыми, и в этот термин также включают производные пептида, где одна или более чем одна аминокислота в пептиде химически замещена, например, ПЭГ или липофильной группой. Термины "пептид" и "полипептид" использованы взаимозаменяемо и предназначены для обозначения одного и того же.
В настоящем контексте термин "фармацевтически приемлемая соль" предназначен для обозначения солей, которые не являются вредными для пациента. Такие соли включают фармацевтически приемлемые соли присоединения кислоты, фармацевтически приемлемые соли металлов, аммония и соли алкилированного аммония. Соли присоединения кислоты включают соли как неорганических кислот, так и органических кислот. Репрезентативные примеры пригодных неорганических кислот включают соляную, бромисто-водородную, йодисто-водородную, фосфорную, серную, азотную кислоту и тому подобное. Репрезентативные примеры пригодных органических кислот включают муравьиную, уксусную, трихлоруксусную, трифторуксусную, пропионовую, бензойную, коричную, лимонную, фумаровую, гликолевую, молочную, малеиновую, яблочную, малоновую, миндальную, щавелевую, пикриновую, пировиноградную, салициловую, янтарную, метансульфоновую, этансульфоновую, винную, аскорбиновую, памовую, бисметиленсалициловую, этандисульфоновую, глюконовую, цитраконовую, аспарагиновую, стеариновую, пальмитиновую, ЭДТА, гликолевую, пара-аминобензойную, глутаминовую, бензолсульфоновую, пара-толуолсульфоновую кислоту и тому подобное. Дополнительные примеры фармацевтически приемлемых солей присоединения неорганической или органической кислоты включают фармацевтически приемлемые соли, приведенные в J. Pharm. Sci. 1977, 66, 2, которая включена здесь путем ссылки. Примеры солей металлов включают соли лития, натрия, калия, магния и тому подобное. Примеры солей аммония и алкилированного аммония включают соли аммония, метиламмония, диметиламмония, триметиламмония, этиламмония, гидроксиэтиламмония, диэтиламмония, бутиламмония, тетраметиламмония и тому подобное.
"Терапевтически эффективное количество" пептида, как используют здесь, означает количество, достаточное для лечения, облегчения или частичной остановки клинических проявлений данного заболевания и его осложнений. Количество, адекватное для осуществления этого, определяют как "терапевтически эффективное количество". Эффективные количества для каждой цели будут зависеть как от типа и тяжести заболевания или повреждения, так и от массы и общего состояния субъекта. Должно быть понятно, что определение подходящей дозировки может быть достигнуто с использованием рутинного экспериментирования путем конструирования матрицы значений и тестирования различных точек в этой матрице, которое находится в пределах компетенции обычного практикующего врача или ветеринара.
Термин "терапия" и "лечение", как используют здесь, означает управляемую помощь пациенту в целях борьбы с состоянием, таким как заболевание или расстройство. В этот термин следует включать полный спектр терапий для данного состояния, которым страдает пациент, таких как введение активного соединения для облегчения симптомов или осложнений, для замедления прогрессирования заболевания, расстройства или состояния, для облегчения или ослабления симптомов и осложнений и/или для лечения или элиминации заболевания, расстройства или состояния, а также для предупреждения состояния, где предупреждение следует понимать как управляемую помощь пациенту в целях борьбы с заболеванием, состоянием или расстройством и включать в него введение активных пептидов для предупреждения возникновения симптомов или осложнений. Пациент, подлежащий лечению, предпочтительно представляет собой млекопитающее, в частности, человека, но может также включать животных, таких как собаки, кошки, коровы, овцы и свиньи. Должно быть понятно, что терапевтический и профилактический (превентивный) режимы представляют отдельные аспекты настоящего изобретения.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В одном воплощении изобретение относится к пептиду, содержащему
а) первую последовательность, полученную в результате делеции и/или замены одной или более чем одной аминокислоты в области, состоящей из аминокислоты №65 до аминокислоты №96 SEQ ID No:2;
или
б) последовательность, полученную в результате консервативной замены вплоть до 10 аминокислот в указанной первой последовательности. В частности, по меньшей мере 2, как, например, по меньшей мере 3, как, например, по меньшей мере 4, как, например, по меньшей мере 5, как, например, по меньшей мере 6 аминокислот делегированы и/или заменены в указанной первой последовательности.
Изобретение также относится к пептидам, полученным путем консервативных замен в более конкретных воплощениях пептида по настоящему изобретению, описанных ниже.
В частности, вплоть 10, как, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 аминокислот могут быть консервативно заменены. В настоящем контексте замена является консервативной, когда один аминокислотный остаток заменен другим аминокислотным остатком из той же группы, то есть другим аминокислотным остатком с подобными свойствами. Аминокислоты можно для удобства разделить на следующие группы на основании их свойств: основные аминокислоты (такие как аргинин и лизин), кислые аминокислоты (такие как глутаминовая кислота и аспарагиновая кислота), полярные аминокислоты (такие как глутамин, гистидин, метионин и аспарагин), алифатические или гидрофобные аминокислоты (такие как аланин, лейцин, изолейцин, валин), ароматические аминокислоты (такие как фенилаланин, триптофан, тирозин) и малые аминокислоты (такие как глицин, аланин, серин и треонин).
В одном воплощении изобретение относится к пептиду, содержащему последовательность, полученную в результате делеции и/или замены одной или более чем одной аминокислоты в области, состоящей из аминокислоты №83 до аминокислоты №86 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, содержащему последовательность, полученную в результате делеции и/или замены одной или более чем одной аминокислоты в области, состоящей из аминокислоты №83 до аминокислоты №88 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, содержащему последовательность, полученную в результате делеции и/или замены одной или более чем одной аминокислоты в области, состоящей из аминокислоты №83 до аминокислоты №90 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, содержащему последовательность, полученную в результате делеции и/или замены одной или более чем одной аминокислоты в области, состоящей из аминокислоты №82 до аминокислоты №88 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, содержащему последовательность, полученную в результате делеции и/или замены одной или более чем одной аминокислоты в области, состоящей из аминокислоты №77 до аминокислоты №92 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, содержащему последовательность, полученную в результате делеции и/или замены одной или более чем одной аминокислоты в области, состоящей из аминокислоты №71 до аминокислоты №92 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, содержащему последовательность, полученную в результате делеции и/или замены одной или более чем одной аминокислоты в области, состоящей из аминокислоты №65 до аминокислоты №92 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, содержащему последовательность, полученную в результате делеции и/или замены одной или более чем одной аминокислоты в области, состоящей из аминокислоты №77 до аминокислоты №96 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, содержащему последовательность, полученную в результате делеции одной или более чем одной аминокислоты в области, состоящей из аминокислоты №83 до аминокислоты №86 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, содержащему последовательность, полученную в результате делеции одной или более чем одной аминокислоты в области, состоящей из аминокислоты №83 до аминокислоты №88 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, содержащему последовательность, полученную в результате делеции одной или более чем одной аминокислоты в области, состоящей из аминокислоты №83 до аминокислоты №90 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, содержащему последовательность, полученную в результате делеции одной или более чем одной аминокислоты в области, состоящей из аминокислоты №82 до аминокислоты №88 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, содержащему последовательность, полученную в результате замены и делеции двух или более чем двух аминокислот в области, состоящей из аминокислоты №77 до аминокислоты №92 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, содержащему последовательность, полученную в результате замены и делеции двух или более чем двух аминокислот в области, состоящей из аминокислоты №71 до аминокислоты №92 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, содержащему последовательность, полученную в результате замены и делеции двух или более чем двух аминокислот в области, состоящей из аминокислоты №65 до аминокислоты №92 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, содержащему последовательность, полученную в результате замены и делеции двух или более чем двух аминокислот в области, состоящей из аминокислоты №77 до аминокислоты №96 SEQ ID No: 2.
В одном воплощении изобретение относится к пептиду, полученному путем делеции и/или замены одной или более чем одной аминокислоты в области, состоящей из аминокислоты №83 до аминокислоты №86 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, полученному путем делеции и/или замены одной или более чем одной аминокислоты в области, состоящей из аминокислоты №83 до аминокислоты №88 SEQ ID NO:2.
В одном воплощении изобретение относится к пептиду, полученному путем делеции и/или замены одной или более чем одной аминокислоты в области, состоящей из аминокислоты №83 до аминокислоты №90 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, полученному путем делеции и/или замены одной или более чем одной аминокислоты в области, состоящей из аминокислоты №82 до аминокислоты №88 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, полученному путем делеции и/или замены одной или более чем одной аминокислоты в области, состоящей из аминокислоты №77 до аминокислоты №92 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, полученному путем делеции и/или замены одной или более чем одной аминокислоты в области, состоящей из аминокислоты №71 до аминокислоты №92 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, полученному путем делеции и/или замены одной или более чем одной аминокислоты в области, состоящей из аминокислоты №65 до аминокислоты №92 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, полученному путем делеции и/или замены одной или более чем одной аминокислоты в области, состоящей из аминокислоты №77 до аминокислоты №96 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, полученному путем делеции одной или более чем одной аминокислоты в области, состоящей из аминокислоты №83 до аминокислоты №86 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, полученному путем делеции одной или более чем одной аминокислоты в области, состоящей из аминокислоты №83 до аминокислоты №88 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, полученному путем делеции одной или более чем одной аминокислоты в области, состоящей из аминокислоты №83 до аминокислоты №90 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, полученному путем делеции одной или более чем одной аминокислоты в области, состоящей из аминокислоты №82 до аминокислоты №88 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, полученному путем замены и делеции двух или более чем двух аминокислот в области, состоящей из аминокислоты №77 до аминокислоты №92 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, полученному путем замены и делеции двух или более чем двух аминокислот в области, состоящей из аминокислоты №71 до аминокислоты №92 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, полученному путем замены и делеции двух или более чем двух аминокислот в области, состоящей из аминокислоты №65 до аминокислоты №92 SEQ ID No:2.
В одном воплощении изобретение относится к пептиду, полученному путем замены и делеции двух или более чем двух аминокислот в области, состоящей из аминокислоты №77 до аминокислоты №96 SEQ ID No:2.
Как обсуждено выше, ИЛ-21 экспрессируется в виде 161-аминокислотного пептида, но претерпевает посттрансляционный процессинг путем удаления аминокислот №1-29 или путем удаления аминокислот №1-31. В настоящее изобретение, таким образом, следует также включать пептиды, содержащие последовательность, полученную в результате удаления и/или делеции одной или более чем одной аминокислоты из области, состоящей из аминокислоты №65 до аминокислоты №96, где N-конец удлинен N-концевыми 29 аминокислотами из SEQ ID No:1 или N-концевой 31 аминокислотой из SEQ ID No:1.
Когда пептиды экспрессируют в клетках млекопитающих, таких как клетки СНО, N-концевой сигнальный пептид часто удаляется так называемой сигнальной пептидазой, что приводит к зрелому пептиду. В данной области техники хорошо известно, что для экспрессии тех же гетерологичных пептидов в прокариотических клетках, таких как, например, Е.соli, часто необходимо посредством рекомбинантной технологии, хорошо известной специалистам в данной области техники, ввести дополнительный N-концевой метионин в последовательность зрелого пептида. Таким образом, подразумевают, что настоящее изобретение включает вышеупомянутые пептиды с N-концевым метионином и без него.
В одном воплощении изобретение относится к пептидам, выбранным из:
A) SEQ ID No:3 (делеция A83-R86), SEQ ID No:4 (делеция А83-К88), SEQ ID No:5 (делеция A83-R90) и SEQ ID No:6 (делеция N82-K88); и
Б) пептиды А) с дополнительным N-концевым Met;
B) пептиды А)-Б), где вплоть до 10 аминокислот консервативно заменены.
В одном воплощении изобретение относится к пептидам, выбранным из
Г) SEQ ID No:7 (К77-Т92 замена), SEQ ID No:8 (I71-T92 замена), SEQ ID No:9 (R65-T92 замена) и SEQ ID No:10 (K77-C96) замена; и
Д) пептиды Г) с дополнительным N-концевым Met; и
Е) пептиды Г)-Д), где вплоть до 10 аминокислот консервативно заменены.
В одном воплощении изобретение относится к фармацевтически приемлемым солям вышеуказанных пептидов.
Можно получить дополнительные производные пептидов по настоящему изобретению посредством присоединения групп, которые будут способствовать продлению времени циркуляции в плазме и/или периода биологического полураспада, либо которые будут снижать иммуногенность. В данной области техники хорошо известно, что такие эффекты могут быть получены путем присоединения определенных групп, таких как полиэтиленгликоль (ПЭГ); липофильные группы, такие как жирные кислоты; белки плазмы, такие как альбумин; или группировки, связывающие альбумин. В качестве примеров уровня техники см., например, WO 01/79271, US 5739208 и WO 03/44056.
Как используют здесь, термин "нуклеиново-кислотная конструкция" предназначен для обозначения любой молекулы нуклеиновой кислоты происхождения кДНК, геномной ДНК, синтетической ДНК или РНК. Термин "конструкция" предназначен для обозначения сегмента нуклеиновой кислоты, который может быть одно- или двухцепочечным и может быть основан на полноразмерной или частичной встречающейся в природе нуклеотидной последовательности, кодирующей интересующий белок. Эта конструкция может возможно содержать другие сегменты нуклеиновой кислоты.
Нуклеиново-кислотная конструкция по изобретению, кодирующая белок по изобретению, может пригодно иметь геномное или кДНК происхождение, например может быть получена путем изготовления геномной или кДНК библиотеки и скрининга на последовательности ДНК, кодирующие весь белок или его участок, путем гибридизации с использованием синтетических олигонуклеотидных зондов в соответствии со стандартными методиками (см. Sambrook et al., цит. выше). Для целей настоящего изобретения последовательность ДНК, кодирующая белок, предпочтительно имеет человеческое происхождение, то есть получена из библиотеки человеческой геномной ДНК или кДНК. В частности, последовательность ДНК может иметь человеческое происхождение, например, кДНК из конкретного типа органов или клеток человека или ген, полученный из человеческой геномной ДНК.
Нуклеиново-кислотная конструкция по изобретению, кодирующая пептид, может быть также получена синтетическим путем с помощью разработанных стандартных способов, например, фосфоамидитного метода, описанного Веаuсаgе and Caruthers, Tetrahedron Letters 22 (1981), 1859-1869, или метода, описанного Matthes et al., EMBO Journal 3 (1984), 801-805. В соответствии с фосфоамидитным методом синтезируют олигонуклеотиды, например, в автоматическом синтезаторе ДНК, очищают, подвергают отжигу, лигируют и клонируют в подходящих векторах.
Кроме того, нуклеиново-кислотная конструкция может иметь смешанное синтетическое и геномное, смешанное синтетическое и кДНК или смешанное геномное и кДНК происхождение, полученная в результате лигирования фрагментов синтетического, геномного или кДНК происхождения (как пригодно), где эти фрагменты соответствуют различным участкам целой нуклеиново-кислотной конструкции, в соответствии со стандартными методиками.
Нуклеиново-кислотную конструкцию можно также получить с помощью полимеразной цепной реакции, используя специфичные праймеры, например, как описано в US 4683202 или Saiki et al., Science 239 (1988), 487-491.
Нуклеиново-кислотная конструкция предпочтительно представляет собой конструкцию ДНК, и далее будет использован исключительно этот термин.
РЕКОМБИНАНТНЫЙ ВЕКТОР
В следующем аспекте настоящее изобретение относится к рекомбинантному вектору, содержащему конструкцию ДНК по изобретению.
Рекомбинантный вектор, в который встраивают конструкцию ДНК по изобретению, может представлять собой любой вектор, который можно удобно подвергать методикам рекомбинантных ДНК, и выбор вектора будет часто зависеть от клетки-хозяина, в которую его вводят. Таким образом, вектор может представлять собой автономно реплицирующийся вектор, то есть вектор, который существует в виде экстрахромосомной молекулы, репликация которой не зависит от репликации хромосомы, например, плазмиду. Альтернативно вектор может представлять собой такой вектор, который при введении в клетку-хозяина интегрирует в геном этой клетки-хозяина и реплицируется вместе с хромосомой(ами), в которую он интегрирован.
Вектор предпочтительно представляет собой экспрессионный вектор, в котором последовательность ДНК, кодирующая белок по изобретению, оперативно сцеплена с дополнительными сегментами, необходимыми для транскрипции ДНК. Как правило, экспрессионный вектор образован из плазмиды или вирусной ДНК, либо может содержать и те, и другие элементы. Термин "оперативно сцепленный" указывает на то, что сегменты упорядочены таким образом, что функционируют в соответствии с их предназначенными целями, то есть транскрипция инициируется в промоторе и продолжается на протяжении всей последовательности ДНК, кодирующей белок.
Промотор может представлять собой любую последовательность ДНК, которая проявляет транскрипционную активность в выбранной клетке-хозяине, и может быть образован из генов, кодирующих белки, либо гомологичных, либо гетерологичных для клетки-хозяина.
Примерами подходящих промоторов для направления транскрипции ДНК, кодирующей белок по изобретению, в клетках млекопитающих являются промотор SV40 (Subramani et al., Mol. Cell Biol. 1. (1981), 854-864), промотор МТ-1 (гена металлотионеина) (Palmiter et al., Science 222 (1983), 809-814) или главный поздний промотор аденовируса 2.
Примером подходящего промотора для использования в клетках насекомых является полиэдриновый промотор (US 4745051; Vasuvedan et al., FEBS Lett. 311. (1992) 7-11), промотор Р10 (J.M. Vlak et al., J. Gen. Virology 69, 1988, pp.765-776), промотор основного белка вируса полиэдроза Autographa californica (EP 397485), промотор немедленно-раннего гена 1 бакуловируса (US 5155037; US 5162222) или промотор замедленно-раннего гена 39К бакуловируса (US 5155037; US 5162222).
Примеры подходящих промоторов для использования в дрожжевых клетках-хозяевах включают промоторы из дрожжевых гликолитических генов (Hitzeman et al., J. Biol. Chem. 255 (1980), 12073-12080; Alber and Kawasaki, J. Mol. Appl. Gen. 1 (1982), 419-434) или генов алкогольдегидрогеназ (Young et al., in Genetic Engineering of Microorganisms for Chemicals (Hollaender et al, eds.), Plenum Press, New York, 1982), либо промоторы ТРИ (US 4599311) или ADH2-4c (Russell et al., Nature 304 (1983), 652-654).
Примерами подходящих промоторов для использования в клетках-хозяевах нитевидных грибов являются, например, промотор ADH3 (McKnight et al., The EMBO J. 4 (1985), 2093-2099) или промотор tpiA. Примерами других полезных промоторов являются промоторы, имеющие происхождение из гена, кодирующего ТАКА-амилазу A. oryzae, аспарагиновую протеиназу Rhizomucor miehei, нейтральную α-амилазу A. niger, кислотоустойчивую α-амилазу A. niger, глюкоамилазу А. niger или A. awamori (gluA), липазу Rhizomucor miehei щелочную протеазу A. oryzae, триозофосфатизомеразу A. oryzae или ацетамидазу A. nidulans. Предпочтительными являются промоторы ТАКА-амилазы и gluA.
Примеры подходящих промоторов для использования в бактериальных клетках-хозяевах включают промотор гена мальтогенной амилазы Bacillus stearothermophilus, гена альфа-амилазы Bacillus licheniformis, гена BAN амилазы Bacillus amyloliquefaciens, гена щелочной протеазы Bacillus subtilis или гена ксилозидазы Bacillus pumilus, либо промоторы PR или PL фага лямбда, либо промоторы Е. coli lac, trp или tac.
Последовательность ДНК, кодирующая белок по изобретению, может быть также, если необходимо, оперативно соединена с подходящим терминатором, таким как терминатор гормона роста человека (Palmiter et al., op. cit), либо терминаторы (для хозяев-грибов) ТРI1 (Alber and Kawasaki, op. cit.) или ADH3 (McKnight et al., op. cit.). Вектор может дополнительно содержать элементы, такие как сигналы полиаденилирования (например, из SV40 или области 5 Elb аденовируса), последовательности транскрипционных энхансеров (например, энхансер SV40) и последовательности трансляционных энхансеров (например, кодирующие последовательности VA РНК аденовирусов).
Рекомбинантный вектор по изобретению может дополнительно содержать последовательность ДНК, обеспечивающую репликацию вектора в данной клетке-хозяине. Примером такой последовательности (когда клетка-хозяин представляет собой клетку млекопитающего) является точка начала репликации SV40.
Когда клетка-хозяин представляет собой дрожжевую клетку, пригодными последовательностями, обеспечивающими репликацию вектора, являются гены репликации REP 1-3 и точка начала репликации дрожжевой 2µ плазмиды.
Когда клетка-хозяин представляет собой бактериальную клетку, последовательностями, обеспечивающими репликацию вектора, являются гены, кодирующие комплекс ДНК-полимеразы III, и точка начала репликации.
Вектор может также содержать селективный маркер, например, ген, продукт которого комплементирует дефект клетки-хозяина, такой как ген, кодирующий дигидрофолатредуктазу (DHFR), или ген TPI Schizosaccharomyces pombe (описанный Р.R. Russell, Gene 40, 1985, pp.125-130), либо ген, который придает устойчивость к лекарственному средству, например, к ампициллину, канамицину, тетрациклину, хлорамфениколу, неомицину, гигромицину или метотрексату. Для нитевидных грибов селективные маркеры включают amdS. pyrG. argB. niaD и sC.
Чтобы направить белок по настоящему изобретению в секреторный биохимический путь клеток-хозяев, в рекомбинантном векторе можно обеспечить секреторную сигнальную последовательность (также известную как лидерная последовательность, препропоследовательность или препоследовательность). Эта секреторная сигнальная последовательность соединена с последовательностью ДНК, кодирующей белок, в правильной рамке считывания. Секреторные сигнальные последовательности обычно расположены 5' к последовательности ДНК, кодирующей белок. Секреторная сигнальная последовательность может представлять собой такую последовательность, которая в норме связана с белком, либо последовательность из гена, кодирующего другой секретируемый белок.
Для секреции из дрожжевых клеток секреторная сигнальная последовательность может кодировать любой сигнальный пептид, который обеспечивает эффективную направленность экспрессируемого белка в секреторный биохимический путь клетки. Этот сигнальный пептид может представлять собой встречающийся в природе сигнальный пептид или его функциональный участок, либо может представлять собой синтетический пептид. Пригодные сигнальные пептиды, которые были обнаружены, представляют собой сигнальный пептид α-фактора (см. US 4870008), сигнальный пептид слюнной амилазы мыши (см. О.Hagenbuchle et al., Nature 289. 1981, pp.643-646), модифицированный сигнальный пептид карбоксипептидазы (см. L.A.Vails et al., Cell 48, 1987, pp.887-897), сигнальный пептид BAR1 дрожжей (см. WO 87/02670) или сигнальный пептид дрожжевой аспарагиновой протеазы 3 (YAP3) (см. М.Egel-Mitani et al., Yeast 6. 1990, pp.127-137).
Для эффективной секреции в дрожжах последовательность, кодирующая лидерный пептид, может быть также встроена ниже сигнальной последовательности и выше последовательности ДНК, кодирующей белок.
Функция лидерного пептида состоит в том, чтобы дать возможность направленной доставки экспрессируемого белка из эндоплазматического ретикулума в аппарат Гольджи и далее в секреторную везикулу для секреции в культуральную среду (то есть экспортирования белка через клеточную стенку или по меньшей мере через клеточную мембрану в периплазматическое пространство дрожжевой клетки). Лидерный пептид может представлять собой лидерный пептид дрожжевого α-фактора (использование которого описано, например, в US 4546082, ЕР 16201, ЕР 123294, ЕР 123544 и ЕР 163529). Альтернативно лидерный пептид может представлять собой синтетический лидерный пептид, который представляет собой, иными словами, лидерный пептид, не обнаруженный в природе. Синтетические лидерные пептиды можно, например, сконструировать, как описано в WO 89/02463 или WO 92/11378.
Для использования в нитевидных грибах сигнальный пептид может для удобства иметь происхождение из гена, кодирующего амилазу или глюкоамилазу Aspergillus sp., гена, кодирующего липазу или протеазу Rhizomucor miehei или липазу Humicola lanuginosa. Сигнальный пептид предпочтительно имеет происхождение из гена, кодирующего ТАКА-амилазу A. oryzae, нейтральную α-амилазу A. niger, кислотоустойчивую амилазу A. niger или глюкоамилазу A. niger.
Для использования в клетках насекомых сигнальный пептид может для удобства иметь происхождение из гена насекомых (см. WO 90/05783), как, например, сигнальный пептид предшественника адипокинетического гормона бабочки Manduca sexta (см. US 5023328).
Методики, используемые для лигирования последовательностей ДНК, кодирующих белок по настоящему изобретению, промотор и возможно терминатор и/или секреторную сигнальную последовательность, соответственно, и для встраивания их в подходящие векторы, содержащие информацию, необходимую для репликации, хорошо известны специалистам в данной области техники (см., например, Sambrook et al., цит. выше).
КЛЕТКИ-ХОЗЯЕВА
Клетка-хозяин, в которую вводят конструкцию ДНК или рекомбинантный вектор по изобретению, может представлять собой любую клетку, которая способна продуцировать белок по настоящему изобретению, и включает бактериальные, дрожжевые, грибные и высшие эукариотические клетки.
Примерами бактериальных клеток-хозяев, которые при культивировании способны продуцировать белок по изобретению, являются грамположительные бактерии, такие как штаммы Bacillus, такие как штаммы B. subtilis, В. licheniformis, В. lentus, В. brevis, В. stearothermophilus, В. alkalophilus, В. amyloliquefaciens, В. coagulans, В. circulans, В. lautus, В. megatherium или B. thuringiensis, либо штаммы Streptomyces, таких как S. lividans или S. murinus, или грамотрицательные бактерии, такие как Echerichia coli. Трансформацию бактерий можно осуществлять путем трансформации протопластов или путем использования компетентных клеток способом, который сам по себе известен (см. Sambrook et al., цит. выше).
При экспрессии белка в бактериях, таких как Е. соli, этот белок может удерживаться в цитоплазме, типично в виде нерастворимых гранул (известных как тельца включения), либо может направляться в периплазматическое пространство последовательностью бактериальной секреции. В первом случае клетки лизируют, и гранулы выделяют и денатурируют, после чего белок снова претерпевает укладку в результате разбавления денатурирующего агента. В последнем случае белок можно выделить из периплазматического пространства путем разрушения клеток, например, в результате озвучивания ультразвуком или осмотического шока, с высвобождением содержимого периплазматического пространства и выделением белка.
Примерами пригодных клеточных линий млекопитающих являются клеточные линии COS (АТСС CRL 1650), ВНК (АТСС CRL 1632, АТСС CCL 10), CHL (АТСС CCL39) или СНО (АТСС CCL 61). Способы трансфекции клеток млекопитающих и экспрессии последовательностей ДНК, введенных в эти клетки, описаны, например, в Kaufman and Sharp, J.Mol.Biol. 159 (1982). 601-621; Southern and Berg, J.Mol.Appl. Genet. 1 (1982), 327-341; Loyter et al., Proc. Natl. Acad. Sci. USA 79 (1982), 422-426; Wigler et al., Cell 14 (1978), 725; Corsaro and Pearson, Somatic Cell Genetics 7 (1981), 603, Graham and van der Eb, Virology 52 (1973), 456; и Neumann et al., EMBO J. 1(1982), 841-845.
Примеры пригодных дрожжевых клеток включают клетки Saccharomyces spp. или Schizosaccharomyces spp., в частности штаммы Saccharomyces cerevisiae или Saccharomyces kluyveri. Способы трансформации дрожжевых клеток гетерологичной ДНК и продуцирование гетерологичных белков из них описаны, например, в US 4599311, US 4931373, US 4870008, 5037743 и US 4845075, все из которых включены здесь путем ссылки. Трансформированные клетки отбирают по фенотипу, определяемому селективным маркером, обычно устойчивости к лекарственному средству или способности к росту в отсутствие конкретного питательного вещества, например, лейцина. Предпочтительным вектором для использования в дрожжах является вектор РОТ1, раскрытый в US 4931373.
Последовательности ДНК, кодирующей белок по изобретению, может предшествовать сигнальная последовательность и возможно лидерная последовательность, например, как описано выше. Дополнительными примерами подходящих дрожжевых клеток являются штаммы Kluyveromyces, таких как К. lactis, Hansenula, например Н. polymorpha, или Pichia, например Р. pastoris (см. Gleeson et al., J.Gen.Microbiol. 132. 1986, pp.3459-3465; US 4882279).
Примерами других грибных клеток являются клетки нитевидных грибов, например, Aspergillus spp., Neurospora spp., Fusarium spp. или Trichoderma spp., в частности штаммы A. oryzae, A. nidulans или A. niger. Использование Aspergillus spp. для экспрессии белков описано, например, в ЕР 272277 и ЕР 230023. Трансформацию F. oxysporum можно, например, осуществлять, как описано Malardieretal., 1989, Gene 78:147-156.
Когда нитевидный гриб используют в качестве клетки-хозяина, его можно трансформировать конструкцией ДНК по изобретению, для удобства путем интеграции этой конструкции ДНК в хромосому хозяина, с получением рекомбинантной клетки-хозяина. Эту интеграцию, как правило, рассматривают как преимущество, поскольку последовательность ДНК наиболее вероятно стабильно сохраняется в клетке. Интеграцию конструкций ДНК в хромосому хозяина можно осуществлять в соответствии с общепринятыми способами, например, путем гомологичной или гетерологичной рекомбинации.
Трансформацию клеток насекомых и продуцирование в них гетерологичных белков можно осуществлять, как описано в US 4745051; US 4879236; US 5155037; 5162222; ЕР 397485, все из которых включены здесь путем ссылки. Клеточная линия насекомых, используемая в качестве хозяина, может пригодно представлять собой клеточную линию Lepidoptera. такую как клетки Spodoptera frugiperda или клетки Trichoplusia ni (см. US 5077214). Условия культивирования могут пригодно быть такими, как описано, например, в WO 89/01029 или WO 89/01028, либо в любой из вышеупомянутых ссыпок.
Затем трансформированную или трансфецированную клетку-хозяина, описанную выше, культивируют в подходящей питательной среде в условиях, дающих возможность экспрессии белка по настоящему изобретению, после чего полученный в результате белок выделяют из культуры.
Среда, используемая для культивирования клеток, может представлять собой любую общепринятую среду, пригодную для выращивания клеток-хозяев, такую как минимальная или комплексная среда, содержащая подходящие добавки. Подходящая среда доступна от коммерческих поставщиков или может быть приготовлена в соответствии с опубликованными рецептами (например, в каталогах Американской Коллекции типовых культур). Белок, продуцируемый клетками, можно затем выделить из культуральной среды с помощью общепринятых методик, включая отделение клеток-хозяев от среды путем центрифугирования или фильтрования, осаждение белковых компонентов надосадочной жидкости или фильтрата с помощью соли, например, сульфата аммония, очистку с помощью ряда хроматографических методик, например ионообменной хроматографии, гель-фильтрационной хроматографии, аффинной хроматографии или тому подобного в зависимости от типа интересующего белка.
Пептиды по настоящему изобретению можно использовать, чтобы вызвать антитела, которые специфично связываются с пептидами по настоящему изобретению. В настоящем контексте "антитела" включают моноклональные и поликлональные антитела и их фрагменты, связывающие антиген, такие как фрагменты F(ab')2 и Fab, включая антитела, сконструированные генной инженерией, и гуманизированные антитела. Антитела называют специфичными, если они связываются с пептидом по настоящему изобретению с Ка, большей или равной 107 М-1. Способы получения антител раскрыты, например, в Hurrell J.G.R. (Ed.) Monoclonal Hybridoma Antibodies: Techniques and Applications, CRC Press, Boca Raton, Florida, 1982 и Sambrok, Molecular Cloning: A Laboratory Manual, Cold Spring Harbour, New York, 1989.
ИЛ-21 применен при лечении вирусных заболеваний, таких как вирус гепатита В, вирус гепатита С, вирус иммунодефицита человека, респираторно-синцитиальный вирус, вирус Эпштейна-Барра, вирус гриппа, цитомегаловирус, вирус герпеса и тяжелый острый респираторный синдром; аллергических заболеваний, таких как астма, аллергический ринит или аллергические заболевания кожи; паразитарных заболеваний, таких как инфекция гельминтами; аутоиммунных заболеваний, таких как отторжение аллотрансплантата и диабет; и рака.
В настоящем контексте "рак" относится к любому неопластическому расстройству, включая такие клеточные расстройства, как саркома, карцинома, меланома, лейкоз, лимфома, раки молочной железы, головы и шеи, яичников, мочевого пузыря, легкого, глотки, гортани, пищевода, желудка, тонкого кишечника, печени, поджелудочной железы, ободочной кишки, женских половых путей, мужских половых путей, простаты, почек и центральной нервной системы. В частности, "рак" предназначен для обозначения не метастатических и метастатических неопластических расстройств, таких как злокачественная меланома, раки кожи, не представляющие собой меланому, почечно-клеточный рак, рак головы и шеи, рак эндокринной системы, рак яичника, мелкоклеточный рак легкого, немелкоклеточный рак легкого, рак молочной железы, рак пищевода, верхний желудочно-кишечный рак, рак ободочной и прямой кишки, рак печени и желчных протоков, рак поджелудочной железы, рак простаты, рак мочевого пузыря, рак яичка, рак шейки матки, рак эндометрия, саркомы костей и мягких тканей, рак центральной нервной системы, лимфома, лейкоз и рак неизвестного первичного происхождения.
В более конкретных аспектах изобретения термины "неопластические расстройства", "рак" или "опухолевый рост" следует понимать как относящиеся ко всем формам неопластического клеточного роста, включая как кистозные, так и солидные опухоли, опухоли костей и мягких тканей, включая как доброкачественные, так и злокачественные опухоли, включая опухоли анальной ткани, желчного протока, мочевого пузыря, клеток крови, кости, кости (вторичные), кишки (ободочной и прямой), головного мозга, головного мозга (вторичные), молочной железы, молочной железы (вторичные), карциноид, опухоли шейки матки, раки у детей, опухоли глаза, зева и глотки (пищевода), головы и шеи, саркому Калоши, опухоли почек, гортани, лейкоз (острый лимфобластный), лейкоз (острый миелоидный), лейкоз (хронический лимфоцитарный), лейкоз (хронический миелоидный), лейкоз (другой), опухоли печени, печени (вторичные), легкого, легкого (вторичные), лимфатических узлов (вторичные), лимфому (Ходжкина), лимфому (не Ходжкина), меланому, мезотелиому, миелому, опухоли яичника, поджелудочной железы, пениса, простаты, кожи, саркомы мягких тканей, опухоли желудка, яичек, щитовидной железы, неизвестную первичную опухоль, опухоли влагалища, вульвы, матки (тела матки).
Опухоли мягких тканей включают злокачественную невриному с моносомией, десмоидную опухоль, липобластому, липому, лейомиому матки, саркому "прозрачных клеток", дерматофибросаркому, саркому Юинга, внескелетную хондромиксосаркому, липомиксосаркому, липосаркому, хорошо дифференцированную альвеолярную рабдомиосаркому и синовиальную саркому.
Специфичные опухоли костей включают неостеогенную фиброму кости, однополостную кисту кости, энхондрому, аневризмальную кисту кости, остеобластому, хондробластому, хондромиксофиброму, остеогенную фиброму кости и злокачественную адамантиному, гигантоклеточную опухоль, фиброзную дисплазию, саркому Юинга, эозинофильную гранулему, остеосаркому, хондрому, хондросаркому, злокачественную фиброзную гистиоцитому и метастатическую карциному.
Лейкозы относятся к ракам лейкоцитов, которые продуцируются костным мозгом. Они включают, но не ограничены ими, четыре основных типа лейкоза: острый лимфобластный (ОЛЛ), острый миелобластный (ОМЛ), хронический лимфобластный (ХЛЛ) и хронический миелоидный (ХМЛ).
В одном воплощении изобретение относится к способам лечения вирусных инфекций, аллергических заболеваний, аутоиммунных заболеваний и рака, как перечислено выше, при котором вводят эффективное количество пептида по настоящему изобретению пациенту, нуждающемуся в этом.
В одном воплощении настоящее изобретение относится к применению пептида по настоящему изобретению для изготовления лекарственного средства для лечения вирусных инфекций, аллергических заболеваний, аутоиммунных заболеваний и рака, как перечислено выше.
В данной области техники хорошо известно, что режимы лечения рака часто включают более чем одно лекарственное средство или метод лечения. В одном воплощении в настоящем изобретении, таким образом, предложен способ лечения рака, при котором вводят эффективное количество пептида по настоящему изобретению в комбинации с эффективными количествами одного или более чем одного из приведенного ниже I-VI. В настоящем изобретении 'в комбинации' означает, что пептид по изобретению вводят (i) до, (ii) одновременно и/или (iii) после лечения одним или более чем одним из приведенного ниже I-VI.
I. Агенты, которые индуцируют гибель опухолевых клеток или гибель инфицированных вирусом клеток
а) общепринятая химиотерапия
б) лучевая терапия
в) моноклональные антитела
г) контроль клеточного цикла/регуляторы апоптоза
д) модуляторы фактора роста и преобразования сигнала
е) ингибиторы васкуляризации опухоли (ингибиторы ангиогенеза, лекарственные средства против ангиогенеза)
ж) адресная доставка вируса (применение рекомбинантного вируса для разрушения опухолевых клеток)
з) противовирусные агенты
и) гормональные агенты
II. Агенты, которые усиливают иммунный ответ против опухолевых клеток или клеток, инфицированных вирусом
л) активаторы иммунной системы
м) ингибиторы иммунной системы (например, агенты, которые ингибируют иммунные сигналы, понижающие регуляцию иммунного ответа), включая противоанергические агенты
н) терапевтические вакцины
III. Агенты, которые препятствуют опухолевому росту, метастазам или распространению клеток, инфицированных вирусом
о) интегрины, модуляторы молекул клеточной адгезии
п) противометастатические агенты
р) модуляторы эндотелиальных клеток
IV. Внутренняя вакцинация
V. Антагонисты тканевого фактора и других факторов, влияющих на каскад коагуляции
с) ингибиторы против фактора Ха, против фактора IIа, антифибриногенные агенты
т) пентасахариды и т.д.
VI. Иммуносупрессивные/иммуномодуляторные агенты
у) агенты, влияющие на хоминг Т-лимфоцитов, например, FTY-720
ф) ингибиторы кальцинурина
х) ингибиторы TOR
Более подробное описание некоторых возможных комбинированных лекарственных средств приведено ниже.
I: Агенты, которые индуцируют гибель опухолевых клеток или гибель инфицированных вирусом клеток
а) Общепринятые химиотерапевтические агенты
В одном воплощении изобретения комбинированную терапию осуществляют путем введения пептида по настоящему изобретению и общепринятых химиотерапевтических агентов. Химиотерапевтические агенты обладают различными механизмами действия, такими как влияние либо
а) на уровне ДНК
б) на уровне РНК
Неограничивающими примерами общепринятых химиотерапевтических агентов на уровне ДНК или на уровне РНК являются антиметаболиты (такие как азатиоприн, цитарабин, флударабин фосфат, флударабин, гемцитабин, цитарабин, кладрибин, капцетабин, 6-меркаптопурин, 6-тиогуанин, метотрексат, 5-фторурацил и гидроксимочевина), алкилирующие агенты (такие как мелфалан, бусульфан, цисплатин, карбоплатин, циклофосфамид, ифосфамид, дакарбазин, прокарбазин, хлорамбуцил, тиотепа, ломустин, темозоламид), антимитотические агенты (такие как винорелбин, винкристин, винбластин, доцетаксел, паклитаксел), ингибиторы топоизомераз (такие как доксорубицин, амсакрин, иринотекан, даунорубицин, эпирубицин, митомицин, митоксантрон, идарубицин, тенипозид, этопозид, топотекан), антибиотики (такие как актиномицин и блеомицин), аспарагиназа, либо антрациклины или таксаны.
В одном воплощении изобретения комбинированную терапию проводят путем введения пептида по настоящему изобретению и дакарбазина (DTIC).
б) Лучевая терапия:
Некоторые опухоли можно лечить облучением или радиофармацевтическими агентами. Источник облучения может быть либо внешним, либо внутренним для пациента, подлежащего лечению. Когда источник является внешним для пациента, эта терапия известна как дистанционная лучевая терапия (EBRT, external beam radiation therapy). Когда источник излучения является внутренним для пациента, это лечение называют брахитерапией (ВТ). Типичные радиоактивные атомы, которые применяют, включают радий, цезий-137, индий-192, америций-241, золото-198, кобальт-57, медь-67, технеций-99, йод-123, йод-131 и индий-111.
Лучевая терапия является стандартной терапией для борьбы с не удаляемыми или неоперабельными опухолями и/или метастазами опухолей. Улучшенные результаты наблюдали при комбинировании лучевой терапии с другими терапиями.
В воплощении изобретения пептид по настоящему изобретению вводят в комбинации с лучевой терапией.
в) Моноклональные антитела (моноклоналы; МАb)
МАb разработаны для лечения как лейкоза и лимфомы, так и солидных опухолей, и данный принцип приобретает все возрастающий интерес. Эти антитела действуют либо путем ингибирования функций, которые являются жизненно важными для выживания опухолевых клеток, либо путем доставки токсического полезного груза, либо путем прерывания ключевых событий передачи сигнала, либо путем индукции антителозависимой клеточно-опосредованной цитотоксичности (ADCC) или комплементнаправленной цитотоксичности (CDC) против опухолевых клеток. Затем гибель опухолевых клеток может привести к высвобождению опухолевых антигенов, которые "вакцинируют" иммунную систему и стимулируют ее к продуцированию вторичного ответа, который, таким образом, направлен на опухолевую клетку (то есть 'внутренняя вакцинация', как описано ниже). Онкогены с гиперэкспрессией и опухолеспецифичные антигены являются ключевыми мишенями для многих mAb, находящихся в разработке.
Опухолевые антигены описаны, например, в Stauss H, Kawakami Y and Parmiani G: Tumor antigens recognized by Т cells and antibodies. Taylor and Frances (2003). Изобретение охватывает антитела, вызванные против этих мишеней. Изобретение также охватывает антитела, вызванные против вирусных антигенов.
В воплощении изобретения пептид по настоящему изобретению комбинируют с антителами, такими как ритуксимаб, алемтузумаб, трастузумаб, гемтузумаб, гемтузумаб-озогамицин (Myelotarg®, Wyeth), цетуксимаб (ErbituxTM), бевацизумаб, HuMax-CD20, HuMax-EGFr, замил и пертузумаб.
В воплощении изобретения пептид по настоящему изобретению комбинируют с ритуксимабом.
В воплощении изобретения пептид по настоящему изобретению комбинируют с цетуксимабом.
В воплощении изобретения пептид по настоящему изобретению комбинируют с бевацизумабом.
В воплощении изобретения пептид по настоящему изобретению комбинируют с бевацизумабом и цетуксимабом.
В воплощении изобретения пептид по настоящему изобретению комбинируют с панитумумабом.
В воплощении изобретения пептид по настоящему изобретению комбинируют с бевацизумабом и панитумумабом.
В воплощении изобретения пептид по настоящему изобретению комбинируют с антителом против тканевого фактора, Ig-подобных рецепторов киллеров (KIR), ламинина-5, EGF-R, VEGF-R, PDGF-R, HER-2/neu или с антителом против опухолевого антигена, такого как PSA, PSCA, СЕА, СА125, KSA и т.д.
В воплощении изобретения пептид по настоящему изобретению вводят вместе с терапевтическим антителом, таким как упомянуты выше, и дополнительно комбинируют с дополнительными ADCC-усиливающими соединениями, например, блокирующими антителами анти-KIR, агонистами NKG2D, антагонистами NKG2A, ИЛ-2, ИЛ-12, ИЛ-15, ИЛ-18 или ИЛ-21.
В другом воплощении изобретения пептид по настоящему изобретению вводят в виде комбинации с антителами против вирусных антигенов.
г) Контроль клеточного цикла/регуляторы апоптоза
Серия регуляторов вовлечена в поддержание нормального клеточного цикла. Соединения, которые направлены на регуляторы, такие как (i) cdc-25 (с NSC 663284 в качестве неограничивающего примера (Pu et al (2003) J Biol Chem 278, 46877)), (ii) циклинзависимые киназы, которые повышенно стимулируют клеточный цикл (со следующими неограничивающими примерами: флавопиридол (L868275, HMR1275; Aventis), 7-гидроксистауроспорин (UCN-01, KW-2401; Kyowa Hakko Кодуо) и росковитин (R-росковитин, CYC202; циклацел), обзор которых сделан Fischer & Gianella-Borradori (2003) Exp Op Invest Drugs 12, 955-970), и (iii) теломераза, фермент, который помогает раковым клеткам перестраивать их теломеры, находятся в пределах объема настоящего изобретения, такие как приведенные ниже
неограничивающие примеры BIBR1532 (Damm et al (2001) EMBO J 20, 6958-6968) и SOT-095 (Tauchi et al (2003) Oncogene 22, 5338-5347). Кроме того, лекарственные средства, которые взаимодействуют с биохимическими путями апоптоза, находятся в пределах объема настоящего изобретения, такие как приведенные ниже неограничивающие примеры: родственный TNF лиганд, индуцирующий апоптоз (TRAIL)/лиганд апоптоза-2 (Apo-2L), антитела, которые активируют рецепторы TRAIL, ИФН-α и антисмысловой Bcl-2 (см. Igney and Krammer (2002) Nature Rev. Cancer 2, 277-288; Makin and Dive (2003) Trends Mol Med 9, 2519; Smyth et al (2003) Immunity 18, 1-6; Panaretakis et al (2003) Oncogene 22, 4543-4556 и приведенные там ссылки). В одном воплощении изобретения пептид по настоящему изобретению комбинируют с одним или более чем одним регулятором клеточного цикла и/или агентом, индуцирующим апоптоз.
В приведенном выше воплощении изобретения соединения выбраны из группы, включающей cdc-25, NSC 663284, флавопиридол, 7-гидроксистауроспорин, росковитин, BIBR1532, SOT-095, родственный TNF лиганд, индуцирующий апоптоз (ТРАIL)/лиганд апоптоза-2 (Apo-2L), антитела, которые активируют рецепторы TRAIL, ИФН-α и антисмысловой Bcl-2.
д) Ингибиторы фактора роста
Ряд mAb против факторов роста и рецепторов факторов роста разработан для лечения рака. Таким образом, в качестве неограничивающего примера, члены семейства рецепторов эпидермальных факторов роста (EGF-R) аномально активированы во многих эпителиальных опухолях, которые часто коррелируют с более агрессивным клиническим течением. Антитела, направленные против внеклеточного домена этих рецепторов, связывающего лиганд, и молекулы низкой молекулярной массы, которые ингибируют их тирозинкиназные домены, находятся в поздней стадии клинической разработки или одобрены для лечения рака либо в качестве единственных агентов, либо в комбинации с другими противораковыми лекарственными средствами. Неограничивающими примерами являются герцептин (моноклональное антитело), цетуксимаб (моноклональное антитело), Tarceva (низкомолекулярный ингибитор) и Iressa (низкомолекулярный ингибитор). Кроме того, лиганд может быть нейтрализован перед связыванием с рецептором.
В одном воплощении изобретения пептид по настоящему изобретению комбинируют с ингибиторами факторов роста.
В воплощении изобретения ингибиторы факторов роста выбраны из группы, включающей герцептин (моноклональное антитело), цетуксимаб (моноклональное антитело), Tarceva (низкомолекулярный ингибитор) и Iressa (низкомолекулярный ингибитор).
В воплощении изобретения пептид по настоящему изобретению комбинируют с герцептином.
е) Ингибиторы васкуляризации опухоли (лекарственные средства против ангиогенеза и антиметастатические агенты)
Опухолевый рост является зависимым от достаточного кровоснабжения и, следовательно, от развития новых кровеносных сосудов. Этот общий признак солидных опухолей оказался привлекательным с терапевтической точки зрения, то есть ожидают сниженный опухолевый рост и регрессию опухоли при лечении пациентов с раком лекарственными средствами против ангиогенеза. В настоящее время более чем 60 лекарственных средств против ангиогенеза проходят клинические испытания, включая встречающийся в природе эндостатин и ангиостатин (обзор приведен в Marx (2003) Science 301, 452-454). Но также более старые химиотерапевтические лекарственные средства, другие лекарственные средства и лучевая терапия обладают антиангиогенными эффектами. В одном типе воплощений настоящего изобретения находится комбинированная терапия ИЛ-21, его аналогами или производными и одним или более чем одним антиангиогенным агентом, таким как приведенные ниже неограничивающие примеры: эндостатин, ангиостатин, антитела, которые блокируют факторы, которые инициируют ангиогенез (например, анти-VEGF авастатин), низкомолекулярные соединения, которые ингибируют ангиогенез посредством ингибирования ключевых элементов в релевантных биохимических путях преобразования сигнала.
Атака на сосудистую систему опухоли и внеклеточный матрикс привлекает возрастающее внимание. Таким образом, разработаны следующие принципы: блокада эндотелиальных клеток, введение ангиостатина и эндостатина, направленность на VEGF и внеклеточный матрикс.
В воплощении изобретения пептид по настоящему изобретению комбинируют с лекарственным средством против ангиогенеза.
В воплощении изобретения лекарственное средство против ангиогенеза выбрано из группы, включающей: авастатин, неовастат, талидомид, РТК787, ZK222584, ZD-6474, SU6668, PD547.632, VEGF-Trap, CEP-7055, NM-3, SU11248.
ж) Адресная доставка вируса
При адресной доставке вируса используют рекомбинантный вирус, обычно некомпетентный по репликации, для непосредственного разрушения опухоли. На практике по меньшей мере один раунд репликации имеет место, прежде чем вирус теряет эту способность. Следовательно, опухоль лизируется, что часто приводит к системной иммунизации, результатом которой является защита. Этот метод усовершенствован дополнительным использованием генетической модификации для усиления иммунного ответа. Например, генетическая инсерция гена человеческого GM-CSF в вирус простого герпеса типа 2 использована для улучшения эффективности вакцины. В одном воплощении изобретения комбинированную терапию проводят путем введения ИЛ-21, его аналога или производного и адресной доставки вируса.
и) Гормональные агенты
Гормональные агенты, прежде всего, известны при лечении гормонально зависимых раков, таких как рак яичника, рак молочной железы и рак простаты, такие как антиандрогенная и антиэстрогенная терапия. Гормоны и антигормоны представляют собой соединения, такие как эстрамустин фосфат, полиэстрадиол фосфат, эстрадиол, анастрозол, экземестан, летрозол, тамоксифен, мегестрол ацетат, медроксипрогестерон ацетат, октреотид, ципротерон ацетат, бикалтумид, флутамид, триторелин, лейпрорелин, бузерелин или гозерелин.
В воплощении изобретения пептид по настоящему изобретению комбинируют с гормональной терапией.
II: Агенты, которые усиливают иммунный ответ против опухолевых клеток или клеток, инфицированных вирусом
л) активаторы иммунной системы
Приведенный ниже перечень компонентов или агентов, которые можно применять вместе с пептидом по настоящему изобретению в комбинированной терапии рака и вирусных инфекций путем усиления эффективности иммунной системы, никоим образом не следует рассматривать как ограничивающий объем изобретения:
Адъюванты:
Иммунотерапия состоит в специфических и неспецифических методах лечения. Примерами неспецифической иммунотерапии являются адъюванты, действующие главным образом в качестве катализаторов для инициации иммунного ответа.
Неограничивающими примерами таких адъювантов вакцин являются QS21, GM-CSF и олигодезоксинуклеотиды CpG, липополисахарид и полиинозиновая: полицитидиловая кислота.
В одном воплощении изобретения пептид по настоящему изобретению комбинируют с одним или более чем одним адъювантом.
В воплощении изобретения адъюванты выбраны из группы, включающей:
QS21, GM-CSF и олигодезоксинуклеотиды CpG, липополисахарид и полиинозиновую: полицитидиловую кислоту, а-галактозилцерамид или его аналоги, гистамина дигидрохлорид или гидроксид алюминия.
Цитокины:
Неограничивающими примерами цитокинов являются ИФН-α, ИФН-β, ИФН-γ, ИЛ-2, РЕС-ИЛ-2, ИЛ-4, ИЛ-6, ИЛ-7, ИЛ-12, ИЛ-13, ИЛ-15, ИЛ-18, ИЛ-21, ИЛ-23, ИЛ-27, ИЛ-28а, ИЛ-28b, ИЛ-29, GM-CSF, лиганд Flt3 или фактор стволовых клеток.
В воплощении изобретения пептид по настоящему изобретению комбинируют с одним или более чем одним цитокином.
В воплощении изобретения ИЛ-21 комбинируют с одним или более чем одним из соединений, выбранных из группы, включающей: ИФН-α, ИФН-β, ИФН-γ, ИЛ-2, ПЭГ-ИЛ-2, ИЛ-4, ИЛ-6, ИЛ-7, ИЛ-12, ИЛ-13, ИЛ-15, ИЛ-18, ИЛ-21, ИЛ-23, ИЛ-27, ИЛ-28а, ИЛ-28b, ИЛ-29, GM-CSF, лиганд Flt3 или фактор стволовых клеток, либо аналог или производное любого из них.
В воплощении изобретения соединения выбраны из группы, включающей: ИФН-α, ИФН-β, ИФН-γ, ПЭГ-ИЛ-2, ИЛ-18, ИЛ-23, ИЛ-27, ИЛ-28а, ИЛ-28b, ИЛ-29.
В воплощении изобретения пептид по настоящему изобретению комбинируют с одним из следующего: ИЛ-2, ПЭГ-ИЛ-2, ИЛ-7, ИЛ-12, ИЛ-15, ИЛ-18 и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с ИЛ-12. В воплощении изобретения пептид по настоящему изобретению комбинируют с ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с ПЭГ-ИЛ-2.
В воплощении изобретения пептид по настоящему изобретению комбинируют с более чем одним из следующего: ИЛ-2, ПЭГ-ИЛ-2, ИЛ-7, ИЛ-12, ИЛ-15, ИЛ-18 и ИФН-α. В воплощении изобретения пептид по настоящему изобретению комбинируют по меньшей мере с одним из следующего: ИЛ-2, ПЭГ-ИЛ-2, ИЛ-7, ИЛ-12, ИЛ-15, ИЛ-18 и ИФН-α, и одним дополнительным активным компонентом. В воплощении изобретения пептид по настоящему изобретению комбинируют по меньшей мере с одним из следующего: ИЛ-2, РЕG-ИЛ-2, ИЛ-7, ИЛ-12, ИЛ-15, ИЛ-18 и ИФН-α, и одним дополнительным цитокином из приведенного выше перечня. В воплощении изобретения пептид по настоящему изобретению комбинируют с ИФН-α и GM-CSF. В воплощении изобретения пептид по настоящему изобретению комбинируют с ИФН-α и тимопентином.
В воплощении изобретения пептид по настоящему изобретению комбинируют с ИФН-γ.
В воплощении изобретения пептид по настоящему изобретению комбинируют с аутологичными TIL и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с ИФН-α и ИЛ-12.
В воплощении изобретения пептид по настоящему изобретению комбинируют с цисплатином и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с цисплатином, тамоксифеном и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с цисплатином, DTIC, тамоксифеном и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с цисплатином, DTIC, тамоксифеном и GM-CSF.
В воплощении изобретения пептид по настоящему изобретению комбинируют с цисплатином, кармустином, DTIC и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с цисплатином, кармустином, DTIC, тамоксифеном и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с цисплатином, кармустином, DTIC, карбоплатином, тамоксифеном и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с цисплатином, DTIC, винбластином, тамоксифеном и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с цисплатином, винбластином, темозоломидом и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с цисплатином, кармустином, DTIC, виндезином, тамоксифеном и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с цисплатином, тамоксифеном и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с цисплатином, винбластином, DTIC и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с DTIC и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с DTIC, GM-CSF и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с DTIC, тимозином-α и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с винбластином и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с 5-фторурацилом и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с фотемустином и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с оксалиплатином и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с оксалиплатином, тамоксифеном и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с оксалиплатином, DTIC, тамоксифеном и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с оксалиплатином, DTIC, тамоксифеном и GM-CSF.
В воплощении изобретения пептид по настоящему изобретению комбинируют с оксалиплатином, кармустином, DTIC и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с оксалиплатином, кармустином, DTIC, тамоксифеном и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с оксалиплатином, кармустином, DTIC, карбоплатином, тамоксифеном и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с оксалиплатином, DTIC, винбластином, тамоксифеном и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с оксалиплатином, винбластином, темозоломидом и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с оксалиплатином, кармустином, DTIC, виндезином, тамоксифеном и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с оксалиплатином, тамоксифеном и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с оксалиплатином, винбластином, DTIC и ИФН-α.
В воплощении изобретения пептид по настоящему изобретению комбинируют с 5-фторурацилом или его перорально активным аналогом.
В воплощении изобретения пептид по настоящему изобретению комбинируют с оксалиплатином и 5-фторурацилом или его перорально активным аналогом.
В воплощении изобретения пептид по настоящему изобретению комбинируют с оксалиплатином, лейковорином и 5-фторурацилом или его перорально активным аналогом.
В воплощении изобретения пептид по настоящему изобретению комбинируют с иринотеканом.
В воплощении изобретения пептид по настоящему изобретению комбинируют с иринотеканом и оксалиплатином.
В воплощении изобретения пептид по настоящему изобретению комбинируют с иринотеканом и цеткусимабом.
В воплощении изобретения пептид по настоящему изобретению комбинируют с иринотеканом и бевацизумабом.
В воплощении изобретения пептид по настоящему изобретению комбинируют с иринотеканом и цеткусимабом и бевацизумабом.
В воплощении изобретения пептид по настоящему изобретению комбинируют с DTIC и аутологичными ЛАК клетками (лимфокинактивированными клетками).
В воплощении изобретения пептид по настоящему изобретению комбинируют с гемцитабином и ИФН-α.
Любую из вышеуказанных комбинаций можно дополнительно комбинировать с ИЛ-2.
Клеточная иммунотерапия
Примеры клеточной иммунотерапии (или адоптивной иммунотерапии) включают обратную инфузию размноженных ex vivo инфильтрирующих опухоль Т клеток или генетически модифицированных Т клеток.
В одном воплощении изобретения комбинированная терапия представляет собой комбинирование введения пептида по настоящему изобретению и клеточной иммунотерапии.
Клеточная иммунотерапия может включать выделение клеток, которые могут стимулировать или вызывать противораковый ответ у пациентов, размножение их в больших количествах и обратного введения их тому же или другому пациенту. В одном аспекте эти клетки могут представлять собой CD4+ или CD8+ Т клетки, распознающие опухолевые специфичные антигены или опухолеассоциированные антигены. В другом аспекте эти клетки могут представлять собой В клетки, экспрессирующие антитела, специфичные к опухолевым специфичным антигенам или опухолеассоциированным антигенам. В другом аспекте эти клетки могут представлять собой NK клетки (естественные киллеры), которые способны уничтожать опухолевые клетки. В предпочтительном аспекте эти клетки могут представлять собой дендритные клетки (DC), которые культивируют ех vivo с фактором размножения DC (например, GM-CSF или Flt3-L), насыщают опухолевыми специфичными антигенами или опухолеассоциированными антигенами и обратно инфузируют пациенту, нуждающемуся в этом. В одном воплощении изобретения комбинированная терапия представляет собой комбинированное введение пептида по настоящему изобретению и клеточной иммунотерапии или адоптивной иммунотерапии.
В воплощении изобретения клеточная адоптивная терапия включает CD4+ или CD8+ Т-лимфоциты, распознающие опухолевые специфичные антигены или опухолеассоциированные антигены.
В воплощении изобретения клеточная адоптивная терапия включает В-лимфоциты, экспрессирующие антитела, специфичные к опухолевым специфичным антигенам или опухолеассоциированным антигенам.
В воплощении изобретения клеточная адоптивная терапия включает NK клетки, которые способны уничтожать опухолевые клетки.
В воплощении изобретения клеточная адоптивная терапия включает дендритные клетки (DC).
В воплощении вышеуказанного дендритные клетки культивируют in vivo с фактором размножения DC (например, GM-CSF или Flt3-L), насыщают опухолевыми специфичными антигенами или опухолеассоциированными антигенами и обратно вводят in vivo.
м) Агенты, которые блокируют ингибиторную передачу сигнала в иммунной системе
Иммунные ответы, включая противоопухолевый и противовирусный ответ, регулируются балансом передачи сигнала через стимуляторные и ингибиторные рецепторы в клетках иммунной системы. Сдвиг в направлении активной передачи сигнала через активаторные рецепторы может привести к более эффективным иммунным ответам, тогда как усиленная передача сигнала через ингибиторные рецепторы может привести к менее продуктивным ответам или даже может нарушить иммунитет. В целях усиления противоопухолевого или противовирусного ответа полезно терапевтическое блокирование передачи сигнала через ингибиторные рецепторы, чтобы сдвинуть баланс в направлении активации. Следовательно, агенты, которые блокируют ингибиторные рецепторы или биохимические пути ингибиторной передачи сигнала, являются предпочтительными агентами для комбинированной терапии в сочетании с пептидом по настоящему изобретению. Неограничивающими примерами таких агентов, которые блокируют ингибиторные рецепторы, являются mAb, специфичные к CTLA-4 (анти-СТLА-4), mAb, специфичные к KIR (анти-KIR), mAb, специфичные к LIR (анти-LIR), mAb, специфичные к CD94 (анти-CD94), или mAb, специфичные к NKG2A (анти-NKG2А).
Противоанергические агенты представляют собой низкомолекулярные соединения, белки, гликопротеины или антитела, которые могут нарушать толерантность к опухолевым и раковым антигенам.
Хотя присутствие лимфоцитов, инфильтрирующих опухоль (TIL), коррелирует с улучшенным клиническим результатом при ряде различных форм рака, существует явная необходимость в улучшении активности этих TIL вследствие анергии или толерантности к опухолевым антигенам. Анергическому состоянию можно в значительном числе случаев противодействовать с помощью моноклональных антител, которые предотвращают индуцированную CTLA-4 анергию или толерантность. На животных моделях и у людей, больных раком, показано, что блокада CTLA-4 улучшает эффективность противораковой терапии, позволяя предположить, что блокаду CTLA-4 можно использовать для нарушения толерантности к раковым и опухолевым антигенам. Неограничивающим примером моноклонального антитела, которое можно применять для индукции активности TIL, является MDX-010 (Phan et al. (2003) Proc. Natl. Acad. Sci. U.S.A. 100: 8372). В одном воплощении изобретения комбинированную терапию осуществляют путем введения пептида по настоящему изобретению и одного или более чем одного агента, который нарушает толерантность к раковым, опухолевым или вирусным антигенам. В воплощении изобретения пептид по настоящему изобретению комбинируют с MDX-010.
В воплощении изобретения пептид по настоящему изобретению комбинируют с антителами против CTLA-4.
В воплощении изобретения пептид по настоящему изобретению комбинируют с антителами против KIR.
В воплощении изобретения пептид по настоящему изобретению комбинируют с антителами против CD94.
В воплощении изобретения пептид по настоящему изобретению комбинируют с антителами против NKG2A.
В воплощении изобретения пептид по настоящему изобретению комбинируют с антителами против ингибиторного рецептора, экспрессируемого на NK клетке, Т-лимфоците или NKT клетке.
В воплощении изобретения пептид по настоящему изобретению комбинируют с антагонистом ингибиторного рецептора.
В воплощении изобретения пептид по настоящему изобретению комбинируют с антагонистом сигнального белка, вовлеченного в передачу ингибиторных сигналов.
н) Терапевтические вакцины
В развитие почти всех раков человека вовлечены генетические изменения, и эти изменения могут приводить к экспрессии измененных молекул в опухолевых клетках и гиперэкспрессии нормальных молекул, соответственно. В принципе эти изменения должны приводить к иммунному ответу у хозяина (иммунологический надзор). Очевидно, что эта теоретическая активация иммунной системы приводит к спонтанной регрессии опухоли только в очень редких исключительных случаях. Это может быть следствием, среди прочих факторов, отсутствия "сигналов опасности", явления, которое привлекло повышенный интерес.
Опухолевые специфичные антигены идентифицированы, и вакцинация такими антигенами может стимулировать иммунную систему на уничтожение опухоли. Опухолевые специфичные антигены (TSA, tumor specific antigens) представляют собой относительно небольшую группу антигенов, примером которых являются антигены рака яичка. Эти гены являются молчащими в нормальной ткани, но экспрессируются раковыми клетками. Они являются высокоспецифичными маркерами заболевания и включают MAGE (ген антигена меланомы), обнаруженные в меланоме.
Опухолеассоциированные антигены (ТАА, tumor-associated antigens) обычно представляют собой антигены дифференциации, экспрессируемые нормальными клетками, но обладающие массовой гиперэкспрессией в раковой ткани. Маркеры, которые первоначально считали специфичными для конкретного рака, в действительности являются достаточно распространенными во многих опухолях, такие как ганглиозиды и муциновые антигены. Классические антигены дифференциации включают MART-1 (антиген меланомы, распознаваемый Т-лимфоцитами) и gp100, и тот, и другой от меланомы, тирозиназу, карциноэмбриональный антиген (СЕА) и gp75.
Мутационные антигены: Точечные мутации являются распространенными при многих раках и часто встречаются в подобной локализации, такой как распространенная мутация Р53 или онкогены ras. Сообщали об индукции in vitro ответов цитотоксических Т-лимфоцитов (CTL) человека против пептидов мутантного р53 и р53 дикого типа. В мышиной модели мутантные дендритные клетки, подвергнутые ударной дозе р53, были способны индуцировать CTL, специфичные к р53, и ингибировать рост установленных опухолей.
Вирусные антигены: Некоторые вирусы являются онкогенными, и продукты генов, кодируемые этими вирусами, могут вызывать иммунные ответы и, таким образом, служить в качестве раковых антигенов. Примером являются белки Е6 и Е7 от вируса папилломы человека типа 16, которые, как показано, индуцируют ответы цитотоксических Т-лимфоцитов in vitro.
Опухолевые специфичные антигены, опухолеассоциированные антигены и/или мутационные антигены и вирусные антигены можно использовать либо в виде пептидов, либо рекомбинантных очищенных антигенов одного агента, либо комбинаций рекомбинантных очищенных антигенов и/или очищенных пулов антигенов, выделенных из раковых клеток или опухолевых клеток, в качестве вакцины, которая вызывает противоопухолевый иммунный ответ. Подобным образом, пептиды, рекомбинантные очищенные антигены одного агента, комбинации рекомбинантных очищенных антигенов и/или очищенные пулы антигенов, выделенные из клеток, инфицированных вирусом, можно использовать в вакцине, которая вызывает ответ против клеток, инфицированных вирусом. Терапевтические вакцины могут также находиться в форме лизатов или экстрактов аутологичных опухолевых клеток, либо лизатов или экстрактов аллогенных опухолевых клеточных линий. Терапевтические вакцины могут также находиться в форме ДНК вакцины, которая вызывает иммунный ответ против раковых и инфицированных вирусом клеток. Указанная ДНК вакцина может состоять из зкспрессионного вектора, кодирующего один антиген или кодирующего антиген вместе с цитокином (например, GM-CSF, ИЛ-2, ИЛ-12 или ИЛ-21), который может усилить иммунный ответ против раковых и инфицированных вирусом клеток. Указанная ДНК вакцина может также состоять из модифицированного вируса (например, вируса птичьей оспы (fowlpox), вируса коровьей оспы или аденовируса), который содержит последовательность ДНК, кодирующую один антиген или кодирующую антиген вместе с цитокином. Терапевтические вакцины могут также находиться в форме антител против идиотипа, которые вызывают иммунный ответ против раковых и инфицированных вирусом клеток. Терапевтические вакцины могут также находиться в форме аутологичных дендритных клеток, насыщенных указанными антигенами или пептидами, образованными из них, вместе с агентом, модифицирующим DC, таким как цитокины, агонисты toll-подобного рецептора (TLR), олигодезоксинуклеотиды CpG, GM-CSF или белки теплового шока.
Указанный опосредованный вакциной вызов противоопухолевого ответа или ответа против клеток, инфицированных вирусом, можно усилить путем введения адъювантов, цитокинов, агонистов toll-подобного рецептора (TLR), олигодезоксинуклеотидов CpG, дендритных клеток, GM-CSF или белков теплового шока. В одном воплощении изобретения комбинированную терапию осуществляют путем введения пептида по настоящему изобретению с одной или более чем одной терапевтической вакциной с адъювантами, цитокинами, агонистами toll-подобного рецептора (TLR), олигодезоксинуклеотидами CpG, дендритными клетками, GM-CSF или белками теплового шока, либо без них.
п) Противометастатические агенты
Метастатические раковые клетки проникают во внеклеточный матрикс (ВКМ) и базальную мембрану кровеносных сосудов с метастазированием органа-мишени (эктопический сайт). ВКМ состоит из белков, заключенных в углеводный комплекс (гепарансульфатпептидогликаны), и протеазы, окружающие опухоль, являются активными при разрушении, таким образом, ткани хозяина. Противометастатические агенты антагонизируют эффект таких протеаз (например, ингибиторы металлопротеиназы) (Coussens et al. Science 2002; 295: 2387-2392). В воплощении настоящего изобретения находится комбинированная терапия пептидом по настоящему изобретению и одним или более чем одним противометастатическим агентом, таким как ингибиторы металлопротеиназы.
IV: Внутренняя вакцинация
"Внутренняя вакцинация" и "терапия внутренней вакцинацией" относится к индуцированной лекарственным средством или облучением клеточной гибели опухолевых клеток, которая приводит к вызову иммунного ответа, направленного на (i) указанные опухолевые клетки в целом или (ii) части указанных опухолевых клеток, включая (а) секретируемые белки, гликопротеины или другие продукты, (б) мембраносвязанные белки или гликопротеины, либо другие компоненты, связанные с мембранами или встроенные в них, и (в) внутриклеточные белки или другие внутриклеточные компоненты. Этот иммунный ответ может быть гуморальным (то есть антитело-комплемент-опосредованным) или клеточно-опосредованным, включая, но не ограничиваясь, развитие цитотоксических Т-лимфоцитов, которые распознают указанные опухолевые клетки или их части. Внутренняя вакцинация имеет много сходств с другими методиками вакцинации и включает многие или все из клеточных компонентов гемопоэтической и иммунной системы с тем преимуществом, что иммуногены или антигенные компоненты являются эндогенными и, таким образом, репрезентативными для антигенного спектра указанных опухолевых клеток. Внутреннюю вакцинацию можно, таким образом, считать персонализированной вакцинацией, которая вызвана применением общих методик лечения рака, приводящих к гибели опухолевых клеток. В дополнение к радиотерапии неограничивающими примерами лекарственных средств и агентов, которые можно применять для индукции указанной гибели опухолевых клеток и внутренней вакцинации, являются общепринятые химиотерапевтические агенты, ингибиторы клеточного цикла, лекарственные средства против ангиогенеза, моноклональные антитела, агенты, индуцирующие апоптоз, и ингибиторы преобразования сигнала.
"Комбинированная терапия пептидом по настоящему изобретению и внутренней вакцинации" относится к комбинированной терапии, где пептид по настоящему изобретению вводят пациентам с раком, которых лечат внутренней вакцинацией. Пептид по настоящему изобретению можно вводить до, одновременно или после проведения внутренней вакцинации.
В воплощении изобретения пептид по настоящему изобретению включают в терапию внутренней вакцинацией.
Генотерапия включает перенос генетического материала в клетку с временным или постоянным изменением клеточного фенотипа. Различные способы исследуют для доставки цитокинов, опухолевых антигенов и дополнительных стимуляторных молекул. В контексте данного изобретения пептид по настоящему изобретению может либо представлять собой агент доставки, либо его вводят совместно. В воплощении данного изобретения пептид по настоящему изобретению можно вводить в виде полинуклеотида. Полинуклеотид описан в WO 00/53761.
VI: Иммуносупрессивные/иммуномодуляторные агенты
у) агенты, влияющие на хоминг Т-лимфоцитов, например, FTY-720
ф) Ингибиторы кальцинурина
Ингибиторы кальцинурина, такие как валсподар, PSC 833, активны при предупреждении развития устойчивости к цитотоксическим агентам благодаря ингибиторным эффектам на MDR-1 и р-гликопротеин.
х) TOR-ингибиторы
TOR-ингибиторы действуют посредством блокирования серин-треонинкиназы млекопитающих TOR (mTOR). Соединения, такие как сиролимус, эверолимус и рапмицин, являются антипролиферативными агентами. Они вовлечены в каскады передачи сигнала далее и, следовательно, являются релевантными при лечении всех типов опухолей (например, антиангиогенных свойств).
В одном воплощении вышеупомянутые методы лечения рака комбинируют с SEQ ID No:2 таким же путем, как приведено для пептида по настоящему изобретению. В одном воплощении в настоящем изобретении предложены фармацевтические композиции, как обсуждено ниже, содержащие пептид с SEQ ID No:2 и один или более чем один из методов лечения рака, как описано выше.
ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ
Другой целью настоящего изобретения является разработка фармацевтического препарата, содержащего пептид по настоящему изобретению, который присутствует в концентрации от 10-15 мг/мл до 200 мг/мл, как, например, 10-10 мг/мл - 5 мг/мл, и где указанный препарат имеет рН от 2,0 до 10,0. Возможно, указанный препарат может содержать один или более чем один дополнительный противораковый агент, как описано выше. Этот препарат может дополнительно содержать буферную систему, консервант(ы), тонический агент(ы), хелатирующий агент(ы), стабилизаторы и сурфактанты. В одном воплощении изобретения фармацевтический препарат представляет собой водный препарат, то есть препарат, содержащий воду. Такой препарат типично представляет собой раствор или суспензию. В следующем воплощении изобретения фармацевтический препарат представляет собой водный раствор. Термин "водный препарат" определен как препарат, содержащий по меньшей мере 50% масс/масс воды. Подобным образом, термин "водный раствор" определен как раствор, содержащий по меньшей мере 50% масс/масс воды, а термин "водная суспензия" определен как суспензия, содержащая по меньшей мере 50% масс/масс воды.
В другом воплощении фармацевтический препарат представляет собой лиофилизированный препарат, к которому врач или пациент добавляет растворители и/или разбавители перед применением.
В другом воплощении фармацевтический препарат представляет собой высушенный препарат (например, высушенный лиофилизацией или распылительной сушкой), готовый к применению без какого-либо предварительного растворения.
В следующем аспекте изобретение относится к фармацевтическому препарату, содержащему водный раствор пептида по настоящему изобретению и буфер, где указанный белок OGP присутствует в концентрации от 0,1-100 мг/мл, и где указанный препарат имеет рН от примерно 2,0 до примерно 10,0.
В другом воплощении изобретения рН препарата выбран из перечня, состоящего из 2,0, 2,1, 2,2, 2,3, 2,4, 2,5, 2,6, 2,7, 2,8, 2,9, 3,0, 3,1, 3,2, 3,3, 3,4, 3,5, 3,6, 3,7, 3,8, 3,9, 4,0, 4,1, 4,2, 4,3, 4,4, 4,5, 4,6, 4,7, 4,8, 4,9, 5,0, 5,1, 5,2, 5,3, 5,4, 5,5, 5,6, 5,7, 5,8, 5,9, 6,0, 6,1, 6,2, 6,3, 6,4, 6,5, 6,6, 6,7, 6,8, 6,9, 7,0, 7,1, 7,2, 7,3, 7,4, 7,5, 7,6, 7,7, 7,8, 7,9, 8,0, 8,1, 8,2, 8,3, 8,4, 8,5, 8,6, 8,7, 8,8, 8,9, 9,0, 9,1, 9,2, 9,3, 9,4, 9,5, 9,6, 9,7, 9,8, 9,9 и 10,0.
В следующем воплощении изобретения буфер выбран из группы, состоящей из ацетата натрия, карбоната натрия, цитрата, глицилглицина, гистидина, глицина, лизина, аргинина, дигидрофосфата натрия, динатрия гидрофосфата, фосфата натрия и трис(гидроксиметил)аминометана, бицина, трицина, яблочной кислоты, сукцината, малеиновой кислоты, фумаровой кислоты, винной кислоты, аспарагиновой кислоты или их смесей. Каждый из этих конкретных буферов составляет альтернативное воплощение изобретения.
В следующем воплощении изобретения препарат дополнительно содержит фармацевтически приемлемый консервант. В следующем воплощении изобретения консервант выбран из группы, состоящей из фенола, орто-крезола, мета-крезола, лара-крезола, метил-пара-гидроксибензоата, пропил-пара-гидроксибензоата, 2-феноксиэтанола, бутил-пара-гидроксибензоата, 2-фенилэтанола, бензилового спирта, хлорбутанола и тиомеросала, бронопола, бензойной кислоты, имидмочевины, хлоргексидина, дегидроацетата натрия, хлоркрезола, этил-пара-гидроксибензоата, бензетония хлорида, хлорфенезина (3-пара-хлорфеноксипропан-1,2-диола) или их смесей. В следующем воплощении изобретения консервант присутствует в концентрации от 0,1 мг/мл до 20 мг/мл. В следующем воплощении изобретения консервант присутствует в концентрации от 0,1 мг/мл до 5 мг/мл. В следующем воплощении изобретения консервант присутствует в концентрации от 5 мг/мл до 10 мг/мл. В следующем воплощении изобретения консервант присутствует в концентрации от 10 мг/мл до 20 мг/мл. Каждый из этих конкретных консервантов составляет альтернативное воплощение изобретения. Применение консерванта в фармацевтических композициях хорошо известно специалистам в данной области техники. Для удобства сделана ссылка на Remington: The Science and Practice of Pharmacy, 20th edition, 2000.
В следующем воплощении изобретения препарат дополнительно содержит изотонический агент. В следующем воплощении изобретения изотонический агент выбран из группы, состоящей из соли (например, хлорида натрия), сахара или сахарного спирта, аминокислоты (например, L-глицина, L-гистидина, аргинина, лизина, изолейцина, аспарагиновой кислоты, триптофана, треонина), альдита (например, глицерола (глицерина), 1,2-пропандиола (пропиленгликоля), 1,3-пропандиола, 1,3-бутандиола), полиэтиленгликоля (например, ПЭГ400) или их смесей. Можно использовать любой сахар, такой как моно-, ди- или полисахариды, либо водорастворимые глюканы, включая, например, фруктозу, глюкозу, маннозу, сорбозу, ксилозу, мальтозу, лактозу, сахарозу, трегалозу, декстран, пуллулан, декстрин, циклодекстрин, растворимый крахмал, гидроксиэтилкрахмал и карбоксиметилцеллюлозу-Na. В одном воплощении сахарная добавка представляет собой сахарозу. Сахарный спирт определен как С4-С8 углеводород, имеющий по меньшей мере одну группу -ОН, и включает, например, маннит, сорбит, инозит, галактит, дульцит, ксилит и арабит. В одном воплощении добавка сахарного спирта представляет собой маннит. Сахара или сахарные спирты, упомянутые выше, можно использовать индивидуально или в комбинации. Не существует фиксированного предела используемого количества до тех пор, пока сахар или сахарный спирт растворим в жидком препарате, и не оказывает вредного воздействия на стабилизирующие эффекты, достигнутые с использованием способов по изобретению. В одном воплощении концентрация сахара или сахарного спирта составляет между примерно 1 мг/мл и примерно 150 мг/мл. В следующем воплощении изобретения изотонический агент присутствует в концентрации от 1 мг/мл до 50 мг/мл. В следующем воплощении изобретения изотонический агент присутствует в концентрации от 1 мг/мл до 7 мг/мл. В следующем воплощении изобретения изотонический агент присутствует в концентрации от 8 мг/мл до 24 мг/мл. В следующем воплощении изобретения изотонический агент присутствует в концентрации от 25 мг/мл до 50 мг/мл. Каждый из этих конкретных изотонических агентов составляет альтернативное воплощение изобретения. Применение изотонического агента в фармацевтических композициях хорошо известно специалистам в данной области техники. Для удобства сделана ссылка на Remington: The Science and Practice of Pharmacy, 20th edition, 2000.
В следующем воплощении изобретения препарат дополнительно содержит хелатирующий агент. В следующем воплощении изобретения хелатирующий агент выбран из солей этилендиаминтетрауксусной кислоты (ЭДТА), лимонной кислоты и аспарагиновой кислоты, а также их смесей. В следующем воплощении изобретения хелатирующий агент присутствует в концентрации от 0,1 мг/мл до 5 мг/мл. В следующем воплощении изобретения хелатирующий агент присутствует в концентрации от 0,1 мг/мл до 2 мг/мл. В следующем воплощении изобретения хелатирующий агент присутствует в концентрации от 2 мг/мл до 5 мг/мл. Каждый из этих конкретных хелатирующих агентов составляет альтернативное воплощение изобретения. Применение хелатирующего агента в фармацевтических композициях хорошо известно специалистам в данной области техники. Для удобства сделана ссылка на Remington: The Science and Practice of Pharmacy, 20th edition, 2000.
В следующем воплощении изобретения препарат дополнительно содержит стабилизатор. Применение стабилизатора в фармацевтических композициях хорошо известно специалистам в данной области техники. Для удобства сделана ссылка на Remington: The Science and Practice of Pharmacy, 20th edition, 2000.
Более конкретно композиции по изобретению представляют собой стабилизированные жидкие фармацевтические композиции, терапевтически активные компоненты которых включают полипептид, который, возможно, проявляет образование агрегатов в процессе хранения в жидких фармацевтических препаратах. Под "образованием агрегатов" подразумевают физическое взаимодействие между молекулами полипептида, которое приводит в результате к образованию олигомеров, которые могут оставаться растворимыми, или больших видимых агрегатов, которые осаждаются из раствора. Под "процессом хранения" подразумевают, что жидкую фармацевтическую композицию или препарат сразу после приготовления не сразу вводят субъекту. Вероятнее, после приготовления ее упаковывают для хранения либо в жидкой форме, либо в замороженном состоянии, либо в высушенной форме для последующего восстановления в жидкой форме или иной форме, пригодной для введения субъекту. Под "высушенной формой" подразумевают, что жидкую фармацевтическую композицию или препарат сушат либо путем сушки вымораживанием (то есть лиофилизации; см., например, Williams and Polli (1984) J. Parenteral Sci. Technol. 38:48-59), либо путем распылительной сушки (см. Masters (1991) в Spray-Drying Handbook (5th ed; Longman Scientific and Technical, Essez, U.K.), pp.491-676; Broadhead et al. (1992) Drug Devel. Ind. Pharm. 18:1169-1206; и Mumenthaler et al. (1994) Pharm. Res. 11: 12-20), либо путем сушки на воздухе (Carpenter and Crowe (1988) Cryobiology 25:459-470; и Roser (1991) Biopharm. 4:47-53). Образование агрегатов полипептидом в процессе хранения жидкой фармацевтической композиции может оказывать вредное воздействие на биологическую активность этого полипептида, результатом чего является потеря терапевтической эффективности фармацевтической композиции. Кроме того, образование агрегатов может вызвать другие проблемы, такие как закупорка трубок, мембран или насосов при введении фармацевтической композиции, содержащей полипептид, с использованием инфузионной системы.
Фармацевтические композиции по изобретению могут дополнительно содержать количество аминокислотного основания, достаточное для уменьшения образования агрегатов полипептидом в процессе хранения композиции. Под "аминокислотным основанием" подразумевают аминокислоту или комбинацию аминокислот, где любая данная аминокислота присутствует либо в форме ее свободного основания, либо в форме ее соли. Где используют комбинацию аминокислот, все эти аминокислоты могут присутствовать в формах их свободных оснований, все могут присутствовать в формах их солей или некоторые могут присутствовать в формах их свободных оснований, тогда как другие присутствуют в формах их солей. В одном воплощении аминокислоты для использования при изготовлении композиций по изобретению представляют собой те, которые несут заряженную боковую цепь, такие как аргинин, лизин, аспарагиновая кислота и глутаминовая кислота. Любой стереоизомер (то есть L, D или их смеси) конкретной аминокислоты (например, глицина, метионина, гистидина, имидазола, аргинина, лизина, изолейцина, аспарагиновой кислоты, триптофана, треонина и их смесей) или комбинации этих стереоизомеров могут присутствовать в фармацевтических композициях по изобретению настолько, насколько конкретная аминокислота присутствует либо в форме ее свободного основания, либо в форме ее соли. В одном воплощении используют L-стереоизомер. Препараты композиций по изобретению можно также готовить с аналогами этих аминокислот. Под "аналогом аминокислоты" подразумевают производное встречающейся в природе аминокислоты, которое вызывает желаемый эффект уменьшения образования агрегатов полипептидом в процессе хранения жидких фармацевтических композиций по изобретению. Пригодные аналоги аргинина включают, например, аминогуанидин, орнитин и N-моноэтил-L-аргинин, пригодные аналоги метионина включают этионин и бутионин, и пригодные аналоги цистеина включают 3-метил-L-цистеин. Как и другие аминокислоты, аналоги аминокислот включают в композиции либо в форме их свободного основания, либо в форме их соли. В следующем воплощении изобретения аминокислоты или аналоги аминокислот используют в концентрации, которая достаточна для предотвращения или замедления агрегации белка.
В следующем воплощении изобретения метионин (или другие серосодержащие аминокислоты или аналоги аминокислот) можно добавлять для ингибирования окисления остатков метионина до метионинсульфоксида, когда полипептид, действующий в качестве терапевтического агента, представляет собой полипептид, содержащий по меньшей мере один остаток метионина, склонный к такому окислению. Под "ингибированием" подразумевают минимальную аккумуляцию окисленных молекул метионина с течением времени. Ингибирование окисления метионина приводит в результате к большему сохранению полипептида в его правильной молекулярной форме. Можно использовать любой стереоизомер метионина (L, D или их смеси) или их комбинации. Количество, которое следует добавлять, должно составлять количество, достаточное для ингибирования окисления остатков метионина, так чтобы количество метионинсульфоксида было приемлемым для контрольных органов. Типично это означает, что композиция содержит не более чем от примерно 10% до примерно 30% метионинсульфоксида. Как правило, это может быть достигнуто путем добавления метионина, так чтобы отношение добавленного метионина к остаткам метионина находилось в интервале от примерно 1:1 до примерно 1000:1, как, например, от 10:1 до примерно 100:1.
В следующем воплощении изобретения препарат дополнительно содержит стабилизатор, выбранный из группы высокомолекулярных полимеров или низкомолекулярных соединений. В следующем воплощении изобретения стабилизатор выбран из полиэтиленгликоля (например, ПЭГ 3350), поливинилового спирта (ПВС), поливинилпирролидона, карбокси-/гидроксицеллюлозы или ее производных (например, НРС, HPC-SL, HPC-L и НРМС), циклодекстринов, серосодержащих веществ, таких как монотиоглицерин, тиогликолевая кислота и 2-метилтиоэтанол, и различных солей (например, хлорида натрия). Каждый из этих конкретных стабилизаторов составляет альтернативное воплощение изобретения.
Фармацевтические композиции могут также содержать дополнительные стабилизирующие агенты, которые дополнительно усиливают стабильность находящегося в них терапевтически активного полипептида. Стабилизирующие агенты, представляющие особый интерес для настоящего изобретения, включают, но не ограничены ими, метионин и ЭДТА, которые защищают полипептид от окисления метионина, и неионный сурфактант, который защищает полипептид от агрегации, обусловленной замораживанием-оттаиванием или механическим сдвигом.
В следующем воплощении изобретения препарат дополнительно содержит сурфактант. В следующем воплощении изобретения сурфактант выбран из детергента; этоксилированного касторового масла; полигликозилированных глицеридов; ацетилированных моноглицеридов; сорбитановых эфиров жирных кислот; блоксополимеров полиоксипропилена-полиоксиэтилена (например, полоксамеров, таких как Pluronic® F68, полоксамер 188 и 407, Тритон Х-100); полиоксиэтиленсорбитановых эфиров жирных кислот; производных полиоксиэтилена и полиэтилена, таких как алкилированные и алкоксилированные производные (твины, например Твин-20, Твин-40, Твин-80 и Brij-35); моноглицеридов или их этоксилированных производных; диглицеридов или их полиоксиэтиленовых производных, спиртов, глицерина, пектинов и фосфолипидов (например, фосфатидилсерина, фосфатидилхолина, фосфатидилэтаноламина, фосфатидилинозита, дифосфатидилглицерина и сфингомиелина); производных фосфолипидов (например, дипальмитоилфосфатидной кислоты) и лизофосфолипидов (например, пальмитоиллизофосфатидил-L-серина и 1-ацил-sn-глицеро-3-фосфатных эфиров этаноламина, холина, серина или треонина) и алкил-, алкоксил(алкилэфир)-, алкокси(алкилэфир)-производных лизофосфатидил- и фосфатидилхолинов, например лауроил- и миристоил-производных лизофосфатидилхолина, дипальмитоилфосфатидилхолина и модификаций полярной головной группы, то есть холинов, этаноламинов, фосфатидной кислоты, серинов, треонинов, глицерина, инозита и положительно заряженных DODAC, DOTMA, DCP, BISHOP, лизофосфатидилсерина и лизофосфатидилтреонина, и глицерофосфолипидов (например, цефалинов), глицерогликолипидов (например, галактопиранозида), сфингогликолипидов (например, церамидов, ганглиозидов), додецилфосфохолина, лизолецитина куриного яйца; производных фусидовой кислоты (например, тауродигидрофусидата натрия и т.д.); длинноцепочечных жирных кислот и их солей С6-С12 (например, олеиновой кислоты и каприловой кислоты); ацилкарнитинов и их производных; Nα-ацилированных производных лизина, аргинина или гистидина, либо ацилированных по боковой цепи производных лизина или аргинина; Nα-ацилированных производных дипептидов, содержащих любую комбинацию лизина, аргинина или гистидина и нейтральной или кислой аминокислоты; Nα-ацилированного производного трипептида, содержащего любую комбинацию нейтральной аминокислоты и двух заряженных аминокислот; DSS (докузата натрия, номер по каталогу CAS [577-11-7], докузата кальция, номер по каталогу CAS [128-49-4], докузата калия, номер по каталогу CAS [7491-09-0]); ДСН (додецилсульфата натрия или лаурилсульфата натрия); каприлата натрия; холевой кислоты или ее производных; желчных кислот и их солей и глициновых или тауриновых конъюгатов; урсодезоксихолевой кислоты; холата натрия; дезоксихолата натрия; таурохолата натрия; гликохолата натрия; N-гексадецил-N,N-диметил-3-аммонио-1-пропансульфоната; анионных (алкиларилсульфонатов) моновалентных сурфактантов, цвиттерионных сурфактантов (например, N-алкил-N,N-диметиламмонио-1-пропансульфонатов, 3-холамидо-1-пропилдиметиламмонио-1-пропансульфоната), катионных сурфактантов (четвертичных аммонийных оснований) (например, цетилтриметиламмония бромида, цетилпиридиния хлорида), неионных сурфактантов (например, додецил-β-D-глюкопиранозида), полоксаминов (например, Tetronic), которые представляют собой тетрафункциональные блоксополимеры, образованные в результате последовательного присоединения пропиленоксида и этиленоксида к этилендиамину; либо сурфактант может быть выбран из группы производных имидазолина, либо их смесей. Каждый из этих конкретных сурфактантов составляет альтернативное воплощение изобретения.
Применение сурфактанта в фармацевтических композициях хорошо известно специалистам в данной области техники. Для удобства сделана ссылка на Remington: The Science and Practice of Pharmacy, 20th edition, 2000.
Возможно, другие ингредиенты могут присутствовать в пептидном фармацевтическом препарате по настоящему изобретению. Такие дополнительные ингредиенты могут включать увлажняющие агенты, эмульгаторы, антиоксиданты, наполнители, тонические модификаторы, хелатирующие агенты, ионы металлов, масляные носители, белки (например, человеческий сывороточный альбумин, желатин или белки) и цвиттерион (например, аминокислоту, такую как бетаин, таурин, аргинин, глицин, лизин и гистидин). Такие дополнительные ингредиенты, конечно, не должны оказывать вредного воздействия на общую стабильность фармацевтического препарата по настоящему изобретению.
Фармацевтические композиции, содержащие пептид по настоящему изобретению, можно вводить пациенту, нуждающемуся в таком лечении, в нескольких сайтах, например в местных сайтах, например в кожу и сайты слизистой оболочки, в сайты, обходящие всасывание, например введение в артерию, в вену, в сердце, и в сайты, которые вовлечены во всасывание, например введение в кожу, под кожу, в мышцу или в брюшину.
Введение фармацевтических композиций по изобретению пациентам, нуждающимся в таком лечении, можно осуществлять посредством нескольких путей введения, например язычного, подъязычного, трансбуккального, введения в рот, перорального, введения в желудок и кишечник, назального, легочного, например, через бронхиолы и альвеолы или их сочетание, эпидермального, кожного, чрескожного, вагинального, ректального, глазного, например, через конъюнктиву, уретрального и парентерального.
Композиции по настоящему изобретению можно вводить в нескольких лекарственных формах, например, в виде растворов, суспензий, эмульсий, микроэмульсий, множественной эмульсии, пенок, мазей, паст, пластырей, твердых мазей, таблеток, таблеток с покрытием, полосканий, капсул, например твердых желатиновых капсул и мягких желатиновых капсул, суппозиториев, ректальных капсул, капель, гелей, распыляемых растворов, порошка, аэрозолей, ингаляционных средств, глазных капель, глазных мазей, глазных полосканий, вагинальных пессариев, вагинальных колец, вагинальных мазей, инъекционного раствора, растворов, преобразующихся in situ, например образующих гель in situ, отвердевающих in situ, осаждающихся in situ, кристаллизующихся in situ, инфузионного раствора и имплантатов.
Композиции по изобретению можно дополнительно компаундировать или соединять, например, посредством ковалентных, гидрофобных и электростатических взаимодействий, с носителем лекарственного средства, с системой доставки лекарственного средства и усовершенствованной системой доставки лекарственного средства в целях дополнительного усиления стабильности пептида по настоящему изобретению, повышения биодоступности, повышения растворимости, уменьшения вредных эффектов, достижения хронотерапии, хорошо известной специалистам в данной области техники, и улучшения соблюдения пациентом режима и схемы лечения, либо любого их сочетания. Примеры носителей, систем доставки лекарственных средств и усовершенствованных систем доставки лекарственных средств включают, но не ограничены ими, полимеры, например целлюлозу и ее производные, полисахариды, например декстран и его производные, крахмал и его производные, поливиниловый спирт, полимеры акрилата и метакрилата, полимеры молочной и гликолевой кислоты и их блоксополимеры, полиэтиленгликоли, белки-носители, например альбумин, гели, например системы термогелей, например блоксополимерные системы, хорошо известные специалистам в данной области техники, мицеллы, липосомы, микросферы, наночастицы, липидные кристаллы и их дисперсии, L2 фазу и ее дисперсии, хорошо известные специалистам в области фазового поведения в системах липид-вода, полимерные мицеллы, множественные эмульсии, самоэмульгирующие, самомикроэмульгирующие циклодекстрины и их производные, а также дендримеры.
Композиции по настоящему изобретению применимы в препарате в виде твердых веществ, полутвердых веществ, порошка и растворов для легочного введения пептида по настоящему изобретению, используя, например, ингалятор с дозатором, ингалятор сухого порошка и небулайзер, где все эти устройства хорошо известны специалистам в данной области техники.
Композиции по настоящему изобретению особенно применимы в препарате в виде систем доставки лекарственных средств регулируемого, ограниченного, пролонгированного, задержанного и замедленного высвобождения. Более конкретно, но не ограничиваясь, композиции применимы в препарате в виде систем парентерального регулируемого высвобождения и ограниченного высвобождения (обе системы приводят к многократному снижению числа введений), хорошо известных специалистам в данной области техники. Даже более предпочтительными являются системы регулируемого высвобождения и ограниченного высвобождения, вводимые подкожно. Без ограничения объема изобретения примерами полезных систем и композиций регулируемого высвобождения являются гидрогели, масляные гели, жидкие кристаллы, полимерные мицеллы, микросферы, наночастицы.
Способы изготовления систем регулируемого высвобождения, полезных для композиций по настоящему изобретению, включают, но не ограничены ими, кристаллизацию, конденсацию, сокристаллизацию, осаждение, соосаждение, эмульгирование, дисперсию, гомогенизацию высокого давления, инкапсуляцию, распылительную сушку, микроинкапсуляцию, коацервацию, разделение фаз, выпаривание растворителя с получением микросфер, экструзию и сверхкритические жидкостные процессы. Общая ссылка сделана на Handbook of Pharmaceutical Controlled Release (Wise, D.L, ed. Marcel Dekker, New York, 2000) и Drug and the Pharmaceutical Sciences vol. 99: Protein Formulation and Delivery (MacNally, E.J., ed. Marcel Dekker, New York, 2000).
Парентеральное введение можно осуществлять путем подкожной, внутримышечной, внутрибрюшинной или внутривенной инъекции с помощью шприца, возможно шприца карандашного типа. Альтернативно парентеральное введение можно осуществлять с помощью инфузионного насоса. Следующей возможностью является композиция, которая может представлять собой раствор или суспензию для введения пептида по настоящему изобретению в форме назального или легочного спрея. В качестве еще одной возможности фармацевтические композиции, содержащие пептид по настоящему изобретению, могут быть также приспособлены для чрескожного введения, например путем безыгольной инъекции или из пластыря, возможно ионтофоретического пластыря, или введения через слизистую оболочку, например трансбуккального введения.
Термин "стабилизированный препарат" относится к препарату с повышенной физической стабильностью, повышенной химической стабильностью или повышенной физической и химической стабильностью.
Термин "физическая стабильность" белкового препарата, как используют здесь, относится к тенденции белка к образованию биологически неактивных и/или нерастворимых агрегатов белка в результате воздействия на белок термомеханических нагрузок и/или взаимодействия с границами раздела и поверхностями, которые являются дестабилизирующими, такими как гидрофобные поверхности и границы раздела. Физическую стабильность водных белковых препаратов оценивают с помощью визуального осмотра и/или измерений мутности после воздействия на препарат, заполненный в подходящие контейнеры (например, картриджи или флаконы), механической/физической нагрузки (например, взбалтывания) при различных температурах в течение различных периодов времени. Визуальный осмотр препаратов проводят в четко фокусированном свете на темном фоне. Мутность препарата характеризуют визуальным баллом распределения степени мутности, например, на шкале от 0 до 3 (препарат, не показывающий мутности, соответствует визуальному баллу 0, а препарат, проявляющий визуальную мутность в дневном свете, соответствует визуальному баллу 3). Препарат классифицируют как физически нестабильный в отношении агрегации белка, когда он показывает визуальную мутность в дневном свете. Альтернативно мутность препарата можно оценить с помощью простых измерений мутности, хорошо известных специалистам в данной области техники. Физическую стабильность водных белковых препаратов можно также оценить путем использования спектроскопического агента или пробы конформационного состояния белка. Эта проба предпочтительно представляет собой малую молекулу, которая преимущественно связывается с не нативным конформером белка. Одним из примеров низкомолекулярной спектроскопической пробы структуры белка является тиофлавин Т. Тиофлавин Т представляет собой флуоресцентный краситель, который широко применяли для обнаружения амилоидных фибрилл. В присутствии фибрилл и, возможно, также других конфигураций белка тиофлавин Т вызывает новый максимум возбуждения примерно при 450 нм и усиленную эмиссию примерно при 482 нм при связывании с фибриллярной формой белка. Несвязанный тиофлавин Т является по существу не флуоресцентным при этих длинах волн.
В качестве проб на изменения в структуре белка от нативных до не нативных состояний можно использовать другие малые молекулы, например пробы на "гидрофобный пэтч", которые преимущественно связываются с доступными гидрофобными пэтчами белка. Эти гидрофобные пэтчи обычно углублены внутри третичной структуры белка в его нативном состоянии, но становятся доступными, как только белок начинает разворачиваться или денатурировать. Примерами этих низкомолекулярных спектроскопических проб являются ароматические гидрофобные красители, такие как антрацен, акридин, фенантролин или тому подобное. Другие спектроскопические пробы представляют собой комплексы металл-аминокислота, такие как комплексы металла кобальта с гидрофобными аминокислотами, такими как фенилаланин, лейцин, изолейцин, метионин и валин, или тому подобное.
Термин "химическая стабильность" белкового препарата, как используют здесь, относится к химическим ковалентным изменениям в структуре белка, приводящим к образованию продуктов химического распада с потенциальной потерей биологической эффективности и/или потенциально повышенными иммуногенными свойствами по сравнению с нативной структурой белка. Различные продукты химического распада могут образоваться в зависимости от типа и природы нативного белка, а также окружающей среды, под воздействием которой находится белок. Элиминации химического распада наиболее вероятно нельзя полностью избежать, и возрастающие количества продуктов химического распада часто наблюдают в процессе хранения и применения белкового препарата, что хорошо известно специалистам в данной области техники. Большинство белков склонно к деамидированию, процессу, при котором амидная группа боковой цепи в остатках глутаминила или аспарагинила гидролизуется с образованием свободной карбоновой кислоты. Другие биохимические пути распада включают образование высокомолекулярных продуктов преобразования, где две или более чем две молекулы белка ковалентно связаны друг с другом посредством трансамидирования и/или дисульфидных взаимодействий, что приводит к образованию ковалентно связанных димерных, олигомерных и полимерных продуктов распада (Stability of Protein Pharmaceuticals, Ahern. T.J. & Manning M.C., Plenum Press, New York 1992). Окисление (например, остатков метионина) можно упомянуть как другой вариант химического распада. Химическую стабильность белкового препарата можно оценить путем измерения количества продуктов химического распада в различные моменты времени после воздействия различных условий окружающей среды (образование продуктов распада может быть часто ускорено, например, повышенной температурой). Количество каждого индивидуального продукта распада часто определяют путем разделения продуктов распада в зависимости от молекулярного размера и/или заряда, используя различные хроматографические методики (например, вытеснительную хроматографию по размеру - ВЭЖХ и/или ВЭЖХ с обращенной фазой).
Следовательно, как изложено выше, "стабилизированный препарат" относится к препарату с повышенной физической стабильностью, повышенной химической стабильностью или повышенной физической и химической стабильностью. Как правило, препарат должен быть стабильным в процессе применения и хранения (в соответствии с рекомендованными условиями применения и хранения) до истечения срока годности.
В одном воплощении изобретения фармацевтический препарат, содержащий пептид по настоящему изобретению, стабилен в течение более чем 6 недель применения и в течение более чем 3 лет хранения.
В другом воплощении изобретения фармацевтический препарат, содержащий пептид по настоящему изобретению, стабилен в течение более чем 4 недель применения и в течение более чем 3 лет хранения.
В следующем воплощении изобретения фармацевтический препарат, содержащий пептид по настоящему изобретению, стабилен в течение более чем 4 недель применения и в течение более чем двух лет хранения.
В следующем воплощении изобретения фармацевтический препарат, содержащий пептид по настоящему изобретению, стабилен в течение более чем 2 недель применения и в течение более чем двух лет хранения.
ПРИМЕРЫ
Тест на активность вариантов ИЛ-21
Белки дикого типа и мутантные белки чИЛ-21 (человеческого ИЛ-21) анализировали, используя клеточный анализ активности с использованием Stat-регулируемой люциферазной репортерной системы.
В этом анализе используют мышиную клеточную линию Baf3, которая стабильно трансформирована для экспрессии человеческого ИЛ-21R и репортерную конструкцию Stat-сшитой люциферазы. Клетки Baf3 эндогенно экспрессируют 'общую цепь' гамма С, которая составляет основной компонент рецепторного комплекса передачи сигнала ИЛ-21. Эту репортерную клеточную линию Ваf3/чИЛ-21Р выращивали в минимальной свободной от ИЛ-3 среде в течение 6 часов перед стимуляцией. Затем проводили анализ доза-ответ, используя стимуляцию клеток в течение 24 часов.
На фиг.1 представлен анализ белков, экспрессируемых транзиторно в клетках HEK293-FS (Stengaard-Pedersen et al. N.Engl. J.Med. (2003) 349:554; Invitrogen). Эти белки анализировали в форме необработанных надосадочных жидкостей, собранных через 48 часов после трансфекции.
На фиг.2 представлен анализ белков дикого типа и мутантных белков чИЛ-21, анализируемых в виде очищенных белков. Chim-IL21 представляет собой ИЛ-21 sub[K77-Т92] (SEQ ID No.7). Здесь конструкции были получены для экспрессии в Е.coli и очищены посредством вторичной укладки белков, присутствующих в тельцах включения.
Альтернативный тест на активность вариантов ИЛ-21
кДНК, кодирующие варианты ИЛ-21, анализируют путем транзиторной экспрессии с последующим анализом активности в Stat-регулируемой репортерной системе.
кДНК трансфицируют в клетки НЕК293 FreeStyle (Stengaard-Pedersen et al. N.Engl. J.Med. (2003) 349:554; Invitrogen). Надосадочные жидкости собирают из среды, свободной от сыворотки, через 48 часов после трансфекции и анализируют в клеточном биологическом анализе. В этом анализе используют мышиную клеточную линию Baf3, стабильно трансфицированную для экспрессии человеческого ИЛ-21R и репортерной конструкции Stat-сшитой люциферазы. Клетки Baf3 эндогенно экспрессируют γс компонент активного рецепторного комплекса ИЛ-21. Репортерную клеточную линию Baf3/чИЛ-21R выращивают в минимальной среде, свободной от ИЛ-3, в течение 18 часов перед стимуляцией. Анализ доза-ответ проводят, используя необработанную надосадочную жидкость из трансфектантов HEK293-FS. Продолжительность стимуляции составляет четыре часа.
ФАРМАКОЛОГИЧЕСКИЕ МЕТОДЫ
Приведенный ниже метод in vitro используют для исследования усиления ADCC (опосредованной антителами клеточной цитотоксичности).
Клетки-мишени, экспрессирующие антиген-мишень, инкубируют с антителом против антигена-мишени и мононуклеарными клетками периферической крови, NK-клетками, нейтрофилами, макрофагами, моноцитами или DC в качестве эффекторных клеток. Эффекторные клетки можно предварительно инкубировать от 1 до 10 суток с ИЛ-21, либо ИЛ-21 можно добавлять в культуру, содержащую как эффекторные клетки, так и клетки-мишени. Другие соединения, которые могут усиливать ADCC, можно включать в культуру или культуру предварительной инкубации. Эффективность ADCC измеряют как специфичное высвобождение 51Сr из клеток-мишеней или как активность LDH, как описано ранее (Golay et al., Haematologica 88:1002-1012, 2003, или Liu et al., Cancer Immun 2: 13, 2002, или Watanabeetal., Breast Cancer Res Treat 53:199-207, 1999).
Определение ADCC проводят, используя анализ на основе проточной цитометрии, как описано ранее (Flieger et. al., J Immunother 23: 480-486, 2000, или Flieger et al., J Immunol Methods 180:1-13, 1995, или Flieger et al., Hybridoma 18:63-68, 1999).
Определение ADCP проводят посредством двухцветного флуоресцентного анализа, как описано в Watanabe et al., Breast Cancer Res Treat 53:199-207, 1999, или Akewanlop et al., Cancer Res 61:4061-4065, 2001.
Метод in vivo определения усиления ADCC изложен ниже:
Лейкозные клетки или трансформированные клетки инъецируют i.v., i.p. или s.c. изогенным животным после обработки терапевтическим антителом, распознающим антиген, экспрессируемый лейкозными клетками или трансформированными клетками, с терапией или без терапии ИЛ-21. Конечными результатами являются опухолевая масса и выживаемость. Вовлеченность ADCC может быть подтверждена путем использования антител, блокирующих FcγRI, или путем использования мышей с дефицитом по FcγRI.
Метод in vivo исследования усиления ADCC в отношении клеток-мишеней человеческого происхождения описан ранее в Zhang et al., Blood 102:284-288, 2003 или Flavell et al. Cancer Res 58:5787-5794, 1998. В соответствии с этими моделями человеческие лейкозные клетки или трансформированные клетки инъецируют i.v., i.p. или s.c. в SCID мышам после обработки терапевтическим антителом, распознающим антиген, экспрессируемый лейкозными клетками или трансформированными клетками, с терапией или без терапии ИЛ-21.
Опухолевые клеточные линии, например клетки легочной карциномы Льюиса (LLC), либо клетки меланомы B16-F10, либо клетки почечной карциномы, либо клетки карциномы молочной железы 4Т1 имплантируют s.c. изогенным мышам. Когда опухоли становятся пальпируемыми, мышей обрабатывают ИЛ-21 в комбинации с другими противораковыми агентами, как описано в данной заявке. Методология описана в Palumbo et al., Cancer Res. 62:6966-6972 (2002); Bove et al., Biochem Biophys Res Commun 291:1001-1005 (2002); Wigginton et al., J Immunol 169:4467-4474 (2002).
Опухолевые клеточные линии, например клетки легочной карциномы Льюиса (LLC) или клетки меланомы B16-F10 имплантируют s.c. изогенным мышам. Первичную опухоль удаляют через 1-4 недели, и мышей обрабатывают ИЛ-21 в комбинации с другими противораковыми агентами, как описано в данной заявке. Методология описана в Palumbo et al., Cancer Res. 62:6966-6972 (2002).
Опухолевые клеточные линии, например клетки легочной карциномы Льюиса (LLC), либо клетки меланомы B16-F10, либо клетки почечной карциномы инъецируют i.v. изогенным мышам, и мышей обрабатывают ИЛ-21 в комбинации с другими противораковыми агентами, как описано в данной заявке. Методология описана в Amirkhosravi et al., Thromb. Haemost. 87:930-936 (2002); Hosaka et al., Cancer Lett 161:231-240 (2000); Maini et al., In vivo 17:119-123 (2003).
Клетки почечной карциномы инъецируют интраренально в одну почку изогенным мышам. Первичную опухоль удаляют через 1-4 недели, и мышей обрабатывают ИЛ-21 в комбинации с другими противораковыми агентами, как описано в данной заявке. Методология описана в Murphy et al., J Immunol 170:2727-2733 (2003).









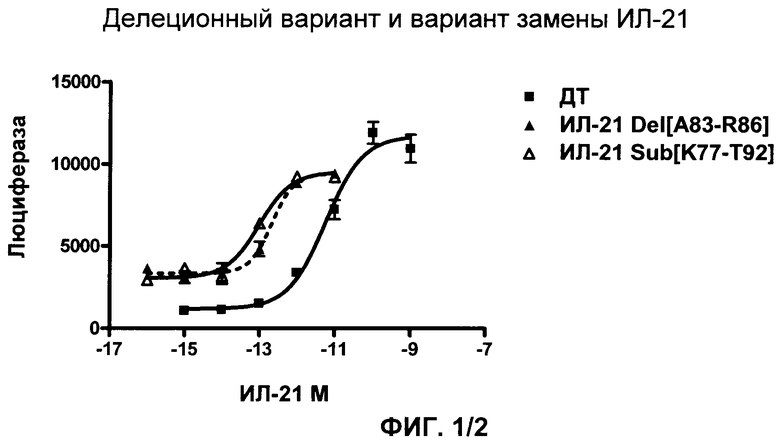
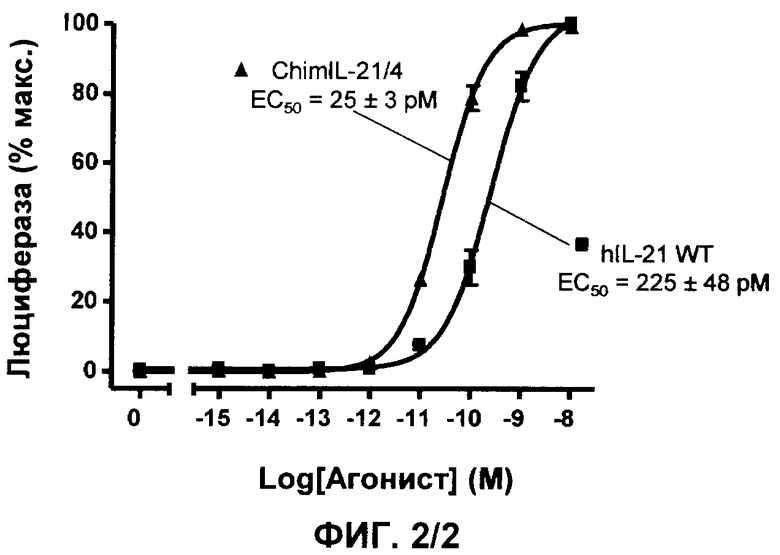
Изобретение относится к новым вариантам пептидов ИЛ-21, где аминокислоты делегированы и/или заменены в области, состоящей из аминокислот №83-96, а также их применению для изготовления лекарственного средства для лечения рака. 6 н. и 2 з.п. ф-лы, 2 ил.
1. Пептид, содержащий аминокислотную последовательность, выбранную
из
A) SEQ ID No:3, SEQ ID No:4, SEQ ID No:5 и SEQ ID No:6; и
Б) пептидов А) с дополнительным N-концевым Met.
2. Пептид, содержащий аминокислотную последовательность, выбранную
из
A) SEQ ID No:7, SEQ ID No:8, SEQ ID No:9 и SEQ ID No:10; и
Б) пептидов А) с дополнительным N-концевым Met.
3. Применение пептида по любому из пп.1 и 2 в изготовлении лекарственного средства для лечения рака.
4. Применение по п.3, где рак выбран из неметастатических и метастатических неопластических расстройств, таких как злокачественная меланома, раки кожи, не представляющие собой меланому, почечно-клеточная карцинома, рак головы и шеи, рак эндокринной системы, рак яичника, мелкоклеточный рак легкого, немелкоклеточный рак легкого, рак молочной железы, рак пищевода, верхний желудочно-кишечный рак, рак ободочной и прямой кишки, рак печени и желчных протоков, рак поджелудочной железы, рак простаты, рак мочевого пузыря, рак яичка, рак шейки матки, рак эндометрия, саркомы костей и мягких тканей, рак центральной нервной системы, лимфома, лейкоз и рак неизвестного первичного происхождения.
5. Применение по п.4, где рак представляет собой злокачественную меланому.
6. Нуклеиново-кислотная конструкция, кодирующая пептид по любому из пп.1 и 2.
7. Вектор, содержащий нуклеиново-кислотную конструкцию по п.6.
8. Клетка-хозяин, содержащая нуклеиново-кислотную конструкцию по п.6 или вектор по п.7.
| ВЫСОКОАФИННЫЕ МУТЕИНЫ ИНТЕРЛЕЙКИНА-4 | 1997 |
|
RU2202364C2 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| SMYTH M J ET AL | |||
| "Cytokines in cancer immunity and immunotherapy", IMMUNOLOGICAL REVIEWS, 2004, Vol:202, Page(s):275-293. | |||
Авторы
Даты
2011-02-20—Публикация
2006-04-18—Подача