Изобретение относится к области медицины, более конкретно к области синтеза новых микобактерицидных (МБЦ) и туберкулоцидных (ТБЦ) дезинфицирующих средств, а именно катионные полимерные соли полидиаллиламмониевого ряда, обладающие in vitro микобактерицидной и туберкулоцидной (т.е. убивающей микобактерии) активностью: вторичный (поли)N,N-диаллиламмоний трифторацетат (ПДААТФА) и третичный (поли)N,N-диаллил-N-метиламмоний трифторацетат (ПДАМАТФА), полученные на основе трифторацетатов диаллиламинов (ДАА) (самого мономера ДАА и N,N-диаллил-N-метиламина (ДАМА)).
Хорошо известно разрушительное воздействие, которое микобактерии оказывают на человечество, в частности туберкулез (ТБ) остается на эпидемиологическом уровне в большинстве частей света [1]. Фактически, за 1990-е годы от ТБ умерло больше людей, чем за любую другую декаду в истории [1]. Более того, с обнаружением относительно недавно патогенных свойств различных «атипичных» микобактерий стало очевидным, что микобактерии многообразны и имеют различные клинические проявления. Все это является важным аргументом для того, чтобы рассматривать микобактерии как наиболее важный тип микроорганизмов, вызывающих заболевания и смертность среди людей [1, 4-7].
Известно, что микобактерии, в частности Mycobacterium tuberculosis, мало восприимчивы к действию биоцидов, к которым можно отнести лекарственные антибиотики и дезинфицирующие средства (ДС) [1-7]. Единственной наиболее важной причиной устойчивости микобактерии к действию биоцидов является непроницаемая природа их клеточной стенки [4-6]. Главной особенностью строения микобактериальной клеточной оболочки, отличающей ее от большинства других бактерий, является сложный комплекс, имеющий во внешнем слое высокое содержание липидов благодаря присутствию длинно-цепочечных миколовых кислот, ковалентно связанных с арабиногалактановым слоем, за которым имеется пептидогликановый слой. В целом такое строение обеспечивает непроницаемость микобактерий для многих растворимых веществ, включая антибиотики и ДС [4-6].
В последние два десятилетия наблюдается развитие устойчивости к лекарственным антибиотикам, используемым в комбинированной терапии ТБ, и прежде всего, к изониазиду (производное пиридина - гидразид изоникотиновой кислоты), который используется с 1952 г. как эффективное противотуберкулезное (ПТБ) средство, оказывающее бактериостатическое действие [1, 4-7]. Согласно данным исследований, причиной этого могут быть генные мутации, происходящие в бактерии в ответ на селективное, направленное на нарушение определенных метаболических процессов действие антибиотиков [4-7]. По утверждениям специалистов, в будущем используемой группы лекарств не будет достаточно для того, чтобы полностью контролировать туберкулез [7]. Риск устойчивости к ПТБ лекарствам становится реальным во многих частях света, но нигде спектр устойчивости к ПТБ лекарствам не является более угрожающим, чем в учреждениях Российской пенитенциарной системы, где более чем 20% от более чем 100000 активных случаев являются лекарственно устойчивыми по данным Всемирной Организации Здравоохранения (ВОЗ) [1].
Эти данные свидетельствуют о том, что одним из основных факторов в борьбе против распространения туберкулеза является применение надежных дезинфицирующих средств, обладающих туберкулоцидной (т.е. убивающей бактерии туберкулеза) активностью.
Сегодня известны ПТБ дезинфицирующие средства, описание и границы использования которых подробно представлены в обзорах [1, 3] и монографии [2].
Метиловый и изопропиловый спирты высокой концентрации в общем считаются отличными микобактерицидными агентами. Концентрация очень важна, поскольку менее 50% водные растворы этилового или изопропилового спирта показывают значительное снижение активности, в то же время этанол в концентрации выше 95% содержит слишком мало воды, чтобы быть эффективным. Существенный недостаток алкоголей в том, что они неактивны в присутствии органических материалов, в том числе мокроты. Более того, алкоголи не используются для стерилизации медицинских инструментов и хирургических материалов, так как они не обладают спороубивающей (спороицидной) активностью и не могут проникать в органические материалы.
Алкиламины. N-додецил-1,3-пропандиамин (имеющий первичную и вторичную аминогруппы, известный как "диамин") используется с 1956 г. как эффективное микобактерицидное дезинфицирующее средство. Диамин не вызывает раздражений. Активность диамина, как предполагается, не зависит от присутствия мокроты, поэтому он используется для дезинфекции выделений больных (обработка полов, рам кроватей, лабораторных поверхностей). В последнее две декады получил распространение N,N-бис(3-аминопропил)додециламин (имеющий третичную и две первичные аминогруппы, торговое название “Лонзабак”, производитель - Швейцарская фирма Лонза) как эффективный противотуберкулезный дезинфектант, обладающий широким спектром антимикробной активности. В РФ и Белоруссии препараты на основе Лонзабак используются для дезинфекции в пищевой промышленности, учреждениях, больницах.
Хлористые соединения. Соединения хлора широко используются в качестве дезинфектантов. Спектр их активности широк, они являются быстродействующими и недорогими препаратами. Еще в 1968 г. гипохлорит натрия рассматривала как потенциально микобактерицидный и хорошо обеззараживающий мокроту и выделения. Их недостаток в том, что они вызывают коррозию, имеют запах и обладают отбеливающим действием.
Формальдегиды. Общепринято, что формальдегиды обладают хорошей микобактерицидной активностью. Однако, они считаются канцерогенными (данные ВОЗ за 2004 г.), поэтому их использование в качестве дезинфектантов ограничено.
Этиленоксид. Это бесцветный взрывчатый, воспламеняющийся, диффундирующий газ, который считается хорошим ТБЦ агентом. Газ не вреден для материалов и поэтому используется для обработки кожи, тканей, бумаги, пластика, дерева, металлов, резины. Этиленоксид применяют для обеззараживания волоконно-оптических эндоскопов, которые могут быть повреждены при обработке в автоклаве. Из-за взрывоопасности газ следует использовать только при осуществлении соответствующего контроля. Одним из главных недостатков этиленоксида является его токсичность.
Глутаральдегид. В отличие от формальдегида, глутаральдегид не вызывает коррозию и оказывает значительно меньшее раздражающее действие. В 60-е годы считалось, что 2% алкилированный глутаральдегид обладает значительной МБЦ активностью. Однако позднее установлено, что 2% алкилированный глутаральдегид недостаточно эффективен относительно M. tuberculosis, и некоторые виды микобактерий устойчивы к действию глутаральдегида. Тем не менее, глутаральдегид считается препаратом высокого класса для дезинфекции эндоскопов при соблюдении соответствующих рекомендаций его использования. В 90-е годы было выявлено, что глутаральдегид вызывает кашель, астму, головную боль, тошноту и рвоту, носовое кровотечение, риниты, аллергические дерматиты.
Перекись водорода. Активность 7.5% перекиси водорода против M.tuberculosis была отмечена в 1996 г. Перекиси водорода применяются для обеззараживания эндоскопов. В 90-е годы было показано, что перекисные соединения менее эффективны против микобактерий, чем глутаральдегид, и могут воздействовать на детали эндоскопов.
Йод и йодоформы. Долгое время йод и йодоформы считались эффективными агентами против M. tuberculosis. В 1953 г. было показано, что 1% раствор йода в 70% спирте обеззараживает термометры, зараженные бактериями ТБ. Йод и йодоформы относительно нетоксичны и применяются для дезинфекции металлических и стеклянных инструментов, а также для предоперационной кожной дезинфекции. В то же время йодоформы исключены из ряда дезинфектантов высокого класса, поскольку их бактерицидная эффективность в отношении М. tuberculosis не доказана.
Соединения фенола. В течение многих лет фенольные соединения считались эффективными против M. tuberculosis. Однако исследователи признают их серьезные недостатки: токсичность и сильный запах, который может адсорбироваться пищей и другими продуктами, а также другие побочные эффекты (накапливание в пористых материалах, что вызывает раздражение и т.д.) при использовании соединений фенола для больничной дезинфекции.
ЧАС. В 80-90-е годы было установлено, что четвертичные аммониевые соединения не обладают заметной микобактерицидной, в том числе и противотуберкулезной активностью даже на уровне бактериостатического действия.
Многие из описанных выше веществ, такие как алкоголи, фенолы, йод, хлористые соединения, известны более сотни лет (алкоголь многие сотни лет), некоторые из них демонстрируют достаточно широкий спектр антимикробной активности. В то же время необходимо подчеркнуть, что известные противотуберкулезные ДС оказывают часто только бактериостатическое (тормозящее рост бактерий) действие и не всегда проявляют бактерицидную ТБЦ (т.е. убивающую бактерии туберкулеза) эффективность [1, 2]. Кроме того, многие из описанных выше ДС производят побочные эффекты, наносящие серьезный ущерб здоровью людей [1, 2].
Обобщая все вышесказанное, можно заключить, что широкий спектр действия ДС, включающий биоцидную активность относительно грамположительных, в том числе M. smegmatis и M. tuberculosis, грамотрицательных бактерий и грибов, является наиболее необходимым, но труднодостижимым свойством дезинфицирующего средства. Таким образом, поиск новых субстанций, препаратов и ДС, проявляющих МКБ И ТБЦ эффективность в сочетании с антимикробной биоцидной активностью широкого спектра, является одной из самых актуальных задач.
Задача настоящего изобретения заключается в поиске новых субстанций, препаратов и ДС, проявляющих МКБ и ТБЦ эффективность в сочетании с антимикробной биоцидной активностью широкого спектра действия.
Авторам предлагаемого изобретения удалось обнаружить, что синтезированные ими ранее новые катионные полимерные соли полидиаллиламмониевого ряда - вторичный ПДААТФА и третичный ПДАМАТФА [8], биоцидная активность которых относительно грамположительных и грамотрицательных бактерий и грибов рода Candida была также впервые установлена [8], проявляют достаточно высокую МКБ и ТБЦ биоцидную (т.е. убивающую микобактерий, в том числе и бактерии туберкулеза) активность, что выделяет их из ряда известных биоцидов, редко сочетающих антимикробную эффективность традиционного спектра действия с МБЦ и ТБЦ активностью.
Поставленная задача решается тем, что предложены вторичные и третичные полидиаллиламмониевые соли общей формулы:
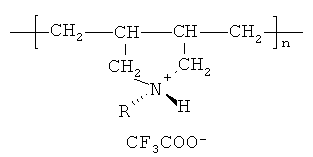
где R=H; R=CH3;
n=114-244 (средневесовая степень полимеризации);
Mw=24000-55000 г/моль (средневесовая молекулярная масса);
δ=1.85 - коэффициент полидисперсности молекулярно-массового распределения Mw-Mn, где Mn - среднечисловая молекулярная масса, в качестве микобактерицидного и туберкулоцидного дезинфицирующего средства.
В результате биологических испытаний установлена минимальная бактерицидная (т.е. убивающая клетки бактерий) концентрация (МБК) от 250 мкг/мл (0.025 вес.%) до 3.5 мкг/мл (0.00035 вес.%) относительно M. smegmatis и от 125 мкг/мл (0.0125 вес.%) до 31 мкг/мл (0.0031 вес.%) относительно М. tuberculosis.
Преимущественное использование полиаминов с Mw от 40000 до 55000 г/моль позволяет снизить МБК до 15-3.5 мкг/мл (0.0015-0.00035 вес.%) относительно M. smegmatis и до 31 мкг/мл (0.0031 вес.%) относительно М. tuberculosis.
Испытания антибактериальной активности синтезированных полидиаллиламмониевых солей и исходных мономеров проводят на следующих образцах:
- поли(диаллиламмонийтрифторацетат) с MW 24000 г/моль;
- поли(диаллилметиламмонийтрифторацетат) с MW 40000 г/моль;
- поли(диаллилметиламмонийтрифторацетат) с MW 55000 г/моль;
- мономер диаллиламмонийтрифторацетат;
- мономер диаллилметиламмонийтрифторацетат.
Изучение антимикобактериальной активности данных препаратов проводят на штаммах М. smegmatis mc2155 и М. tuberculosis RvH37 в жидкой среде Сатона с добавлением БСА (бычий сывороточный альбумин), NaCl и глюкозы в соответствии с принятой методикой [9] в пробирках объемом 15 мл с добавлением 2 мл среды без перемешивания при 37°С.
Антимикробную активность различных концентраций синтезированных полиаминов в отношении этих микобактерии исследуют при концентрации бактерий 7.6×105 КОЕ/мл (колониеобразующие единицы, КОЕ). Микобактерицидный эффект подтверждается при высеве бактерий, обработанных при различных концентрациях полимеров, на плотную среду с целью контроля за ростом обработанных бактерий и определения количества колониеобразующих единиц. Для этого исходное количество обработанных в течение трех суток бактериальных клеток разводят несколько раз в соотношении 1:10 и высевают по 100 мкл культуры из каждого разведения на чашку Петри с плотной средой Сатона.
В результате определяют минимальные бактерицидные концентрации полимеров относительно микобактерий М. smegmatis (3.5 мкг/мл) и М. tuberculosis (31 мкг/мл) (Табл.1). После инкубирования клеток в жидкой среде в присутствии полимера, взятого при минимальной бактерицидной концентрации, в течение 1 месяца при 37°С видимого роста микобактерий не наблюдают.
Необходимо подчеркнуть, что предложенные полидиаллиламмониевые соли ПДААТФА И ПДАМАТФА оказывают бактерицидное (т.е. убивающее клетки бактерий) действие на изученные микобактерий М. smegmatis и М. tuberculosis. Это выгодно отличает их от многих известных описанных выше противотуберкулезных ДС и от антибиотиков, оказывающих в подавляющем большинстве бактериостатическое (ингибирующее, тормозящее рост бактерий) действие [1-7, 10].
Найденные МБК полимеров ПДААТФА и ПДАМАТФА значительно ниже концентраций известных ДС, применяемых в рабочих растворах (Таблица 2). Более того, полученные значения МБК сопоставимы с минимальными ингибирующими бактериостатическими концентрациями (МИК) антибиотиков. Так, МИК в отношении микобактерий М. tuberculosis для канамицина составляет 1-8 мкг/мл, для циклосерина 5-20 мкг/мл, для пиразинамида 20-100 мкг/мл [10].
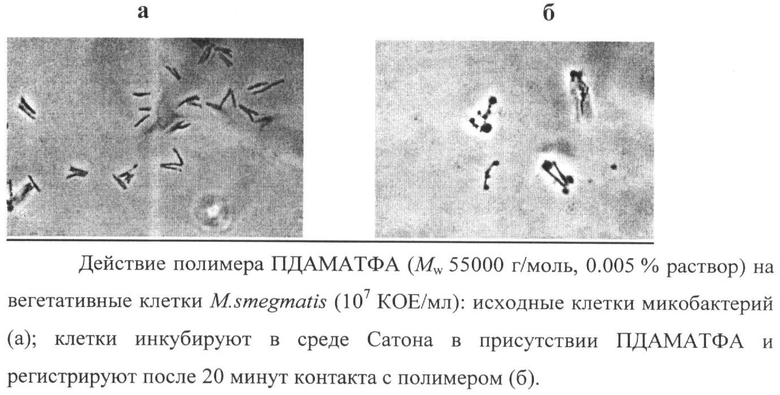
Можно сделать вывод, что предложенные вторичные и третичные полидиаллиламмониевые соли оказывают более эффективное разрушительное действие на клетки микобактерий, включая М. tuberculosis, чем известные ДС и антибиотики. Помимо прямых биологических исследований это подтверждается микроскопическим изучением поведения микобактерий М. smegmatis, находящихся под воздействием ПДАМАТФА (MW 55000 г/моль, 0.005% раствор).
Изучение проводят с помощью микроскопа Eclipse Е4000, Nicon, Japan, увеличение в 1000 раз, минимальные размеры видимого объекта составляют 0.2-0.5 мкм. На предметное стекло помещают 5 мкл образца ((а) клеточная суспензия, 107 КОЕ/мл, в среде Сатона); (б) клеточная суспензия, 107 КОЕ/мл, в среде Сатона в присутствии полимера; (с) раствор полимера) и накрывают покровным стеклом. Используется флуоресцентный краситель иодид пропидиума, который обладает способностью связываться с нуклеиновыми кислотами поврежденных клеток; конечная концентрация в растворе 3 мкМ; длина волны возбуждения λ 510-560 нм.
Наблюдения показывают, что раствор полимера (случай (с)) оптически прозрачен. Сопоставление наблюдений в случаях (а) и (б) позволяет заключить, что гибель бактерий происходит достаточно быстро, в течение 15-30 минут. За это время под действием полимера на клетках микобактерии (в частности, изучаемого ПДАМАТФА) происходит образование неопределенных пока сферовидных структур, сама клетка имеет уменьшенный поперечный размер, теряет контраст и, очевидно, деградирует, становясь нежизнеспособной (чертеж). Последнее следует из окрашивания обработанных иодидом пропидиума клеток, что свидетельствует о необратимом нарушении клеточного барьера проницаемости.
При аналогичном микроскопическом исследовании действия антибиотиков (рифампицин, изониазпид) на клетки М. smegmatis выявляется, что при тех же концентрациях, что и ПДАМАТФА, необходимо несколько дней для нарушения проницаемости клеточной стенки микобактерии М. smegmatis и появления окрашивания клеток иодидом пропидиума.
В биологических исследованиях мибактерицидного действия ПДААТФА и ПДАМАТФА обнаружено, что с уменьшением количества звеньев в цепи полиаминов, т.е. с уменьшением степени полимеризации n, бактерицидная активность полимеров уменьшается (см. Табл.1).
Мономеры, а именно трифторацетатные соли вторичного и третичного диаллиламинов (необходимо отметить, что исходные мономеры имеют другую структуру, нежели звенья синтезированных полидиаллиламинов) не обладают микобактерицидной активностью (Табл.3).
Среди известных противотуберкулезных ДС и лекарственных препаратов предложенные полидиаллиламмониевые соли - вторичный ПДААТФА и третичный ПДАМАТФА, активными центрами которых являются соответственно вторичные (NH2)+ и третичные (NCH3H)+ аммониевые группы пирролидиниевых звеньев макроцепи - представляют собой совершенно новые структуры, проявляющие МКБ и ТБЦ эффективность. МКБ и ТБЦ активность пирролидиновых и пирролидиниевых циклов и/или их производных не была известна до настоящего времени. Как отмечено выше, известные биоциды ЧАС и поли(ЧАС), имеющие положительно заряженный четвертичный азот в качестве активных центров, не обладают МБЦ и ТБЦ активностью. Среди известных ДС и лекарственных препаратов, обладающих противотуберкулезными свойствами, не присутствуют соединения полимерной природы. В то же время, полимерная природа синтезированных соединений является положительным фактором с точки зрения уменьшения их токсичности и провоцирования дыхательной аллергии различного рода, создания устойчивой поверхностной пленки и т.д.
Результаты биологических и микроскопических исследований полимеров ПДААТФА и ПДАМАТФА, свидетельствующие о быстром микобактерицидном действии, позволяют предположить, что их биоцидная активность обусловлена фатальным нарушением целостности клеточной стенки и проницаемости клеточной мембраны микобактерий и, судя по времени воздействия, не направлена на специфические метаболические процессы клетки, подобно известным антибиотикам. Поэтому можно полагать, что возможное использование полимеров ПДААТФА и ПДАМАТФА в качестве ДС не вызовет устойчивости микобактерий к их биоцидному действию, как это наблюдается в случае антибиотиков [1-7].
Таким образом, предложенные полидиаллиламмониевые соли ПДААТФА и ПДАМАТФА проявляют значительную микобактерицидную и туберкулоцидную активность при весьма низких бактерицидных концентрациях в сочетании с установленной ранее высокой биоцидной эффективностью широкого спектра. По своим данным предложенные полидиаллиламмониевые соли выделяются из ряда известных биоцидов, что позволяет считать их уникальными среди подобных, применяемых в современной практике для противотуберкулезной дезинфекции.
Литература
1. Lauzardo, М., Rubin, J. Mycobacterial disinfection. In Disinfection, Sterilization and Preservation; Block, S.S., Ed.; Lippincott Williams&Wilkins: New-York, 2001; Ch. 26, p.513-528.
2. Disinfection, Sterilization and Preservation; Block, S.S., Ed.; Lippincott Williams&Wilkins: New-York, 2001.
3. McDonnell, G.; Russell, A.D. Clinical Microbiology Reviews 1999, 12, 147-179.
4. Franklin, T.J.; Snow, G.A. Biochemistry and Molecular Biology of Antimicrobial Drug Action; Springer-Verlag: New York, 2005; pp.39-41, 123-126, 160-164.
5. Russel, A.D. Bacterial sensitivity and resistance. D. Micobacterial agents. In Principal and Practice of Disinfection, Preservation and sterilization; 3rd edn, Russel, A.D., Hugo, W.B. and Ayliffe, G.A.J., Eds.; Blackwell Science: Oxford, 1999; p.321-332.
6. Russel, A. D. Bacterial resistance to disinfectants: present knowledge and future problems. J. Hospital Infections 1999, 43 (Suppl.), S57-S68.
7. Enarson, D.A. Global Control of Tuberculosis and New Drugs: Public Health aspects of New Drug Developments for Tuberculosis. In Development of New Antituberculosis Drugs; Yew, W.W., Ed.; Nova Science Publishers: New York, 2006, p.1-16.
8. RU 2272045 C1, 20.03.2006.
9. Nancy D. Connell. Mycobacterium: Isolation, Maintenance, Transformation, and Mutant Selection. // Methods in Cell Biology. 1994. V.45. Chapter 6. P.107-125.
10. Martina Casenghi. Development of new drugs for ТВ chemotherapy. 2006. Campaign for Access to Essential Medicines. Medecins Sans Frontieres. Geneva. Switzerland.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ЭФФЕКТИВНОСТИ ДЕЗИНФИЦИРУЮЩИХ СРЕДСТВ, ПРИМЕНЯЕМЫХ В ПРОТИВОТУБЕРКУЛЕЗНЫХ УЧРЕЖДЕНИЯХ | 2008 |
|
RU2364629C1 |
| ПРИМЕНЕНИЕ АНТИСЕПТИЧЕСКОГО И ДЕЗИНФИЦИРУЮЩЕГО СРЕДСТВА | 2022 |
|
RU2801796C1 |
| ПОЛИДИАЛЛИЛАМИНЫ И СОДЕРЖАЩЕЕ ИХ ДЕЗИНФИЦИРУЮЩЕЕ СРЕДСТВО | 2004 |
|
RU2272045C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ И ДОПОЛНИТЕЛЬНОЙ ХИМИОТЕРАПИИ ТУБЕРКУЛЕЗА | 2004 |
|
RU2295330C2 |
| ПРОТИВОТУБЕРКУЛЕЗНОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО: КОМПОЗИЦИЯ ИМИДАЗО[1,2-b]ТЕТРАЗИНА С ПИРАЗИНАМИДОМ | 2013 |
|
RU2545458C2 |
| Противотуберкулёзное средство на основе (Z)-3-(3,3-Диметил-2-оксобутилиден)-3,4-дигидро-2H-1,4-бензоксазин-2-она и способ его синтеза | 2020 |
|
RU2748748C1 |
| ФУРИЛИДЕНФУРАНОНОВЫЕ ПРОИЗВОДНЫЕ УСНИНОВОЙ КИСЛОТЫ КАК НОВЫЕ ПРОТИВОТУБЕРКУЛЕЗНЫЕ АГЕНТЫ | 2013 |
|
RU2533707C1 |
| АМИНОТИАЗОЛЬНЫЕ ПРОИЗВОДНЫЕ УСНИНОВОЙ КИСЛОТЫ КАК НОВЫЕ ПРОТИВОТУБЕРКУЛЕЗНЫЕ АГЕНТЫ | 2012 |
|
RU2483722C1 |
| ЧЕТВЕРТИЧНЫЕ АММОНИЙНЫЕ ПРОИЗВОДНЫЕ 2-АМИНОТИОФЕН-3-КАРБОКСИЛАТОВ, ОБЛАДАЮЩИЕ ПРОТИВОТУБЕРКУЛЕЗНОЙ АКТИВНОСТЬЮ | 2016 |
|
RU2629369C1 |
| СЕЛЕКТИВНЫЕ ИНГИБИТОРЫ ГЛИЦЕРАЛЬДЕГИД-3-ФОСФАТДЕГИДРОГЕНАЗЫ МИКОБАКТЕРИЙ | 2017 |
|
RU2661151C1 |
Изобретение относится к области медицины, к дезинфицирующим средствам. Дезинфицирующее средство - это вторичный (поли)N,N-диаллиламмоний трифторацетат (ПДААТФА) и третичный (поли)N,N-диаллил-N-метиламмоний трифторацетат (ПДАМАТФА), полученные на основе трифторацетатов диаллиламинов (ДАА) (самого мономера ДАА и N,N-диаллил-N-метиламина (ДАМА)), Полидиаллиламмониевые соли общей формулы:

где R=Н; R=СН3; n=114-244 (средневесовая степень полимеризации); Мw=24000-55000 г/моль (средневесовая молекулярная масса); δ=1.85 - коэффициент полидисперсности молекулярно-массового распределения Mw-Mn, где Mn - среднечисловая молекулярная масса, в качестве микобактерицидного и туберкулоцидного дезинфицирующего средства. Изобретение обеспечивает гибель бактерий в течение 15-30 мин и обладает in vitro микобактерицидной и туберкулоцидной активностью. 3 табл., 1 ил.
Дезинфицирующее средство, обладающее микобактерицидной и туберкулоцидной активностью, представляющее собой полидиаллиламмониевую соль общей формулы

где R - H; R - CH3;
n=114-244 (средневесовая степень полимеризации);
Mw=24000-55000 г/моль (средневесовая молекулярная масса);
δ=1,85 - коэффициент полидисперсности молекулярно-массового распределения Mw-Mn, где Mn - среднечисловая молекулярная масса.
| ПОЛИДИАЛЛИЛАМИНЫ И СОДЕРЖАЩЕЕ ИХ ДЕЗИНФИЦИРУЮЩЕЕ СРЕДСТВО | 2004 |
|
RU2272045C1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Стабилизатор для самосвалов | 1974 |
|
SU516554A1 |
| MX PA02000492 A, 02.07.2002. | |||
Авторы
Даты
2011-04-10—Публикация
2009-10-13—Подача