Изобретение относится к области синтеза новых полиэлектролитов катионного типа на основе трифторацетатов диаллиламинов - мономеров ряда N,N-диаллиламина (ДАА) (самого мономера ДАА и N,N-диаллил-N-метиламина (ДАМА)) - и может быть использовано в различных областях народного хозяйства и, в частности, медицине.
Круг синтетических полиэлектролитов весьма узок. В настоящее время исследователи рассматривают возможности регулирования строения, структуры и молекулярных масс, распределения химических звеньев в макромолекулах, а также дизайна последовательностей в синтетических сополимерах с целью достижения необходимых функциональных свойств образующихся полиэлектролитов.
Известны поличетвертичные аммониевые соли на основе мономеров ряда ДАА в кватернизованной форме - четвертичных солей ряда N,N-диаллил-N,N-диалкиламмония (ДАДАА). Эти мономеры сравнительно легко полимеризуются под действием химических радикальных инициаторов с образованием высокомолекулярных катионных полиэлектролитов [1, 2].
Однако в полимерах, полученных на основе мономеров ряда ДАДАА, отсутствуют функциональные группы, способные к различного рода модификациям.
Представляют интерес мономеры ряда ДАА и сам ДАА. В этих мономерах и полимерах на их основе заложены хорошие возможности для химической модификации.
Предпринятые ранее попытки осуществить процессы радикальной полимеризации аллильных и диаллильных соединений не имели успеха. Это обусловлено реакцией деградационной передачи цепи на мономер, сопровождающейся отрывом подвижного атома α-водорода аллильной группы мономера радикалами, что приводит к образованию малореакционноспособных аллильных радикалов передачи, кинетическому обрыву цепи и получению только низкомолекулярных олигомерных продуктов (схема 1) [3-10].
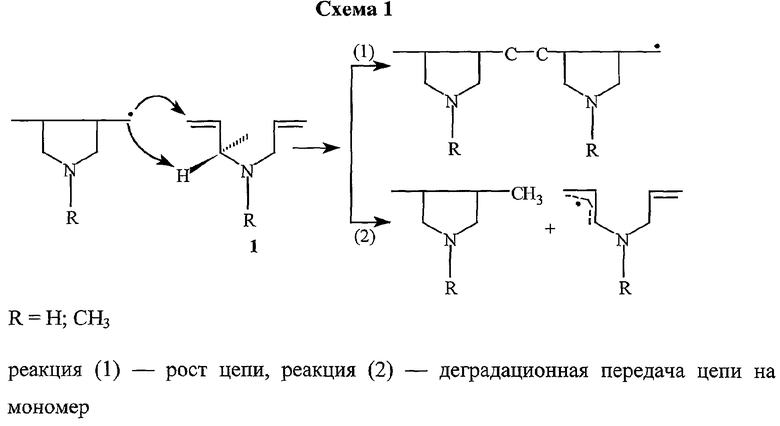
Ранее было показано, что скорость полимеризации аллильных и диаллильных соединений заметно возрастает в комплексообразующих и кислых средах, увеличиваясь с ростом протонодонорных свойств кислоты-растворителя и основности мономеров [5-10]. При этом в ряде случаев деградационная передача цепи на мономер может частично трансформироваться в эффективную передачу [6, 7, 10].
Тем не менее, никому из вышеуказанных авторов не удалось преодолеть изложенные принципиальные трудности и получить достаточно высокомолекулярные продукты.
Например, при полимеризации гидрохлорида ДАМА (мономерная соль ДАМА·HCl) под действием γ-излучения и термического инициирования (30 и 65°С) средневесовая степень полимеризации (n) полимерных солей составила не более 4-12 [11].
В работе [12] получены полимерные соли - гидрохлориды поли(диаллилалкиламмония) с рядом алкильных заместителей, включая СН3, но нет сведений о величинах их молекулярных масс, приводятся только значения характеристических вязкостей полимеров. В той же работе сообщается о получении полиоснования полидиаллилметиламин путем выделения из полимеризационной смеси в результате полимеризации мономерной соли (ДАМА·HCl), однако не даны значения его характеристической вязкости и молекулярной массы.
В литературе приводятся данные 13С ЯМР спектральных исследований полиоснования полидиаллилметиламин со степенью полимеризации n=20 [13], также полученного путем выделения из полимеризационной смеси в результате полимеризации мономерной соли (ДАМА·HCl).
Авторам предлагаемого изобретения удалось обнаружить неизвестные ранее мономерные системы, представляющие собой эквимолекулярные трифторацетатные соли мономеров ряда ДАА (ДАМА·ТФК и ДАА·ТФК), и впервые синтезировать их по специально разработанной методике.
Структура полученных мономерных систем подтверждена элементным анализом, спектрами 1Н ЯМР и термограммами ДСК (метод дифференциальной сканирующей калориметрии) (фиг.1).
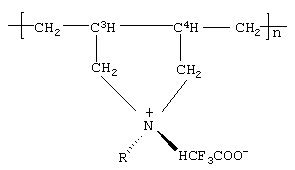
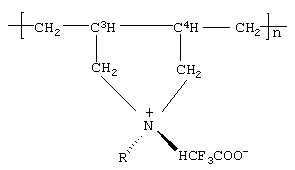
На основе указанных новых мономерных систем были впервые синтезированы полидиаллиламины общей формулы:
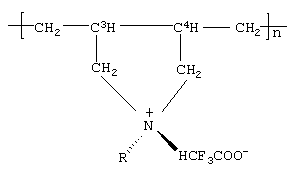
где R=H; СН3;
n=107-308 (средневесовая степень полимеризации);
ММ=24000-65000 г/моль (средневесовая молекулярная масса);
ширина молекулярно-массового распределения δ=1,85.
Эти высокомолекулярные соединения представляют собой третичные и вторичные полидиаллиламины, а именно трифторацетатные соли ряда поли(диаллиламинов) - поли(ДАМАТФК) и поли(ДААТФК). Растворимость мономеров и полимеров приведена в таблице 1. Структура синтезированных полимеров установлена на основе данных элементного анализа и спектров 1H и 13С ЯМР. В соответствии с анализом содержания фтора, одно мономерное звено полисолей поли(ДАМАТФК) и поли(ДААТФК) содержит одну молекулу ТФК. Сравнение относительных интенсивностей сигналов пар атомов С(3,4), приписываемых цис-транс-замещенным пирролидиновым кольцам полимера поли(ДАМАТФК), показывает, что отношение цис:транс составляет приблизительно 5:1 в соответствии с данными [13], а также [1] для поли(N,N-диаллил-N-диметидаммонийхлорида) (поли(ДАДМАХ)).
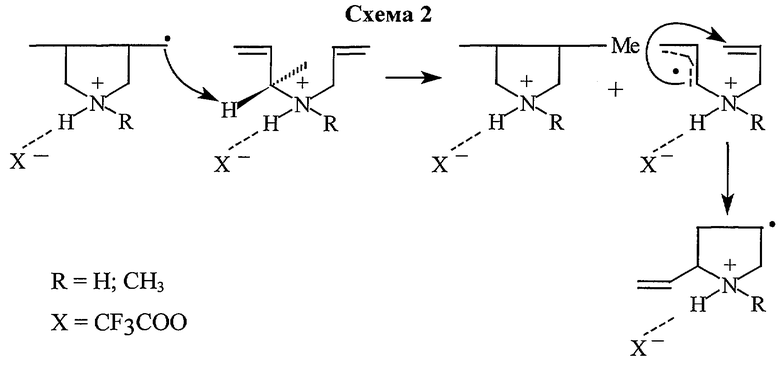
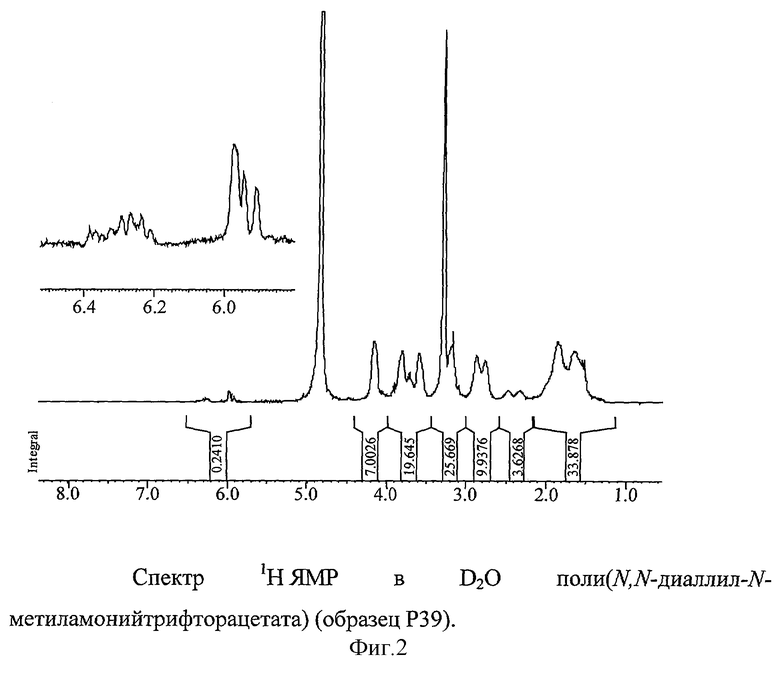
По данным спектров 1Н и 13С ЯМР полимерные соли поли(ДАМАТФК) и поли(ДААТФК) имеют концевые винильные группы (область 5.9-6.4 м.д.) и группы СН3 (1.25 м.д., регистрируется наиболее отчетливо в спектре полимера поли(ДААТФК)) (фиг.2). (Эти сигналы не исчезают при повторном переосаждении образцов Et2O и наблюдаются после двухлетнего хранения образцов). Присутствие указанных сигналов свидетельствует о том, что в описываемых процессах в ходе передачи цепи на мономер генерируются активные радикалы роста, т.е. деградационная передача цепи на мономер трансформируется в эффективную передачу цепи (схема 2).
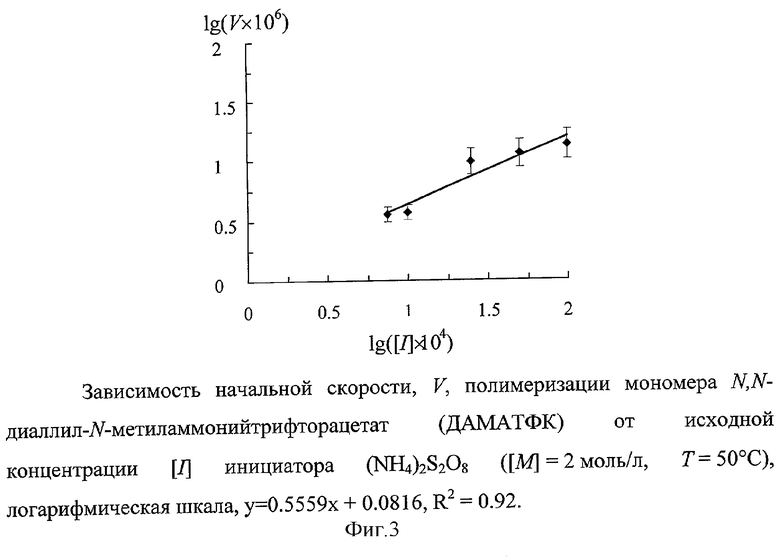
Установленный половинный кинетический порядок реакции полимеризации по инициатору (˜0.5) свидетельствует о бимолекулярном механизме обрыва цепей (фиг.3). Следовательно, в данной системе акты деградационной передачи цепи на мономер, присущие аллильным соединениям, не обнаруживаются, а передача цепи становится эффективной. Это подтверждает вывод, сделанный на основе спектров 1Н ЯМР полисолей поли(ДАМАТФК) и поли(ДААТФК).
Полученные результаты свидетельствуют о том, что в ходе полимеризации молекулы мономеров, радикалов роста и передачи цепи находятся в протонированной форме, благодаря чему в предложенных полимеризационных системах устранены все явления деградационной передачи цепи на мономер, свойственные аллильным мономерам. Это согласуется с данными предварительных 1Н ЯМР исследований растворов мономерных систем, в которых показано, что в растворах найденных мономерных систем сами мономеры находятся преимущественно в протонированной форме. Факт протонирования подтверждается характерным существенным сдвигом в слабое поле сигналов протонов групп N-СН3 и α-СН2 в спектрах 1H ЯМР растворов различной концентрации в Ме2СО-d6 мономерных солей и эквимолекулярной смеси диаллилметиламина с трифторуксусной кислотой (табл.2).
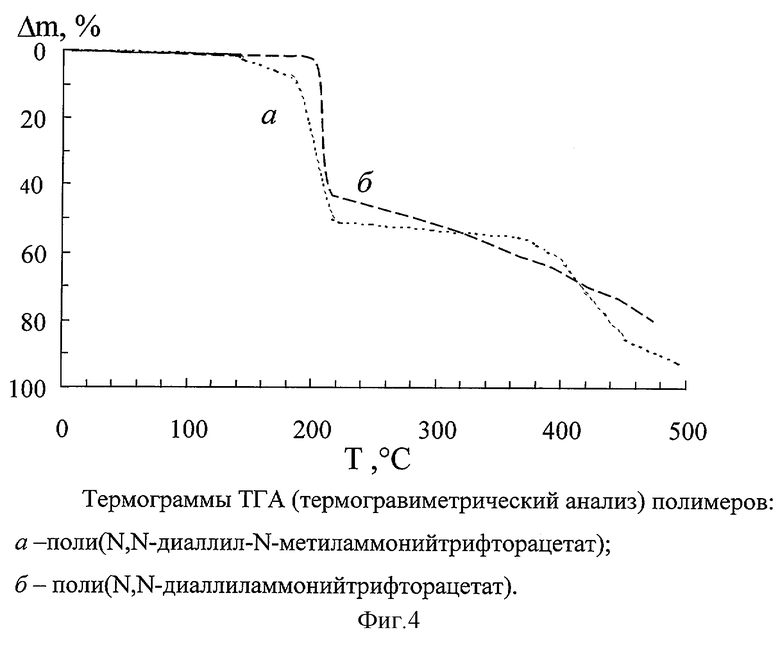
В табл. 3 приводятся вязкостные и молекулярно-массовые характеристики полимеров (значения средневесовых молекулярных масс (MW) определены седиментационным ультрацентрифугированием по методам Арчибальда и скоростной седиментации). Найденные эмпирические константы К и α для пары поли(ДАМАТФК) - растворитель составляют: α=0.54, К=6.87·10-4. Ширина молекулярно-массового распределения составляет: δ=PW/PN≈1.85 (PW и PN - соответственно средневесовая и среднечисловая степени полимеризации). Для оценки величины PN сравнивают интенсивность сигналов протонов концевой винильной группы с суммой интенсивностей сигналов протонов макроцепи в спектрах 1Н ЯМР (см. фиг.2). На фиг.4 представлены результаты исследований методом термогравиметрического анализа, ТГА, термофизических свойств новых полимеров, свидетельствующие о термической стабильности этих полимеров до 180°С.
Константы передачи цепи на мономер, CМ, полученные с помощью уравнения Майо, даны в табл.4. Относительно низкие значения CM по сравнению с полимеризацией аллильных соединений и близкие по величине к константам передачи цепи для полимеризации четвертичных солей ряда ДАДАА (см. табл.4) указывают на принципиальную возможность получения полимеров с высокими значениями MW на основе мономеров ряда ДАА в некватернизованной форме. Величины n (107-308) превосходят на один-три порядка значения, полученные ранее. Так, в указанной ранее работе [11] для образцов полисоли, синтезированной из гидрохлорида ДАМА, величины n составляют 4-12. По нашему мнению, достигнутые результаты открывают возможность для получения семейства новых высокомолекулярных полидиаллиламинов на основе мономеров ряда ДАА, а также ряда аллиламина в некватернизованной форме, обладающих широкими возможностями для химической модификации.
Синтез полимеров осуществляют радикальной полимеризацией смеси ДАМА-ТФК, солей ДАМА·ТФК и ДАА·ТФК в водных растворах в условиях термического (30 и 50°С) и фото-инициирования (20°С) в присутствии химического радикального инициатора (NH4)2S2O8 (ПСА). Конкретные детали процессов получения и выделения полимеров описаны в примерах 1-4.
В качестве иллюстрации приводятся следующие примеры.
Получение новых мономеров
Пример 1. N,N-Диаллил-N-метиламмонийтрифторацетат (ДАМА·ТФК)
К раствору 29.64 г (0.26 моля) ТФК в 200 мл абс. гексана при -5-0°С в токе Ar в течение 1 ч при интенсивном перемешивании добавляют 28.86 г (0.26 моля) ДАМА. Выпавшую в виде слегка желтоватого масла соль ДАМА·ТФК дважды промывают гексаном. Остаток растворителя удаляют на роторном испарителе. Продукт очищают осаждением гексаном из раствора в МеОН. Выход 49.73 г (85%). Состав и структура подтверждены элементным анализом и спектром 1H ЯМР. (C9H14NO2F3) (225.2): Вычислено (%): С 48.00, Н 6.22, N 6.22, F 25.33. Найдено (%): С 47.75, Н 6.08, N 6.79, F 26.03. 1Н ЯМР (1.13 мол·л-1; Ме2СО-d6): δ=2.78 (с, 3Н, CH3N), 3.80 (д, 4Н, 2α-СН2, J=6.96 Гц), 5.53 (м, 4Н, 2γ-СН2), 6.03 (м, 2Н, 2β-СН). Синтезированная соль ДАМА·ТФК представляет собой при комнатной температуре прозрачную маслянистую жидкость, что подтверждается термограммой, полученной методом дифференциальной сканирующей калориметрии, ДСК (фиг.1, а). Температура плавления: Тпл=6.4°С.
Пример 2. N,N-Диаллиламмонийтрифторацетат (ДАА·ТФК)
Получают по методике для ДАМА·ТФК, добавляя к 29.64 г (0.26 моля) ТФК 25.22 г (0.26 моля) ДАА. Выход 48.83 г (89%). Состав и структура подтверждены элементным анализом и спектром 1Н ЯМР. (C8H12NO2F3) (211.09): Вычислено (%): С 45.52, Н 5.69, N 6.63, F 26.99. Найдено (%): С 45.33, Н 5.51, N 6.64, F 27.27. 1Н ЯМР (1.13 моль·л-1, Ме2СО-d6, δ, м.д.): 3.71 (д, 4Н, J=6.43 Гц, 2α-СН2); 5.47 (м, 4Н, 2γ-СН2); 6.00 (м, 2Н, 2β-СН). Полученная соль представляет собой при комнатной температуре белые кристаллы. Термограмма ДСК дана на фиг.1, б. Тпл=57.5°С.
Получение новых полимеров
Пример 3. Поли(N,N-диаллил-N-метиламмонийтрифторацетат).
Приготовление полимеризационного раствора из мономерной смеси (ДАМА-ТФК): в пикнометр, частично заполненный дистиллированной Н2О, добавляют 22.8 г (0.2 моля) ТФК, 22.2 г (0.2 моля) ДАМА и 11.35·10-2 г (4.98·10-4 моля) инициатора ПСА, доводя до объема 100 мл. Приготовление полимеризационного раствора из мономерной соли ДАМА·ТФК: в пикнометре объемом 100 мл к 45.00 г (0.2 молям) ДАМА·ТФК добавляют 11.35·10-2 г (4.98·10-4 моля) ПСА и дистиллированную Н2О. Полученный раствор помещают в ампулу, дегазируют на вакуумной установке при замораживании жидким N2, запаивают и термостатируют. При фотоинициировании дегазированный раствор помещают в токе Ar в кварцевый реактор и облучают полным светом лампы ДРШ-250 (излучение: λ=200-400 нм и видимая область спектра, поглощение λmax=240 нм, время облучения указано в табл.3). Полимер высаживают в Et2O. Очищают переосаждением Et2O из раствора в МеОН. Образец Р41: выход 3.78 г (8.4%). (4). (C9H14NO2F3)n (225.2)n: Вычислено (%): С 48.00, Н 6.22, N 6.22, F 25.33; Найдено (%): С 47.00, Н 6.07, N 6.12, F 25.03. Мη=27000 (см. табл.4). Выделенная полисоль поли(ДАМАТФК) представляет собой желтоватое твердое вещество.
Пример 4. Поли(N,N-диаллиламмонийтрифторацетат).
Приготовление исходных растворов и полимеризацию проводят по методикам, приведенным для синтеза поли(ДАМАТФК). Приготовление полимеризационного раствора из мономерной соли ДАА·ТФК: к 63.3 г (0.3 моля) ДАА·ТФК добавляют 0.023 г (1.0·10-4 моля) ПСА и дистиллированную Н2О. Затем содержимое переносят в пикнометр и доливают Н2О до объема 100 мл. Образец Р49: выход 2.66 г (4.2%). (C8H12NO2F3)n (211.09)n: Вычислено (%): С 45.52, Н 5.69, N 6.63, F 26.99. Найдено (%): С 45.47, Н 5.57, N 6.61, F 26.84. MW=65000 (см. табл.4). Выделенная полисоль поли(ДААТФК) представляет собой желтоватое твердое вещество.
Синтезированные полиамины обладают бактерицидной и фунгицидной активностью и могут быть использованы в области синтеза новых дезинфицирующих средств (ДС).
Для профилактики инфекционных заболеваний практика здравоохранения нуждается в эффективных ДС с широким спектром антимикробной активности. Существующая в настоящее время сложная эпидемиологическая ситуация (высокий уровень заболеваемости вирусными и бактериальными инфекциями, появление новых и возвращение старых инфекций, формирование полирезистентных штаммов возбудителей инфекций, прецеденты биотерроризма) обосновывают рост требований к ДС и стимулирует поиск новых препаратов, обладающих бактериологической активностью.
На сегодняшний день существует большое количество ДС на основе различных активно действующих веществ. На основании данных научной литературы и анализа ассортимента ДС показано, что наиболее широкое распространение получили четвертичные аммониевые соединения (ЧАС), амины, производные гуанидина и как самостоятельные действующие вещества и как композиционные препараты [15, с.45]. Более 35% ДС составляют ЧАС, из которых получены, наиболее изучены и используются около 30 активных соединений [15, с.187-189]. ЧАС проявляют умеренную биоцидную активность. Противомикробная активность ЧАС зависит от типа заместителей у атома азота, длины углеродной цепи радикала, степени его насыщенности и разветвленности, наличия гидроксильных, эфирных групп и т.п. Соединения, содержащие у атома четвертичного азота радикалы с С<8 лишены или проявляют умеренные противомикробные свойства [15, с.187-189].
К поличетвертичным аммониевым солям, практически лишенным бактерицидной и фунгицидной активности, относится и наиболее близкий по структуре прототип синтезированных авторами третичных и вторичных полидиаллиламинов, упоминаемый выше полимер поли(ДАДМАХ), содержащий атом четвертичного азота в пятичленном цикле мономерного звена [16].
Широкое распространение получили также препараты класса полигуанидинов, в частности полигексаметиленгуанидин (ПГМГ) [17]. Антимикробное действие производных гуанидина известно давно, гуанидиновые антисептики широко применяются в мире, поскольку они значительно эффективнее ЧАС, поверхностно-активных веществ (ПАВ), производных фенола и хлорактивных дезинфицирующих препаратов, стабильны и неагрессивны, не образуют токсичных продуктов, не инактивируются белками, биоразлагаемы.
В России ДС подобного класса производят заводским способом в виде ПГМГ хлорида («метацид») и ПГМГ фосфата («фогуцид») [17]. Нужно отметить, что довольно длительное их применение привело к значительному снижению эффекта биологической активности в большинстве случаев.
В последнее время стали производить препараты, созданные на основе N,N-бис(3-аминопропил)додециламина, «Lonzabac 12-100» (Лонзабак) швейцарской фирмы «Lonza», обладающего широким спектром биоцидной активности [15, с.155, 166]. Наличие гидрофобной алифатической цепи и гидрофильных полярных аминогрупп в структуре третичного алкиламина Лонзабак позволяет ему в зависимости от рН среды проявлять характерные признаки как аминов, так и ЧАС. Данные свойства третичных алкиламинов дают возможность существенно расширить спектр их биоцидной активности. Однако фунгицидная активность препарата незначительна, что является весьма отрицательным фактором, учитывая широкое распространение грибковых инфекций в последние годы. Кроме того, Лонзабак является дорогостоящим препаратом, который производится за рубежом.
За последние 10 лет не появилось ни одного принципиально нового химического соединения, обладающего антимикробной активностью, и большинство ДС являются многокомпонентными композициями [15, с.45], в то время как микроорганизмы обладают способностью со временем вырабатывать устойчивость к ряду из них, в том числе к ЧАС, ПГМГ, Лонзабаку, хлорсодержащим и др.
Поэтому поиск новых субстанций и препаратов, позволяющих расширить ряд ДС, всегда является актуальной задачей.
Поставленная задача решается тем, что дезинфицирующее средство, включающее активную составляющую и растворитель - воду, в качестве активной составляющей содержит полидиаллиламины общей формулы:
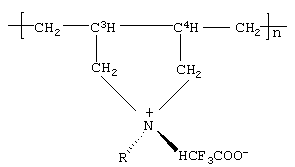
где R-H; R=СН3;
n=107-308 (средневесовая степень полимеризации);
ММ=24000-65000 г/моль (средневесовая молекулярная масса);
ширина молекулярно-массового распределения δ=1.85;
при минимальной подавляющей концентрации от 1.25·10-4 г/мл до 1.5·10-6 г/мл.
Преимущественное использование полиаминов с ММ от 55000 до 65000 г/моль позволяет снизить минимальную подавляющую концентрацию: от 1.5·10-5 г/мл до 1.5·10-6 г/мл.
Испытания антибактериальной активности синтезированных полиаминов проводят на следующих образцах:
- поли(диаллиламмонийтрифторацетат) с MW 65000 г/моль;
- поли(диаллиламмонийтрифторацетат) с MW 24000 г/моль;
- поли(диаллилметиламмонийтрифторацетат) с MW 55000 г/моль;
- поли(диаллилметиламмонийтрифторацетат) с MW 24000 г/моль;
- мономер диаллиламмонийтрифторацетат;
- мономер диаллилметиламмонийтрифторацетат;
- трифторуксусная кислота;
в отношении трех видов микроорганизмов: кишечной палочки (E.coli ATCC 25922), золотистого стафилококка (S.aureus ATCC 6538P) и гриба рода кандида (C.albicans 865-653) из международной коллекции штаммов (ГИСК им. Тарасовича МЗ РФ).
Все исследования осуществляют методом, рекомендованным НИИ дезинфекции и стерилизации (Методические рекомендации, 1968 г.)
Подлежащие изучению тест-образцы разводят в дистиллированной воде методом двукратных серийных разведений до исходных концентраций каждого - 0,1% (10-3 г/мл). Каждый испытуемый образец подлежит одинаковому разведению в 30 пробирках (по 1 мл каждая) - всего 15 рядов. Каждый из трех рядов, содержащий 10 разных концентраций одного и того же образца, засевают 0,1 мл из упомянутых выше тест-штаммов. Суспензии из каждого тест-штамма готовят по оптическому стандарту №10 (ГИСК им. Тарасовича). Тест-культуры вносят в опытные и контрольные пробирки (контрольные пробирки содержат 1 мл дистиллированной воды и 0,1 мл тест-культуры). Затем все пробирки с различными разведениями исследуемых образцов с внесенными в них тест-микробами оставляют на 1,5 часа при комнатной температуре. Затем производят высевы тест-микроорганизмов из каждой опытной и контрольной пробирок на следующие селективные среды, разлитые в чашки Петри:
Агар Эндо (кишечная палочка), среда Мюллер-Хинтон (стафилококк), кандида агар (грибы рода кандида).
Затем чашки с посевами тест-микробов инкубируют при температуре 37°С в течение 18 часов. На следующие сутки определяют минимальные тормозящие рост тест-микробов концентрации (в %), при которых наблюдается полное ингибирование их роста.
В табл.5 приведены данные по выявлению антибактериального действия исследуемых тест-образцов в отношении указанных выше микроорганизмов.
Минимальные подавляющие концентрации (МПК) для поли(ДААТФК) и поли(ДАМАТФК) соответственно составляют: 1.5·10-3 % (1.5·10-5 г/мл) и 7.0·10-4 % (7.0·10-6 г/мл) в отношении кишечной палочки; 1.5·10-4 % (1.5·10-6 г/мл) и 7.0·10-4 % (7.0·10-6 г/мл) в отношении золотистого стафилококка; 1.5·10-4 % (1.5·10-6 г/мл) и 3.5·10-4 % (3.5·10-6 г/мл) в отношении грибов рода кандида. Эти результаты свидетельствуют о высокой противомикробной активности этих полимеров. С уменьшением молекулярной массы полимеров (до ММ=24000, n=107 для поли(ДААТФК), n=114 для поли(ДАМАТФК)) бактерицидная активность указанных полимеров несколько уменьшается соответственно до значений МПК: 1.25·10-2 % (1.25·10-4 г/мл) и 6.2·10-3 % (6.2·10-5 г/мл) в отношении кишечной палочки; 3.1·10-4 % (3.1·10-5 г/мл) и 6.2·10-5 % (6.2·10-5 г/мл) в отношении золотистого стафилококка; однако фунгицидная активность остается высокой для обоих полимеров, МПК=3.5·10-4 % (3.5·10-6 г/мл) в отношении грибов рода кандида. Исходные мономеры и ТФК не обладают противомикробной активностью даже в концентрации 0.025% в отношении стафилококка, 0.05% в отношении кишечной палочки и грибов рода кандида, за исключением мономера ДАМАТФК, МПК которого составляет 0.05% в отношении грибов рода кандида. Эти данные указывают на определяющую роль полимерной природы описываемых соединений, содержащих пирролидиновые кольца в мономерных звеньях макроцепи, в механизме их противомикробной активности. В то же время очевидно, что для подавления роста грибов рода кандида длина полимерной цепи не является столь существенной, как для кишечной палочки и золотистого стафилококка.
Синтезированные полимеры поли(ДАМАТФК) и поли(ДААТФК) не имеют полных структурных аналогов среди известных соединений, обладающих антибактериальной активностью, и в этом смысле являются принципиально новыми химическими соединениями, обладающими высокой бактерицидной и фунгицидной активностью. Как указывалось выше, наиболее близкий по структуре аналог синтезированных полимеров - поли(ДАДМАХ) практически не обладает антибактериальной активностью и не используется в качестве ДС [16]. Так по данным профессора А.Ф.Мороз (ГУ НИИЭМ им. Н.Ф.Гамалеи), минимальная подавляющая концентрация в отношении Salmonella typhosa составила для раствора поли(ДАДМАХ) не менее 3% (3.0·10-2 г/мл). Бактерицидная и фунгицидная активность синтезированных авторами полиаминов сравнима с антибактериальной активностью наиболее эффективных ДС, представителей ряда полиаминов и аминов - ПГМГ, ПГМГ в комбинации с Лонзабак, а ряде случаев превышает ее (см. табл.5).
Полимерная природа описываемых соединений является положительным фактором с точки зрения уменьшения их токсичности и провоцирования дыхательной аллергии различного рода, создания устойчивой поверхностной пленки и т.д.
Подтверждение проведенных испытаний биологической активности приводится в прилагаемых официальных отчетах ГУ НИИЭМ им. Н.Ф.Гамалеи РАМН.
Растворимость мономеров и полимеров (р - растворимый, н - нерастворимый)
\
Химические сдвиги протонов (δ) в спектрах ЯМР 1Н и разности (Δδ=δсоль,смесь-δмономер) для групп N-CH3 и N-CH2-CH=CH2 мономеров, их смесей и солей с ТФК; растворитель Me2CO-d6 (δ=2.05 м.д.)
м.д.
Характеристическая вязкость ([η]) и молекулярно-массовые характеристики различных образцов полимерных солей, полученных полимеризацией мономеров ДАМАТФК и ДААТФК в водных растворах в условиях термического (Δ) и фотоинициирования (hν) в присутствии инициатора (NH4)2S2O8.
** Значение PN получено из спектра 1H NMR (см. текст).
*** Оценено с использованием значений РN и δ.
**** Получено методом скоростной седиментации.
Эффективные константы передачи цепи на мономер СM при полимеризации-ряда аллильных и диаллильных мономеров
Результаты испытаний антибактериальной и антигрибковой активности водных растворов тест-образцов в отношении 3-х видов микроорганизмов.
СПИСОК ЛИТЕРАТУРЫ
1. Кабанов В.А., Топчиев Д.А. // Высокомолек. соед. 1988. Т.30. №. С.675.
2. Butler G.B. Cyclopolymerization and cyclocopolymerization. New York: Marcel Dekker, 1992.
3. Bartlett P.O., Altschul R. //J. Am. Chem. Soc. 1945. V.67. №. Р.812.
4. Litt M., Eirich F.R. // J. Polym. Sci. 1960. V.45. №. P.379.
5. Щербина Ф.Ф., Федорова И.И., Горлов Ю.И. // Высокомолек. соед. А. 1970. Т.12. №. С.2042.
6. Зубов В.П., Гарина Е.С., Корнильева В.Ф., Мастерова М.Н., Кабанов В.А., Полак Л.С. // Высокомолек. соед. А. 1973. Т.15. №. С.100.
7. Мастерова М.Н., Андреева Л.И., Зубов В.П., Полак Л.С., Кабанов В.А. // Высокомолек. соед. А. 1976. Т.48. №. С.1957.
8. Крейндель М.Я., Андреева Л.И., Каплан А.М., Голубев В.Б., Мастерова М.Н., Зубов В.П., Полак Л.С., Кабанов В.А. // Высокомолек. соед. А. 1976. Т.18. №. С.2233.
9. Маддукури Виджая Кумар, Мастерова М.Н., Голубев В.Б., Зубов В.П., Кабанов В.А.// Вестн. Моск. Ун-та. Сер.2. Химия. 1979. Т.20. №. С.490.
10. Zubov V.P., Vijaya Kumar M., Masterova M.N., Kabanov V.A. //J. Macromol. Sci.-Chem. 1979. V.A13. №. P.111.
11. Jakson M.B. // J. Macromol. Sci.-Chem. 1976. V.A10, №. P.959.
12.Negi Y., Harada S., Ishizuka O. // J. Polymer Sci. A-1. 1967. V.5. P.1951.
13. Johns S.R., Willing R.I., Middleton S., Ong A.K. // J. Macromol. Sci-Chem. 1976. V.A10. №5. P.875.
14. Топчиев Д.А., Нажметдинова Г.Т., Крапивин А.М., Шрейдер В.А., Кабанов В.А. // Высокомолек. соед. 1982. Т.24. №. С.473.
15. Задачи современной дезинфектологии и пути их решения. Материалы Всероссийской научной конференции. 22-24 октября 2003.
16. Merianos J.J. Disinfection, Sterilization, and Preservation. 4th ed. Ed. Seymour S.B. Philadelphia. 1991. Chapter 13.
17. Гембицкий П.А., Топчиев Д.А., Воинцева И.И. Полигексаметиленгуанидин. Синтез, химические превращения, биоцидные свойства и область применения. Обзор.
Изобретение относится к области синтеза новых полиэлектролитов катионного типа на основе трифторацетатов диаллиламинов - мономеров ряда N,N-диаллиламина (ДАА) (самого мономера ДАА и N,N-диаллил-N-метиламина (ДАМА)) и может быть использовано в различных областях народного хозяйства и, в частности, медицине. Описаны полидиаллиламины общей формулы:
где R=H; СН3; n=107-308; (средневесовая степень полимеризации); ММ=24000-65000 г/моль (средневесовая молекулярная масса); ширина молекулярно-массового распределения δ=1,85; водный раствор которых может быть использован в качестве дезинфицирующего средства при минимальной подавляющей концентрации от 1.25·10-4 г/мл до 1.5·10-6 г/мл. 2 н.п. ф-лы, 5 табл., 4 ил.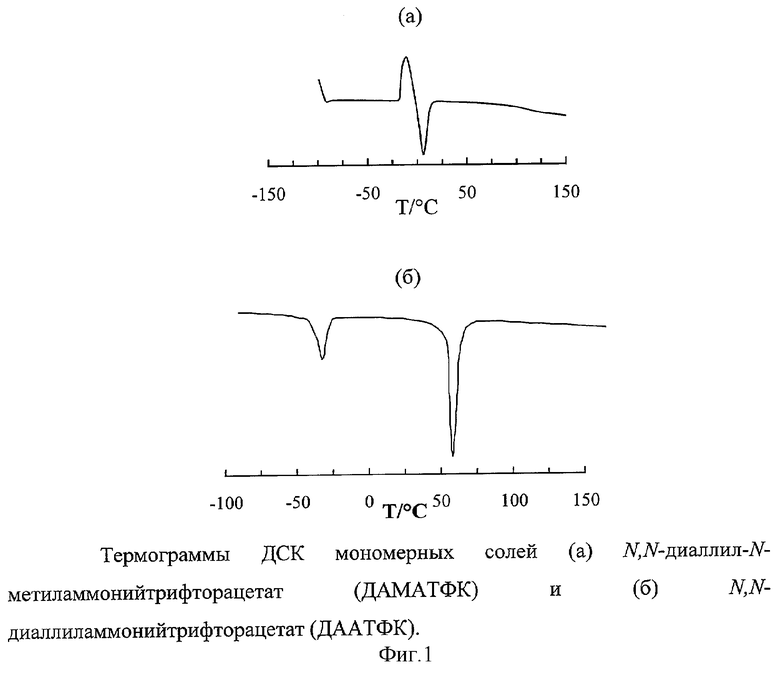
где R=H; СН3;
n=107-308 (средневесовая степень полимеризации);
ММ=24000-65000 г/моль (средневесовая молекулярная масса);
ширина молекулярно-массового распределения δ=1,85.

где R=H; СН3;
n=107-308 (средневесовая степень полимеризации);
ММ=24000-65000 г/моль (средневесовая молекулярная масса);
ширина молекулярно-массового распределения δ=1,85,
при минимальной подавляющей концентрации от 1,25·10-4 до 1,5·10-6 г/мл.
Авторы
Даты
2006-03-20—Публикация
2004-09-28—Подача