Изобретение относится к фармакологии, а именно к получению биологически активных соединений хлоринового ряда (см. обзор: E.S.Nyman, P.H.Hynninen, J. Photochem. Photobiol. В: Biology, Vol.73, pp. 1-28 (2004). Reserch advances in the of tetrapyrrolic photosensitizers for photodynamic therapy.). Изобретение может быть использовано для получения солей эфиров моноамида хлорина е6 общей формулы (1), которые могут найти применение в качестве высокоэффективных фотосенсибилизаторов (далее - ФС) для фотодинамической терапии рака и других новообразований различного генезиса, а также флюоресцентной диагностики раковых клеток.
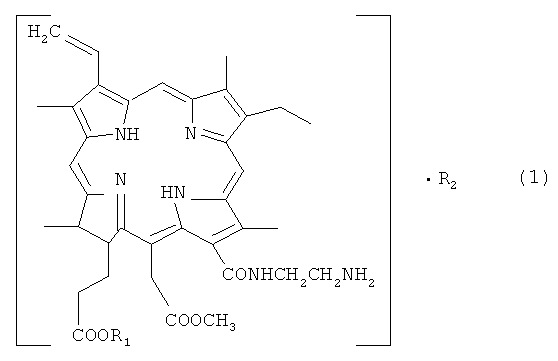
Например, могут быть получены такие производные моноамида хлорина е6 общей формулы (1) как адипинаты моноамида эфира хлорина е6 (рис.1 - показан частный случай общей формулы (1) для соли двухосновной адипиновой кислоты).
Рис 1.

I, R=Me; Et
Таким образом могут быть получены соли одноосновных кислот, например уксусной или пировиноградной, двухосновных, например адипиновой или щавелевой, или трехосновных, например лимонной или хвощевой. Эти соединения могут быть использованы в тех же случаях, в каких применяются известные фотосенсибилизаторы, препараты разрешенные для применения в России, основу которых составляют соли хлорина е6 (рис.2),
Рис.2.

C34H36N4O6
MW 596.68
или же NPE6 (аспартилхлорин е6) (рис.3),
Рис. 3.
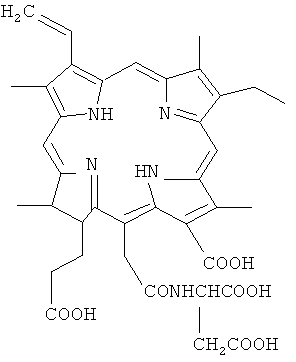
C38H41N5O9
MW 711.77
поскольку они все являются производными одного и того же макроцикла - хлорина е6 и поэтому имеют сходные спектральные характеристики (основная полоса поглощения при 662 нм в спирте и других органических средах и спектры флюоресценции), так и в других случаях, когда необходимо принципиально изменить биораспределение препарата в организме, поскольку предлагаемые нами ФС относятся к катионнозаряженным хлоринам. Все же известные и официально разрешенные к применению ФС в РФ (рис.2) относятся к классу водорастворимых солей (калиевых, натриевых или N-метилглюкаминовых) хлорина е6, который представляет собой трикислоту и относятся, таким образом, к анионнозаряженным ФС (см. RU 2144538, RU 2183956, RU 2276976, RU 2276976, US 6969765, US 5330741, WO 2004/089409 A3).
Моно-L-Аспартилхлорин е6 (NPE6, TALAPORFIN или LASERPHYRIN) (см. рис.3), являющийся амидным производным хлорина е6, представляет собой тетракислоту, а ее натриевые соли также прекрасно растворимы в воде (см.: Roberts, W.G., et al., In Vitro Characterization of Monoaspartyl Chlorin e6 and Diaspartyl Chlorin e6 for Photodynamic Therapy, J. Nat'l. Can. Inst., 80:330-336(1988).
Характерной особенностью хлорина е6 является тот факт, что в зависимости от растворителя его спектральные характеристики сильно варьируют. Так, известно, что в водных средах его максимум поглощения смещается в коротковолновую область от 662 нм в спирте до 655 нм в водном растворе при рН 9.0 и выше.
Известно, что в раковых очагах за счет бурного роста клеток и происходит некоторое изменение рН в сторону понижения, поэтому целью настоящего изобретения было создание ФС с одной стороны, имеющего те же фотофизические характеристики, что и у известных ФС, чтобы использовать такие же лицензированные лазеры для ФДТ, а с другой - заменить отрицательный заряд на периферии хлоринового макроцикла на положительный путем введения в периферический заместитель аминогруппы с тем, чтобы изменить распределение ФС в организме и еще более увеличить тропность ФС к опухолям. При этом найденная структура дополнительно обеспечивает возможность управления распределения ФС в организме за счет сочетания различных алкилов и различных органических кислот разной основности.
Таким образом, поставленная задача была решена при синтезе производных моноамида хлорина е6 общей формулы (1),

где R1 означает линейный или разветвленный алкил, имеющий от 1 до 4 атомов углерода, R2 означает соли фармацевтически приемлемых органических кислот.
Данное вещество может быть применено в качестве фотосенсибилизатора, содержащего производные моноамида хлорина е6, которые имеют вышеуказанную общую формулу (1).
Данное вещество может быть получено следующим способом: обеспечивают взаимодействие спирта, содержащего R1, и хлорина е6 для образования эфира феофорбида хлорина е6, содержащего R1, обеспечивают взаимодействие образованного эфира с этилендиамином для образования моноамида вышеуказанного эфира, обеспечивают взаимодействие образованного моноамида с фармацевтически приемлемой органической кислотой для образования соли вышеуказанного моноамида. В настоящее время в качестве сырья, содержащего хлорин е6, целесообразно применять спирулину.
В качестве примеров осуществления выбраны в настоящее время одни из наиболее экономически целесообразных по стоимости компонентов и простоте получения.
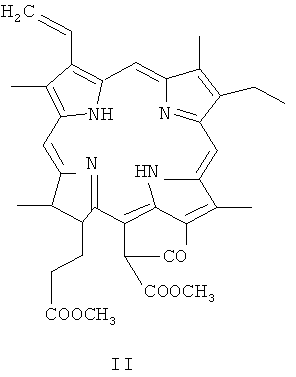
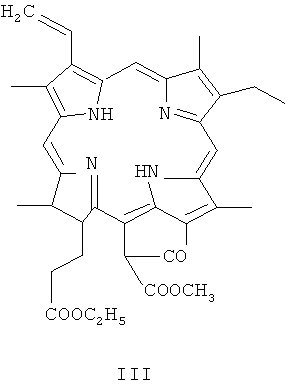
Спирулина обрабатывается метанолом или этанолом, содержащим 5-10% конц. серной кислоты при комнатной температуре в течение 12 часов, затем биомассу отфильтровывают, из фильтрата выделяют метилфеофорбид а (II) (Рис.4) или этилфеофорбид а (III) (Рис.5), который в растворе хлористого метилена, хлороформа или другого подходящего растворителя обрабатывают 0.5 г·экв свежеперегнанного этилендиамина в течение 3-4 часов при комнатной температуре до окончания реакции (спектральный и хроматографический тест), растворитель удаляют в вакууме, кристаллический остаток суспендируют в дист. воде, отфильтровывают, промывают на фильтре дист. водой до отсутствия в фильтрате щелочной реакции за счет присутствия непрореагировавшего этилендиамина, сушат в вакууме при комнатной температуре и получают соответствующий метиловый эфир амида - моноэтилендиаминмоноамид хлорина е6 (IV) (Рис.6). Аналогичным образом получают соответствующий этиловый эфир (V) (Рис.7) исходя из этилфеофорбида а (II) и этилендиамина с количественным выходом.
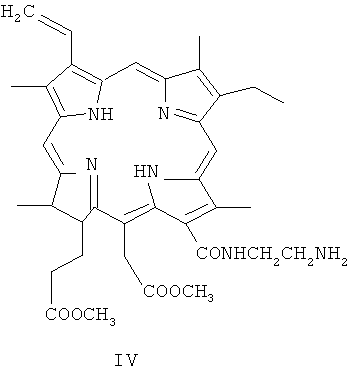
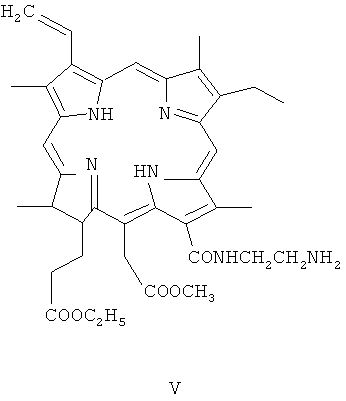
Хлоринамидамины легко растворимы в органических растворителях (хлористый метилен, хлороформ, дихлорэтан), несколько труднее в ацетоне или спирте. Эти соединения в двухфазной системе (орг. растворитель - вода) исключительно легко переходят в водную фазу при ее подкислении за счет образования трикатиона хлоринамидов.
Все известные ФС на основе хлорина е6 для внутривенного использования представляют собой или водные растворы (концентрация ~30 мг хлорина е6 в 10 мл воды, т.е. 0,35% раствор для РАДАХЛОРИНА или 0,5% раствор для ФОТОДИТАЗИНА с последующим разведением до 100 мл), или приготовленный раствор порошка 100 мг тринатриевой соли хлорина е6 совместно с поливинилпирролидоном в 100 мл воды. Таким образом, концентрация ФС, рассчитанная по содержанию хлорина е6, в инъекционном растворе не превышает 0,3-1,0 мг/мл.
Для получения ФС (I, R=Me, Et) исходя из соединений IV и V (рис.6) и (рис.7) поступают следующим образом: растворяют 30 мг хлорина IV или V в 5 мл этанола ректификата, добавляют 5 мл апирогенной воды, фильтруют через миллипоры 0,22 ммк, доводят водой общий инъекционный объем до 100 мл и используют по назначению.
Среди многочисленных производных хлорина е6 и мезохлорина е6, испытанных в качестве потенциальных ФС для ФДТ, известны два моноамида с этилендиамином (соединения VI и VII, рис.8 и рис.9), однако они не отличались какими-либо заметными положительными свойствами от традиционного хлорина е6 и поэтому не использовались в дальнейшем для разработки практически важного лекарственного препарата на их основе. Синтез соединений VI и VII осуществлялся исходя из феофорбида а (или мезофеофорбида а) или непосредственно из хлорина е6 (мезохлорина е6). Наличие у соединений VI и VII карбоксильных групп сводило на нет влияние аминогруппы, т.к. образование цвиттерионной структуры в значительной степени затрудняло выделение данных амидов, благодаря их растворимости как в кислой, так и в щелочной водной среде.
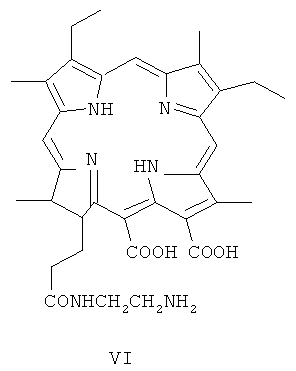

Преимущества при получении хлоринамидоаминов IV и V по сравнению с известными ФС на основе солей хлорина е6 заключаются в следующем:
1. Раскрытие циклопентанового экзоцикла в алкилфеофорбиде а до производных хлорина е6 с помощью этилендиамина происходит в мягких условиях и с количественным выходом, по сравнению с использованием водной щелочи для реакций традиционного превращения феофорбидов а в хлорин е6;
2. В процессе получения амидохлоринов отсутствуют процессы деградации хлоринов до смеси других производных (например, пурпурина, хлорина е4 и др. (см. ссылку из http://www.sciencedirect.com/ поиск на chlorin е6 Н.А.Isakau, T.V.Trukhacheva and P.T.Petrov Isolation and identification of impurities in chlorin е6 Journal of Pharmaceutical and Biomedical Analysis, In Press, Corrected Proof, Available online 24 May 2007, или патент RU 2183956).
3. Получение амидохлоринов исходя из алкилфеофорбида а легко поддается масштабированию до нескольких десятков грамм в обычной химической лаборатории без привлечения специального и дорогостоящего оборудования по сравнению с синтезом хлорина е6, получение которого требует проведения реакции в условиях, максимально защищенных от действия кислорода воздуха, использования относительно больших объемов водных растворов на 1 г сырья, применения многократного промывания большими объемами апирогенной водой осадка хлорина е6 от сопутствующих примесей с последующим центрифугированием.
4. Устойчивость фотосенсибилизаторов, приготовленных из амидохлоринов при хранении значительно выше, чем фотосенсибилизаторов на основе солей хлорина е6, что весьма существенно при создании лекформ.
5. Для повышения растворимости амидохлоринов в водно-спиртовых растворах при создании инъекционных форм ФС взаимодействием с органическими кислотами получены соответствующие соли, которые устойчивы в сухом виде или водно-спиртовых растворах при хранении.
Пример 1. К суспензии 100 г лиофильно высушенной спирулины в 300 мл метанола приливают при интенсивном перемешивании 30 мл конц. серной кислоты в течение 5 минут, перемешивают 12 часов, биомассу спирулины отфильтровывают на стеклянном фильтре № 2, промывают биомассу на фильтре 100 мл метанола, объединенный фильтрат упаривают в вакууме до половины объема, разбавляют дист. водой до 500 мл, нейтрализуют при охлаждении до 10-15°С водным 10%-ным раствором щелочи (КОН или NaOH), выпавший осадок отфильтровывают через слой 2 см целита на стеклянном фильтре (D 9 см), промывают горячей водой до отсутствия в фильтрате неорганических солей, сушат на воздухе, целит промывают петролейным эфиром или гексаном от жирорастворимых примесей, и затем продукт извлекают смесью хлористого метилена-ацетона (10:1), упаривают досуха, хроматографируют на колонке с силикагелем, фракцию, содержащую метилфеофорбид а упаривают в вакууме досуха, добавляют раствор 1 мл свежеперегнанного этилендиамина в 20 мл хлористого метилена, перемешивают 2 часа, к раствору добавляют 50 мл воды, встряхивают, органический слой отделяют, промывают водой еще 2 раза до полного извлечения непрореагировавшего этилендиамина, органический слой отделяют, упаривают, хроматографируют на колонке с силикагелем в системе хлористый метилен-метанол (95:5), основную фракцию отделяют, упаривают и получают 350 мг 18-аминоэтилкарбамоил-20-метоксикарбонилметил-8-этенил-13-этил-2,3-дигидро-3,7,12,17-тетраметил-21Н,23Н-2-(2-метоксикарбонилэтил) порфина (IV).
Пример 2. Аналогично, из 100 г лиофильно высушенной спирулины и 300 мл абс. спирта получают 230 мг 18-аминоэтилкарбамоил-20-метоксикарбонилметил-8-этенил-13-этил-2,3-дигидро-3,7,12,17-тетраметил-21Н,23Н-2-(2-этоксикарбонилэтил)порфина(V).
Пример 3. Смесь 250 мг метилфеофорбида а и 0.5 мл этилендиамина в 15 мл хлористого метилена выдерживают при перемешивании 3 часа и выделяют 270 мг хлорина IV.
Пример 4. Аналогично из 250 мг этилфеофорбида а и 0.5 мл этилендиамина получают 220 мг хлорина V.
Пример 5. К раствору 50 мг хлорина IV в 10 мл смеси хлористый метилен-этанол (1:1) приливают рассчитанное количество 13 мг (1 г·-экв) адипиновой кислоты в 5 мл этанола, раствор упаривают досуха в вакууме и получают соль - адипинат IV (1, R=Me).
Пример 6. Аналогично из хлорина V получают соль - адипинат V (1, R=Et).
Уровень техники:
RU 2144538 (от 2000.01.20) Способ получения водорастворимых хлоринов;
RU 2183956 (от 2002.06.27) Фотосенсибилизатор и способ его получения;
US 6969765 (2005-11-29) Photosensitizer and method for production thereof;
US 5330741 (1994-07-19) Long-wavelength water soluble chlorin photosensitizers useful for photodynamic therapy and diagnosis of tumors;
RU 2276976 (от 2006.02.10) Фотосенсибилизатор и метод его получения;
RU 2152790 (от 2000.07.20) Агент для фотодинамической диагностики и терапии онкологических заболеваний;
WO 2004/089409 A3 (2004.10.21) Agent for the photodynamic diagnosis and therapy of malignant tumors.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРИНА e6 | 2006 |
|
RU2330037C1 |
| ФОТОСЕНСИБИЛИЗАТОР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2367434C1 |
| ФОТОСЕНСИБИЛИЗАТОР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2004 |
|
RU2276976C2 |
| ФОТОСЕНСИБИЛИЗАТОР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2523380C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ВНУТРИГЛАЗНЫХ НОВООБРАЗОВАНИЙ | 2011 |
|
RU2467777C1 |
| ФОТОСЕНСИБИЛИЗАТОР ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2013 |
|
RU2548726C2 |
| ФОТОСЕНСИБИЛИЗАТОР ДЛЯ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2017 |
|
RU2646477C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРАСТВОРИМЫХ ХЛОРИНОВ | 1998 |
|
RU2144538C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛФЕОФОРБИДА (А) | 2012 |
|
RU2490273C1 |
| ВЕЩЕСТВО, ОБЛАДАЮЩЕЕ АНТИГЛИОМНОЙ АКТИВНОСТЬЮ, И СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ГЛИОБЛАСТОМЫ | 2022 |
|
RU2794666C1 |
Изобретение относится к фармакологии, а именно к получению биологически активных соединений, и может быть использовано для получения солей моноамидов эфиров хлорина е6. Способ получения фотосенсибилизатора заключается в обработке суспензии лиофильно высушенной спирулины, например, в метаноле или абсолютном спирте до получения алкилфеофорбида а с взаимодействием последнего, например, с этилендиамином, предпочтительно, в органическом растворителе, выделении соответствующего эфира моноамида хлорина е 6, его растворении в спирте и добавлении, например, адипиновой кислоты в мольном соотношении 2:1. К фотосенсибилизатору, имеющему структурную формулу (1), добавляют апирогенную воду так, чтобы содержание соли хлорина составляло 30-40 мг в 10 мл смеси спирт-вода (1:1). Технический результат: замена отрицательного заряда на периферии хлоринового макроцикла на положительный путем введения в периферический заместитель аминогруппы для получения катионнозаряженных хлоринов для изменения распределения фотосенсибилизатора в организме для повышения тропности к опухолям, при этом обеспечивается дополнительная возможность управления распределением за счет сочетания различных алкилов и различных органических кислот разной основности в структурной формуле (1) посредством новой лекарственной формы, обладающей более высокими терапевтическими свойствами для лечения рака и других заболеваний методами фотодинамической терапии рака и других новообразований различного генезиса по сравнению с известными лекарственными препаратами, содержащими хлорин е6. 3 н. и 2 з.п. ф-лы, 9 ил.

1. Производные моноамида хлорина e6 общей формулы (1),
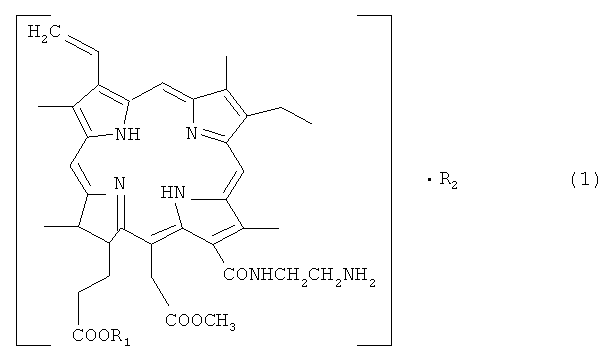
где R1 означает линейный или разветвленный алкил, имеющий от 1 до 4 атомов углерода,
R2 означает соль фармацевтически приемлемых органических кислот.
2. Фотосенсибилизатор, содержащий производные моноамида хлорина е6, отличающийся тем, что данные производные указаны в п.1.
3. Способ получения производных по п.1, характеризующийся тем, что обеспечивают взаимодействие спирта, содержащего R1, и хлорина е6 для образования эфира феофорбида хлорина е6, содержащего R1,
обеспечивают взаимодействие образованного эфира с этилендиамином для образования моноамида вышеуказанного эфира, обеспечивают взаимодействие образованного моноамида с фармацевтически приемлемой органической кислотой для образования соли вышеуказанного моноамида.
4. Способ по п.3, отличающийся тем, что в качестве сырья, содержащего хлорин е6, применяют спирулину.
5. Способ по любому из пп.3 и 4, отличающийся тем, что обеспечивают взаимодействие образованного эфира с этилендиамином в среде, содержащей спирт.
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРАСТВОРИМЫХ ХЛОРИНОВ | 1998 |
|
RU2144538C1 |
| US 5002962 А, 26.03.1991 | |||
| US 5330741 A, 19.07.1994 | |||
| ROBERTS W.G | |||
| et al // J.Nat`l | |||
| Can | |||
| Inst., v.80, p.330-336 (1988). | |||
Авторы
Даты
2011-04-20—Публикация
2007-12-05—Подача