Область техники
Данное изобретение относится к новым способам получения фторированных органических соединений газофазным методом. В частности, данное изобретение относится к способам получения фторированных алканов, фторированных алкенов и фторуглеводородных полимеров газофазным методом.
Уровень техники
Фторированные углеводороды (HFC's), в частности фторированные алкены, такие как 2,2,3,3-тетрафтор-1-пропен (R-1234yf), и фторированные алканы, такие как 1,1,1,2,2-пентафторпропан (R-245cb), известны в качестве эффективных охладителей, средств для тушения огня, среды для передачи тепла, пропеллентов, вспенивающих агентов, раздувающих агентов, газообразных диэлектриков, стерильных носителей, среды для полимеризации, жидкостей для удаления частиц, жидких носителей, полированных абразивных составов, вытесняющих осушающих агентов и рабочих жидкостей для гидравлических приводов. В отличие от хлорфторуглеводородов (CFC's) и хлорфторуглеводородов, содержащих водород (HCFCs), которые могут наносить вред озоновому слою земли, HFCs не содержат хлора и поэтому не представляют угрозы озоновому слою.
Некоторые методы получения фторированных углеводородов известны. Например, в патенте США №6184426 (Belen'Kill) описан способ получения R-245cb путем реакции в жидкой фазе тетрафторэтилена (TFE) и метилфторида в присутствии пентафторида сурьмы в качестве катализатора. Другие способы получения фторированных алканов, содержащих водород, включают способы, описанные в WO 97/02227 (DuPont), когда четырехфтористый углерод или хлортрифторметан реагирует с фторированным этиленовым соединением в жидкой фазе с получением фторированного пропана или хлорфторпропана.
Способы получения водородсодержащих фторалкенов также известны. Например, описано получение R-1234yf из трифторацетилацетона и тетрафторида серы. См. Banks et al., Journal of Fluorine Chemistry, vol.82, Iss.2, p.171-174 (1997). Кроме того, в патенте США №5162594 (Krespan) описан способ взаимодействия тетрафторэтилена с другим фторированным этиленовым соединением в жидкой фазе с получением полифторолефина.
Однако упомянутые выше способы имеют серьезные недостатки, заключающиеся в том, что они являются реакциями сольватации, то есть для облегчения протекания реакции необходим растворитель. Реакции сольватации обладают рядом недостатков. Например, некоторые растворители представляют опасность для здоровья и вредны для окружающей среды. Кроме того, их применение может резко увеличить расходы, связанные с синтезом фторуглеводородов, из-за высокой стоимости самого растворителя, а также дополнительных расходов на его регенерацию. Дополнительным недостатком является то, что продукт получается в жидкой фазе, а не в газовой. Процессы разделения жидких фаз затруднены и требуют больших расходов, чем разделение газовых фаз.
Следовательно, продолжает существовать необходимость в создании способов эффективного получения некоторых фторированных углеводородов, таких как R-1234yf и R-245cb в газовой фазе. Эти и другие цели достигаются данным изобретением.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Заявители разработали экономичный способ получения фторированных органических соединений, включая фторводородсодержащие пропаны и фторводородсодержащие пропены, включающий взаимодействие фторированного олефина с метилфторидом в газовой фазе. Обычно сольватирующие агенты применяют для получения фторводородсодержащих пропанов. Считали, что эти сольватирующие агенты, которые применяются для осуществления физического контакта между реагентами, необходимы для облегчения реакции синтеза. Применение сольватирующих агентов требовало осуществления этих реакций в жидкой фазе. Заявители установили, однако, что реакция синтеза может также протекать в отсутствие сольватирующих агентов и поэтому ее можно проводить в газовой фазе. Кроме того, заявители обнаружили также, что такой способ осуществления реакции в газовой фазе приводит к получению не только фторуглеводорода, но также фторсодержащего пропена.
Таким образом, согласно некоторым предпочтительным вариантам данного изобретения предложены способы получения фторированных органических соединений путем взаимодействия в газовой фазе и в присутствии кислоты Льюиса в качестве катализатора метилфторида с по меньшей мере одним фторированным олефином, имеющим формулу
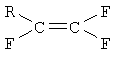
где R означает F, Cl, C1-C2 фторированный алкил или фторированный алкенил, содержащий 2 атома углерода, с получением по меньшей мере одного продукта, содержащего по меньшей мере 3 атома углерода. Предпочтительно проводить эту реакцию практически в отсутствие агентов сольватирования.
Не опираясь на какую-либо конкретную теорию, полагают, что в соответствии с некоторыми вариантами метилфторид реагирует с катализатором с образованием иона карбония. Этот ион карбония, в свою очередь, реагирует с фторированным олефином с образованием галогенированного алкана. Кроме того, часть галогенированного алкана может реагировать с катализатором с образованием галогенированного алкена. Таким образом, способы синтеза по изобретению обладают заметным преимуществом, они не требуют агента сольватирования, и так как продукт получается в газовой фазе, выделение этого продукта и его очистка являются экономичными способами.
Согласно особенно предпочтительным вариантам метилфторид реагирует с тетрафторэтиленом, хлортрифторэтиленом или их смесью в присутствии активированного угля в качестве катализатора, пропитанного пентафторидом сурьмы, с получением R-1234yf, R-245cb или их сочетания.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Данное изобретение предусматривает каталитическую реакцию присоединения в газовой фазе, при этом по меньшей мере один фторированный олефин соединяется с метилфторидом с получением продукта, содержащего по меньшей мере три атома углерода. Согласно некоторым предпочтительным вариантам реакция может быть представлена следующим образом:
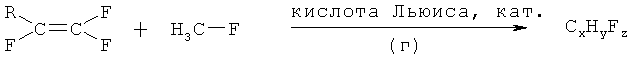
где R обозначает F, Cl, C1-С2 фторированный алкил или фторированный алкенил, содержащий 2 атома углерода,
Х обозначает целое число от 3 до 5,
Y обозначает целое число от 2 до 3 и
Z обозначает целое число от 4 до 9.
Используемый здесь термин "фторированный" относится к органическому соединению, содержащему по меньшей мере один атом фтора. Таким образом, фторированные соединения включают водородсодержащие фторуглеводороды, фторуглеводороды, хлорфторуглеводороды и т.п.
Предпочтительные фторированные олефиновые реагенты включают CCIF=CF2, CF2=CF2, CF3CF=CF2, CF3CF2CF=CF2 и CF2=CF-CF=CF2, при этом особенно предпочтительными являются тетрафторэтилен (TFE) и хлортрифторэтилен (CTFE). Каждое из этих соединений является доступным в целом ряде коммерческих источников. Согласно некоторым предпочтительным вариантам фторированные олефиновые реагенты включают комбинацию по меньшей мере двух из упомянутых выше фторированных олефинов.
Катализатор кислота Льюиса согласно данному изобретению является галогенидом металла или металлоида, который способен принимать пару электронов от координирующей ковалентной связи. Такие катализаторы включают, без ограничения, соединения, содержащие по меньшей мере один атом, выбранный из группы, состоящей из Sb и Al, и по меньшей мере один атом, выбранный из группы, состоящей из F, Cl, Br и I. Примеры хлоридных катализаторов, подходящих для применения согласно данному изобретению, включают, но без ограничения, SbCl5 и AlCl3 и частично фторированные соединения таких хлоридов. Примеры фторидных катализаторов, пригодных для применения по изобретению, включают, но без ограничения, SbF5, SbF3 и частично хлорированные соединения таких фторидов. Предпочтительные кислоты Льюиса включают SbF5, SbF3 и SbCl5, при этом SbF5 является особенно предпочтительным соединением. Согласно некоторым предпочтительным вариантам может быть применена комбинация по меньшей мере двух из упомянутых выше катализаторов.
По некоторым предпочтительным вариантам катализаторами кислотами Льюиса пропитывают активированный углеродный субстрат. Пропитанные активированные углеродные субстраты согласно данному изобретению представляют собой углеродистые материалы, которые содержат каталитические соединения, распределенные тонким слоем на их внутренней поверхности. Активированные углеродные материалы обычно имеют пористую структуру и большую площадь внутренней поверхности. Объем пор активированных углеродных материалов обычно больше 0,2 мл/г, а площадь внутренней поверхности обычно больше 400 м2/г. Ширина пор колеблется от 0,3 нм до нескольких тысяч нм.
При пропитке используются физические свойства активированного углерода для повышения активности катализатора. Например, активированный углерод применяется частично как инертный пористый носитель для распределения катализаторов на большой внутренней поверхности материала, тем самым делая их более доступными для реагентов.
Согласно предпочтительным вариантам пропитка протекает путем осаждения катализатора на высушенном активированном углероде в атмосфере азота при 0-5°С.
Фторуглеводороды согласно данному изобретению предпочтительно имеют формулу
CxHyFz
где Х обозначает целое число от 3 до 5,
Y обозначает целое число от 2 до 3 и
Z обозначает целое число от 4 до 9.
Предпочтительные фторуглеводородные продукты, полученные по изобретению, включают фторированные алканы и фторированные алкены. Если данное изобретение предусматривает непрерывный способ, поток продукта будет включать или один, или оба этих продукта. Предпочтительные фторуглеводороды будут содержать по меньшей мере 3 атома углерода и могут, в случае когда R обозначает фторированный алкенил, представлять собой полимерные продукты. Примеры предпочтительных фторуглеводородов включают, но без ограничения, CH3CF2CF3, CH3CF2CF3, CH3CF2CF2CF3, CH3CF2CF2CF2CF3, CH2=CFCF3, CH2=CFCF2CF3, а также СН2=CFCF2CF2CF3. Наиболее предпочтительные фторуглеводороды включают тетрафторпропены, особенно 2,3,3,3-тетрафтор-1-пропен, и пентафторпропаны, особенно 1,1,1,2,2-пентафторпропан.
Согласно наиболее предпочтительному варианту данного изобретения метилфторид реагирует с хлортрифторэтиленом в газовой фазе и в присутствии катализатора, включающего активированный углерод, пропитанный пентафторидом сурьмы. Можно ожидать, что основным продуктом такой реакции будет 1-хлор-2,2,3,3-тетрафторпропан. Неожиданно заявители установили, что действительным продуктом этой реакции является в основном смесь 2,3,3,3-тетрафтор-1-пропен и 1,1,1,2,2-пентафторпропан. Не ограничиваясь какой-либо конкретной теорией, заявители полагают, что этот вариант протекает по следующей схеме реакции:
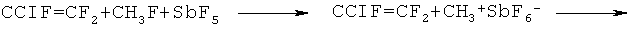
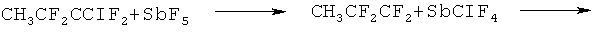
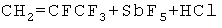
Реакция согласно данному изобретению проводится в газовой фазе, предпочтительно при температуре от примерно 40°С до примерно 150°С и при давлении от примерно 0,5 ф/дюйм2 (34,47 кПа) до примерно 150 ф/дюйм2 (1034,2 кПа). Наиболее предпочтительно проводить реакции при температуре от примерно 50°С до примерно 70°С и при давлении от примерно 10 ф/дюйм2 (68,94 кПа) до примерно 20 ф/дюйм2 (137,89 кПа).
Оптимальные температура и давление для конкретной реакции будут зависеть отчасти от желательного конечного продукта. Хотя обычно конверсия реагентов возрастает с повышением температуры и давления, относительно высокое давление паров SbF5 сдерживает рост температуры реакции и давления. Специалист в данной области с учетом данного описания сможет легко определить оптимальные величины температуры и давления для данной реакции без необходимости проведения ненужных экспериментов.
Способ по данному изобретению может проводиться периодически или более предпочтительно непрерывно. По некоторым предпочтительным вариантам в случае непрерывного процесса реагенты смешивают вместе, нагревают, затем пропускают через слой катализатора с целью получения потока продукта. Желательный выход продукта обычно получается при одном проходе смеси реагентов через слой катализатора. Однако данное изобретение не ограничено такими операциями, а может включать осуществление множества проходов. Согласно некоторым предпочтительным вариантам кислоты в потоке продукта нейтрализуют в скруббере. Поток продукта можно фракционировать (например, путем перегонки) для выделения индивидуальных продуктов.
ПРИМЕРЫ
Дополнительные признаки данного изобретения раскрыты в следующих примерах, которые никоим образом не ограничивают данное изобретение.
Примеры 1-5
Эти примеры показывают активность разных катализаторов.
Получение катализаторов
Катализатор А
Катализатор, включающий активированный уголь, пропитанный SbF5, получают путем сушки 100 г активированного угля в печке при температуре, равной 180°С, под вакуумом в течение 72 ч.
После сушки на углерод наносят покрытие из алюминиевой фольги и затем постепенно охлаждают до комнатной температуры под вакуумом.
Бутылку из HDPE (ПЭВД) объемом 250 мл промывают безводным N2 для удаления воздуха. Затем в бутылку в перчаточной камере помещают примерно 50 г высушенного активированного угля в атмосфере азота. В перчаточной камере медленно добавляют 50 г SbF5 (примерно 2 г/мин) к активированному углю при вращении бутылки. Содержимое в бутылке перемешивают прутком из пластика до тех пор, пока не адсорбируется в порах угля вся жидкость, или до тех пор, пока не перестанут выделяться пары SbF5.
Катализатор В
Повторяют процедуру, описанную для катализатора А, за исключением того, что (1) бутылку погружают в баню с температурой 0-5°С для облегчения адсорбции SbF5 в поры активированного угля и (2) SbF5 добавляют в бутылку со скоростью 5 г/мин.
Катализатор С
Процедуру, описанную для катализатора В, повторяют, за исключением того, что к 50 г активированного угля добавляют только 20 г SbF5.
Катализатор D
Повторяют процедуру, описанную для катализатора В, за исключением того, что пропитывают 30 г SbF5 50 г активированного угля и затем фторируют в реакторе Монеля (1/2 дюйма), пропуская 30 г/ч HF при температуре 70°С в течение 20 ч под давлением 50 ф/дюйм2 (344,7 кПа). После фторирования пропускают 50 стандартных см3 в мин (SCCM) N2 через слой катализатора при температуре 30°С в течение 30 ч для удаления HF из слоя катализатора.
Катализатор Е
Повторяют процедуру, описанную для катализатора В, за исключением того, что 50 г высушенного активированного угля пропитывают 50 г SbF3 и затем фторируют в реакторе Монеля (1/2 дюйма) 10 г/ч F2 (смесь 50 вес.% N2 и 50 вес.% F2) при температуре 70°С в течение 30 ч под давлением 50 ф/дюйм2 (344,7 кПа). После фторирования через слой пропускают 50 SCCM 100 вес.% N2 при температуре 30°С в течение 2 ч для удаления свободного F2 из слоя.
Активность катализаторов
Активность каждого из описанных выше катализаторов определяют следующим образом.
В проточный реактор Монеля (1/2 дюйма) загружают 50 г свежеприготовленного катализатора и затем равномерно нагревают до 50°С. Газообразную смесь CTFE и CH3F при давлении 20 ф/дюйм2 (137,89 кПа) нагревают до 40°С в нагревателе, который связан с реактором. Нагретую смесь реагентов пропускают в реактор со скоростью 20 SCCM. Линия выхода из реактора соединена on-line с GC (ГХ) и GCMS (ГХ-МС) для анализа. Используют 15% раствор КОН для промывки при температуре 50°С для нейтрализации кислот, выходящих из реактора. Поток газов, выходящий из раствора для промывки, затем конденсируют в цилиндре в атмосфере жидкого N2 и затем фракционируют (перегоняют) для выделения продуктов. Результаты для каждого катализатора показаны ниже.
Из этих данных видно, что катализатор В является самым активным катализатором в указанных реакционных условиях.
Примеры 6-14
Эти примеры показывают величины степени конверсии хлортрифторэтилена (CTFE) и тетрафторэтилена (TFE) в присутствии катализатора на основе Sb. В проточный реактор Монеля (1/2 дюйма) загружают 50 г свежеприготовленного катализатора В и равномерно нагревают до температуры, указанной ниже в таблице. Газообразную смесь CTFE или TFE и CH3F нагревают до температуры на 10°С ниже температуры реактора. Нагретая смесь реагентов затем пропускается в реактор со скоростью 20 SCCM и при давлении, указанном ниже в таблице. Линия выхода из реактора соединена on-line с GC (ГХ) и GCMS (ГХ-МС) для анализа. Используют 15% раствор КОН для промывки при температуре 50°С для нейтрализации кислот, выходящих из реактора. Поток газов, выходящий из раствора для промывки, затем конденсируют в цилиндре в атмосфере жидкого N2 и затем фракционируют (перегоняют) для выделения продуктов. Результаты для каждого опыта показаны ниже.
Видно, что реакция является более селективной по отношению к TFE, а не к CTFE, но подача CTFE приводит к большей степени конверсии в CF3CF=СН2.
Выше описаны несколько конкретных примеров изобретения, но специалистам ясно, что возможны различные изменения, модификации и усовершенствования. Такие изменения, модификации и усовершенствования очевидны из этого описания, они являются его частью, хотя явно в нем не описаны. Соответственно, приведенное выше описание является только примером и не ограничивает данное изобретение. Изобретение ограничено только формулой изобретения с учетом эквивалентов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 2,3,3,3-ТЕТРАФТОРПРОПЕНА | 2010 |
|
RU2547440C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФТОРИРОВАННЫХ ОЛЕФИНОВ (ВАРИАНТЫ) | 2007 |
|
RU2457195C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИФТОРОЛЕФИНОВ, ФТОР-1-ЭТИЛЦИКЛОПЕНТЕН И ПЕРФТОР-2,3-ДИХЛОГЕКС-2-ЕН ИЛИ ПЕРФТОР-4,5-ДИХЛОРОКТ-4-ЕН | 1991 |
|
RU2093502C1 |
| СПОСОБЫ ГЕОМЕТРИЧЕСКОЙ ИЗОМЕРИЗАЦИИ ГАЛОИДИРОВАННЫХ ОЛЕФИНОВ | 2007 |
|
RU2455272C2 |
| КАТАЛИТИЧЕСКОЕ ГАЗОФАЗНОЕ ФТОРИРОВАНИЕ | 2015 |
|
RU2654694C2 |
| КАТАЛИТИЧЕСКОЕ ГАЗОФАЗНОЕ ФТОРИРОВАНИЕ | 2011 |
|
RU2571415C2 |
| ПОЛИМЕРИЗАЦИЯ В ВОДНОЙ ЭМУЛЬСИИ БЕЗ ЭМУЛЬГАТОРА ДЛЯ ПОЛУЧЕНИЯ СОПОЛИМЕРОВ ФТОРИРОВАННОГО ОЛЕФИНА И УГЛЕВОДОРОДНОГО ОЛЕФИНА | 2003 |
|
RU2342403C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФТОРИРОВАННЫХ АЛКАНОВ | 2007 |
|
RU2461539C2 |
| ФТОРСОДЕРЖАЩИЕ ПОВЕРХНОСТНО-АКТИВНЫЕ ВЕЩЕСТВА ДЛЯ ПОЛУЧЕНИЯ ФТОРПОЛИМЕРОВ | 2006 |
|
RU2458041C2 |
| ПРОЦЕСС ПОЛУЧЕНИЯ ФТОРПОЛИМЕРА, ИМЕЮЩЕГО НИТРИЛЬНЫЕ КОНЦЕВЫЕ ГРУППЫ | 2003 |
|
RU2346008C2 |
Изобретение относится к способу получения фторированных органических соединений, включающему взаимодействие метилфторида с по меньшей мере одним фторированным олефином, имеющим структурную формулу
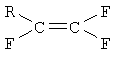 ,
,
где R означает F, Cl, C1-C2 фторированный алкил или фторированный алкенил, содержащий 2 атома углерода, с получением по меньшей мере одного продукта, содержащего по меньшей мере 3 атома углерода, при этом указанное взаимодействие происходит в газовой фазе и в присутствии в качестве катализатора кислоты Льюиса, которой пропитывают активированный углерод. Технический результат - экономичный способ получения фторированных органических соединений. 9 з.п. ф-лы, 2 табл.
1. Способ получения фторированных органических соединений, включающий взаимодействие метилфторида с по меньшей мере одним фторированным олефином, имеющим структурную формулу
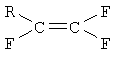
где R означает F, Cl, C1-C2 фторированный алкил или фторированный алкенил, содержащий 2 атома углерода, с получением по меньшей мере одного продукта, содержащего по меньшей мере 3 атома углерода, при этом указанное взаимодействие происходит в газовой фазе и в присутствии в качестве катализатора кислоты Льюиса, которой пропитывают активированный углерод.
2. Способ по п.1, отличающийся тем, что фторированный олефин выбирают из группы, состоящей из тетрафторэтилена, хлортрифторэтилена и их сочетаний.
3. Способ по п.1, отличающийся тем, что указанный продукт включает фторутлеводород.
4. Способ по п.1, отличающийся тем, что указанный продукт включает полимер фторуглеводорода.
5. Способ по п.3, отличающийся тем, что фторуглеводород представляет собой фторированный С3-С5-алкан, фторированный С3-С5-алкен или некоторые их смеси.
6. Способ по п.3, отличающийся тем, что фторуглеводород представляет собой 2,3,3,3-тетрафтор-1-пропен.
7. Способ по п.3, отличающийся тем, что фторуглеводород представляет собой 1,1,1,2,2-пентафторпропан.
8. Способ по п.1, отличающийся тем, что катализатор кислота Льюиса представляет собой галоидид металла или металлоида, нанесенный пропиткой на активированный уголь.
9. Способ по п.9, отличающийся тем, что катализатор содержит по меньшей мере один атом, выбранный из группы, состоящей из Sb и А1.
10. Способ по п.1, отличающийся тем, что реакцию проводят практически в отсутствие сольватирующего агента.
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| BELEN'KII G et al | |||
| Electrophilic, catalytic alkylation of polyfluoroolefins by some fluoroalkanes, Journal of fluorine chemistry, vol.108, no.1, 2001, pages 15-20 | |||
| СПОСОБ ПОЛУЧЕНИЯ ФТОРОЛЕФИНОВ | 1999 |
|
RU2210559C2 |
Авторы
Даты
2011-04-27—Публикация
2006-05-05—Подача